ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится к новому, первому соединению класса альдегидов, пригодному для использования в качестве душистого вещества, способу его производства и парфюмерной композиции, содержащей это соединение класса альдегидов, и, кроме этого, ко второму соединению класса альдегидов, пригодному для использования в качестве сырья для первого соединения класса альдегидов.
УРОВЕНЬ ТЕХНИКИ
[0002] Соединение, имеющее аромат и приятный вкус, может быть с успехом использовано в качестве компонента парфюмерной композиции, и в последнее время в качестве душистых веществ и сырья для душистых веществ внимание привлекли алкилбензальдегиды и их производные.
В Патентом документе 1 указано, что 3-(4-(втор-бутил)-2-метилфенил)пропан и 3-(4-изобутил-2-метилфенил)-2-метилпропаналь обладают определенным ароматом.
Список цитируемой литературы
Патентные документы
[0003] Патентный документ 1: JP 2018-138550 A
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Техническая задача
[0004] Целью настоящего изобретения является обеспечение нового первого соединения класса альдегидов, пригодного для использования в качестве душистого вещества и компонента парфюмерной композиции, способа производства этого соединения класса альдегидов, а также парфюмерной композиции, содержащей первое соединение класса альдегидов в качестве активного компонента, и применение этого соединения в качестве душистого вещества. Кроме этого, другой целью настоящего изобретения является обеспечение нового второго соединения класса альдегидов, пригодного для использования в качестве сырья для первого соединения класса альдегидов.
Решение поставленной задачи
[0005] Авторами настоящего изобретения синтезированы различные соединения, изучены их ароматы и установлено, что некоторые альдегиды обладают ароматом с оттенком ландыша, тем самым, было сделано настоящее изобретение.
[0006] Настоящим изобретение обеспечиваются следующие аспекты (1)-(6).
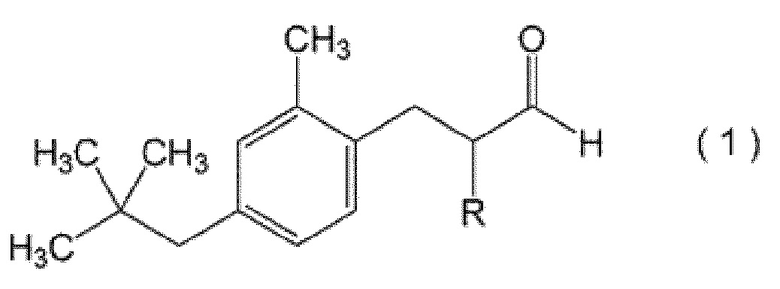
(1) Соединение, представленное следующей формулой (1)
[0007]
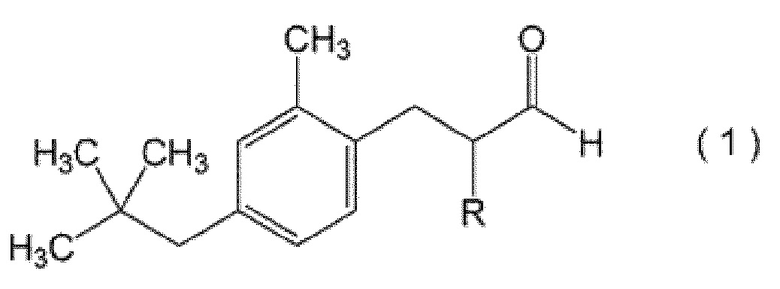
при этом, в формуле (1) R означает атом водорода или метильную группу.
[0008] (2) Соединение по п. 1, в котором R означает атом водорода.
(3) Парфюмерная композиция, содержащая соединение по п. 1 или п. 2.
(4) Применение соединения по п. 1 или 2 в качестве душистого вещества.
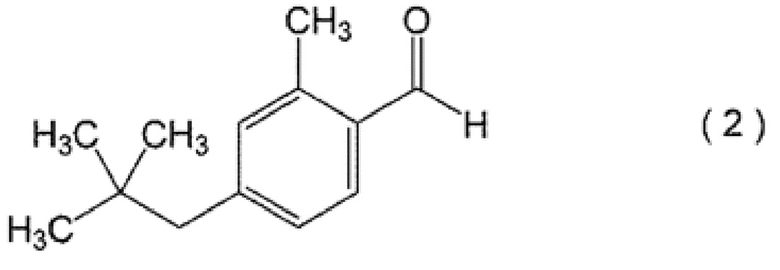
(5) Соединение, представленное следующей формулой (2)
[0009] 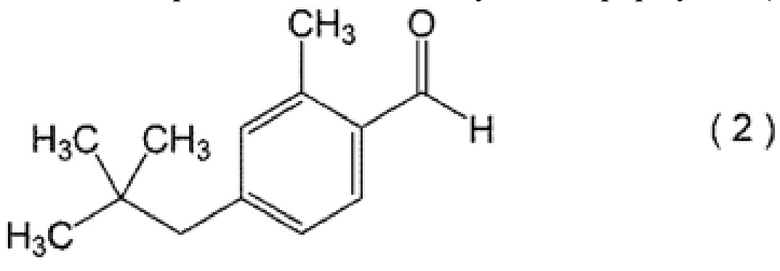
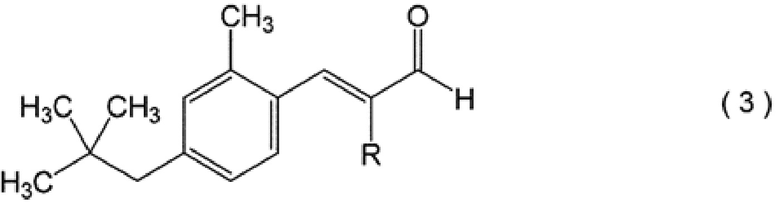
[0010] (6) Способ производства соединения формулы (1), при этом, способ включает следующие стадии, осуществляемые в указанном порядке, на которых проводят альдольную конденсацию соединения формулы (2) с ацетальдегидом или пропиональдегидом с образованием соединения формулы (3); проводят гидрирование соединения формулы (3) с образованием соединения формулы (1):
[0011] 
[0012] 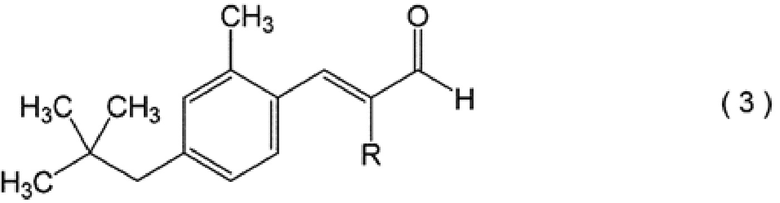
при этом, в формуле (3) R означает атом водорода или метильную группу; и
[0013] 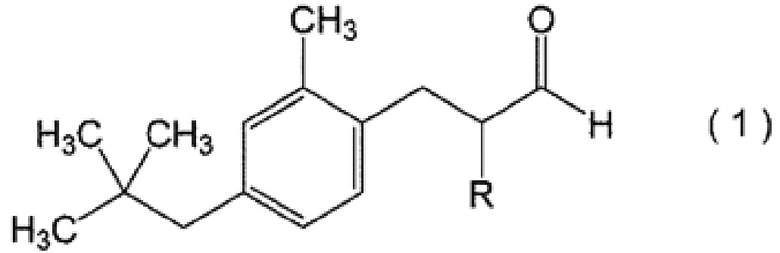
при этом, в формуле (1) R означает атом водорода или метильную группу.
Преимущества изобретения
[0014] Благодаря настоящему изобретению возможно обеспечение нового первого соединения класса альдегидов, пригодного для использования в качестве душистого вещества и компонента парфюмерной композиции, способа производства этого соединения, а также парфюмерной композиции, содержащей первое соединение класса альдегидов в качестве активного компонента, и применение этого соединения в качестве душистого вещества. Кроме этого, благодаря настоящему изобретению возможно обеспечение нового второго соединения класса альдегидов, пригодного для использования в качестве сырья для первого соединения класса альдегидов.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[0015] Далее настоящее изобретение описано на примерах. Отметим, что в нижеследующем описании выражение «от А до В» с указанием числового диапазона означает «больше или равно А и меньше или равно В» (когда А<В) или «меньше или равно А и больше или равно В» (когда А>В). Другими словами, выражение «от А до В» означает числовые диапазоны, включающие конечные точки А и В.
Кроме этого, термины «массовых частей» и «% масс.» являются синонимичными терминам «весовых частей» и «% вес.», соответственно.
[0016] Соединение, представленное формулой (1)
Первое соединение класса альдегидов, соответствующее настоящему изобретению, может быть представлено следующей формулой (1):

при этом в формуле (1) R означает атом водорода или метильную группу.
[0017] В формуле (1) R означает атом водорода или метильную группу. Из них с точки зрения ароматических свойств предпочтительным является атом водорода.
[0018] Альдегид, представленный формулой (1), включает асимметричный атом углерода, когда R является метильной группой. В этом случае соединение может включать только один получаемый из него оптический изомер или может представлять собой смесь, содержащую множество оптических изомеров в любом соотношении.
[0019] Соединение, представленное формулой (1), является новым соединением.
Первое соединение класса альдегидов, представленное формулой (1) имеет ароматом с оттенком ландыша, пригодно для использования в качестве душистого вещества и компонента парфюмерной композиции и, кроме этого, имеет аромат с цветочным оттенком, альдегидным оттенком и зеленым оттенком одновременно.
[0020] Соединение, представленное формулой (1), пригодно для использования в качестве душистого вещества, так как это соединение обладает превосходным ароматом, как описано ниже. Вообще, душистое вещество редко используют индивидуально и часто используют в составе парфюмерной композиции, изготавливаемой путем составления из множества душистых веществ в соответствии с поставленной целью. Первое соединение класса альдегидов, соответствующее одному из вариантов осуществления настоящего изобретения, пригодно для использования в качестве душистого вещества, подлежащего смешиванию с другими в парфюмерной композиции (также именуемого «компонент парфюмерной композиции»). В качестве душистого вещества одно из соединений, представленных формулой (1), может быть использовано индивидуально, либо два эти соединения могут быть использованы в сочетании.
Кроме этого, соединение, представленное формулой (1), соответствующее настоящему изобретению, может включать небольшое количество примесей, побочных продуктов, загрязнителей и т.п. при условии, что это не принижает эффекты настоящего изобретения.
Соединение, представленное формулой (1), имеет ароматом с оттенком ландыша, как описано выше, а также имеет аромат с цветочным оттенком, альдегидным оттенком, зеленым оттенком и т.п. и также обладает превосходной диффузионной способностью.
Соединение, представленное формулой (1), соответствующее настоящему изобретению, может быть индивидуально использовано в качестве душистого вещества и добавлено во множество парфюмерных и косметических средств, медицинских и гигиенических материалов, а также в медицинские принадлежности, товары домашнего обихода, пищевые продукты и т.п. с целью придания им аромата или приятного вкуса. В качестве альтернативы, соединение, представленное формулой (1), соответствующее настоящему изобретению, может быть смешано с другим компонентом парфюмерной композиции и т.п. с целью изготовления парфюмерной композиции, описанной ниже, которая может быть добавлена во множество продуктов с целью придания им аромата или приятного вкуса. Из этих вариантов, с точки зрения получения заданного аромата или вкуса является предпочтительным, чтобы соединение, соответствующее одному из вариантов осуществления настоящего изобретения, было смешано с другими в парфюмерной композиции в качестве ее компонента, и парфюмерная композиция была добавлена в продукт с целью ароматизации продукта.
[0021] Парфюмерная композиция
Парфюмерная композиция настоящего изобретения в качестве активного компонента содержит соединение, представленное формулой (1), которое представляет собой первое соединение класса альдегидов настоящего изобретения. Парфюмерная композиция настоящего изобретения не имеет определенных ограничений при условии, что содержит, по меньшей мере, одно первое соединение класса альдегидов настоящего изобретения и может содержать два первых соединения класса альдегидов настоящего изобретения. Отметим, что душистое вещество предназначено для придания, по меньшей мере, либо аромата, либо приятного вкуса (далее выражение «по меньшей мере, либо аромата, либо приятного вкуса» также имеет форму «аромата и т.п.»).
Парфюмерная композиция, соответствующая одному из вариантов осуществления настоящего изобретения, должна содержать в качестве активного компонента только первое соединение класса альдегидов, соответствующее одному из вариантов осуществления настоящего изобретения, и другие компоненты не имеют определенных ограничений. Однако, парфюмерная композиция, предпочтительно, содержит другой душистый компонент (далее также именуемый «известное душистое вещество»).
Отметим, что «парфюмерная композиция» - это композиция, которую добавляют в различные парфюмерные и косметические средства, медицинские принадлежности, пищевые продукты, напитки и т.п. для придания им аромата и т.п., или композиция, которую используют как таковую в духах и т.п. Парфюмерная композиция, если нужно, помимо известного душистого вещества может содержать добавку, такую как растворитель.
Добавляемое количество первого соединения класса альдегидов, соответствующего одному из вариантов осуществления настоящего изобретения, зависит от типа первого соединения класса альдегидов, соответствующего одному из вариантов осуществления настоящего изобретения, типа аромата, который нужно получить, интенсивности аромата и т.п. Количество первого соединения класса альдегидов, соответствующего одному из вариантов осуществления настоящего изобретения, представленного формулой (1), в парфюмерной композиции составляет, предпочтительно, 0,001% масс. или более, более предпочтительно, 0,01% масс. или более, еще более предпочтительно, 0,1% масс. или более, предпочтительно, 90% масс. или менее, более предпочтительно, 70% масс. или менее, еще более предпочтительно, 50% масс. или менее.
[0022] Известное душистое вещество не имеет определенных ограничений при условии, что оно является известным душистым компонентом, и может быть использован широкий спектр душистых веществ. Например, могут быть выбраны и использованы в любом соотношении компонентов в смеси одно или несколько душистых веществ из приведенных далее. Примеры таких веществ включают углеводороды, такие как лимонен, α-пинен, β-пинен, терпинен, цедрен, лонждифолен, и валансен; спирты, такие как линалоол, цитронеллол, гераниол, нерол, терпинеол, дигидромирценол, этиллиналоол, фарнезол, неролидол, цис-3-гексенол, цедрол, ментол, борнеол, β-фенилэтиловый спирт, бензиловый спирт, фенилгексанол, 2,2,6-триметилциклогексил-3-гексанол, 1-(2-трет-бутилциклогексилокси)-2-бутанол, 4-изопропилциклогексанметанол, 4-трет-буитлциклогексанол, 4-метил-2-(2-метилпропил)тетрагидро-2H-пиран-4-ол, 2-метил-4-(2,2,3-триметил-3-циклопентен-1-ил)-2-бутен-1-ол, 2-этил-4-(2,2,3-триметил-3-циклопентен-1-ил)-2-бутен-1-ол, изокамфилциклогексанол и 3,7-диметил-7-метоксиоктан-2-ол; фенолы, такие как эвгенол, тимол и ванилин; сложные эфиры, такие как линалилформиат, цитронеллилформиат, геранилформиат, н-гексилацетат, цис-3-гексенилацетат, линалилацетат, цитронеллилацетат, геранилацетат, нерилацетат, терпинилацетат, нопилацетат, борнилацетат, изоборнилацетат, o-трет-бутилциклогексилацетат, п-трет-бутилциклогексилацетат, трициклодеценилацетат, бензилацетат, стиралилацетат, циннамилацетат, диметилбензилкарбинилацетат, 3-пентилтетрагидропиран-4-ил-ацетат, цитронеллилпропионат, трициклодеценилпропионат, аллилциклогексилпропионат, этил-2-циклогексилпропионат, бензилпропионат, цитронеллилбутират, диметилбензилкарбинил-н-бутират, трициклодеценилизобутират, метил-2-ноненоат, метилбензоат, бензилбензоат, метилциннамат, метилсалицилат, н-гексилсалицилат, цис-3-гексенилсалицилат, геранилтиглат, цис-3-гексенилтиглат, метилжасмонат, метилдигидрожасмонат, метил-2,4-дигидрокси-3,6-диметилбензоат, этилметилфенилглицидат, метилантранилат и FRUITATE; альдегиды, такие как н-октаналь, н-деканаль, н-додеканаль, 2-метилундеканаль, 10-ундеканаль, цитронеллаль, цитраль, гидроксицитронеллаль, диметилтетрагидробензальдегид, 4(3)-(4-гидрокси-4-метилпентил)-3-циклогексен-1-карбоальдегид, 2-циклогексилпропаналь, п-трет-бутил-α-метилгидрокоричный альдегид, п-изопропил-α-метилгидрокоричный альдегид, п-этил-α,α-диметилгидрокоричный альдегид, α-амилкоричный альдегид, α-гексил коричный альдегид, пиперональ и α-метил-3,4-метилендиоксигидрокоричный альдегид; кетоны, такие как метилгептенон, 4-метилен-3,5,6,6-тетраметил-2-гептанон, амилциклопентанон, 3-метил-2-(цис-2-пентен-1-ил)-2-циклопентен-1-он, метилциклопентенолон, розовые кетоны, γ-метилионон, α-ионон, карбон, ментон, камфора, нуткатон, бензилацетон, анизилацетон, метил-β-нафтилкетон, 2,5-диметил-4-гидрокси-3(2H)-фуранон, мальтол, 7-ацетил-1,2,3,4,5,6,7,8-октагидро-1,1,6,7-тетраметилнафталин, мускон, циветон, циклопентадеканон и циклогексадеканон; ацетали и кетали, такие как ацетальдегид этилфенилпропилацеталь, цитральдиэтилацеталь, фенилацетальдегид глицеринацеталь и этилацетоацетат этиленгликолькетали; простые эфиры, такие как анетол, β-нафтилметиловый эфир, β-нафтиэтиловый эфир, лимоненоксид, розеноксид, 1,8-цинеол и рацемический или фотоактивный додекагидро-3a,6,6,9a-тетраметилнафто[2,1-b]фуран; нитрилы, такие как цитронеллилнитрил; лактоны, такие как γ-ноналактон, γ-ундекалактон, σ-декалактон, γ-жасмолактон, кумарин, циклопентадеканолид, циклогексадеканолид, амбреттолид, этиленбрассилат и 11-оксагексадеканолид; и другие душистые материалы, такие как природные эфирные масла и натуральные экстракты апельсина, лимона, бергамота, мандарина, перечной мяты, курчавой мяты, лаванды, ромашки, розмарина, эвкалипта, шалфея, базилика, розы, герани, жасмина, иланг-иланга, аниса, гвоздики, имбиря, муската, кардамона, кедра, японского кипариса, сандалового дерева, ветивера, пачули и лабданума.
[0023] Кроме этого, помимо душистых компонентов, парфюмерная композиция в качестве компонентов также может содержать поверхностно-активное вещество, такое как лаурилсульфатный эфир полиоксиэтилена; растворитель, такой как дипропиленгликоль, диэтилфталат, этиленгликоль, пропиленгликоль, метилмиристат, триэтилцитрат и т.п.; антиоксидант, такой как ВНТ (дитретичный бутилгидрокситолуол) и витамин Е (токоферол); краситель и т.п., и, предпочтительно, содержит, по меньшей мере, антиоксидант.
[0024] Первое соединение класса альдегидов, соответствующее одному из вариантов осуществления настоящего изобретения, представленное формулой (1), которое имеет аромат с оттенком ландыша, одновременно имеет аромат с белым цветочным оттенком, альдегидным оттенком или зеленым оттенком помимо оттенка ландыша при сочетании с известным душистым веществом. Таким образом, первое соединение класса альдегидов целесообразным образом добавляют в различные парфюмерные и косметические средства, медицинские и гигиенические материалы, а также медицинские принадлежности, товары домашнего обихода, пищевые продукты и т.п. с целью придания им аромата и т.п.
[0025] Примеры продуктов, в которые может быть добавлено первое соединение класса альдегидов, соответствующее одному из вариантов осуществления настоящего изобретения, представленное формулой (1), с целью придания аромата и т.п. и улучшения аромата и т.п. этого продукта (объекта), включают различные продукты, такие как парфюмерные и косметические средства, медицинские и гигиенические материалы, смешанные товары, напитки, пищевые продукты, квази-фармацевтические продукты и медицинские принадлежности; парфюмерная композиция может быть использована в качестве компонента для придания аромата и т.п., например, душистым продуктам, таким как духи и одеколоны; косметическим средствам по уходу за волосами, таким как шампуни, ополаскиватели, средства для укрепления волос, кремы, муссы, гели, мази, спреи и т.п. для волос; косметическим средствам по уходу за кожей, таким как лосьоны, эссенции, кремы, молочные лосьоны, косметические маски, основа под макияж, пудра, губная помада и различные продукты для макияжа; различным медицинским и санитарным моющим средствам, таким как средства для мытья посуды, стиральные моющие средства, умягчители, дезинфицирующие моющие средства, моющие средства против запаха, ароматизаторы помещений, средства по уходу за мебелью, средства для очистки стекол, средства для очистки мебели, средства для мытья полов, дезинфицирующие средства, инсектициды, отбеливатели, бактерициды, репелленты и т.п.; квази-фармацевтическим продуктам, таким как зубные пасты, жидкости для полоскания рта, добавки для ванн, средства от пота и жидкости для перманентной завивки волос; смешанным товарам, таким как туалетная бумага и косметическая бумага; медицинским принадлежностям; пищевым продуктам и т.п.
[0026] Количество парфюмерной композиции, добавляемое в продукт, не имеет определенных ограничений, добавляемое количество парфюмерной композиции может быть выбрано в широком диапазоне в зависимости от типа, природы и органолептических эффектов содержащего отдушку продукта. Например, это количество может составлять 0,00001% масс. или более, предпочтительно, 0,0001% масс. или более, более предпочтительно, 0,001% масс. или более. В случае такого продукта, как духи, например, это количество может составлять 100% масс., предпочтительно, 80% масс. или менее, более предпочтительно, 60% масс. или менее, еще более предпочтительно, 40% масс. или менее.
[0027] Соединение, представленное формулой (2)
Второе соединение класса альдегидов настоящего изобретения представлено следующей формулой (2).
[0028] 
[0029] Соединение, представленное приведенной выше формулой (2), пригодно для использования в качестве промежуточной формы синтеза (или сырья синтеза) первого соединения класса альдегидов настоящего изобретения, описанного выше.
Помимо соединения, представленного формулой (1), также ожидается, что из соединения, представленного формулой (2), может быть синтезировано соединение, пригодное для использования в качестве другого душистого вещества.
Способ синтеза соединения, представленного формулой (1), и способ использования соединения, представленного формулой (2), в качестве промежуточной формы синтеза (или сырья синтеза) соединения, представленного формулой (1), будет описан ниже.
Отметим, что в соответствии с настоящим изобретением при синтезе соединения, представленного формулой (1), соединение, представленное формулой (2), может содержать небольшое количество примесей, побочных продуктов, загрязнителей и т.п. при условии, что это не принижает эффекты настоящего изобретения.
[0030] Способ производства соединения, представленного формулой (2)
В соответствии с настоящим изобретением, способ производства соединения, представленного формулой (2), не имеет определенных ограничений. К его примерам относится способ, в соответствии с которым проводят реакцию неопентилтолуола с монооксидом углерода в присутствии трифлатной кислоты (трифторметансульфокислота) при повышенном давлении, однако, предпочтительно, это соединение производят посредством реакции 3-неопентилтолуола с монооксидом углерода в присутствии фтороводорода и трифторида бора.
В частности, эта реакция представлена следующим уравнением:
[0031] 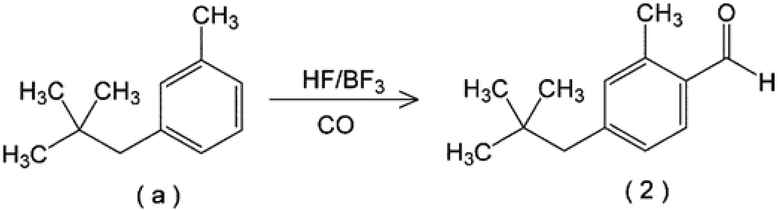
[0032] Отметим, что в приведенной выше реакции 3-неопертилтолуол легко поддается формилированию в положении 4 и в положении 6; предпочтительно, формилирование проводят в положении 6 путем повышения региоселективности. Региоселективность формилирования зависит от количества фтороводорода и трифторида бора относительно 3-неопентилтолуола, давления монооксида углерода, времени реакции, температуры реакции и т.п., как описано ниже. Оптимизация этих параметров позволяет повысить региоселективность.
[0033] Фтороводород (HF) также выполняет в этой реакции роль растворителя. Предпочтительно, с точки зрения реакционной способности, фтороводород является, по существу, безводным фтороводородом. Отметим, что выражение «по существу, безводный» означает, что содержание воды составляет 5% масс. или менее, предпочтительно, 1% масс. или менее, более предпочтительно, 0,1% масс. или менее.
Молярное отношение фтороводорода к 3-неопентилтолуолу (фтороводород/3-неопентилтолуол) составляет, предпочтительно, 1,5 или более, более предпочтительно, 3,0 или более, еще более предпочтительно, 5,0 или более с точки зрения реакционной способности с монооксидом углерода и подавления побочных реакций и составляет, предпочтительно, 30,0 или менее, более предпочтительно, 20,0 или менее, еще более предпочтительно, 12,0 или менее с точки зрения экономической эффективности и эффективности производства.
[0034] Молярное отношение трифторида бора (BF3) к 3-неопентилтолуолу (трифторид бора/3-неопентилтолуол) составляет, предпочтительно, 0,1 или более, более предпочтительно, 0,5 или более, еще более предпочтительно, 1,0 или более, еще более предпочтительно, 1,2 или более и, предпочтительно, 5,0 или менее, более предпочтительно, 3,0 или менее, еще более предпочтительно, 2,0 или менее с точки зрения региоселективности, благоприятствующей формилированию.
[0035] Температура, при которой монооксид углерода вступает в реакцию, составляет, предпочтительно, -50°С или выше, более предпочтительно, -40°С или выше и, предпочтительно, 30°С или ниже, более предпочтительно, 10°С или ниже, еще более предпочтительно, 5°С или ниже с точки зрения повышения реакционной способности, подавления побочных реакций и повышения селективности в положении введения формильной группы.
Реакцию между 3-неопентилтолуолом и монооксидом углерода проводят, предпочтительно, при повышенном давлении.
Давление в ходе реакции составляет, предпочтительно, 1,0 МПа изб. или более, более предпочтительно, 1,5 МПа изб. или более, еще более предпочтительно, 1,8 МПа изб. или более и составляет, предпочтительно, 3,0 МПа изб. или менее, более предпочтительно, 2,5 МПа изб. или менее, еще более предпочтительно, 2,2 МПа изб. или менее как парциальное давление монооксида углерода с точки зрения повышения реакционной способности и подавления побочных реакций.
[0036] В контексте настоящего изобретения время реакции не имеет определенных ограничений и составляет, предпочтительно, 10 мин или более, более предпочтительно, 20 мин или более, еще более предпочтительно, 30 мин или более и составляет, предпочтительно, 24 часа или менее, более предпочтительно, 12 часов или менее, еще более предпочтительно, 5 часов или менее с точки зрения достаточного прогресса реакции, подавления побочных реакций и разложения продуктов, а также эффективности производства.
[0037] Способ производства, соответствующий настоящему изобретению, может быть осуществлен в присутствии растворителя. Используемый растворитель не имеет определенных ограничений при условии, что в этом растворителе хорошо растворяется сырье реакции, и растворитель инертен к фтороводороду и трифториду бора. В качестве примеров можно привести насыщенные алифатические углеводороды, такие как гексан, гептан и декан, ароматические углеводороды, такие как бензол и толуол, и галогенированные алифатические углеводороды, такие как хлороформ, метиленхлорид и дихлорэтан. Один тип из этих растворителей может быть использован индивидуально, либо два или более типов могут быть использованы в сочетании.
Используемое количество растворителя не имеет определенных ограничений, требуется только, чтобы оно было выбрано надлежащим образом с точки зрения однородности реакции, скорости реакции и удаления растворителя.
Отметим, что в контексте настоящего изобретения фтороводород, присутствующий в ходе реакции, также выполняет роль растворителя, таким образом, растворитель может не использоваться.
[0038] Описанная выше реакция может быть проведена любым способом, например, периодическим, полу-периодическим, непрерывным и т.п., однако, предпочтительно, относится к непрерывному типу с точки зрения возможности извлечения и рециркуляции катализатора и с точки зрения эффективности производства.
Устройство, применяемое в данном способе производства, представляет собой устройство для проведения реакции, обеспечивающее достаточное перемешивание жидкой фазы и газовой фазы и регулирование температуры при повышенном давлении.
Например, в непрерывном режиме сначала в реактор, оборудованный мешалкой, помещают фтороводород и трифторид бора, содержимое реактора перемешивают, температуру жидкости доводят до заданной величины и поддерживают постоянной. Затем, подавая монооксид углерода, давление увеличивают до надлежащего давления реакции, монооксид углерода продолжают подавать так, чтобы давление оставалось постоянным. Затем, если нужно, осуществляют реакцию в полу-непрерывном режиме, подавая 3-неопентилтолуол, растворенный в растворителе. Затем начинают подачу фтороводорода, трифторида бора и 3-неопентилтолуола, надлежащим образом растворенного в растворителе, и непрерывно отводят раствор продукта реакции.
После удаления фтороводорода и трифторида бора из реакционного раствора, содержащего 2-метил-4-неопентилбензальдегид, реакционный раствор может быть очищен каким-либо известным способом, таким как дистилляция или экстракция. Для удаления из реакционного раствора фтороводорода может быть проведена нейтрализующая промывка водой с использованием водного раствора гидроксида натрия.
[0039] Отметим, что соединение, представленное формулой (а) выше (3-неопентилтолуол), может быть синтезировано следующим образом.
[0040] 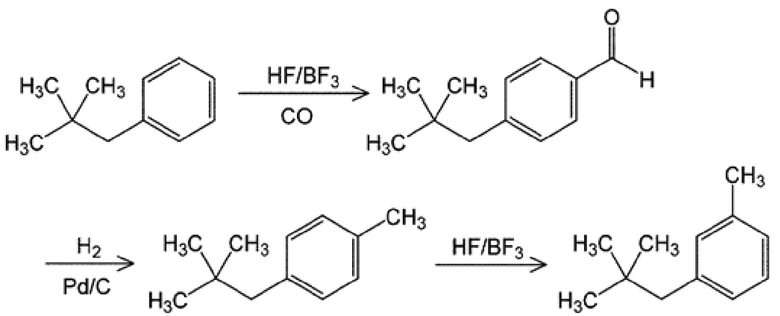
[0041] Проводят реакцию неопентилбензола с монооксидом углерода в присутствии фтороводорода и трифторида бора с целью формилирования п-положения неопентильной группы с образованием 4-неопентилбензальдегида.
Затем полученный 4-неопентилбензальдегид восстанавливают в присутствии палладиевого катализатора с целью восстановления формильной группы до метильной группы.
Затем проводят изомеризацию полученного 4-неопентилтолуола в присутствии фтороводорода и трифторида бора, образующийся в результате реакции изомеризации 3-неопентилтолуол отделяют, получая, тем самым, 3-неопентилтолуол.
[0042] Способ производства соединения, представленного формулой (1)
Соединение, представленное формулой (1), может быть произведено любым способом, примером способа производства является способ, в соответствии с которым проводят бромирование в положении 6 3-неопентилтолуола, кроме того, проводят реакцию с аллиловым спиртом в присутствии вторичного амина и палладиевого катализатора, пропанольную боковую цепь полученного соединения окисляют. В отношении этого способа делается ссылка на JP 2017 -533926.
В соответствии с настоящим изобретением, соединение, представленное формулой (1), предпочтительно, производят следующим способом производства. А именно, способ производства включает следующие стадии (i)-(ii), проводимые в указанном порядке, на которых:
(i) осуществляют альдольную конденсацию соединения, представленного формулой (2), приведенной выше, с ацетальдегидом или пропиональдегидом с образованием соединения, представленного формулой (3), приводимой ниже; и
(ii) осуществляют гидрирование соединения, представленного формулой (3), приводимой ниже, с образованием соединения, представленного формулой (1), приведенной выше.
[0043] 
при этом, в формуле (3) R означает атом водорода или метильную группу; и
[0044] Уравнение реакции приведено ниже.
[0045] 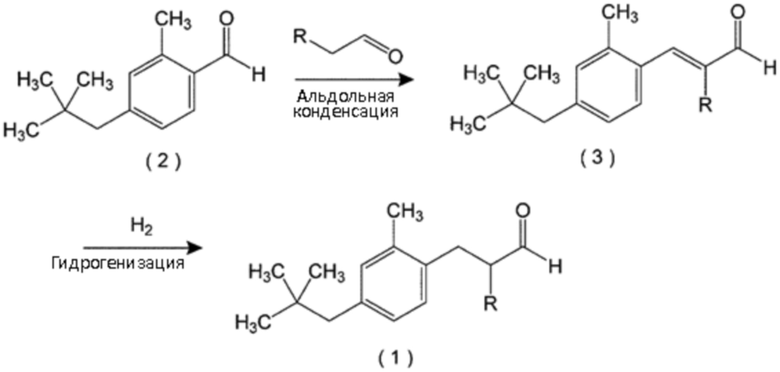
при этом, в формуле (3) R означает атом водорода или метильную группу.
[0046] Стадия (i)
Стадия (i) является стадией, заключающейся в проведении альдольной конденсации соединения, представленного формулой (2), приведенной выше, с ацетальдегидом или пропиональдегидом с образованием соединения, представленного формулой (3), приведенной выше.
Более конкретно, проводят реакцию соединения, представленного формулой (2), с ацетальдегидом или пропиональдегидом, предпочтительно, в присутствии основного соединения в качестве катализатора.
Примерами основного соединения, используемого в качестве катализатора, являются гидроксид натрия, гидроксид калия, бикарбонат натрия или их смесь.
Количество основного соединения составляет, предпочтительно, 0,05 эквивалента или более, более предпочтительно, 0,1 эквивалента или более, еще более предпочтительно, 0,2 эквивалента или более, и составляет, предпочтительно, 3 эквивалента или менее, более предпочтительно, 1 эквивалент или менее, еще более предпочтительно, 0,5 эквивалента или менее относительно одного эквивалента соединения, представленного формулой (2).
Добавляемое количество ацетальдегида или пропиональдегида составляет, предпочтительно, 1,0 эквивалента или более, более предпочтительно, 1,05 эквивалента или более, и составляет, предпочтительно, 1,5 эквивалента или менее, более предпочтительно, 1,1 эквивалента или менее относительно одного эквивалента соединения, представленного формулой (2).
Ацетальдегид или пропиональдегид, предпочтительно, добавляют последовательно или непрерывно во времени, например, предпочтительно, добавляют по каплям.
[0047] Описанную выше реакцию проводят, предпочтительно, в растворителе, и к примерам надлежащего растворителя относятся различные смешивающиеся с водой органические растворители. А именно, предпочтительными примерами являются спирты, такие как метанол, этанол, 1-пропанол, 2-пропанол, трет-бутанол, аллиловый спирт, этиленгликоль, пропиленгликоль и диэтиленгликоль, более предпочтительными примерами являются метанол, этанол, 1-пропанол, 2-пропанол, трет-бутанол, этиленгликоль, пропиленгликоль и диэтиленгликоль.
Температура реакции не имеет определенных ограничений и составляет, предпочтительно, 0°С или выше, более предпочтительно, 3°С или выше, еще более предпочтительно, 5°С или выше с точки зрения скорости реакции и составляет, предпочтительно, 50°С или ниже, более предпочтительно, 40°С или ниже, еще более предпочтительно, 30°С или ниже с точки зрения подавления побочных реакций.
Время реакции не имеет определенных ограничений при условии, что в достаточной степени происходит конденсация, и составляет, предпочтительно, 10 мин или более, более предпочтительно, 30 мин или более, еще более предпочтительно, 1 час или более и составляет, предпочтительно, 24 часа или менее, более предпочтительно, 12 часов или менее, еще более предпочтительно, 6 часов или менее, еще более предпочтительно, 3 часа или менее.
[0048] Реакцию нужно только остановить путем нейтрализации. Например, реакцию нужно только остановить путем добавления кислоты, такой как уксусная кислота.
Кроме этого, способ выделения соединения, представленного формулой (3), из реакционного раствора не имеет определенных ограничений; выделение может быть осуществлено путем надлежащего сочетания методик разделения жидкостей, экстракции, хроматографии и т.п. Например, малополярный или неполярный органический растворитель добавляют в реакционный раствор, соединение, представленное формулой (3) переводят в масляную фазу. Масляную фазу высушивают, например, сульфатом магния. Затем фильтрат, полученный при фильтрации, концентрируют, затем путем очистки концентрата в хроматографической колонке выделяют целевое соединение.
[0049] Стадия (ii)
Стадия (ii) является стадией, на которой осуществляют гидрирование соединения, представленного формулой (3), приведенной выше, полученного на стадии (i), с образованием соединения, представленного формулой (1), приведенной выше.
Способ гидрирования не имеет определенных ограничений; гидрирование может быть проведена любым известным способом с использованием катализатора гидрирования.
Катализатор гидрирования не имеет определенных ограничений; может быть использован любой известный катализатор. Примерами надлежащего катализатора являются гетерогенные катализаторы гидрирования на подложке, в которых металл, такой как Ni, Pt, Pd, Ru и т.п., нанесен на углерод, оксид кремния, оксид алюминия, диатомовую землю и т.п.; так называемый, катализатор гидрирования Циглера, в котором использована соль переходного металла, такая как соль органической кислоты или соль ацетилацетона, и металла, такого как Ni, Co, Fe или Cr и т.п., и восстановитель, такой как алюминийорганическое соединение; и гомогенный катализатор гидрирования, такой как, так называемый, металлоорганический комплекс, содержащий металлоорганическое соединение, такое как Ti, Ru, Rh, Zr и т.п.
[0050] Температура реакции гидрирования составляет, предпочтительно, 0°С или выше, более предпочтительно, 10°С или выше, еще более предпочтительно, 20°С или выше и составляет предпочтительно, 200°С или ниже, более предпочтительно, 150°С или ниже, еще более предпочтительно, 100°С или ниже с точки зрения реакционной способности и подавления побочных реакций.
Давление водорода, используемого в реакции гидрирования, составляет, предпочтительно, 0,01 МПа изб. или более, более предпочтительно, 0,03 МПа изб. или более, еще более предпочтительно, 0,05 МПа изб. или более и составляет, предпочтительно, 10 МПа изб. или менее, более предпочтительно, 3 МПа изб. или менее, еще более предпочтительно, 1 МПа изб. или менее, еще более предпочтительно, 0,5 МПа изб. или менее.
Время реакции не имеет определенных ограничений и составляет, предпочтительно, 3 мин или более, более предпочтительно, 10 мин или более, еще более предпочтительно, 30 мин или более и составляет, предпочтительно, 24 часа или менее, более предпочтительно, 12 часов или менее, еще более предпочтительно, 8 часов или менее.
[0051] Реакция гидрирования может быть проведена в присутствии растворителя. Используемый растворитель не имеет определенных ограничений при условии, что не ингибирует реакцию гидрирования, примерами растворителя являются углеводородные растворители, в том числе: алифатические углеводороды, такие как пентан, гексан, изопентан, гептан, октан и изооктан; циклоалифатические углеводороды, такие как циклопентан, метилциклопентан, циклогексан, метилциклогексан и этилциклогексан; и ароматические углеводороды, такие как бензол, толуол, этилбензол и ксилол. Один тип из указанных может быть использован индивидуально, либо два или несколько типов из указанных могут быть использованы в сочетании.
[0052] Способ выделения и очистки соединения, представленного формулой (1), из реакционного раствора не имеет определенных ограничений; может быть надлежащим образом выбран и осуществлен любой известный способ. Конкретными примерами являются фильтрация, хроматография и дистилляция; они могут быть использованы в сочетании для надлежащей очистки.
ПРИМЕРЫ
[0053] Далее настоящее изобретение описано более подробно на примерах и сравнительных примерах, однако, настоящее изобретение этими примерами не ограничивается.
[0054] Анализ спектра ядерного магнитного резонанса (ЯМР)
Устройство: JEOL JNM-AL-400 400 МГц (от компании JEOL)
Растворитель: дейтерированный хлороформ (CDCl3)
Режим измерения: 1H, 13C
Внутренний стандарт: тетраметилсилан (TMS)
[0055] Масс-спектрометрия
Устройство: GCMS-QP 2010 Ultra (от компании Shimadzu Corporation)
Метод ионизации: EI (электронная ионизация)
[0056] Оценка оттенка
Для проведения оценки оттенка (типа запаха) полученного соединения им пропитывали фильтровальную бумагу шириной 8 мм и длиной 15 см и предоставляли возможность эксперту нюхать фильтровальную бумагу.
[0057] Примеры
В следующих ниже примерах, когда синтезированного количества было недостаточно для обеспечения сырья для последующего синтеза, тот же синтез повторяли много раз до получения необходимого количества.
Синтез 4-неопентилбензальдегида
В качестве реактора формилирования использовали автоклав объемом 500 мл, оборудованный мешалкой типа NAC drive, 3 впускными соплами в верхней части и 1 выпускным соплом в нижней части; внутреннюю температуру в автоклаве регулировали с помощью рубашки.
Хладагент пропускали в рубашке, в охлажденный до -25°С автоклав загружали 134,2 г (6,71 моля) фтороводорода.
Затем при перемешивании добавляли 70,6 г (1,04 моля) трифторида бора и регулировали температуру так, чтобы она не превышала -25°С.
После добавления трифторида бора давление увеличивали до 2 МПа изб. монооксидом углерода, температуру в автоклаве поддерживали равной -25°С и добавляли 1000,0 г (0,67 моля) неопентилбензола (от компании Tokyo Chemical Industry Co., Ltd.).
После перемешивания в течение 90 мин при температуре -25°С и давлении 2 МПа реакционную смесь в автоклаве экстрагировали ледяной водой. Экстрагированную смесь хорошо встряхивали, после чего отделяли масляный слой. После того, как масляный слой нейтрализовали и промыли водой, масляный слой очищали путем дистилляции (131°С, 15 торр) и получили 87,5 г (0,50 моля) 4-неопентилбензальдегида, представлявшего собой бесцветную прозрачную жидкость.
Структурная формула, спектр ЯМР и результаты масс-спектрометрического анализа полученного 4-неопентилбензальдегида были следующими.
[0058] 4-неопентилбензальдегид
1H ЯМР (400 МГц, CDCl3) δ 0,92 (9H, с), 2,58 (2H, с), 7,28-7,30 (2H, д, J=8,0 Гц), 7,78-7,80 (2H, д, J=8,0 Гц), 9,99 (1H, с)
13C ЯМР (100 МГц, CDCl3) ≥≥29,5, 32,1, 50,4, 129,3, 131,1, 134,5, 147,4, 192,2
MS(EI):m/z (%) 57(50), 91(45), 120(100), 161(10), 176(M+・, 5)
[0059] 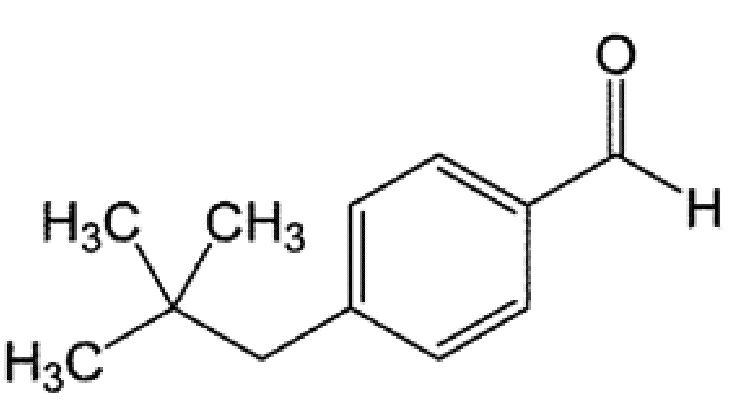
[0060] Синтез 4-неопентилтолуола
50,0 г (0,28 моля) 4-неопентилбензальдегида, 25,0 г гептана и 2,5 г (5% вес.) 10% Pd/C поместили в автоклав объемом 200 мл. После того, как внутреннее пространство реактора продули азотом, начали замещение водородом. Давление увеличили до 1,0 МПа изб., подавая водород, температуру увеличили до 50°С при перемешивании. После увеличения температуры реакцию проводили 10 часов, поддерживая давление и температуру равными 1,0 МПа изб. и 50°С, соответственно.
Сырой реакционный раствор отфильтровали для удаления катализатора, фильтрат сконцентрировали в роторном испарителе. Полученный концентрат очистили путем дистилляции (97°С, 20 торр), и получили 33,9 г (0,21 моля) 4-неопентилтолуола, представлявшего собой бесцветную прозрачную жидкость.
Структурная формула, спектр ЯМР и результаты масс-спектрометрического анализа полученного 4-неопентилтолуола были следующими.
[0061] 4-неопентилтолуол
1H ЯМР (400 МГц, CDCl3) δ 0,89 (9H, с), 2,31 (3H, с), 2,45 (2H, с), 6,99-7,02 (2H, д, J=8,4 Гц), 7,05-7,07 (2H, д, J=8,4 Гц)
13C ЯМР (100 МГц, CDCl3) δ 21,2, 29,5, 31,8, 50,0, 128,5, 130,5, 135,2, 136,8
MS(EI):m/z (%) 57(88), 77(12), 91(41), 106(100), 147(17), 162(M+・, 48)
[0062] 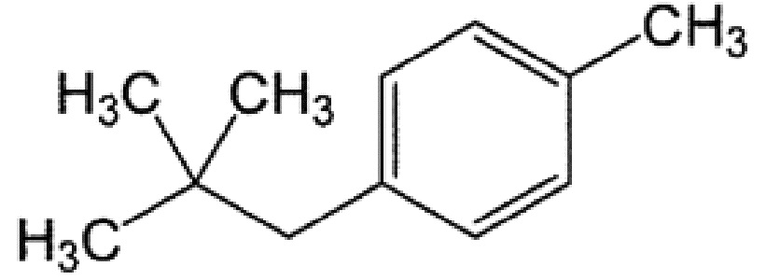
[0063] Синтез 3-неопентилтолуола
В качестве реактора изомеризации использовали автоклав объемом 500 мл, оборудованный мешалкой типа NAC drive, 3 впускными соплами в верхней части и 1 выпускным соплом в нижней части; внутреннюю температуру в автоклаве регулировали с помощью рубашки.
Хладагент пропускали в рубашке, в охлажденный до 0°С автоклав загружали 191,5 г (9,57 моля) фтороводорода.
Затем при перемешивании добавляли 47,7 г (0,70 моля) трифторида бора и регулировали температуру так, чтобы она не превышала 15°С.
После добавления трифторида бора добавляли смешанный раствор 38,5 г (0,24 моля) 4-неопентилтолуола и 38,5 г гексана, поддерживая температуру в автоклаве равной 15°С.
После перемешивания в течение 4 часов при температуре 15°С реакционную смесь в автоклаве экстрагировали ледяной водой. После того, как выгружаемый продукт хорошо встряхнули, масляный слой отделяли и промывали нейтрализованной водой.
Эти операции осуществили три раза, весь полученный масляный слой сконцентрировали в роторном испарителе. Полученный концентрат очистили путем дистилляции (93°С, 20 торр), и получили 87,0 г (0,53 моля) 3-неопентилтолуола, представлявшего собой бесцветную прозрачную жидкость.
Структурная формула, спектр ЯМР и результаты масс-спектрометрического анализа полученного 3-неопентилтолуола были следующими.
[0064] 3-неопентилтолуол
1H ЯМР (400 МГц, CDCl3) δ 0,90 (9H, с), 2,33 (3H, с), 2,45 (2H, с), 6,91-6,93 (1H, д, J=8,0 Гц), 6,93 (1H, с), 7,00-7,02 (1H, д, J=7,6 Гц), 7,13-7,17 (1H, т, J=7,6 Гц)
13C ЯМР (100 МГц, CDCl3) δ 21,6, 29,6, 31,8, 50,3, 126,6, 127,6, 127,7, 131,4, 137,1, 139,8
MS(EI):m/z (%) 57(96), 77(13), 91(45), 106(100), 147(16), 162(M+・, 48)
[0065] 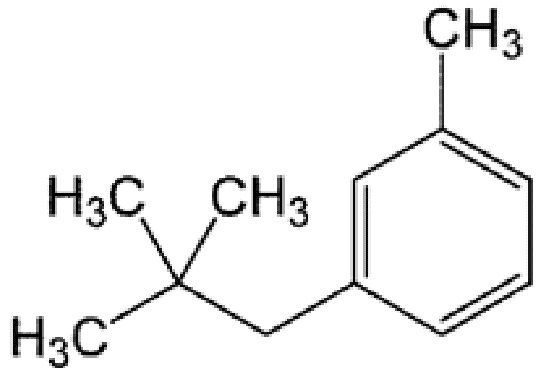
[0066] Синтез 2-метил-4-неопентилбензальдегида
В качестве реактора формилирования использовали автоклав объемом 500 мл, оборудованный мешалкой типа NAC drive, 3 впускными соплами в верхней части и 1 выпускным соплом в нижней части; внутреннюю температуру в автоклаве регулировали с помощью рубашки.
Хладагент пропускали в рубашке, в охлажденный до -25°С автоклав загружали 43,0 г (2,15 моля) фтороводорода.
Затем при перемешивании добавляли 29,5 г (0,44 моля) трифторида бора и регулировали температуру так, чтобы она не превышала -25°С.
После добавления трифторида бора давление увеличивали до 2 МПа изб. монооксидом углерода, температуру в автоклаве поддерживали равной -25°С и добавляли 47,1 г (0,29 моля) 3-неопентилтолуола и 47,1 г гептана.
После перемешивания в течение 120 мин при температуре -25°С и давлении 2 МПа реакционную смесь в автоклаве экстрагировали ледяной водой. После того, как выгружаемый продукт хорошо встряхивали, масляный слой отделяли и промыли нейтрализованной водой.
Эти операции осуществили три раза, весь полученный масляный слой сконцентрировали в роторном испарителе, концентрат очистили путем дистилляции (139°С, 15 торр) и получили 82,1 г (0,43 моля) 2-метил-4-неопентилбензальдегида, представлявшего собой бесцветную прозрачную жидкость.
Структурная формула, спектр ЯМР и результаты масс-спектрометрического анализа полученного 4-неопентилбензальдегида были следующими.
[0067] 2-метил-4-неопентилбензальдегид
1H ЯМР (400 МГц, CDCl3) δ 0,92 (9H, с), 2,52 (2H, с), 2,65 (3H, с), 7,01 (1H, с), 7,11-7,13 (1H, д, J=7,6 Гц), 7,69-7,71 (1H, д, J=7,6 Гц), 10,23 (1H, с)
13C ЯМР (100 МГц, CDCl3) δ 19,7, 29,5, 32,1, 50,3, 128,5, 131,8, 132,3, 133,9, 139,9, 146,4, 192,5
MS(EI):m/z (%) 57(65), 77(8), 91(26), 105(40), 134(100), 175(11), 190(M+・, 29)
[0068] 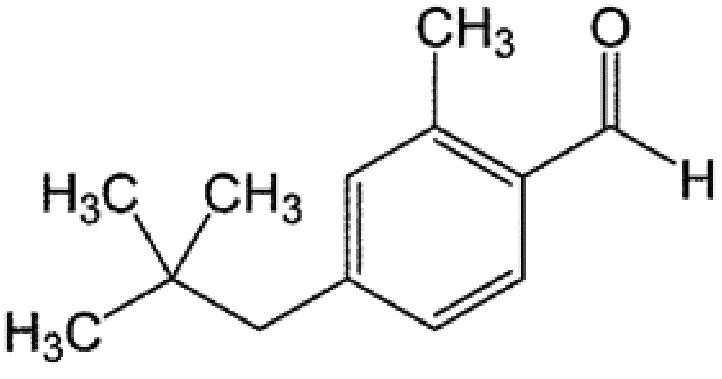
[0069] Синтез (Е)-3-(2-метил-4-неопентилфенил)пропеналя
В круглодонную колбу объемом 100 мл поместили 15,0 г (0,08 моля) 2-метил-4-неопентилбензальдегида, 15 г метанола в качестве растворителя и 2,1 г (0,03 моля) 50% водного раствора NaOH в качестве катализатора и охладили до 10°С.
Затем по каплям при перемешивании добавили 3,9 г (0,09 моля) ацетальдегида, поддерживая температуру не более 15°С. Спустя 2 часа реакции добавили 2,0 г (0,03 моля) уксусной кислоты для закалки.
После закалки провели операции экстрагирования и разделения, используя гептан, масляный слой высушили сульфатом магния, фильтрат, полученный при фильтрации, сконцентрировали в роторном испарителе.
Полученный концентрат очистили в хроматографической колонке (силикагель, гексан:этилацетат=93:7) и получили 5,0 г (0,02 моля) (Е)-3-(2-метил-4-неопентилфенил)пропеналя, представлявшего собой желтый твердый материал.
Структурная формула, спектр ЯМР и результаты масс-спектрометрического анализа полученного (Е)-3-(2-метил-4-неопентилфенил)пропеналя были следующими.
[0070] (Е)-3-(2-метил-4-неопентилфенил)пропеналь
1H ЯМР (400 МГц, CDCl3) δ 0,92 (9H, с), 2,47 (3H, с), 2,49 (2H, с), 6,63-6,69 (1H, дд, J=7,6 Гц, 16 Гц), 7,01 (1H, с), 7,01-7,03 (1H, д, J=9,6 Гц), 7,51-7,53 (1H, д, J=7,6 Гц), 7,74-7,78 (1H, д, J=16 Гц), 9,70-9,72 (1H, д, J=7,6 Гц)
13C ЯМР (100 МГц, CDCl3) δ 19,9, 29,6, 32,1, 50,2, 126,3, 128,8, 129,0, 130,5, 133,3, 137,4, 143,7, 150,6, 194,1
MS(EI):m/z (%) 57(71), 91(11), 115(16), 131(17), 145(100), 160(70), 201(29), 216(M+・, 16)
[0071] 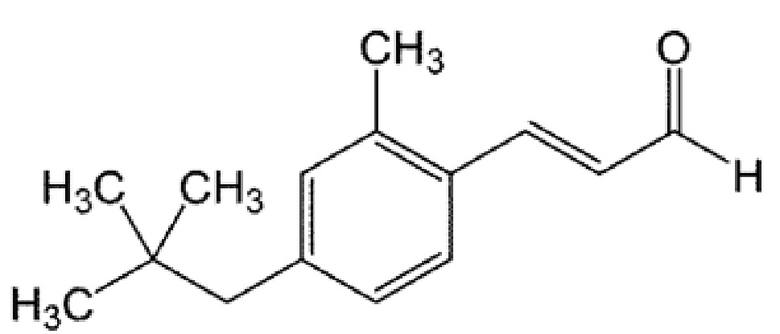
[0072] Синтез 3-(2-метил-4-неопентилфенил)пропаналя
0,7 г (0,003 моля) (Е)-3-(2-метил-4-неопентилфенил)-пропеналя, 35,0 г гептана в качестве растворителя и 0,07 г (10% вес.) 10% Pd/C в качестве катализатора поместили в автоклав объемом 200 мл. После того, как внутреннее пространство реактора продули азотом, начали замещение водородом. Давление увеличили до 0,1 МПа изб., подавая водород, смесь перемешивали. После увеличения давления реакцию проводили 1 час, поддерживая давление и температуру равными 0,1 МПа изб. и 25°С, соответственно.
Сырой реакционный раствор отфильтровали для удаления катализатора, фильтрат сконцентрировали в роторном испарителе. Полученный концентрат очистили в хроматографической колонке (силикагель, гексан:этилацетат=96:4) и получили 0,4 г (0,002 моля) 3-(2-метил-4-неопентилфенил)пропаналя, представлявшего собой бесцветную прозрачную жидкость.
Структурная формула, спектр ЯМР, результаты масс-спектрометрического анализа и оттенок полученного 3-(2-метил-4-неопентилфенил)пропаналя были следующими.
[0073] 3-(2-метил-4-неопентилфенил)пропаналь
1H ЯМР (400 МГц, CDCl3) δ 0,89 (9H, с), 2,29 (3H, с), 2,42 (2H, с), 2,71-2,75 (2H, т, J=7,8 Гц), 2,90-2,94 (2H, т, J=7,8 Гц), 6,89-6,91 (1H, д, J=7,6 Гц), 6,91 (1H, с), 7,00-7,02 (1H, д, J=7,2 Гц), 9,85 (1H, с)
13C ЯМР (100 МГц, CDCl3) δ 19,5, 25,2, 29,5, 31,8, 44,2, 49,8, 127,8, 128,4, 132,7, 135,1, 135,7, 138,0, 202,0
MS(EI):m/z (%) 57(100), 77(7), 91(19), 105(19), 118(57), 129(28), 144(90), 162(25), 203(8), 218(M+・, 30)
Оттенок: ландыш, белый цветочный, альдегидный, зеленый
Отметим, что оттенок имел маслянистую ноту морского бриза, немного более сильную, чем у лилиаля, и представлял собой оттенок, похожий на промежуточный между лилиалем и сильвиалем.
[0074] 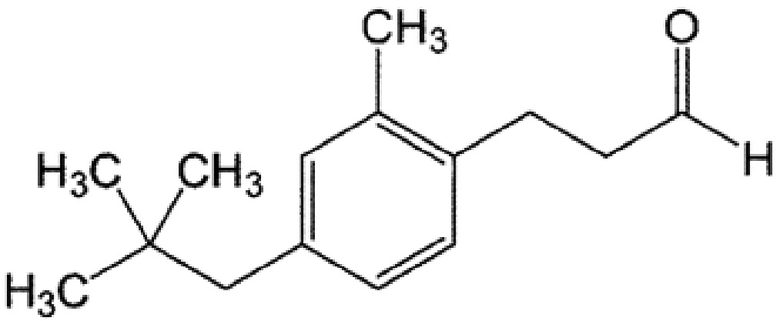
[0075] Синтез (Е)-3-(2-метил-4-неопентилфенил)-2-пропеналя
В круглодонную колбу объемом 100 мл поместили 15,0 г (0,08 моля) 2-метил-4-неопентилбензальдегида, 15,0 г метанола в качестве растворителя и 2,0 г (0,03 моля) 50% водного раствора NaOH в качестве катализатора и поддерживали температуру равной 25°С.
Затем по каплям при перемешивании добавили 5,0 г (0,09 моля) пропиональдегида, поддерживая температуру не более 25°С. Спустя 2 часа реакции добавили 1,6 г (0,03 моля) уксусной кислоты для закалки.
После закалки провели операции экстрагирования и разделения, используя гептан, масляный слой высушили сульфатом магния, фильтрат, полученный при фильтрации, сконцентрировали в роторном испарителе.
Полученный концентрат очистили в хроматографической колонке (силикагель, гексан:этилацетат=95:5) и получили 13,3 г (0,06 моля) (Е)-3-(2-метил-4-неопентилфенил)-2-метилпропеналя, представлявшего собой желтую жидкость.
Структурная формула, спектр ЯМР и результаты масс-спектрометрического анализа полученного (Е)-3-(2-метил-4-неопентилфенил)-2-метилпропеналя были следующими.
[0076] (E)-3-(2-метил-4-неопентилфенил)-2-метилпропеналь
1H ЯМР (400 МГц, CDCl3) δ 0,93 (9H, с), 1,98 (3H, с), 2,35 (3H, с), 2,49 (2H, с), 7,01-7,03 (1H, д, J=6,4 Гц), 7,03 (1H, с), 7,28-7,30 (1H, д, J=8,4 Гц), 7,43 (1H, с), 9,63 (1H, с)
13C ЯМР (100 МГц, CDCl3) δ 11,0, 19,9, 29,4, 31,8, 50,0, 127,9, 128,3, 131,4, 132,6, 136,5, 138,5, 141,3, 148,3, 195,5
MS(EI):m/z (%) 57(56), 91(7), 105(7), 115(10), 128(12), 145(11), 159(100), 174(33), 215(46), 230(M+・,12)
[0077] 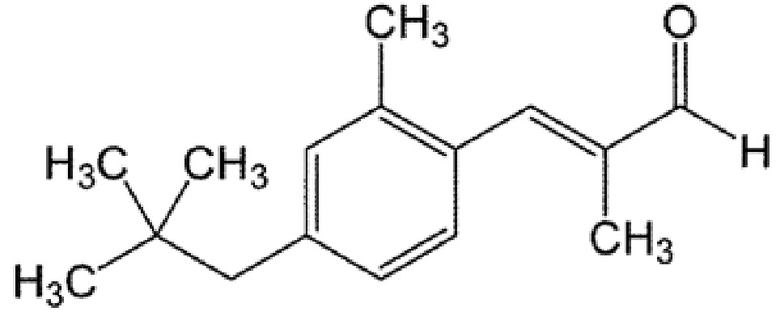
[0078] Синтез 3-(2-метил-4-неопентилфенил)-2-метилпропаналя
13,3 г (0,006 моля) (Е)-3-(2-метил-4-неопентилфенил)-2-метилпропеналя, 40,0 г 5% водного раствора Na2CO3 и 0,3 г (2% вес.) 5% Pd/C поместили в автоклав объемом 200 мл. После того, как внутреннее пространство реактора продули азотом, начали замещение водородом. Давление увеличили до 0,4 МПа изб., подавая водород, температуру увеличили до 75°С. После увеличения температуры реакцию проводили 7 часов, поддерживая давление и температуру равными 0,4 МПа изб. и 75°С, соответственно.
Сырой реакционный раствор отфильтровали для удаления катализатора, фильтрат сконцентрировали в роторном испарителе. Полученный концентрат очистили в хроматографической колонке (силикагель, гексан:этилацетат=96:4), затем очистили путем дистилляции (102°С, 1 торр) и получили 6,7 г (0,03 моля) 3-(2-метил-4-неопентилфенил)-2-метилпропаналя, представлявшего собой бесцветную прозрачную жидкость.
Структурная формула, спектр ЯМР, результаты масс-спектрометрического анализа и оттенок полученного 3-(2-метил-4-неопентилфенил)-2-метилпропаналя были следующими.
[0079] 3-(2-метил-4-неопентилфенил)-2-метилпропаналь
1H ЯМР (400 МГц, CDCl3) δ 0,89 (9H, с), 1,10-1,12 (3H, д, J=6,8 Гц), 2,29 (3H, с), 2,43 (2H, с), 2,54-2,57 (1H, дд, J=8,4 Гц, 14,0 Гц), 2,63-2,68 (1H, м), 3,05-3,10 (1H, дд, J=6,0 Гц, 14,0 Гц), 6,89-6,91 (1H, д, J=7,6 Гц), 6,92 (1H, с), 6,99-7,01 (1H, д, J=7,6 Гц), 9,72 (1H, с)
13C ЯМР (100 МГц, CDCl3) δ 13,6, 19,6, 29,5, 31,8, 33,7, 47,0, 49,8, 128,2, 129,0, 032,8, 134,4, 135,3, 138,0, 204,7
MS(EI):m/z (%) 57(93), 77(6), 91(12), 105(27), 119(100), 131(8), 143(24), 158(64), 175(25), 214(8), 232(M+・,38)
Оттенок: ландыш, белый цветочный, зеленый, древесный
Отметим, что оттенок имел ноту морского бриза и альдегидную ному, немного более слабые, чем у лилиаля, и, соответственно, был немного похож на древесно-амбровый с чистым ландышевым тоном. Было понятно, что это соединение обладает большим потенциалом с точки зрения оттенка запаха.
[0080] 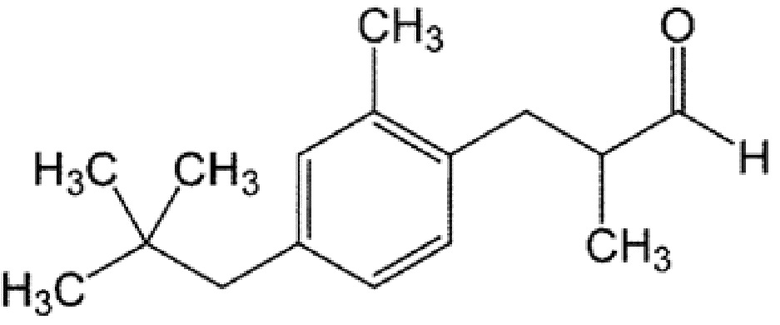
[0081] 1 оценка парфюмерной композиции
Результаты оценки запаха 3-(2-метил-4-неопентилфенил)-пропаналя выявили оттенок, сходный с лилиалем и сильвиалем. Следовательно, провели оценку следующих трех композиций, которые представляют собой модельные композиции лилиаля, после того, как в них вместо лилиаля добавили 3-(2-метил-4-неопентилфенил)пропаналь.
Композиции 1-3 представлены в таблице, приведенной ниже. Отметим, что композиция 1 имеет цветочный пудровый оттенок, композиция 2 имеет оттенок ландыша, композиция 3 имеет фруктово-цветочный оттенок.
[0082] Таблица 1-1
* массовых частей
** диметилбензилкарбинил
[0083] Таблица 1-2
* массовых частей
** дипропиленгликоль
[0084] Таблица 1-3
* массовых частей
** диметилбензилкарбинил
*** дипропиленгликоль
[0085] Композиция 1: Примеры 1-1 и 1-2
В примере 1-1 парфюмерную композицию получили таким же образом за исключением того, что в композицию 1 добавили 320 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя вместо 320 масс. частей лилиаля, и изучили ее оттенок.
Кроме этого, в примере 1-2 парфюмерную композицию получили таким же образом за исключением того, что в композицию 1 добавили 120 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя и 200 масс. частей дипропиленгликоля вместо 320 масс. частей лилиаля, и изучили ее оттенок. То есть, в примере 1-2 произвели оценку при добавленном количестве, уменьшенном до 37,5% лилиаля.
Отметим, что дипропиленгликоль не имеет запаха и добавлен для разбавления 3-(2-метил-4-неопентилфенил)пропаналя.
[0086] Композиция 2: Примеры 2-1 и 2-2
В примере 2-1 парфюмерную композицию получили таким же образом за исключением того, что в композицию 2 добавили 350 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя вместо 350 масс. частей лилиаля, и изучили ее оттенок.
Кроме этого, в примере 2-2 парфюмерную композицию получили таким же образом за исключением того, что в композицию 2 добавили 150 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя и 200 масс. частей дипропиленгликоля вместо 350 масс. частей лилиаля, и изучили ее оттенок. То есть, в примере 2-2 произвели оценку при добавленном количестве, уменьшенном до 42,9% лилиаля.
[0087] Композиция 3: Примеры 3-1 и 3-2
В примере 3-1 парфюмерную композицию получили таким же образом за исключением того, что в композицию 3 добавили 50 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя вместо 50 масс. частей лилиаля, и изучили ее оттенок.
Кроме этого, в примере 3-2 парфюмерную композицию получили таким же образом за исключением того, что в композицию 3 добавили 20 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя и 30 масс. частей дипропиленгликоля вместо 50 масс. частей лилиаля, и изучили ее оттенок. То есть, в примере 3-2 произвели оценку при добавленном количестве, уменьшенном до 40% лилиаля.
[0088] Оценка оттенка
Каждую из композиций 1-3, описанных выше, разбавили 10-ркатно 9000 частями триэтилцитрата и изучили оттенок запаха парфюмерных композиций.
Для оценки оттенка соединением пропитывали фильтровальную бумагу шириной 8 мм и длиной 15 см и предоставляли возможность эксперту нюхать фильтровальную бумагу.
[0089] В результате оценки оттенка запаха парфюмерной композиции и в результате сравнения парфюмерных композиций, полученных в примерах 1-1, 2-1 и 3-1, с композициями 1, 2 и 3, соответственно, установлено, что имеется оттенок, подобный оттенку композиций 1, 2 и 3, каждая из которых представляет собой парфюмерную композицию, содержащую лилиаль, но интенсивность запаха выше.
Кроме этого, в результате оценки оттенка в каждом из примеров 1-2, 2-2 и 3-2, в которых добавленное количество было уменьшено, установлено наличие запаха, интенсивность которого сравнима со случаем, в котором добавляли лилиаль. Было показано, что 3-(2-метил-4-неопентилфенил)пропаналь является более сильным душистым веществом, чем лилиаль.
[0090] Оценка стойкости запаха
Стойкость запаха оценивали путем сравнения с лилиалем. Участок длиной 1 см на конце фильтровальной бумаги шириной 8 мм и длиной 15 см пропитывали 3-(2-метил-4-неопентилфенил)пропаналем и лилиалем и оценивали интенсивность запаха непосредственно после пропитывания. Затем фильтровальную бумагу оставляли при комнатной температуре и оценивали интенсивность каждого запаха через 6 часов и 18 часов.
[0091] В результате оценки стойкости запаха установлено, что 3-(2-метил-4-неопентилфенил)пропаналь имел достаточно сильный запах даже через 6 часов, и запах ощущался как более интенсивный, чем запах лилиаля. Через 18 часов 3-(2-метил-4-неопентилфенил)пропаналь еще имел запах, тогда как запах лилиаля был очень слабым и едва уловимым.
[0092] 2 оценка парфюмерной композиции
В документе JP 2018-138550A в качестве душистого вещества, альтернативного лилиалю, описано следующее соединение (далее, нимфеаль). Таким образом, провели оценку двух описанных далее композиций, представлявших собой модельные композиции нимфеаля, в которые вместо нимфеаля добавили 3-(2-метил-4-неопентилфенил)пропаналь.
Композиции 4 и 5 представлены в таблице, приведенной ниже. Отметим, что композиция 4 имеет зеленый цветочный оттенок, и композиция 5 имеет цветочно-фруктовый оттенок.
[0093] 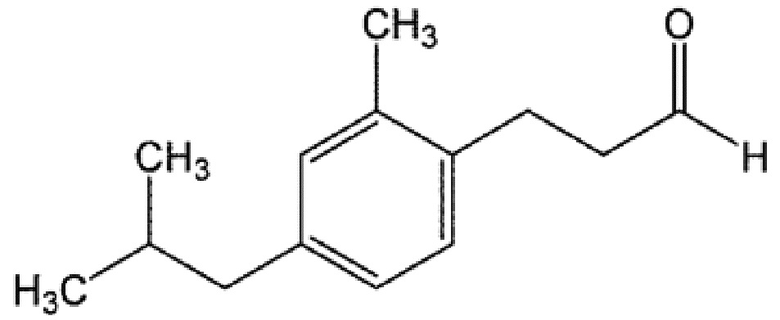 нимфеаль
нимфеаль
[0094] Таблица 2-1
* массовых частей
** дипропиленгликоль
[0095] Таблица 2-2
* массовых частей
** диметилбензилкарбинил
*** дипропиленгликоль
[0096] Композиция 4: пример 4
В примере 4 парфюмерную композицию получили таким же образом за исключением того, что в композицию 4 добавили 50 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя вместо 50 масс. частей нимфеаля, и изучили ее оттенок.
[0097] Композиция 5: пример 5
В примере 5 парфюмерную композицию получили таким же образом за исключением того, что в композицию 5 добавили 180 масс. частей 3-(2-метил-4-неопентилфенил)пропаналя вместо 180 масс. частей нимфеаля, и изучили ее оттенок.
[0098] Оценка оттенка
Оттенок парфюмерной композиции оценивали в отношении описанных выше композиций 4 и 5.
Для оценки оттенка соединением пропитывали фильтровальную бумагу шириной 8 мм и длиной 15 см и предоставляли возможность эксперту нюхать фильтровальную бумагу.
[0099] В результате оценки оттенка запаха парфюмерных композиций и в результате сравнения парфюмерных композиций, полученных при примере 4 и примере 5, с композицией 4 и композицией 5, соответственно, было установлено наличие сильного обонятельного импульса и высокой интенсивности средней ноты в примерах 4 и 5. Более конкретно, спустя от 30 минут до, примерно, 3 часов отчетливее воспринималось плотное и сильное зеленое цветочное ощущение.
Применимость в промышленности
[0100] Соединение, представленное формулой (1), соответствующее настоящему изобретению, пригодно для использования в качестве душистого вещества (сырья для парфюмерной композиции); ожидается, что оно найдет применение в качестве душистого вещества, альтернативного лилиалю. Кроме этого, было обнаружено, что соединение, представленное формулой (1), соответствующее настоящему изобретению, является более сильным душистым веществом с более стойким запахом, чем лилиаль. Кроме этого, даже по сравнению с нимфеалем, который представляет собой другую альтернативу лилиалю, было обнаружено, что данное соединение обладает особенно высокой интенсивностью средней ноты и замечательным ароматом.
Изобретение относится к соединению формулы (1) класса альдегидов, где R означает атом водорода. Также изобретение относится к парфюмерной композиции, содержащей соединение формулы (1), и его применению в качестве душистого вещества. Способ производства соединения формулы (1) включает альдольную конденсацию соединения формулы (2) с ацетальдегидом с образованием соединения формулы (3) и гидрирование соединения формулы (3) с образованием соединения формулы (1), где R в соединении формулы (3) означает атом водорода. Технический результат - соединение формулы (1), пригодное для использования в качестве душистого вещества и компонента парфюмерной композиции. 4 н.п. ф-лы, 5 табл., 8 пр.
 ,
,  ,
,  .
.
1. Соединение, представленное формулой (1)
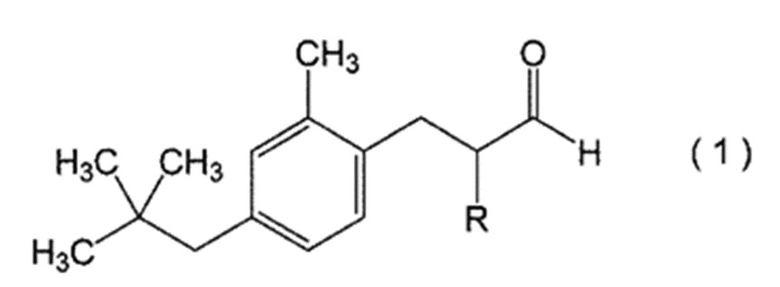
при этом в формуле (1) R означает атом водорода.
2. Парфюмерная композиция, содержащая соединение по п.1 в количестве от 0,001% масс. или более и 90 масс. или менее.
3. Применение соединения по п.1 в качестве душистого вещества.
4. Способ производства соединения, представленного формулой (1), при этом способ включает следующие стадии, осуществляемые в указанном порядке, на которых проводят альдольную конденсацию соединения, представленного формулой (2), с ацетальдегидом с образованием соединения, представленного формулой (3); и проводят гидрирование соединения, представленного формулой (3), с образованием соединения, представленного формулой (1):
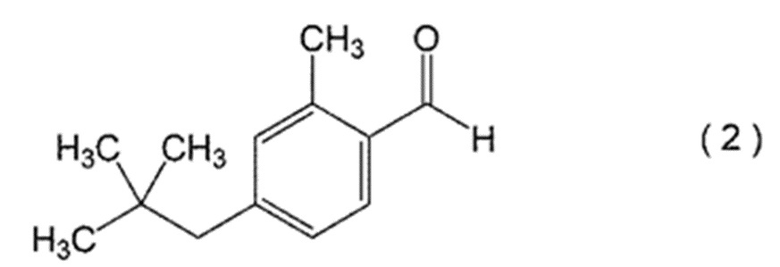
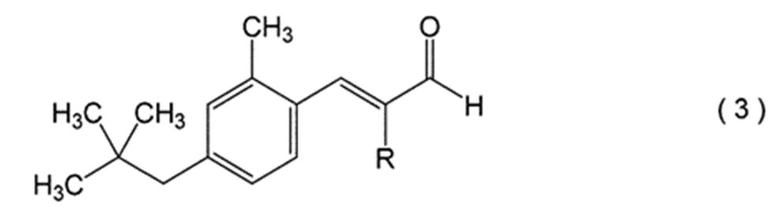
при этом в формуле (3) R означает атом водорода; и
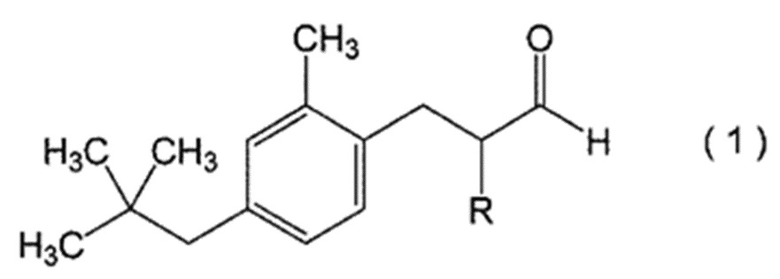
при этом в формуле (1) R означает атом водорода.
| JP 2016523828 A, 12.08.2016 | |||
| JP 2018502057 A, 25.01.2018 | |||
| JP 2016530227 A, 29.09.2016 | |||
| Усовершенствование органических соединений или усовершенствование, относящееся к органическим соединениям | 2014 |
|
RU2669029C1 |
Авторы
Даты
2025-02-17—Публикация
2020-10-16—Подача