Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии.
Популярность коронарного шунтирования без искусственного кровообращения (OPCAB) значительно варьирует по всему миру от 20% в Европе и США до 56% в Азии [1]. В настоящее время большинство исследователей придерживаются мнения о том, что OPCAB снижает частоту таких ранних клинических осложнений, как низкий сердечный выброс, послеоперационная почечная дисфункция, потребность в переливании крови и продолжительность пребывания в отделении интенсивной терапии и стационаре [2]. Доказано, что OPCAB позволяет достигать лучших результатов по смертности и неблагоприятным сердечно-сосудистым событиям в группах высокого хирургического риска, в частности у пациентов с нарушенной функцией левого желудочка [3]. В рекомендациях ESC/EACTS 2018 года по реваскуляризации миокарда OPCAB показана для подгрупп пациентов с высоким риском, которые должны быть оперированы хирургами с опытом подобных вмешательств (класс IIа, уровень Б) [4,5].
Функционирование аутовенозных шунтов зависит от многих факторов, включая исходное состояние подкожной вены, диаметр целевой коронарной артерии и состояние дистального русла, хирургические навыки, интраоперационную обработку венозного кондуита, консервативную терапию в послеоперационном периоде [6]. Одним из модифицируемых, но часто недооцененных факторов улучшения функционального состояния венозных кондуитов является интраоперационная подготовка венозных кондуитов, в том числе гидравлическая дилатация. Гидравлическую дилатацию венозных кондуитов повсеместно применяют для профилактики спазма, возникающего вследствие сокращения гладких миоцитов в ответ на различные раздражители, и для оценки герметичности расправленного венозного кондуита. Классическая методика подразумевает ручное нагнетание раствора под неконтролируемо высоким давлением. При неконтролируемой дилатации венозных кондуитов нагнетается давление, порой превышает 300 мм рт. ст., а радиальное давление на стенку кондуита может достигать 600-700 мм рт. ст. [7]. Дилатация под неконтролируемым давлением оказывает отрицательное действие на морфофункциональное состояние венозного кондуита [8]. Формируются структурные нарушения в виде очаговой и диффузной десквамации эндотелия, деформации и изменения конфигурации сохранившихся эндотелиоцитов, а также деструкции и некроза гладких миоцитов медии [9]. Выбор среды хранения и способа гидравлической дилатации крайне важен для сохранения морфофункциональной целостности венозных кондуитов. Применение физиологического раствора становится причиной повреждения и изменения конфигурации эндотелия и отека стенки [10]. Наиболее оптимальной и доступной средой для хранения и дилатации венозных кондуитов является гепаринизированная кровь, так как она обеспечивает воздействие тех же белков, буферных систем и электролитов, что и in vivo. Применение крови для хранения и гидравлической дилатации венозных кондуитов позволяет добиться оптимальных результатов целостности структур венозной стенки и эндотелий-зависимой вазорелаксации [9]. Таким образом, разработка способов подготовки кондуита, сочетающих атравматичную дилатацию, не превышающую физиологического уровня артериального давления с использованием гепаринизированной крови, является актуальной для морфофункциональной сохранности венозного кондуита.
Известен способ оптимальной гидравлической дилатации в процессе подготовки аутовенозных кондуитов при операциях коронарного шунтирования, защищенный патентом Российской Федерации на изобретение № 2661735 [https://patenton.ru/patent/RU2661735C1], где интактный венозный кондуит после выделения канюлируют и помещают в холодный раствор гепаринизированной крови. К аортальной магистрали аппарата искусственного кровообращения через порт Люера предварительно присоединяют переходник в форме тройника, к которому фиксируют дополнительный переходник по типу «папа-папа» для соединения с венозным кондуитом. После канюляции аорты венозный кондуит через переходники соединяют с аортальной магистралью. Запускают искусственное кровообращение с перфузионным давлением 50-70 мм рт. ст. (в среднем 65 мм рт. ст.), тщательно проверяют герметичность кондуита, накладывают дополнительные сосудистые клипы.
Недостатком данного способа является снижение артериального давления во время искусственной перфузии, что препятствует эффективному расправлению вены и контролю герметичности.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задачей изобретения является: создание способа, позволяющего исключить травмирующее влияние неконтролируемого гидродинамического давления на стенку будущего венозного шунта, негативное влияние высокого гидростатического давления на морфофункциональное состояние вены и обеспечить оптимальные условия кондиционирования вплоть до формирования аортокоронарного шунта.
Поставленная задача решается способом, представляющим собой присоединение большой подкожной вены к восходящей аорте с помощью кардиоплегической канюли, через систему переходников после ее забора. Выполняют пуск крови из аорты снятием зажима с кардиоплегической канюли. Свободным потоком артериальной крови из аорты вымывают остаточные тромбы, затем накладывают мягкий сосудистый зажим на свободный конец кондуита. Начинают дилатацию, артериальным давлением из аорты с контролем герметичности сосуда, этим исключают травмирующее влияние неконтролируемого гидродинамического давления на стенку будущего венозного шунта. Далее кондуит оставляют в положении дилатации с открытой кардиоплегической канюлей вплоть до момента его использования. Таким образом, кондуит остается расправленным и заполненным артериальной кровью из аорты вплоть до использования.
Идентичной совокупности признаков не обнаружено в патентной и научно-медицинской литературе.
Предлагаемый в качестве изобретения способ может быть использован для подготовки венозного кондуита к аортокоронарному шунтированию на работающем сердце у больных ишемической болезнью сердца, чем повышает качество лечения.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Изобретение будет понятно из следующего описания и приложенных к нему фигур.
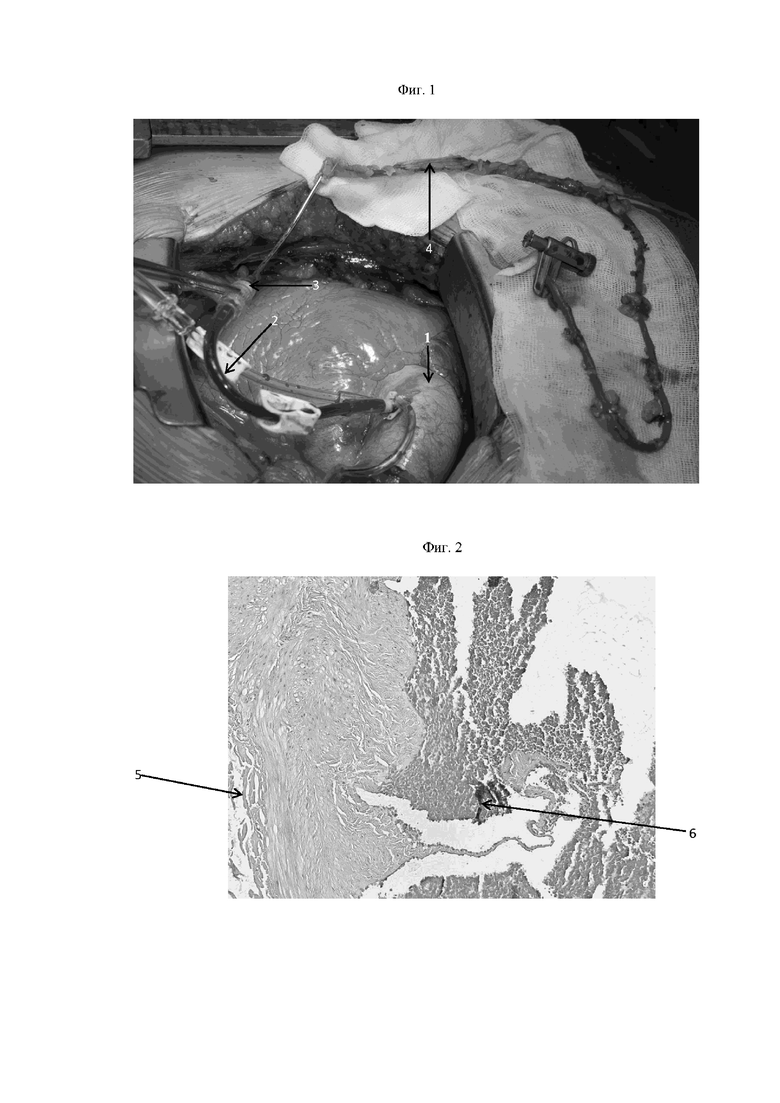
На фиг.1 изображен способ дилатации венозного кондуита для аортокоронарного шунтирования без искусственного кровообращения.
1. Аорта.
2. Кардиоплегическая канюля.
3. Игла ирригационная.
4. Реверсивная вена с зажимом на свободном конце.
На фиг.2 - морфологическая картина изменений стенки сосуда после ручной гидравлической дилатации. Отслоение эндотелия и пристеночный тромбоз. Ув.600, гематоксилин эозин.
5. Отслоение эндотелия.
6. Пристеночный тромбоз.
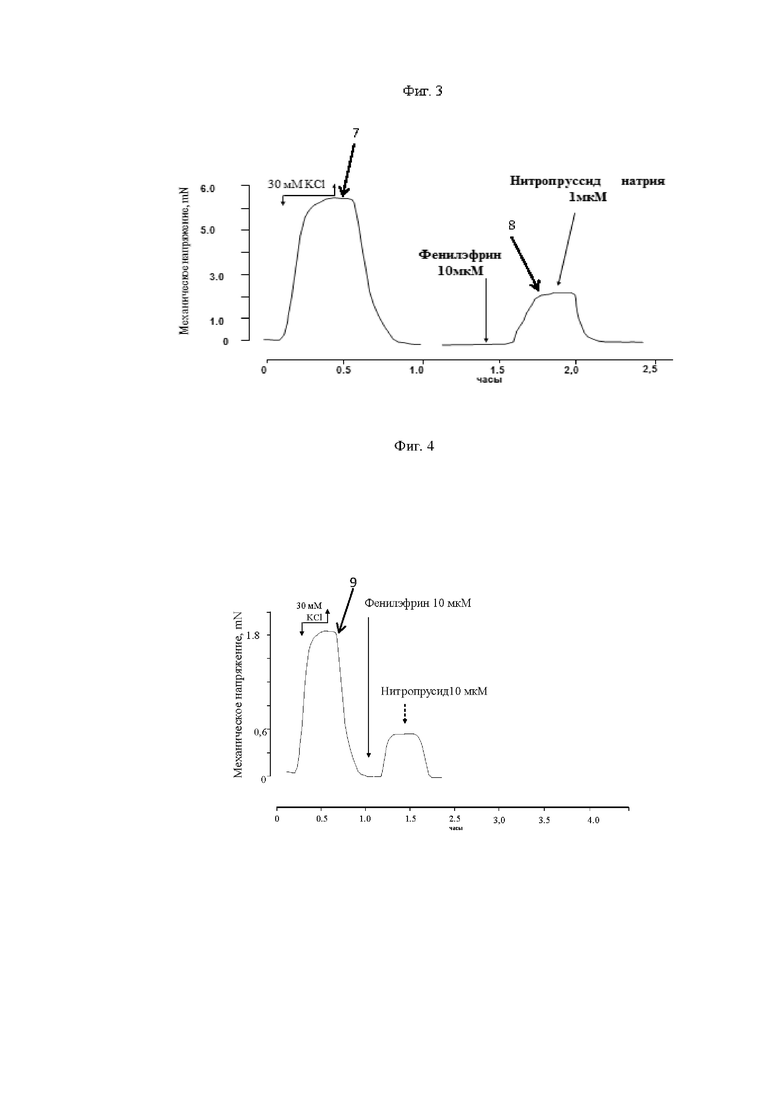
На фиг.3 - исследование сократительного ответа вены после предлагаемого способа дилатации.
7. Физиологическая дилатации из восходящей аорты.
На фиг.4 - исследование сократительного ответа венозного кондуита после ручной гидравлической дилатации.
8. Снижение амплитуды мышечного напряжения на всех фазах исследования.
Способ осуществляют следующим образом: Положение пациента на спине. После индукционного вводного наркоза проводят интубацию, катетеризируют центральную вену и лучевую артерию слева. В условиях нейролептаналгезии готовят операционное поле раствором антисептика и драпировку. Выполняют стернотомию с последующей Т-образной перикардиотомией. Вводят раствор гепарина 300 ЕД на 1 кг массы тела больного. Параллельно выделяют большую подкожную вену с разрезом кожи, на протяжении необходимой длины кондуита. На восходящую аорту 1 в месте планируемого расположения проксимальной части шунта накладывают кисетный или П-образный шов и устанавливают кардиоплегическую канюлю 2. Последнюю через стандартный переходник соединяют с ирригационной иглой 3, оливу которой фиксируют в реверсированной вене, с перекрытым зажимом свободным концом 4 (Фиг.1). Затем зажим с вены снимают. Аортальным давлением вымывают остаточные тромбы и воздух до получения равномерной струи крови. Вновь накладывают зажим на кондуит и начинают гидравлическую дилатацию с помощью артериального давления из аорты. На расправленной вене производят ревизию кондуита и клипируют незакрытые коллатерали. В положении дилатации кондуит оставляют вплоть до использования.
Клинический пример
Пациент С., 60 лет. Диагноз: ИБС. Стенокардия напряжения, ФК III. Атеросклероз коронарных артерий (Правый тип кровоснабжения. Правая коронарная артерия окклюзия в 1/3, передняя нисходящая артерия стеноз в 2/3 75%, ). НК I, ФК II по NYHA.
Эхокардиография до операции: нарушения глобальной и локальной сократимости, патологии клапанов не выявлено. Ультразвуковое сканирование вен нижних конечности: вены проходимы, не расширены, компрессивность сохранена. 17.11.23 - выполнена операция аортокоронарного и маммарокоронарного шунтирования коронарных артерий без искусственного кровообращения. После забора вены и оценки необходимой длины, излишний сегмент вены отсекли и использовали для ручной стандартной гидравлической дилатации для сравнительных исследований. Основной сегмент вены, предназначенный для шунтирования дилатировали предложенным способом из аорты. По окончании основного этапа выполняли флоуметрическую оценку кровотока по шунтам: объемная кровотока 56 мл/мин пульсативный индекс 1,7, диастолическое наполнение 70%. Операция закончена в обычном порядке. Образцы вен ручной неуправляемой гидравлической дилатации и физиологической дилатации из восходящей аорты направлены на биофизическое и морфологическое исследование. Послеоперационный период протекал без осложнений. На 10-й день после операции пациент выписан из стационара без клиники стенокардии.
По данным морфологического исследования в сегменте вены, подготовленной предлагаемым способом, патологических изменений не обнаружено. После ручной неконтролируемой дилатации отмечено отслоение эндотелия 5 и пристеночный тромбоз 6 (Фиг.2).
Исследование сократительной активности гладких мышц проводили методом механографии. Амплитуду сократительных ответов рассчитывали с учетом величины гиперкалиевого сокращения в виде процентного соотношения (эквимолярное замещение 30 мМ NaCl на KCl) и/или фенилэфрин-индуцированного сокращения, которые принимали за 100%. Релаксацию определяли с помощью добавления к предсокращенным сегментам вен нитропруссида натрия. Установлено, что при введении гиперкалиевый раствор увеличивает сокращения гладкомышечного препарата при обоих методах дилатации. Однако амплитуда сокращения существенно выше во фрагментах вен, после физиологической дилатации из восходящей аорты 7.
(Фиг.3) Реакция на фенилэфрин биоптата вены после ручной дилатации вены оказалась значительно снижена 8 (Фиг.4). Нитропруссид натрия вызывал полное снижение напряжения гладкомышечного препарата, предсокращенного как фенилэфрином, так и гиперкалиевым раствором в обоих случаях.
Предлагаемый в качестве изобретения способ апробирован на 23 пациентах во время операции аортокоронарное шунтирование на работающем сердце и позволяет исключить травмирующее влияние неконтролируемого гидродинамического давления на стенку будущего венозного шунта, негативное влияние высокого гидростатического давления на морфофункциональное состояние вены и обеспечить оптимальные условия кондиционирования вплоть до формирования аортокоронарного шунта.
Список используемой литературы
1. Chan J, Dimagli A, Dong T, Fudulu DP, Sinha S, Angelini GD. Trend and early clinical outcomes of off-pump coronary artery bypass grafting in the UK. Eur J Cardiothorac Surg 2023; doi:10.1093/ejcts/ezad27.
2. Naito S, Demal TJ, Sill B, Reichenspurner H, Onorati F, Gatti G et al.Impact of surgeon experience and centre volume on outcome after offpump coronary artery bypass surgery: results from the European Multicenter Study on Coronary Artery Bypass Grafting (E-CABG)
Registry. Heart Lung Circ 2022.
3. Ueki C, Miyata H, Motomura N, Sakaguchi G, Akimoto T, Takamoto S Off-pump versus on-pump coronary artery bypass grafting in patients
with left ventricular dysfunction. J Thorac Cardiovasc Surg 2016;151: 1092-8.
4. Neumann FJ, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U et al.; ESC Scientific Document Group. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J 2019;40:87-165.
5. Beckmann A, Meyer R, Lewandowski J, Markewitz A, Blaßfeld D, Boning A. German Heart Surgery Report 2021: the annual updated registry of the German Society for Thoracic and Cardiovascular Surgery. Thorac Cardiovasc Surg 2022;70:362-76.
6. Harskamp RE, Lopes RD, Baisden CE, et al. Saphenous vein graft failure after coronary artery bypass surgery: pathophysiology, anagement, and future directions. Ann Surg. 2013; 257 (5):824-833. doi: 10.1097/SLA.0b013e318288c38d.
7. Stigler R, Steger C, Schachner T, et al. The impact of distension pressure on acute endothelial cell loss and neointimal proliferation in saphenous vein grafts. Eur J Cardiothorac Surg. 2012; 42 (4): 74-79. doi: 10.1093/ejcts/ezs402.
8. Yumun G, Ozcan G, Gelincik I, et al. Effects of moderate pressure distention on the proximal and distal sections of the saphenous vein. Intern J Clin Experim Pathol. 2016; 9 (8): 8359-8365.
9. Cheung-Flynn J, Song J, Voskresensky I, et al. Limiting injury during saphenous vein graft preparation for coronary arterial bypass prevents metabolic decompensation. Scient Reports. 2017; 7 (1):1-16. doi: 10.1038/s41598-017-13819-w.
10. Wise ES, Hocking KM, Luo W, et al. Traditional graft preparation decreases physiologic responses, diminishes viscoelasticity, and reduces cellular viability of the conduit: a porcine saphenous vein model. Vasc Med. 2016; 21(5): 413-421. doi: 10.1177/1358863X1664904.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оптимальной гидравлической дилятации в процессе подготовки аутовенозных кондуитов при операциях коронарного шунтирования | 2017 |
|
RU2661735C1 |
| Способ забора аутовенозного кондуита для шунтирования коронарных артерий | 2024 |
|
RU2840604C1 |
| СПОСОБ ЭНДОСКОПИЧЕСКОГО ЗАБОРА ВЕНОЗНОГО КОНДУИТА ДЛЯ ОПЕРАЦИИ КОРОНАРНОГО ШУНТИРОВАНИЯ | 2014 |
|
RU2561001C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ОЦЕНКИ НЕСОСТОЯТЕЛЬНОСТИ КОРОНАРНЫХ ШУНТОВ | 2014 |
|
RU2556785C1 |
| СПОСОБ ПРОФИЛАКТИКИ СПАЗМА ЛУЧЕВОЙ АРТЕРИИ, ИСПОЛЬЗУЕМОЙ В КАЧЕСТВЕ КОРОНАРНОГО ШУНТА У ПАЦИЕНТОВ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2014 |
|
RU2547255C1 |
| СПОСОБ ПОЛНОЙ МАЛОИНВАЗИВНОЙ ЭНДОСКОПИЧЕСКИ АССИСТИРОВАННОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА ПРИ МНОГОСОСУДИСТОМ АТЕРОСКЛЕРОТИЧЕСКОМ ПОРАЖЕНИИ КОРОНАРНОГО РУСЛА | 2019 |
|
RU2723751C1 |
| СПОСОБ ОПТИЧЕСКОЙ КОГЕРЕНТНОЙ ТОМОГРАФИИ ДЛЯ ИНТРАОПЕРАЦИОННОЙ ГИСТОМОРФОЛОГИЧЕСКОЙ ОЦЕНКИ ЦЕЛОСТНОСТИ КОРОНАРНЫХ КОНДУИТОВ ПРИ АОРТОКОРОНАРНОМ ШУНТИРОВАНИИ | 2018 |
|
RU2677785C1 |
| СПОСОБ ПРЯМОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА ПРИ ИЗОЛИРОВАННОМ УСТЬЕВОМ ПОРАЖЕНИИ СТВОЛА ЛЕВОЙ КОРОНАРНОЙ АРТЕРИИ | 2014 |
|
RU2551187C1 |
| Способ профилактики реперфузионного повреждения миокарда в хирургии врожденных пороков сердца | 2019 |
|
RU2718308C1 |
| Модифицированный способ забора аутовены по методике "No-touch" | 2019 |
|
RU2763259C2 |
Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии. Присоединяют большую подкожную вену к восходящей аорте с помощью кардиоплегической канюли, через систему переходников после ее забора. Выполняют пуск крови из аорты снятием зажима с кардиоплегической канюли. Свободным потоком артериальной крови из аорты вымывают остаточные тромбы, затем накладывают мягкий сосудистый зажим на свободный конец кондуита. Начинают дилатацию, артериальным давлением из аорты с контролем герметичности сосуда. Далее кондуит оставляют в положении дилатации с открытой кардиоплегической канюлей вплоть до момента его использования. Таким образом, кондуит остается расправленным и заполненным артериальной кровью из аорты вплоть до использования. Способ позволяет исключить травмирующее влияние неконтролируемого гидродинамического давления на стенку будущего венозного шунта, негативное влияние высокого гидростатического давления на морфофункциональное состояние вены и обеспечить оптимальные условия кондиционирования вплоть до формирования аортокоронарного шунта. 4 ил., 1 пр.
Способ физиологической дилатации аутовенозного кондуита для подготовки к аортокоронарному шунтированию без искусственного кровообращения, заключающийся в том, что венозный кондуит после выделения присоединяют к восходящей аорте с помощью кардиоплегической канюли, через систему переходников, открывают свободный поток артериальной крови из аорты, накладывают мягкий сосудистый зажим на дистальный сегмент кондуита и оставляют его в состоянии дилатации до формирования аорто-коронарного шунта.
| Способ оптимальной гидравлической дилятации в процессе подготовки аутовенозных кондуитов при операциях коронарного шунтирования | 2017 |
|
RU2661735C1 |
| RU 2018127835 A, 31.01.2020 | |||
| Вечерский Ю.Ю., Манвелян Д.В., Затолокин В.В | |||
| Способ оптимальной гидравлической дилатации венозных кондуитов для аортокоронарного шунтирования, Ангиология и сосудистая хирургия, 2021, т | |||
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| Способ получения морфия из опия | 1922 |
|
SU127A1 |
| Леднев П.В., Белов Ю.В., Стоногин А.В., Лысенко А.В., Салагаев Г.И | |||
| Мобилизация | |||
Авторы
Даты
2025-03-12—Публикация
2024-07-12—Подача