ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способу селективной гидрогенизации газообразной смеси с высоким содержанием ацетилена. Более конкретно, изобретение направлено на способ превращения метана в соединения с добавленной стоимостью, в соответствии с которым газообразную смесь, содержащую водород, а также ацетилен в высокой концентрации, полученную путем пиролиза метана (например, бескислородное взаимодействие двух молекул метана), подвергают селективной гидрогенизации в присутствии биметаллического катализатора на подложке с получением этилена из присутствующего в газообразной смеси ацетилена, тогда как непрореагировавшие метан и водород отводят как побочные продукты и/или рециркулируют.
УРОВЕНЬ ТЕХНИКИ
Метан представляет собой соединение, в наибольшем количестве содержащееся в природном газе; и на его долю приходится вдвое больше углерода, чем на другие известные ископаемые топлива. А именно, сообщалось, что запасы природного газа богаче, чем запасы угля и нефти, взятых вместе. По мере постепенного исчерпания запасов угля и нефти, использование природного газа оказывает все большее влияние на глобальный энергетический баланс. То есть, поскольку запасы природного газа больше, чем запасы нефти, метан рассматривают как наиболее реалистичное альтернативное сырье, способное заменить нефть по мере истощения ее запасов. Ведутся всесторонние исследования, направленные на разработку технологий превращения метана в более тяжелые материалы с добавленной стоимостью, такие как этилен, бензол, нафта, дизельное масло и т.д.
Известными способами превращения метана в более тяжелые углеводороды являются способ прямой конверсии и способ косвенной конверсии. Способ косвенной конверсии включает, главным образом, получение синтез-газа путем парового реформинга и т.п., тогда как в способе прямой конверсии промежуточная стадия, такая как стадия получения синтез-газа, отсутствует. В настоящее время наиболее коммерчески успешные способы получения из метана продуктов с добавленной стоимостью основаны на синтезе углеводородных соединений из синтез-газа, полученного путем частичного окисления метана. Например, в процессе Фишера-Тропша углеводороды и т.п. получают из синтез-газа с использованием металлического катализатора (Co, Fe). Однако, эта технология косвенной конверсии включает несколько стадий, эффективность реакции низкая, а в некоторых регионах трудно обеспечить рентабельность из-за высокой себестоимости, связанной с тем, что рабочие условия включают высокую температуру и высокое давление.
В качестве альтернативы был предложен способ прямой конверсии метана без необходимости промежуточного получения синтез-газа. Обычно, производство углеводородов С2+ (например, таких углеводородов С2, как этан, этилен и/или ацетилен, и ароматических соединений, таких как бензол) предлагают проводить путем окислительного взаимодействия метана (например, Публикация заявки на патент Кореи №10-2018-0113448). Другой способ прямой конверсии метана заключается в получении углеводородов С2+ по бескислородному механизму. Однако, способ прямой конверсии, описанный выше, отличается тенденцией к образованию побочных продуктов. По механизму окислительной конверсии могут образовываться оксиды углерода (СО, СО2 и т.д.), а по бескислородному механизму может образовываться кокс, вызывающий деактивацию катализатора.
Тем не менее, ведутся исследования, направленные на устранение таких проблем, как образование кокса, при сохранении всех преимуществ способа прямой конверсии. В этом отношении, авторы настоящего изобретения попытались повысить степень превращения метана и подавить образование кокса путем более точного регулирования условий реакции, в том числе, отношения водорода к метану, температуры пиролиза, давления в ходе реакции, времени пребывания и т.п., в присутствии водорода во время пиролиза метана. При этом, когда пиролиз метана проводят в определенных условиях реакции, направленных на повышение степени превращения метана и максимальное подавление образования кокса, в качестве углеводорода С2 может образовываться, главным образом, ацетилен, и газообразный продукт, остающийся после отделения от продуктов пиролиза ароматики (например, бензола), содержит ацетилен в высокой концентрации. Кроме того, когда в ходе пиролиза стремятся достичь максимальной степени превращения метана, рентабельность увеличивается, однако, в избытке образуется кокс, из-за чего функционирование становится невозможным. Напротив, при функционировании с заданной степенью превращения метана продукты пиролиза метана неизбежно содержат водород и непрореагировавший метан. В принципе, продукты пиролиза метана, полученные после отделения ароматики, характеризуются более высокой концентрацией ацетилена, чем любые традиционные продукты пиролиза метана. Продукты пиролиза, содержащие ацетилен в высокой концентрации, могут быть получены даже тогда, когда пиролиз осуществляют с использованием реактора с высокотемпературной плазмой в регулируемых условиях реакции, направленных на повышение степени превращения метана и подавление образования кокса, однако, недостатком использования плазменного реактора является низкая рентабельность процесса. Между тем, описанные в литературе катализаторы конверсии ацетилена, пригодные для гидрогенизации ацетилена до этилена, включают платиновый катализатор на подложке, палладиевый катализатор на подложке и т.д., возможности этих катализаторов по увеличению степени превращения ацетилена, присутствующего в продуктах пиролиза, содержащих ацетилен в высокой концентрации, и селективности в отношении этилена ограничены. Кроме того, в традиционном процессе конверсии ацетилена ацетилен и водорода присутствуют в эквивалентных количествах, а продукты пиролиза характеризуются высоким отношением водорода к ацетилену.
Кроме того, продукты пиролиза метана содержат значительное количество водорода. Водород характеризуется высоким энергетическим КПД, в процессе его горения помимо воды не образуется никаких вредных побочных продуктов. В силу этих преимуществ ценность водорода как источника чистой энергии в последнее время существенно возросла. Если бы удалось эффективно осуществлять извлечение водорода, образующегося в качестве побочного продукта дегидрогенизации в ходе пиролиза метана, это было бы преимуществом с точки зрения повышения рентабельности процесса в целом.
Следовательно, требуется селективный катализатор гидрогенизации, обеспечивающий максимальный выход этилена из продуктов пиролиза метана, содержащих ацетилен в высокой концентрации, в частности, практически не содержащих этилена, в отличие от традиционных технологий с использованием бескислородного взаимодействия метана, и способ, позволяющий расширить использование водорода из продуктов пиролиза.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Один из вариантов осуществления настоящего изобретения направлен на обеспечения способа производства этилена с высоким выходом путем селективной гидрогенизации газообразной смеси, содержащей ацетилен в высокой концентрации и полученной в процессе пиролиза метана.
Другой вариант осуществления настоящего изобретения направлен на обеспечения эффективного способа извлечения или использования водорода, а также этилена из продуктов пиролиза метана.
В одном из аспектов настоящим изобретением обеспечивается способ селективной гидрогенизации, включающий стадии, на которых:
а) обеспечивают газообразную смесь, содержащую, по меньшей мере, 2% мол. ацетилена, по меньшей мере, 50% мол. водорода и до 48% мол. метана,
b) производят продукт гидрогенизации, характеризующийся увеличенной концентрацией этилена по сравнению с газообразной смесью, путем гидрогенизации газообразной смеси в присутствии катализатора гидрогенизации, в котором первый металл М1, активный в отношении гидрогенизации, и второй металл М2, функцией которого является индуцирование селективной гидрогенизации, нанесены на пористую подложку, и
с) отделяют и извлекают этилен и водород из продукта гидрогенизации,
при этом, первый металл М1 представляет собой, по меньшей мере, один металл, выбранный из группы, состоящей из Pd, Pt, Rh, Ir, Ni и Co, и второй металл M2 представляет собой, по меньшей мере, один металл, выбранный из группы, состоящей из Cu, Ag, Au, Zn, Ga и Sn, и
количество первого металла М1 и второго металла М2 в катализаторе гидрогенизации составляет от 0,15 до 2% вес. и от 0,8 до 30% вес., соответственно, и удовлетворяет уравнению 1:
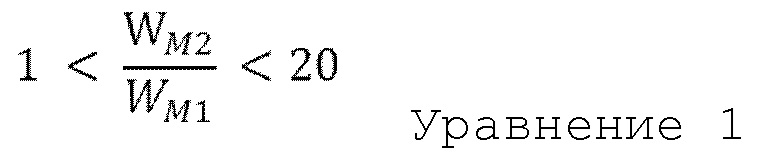
в котором WM1 означает весовое процентное содержание первого металла в катализаторе гидрогенизации, и WM2 означает весовое процентное содержание второго металла в катализаторе гидрогенизации.
В соответствии с одним из примерных вариантов осуществления изобретения, газообразная смесь может содержать от 3 до 10% мол. ацетилена, от 52 до 75% мол. водорода и от 18 до 45% мол. метана.
В соответствии с одним из примерных вариантов осуществления изобретения, газообразная смесь может дополнительно содержать углеводороды С2, отличные от ацетилена, в концентрации не более 1% мол.
В соответствии с одним из примерных вариантов осуществления изобретения, газообразная смесь может дополнительно содержать, по меньшей мере, один углеводород, выбранный из группы, состоящей из углеводородов С3 - С5, в концентрации не более 1% мол.
В соответствии с одним из примерных вариантов осуществления изобретения, стадия b) может быть осуществлена без подвода водорода извне.
В соответствии с одним из примерных вариантов осуществления изобретения, первый металл М1 может характеризоваться энергией адсорбции водорода от -4 до -2 эВ, второй металл М2 может характеризоваться энергией адсорбции водорода от -1 до 0 эВ.
В соответствии с одним из примерных вариантов осуществления изобретения, первый металл М1 и второй металл М2 в катализаторе гидрогенизации могут являться палладием (Pd) и медью (Cu), соответственно.
В соответствии с одним из примерных вариантов осуществления изобретения, пористая подложка катализатора гидрогенизации может представлять собой, по меньшей мере, один материал, выбранный из группы, состоящей из оксида алюминия, диоксида кремния, углерода, диоксида циркония, диоксида титана, диоксида церия и карбида кремния.
В соответствии с одним из примерных вариантов осуществления изобретения, катализатор гидрогенизации может быть получен способом, включающим стадии, на которых: подготавливают твердый прекурсор путем пропитки подложки разбрызгиванием раствора комбинированного прекурсора, в котором объединены прекурсор первого металла М1 и прекурсор второго металла М2.
В соответствии с одним из примерных вариантов осуществления изобретения, способ получения катализатора гидрогенизации может дополнительно включать восстановление прекурсора первого металла М1 и второго металла М2 в твердом прекурсоре при температуре от 200 до 400°С в восстановительной атмосфере.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Изложенные выше и другие цели, отличительные особенности и преимущества изобретения станут более ясны по прочтении нижеследующего подробного описания в сочетании с прилагаемыми чертежами, на которых:
На фиг. 1 приведена схема процесса производства этилена, объединяющая процесс пиролиза метана и процесс гидрогенизации ацетилена;
На фиг. 2 схематично показана структура устройства, использованного в примере;
Фиг. 3А - 3I представляют собой графики конверсии метана в разных рабочих условиях (температура, рабочее давление, объемное отношение водород/метан и время пребывания) (представленные как логарифмическая величина давления реакции (от 0,1 до 10 атм) относительно времени пребывания (с));
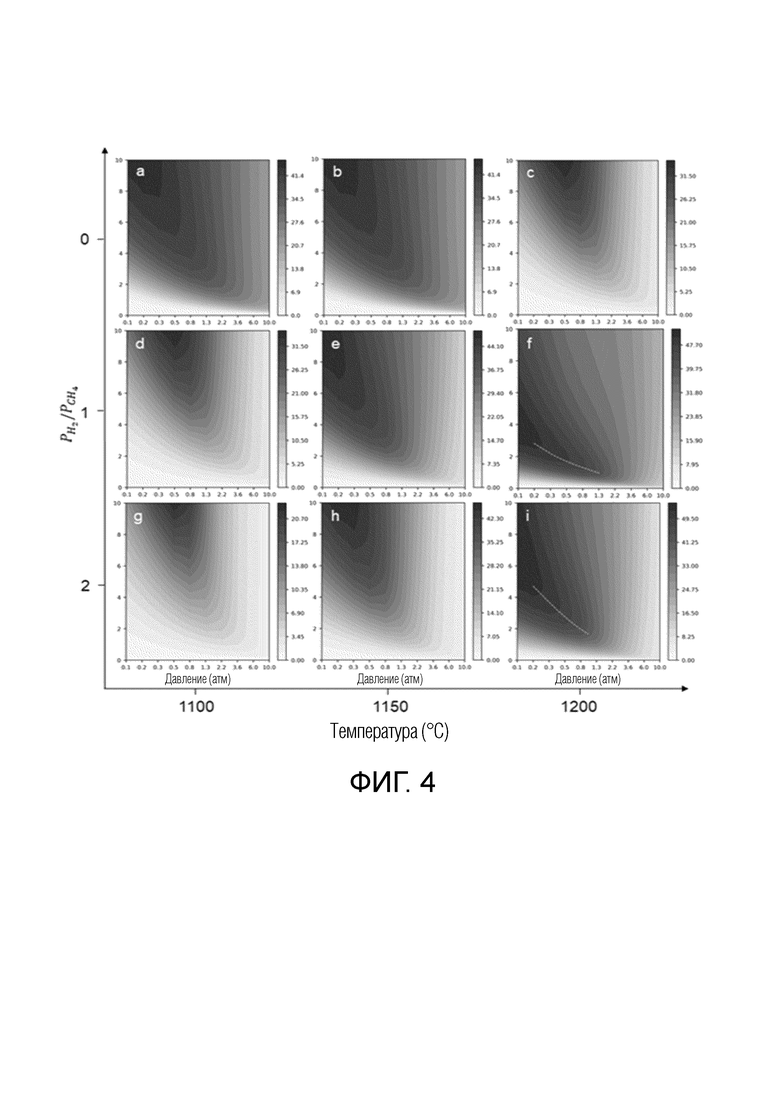
Фиг. 4А - 4I представляют собой графики выхода углеводородов С2 и бензола в разных рабочих условиях;
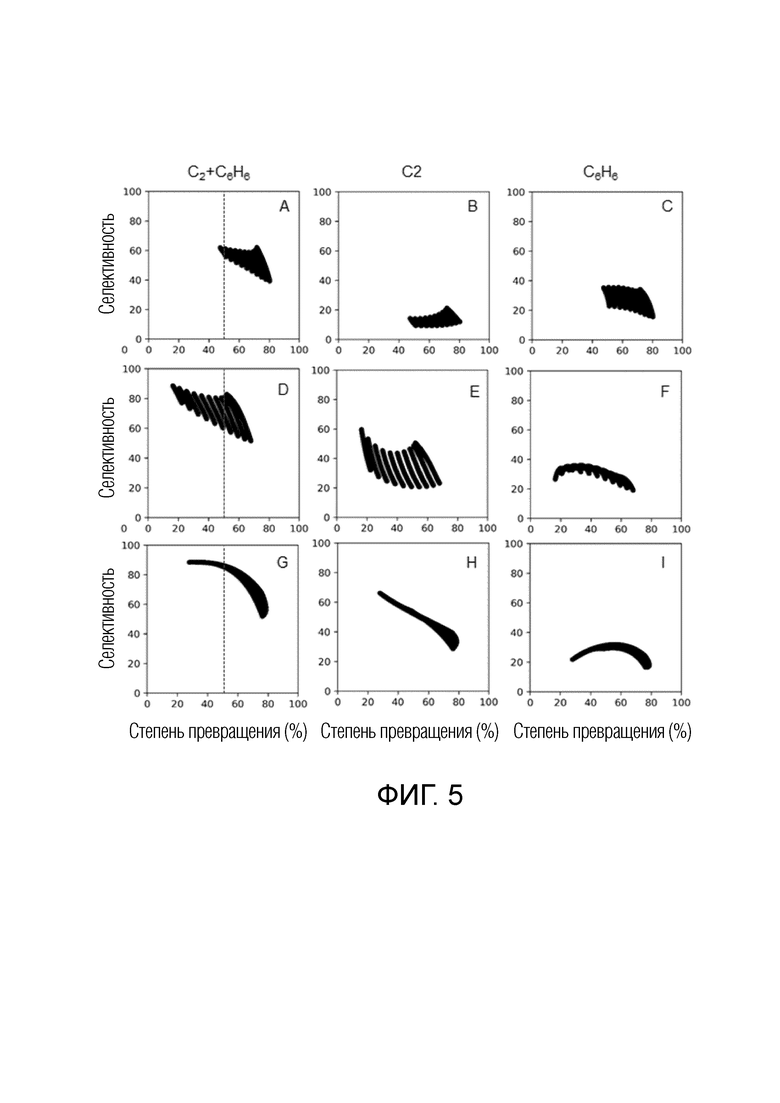
На фиг. 5А - 5I приведены результаты моделирования, представляющие собой график селективности в отношении С2+С6Н6 (фиг. 5А, 5D, 5G), С2 (фиг. 5В, 5Е, 5Н) и С6Н6 (фиг. 5С, 5F, 5I) относительно конверсии метана при одновременной подаче водорода, при различном давлении реакции и при температуре 1200°С для времени пребывания 1-5 с (на фиг. 5А, 5В и 5С H2/CH4=0, 1-10 бар; на фиг. 5D, 5Е и 5F H2/CH4=1, 0,1-10 бар; на фиг. 5G, 5Н и 5I H2/CH4=1, 0-0,5 бар);
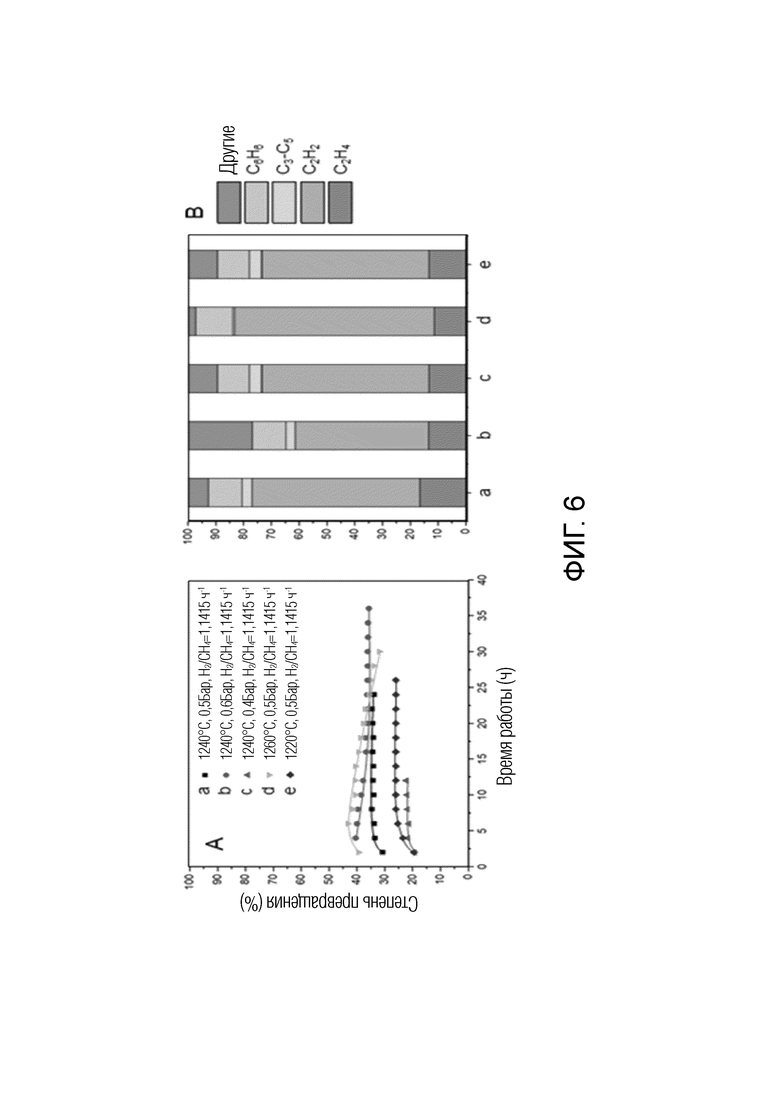
Фиг. 6А представляет собой график конверсии метана относительно TOS (time on stream, время работы) для разных условий пиролиза, Фиг. 6В представляет собой график средней селективности продуктов в разных условиях пиролиза;
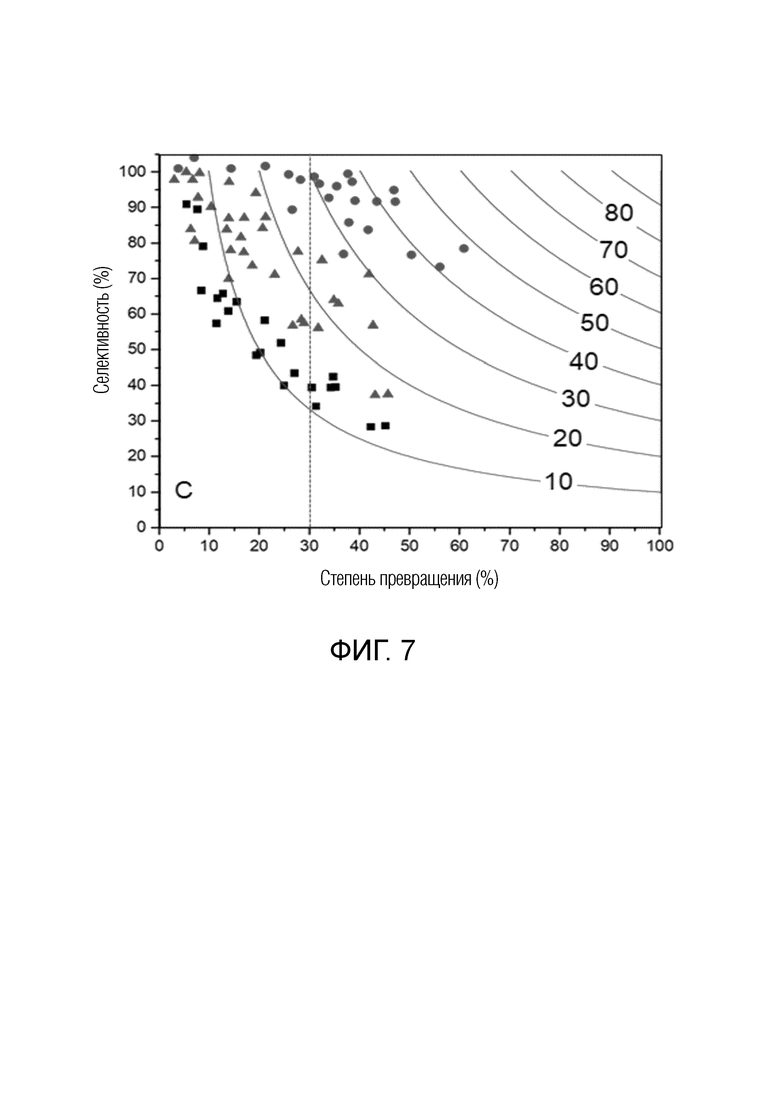
Фиг. 7 представляет собой график селективности углеводородов ≤C6 относительно конверсии в разных условиях (на котором черные квадраты соответствуют условиям H2/CH4=0 и атмосферного давления, синие треугольники соответствуют условиям H2/CH4=1 и атмосферного давления, красные круги соответствуют условиям H2/CH4=1 и давления ниже атмосферного, изолиниями показан выход, каждая точка означает среднюю величину отдельных экспериментов); и
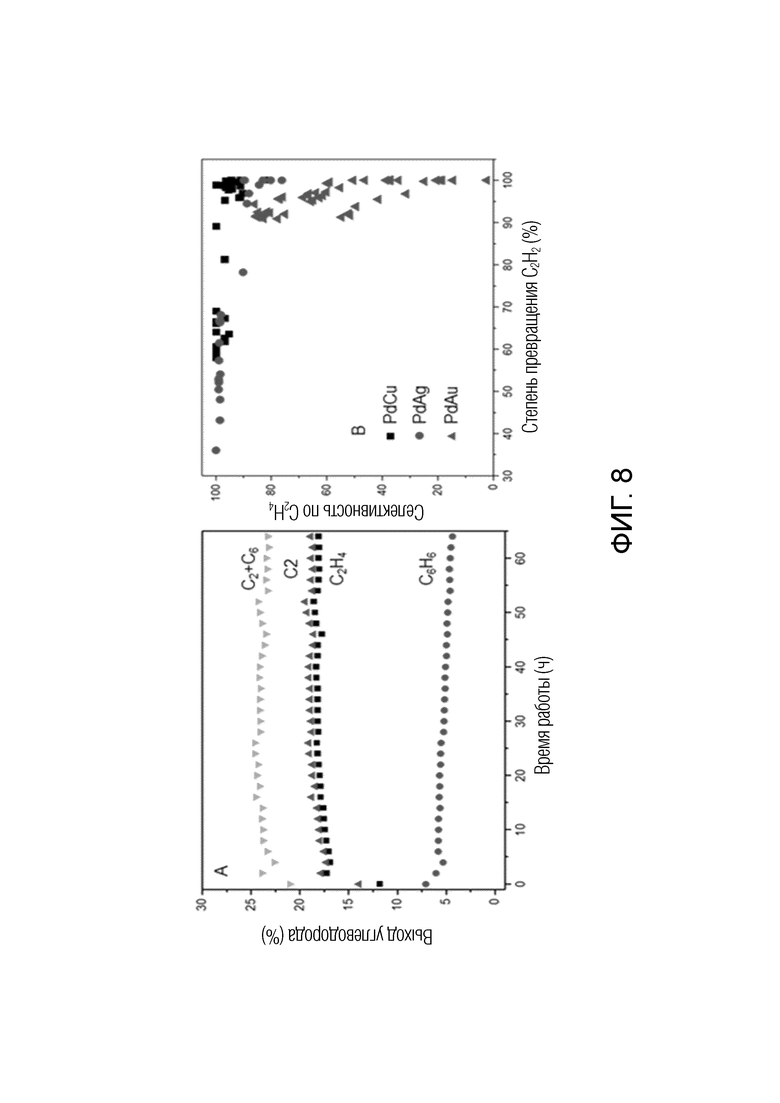
Фиг. 8А представляет собой график выхода углеводородов в результате пиролиза метана и гидрогенизации с использованием катализатора PdCu (условия пиролиза: 1235°С, 0,5 бар, H2/CH4=1, GHSV=1415 ч-1 (gas hourly space velocity, часовая объемная скорость газа); условия гидрогенизации: 100°С, 0,5 бар, WHSV=4 (weight hour space velocity, часовая объемная скорость на единицу массы катализатора), фиг. 8В представляет собой график селективности в отношении этилена при индивидуальном использовании катализаторов PdCu, PdAg и PdAu (при этом, температуру в каталитическом реакторе изменяют с целью регулирования конверсии ацетилена).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение может быть реализовано во всей полноте на основании нижеследующего описания. Следует понимать, что это описание охватывает предпочтительные варианты осуществления настоящего изобретения, которыми изобретение не ограничивается. Кроме этого, прилагаемые чертежи приведены для облегчения понимания настоящего изобретения, и ими изобретение не ограничивается.
В настоящем документе термины использованы в следующих значениях.
Термин «кокс» может означать углеводород с низким содержанием водорода, в частности, остаточный твердый углеродный побочный продукт.
Термин «взаимодействие» может означать химическую реакцию, в которой две одинаковые молекулы реагируют друг с другом, образуя более крупную молекулу в узком смысле.
Термин «взаимодействие метана» может означать реакцию, в которой из метана образуются не только углеводороды С2 (например, этан, этилен, ацетилен и т.д.), но и более тяжелые углеводороды (С2+) (например, бензол, нафталин и т.д.).
Термин «пиролиз» может означать реакцию, в которой углеводороды разлагаются под действием тепла и т.п. даже без добавления кислорода или содержащих кислород реагентов, и в настоящем описании может рассматриваться как включающий реакцию превращения одного соединения в один или несколько других материалов при подведении к нему тепла.
Термин «гетерогенный катализатор» может означать катализатор, фаза которого отлична от фазы реагента в ходе каталитической реакции, например, катализатор, который не растворяется в реакционной среде. Для прохождения реакции на гетерогенном катализаторе необходимо, чтобы, по меньшей мере, один реагент диффундировал и адсорбировался на поверхности гетерогенного катализатора, а по окончании реакции продукт должен десорбироваться с поверхности гетерогенного катализатора.
Термин «подложка» может означать материал (обычно, твердый материал) с большой удельной площадью поверхности, к которой прикреплен или на которую нанесен каталитически активный компонент.
Термин «гидрогенизация» может означать реакцию, в ходе которой содержание водорода в некотором соединении увеличивается в результате химического присоединения водорода, по меньшей мере, к части соединения, осуществляемую путем приведения этого соединения в контакт с катализатором в присутствии водорода.
Термин «пропитка» может означать способ получения катализатора путем пропитки подложки раствором, в котором растворен прекурсор катализатора, и сушки и/или обжига (или восстановительной обработки), если нужно.
Термин «степень конверсии» может означать число молей сырья, преобразованного в соединение, отличное от сырья, на один моль сырья.
Термин «селективность» может означать число молей целевого продукта на один моль преобразованного сырья.
В соответствии с одним из вариантов осуществления, настоящим изобретением обеспечивается способ селективного превращения ацетилена в этилен путем гидрогенизации газообразной смеси. Газообразная смесь, обычно, может являться продуктом пиролиза метана, в частности, газообразной смесью, оставшейся после отделения С6 и более тяжелых углеводородов, в частности, ароматических углеводородов от продуктов пиролиза метана. Следовательно, газообразная смесь может, по существу, не содержать ароматических углеводородов, таких как бензол, толуол, нафталин и т.п.
В соответствии с одним из вариантов осуществления изобретения, газообразная смесь, которая является сырьем реакции гидрогенизации, может содержать ацетилен в относительно высокой концентрации по сравнению с традиционными продуктами пиролиза метана. По существу, образование газообразной смеси, содержащей ацетилен в высокой концентрации, является результатом явления, заключающегося в том, что в ходе пиролиза в присутствии водорода в регулируемых условиях реакции пиролиза (температура, давление, время пребывания и т.д.), направленных на повышение степени конверсии метана и максимальное подавление образования кокса во время пиролиза, метан превращается, главным образом, в ацетилен, а не в этилен. Газообразная смесь с таким составом может быть получена из продукта бескислородного пиролиза метана (в частности, продукта бескислородного взаимодействия метана), продукта плазменного пиролиза (или взаимодействия) метана или их сочетания. В частности, газообразную смесь, применимую в данном варианте осуществления изобретения, получают обычным пиролизом метана, в частности, по реакции пиролиза, в которой не используется кислород (бескислородный пиролиз), и поэтому она, по существу, не содержит монооксид углерода, диоксид углерода и т.д.
В соответствии с одним из вариантов осуществления изобретения, концентрация ацетилена в газообразной смеси может составлять, по меньшей мере, около 2% мол., в частности, от 3 до 10% мол., более конкретно, от 4 до 8% мол. Концентрация ацетилена, указанная выше, отличается от концентрации в традиционных продуктах пиролиза метана, где концентрация ацетилена меньше, примерно, 2% мол. (в частности, составляет от 0,5 до 1% мол.), а концентрация углеводородов С2, отличных от ацетилена, таких как этан и этилен, относительно высокая.
Газообразная смесь может дополнительно содержать водород, образующийся как побочный продукт в результате реакции связывания С-С во время пиролиза метана, и/или водород, подаваемый или вступающий в реакцию одновременно с метаном с целью повышения степени конверсии и подавления образования кокса в ходе пиролиза метана, как описано ниже. Например, газообразная смесь может содержать водород в количестве, по меньшей мере, около 50% мол., в частности, от 52 до 75% мол. более конкретно, от 60 до 65% мол. Кроме этого, обычно, газообразная смесь может содержать метан, не преобразованный в ходе реакции пиролиза (т.е., непрореагировавший метан). Например, концентрация метана составляет до, примерно, 48% мол., в частности, от 18 до 45% мол., более конкретно, от 28 до 35% мол.
В соответствии с одним из вариантов осуществления изобретения, газообразная смесь может содержать, примерно, от 4 до 7% мол. ацетилена, примерно, от 62 до 64% мол. водорода и, примерно, от 30 до 33% мол. метана.
В соответствии с одним из примерных вариантов осуществления изобретения, газообразная смесь может дополнительно содержать углеводороды С2, отличные от ацетилена. При этом, углеводороды С2 могут представлять собой этан и/или этилен. Концентрация углеводородов С2, отличных от ацетилена, может составлять, например, менее, примерно, 1% мол., в частности, менее, примерно, 0,75% мол., более конкретно, менее, примерно, 0,5% мол. В одном из конкретных вариантов осуществления изобретения концентрация этилена в газообразной смеси может составлять, например, менее, примерно, 1% мол., в частности, менее, примерно, 0,75% мол., более конкретно, менее, примерно, 0,5% мол.
Кроме того, в соответствии с одним из примерных вариантов осуществления изобретения, газообразная смесь может содержать другие углеводороды, например, углеводороды С3 - С5, оставшиеся после отделения от продуктов пиролиза метана ароматических соединений. Такие углеводороды, обычно, могут присутствовать в концентрации менее, примерно, 1% мол., в частности, менее, примерно, 0,75% мол., более конкретно, менее, примерно, 0,5% мол.
В соответствии с одним из вариантов осуществления изобретения, ацетилен газообразной смеси может быть превращен в этилен путем селективной гидрогенизации с использованием катализатора. А именно, водород, присутствующий в газообразной смеси, может быть использован как есть, без необходимости отдельной подачи извне водорода, требуемого для гидрогенизации ацетилена. Хотя подача водорода из внешнего источника для достижения парциального давления водорода, достаточного для эффективной гидрогенизации ацетилена, строго не исключается, добавляемое количество водорода в этом случае может быть значительно уменьшено. В этом отношении, молярное отношение H2/C2H2 в продуктах реакции перед проведением селективной гидрогенизации ацетилена до этилена может быть надлежащим образом отрегулировано в диапазоне, например, от 5 до 35, в частности, от 8 до 30, более конкретно, от 9 до 20, еще более конкретно, от 10 до 15.
Вместе с тем, гидрогенизация может быть проведена в присутствии катализатора. При этом, необходим катализатор, активный в отношении повышения степени конверсии ацетилена и селективности в отношении этилена в газообразной смеси с высокой концентрацией ацетилена по сравнению с традиционными продуктами пиролиза. С этой целью в данном варианте осуществления изобретения гидрогенизацию проводят в присутствии гетерогенного катализатора, в котором, по меньшей мере, два металла, в частности, первый металл М1, активный в отношении гидрогенизации, и второй металл М2, функцией которого является индуцирование селективной гидрогенизации, нанесены на пористую подложку. Поскольку эта функция металла может быть выражена количественно через энергию адсорбции дополнительного атома Н посредством расчета методом теории функционала плотности (density functional theory, DFT), первый металл М1 может характеризоваться энергией адсорбции водорода, примерно, от -4 до -2 эВ, и второй металл М2 может характеризоваться энергией адсорбции водорода от -1 до 0 эВ.
Первый металл М1 может представлять собой, по меньшей мере, один металл, выбранный из группы, состоящей из Pd, Pt, Rh, Ir, Ni и Co, и второй металл M2 может представлять собой Pd. Второй металл M2 также может представлять собой, по меньшей мере, один металл, выбранный из группы, состоящей из Cu, Ag, Au, Zn, Ga и Sn, в частности, может являться Cu. В соответствии с конкретным вариантом осуществления изобретения, сочетание металлов, нанесенных на подложку, может быть сочетанием Pd и Cu, а причина их выбора может быть объяснена эффектом образования сплава. Катализатор гидрогенизации, используемый в этом варианте осуществления изобретения, является катализатором, содержащим два типа активных металлических компонентов, и первый металл (в частности, Pd) и второй металл (в частности, Cu) могут находиться в кристаллическом состоянии, а также могут находиться в форме сплава или быть нанесенными в такой форме, что непосредственно или очень тесно контактируют друг с другом. Кроме этого, первый металл М1 может присутствовать в форме отдельного атома, а второй металл М2 может присутствовать в форме наночастиц.
В одном из примерных вариантов осуществления изобретения размер частиц активных металлов (или каждого из металлов - первого и второго) в катализаторе гидрогенизации может составлять, например, около 100 нм или менее, в частности, от 10 до 70 нм, более конкретно, от 20 до 50 нм.
В соответствии с одним из вариантов осуществления изобретения, количество первого металла М1 в катализаторе гидрогенизации может составлять, например, от 0,15 до 2% вес., в частности, примерно, от 0,2 до 1% вес., более конкретно, от 0,21 до 0,5% вес. Поскольку количество первого металла влияет на активность и селективность гидрогенизации, может быть выгодно, чтобы оно соответствовало указанному диапазону. Кроме этого, количество второго металла М2 может составлять, например, от 0,8 до 30% вес., в частности, примерно, от 1 до 10% вес., более конкретно, от 1,5 до 5% вес. Если количество второго металла слишком большое или слишком маленькое, активность катализатора может быть недостаточной, либо может происходить неселективная гидрогенизация. Следовательно, желательно, чтобы количество второго металла соответствовало указанному диапазону.
При этом, в одном из примерных вариантов осуществления изобретения первый металл М1 и второй металл М2 могут сочетаться в заданном соотношении в зависимости от свойств каждого металла. В этом отношении, катализатор гидрогенизации может удовлетворять уравнению 1, приведенному ниже (на основании анализа ICP-OES (Inductively Coupled Plasma optical emission spectroscopy, оптическая эмиссионная спектроскопия с индукционно-связанной плазмой)).
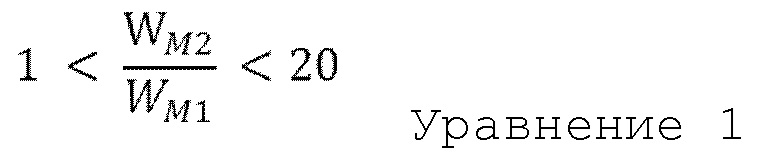
В уравнении 1 WM1 означает весовое процентное содержание первого металла в катализаторе гидрогенизации, и WM2 означает весовое процентное содержание второго металла в катализаторе гидрогенизации.
В соответствии с одним из примерных вариантов осуществления изобретения, 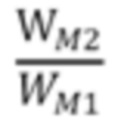 может лежать в диапазоне, например, от 2 до 10, в частности, от 3 до 8, более конкретно, от 4 до 7. Если количество первого металла М1 относительно второго металла М2 не соответствует заданному диапазону, может заметно снижаться активность, либо может возникать явление снижения селективности в отношении ацетилена во время гидрогенизации. Следовательно, количество каждого активного металлического компонента желательно поддерживать в рамках указанного диапазона.
может лежать в диапазоне, например, от 2 до 10, в частности, от 3 до 8, более конкретно, от 4 до 7. Если количество первого металла М1 относительно второго металла М2 не соответствует заданному диапазону, может заметно снижаться активность, либо может возникать явление снижения селективности в отношении ацетилена во время гидрогенизации. Следовательно, количество каждого активного металлического компонента желательно поддерживать в рамках указанного диапазона.
При этом, подложка для нанесения двух металлов (первого и второго металла) может представлять собой, по меньшей мере, один материал, выбранный из группы, состоящей из оксида алюминия, диоксида кремния, углерода, диоксида циркония, диоксида титана, диоксида церия и карбида кремния. В частности, может быть использован оксид алюминия, более конкретно, гамма-оксид алюминия.
В соответствии с одним из примерных вариантов осуществления изобретения, подложка может являться пористой подложкой, и пористость подложки может быть выбрана так, чтобы реагент или продукт при диффузии в подложку надолго в ней не задерживались.
В этом отношении, подложка может иметь следующие свойства:
- удельная площадь поверхности (по методу Брунауэра-Эммета-Теллера, ВЕТ): по меньшей мере, около 300 м2/г, в частности, от 400 до 700 м2/г, более конкретно, от 500 до 600 м2/г;
- объем пор: по меньшей мере, около 0,5 см3/г, в частности, от 0,75 до 2 см3/г, более конкретно, от 1 до 1,5 см3/г; и
- средний размер пор: примерно, от 50 до 200 Å, более конкретно, от 100 до 150 Å.
Кроме этого, в соответствии с одним из примерных вариантов осуществления изобретения, подложка может иметь различные формы, известные в данной области, а также быть порошкообразной. В качестве примеров можно привести сферическую форму (в том числе полую), цилиндрическую форму (в том числе полую), форму гранул, таблеток, колец, седел, звезд, сот, катышков, трехдольчатую и четырехдольчатую форму и т.п. В сущности, в качестве иллюстрации подготовки подложки заданной формы можно назвать формование в пресс-форме, известное в данной области, способ экструзии, распылительной сушки, окатывания, капания масла и т.д. Кроме этого, средний размер подложки, имеющей форму, примеры которой приведены выше, может лежать в диапазоне, например, от 1 до 5 мм, в частности, от 1,5 до 3 мм, более конкретно, от 2 до 2,75 мм, при этом, числовые диапазоны являются иллюстративными.
В соответствии с одним из примерных вариантов осуществления изобретения, катализатор гидрогенизации может быть получен любым способом нанесения, известным в данной области, примерами которого являются пропитка, осаждение, ионный обмен, адсорбция из раствора и т.д. В частности, может быть применена пропитка, более конкретно, пропитка по влагоемкости или модифицированная пропитка по влагоемкости.
В одном из конкретных вариантов осуществления изобретения, катализатор может быть получен способом пропитки. С этой целью металл может быть использован в форме прекурсора, в частности, соединения металла, более конкретно, соли металла или комплекса и т.д., которые могут быть выбраны из соединений, растворимых в среде, используемой для приготовления пропиточного раствора (в частности, в водной среде). Например, когда первый из активных металлов является палладием, его прекурсор может быть солью органической кислоты или солью неорганической кислоты, комплексом, гидроксидом, галогенидом или их сочетанием. Например, прекурсор палладия может представлять собой, по меньшей мере, одно соединение, выбранное из ацетата палладия, хлорида палладия, нитрата палладия, нитрата палладия-аммония, сульфата палладия, карбоната палладия, гидроксида палладия, галогенида палладия, их гидратов и т.п., при этом, приведенные примеры являются иллюстративными. Более конкретно, в качестве прекурсора может быть использован нитрат палладия-аммония. С другой стороны, когда вторым металлом является медь, его прекурсор может представлять собой, по меньшей мере, одно соединение, выбранное, например, из гидроксид-фосфата меди, нитрата меди, сульфата меди, ацетата меди, формиата меди, хлорида меди (II), йодида меди и т.д., более конкретно, может быть использован нитрат меди.
В соответствии с одним из примерных вариантов осуществления изобретения, пропиточный раствор может быть приготовлен путем последовательного или одновременного введения в среду прекурсора первого металла и прекурсора второго металла. При этом, общая концентрация прекурсоров активного металла (прекурсора первого металла и прекурсора второго металла) в пропиточном растворе может быть отрегулирована в диапазоне, например, от 0,01 до 2 мкМ, в частности, от 0,1 до 1 мкМ, более конкретно, от 0,25 до 0,75 мкМ в зависимости от количества первого и второго металлов, которые должны быть нанесены в готовом катализаторе, и от соотношения первого металла и второго металла. Кроме этого, рН раствора, содержащего прекурсор первого металла и прекурсор второго металла, может быть отрегулирован в диапазоне, например, от 1 до 3, в частности, от 1,2 до 2, более конкретно, от 1,3 до 1,5 с целью эффективного диспергирования прекурсора металла на подложке. С этой целью в пропиточный раствор может быть добавлен кислотный компонент, известный в данной области. Кислотный компонент может представлять собой, по меньшей мере, одно соединение, выбранное из азотной кислоты, серной кислоты, соляной кислоты, щавелевой кислоты и т.п.
Способ пропитки не ограничивается конкретным процессом при условии, что раствор прекурсора металла (т.е., комбинированный раствор прекурсоров первого и второго металлов) может в достаточной степени контактировать с порами подложки. Например, раствор прекурсоров металлов может быть нанесен на подложку разбрызгиванием с получением твердого прекурсора. В качестве альтернативы, подложка может быть погружена в раствор прекурсоров металлов, например, примерно, при 15-80°С (в частности, от 20 до 50°С, более конкретно, при комнатной температуре), примерно, на 0,5-3 часа (в частности, от 1 до 2 часов). Однако, эти условия приведены в качестве иллюстрации.
После пропитки подложки активными металлами, как описано выше, может быть проведен процесс сушки, например, в содержащей кислород атмосфере (в частности, в окружающем воздухе). При этом, температура сушки может лежать в диапазоне, например, от 60 до 150°С, в частности, от 70 до 100°С, однако, этими диапазонами не ограничивается. Кроме этого, время сушки может лежать в диапазоне, например, от 3 до 24 часов, в частности, от 6 до 12 часов. В результате сушки прекурсор металла может прочнее прикрепиться к подложке. В конце концов может быть получена структура, в которой подложка покрыта прекурсорами активных металлов, например, сердцевинно-оболочечная структура.
После получения твердого прекурсора, в котором прекурсор первого металла и прекурсор второго металла прикреплены к подложке или осаждены на подложку, как описано выше, металлический компонент может быть переведен в восстановленную, или элементарную, форму путем восстановительной обработки. При этом, хотя обжиг или тепловая обработка перед восстановительной обработкой не исключается, восстановительная обработка твердого прекурсора может быть проведена без обжига.
При проведении восстановительной обработки может быть использован чистый водород или водород, разбавленный инертным газом (например, N2, He, Ar и т.д.), при этом, температура может лежать в диапазоне, например, от 200 до 400°С, в частности, от 220 до 380°С, более конкретно, от 250 до 350°С. При этом, скорость нагревания может лежать в диапазоне, например, от 3 до 10°С/мин, в частности, от 4 до 8°С/мин, более конкретно, от 5 до 7°С/мин. Кроме того, длительность восстановительной обработки не имеет определенных ограничений и может лежать в диапазоне, например, от 0,5 до 24 часов, в частности, от 1 до 12 часов. Например, когда восстановительный газ разбавлен инертным газом, концентрация восстановительного газа может лежать в диапазоне, например, от 2 до 5% об. Кроме этого, давление во время восстановительной обработки может лежать в диапазоне, например, от, приблизительно, атмосферного до 10 бар (обычно, это атмосферное давление).
В соответствии с одним из примерных вариантов осуществления изобретения, газообразную смесь, содержащую ацетилен в высокой концентрации, гидрогенизируют в присутствии катализатора, описанного выше. При этом, температура гидрогенизации может лежать в диапазоне от комнатной температуры до 250°С, в частности, от 40 до 200°С, более конкретно, от 50 до 150°С. Кроме этого, давление гидрогенизации может лежать в диапазоне, например, от 0,2 до 1 бар, в частности, от 0,3 до 0,8 бар, более конкретно, от 0,4 до 0,7 бар.
В соответствии с одним из примерных вариантов осуществления изобретения, гидрогенизация может быть проведена в периодическом или непрерывном режиме, однако, непрерывный режим является предпочтительным с точки зрения рентабельности процесса и т.п. При этом, тип реактора не имеет определенных ограничений, например, может быть использован реактор для газообразной среды с неподвижным слоем, реактор с псевдоожиженным слоем и т.п.; преимущественно может быть использован реактор с неподвижным слоем. Кроме этого, часовая объемная скорость газа (GHSV) определяется в зависимости от производительности по этилену и степени конверсии при контакте с катализатором. Если часовая объемная скорость газа слишком низкая, может снижаться производительность, тогда как если часовая объемная скорость газа слишком большая, может быть недостаточным контакт с катализатором. Учитывая это, часовая объемная скорость газа может быть выбрана в диапазоне, например, от 1 до 15 л/гкат·ч-1, в частности, от 2 до 10 л/гкат·ч-1, более конкретно, от 3 до 5 л/гкат·ч-1.
В соответствии с одним из примерных вариантов осуществления изобретения, степень конверсии ацетилена в газообразной смеси, являющейся сырьем, может составлять, например, по меньшей мере, около 95%, в частности, по меньшей мере, около 97,5%, более конкретно, от 99 до 99,9%, кроме этого, селективность в отношении этилена может составлять, например, по меньшей мере, около 95%, в частности, по меньшей мере, около 97,5%, более конкретно, от 99 до 99,9%. При этом, приведенные числовые диапазоны являются иллюстративными.
Продукт гидрогенизации может быть отделен или очищен с использованием сочетания способов, известных в данной области (например, перегонка, PSA (pressure swing adsorption, адсорбция со сдвигом давления) и т.д.) с целью извлечения из него этилена и водорода. Однако, продукт гидрогенизации еще может содержать метан и водород, оставшиеся после гидрогенизации, и метан и часть водорода во время отделения могут быть рециркулированы. При этом, метан и водород могут быть рециркулированы индивидуально или в форме газообразной смеси. Например, метан и водород могут быть рециркулированы в форме газообразной смеси, подаваемой в реактор пиролиза вместе со свежим содержащим метан сырьем (или его сочетанием с водородом). В этом случае молярное отношение CH4/H2 в рециркулируемом потоке может лежать в диапазоне, например, от 0,05 до 1, более конкретно, от 0,1 до 0,8, еще более конкретно, от 0,2 до 0,5.
Сочетание пиролиза и гидрогенизации
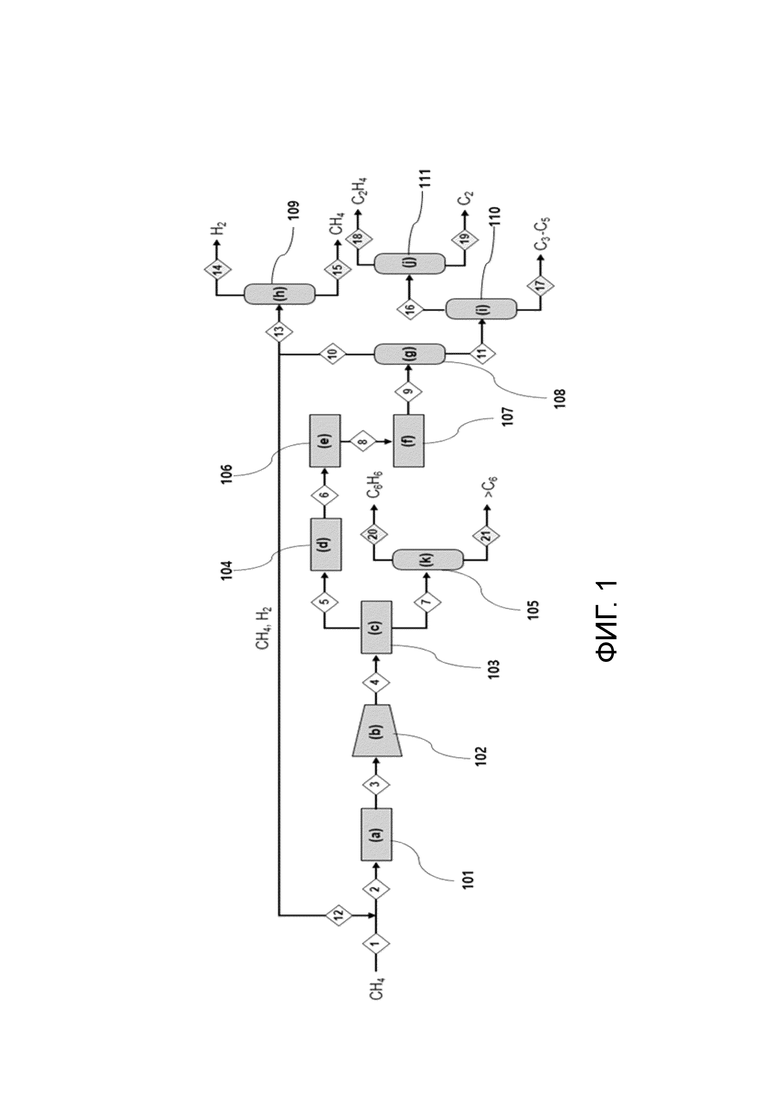
Примерный процесс производства этилена, объединяющий процесс пиролиза метана и процесс гидрогенизации ацетилена, показан на фиг. 1. Этот пример приведен для углубления понимания настоящего изобретения, в частности, процесс пиролиза перед гидрогенизацией может быть проведен по-разному и не обязательно ограничивается вариантом осуществления, описываемым ниже в качестве примера.
Как показано на фигуре, содержащий метан газ 1 в качестве сырья подают в реактор 101 пиролиза в форме газообразной смеси 2 метана и водорода, соединенной с рециркулируемой газообразной смесью (смесь 12 метана и водорода). Например, содержащий метан газ 1, который состоит исключительно из метана или содержит не только метан, но и разжижающий газ, может быть подан в реактор 101 пиролиза. Например, разжижающий газ может представлять собой, по меньшей мере, один газ, выбранный из группы, состоящей из азота, диоксида углерода и сероводорода, количество которого может составлять, самое большее, около 20% мол., в частности, до, примерно, 10% мол, более конкретно до, примерно, 5% мол., еще более конкретно до, примерно, 3% мол., однако, приведенные диапазоны являются иллюстративными.
При этом, тип реактора пиролиза не имеет определенных ограничений, это может быть радиальный трубчатый реактор в силу достаточной эффективности теплопередачи в нем. Кроме того, материал, из которого изготовлен реактор пиролиза, в частности, реактор прямой бескислородной конверсии, может являться, по меньшей мере, одним материалом, выбранным из оксида алюминия, SiC, сплава FeCrAl, Inconel (NiCr) и т.п.
Как известно, молекула метана является неполярной, стабильностью структуры подобна инертному газу, энергия связи С-Н равна 4345 кДж/моль, с высокой термодинамической устойчивостью. Из-за высокой химической и термодинамической устойчивости метан трудно поддается преобразованию в другие соединения. В данном варианте осуществления изобретения побочные продукты - углеводороды С2+ и водород - образуются из метана в ходе реакции прямого бескислородного взаимодействия или реакции взаимодействия в плазме в процессе пиролиза. Далее описан, главным образом, процесс пиролиза, включающий реакцию прямого бескислородного взаимодействия.
В ходе пиролиза после активации метана до метильного радикала проходит реакция радикального типа. Температуру и давление реакции следует тонко регулировать, чтобы повысить степень конверсии метана и подавить образование кокса. Например, температура пиролиза может лежать в диапазоне, например, от 1000 до 1400°С, в частности, от 1050 до 1350°С, более конкретно, от 1100 до 1300°С, еще более конкретно, от 1150 до 1250°С. Кроме того, давление в ходе пиролиза может лежать в диапазоне, например, от 0,1 до 1 бар, в частности, от 0,2 до 0,8 бар, более конкретно, от 0,3 до 0,7 бар, еще более конкретно, от 0,4 до 0,6 бар. Кроме того, часовая объемная скорость газа (GHSV) может быть выбрана из диапазона, например, от 300 до 3600 ч-1, в частности, от 720 до 1800 ч-1, более конкретно, от 900 до 1600 ч-1, еще более конкретно, от 1200 до 1440 ч-1.
В этом варианте осуществления изобретения, как описано выше, рециркулируемая газообразная смесь, подаваемая в реактор вместе со свежим содержащим метан сырьем, содержит метан и водород. Таким образом, реакция пиролиза происходит в присутствии водорода, что является эффективным с точки зрения повышения степени конверсии метана и подавления образования кокса. В этих условиях реакции метан может превращаться, главным образом, в ацетилен, а не в этилен, если рассматривать углеводороды С2. В этом отношении состав материалов в реакторе пиролиза может удовлетворять уравнению 2, приведенному ниже.
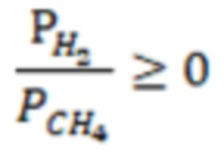 уравнение 2
уравнение 2
в котором РН2 означает парциальное давление водорода в газообразной смеси, подаваемой в реактор, РСН4 означает парциальное давление метана в газообразной смеси, подаваемой в реактор.
В одном из примерных вариантов осуществления изобретения 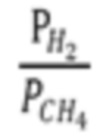 может быть установлено в диапазоне, например, от 0,5 до 3, в частности, от 0,7 до 2,5, более конкретно, от 0,9 до 1,5.
может быть установлено в диапазоне, например, от 0,5 до 3, в частности, от 0,7 до 2,5, более конкретно, от 0,9 до 1,5.
В одном из примерных вариантов осуществления изобретения пиролиз может быть проведен в присутствии катализатора (например, катализатора на подложке), и металл, выполняющий функцию активации метана, может представлять собой, по меньшей мере, один металл, выбранный из группы, состоящей из железа (Fe), хрома (Cr), ванадия (V), молибдена (Mo), вольфрама (W) и т.д. Кроме этого, используемая подложка может быть пористой подложкой, изготовленной из неорганического оксидного материала, например, по меньшей мере, одного материала, выбранного из оксида алюминия, диоксида кремния, диоксида титана, диоксида циркония, оксида магния, диоксида церия и т.п. Кроме этого, количество активного металла в катализаторе может быть установлено в диапазоне, например, от 0,1 до 10% вес., в частности, от 0,3 до 8% вес., более конкретно, от 0,5 до 5% вес. Описанный выше состав катализатора является иллюстративным примером, и настоящее изобретение им не ограничивается.
В соответствии с одним из примерных вариантов осуществления изобретения, степень конверсии метана в результате пиролиза в условиях реакции, описанных выше, может лежать в диапазоне от, примерно, 10 до 50%. При этом, чем ниже степень конверсии метана, тем выше селективность в отношении углеводородов С2+. Например, селективность в отношении углеводородов С2+ при степени конверсии метана в диапазоне от 0 до 10% может достигать, по меньшей мере, около 99,9%, селективность в отношении углеводородов С2+ при степени конверсии метана в диапазоне от 10 до 20% может достигать, по меньшей мере, около 99,5%, селективность в отношении углеводородов С2+ при степени конверсии метана в диапазоне от 20 до 30% может достигать, по меньшей мере, около 95%, селективность в отношении углеводородов С2+ при степени конверсии метана в диапазоне от 30 до 40% может достигать, по меньшей мере, около 90%, селективность в отношении углеводородов С2+ при степени конверсии метана в диапазоне от 40 до 50% может достигать, по меньшей мере, около 80%. Если степень конверсии метана слишком большая, селективность в отношении углеводородов С2+ может быть снижена до, примерно, 70%, тогда как если степень конверсии метана слишком уменьшена, может быть недостаточным выход. Следовательно, выгодно поддерживать степень конверсии метана в диапазоне, например, от 10 до 50%, в частности, от 20 до 40%, более конкретно, от 30 до 35%.
Кроме этого, селективность в отношении ацетилена в продукте пиролиза может лежать в диапазоне, например, по меньшей мере, около 55%, в частности, по меньшей мере, около 60%, более конкретно, от 65 до 70%, а селективность в отношении ароматических соединений (в частности, бензола) может составлять, например, около 30% или менее, в частности, от 5 до 25%, более конкретно, от 10 до 20%.
В соответствии с одним из примерных вариантов осуществления изобретения, продукт пиролиза, помимо ацетилена и ароматики, может дополнительно содержать, по меньшей мере, одно соединение, выбранное из группы, состоящей из этана, этилена, углеводородов С3-С5 и т.п., и его количество может составлять, например, около 40% об. или менее, в частности, 30% об. или менее, более конкретно, около 20% об. или менее относительно количества продукта пиролиза.
Как показано на фиг. 1, продукт 3 пиролиза пропускают через вакуумный насос 102, получая поток 4 со сниженным давлением, который затем быстро охлаждают, например, до температуры от -20 до 25°С (в частности, от -10 до 0°С) в башенном охладителе 103. В описываемом варианте осуществления изобретения газообразную смесь разделяют на верхний поток 5, содержащий углеводороды С5 и водород, и нижний поток 7, содержащий углеводороды С6+ (в частности, бензол и более тяжелые углеводороды). Затем нижний поток 7 разделяют на бензол 20 и более тяжелую фракцию 21 в колонне 105 отделения бензола, откуда он может быть отведен. С другой стороны, верхний поток 5 представляет собой фракцию, содержащую метан, водород и ацетилен, как описано выше, и является газообразной смесью, которая, возможно, может также содержать углеводороды С2 (этан и/или этилен), отличные от ацетилена, и углеводороды С3-С5. Эта газообразная смесь может быть подана в конвертер 104 ацетилена, где может быть проведена селективная гидрогенизация ацетилена, как описано выше.
После этого давление продукта 6 гидрогенизации увеличивают, например, до величины от 10 до 50 бар (в частности, примерно, от 15 до 30 бар), пропуская через компрессор 106 технологического газа, поток 8 повышенного давления может быть охлажден, например, до температуры от -75 до -45°С (в частности, от -60 до -55°С) в холодильной камере 107. Охлажденный поток 9 подают в деметанизатор 108, откуда в качестве верхнего потока отводят газообразную смесь 10, состоящую из метана и более легкого водорода, тогда как поток 11 углеводородов С2+ отводят как нижний поток и затем разделяют на поток 16 углеводородов С2 и поток 17 углеводородов С3-С5 в деэтанизаторе 110. После этого поток 16 углеводородов С2 разделяют на этилен 18 и поток 19 углеводородов С2, отличных от этилена, в устройстве 111 разделения С2. Каждое устройство: деметанизатор 108, деэтанизатор 110 и устройство 111 разделения С2 функционирует в криогенных условиях.
С другой стороны, газообразную смесь 10 разделяют на рециркулируемый поток 12 и отводимый поток 13, рециркулируемый поток соединяют с содержащим метан сырьем и подают в реактор 101 пиролиза. Отводимый поток 13 подают в адсорбер 109 со сдвигом давления и разделяют на водород 14 и метан 15.
В описанном выше варианте осуществления изобретения, поскольку принцип работы блока разделения и очистки после проведения пиролиза и селективной гидрогенизации известен в данной области, описание дополнительных подробностей в этом отношении опускается.
В соответствии с другим вариантом осуществления изобретения, процесс, показанный на фиг. 1, может быть реализован способом, в котором изменено расположение башенного охладителя, вакуумного насоса, конвертера ацетилена и т.д., но сохранена основная конфигурация. Например, когда башенный охладитель, вакуумный насос и конвертер ацетилена расположены последовательно по потоку ниже реактора пиролиза метана, конвертер ацетилена может функционировать при атмосферном или более высоком давлении. Кроме этого, эти технологические установки могут быть расположены последовательно в порядке вакуумный насос, конвертер ацетилена и башенный охладитель или в порядке конвертер ацетилена, вакуумный насос, башенный охладитель. В качестве альтернативы, хотя эти технологические установки могут быть расположены в порядке конвертер ацетилена, вакуумный насос, башенный охладитель или в порядке конвертер ацетилена, башенный охладитель, вакуумный насос, когда углеводороды С6+ поступают на катализатор конверсии ацетилена, срок службы катализатора может сокращаться, что может быть нежелательно.
Для лучшего понимания настоящего изобретения далее приведены примеры, которые лишь поясняют настоящее изобретение и не должны рассматриваться как ограничивающие объем настоящего изобретения.
ПРИМЕРЫ
Получение катализатора
Подложку из оксида алюминия трехдольчатой формы приобрели у компании Saint-Gobain (USA) и использовали без дополнительной очистки. Перед нанесением активных металлов подложку сушили в течении ночи при 80°С в конвекционной печи. Нитрат палладия-аммония (Sigma, 99,9%) в качестве прекурсора первого металла и нитрат меди (Sigma, 99,9%), нитрат золота (Sigma, 99,9%) или нитрат серебра (Sigma, 99,9%) в качестве прекурсора второго металла растворяли в кислом водном растворе (кислотный компонент: 10% вес. азотная кислота). Нанесение металлов проводили способом модифицированной пропитки по влажности, полученный твердый прекурсор сушили при 80°С в конвекционной печи и восстанавливали водородом при 300°С в течении 6 часов (скорость нагревания 5°С/мин). Катализатор, в котором металлический сплав был нанесен на подложку из оксида алюминия, был представлен формулой x%Pdy%M (где х и у означают процентное содержание по весу каждого металла, М означает второй металл (Cu, Ag, или Au)).
Пиролиз и гидрогенизация метана
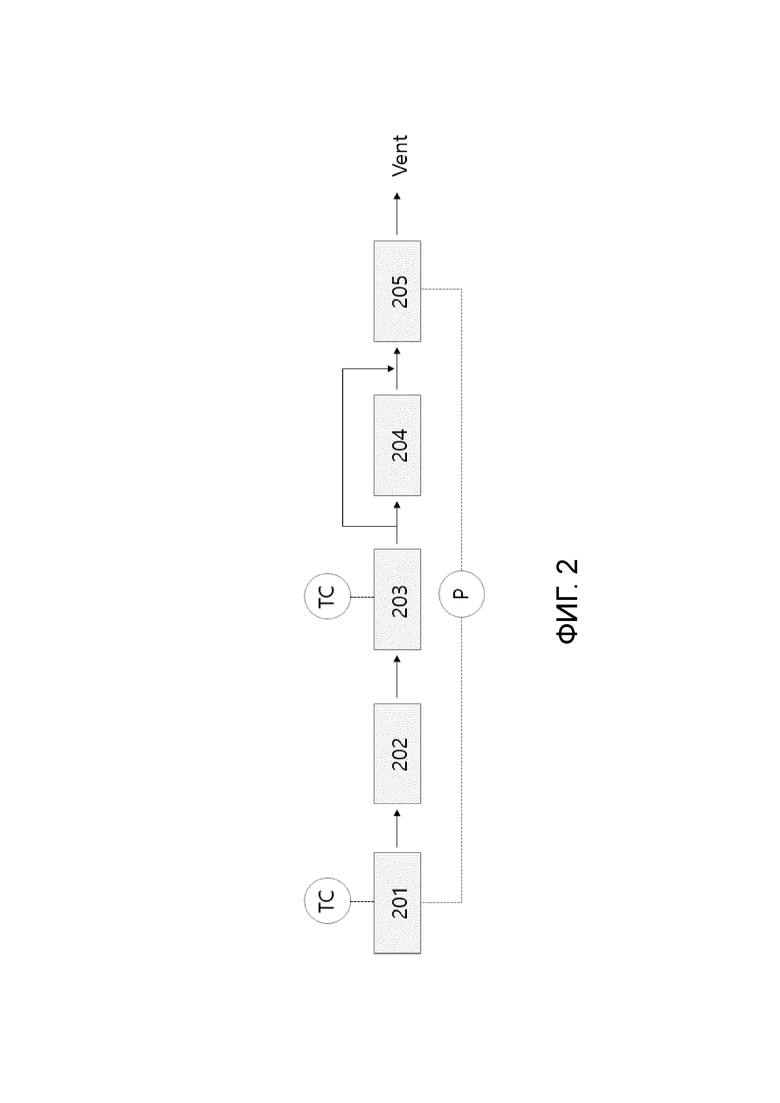
Пиролиз и гидрогенизацию метана проводили в системе с непрерывным потоком. Структура устройства, использованного в данном примере, схематично показана на фиг. 2.
Как показано на чертеже, экспериментальное устройство, вообще, включало пиролизную печь 201, охладитель 202, реактор 203 гидрогенизации, онлайновый газовый хроматограф 204 и вакуумный насос 205. Использовали, главным образом, поток между реактором 203 гидрогенизации и вакуумным насосом 205, а на время анализа переключались с верхнего потока на поток через онлайновый газовый хроматограф 204. Кроме этого, ТС и Р означают термопару и регулятор давления, соответственно.
Более конкретно, в зоне пиролиза метана в центре электропечи, оборудованной нагревательным элементом из силицида молибдена (MoSi2), поместили трубчатый реактор из оксида алюминия (99,9%, наружный диаметр 1/2 дюйма, 12,7 мм). До начала реакции реактор подвергли тепловой обработке при 700°С 2 часа в потоке воздуха (10 мл/мин, 99,9%) для удаления примесей (скорость нагревания 10°С/мин). Газообразную смесь азота, метана (99,999%, Rigas) и водорода (UHP, Riga) подавали в реактор посредством регулятора массового расхода (5850E, Brooks Instrument). Отходящий поток продукта пиролиза охлаждали до -10°С, отделяя таким образом следовые количества полициклической ароматики. Охлажденный газ подавали в зону гидрогенизации, где в центре электропечи был расположен реактор (наружный диаметр 1/2 дюйма, 12,7 мм, 300 мм·л) из нержавеющей стали. Во всех экспериментах реакционная система функционировала под давлением ниже атмосферного, давление реакции регулировали при помощи мембранного вакуум-регулятора (Buchi, V800) и химически-стойкого электромагнитного клапана (Parker). Трубопровод перекачки нагревали до 100°С для предотвращения возможной конденсации. Пробы продукта отбирали с интервалом 2 часа при помощи онлайнового газового хроматографа (Agilent Technology, 7890A), оборудованного капиллярной колонкой HP-PLOT/Al2O3 (50 м х 0,32 мм х 8,0 мм) для пламенно-ионизационного детектора (flame ionized detector, FID) или капиллярной колонкой HP-Molesieve (30 м x 0,53 мм x 20 мм) для термокондуктометрического детектора (thermal conductivity detector, TCD). Газохроматографическая колонка предназначалась для разделения водорода, азота и углеводородов с целью получения информации о степени конверсии метана и количественного анализа концентрации этилена, этана, ацетилена и бензола. Также учитывались следовые количества продуктов С3-С5.
Кроме того, микрокинематическое моделирование, примененное в этом примере, осуществляли при помощи пакета программного обеспечения CANTERA.
Результаты и их пояснение
Моделирование пиролиза метана
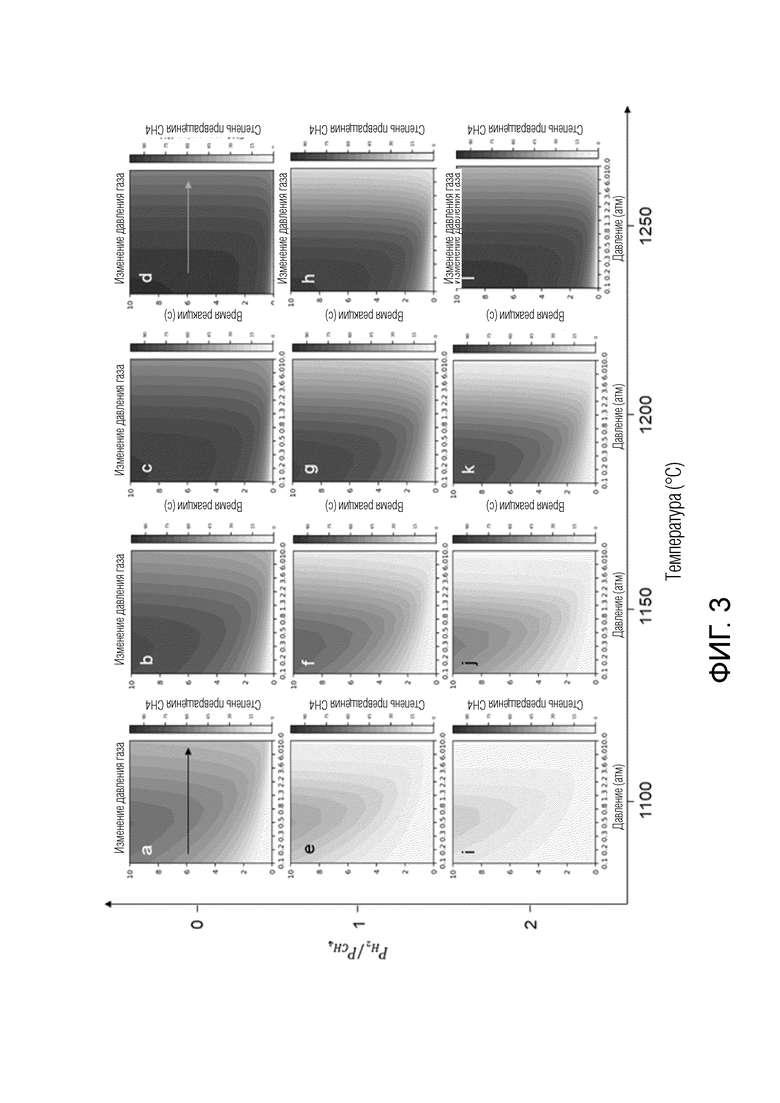
Для выявления оптимальных условий реакции превращения метана в углеводороды с добавленной стоимостью в качестве основных продуктов реакции, провели моделирование пиролиза метана, принимая во внимание четыре параметра реакции (температура: 1150-1250°С; давление: 0,1-10 бар; отношение H2/CH4: 0-1; время пребывания: 0-10 секунд). Влияние каждого параметра реакции на степень конверсии метана и выход продукта изображены изолиниями на фиг. 3А - 3I и 4А - 4I. Каждый график, представленный на фиг. 3А - 3I, отражает влияние сочетания четырех параметров реакции. Степень конверсии метана увеличивалась с увеличением времени пребывания независимо от температуры, тогда как с увеличением отношения H2/CH4 снижалась. Однако, результаты были разными в зависимости от рабочего давления. При температурах до 1150°С график степени конверсии метана имел пиковую форму.
Как показано на фиг. 3А, при 1100°С степень конверсии метана была равна, примерно, 45% при 0,2 бар, достигала пиковой величины 60% при 1 бар и снижалась до 45% при 10 бар (время пребывания 6 секунд) (черная стрелка). Между тем, при 1250°С степень конверсии метана постепенно снижалась по мере увеличения давления реакции (желтая стрелка на фиг. 3D), начиная с 87% при 0,2 бар и достигая 10% при 10 бар (H2/CH4=0; время пребывания 6 секунд). Аналогичная тенденция наблюдалась при 1250°С вне зависимости от того, подавали ли дополнительно водород (фиг. 3D, 3Н, 3I). Следует отметить, что рабочее давление на фиг. 3А - 3I представлено как логарифмическая величина, и что степень конверсии метана чувствительна к изменению давления реакции, особенно при давлении ниже атмосферного. Кроме этого, наивысшая степень конверсии метана была достигнута при давлении ниже атмосферного в ходе увеличения температуры реакции. Предположительно, причина в том, что общая степень конверсии метана термодинамически ограничена присутствием газообразного водорода, легко образующегося в ходе пиролиза метана.
Затем исследовали выход углеводородов, при этом, на основании моделирования определяли выход каждого конкретного углеводорода (этана, этилена, ацетилена и бензола), полученные результаты показаны на фиг. 4А - 4I.
При отношении H2/CH4, равном 0, выход конкретного углеводородного продукта увеличивался с увеличением давления реакции и времени пребывания вне зависимости от температуры (желтые стрелки на фиг. 4А - 4С). Наибольший выход углеводорода при 1100°С, показанный на фиг. 4I, соответствовал тому же диапазону, что и в случае наибольшей степени конверсии, вне зависимости от подачи водорода. Однако, когда температуру увеличивали до 1200°С (фиг. 4F), наибольший выход конкретного продукта получали при 0,5 бар и времени пребывания 3 секунды, что отличается от наибольшей наблюдаемой степени конверсии метана (фиг. 3G). Это различие отражает превращение метана в другие углеводороды, главным образом, полициклические ароматические углеводороды. Результаты моделирования подтверждают представление о том, что регулирование давления реакции и подача водорода являются важными факторами для пиролиза метана с точки зрения селективного получения более тяжелых углеводородов.
В сущности, влияние низкого давления и одновременной подачи углеводородов и водорода на селективность в отношении углеводородов во время пиролиза метана может быть подтверждено путем построения графика зависимости степени конверсии от селективности, как показано на фиг. 5А - 5I. При моделировании этой зависимости в целях выявления влияния давления реакции и подачи водорода условия эксперимента при заданной температуре 1200°С разделили на три области: когда водород подавали (фиг. 5А - 5С), когда водород не подавали (фиг. 5D - 5I), когда рабочее давление было ниже атмосферного (фиг. 5G - 5I), и когда рабочее давление было выше атмосферного (фиг. 5А - 5F).
Измерение степени конверсии метана в зависимости от селективности в отношении углеводородов (этана, этилена, ацетилена и бензола) позволяет спрогнозировать идеальный состав продукта, который строго определяется рабочими условиями. Как явствует из сравнения фиг. 5А и 5D, когда дополнительно подавали водород, общая степень конверсии метана снижалась, Однако, селективность в отношении углеводородов увеличивалась. Например, при нормальных рабочих условиях селективность в отношении С2+С6, достижимая при степени конверсии метана 50%, составляла около 60% (пунктирные линии на фиг. 5А - 5I), но когда также подавали водород, составляла около 80%. Такое повышение можно отнести, главным образом, на счет увеличения селективности в отношении С2 (фиг. 5В и 5Е). Это указывает на то, что водород оказывает значительное влияние на ингибирование образования полициклической ароматики.
К тому же, когда рабочее давление в ходе пиролиза метана устанавливают меньшим атмосферного, диапазон селективности для данной степени конверсии метана может сужаться. Например, для степени конверсии метана около 50% селективность составляла от 60 до 80% при давлении от 1 до 10 бар, но 85% при давлении от 0,1 до 0,5 бар. Такое различие результатов позволяет предположить, что при рабочем давлении ниже атмосферного и одновременной подаче водорода можно достичь максимальной селективности в отношении углеводородов С2+С6 в ходе пиролиза метана.
Экспериментальное подтверждение
Провели дополнительные эксперименты при давлении пиролиза метана ниже атмосферного и одновременной подаче водорода. Для отбора газообразного продукта, выводимого из реактора, снабженного вакуумным насосом, в газообразном отходящем потоке в мягких условиях собирали летучую твердую фазу. Также проводили анализ (данные не показаны) следовых количеств полициклических ароматических углеводородов, таких как нафталин, антрацен и пирен, в полученных углеводородах. Газообразный продукт быстро перемещали в анализатор, примерно, за 1 минуту (фиг. 2).
Результаты эксперимента по пиролизу метана показаны на фиг. 6А и 6В. Рабочие условия, включающие температуру 1240°С, отношение H2/CH4=1, давление 0,5 бар и GHSV=1415 ч-1, выбрали в качестве базовых условий пиролиза метана. В этих условиях средняя степень конверсии метана составляла 34%, селективность в отношении тяжелых углеводородов до бензола составляла 93%. Когда рабочее давление увеличили до 0,6 бар, сначала степень конверсии увеличилась до 41%, а затем постепенно снизилась до 36%, что можно рассматривать как проблему, связанную с теплопередачей, из-за отложения кокса на стенках трубчатого реактора из оксида алюминия. С другой стороны, когда начальное давление реакции составляло 0,4 бар, средняя степень конверсии метана быстро снижалась до 21%, что согласуется с результатами моделирования, показавшими, что степень конверсии метана чувствительна к давлению реакции, как описано выше. Когда температуру увеличивали при постоянном рабочем давлении, сначала увеличившаяся до 43% степень конверсии затем, через 30 часов, снижалась до 32%. Это указывает на то, что для стабильного получения углеводородов следует выбирать надлежащую температуру реакции. Кроме этого, в самых мягких условиях 1220°С и 0,5 бар получили стабильную степень конверсии метана, равную 26%, и селективность в отношении углеводорода, равную 95%.
Кроме этого, на фиг. 7 результаты эксперимента представлены как график степени конверсии относительно селективности в отношении конкретных углеводородов. Как и результаты моделирования, показанные на фиг. 5, результаты эксперимента разделили на три области в зависимости от наличия подачи водорода и давления реакции. В этом эксперименте температуру регулировали в диапазоне от 1000 до 1260°С для достижения целевой степени конверсии метана.
В соответствии с результатами эксперимента, высокую селективность в отношении углеводородов (С2+С6) получили при степени конверсии метана менее 10% (черные квадраты на фиг. 7). Однако, когда степень конверсии метана увеличилась до, примерно, 40%, селективность в отношении углеводородов резко снизилась до, примерно, 30%, главным образом, из-за образования полициклических ароматических углеводородов и/или кокса. Когда подавали водород, селективность, достижимая при степени конверсии метана 40%, составляла около 80% (синие треугольники на фиг. 7). Это является результатом повышенной селективности в отношении С2 и указывает на то, что водород оказывает существенное влияние на подавление образования полициклических ароматических углеводородов. Кроме этого, когда пиролиз метана проводили при давлении ниже атмосферного, селективность увеличивалась. Например, селективность в отношении углеводородов при степени конверсии метана, равной 50%, составляла около 90% при рабочем давлении от 0,3 до 0,5 бар. Как показали результаты эксперимента, наибольший выход углеводорода наблюдался при средней степени конверсии метана 36,9% при 1275°С и 0,3 бар. Эти результаты эксперимента позволяют предположить, что процесс пиролиза метана является перспективным для получения трех основных веществ, а именно, ацетилена, водорода и бензола, в условиях, при которых подавляется образование прекурсоров кокса, таких как полициклические ароматические углеводороды.
Оценка эффективности катализатора
Отходящий газ с уникальным химическим составом получали путем пиролиза метана, описанного выше; продукт пиролиза метана, в котором степень конверсии метана поддерживали равной 30% и из которого удаляли углеводороды С7 и выше, подавали в качестве сырья на гидрогенизацию. Из продукта пиролиза метана удаляли полициклические ароматические углеводороды, следовые количества углеводородов С3-С5 не учитывали, состав продукта приведен в таблице 1 ниже.
Таблица 1
Как показано в таблице 1, когда степень конверсии метана составляла около 30%, соответствующая концентрация метана, водорода и ацетилена в газообразной смеси, подаваемой в реактор гидрогенизации, составляла 32,2%, 62,5%, и 4,5%, что больше, чем в газе, используемом с палладиевыми катализаторами в традиционных конвертерах ацетилена в последние десятилетия. Учитывая это, в настоящем примере использовали катализатор, состоящий из PdCu, PdAu и PdAg, в каждом случае, нанесенного на подложку из оксида алюминия. В целях тестирования катализатор готовили путем регулирования содержания металла способом простой пропитки по влагоемкости.
На фиг. 8А приведен общий выход ацетилена и бензола в гибридной системе пиролиза метана и гидрогенизации с использованием PdCu катализатора. Как показано на фигуре, во время гидрогенизации 99,5% ацетилена превращалось в этилен на PdCu катализатора, и деактивация катализатора не наблюдалась даже через 65 часов. Выход этилена и С2+С6 в гибридной системе составлял 20% и 24%, соответственно. Хотя PdAg катализатор и PdAu катализатор продемонстрировали более низкую каталитическую активность, чем PdCu катализатор, PdAg катализатор также характеризовался относительно высокой селективностью (98%) при степени конверсии метана около 60% и поэтому также считается перспективным (фиг. 8В). При использовании PdAu катализатора получили высокую степень конверсии ацетилена, однако основным продуктом был этан, что указывает на то, что применимость этого катализатора для селективной гидрогенизации газообразной смеси, содержащей ацетилен в высокой концентрации и водород, ограничена. Полученные результаты позволяют предположить, что гибридная система, соответствующая настоящему примеру, обладает большим потенциалом с точки зрения непрерывного получения ценного этилена из метана.
При этом, весовое соотношение Pd и Cu, нанесенных на подложку, в составе катализатора гидрогенизации регулировали, как показано в таблице 2 ниже.
Таблица 2
(Сравн. пример)
(Пример)
(Пример)
(Пример)
(Сравн. пример)
Таблица 3
(oC)
Как показано в таблицах 2 и 3, в присутствии 0,2Pd катализатора, не содержащего Cu (сравнительный пример), была достигнута высокая степень конверсии по сравнению с использованием 0,2Pd1Cu, 0,2Pd2Cu и 0,2Pd3Cu, которые содержали Cu, однако, селективность в отношении этилена была низкой, к тому же, в присутствии 1Cu без Pd (сравнительный пример) эффективность в отношении гидрогенизации ацетилена была очень низкой. Было подтверждено, что в присутствии катализаторов, содержащих Pd и Cu в соответствии с примерами, степень конверсии снижается, но селективность в отношении этилена увеличивается при той же температуре с увеличением содержания Cu. В частности, тенденция к увеличению селективности с увеличением содержания Cu от 1% вес. до 3% вес. указывает на то, что атомы Pd находятся на наночастицах Cu, низкоэффективных в отношении гидрогенизации ацетилена, однако, создающих в этом катализаторе среду, в которой атомы Pd могут селективно гидрогенизировать ацетилен, тем самым, обеспечивая селективную гидрогенизацию ацетилена, присутствующего в высокой концентрации.
Из приведенного описания явствует, что способ производства этилена и водорода из газообразной смеси в соответствии с одним из вариантов осуществления настоящего изобретения пригоден для получения этилена с высоким выходом путем селективной гидрогенизации ацетилена в газообразной смеси в присутствии биметаллического катализатора на подложке, принимая во внимание состав продуктов, содержащих ацетилен в относительно высокой концентрации в зависимости от условий реакции пиролиза метана. Кроме этого, водород может быть извлечен из газообразной смеси и выгодно использован, а также применен в качестве источника водорода для селективной гидрогенизации ацетилена, тем самым, устраняя потребность в подводе водорода из внешних источников. Кроме этого, когда метан и/или водород отделяют от продуктов гидрогенизации и рециркулируют в осуществляемую выше по потоку реакцию пиролиза метана, возможно увеличение степени конверсии метана и подавление образования кокса во время пиролиза метана. В частности, может быть увеличена селективность в отношении ацетилена, благодаря чему возможно получение газообразной смеси, в которой большую часть углеводородов С2 в продуктах пиролиза метана составляет ацетилен. В сущности, способ, соответствующий данному варианту осуществления изобретения, особенно выгоден для внедрения в промышленности из-за повышения эффективности превращения метана в базовые химические соединения с добавленной стоимостью и т.д. путем селективной гидрогенизации, отдельно или в сочетании с другими процессами выше или ниже по потоку.
Для специалистов в данной области очевидны возможные модификации или изменения настоящего изобретения, и все подобные модификации или изменения могут рассматриваться включенными в объем настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БОЛЕЕ ЭНЕРГОЭФФЕКТИВНЫЙ СПОСОБ ГИДРОГЕНИЗАЦИИ С5 | 2013 |
|
RU2627657C2 |
| СПОСОБ ХИМИЧЕСКОЙ ПЕРЕРАБОТКИ СМЕСЕЙ ГАЗООБРАЗНЫХ УГЛЕВОДОРОДОВ (АЛКАНОВ) C-C В ОЛЕФИНЫ C-C (ЭТИЛЕН И ПРОПИЛЕН) | 2010 |
|
RU2435830C1 |
| ПОЛУЧЕНИЕ ЖИДКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2405764C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ ИЗ АЛИФАТИЧЕСКИХ | 2008 |
|
RU2461537C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ И СИНТЕЗ-ГАЗА ИЗ МЕТАНА | 2007 |
|
RU2458899C2 |
| ИНТЕГРИРОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ ВИНИЛХЛОРИДА | 2001 |
|
RU2184721C1 |
| КОНВЕРСИЯ ТЯЖЕЛЫХ ИСКОПАЕМЫХ УГЛЕВОДОРОДОВ И МОДЕРНИЗАЦИЯ С ИСПОЛЬЗОВАНИЕМ РАДИОЧАСТОТНОЙ ИЛИ МИКРОВОЛНОВОЙ ЭНЕРГИИ | 2012 |
|
RU2636151C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2418780C2 |
| ПОЛУЧЕНИЕ АЛКИЛИРОВАННЫХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2417974C2 |
| СПОСОБ УДАЛЕНИЯ КИСЛОРОДА ИЗ СОДЕРЖАЩИХ ОЛЕФИНЫ ТЕХНОЛОГИЧЕСКИХ ПОТОКОВ | 2003 |
|
RU2312128C2 |
Настоящее изобретение относится к способу селективной гидрогенизации газообразной смеси с высоким содержанием ацетилена. Описан способ селективной гидрогенизации, включающий стадии, на которых: а) обеспечивают газообразную смесь, содержащую от 2 до 10% мол. ацетилена, от 50 до 75% мол. водорода и от 18 до 48% мол. метана, при этом концентрация отличных от ацетилена углеводородов С2 в смеси составляет не более 1% мол.; b) производят продукт гидрогенизации, содержащий этилен, полученный из указанной газообразной смеси, путем гидрогенизации газообразной смеси в присутствии катализатора гидрогенизации, в котором первый металл (М1), активный в отношении гидрогенизации, и второй металл (М2), функцией которого является индуцирование селективной гидрогенизации, нанесены на пористую подложку, и с) отделяют и извлекают этилен и водород из продукта гидрогенизации, при этом первый металл (М1) представляет собой, по меньшей мере, один металл, выбранный из группы, состоящей из Pd, Pt, Rh, Ir, Ni и Co, и второй металл (M2) представляет собой, по меньшей мере, один металл, выбранный из группы, состоящей из Cu, Ag, Au, Zn, Ga и Sn, и количество первого металла (М1) и второго металла (М2) в катализаторе гидрогенизации составляет от 0,15 до 2% вес. и от 0,8 до 30% вес., соответственно, и удовлетворяет уравнению: 3≤WM2/ WM1<20, в котором WM1 означает весовое процентное содержание первого металла в катализаторе гидрогенизации, и WM2 означает весовое процентное содержание второго металла в катализаторе гидрогенизации. Технический результат – получение в качестве продукта гидрогенизации газообразной смеси, содержащей, в частности, ацетилен и водород, этилена как ценного химического сырья. 15 з.п. ф-лы, 8 ил., 3 табл., 5 пр.
1. Способ селективной гидрогенизации, включающий стадии, на которых:
а) обеспечивают газообразную смесь, содержащую от 2 до 10% мол. ацетилена, от 50 до 75% мол. водорода и от 18 до 48% мол. метана, при этом концентрация отличных от ацетилена углеводородов С2 в смеси составляет не более 1% мол.;
b) производят продукт гидрогенизации, содержащий этилен, полученный из указанной газообразной смеси, путем гидрогенизации газообразной смеси в присутствии катализатора гидрогенизации, в котором первый металл (М1), активный в отношении гидрогенизации, и второй металл (М2), функцией которого является индуцирование селективной гидрогенизации, нанесены на пористую подложку, и
с) отделяют и извлекают этилен и водород из продукта гидрогенизации,
при этом первый металл (М1) представляет собой, по меньшей мере, один металл, выбранный из группы, состоящей из Pd, Pt, Rh, Ir, Ni и Co, и второй металл (M2) представляет собой, по меньшей мере, один металл, выбранный из группы, состоящей из Cu, Ag, Au, Zn, Ga и Sn, и
количество первого металла (М1) и второго металла (М2) в катализаторе гидрогенизации составляет от 0,15 до 2% вес. и от 0,8 до 30% вес., соответственно, и удовлетворяет уравнению 1:
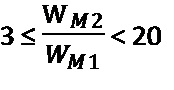 Уравнение 1
Уравнение 1
в котором WM1 означает весовое процентное содержание первого металла в катализаторе гидрогенизации, и WM2 означает весовое процентное содержание второго металла в катализаторе гидрогенизации.
2. Способ по п. 1, в котором газообразная смесь, обеспечиваемая на стадии а), получена путем удаления ароматических соединений из продукта пиролиза метана.
3. Способ по п. 1, в котором источник метана представляет собой, по меньшей мере, один источник, выбранный из группы, состоящей из метана, природного газа и биогаза.
4. Способ по п. 1, дополнительно включающий рециркуляцию метана и, по меньшей мере, части водорода из продукта гидрогенизации в реакцию пиролиза метана.
5. Способ по п. 4, в котором рециркуляцию проводят при молярном отношении CH4/H2 от 0,05 до 1.
6. Способ по п. 1, в котором газообразная смесь содержит от 3 до 10% мол. ацетилена, от 52 до 75% мол. водорода и от 18 до 45% мол. метана.
7. Способ по п. 1, в котором газообразная смесь дополнительно содержит, по меньшей мере, один углеводород, выбранный из группы, состоящей из углеводородов С3 - С5, в концентрации не более 1% мол.
8. Способ по п. 1, в котором стадию b) осуществляют без подвода водорода извне.
9. Способ по п. 1, в котором первый металл (М1) и второй металл (М2) в катализаторе гидрогенизации являются палладием (Pd) и медью (Cu), соответственно.
10. Способ по п. 1, в котором пористая подложка катализатора гидрогенизации представляет собой, по меньшей мере, один материал, выбранный из группы, состоящей из оксида алюминия, диоксида кремния, углерода, диоксида циркония, диоксида титана, диоксида церия и карбида кремния.
11. Способ по п. 10, в котором пористая подложка характеризуется удельной площадью поверхности (по ВЕТ), по меньшей мере, 300 м2/г, объемом пор, по меньшей мере, 0,5 см3/г и средним размером пор от 50 до 200 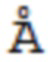 .
.
12. Способ по п. 1, в котором катализатор гидрогенизации получен способом, включающим стадии, на которых: подготавливают твердый прекурсор путем пропитки подложки разбрызгиванием раствора комбинированного прекурсора, в котором объединены прекурсор первого металла М1 и прекурсор второго металла М2.
13. Способ по п. 12, где данный способ дополнительно включает восстановление прекурсора первого металла (М1) и прекурсора второго металла (М2) в твердом прекурсоре при температуре от 200 до 400°С в восстановительной атмосфере.
14. Способ по п. 13, в котором восстановление проводят в атмосфере чистого водорода или в атмосфере водорода, разбавленного инертным газом.
15. Способ по п. 1, в котором стадию b) гидрогенизации проводят при температуре от комнатной температуры до 250°С и под давлением от 0,2 до 1 бар.
16. Способ по п. 15, в котором стадию b) проводят в непрерывном режиме, при этом часовую объемную скорость газа поддерживают в диапазоне от 1 до 15 л/гкат⋅ч-1.
| KR 1020180113448 A, 16.10.2018 | |||
| Устройство для профессионального отбора радиотелеграфистов | 1985 |
|
SU1317468A1 |
| US 8460937 B2, 11.06.2013 | |||
| Приспособление для защиты грудных детей от отравляющих веществ | 1933 |
|
SU36181A1 |
| US 20150353449 A1, 10.12.2015 | |||
| Способ получения поваренной соли из рапы морского типа | 1928 |
|
SU13242A1 |
| СПОСОБ ПРОМЫШЛЕННОГО ПОЛУЧЕНИЯ ОЛЕФИНОВ С ИСПОЛЬЗОВАНИЕМ КАТАЛИТИЧЕСКОЙ ПЕРЕГОНКИ (ВАРИАНТЫ) | 1997 |
|
RU2167188C1 |
Авторы
Даты
2025-03-14—Публикация
2022-10-25—Подача