Изобретение относится к области переработки углеводородных газов, в частности природного, попутного нефтяного газа и иных газовых смесей, образующихся на различных стадиях переработки углеводородного и иного органического сырья и содержащих в качестве основных компонентов низшие алканы, в частности парафины или предельные углеводороды с числом атомов углерода от 1 до 6 (C1-С6 алканы).
Эти соединения являются наименее реакционноспособными из всех органических веществ и самостоятельно не используются в производстве химической продукции. Они имеют широкое применение в качестве энергоносителей, однако их транспортировка на значительные расстояния от места добычи или образования в качестве побочных продуктов различных производств является весьма металло- и энергоемкой и экономически нецелесообразна при относительно небольшом объеме производства.
В связи с этим значительные объемы таких газовых смесей подвергаются факельному сжиганию или выбрасываются в атмосферу, нанося ущерб окружающей среде. Однако они создают гораздо более интенсивный парниковый эффект по сравнению с CO2, являющимся основным продуктом их сгорания.
Как правило, основным компонентом газовых смесей рассматриваемого типа является метан, и в значительной мере задача их химической переработки сводится к вовлечению в реакцию именно метана, который обладает наименьшей реакционной способностью из всех углеводородов.
Известен способ прямого превращения метана в жидкие продукты, например метанол, прямым окислением (B.C.Арутюнов, О.В.Крылов. Окислительные превращения метана. М.: Наука, 1998 г., 361 стр.).
В известном способе процесс протекает при высоких давлениях, предпочтительно не ниже 70 атм, и температурах 350-600°С. Для его осуществления к газу добавляют до 5 об.% кислорода и ведут процесс до его полного превращения. При этом степень превращения метана не превышает нескольких процентов, а выход метанола достигает 2-3% на пропущенный метан. При добавлении большего количества кислорода удается добиться более высокой конверсии метана, однако выход целевого продукта резко снижается из-за преобладания глубокого окисления.
При более низком атмосферном давлении протекает окисление метана в формальдегид, однако по тем же причинам, а именно преобладание процессов глубокого окисления при возрастании степени превращения, его максимально достижимый выход не превышает 1,5-2% на пропущенный метан.
Метан может быть превращен в высшие, в т.ч. жидкие, углеводороды в процессе дегидрирования, протекающего в присутствии твердых контактов, как правило, нанесенных на цеолиты металлов, предпочтительно вольфрама и молибдена (B.C.Арутюнов, О.В.Крылов. Окислительные превращения метана. М.: Наука, 1998 г., 361 стр.).
В этом процессе может быть достигнут более высокий выход целевых продуктов, однако он имеет ряд недостатков:
(а) быстрое падение активности контактов и необходимость их регенерации через относительно короткий промежуток времени;
(б) энергозатратность;
(в) низкая производительность;
(г) сложное аппаратурное оформление процесса.
Известен способ получения этилена из природного газа по реакции окислительной конденсации метана (ОКМ) (B.C.Арутюнов, О.В.Крылов. Окислительные превращения метана. М.: Наука, 1998 г., 361 стр.).
Из всех рассмотренных реакций прямого превращения метана в этом процессе возможно достижение максимального выхода целевого продукта, в частности, по подтвержденным данным, до 12-15% этилена и дополнительно 5-8% этана. Для осуществления способа предложено большое количество катализаторов, ведущих процесс окислительной конденсации метана, который наиболее эффективно протекает при 800-900°С, атмосферном или повышенном до 3-5 атм давлении и подаче метана и кислорода в отношении 2-10. Процесс ведут до полного превращения кислорода, при котором реакционная смесь содержит целевые продукты этилен и этан, оксиды углерода, воду и некоторое количество иных углеводородов - ацетилен и соединения С3+. Коэффициент использования сырья (метана) увеличивается при организации процесса с рециклом. Оптимизация процесса ведется по всем указанным параметрам (катализатор, температура, давление, состав исходной смеси, кратность циркуляции), а также по типу реактора, скорости подачи сырья и др. На эффективность процесса в целом также влияет способ выделения и очистки целевого продукта, возможность и степень утилизации тепла и побочных продуктов.
Известен способ конвертирования метана и С2-С6 алканов в олефины С2-С3 (этилен и пропилен) без их предварительного разделения. Способ включает стадии совместной переработки метана и С2 алканов:, окислительной конденсации метана (ОКМ), неокислительного пиролиза в одном реакторе с псевдоожиженным слоем; при этом на стадии пиролиза используется тепло реакции ОКМ (Патент США №5118898, МПК С07С 2/84, опубл. 02.06. 1992 г.).
Наиболее близким по технической сущности и достигаемому результату является интегрированный способ получения олефинов, который осуществляют путем конверсии метана, содержащегося в метансодержащей газовой смеси, в высшие углеводороды на стадии окислительного сочетания (синоним ОКМ) в присутствии катализатора, воздуха и/или кислорода с молярным соотношением СН4/O2 от 1 до 100, при температуре от 500 до 1000°С, давлении 0,01-10 атм и времени контакта 0,01-10 сек. Затем осуществляют дегидрогенизацию указанных высших углеводородов с помощью катализатора при температуре от 400 до 950°С, давлении 0,01-10 атм и продолжительности контакта 0,01-50 сек с получением смеси, содержащей соответствующие олефины. Далее удаляют из этой смеси Н2O, СO2, СО и Н2, удаляют из смеси олефинов неконвертированный метан и рециркулируют его на вход стадии окислительного сочетания, отделяют от смеси олефинов этилен, отделяют от смеси олефинов этан. В описании также упоминается, что при значительном содержании алканов С2+ смесь рекомендуется сразу подавать на стадию дегидрирования (Патент РФ №2100334, МПК С07С 2/84, С07С 5/333, опубл. 27.12.1997).
Однако при переработке известными способами газовых смесей, содержащих значительное количество высших по сравнению с метаном алканов (С2-С6) возникают дополнительные сложности, связанные с тем, что реакционная способность этих углеводородов значительно выше, чем у метана. В результате, при их подаче в реактор одновременно с метаном они окисляются в первую очередь, потребляя значительное количество кислорода, а метан в реакцию не вовлекается. Кроме того, в условиях реакции окислительной конденсации метана (ОКМ) алканы С2-С6 подвергаются глубокому окислению, что дополнительно резко увеличивает потребление кислорода), и крекингу с образованием углеродистых отложений, приводящих к дезактивации катализаторов. Также предварительное отделение С2-С6 алканов от метана связано с серьезными техническими трудностями и высокими энергозатратами из-за низкого, в пределах нескольких объемных процентов, их содержания в рассматриваемых смесях.
Технической задачей, на решение которой направлено заявляемое изобретение, является создание нового эффективного способа химической переработки смесей газообразных углеводородов (алканов) С1-С6 в олефины С2-С3 (этилен и пропилен), которые могут служить химическим сырьем для дальнейшей переработки, или в жидкие продукты, транспортировка которых сопряжена с меньшими затратами.
Поставленная техническая задача решается тем, что в способе химической переработки смесей газообразных углеводородов (алканов) С1-С6 в олефины С2-С3 (этилен и пропилен), заключающемся в осуществлении реакций окислительной конденсации метана и пиролиза алканов С2-С6, согласно предложенному изобретению осуществляют окислительный пиролиз алканов С1-С6, который проводят при температуре от 450°С до 850°С, давлении от 1 атм до 40 атм и подаче не более 15 об.% кислорода в присутствии оксидных катализаторов без предварительного разделения исходной смеси газообразных углеводородов (алканов) С1-С6 на составляющие компоненты и/или отделения метана, реакцию окислительной конденсации метана осуществляют в потоке метана, отделенного от продуктов окислительного пиролиза алканов С2-С6, в присутствии оксидных катализаторов при температуре от 700°С до 950°С, давлении от 1 атм до 10 атм и мольном соотношении метана и кислорода в интервале от 2:1 до 10:1, при этом выделение продуктов окислительной конденсации метана проводят совместно или частично совместно с выделением продуктов окислительного пиролиза алканов С2-С6, а отделенные от реакционных газов метан, этан и алканы С3+ подвергают рециклу и направляют повторно на стадии окислительной конденсации метана и пиролиза алканов С3-С6 соответственно.
Кроме того, что оксидный катализатор выбирают из группы: оксиды щелочноземельных элементов Mg, Ca, Sr, Ba, оксиды редкоземельных элементов La, Се, Nd, Sm или их смеси, промотированные добавками щелочных элементов (Li, Na, К, Rb, Cs), Sb, Bi и/или Pb, нанесенными на носители Аl2О3, SiO2, TiO2, ZrO2, НfO2, алюминаты, силикаты щелочноземельных элементов, силикаты редкоземельных элементов.
Кроме того, состав оксидного катализатора выбирают в соответствии с эмпирической формулой
М1 aМ2 bМ3 2О3+m,
где М1 - щелочноземельный элемент, выбранный из группы Mg, Ca, Sr, Ba (или их комбинация);
М2 - щелочной элемент, выбранный из группы Li, Na, К, Rb, Cs (или их комбинация);
М3 - редкоземельный элемент, выбранный из группы La, Се, Nd, Sm (или их комбинация);
а - грамм-атомный показатель элемента, значение которого выбирают от 0,005 до 250;
b - грамм-атомный показатель элемента, значение которого выбирают от 0 до 20;
m - стехиометрический коэффициент, определяемый соотношением компонентов М1, М2 и М3.
Кроме того, состав оксидного катализатора выбирают в соответствии с эмпирической формулой
NaXWYMZSiO2+n,
где М - химический элемент Мn или Се,
X, Y, Z - грамм-атомные соотношения элементов, из которых значение Х выбирают от 0,01 до 0,4; значение Y выбирают от 0,005 до 0,2; значение Z выбирают от 0,005 до 0,4.
Кроме того, оксидный катализатор окислительного пиролиза алканов С2-С6 выбирают из группы: смешанные оксиды хрома, никеля и/или ванадия и сурьмы, нанесенные на носители Аl2О3, SiO2, TiO2, ZrO2, HfO2, MgO.
Кроме того, выделение продуктов окислительной конденсации метана осуществляют частично совместно с выделением продуктов окислительного пиролиза алканов С2-С6 при содержании углеводородов (алканов) С2-С6 в исходной смеси выше 15-20% в пересчете на число атомов углерода по отношению к метану.
Кроме того, выделение продуктов окислительной конденсации метана осуществляют совместно с выделением продуктов окислительного пиролиза алканов С2-С6, при содержании углеводородов (алканов) С2-С6 в исходной смеси ниже 10-15% в пересчете на число атомов углерода по отношению к метану.
Кроме того, разделение части продуктов окислительной конденсации метана - фракции углеводородов С2+ - осуществляют совместно с выделением продуктов окислительного пиролиза исходной смеси углеводородов C1-С6, при содержании углеводородов (алканов) С2-С6 в исходной смеси выше 10-15% в пересчете на число атомов углерода по отношению к метану.
Технический результат, достижение которого обеспечивается реализацией заявляемой совокупностью существенных признаков изобретения, состоит в увеличении степени превращения исходного сырья, а именно углеводородов (алканов) С2-С6, в целевые продукты - олефины С2-С3 (этилен и пропилен), а также в снижении энергозатрат на выделение целевых продуктов.
Сущность изобретения поясняется чертежами, где
на фиг.1 представлена блок-схема установки, реализующей предложенный способ при относительно низких концентрациях алканов С2-С6 в исходной смеси до 10-15% в пересчете на число атомов углерода по отношению к метану;
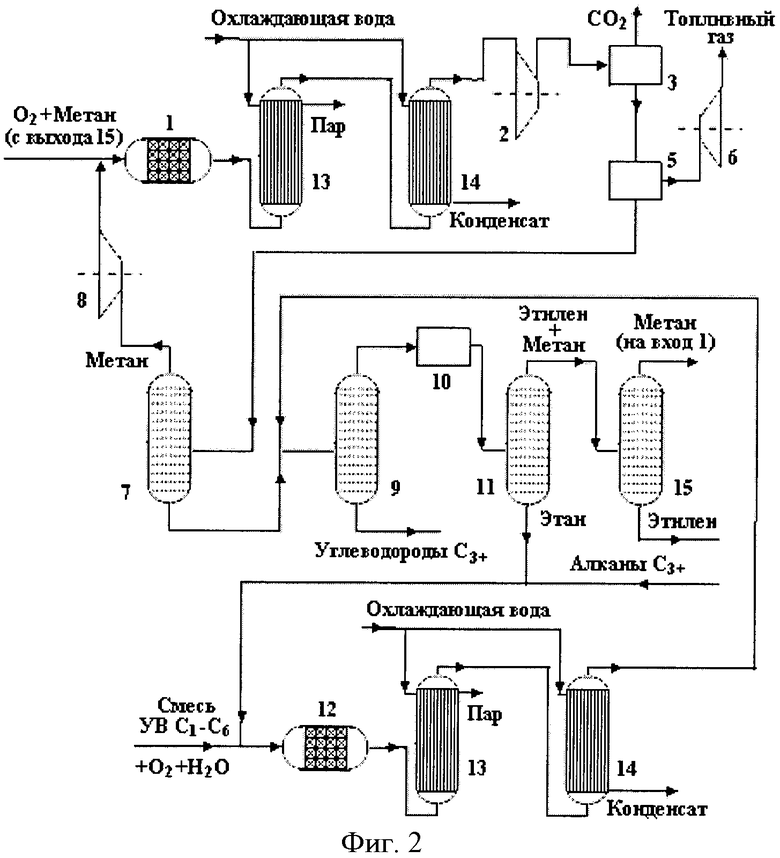
на фиг.2 представлена блок-схема установки, реализующей предложенный способ при более высоких концентрациях алканов С2-С6 в исходной смеси выше 15-20% в пересчете на число атомов углерода по отношению к метану.
Фиг.1 и 2 содержат следующие позиции:
1 - реактор окислительной конденсации метана (ОКМ);
2 - компрессор реакционного газа;
3 - узел этаноламиновой очистки;
4 - узел щелочной промывки, осушки и охлаждения до минус 100°С с помощью пропиленового и этиленового холодильных циклов;
5 - узел выделения топливного газа;
6 - турбодетандер;
7 - колонна низкотемпературной ректификации (выделения метана);
8 - турбодетандер ;
9 - колонна низкотемпературной ректификации (выделения этан-этиленовой фракции);
10 - блок очистки от ацетилена (промывкой диметилформамидом или селективным гидрированием в присутствии Pd-содержащего катализатора);
11 - колонна низкотемпературной ректификации (выделения товарного этилена);
12 - реактор пиролиза (или окислительного пиролиза) алканов С2-С6;
13 - закалочно-испарительный теплообменный аппарат (генератор пара высокого давления);
14 - теплообменный аппарат, в котором газовая смесь охлаждается до ~30°С с конденсацией основной части реакционной воды;
15 - колонна низкотемпературной ректификации (выделения метана).
Примеры технологических схем реализации процесса по предложенному способу представлены на фиг. 1 и 2.
При относительно низких концентрациях алканов С2-С6 в исходной смеси до 10-15% в пересчете на число атомов углерода по отношению к метану предложенный способ осуществляется на установке, блок-схема которой представлена на фиг.1. Исходная смесь углеводородов C1-С6, возможно с добавлением паров воды и/или окислителя (кислорода или воздуха) совместно с рецикловыми этаном и алканами С3+ (в основном пропаном), подается в реактор 12 пиролиза (или окислительного пиролиза), в котором основная часть алканов С2-С6 конвертируется, в том числе с образованием этилена и пропилена.
Реакцию пиролиза (окислительного пиролиза) алканов С2-С6 проводят при температуре от 450°С до 850°С (предпочтительно от 500°С до 750°С), давлении от 1 атм до 40 атм (предпочтительно 1 атм до 10 атм) и подаче не более 15 об.% кислорода (предпочтительно не более 10 об.%) в присутствии оксидных катализаторов.
На выходе из реактора 12 реакционная смесь соединяется с потоком реакционной смеси из реактора 1 окислительной конденсации метана (ОКМ).
При этом реакцию окислительной конденсации метана в реакторе 1 проводят в присутствии оксидных катализаторов при температуре от 700°С до 950°С (предпочтительно от 750°С до 900°С), давлении от 1 атм до 10 атм (предпочтительно от 1 атм до 3 атм) и мольном соотношении метана и кислорода в интервале от 2:1 до 10:1
Соединенный поток газов последовательно охлаждается в каскаде теплообменных аппаратов. На фиг.1 представлено два теплообменных аппарата 13 и 14, в первом из которых при предварительном охлаждении генерируется высокопотенциальный пар, а во втором происходит отделение основного количества реакционной воды в виде конденсата. После охлаждения до 30°С реакционная смесь через компрессор 2 реакционного газа поступает в узел 3 этаноламиновой очистки, где отделяется основное количество СO2. В узле 4 происходит доочистка потока щелочной промывкой, осушка и охлаждение до минус 100°С с помощью пропиленового и этиленового холодильных циклов. В узле 5 происходит выделение топливного газа, в который уходят водород, оксид углерода, азот, остатки кислорода и небольшая часть метана. Этот поток дросселируется до давления 0.3-0.5 МПа через турбодетандер 6. В колонне 7 выделяется непрореагировавший метан, который через турбодетандер 8 после смешения с окислителем (кислород или воздух) подается в реактор 1 ОКМ.
Из куба колонны 7 выводится фракция C2+, которая поступает в колонну 9. Кубовый остаток из этой колонны состоит в основном из углеводородов С3+, при разделении которой (узел разделения на схеме не показан) получают пропилен и смесь алканов С3+, которая возвращается в реактор 12. Из верхней части этой колонны выводится этан-этиленовая фракция, содержащая примеси ацетилена. Удаление ацетилена производится в очистном блоке 10 промывкой диметилформамидом или селективным гидрированием в присутствии Pd-содержащего катализатора. Выделение товарного этилена производится в колонне 11. Кубовый продукт этой колонны - этан - возвращается в реактор 12.
При относительно высоких концентрациях алканов С2-С6 в исходной смеси, выше 10-15% в пересчете на число атомов углерода по отношению к метану, предложенный способ осуществляется на установке, блок-схема которой представлена на фиг.2. Отличием реализации процесса по этой схеме является то, что выделенные из реакционных газов этан и смесь алканов С3+ соединяются с потоком исходной смеси и подаются на вход реактора 12, а на вход колонны 9 низкотемпературной ректификации подается смесь газов после реактора 12 и конденсации реакционной воды и кубовый остаток из колонны 7, содержащий углеводородную часть С2+ после разделения реакционной смеси из реактора 1 ОКМ.
При этом оксидный катализатор выбирают из группы: оксиды щелочноземельных элементов Mg, Са, Sr, Ва, оксиды редкоземельных элементов La, Се, Nd, Sm или их смеси, промотированные добавками щелочных элементов (Li, Na, К, Rb, Cs), Sb, Bi и/или Pb, нанесенными на носители Аl2О3, SiO2, TiO2, ZrO2, НfO2, алюминаты, силикаты щелочноземельных элементов, силикаты редкоземельных элементов.
Также состав оксидного катализатора выбирают в соответствии с эмпирической формулой
М1 aМ2 bМ3 2O3+m,
где М1 - щелочноземельный элемент, выбранный из группы Mg, Ca, Sr, Ва (или их комбинация);
М2 - щелочноземельный элемент, выбранный из группы Li, Na, К, Rb, Cs (или их комбинация);
М3 - редкоземельный элемент, выбранный из группы La, Се, Nd, Sm (или их комбинация);
а - грамм-атомный показатель элемента, значение которого выбирают от 0,005 до 250;
b - грамм-атомный показатель элемента, значение которого выбирают от 0 до 20;
m - стехиометрический коэффициент, определяемый соотношением компонентов М1, М2 и М3.
Кроме того, состав оксидного катализатора выбирают в соответствии с эмпирической формулой
NaXWYMZSiO2+n,
где М - химический элемент Мn или Се,
X, Y, Z - грамм-атомные соотношения элементов, из которых значение Х выбирают от 0,01 до 0,4; значение Y выбирают от 0,005 до 0,2; значение Z выбирают от 0,005 до 0,4.
Кроме того, оксидный катализатор выбирают из группы: смешанные оксиды хрома, никеля и/или ванадия и сурьмы, нанесенные на носители Аl2О3, SiO2, TiO2, ZrO2, НfO2, MgO.
Оксидные катализаторы, проявляющие высокую эффективность в процессах окислительной конденсации метана и окислительного дегидрирования низших алканов, широко известны и подробно описаны в научно-технической литературе.
Сведения об оксидных катализаторах, которые выбирают в соответствии с эмпирической формулой М1 aМ2 bМ3 2О3+m, например, приводятся на стр.223-239 монографии B.C.Арутюнова, О.В.Крылова (Окислительные превращения метана. М.: Наука, 1998), где описаны каталитические свойства смешанных оксидов, содержащих в различных соотношениях катионы редкоземельных, щелочноземельных и щелочных металлов, и дана подробная библиография (ссылки на патенты и научные публикации). Совокупность этих данных показывает, что наиболее эффективны системы, содержащие первые члены ряда лантаноидов (La, Nd, Sm и в определенных комбинациях - также Се и Рr). Лучшие показатели по выходу продуктов ОКМ на катализаторах этого семейства (подтвержденные независимо многими авторами) достигают 18-19% при селективности выше 60%.
На стр.245 той же монографии описаны оксидные катализаторы, соответствующие эмпирической формуле NaXWYMnZSiO2+n и впервые предложенные в работе [Fang X.P., Li S.B., Lin J.Z. J. Mol. Catal. (China), v.6, 1992, p.225]. Эти катализаторы (например, состава 20%Na2WO4+5%Mn/SiO2) позволяют получить наиболее высокий подтвержденный выход продуктов ОКМ (20-22%), но при более высокой температуре (850-900°С) по сравнению с оптимумом для систем, содержащих лантаноиды (750-850°С).
Катализаторы этих же двух групп проявляют высокую активность в процессе окислительного пиролиза алканов С2-С6 (см., например, [L.Leveles, Oxidative conversion of lower alkanes to olefins. PhD Thesis. Universiteit Twente, Enschede, The Netherlands, 2002; С. Boyadjian, L. Lefferts, K. Seshan. Catalytic oxidative cracking of hexane as a route to olefins. Appl. Catal. A. 2010. V.372. P.167-174]).
Одними из наиболее эффективных катализаторов в процессе окислительного пиролиза низших алканов являются нанесенные на Аl2О3, SiO2, TiO2, ZrO2, HfO2, MgO ванадийсодержащие оксиды, лучше - модифицированные добавками сурьмы, а также хрома, никеля и некоторых других элементов. Влияние типа носителя и состава активного компонента на выход продуктов подробно описано в литературе (см., например, Е.А.Mamedov, V.Cortes Corberan, Oxidative dehydrogenation of lower alkanes on vanadium oxide-based catalysts. The present state of the art and outlooks, Appl. Catal. A. 127 (1995) 1-40; V.P.Vislovskiy, V.Yu.Bychkov, M.Yu.Sinev, N.T.Shamilov, P.Ruiz, Z.Schay. Physico-chemical properties of V-Sb-oxide systems and their catalytic behaviour in oxidative dehydrogenation of light paraffins (2000) Catalysis Today, 61 (1-4), pp.325-331).
Все интервалы параметров предложенного способа указаны в предельно допустимых значениях, выбор параметров способа за пределами заявленных интервалов значений не обеспечивает достижения указанного технического результата.
Предложенный способ обеспечивает увеличение степени превращения исходного сырья - углеводородов (алканов) С2-С6 - в целевые продукты - олефины С2-С3 (этилен и пропилен), позволяет снизить энергозатраты на выделение целевых продуктов, а также снизить металлоемкость оборудования на единицу продукции.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЙ СПОСОБ ПРОИЗВОДСТВА ЭТИЛЕНА И ЕГО ПРОИЗВОДНЫХ И ЭЛЕКТРОЭНЕРГИИ ИЗ ПРИРОДНОГО ГАЗА | 2010 |
|
RU2447048C1 |
| КАТАЛИТИЧЕСКИЙ СПОСОБ ПЕРЕРАБОТКИ МЕТАНА | 2008 |
|
RU2394805C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ ЭТИЛЕНА И СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА С ИСПОЛЬЗОВАНИЕМ ЭТОГО КАТАЛИЗАТОРА | 2013 |
|
RU2523013C1 |
| СПОСОБЫ И СИСТЕМЫ ПЕРЕРАБОТКИ ПРИРОДНОГО ГАЗА | 2013 |
|
RU2664802C2 |
| СПОСОБ ОКИСЛИТЕЛЬНОГО ГАЛОГЕНИРОВАНИЯ C УГЛЕВОДОРОДОВ ДО ГАЛОГЕНИРОВАННЫХ C УГЛЕВОДОРОДОВ И СВЯЗАННЫЕ С НИМ ИНТЕГРИРОВАННЫЕ СПОСОБЫ | 2002 |
|
RU2286329C2 |
| КОМПЛЕКСНЫЙ СПОСОБ КАТАЛИТИЧЕСКОЙ ПЕРЕРАБОТКИ ПРИРОДНОГО ГАЗА С ПОЛУЧЕНИЕМ НИЗШИХ ОЛЕФИНОВ | 2011 |
|
RU2451005C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА, КАТАЛИЗАТОР, ПРИГОТОВЛЕННЫЙ ПО ЭТОМУ СПОСОБУ, И СПОСОБ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА С ИСПОЛЬЗОВАНИЕМ ПОЛУЧЕННОГО КАТАЛИЗАТОРА | 2013 |
|
RU2515497C1 |
| Способ переработки нефтезаводских газов | 2017 |
|
RU2688932C1 |
| ИНТЕГРИРОВАННЫЙ СПОСОБ КРЕКИНГА С ПСЕВДОСЖИЖЕННЫМ КАТАЛИЗАТОРОМ И ОКИСЛИТЕЛЬНОГО ДЕГИДРИРОВАНИЯ ПРОПАНА | 2018 |
|
RU2702895C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ С-С | 2015 |
|
RU2570818C1 |
Изобретение относится к способу химической переработки смесей газообразных углеводородов (алканов) С1-С6 в олефины С2-С3 (этилен и пропилен), заключающемуся в осуществлении реакций окислительной конденсации метана и пиролиза алканов С2-С6, характеризующемуся тем, что осуществляют окислительный пиролиз алканов С2-С6, который проводят при температуре от 450°С до 850°С, давлении от 1 атм до 40 атм и подаче не более 15 об.% кислорода в присутствии оксидных катализаторов без предварительного разделения исходной смеси газообразных углеводородов (алканов) C1-С6 на составляющие компоненты и/или отделения метана, реакцию окислительной конденсации метана осуществляют в потоке метана, отделенного от продуктов окислительного пиролиза алканов С2-С6, в присутствии оксидных катализаторов при температуре от 700°С до 950°С, давлении от 1 атм до 10 атм и мольном соотношении метана и кислорода в интервале от 2:1 до 10:1, при этом выделение продуктов окислительной конденсации метана проводят совместно или частично совместно с выделением продуктов окислительного пиролиза алканов С2-С6, а отделенные от реакционных газов метан, этан и алканы С3+ подвергают рециклу и направляют повторно на стадии окислительной конденсации метана и пиролиза алканов С2-С6 соответственно. Предложенный способ обеспечивает увеличение степени конверсии превращения исходного сырья - углеводородов (алканов) С2-С6 - в целевые продукты - олефины С2-С3 (этилен и пропилена), позволяет снизить энергозатраты на выделение целевых продуктов, а также снизить металлоемкость оборудования на единицу продукции. 7 з.п. ф-лы, 2 ил.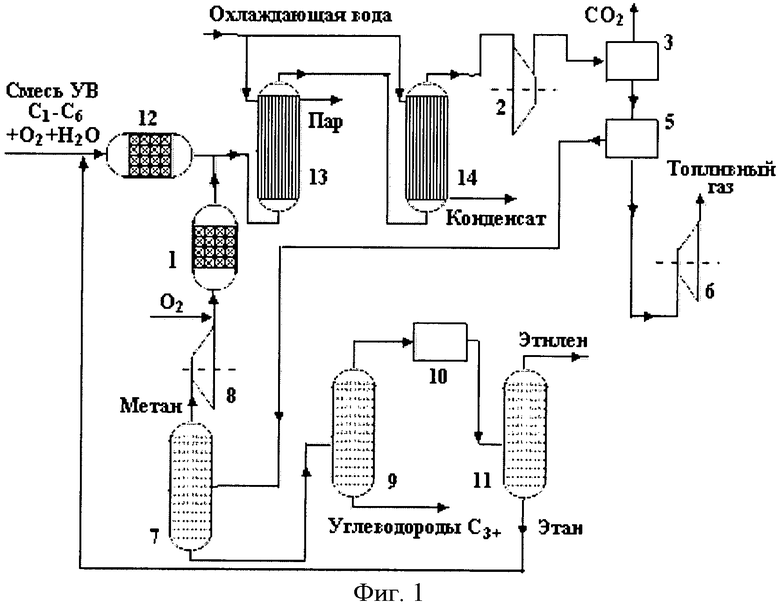
1. Способ химической переработки смесей газообразных углеводородов (алканов) С1-С6 в олефины С2-С3 (этилен и пропилен), заключающийся в осуществлении реакций окислительной конденсации метана и пиролиза алканов С2-С6, отличающийся тем, что осуществляют окислительный пиролиз алканов С2-С6, который проводят при температуре от 450°С до 850°С, давлении от 1 атм. до 40 атм. и подаче не более 15 об.% кислорода в присутствии оксидных катализаторов без предварительного разделения исходной смеси газообразных углеводородов (алканов) С1-С6 на составляющие компоненты и/или отделения метана, реакцию окислительной конденсации метана осуществляют в потоке метана, отделенного от продуктов окислительного пиролиза алканов С2-С6, в присутствии оксидных катализаторов при температуре от 700°С до 950°С, давлении от 1 атм. до 10 атм. и мольном соотношении метана к кислороду в интервале от 2:1 до 10:1, при этом выделение продуктов окислительной конденсации метана проводят совместно или частично совместно с выделением продуктов окислительного пиролиза алканов С2-С6, а отделенные от реакционных газов метан, этан и алканы С3+ подвергают рециклу и направляют повторно на стадии окислительной конденсации метана и пиролиза алканов С3-С6 соответственно.
2. Способ по п.1, отличающийся тем, что оксидный катализатор выбирают из группы: оксиды щелочноземельных элементов Mg, Ca, Sr, Ba, оксиды редкоземельных элементов La, Се, Nd, Sm или их смеси, промотированные добавками щелочных элементов (Li, Na, К, Rb, Cs), Sb, Bi и/или Рb, нанесенными на носители Аl2О3, SiO2, TiO2, ZrO2, НfO2, алюминаты, силикаты щелочноземельных элементов, силикаты редкоземельных элементов.
3. Способ по п.1, отличающийся тем, что состав оксидного катализатора выбирают в соответствии с эмпирической формулой
М1 aМ2 bМ3 2O3+m,
где М1 - щелочноземельный элемент, выбранный из группы Mg, Ca, Sr, Ва (или их комбинация);
М2 - щелочноземельный элемент, выбранный из группы Li, Na, К, Rb, Cs (или их комбинация);
М3 - редкоземельный элемент, выбранный из группы La, Се, Nd, Sm (или их комбинация);
а - грамм-атомный показатель элемента, значение которого выбирают от 0,005 до 250;
b - грамм-атомный показатель элемента, значение которого выбирают от 0 до 20;
m - стехиометрический коэффициент, определяемый соотношением компонентов М1, М2 и М3.
4. Способ по п. 1, отличающийся тем, что состав оксидного катализатора выбирают в соответствии с эмпирической формулой
NaXWYMZSiO2+n,
где М - химический элемент Мn или Се,
X, Y, Z - грамм-атомные соотношения элементов, из которых значение Х выбирают от 0,01 до 0,4; значение Y выбирают от 0,005 до 0,2; значение Z выбирают от 0,005 до 0,4.
5. Способ по п.1, отличающийся тем, что оксидный катализатор окислительного пиролиза алканов C1-С6 выбирают из группы: смешанные оксиды хрома, никеля и/или ванадия и сурьмы, нанесенные на носители Аl2О3, SiO2, TiO2, ZrO2, HfO2, MgO.
6. Способ по п.1, отличающийся тем, что выделение продуктов окислительной конденсации метана осуществляют частично совместно с выделением продуктов окислительного пиролиза алканов С2-С6 при содержании углеводородов (алканов) С2-С6 в исходной смеси выше 15-20% в пересчете на число атомов углерода по отношению к метану.
7. Способ по п.1, отличающийся тем, что выделение продуктов окислительной конденсации метана осуществляют совместно с выделением продуктов окислительного пиролиза алканов С2-С6 при содержании углеводородов (алканов) С2-С6 в исходной смеси ниже 10-15% в пересчете на число атомов углерода по отношению к метану.
8. Способ по п.1, отличающийся тем, что разделение части продуктов окислительной конденсации метана - фракции углеводородов С2+ - осуществляют совместно с выделением продуктов окислительного пиролиза исходной смеси углеводородов C1-С6, при содержании углеводородов (алканов) С2-С6 в исходной смеси выше 10-15% в пересчете на число атомов углерода по отношению к метану.
| US 5118898 А, 02.06.1992 | |||
| ИНТЕГРИРОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ, В ЧАСТНОСТИ ЭТИЛЕНА И ПРОПИЛЕНА, ИЗ МЕТАНСОДЕРЖАЩИХ ГАЗОВЫХ СМЕСЕЙ | 1993 |
|
RU2100334C1 |
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДОВ C - C | 1998 |
|
RU2134675C1 |
| US 5113032 A, 12.05.1992. | |||
Авторы
Даты
2011-12-10—Публикация
2010-05-17—Подача