Изобретение относится к медицине, а именно к реконструктивно-восстановительной хирургии, торакальной хирургии и онкологии, и может найти применение при замещении пострезекционных грудинно-реберных дефектов у пациентов с первичными и вторичными злокачественными новообразованиями и опухолеподобными заболеваниями грудной стенки, а также с раневыми дефектами травматического, инфекционно-воспалительного и радиационного генеза, врожденными и приобретенными деформациями, требующими одномоментной или отсроченной реконструкции каркаса грудной клетки.
Резекционный этап оперативных вмешательств при такой патологии предполагает удаление пораженных опухолью, гнойно-воспалительным процессом или деформированных мягкотканых и костных структур грудной стенки. В результате закономерно формируется пострезекционный или раневой дефект грудной стенки, который требует для нормального жизнеобеспечения одномоментной или отсроченной реконструкции с сохранением анатомо-физиологического объема грудной полости, при этом немаловажна и эстетическая оставляющая (Резекция грудной стенки при новообразованиях с реконструкцией никелид-титановыми имплантами / Е. Б. Топольницкий, Н. А. Шефер, Е. С. Марченко [и др.] // Онкология. Журнал им. П.А. Герцена. – 2021. – Т. 10, № 2. – С. 22-28. – DOI 10.17116/onkolog20211002122).
Мировые тренды реконструктивной хирургии грудной стенки указывают на приоритетный выбор в пользу применения несвободных кожно-жировых и кожно-мышечных лоскутов для пластического замещения мягкотканого дефекта, в том числе в самых изысканных и оригинальных вариантах их перемещения (Реконструкция пострезекционных дефектов грудной стенки при хирургическом лечении больных инвазивным немелкоклеточным раком легкого / Е. Б. Топольницкий, Н. А. Шефер, Е. С. Марченко [и др.] // Хирургия. Журнал им. Н.И. Пирогова. – 2022. – № 12. – С. 31-40. – DOI 10.17116/hirurgia202212131; Медведчиков-Ардия, М. А. Современные возможности пластики грудной стенки с помощью большой грудной мышцы / М. А. Медведчиков-Ардия, Е. А. Корымасов, А. С. Бенян // Наука и инновации в медицине. – 2024. – Т. 9, № 2. – С. 154-160. – DOI 10.35693/SMI568135). Вопрос выбора пластического материала и оптимальной методики замещения дефектов каркаса грудной клетки остается дискуссионным. В большинстве случаев для восстановления реберно-грудинного остова после резекции грудной стенки используют сетчатые и/или монолитные имплантаты из различных материалов. В публикациях последних лет упоминается об использовании в клинической практике для этих целей в качестве армирующего материала полипропилена, политетрафторэтилена (Gore-tex), титана, системы Stratos или Synthes Matrix Rib, а также их комбинации (Новый метод закрытия дефектов грудной стенки / Г. Ц. Дамбаев, В. Э. Гюнтер, С. Г. Филиппов [и др.] // Бюллетень сибирской медицины. – 2002. – Т. 1, № 1. – С. 107-109; Соболевский В.А., Диков Ю.Ю. Первый опыт использования реконструктивной системы STRATOS и пластины Gore-Tex Dual-Mesh для замещения субтотального дефекта грудины. Саркомы костей, мягких тканей и опухоли кожи. 2013;1:81-84).
Также широко анонсируется возможность замещения пострезекционных дефектов, в том числе костно-хрящевого каркаса грудной стенки, протезами, созданными при помощи устройств трехмерной печати с учетом индивидуальных особенностей строения тела пациента (Курильчик А.А., Иванов В.Е., Стародубцев А.Л. и др. Варианты хирургического лечения онкологических больных с использованием 3D-имплантатов. 2022;14(3):11–9. DOI: 10.17650/2219-4614-2022-14-3-11-19).
Известно устройство (Патент US 7033377, опубл. 2006-04-25 A61B17/82), которое позиционируют вокруг реберной хрящевой части каждого из парного набора ребер, расположенных на противоположных сторонах резецированной грудины, одновременно окружая переднюю и заднюю части грудины, содержащее соединенные элементы крепления направляющих для введения, каждый из которых имеет первую и вторую концевые части, первую и вторую боковые части, корпусную часть, переднюю и заднюю поверхности, две части ног в форме полумесяца со смещенными под углом частями, множество поверхностей зацепления с грудиной, ребром и реберным хрящом и поворотный стопорный элемент, шарнирно прикрепленный к направляющему элементу для введения, дополнительно содержащий захватывающий механизм, имеющий смещенные под углом зубчатые структуры на первой стороне, взаимодействующие с возвратно-поступательными зубчатыми структурами, интегрированными на первой стороне вставного элемента, для позиционирования, фиксации на месте и функционального объединения вставного элемента, поворотного фиксатора и направляющей для вставки.
Недостатком известного устройства является высокий риск прорезывания проволочных фиксаторов с последующим смещением устройства, травматичность, неудовлетворительные эстетические и функциональные результаты, узкая область применения при дефектах грудины, отсутствие конгруэнтности с дефектом за счет выбора метода изготовления конструкций и риск его разрушения при повышенных циклических нагрузках при дыхании.
Известен индивидуальный 3-D имплант для замены пораженного опухолью участка грудины в размере от ярёмной вырезки до промежутка между вторым и третьим реберными вырезками тела грудины, выполненный путем послойного сплавления металлического порошка на основе результатов компьютерной томографии грудной стенки и с помощью полученных сканов (Патент 2760620, опубл. 29.11.21г., A61F 2/28). Имплант выполнен в виде перфорированного объёмного тела в виде «краба» со связанными внутренними полостями, имеющее с каждой стороны по два реберных отростка, снабженные «клещевидными» соединениями, имеющими нижнюю часть, слитную с телом, а верхнюю – подвижную, прикрепленную к нижней посредством соединения «ухо-вилка». Верхняя и нижняя части выполнены со сквозными отверстиями для проведения проволоки. Тело в виде «краба» с внутренней и наружной стороны имеет шероховатую поверхность, а его реберные отростки имеют шероховатую поверхность только с внутренней стороны.
Недостатком импланта и описанной методики его применения является недостаточная биомеханическая совместимость с высокоподвижными структурами грудной клетки, высокий риск прорезывания фиксирующей проволоки с фрагментацией костных структур и смещением устройства, ограниченность области применения при дефектах только верхней трети грудины. При хирургическом лечении онкологических заболеваний с применением индивидуальных 3-D имплантов с виртуальными размерами, изготовленных перед операцией на основе компьютерных томограмм, существует высокая вероятность их несоответствия фактическим размерам пострезекционного дефекта во время операции. Это снижает эффективность онкологического лечения, ограничивая возможности хирурга в объеме резекции тканей, или является поводом отказа в проведении оперативного вмешательства, а при недостаточном отступе от опухоли снижает радикальность лечения.
Известно изобретение применимое для пластики обширных пострезекционных окончатых дефектов стенок грудной клетки (Патент РФ 2393808, опубл. 10.07.10г., A61B17/56). Накладывают на образованный пострезекционный дефект лоскут никелид-титановой ткани и фиксируют к краям дефекта. Укладывают поверх и поперек лоскута никелид-титановой ткани, по крайней мере, один ленточный, анатомически сформованный никелид-титановый элемент жесткости, опирают его концами на костные структуры краев пострезекционного окончатого дефекта и фиксируют к лоскуту никелид-титановой ткани. Используемое в способе устройство (модуль сборки) выполнен из сплава никелида титана в виде, имитирующем естественное ребро. Набор таких модулей устанавливают на место резецированного участка грудной клетки с опорой концов каждого модуля на маргинальные остатки костных структур (например, грудины и культей ребер). Устройство имеет ряд недостатков, снижающих постоперационный ресурс состоятельности лечения.
1. Пластинчатая форма модуля разрешает однонаправленную, нормально к плоскости пластины, деформацию, в отличие от двунаправленной (по нормали и касательной) - естественного ребра. Отличие приводит к ригидности грудной клетки с ограничением дыхательной экскурсии и снижением жизненной емкости легких.
2. Опорное, без спецификации, соединение имплантата с костной тканью приводит в дыхательной динамике к взаимному перемещению, конфликтному трению в месте контакта, травматизации кости и ослаблению связи искусственной стенки с грудной клеткой. Эти недостатки снижают ресурс состоятельности и стимулируют совершенствование техники лечения.
Известна полезная модель, которая относится к медицине и может быть использована в ортопедии, онкологии, нейрохирургии, травматологии и ветеринарии (Патент РФ 213359, опубл. 07.09.2022, A61B17/68). Устройство предназначено для реконструктивной пластики различных дефектов каркаса, включая грудную стенку и кости таза, производимых при онкологических операциях, преимущественно для замещения резецированного участка. Модуль для реконструкции пострезекционных каркасных дефектов грудной клетки и костей таза из сверхэластичного и износостойкого материала представляет собой каркас в виде плоской регулярной, однонаправленно транслированной проволочной структуры из последовательности петлеобразных изгибов и дополнительно содержит внешний чехол-оплетку, выполненный в виде сетчатого кругового полотна, внутри которого расположена проволочная структура каркаса. На сетчатый чехол-оплетку модуля нанесено покрытие, содержащее регенерирующие средства.
Недостатком известной полезной модели является высокий риск развития локального инфекционного процесса (парапротезной инфекции) в области операции, что является показанием к удалению имплантата, но это не всегда выполнимо, а при прогрессировании воспаления может закончиться общей интоксикацией с развитием сепсиса. В условиях парапротезной инфекции внешний чехол-оплетка, выполненный в виде сетчатого кругового полотна, будет являться депо для инфекции и не оставляет шансов на санацию очага воспаления при наличии имплантата.
Наиболее близким по технической сущности и принятым за прототип является изобретение (Патент РФ 2694213, опубл. 09.07.2019г., A61B17/56), где модуль для каркасной реконструкции грудной клетки выполнен из сверхэластичного никелида титана в виде плоской регулярной, однонаправленно транслированной проволочной структуры из последовательности петлеобразных изгибов, расположенных относительно оси трансляции. Изобретение обеспечивает повышение состоятельности операции и увеличение срока функционирования.
Недостатком известного изобретения является риск миграции модуля при несостоятельности в точках c жесткой резьбовинтовой фиксацией имплантата к грудине и в целом из описания изобретения не понятно, как осуществляется скрепление модулей между собой и фиксация к окружающим тканям. Формулировка достаточно расплывчатая и это при том, что от порядка указанного действия зависит безопасность и эффективность хирургического лечения. Таким образом, из описания формулы порядок логических действий не вытекает естественным образом, что делает способ не всегда выполнимым на уровне пользователя. Также имплант не обладает антибактериальными свойствами и поэтому имеется высокий риск развития парапротезной инфекции в области операции. Более того, как и у большинства имплантов, его применение противопоказано в инфицированные ткани, что присутствует всегда в случае распадающихся злокачественных опухолей и при раневых дефектах инфекционно-воспалительного генеза.
Технический результат предлагаемого изобретения - повышение безопасности и эффективности восстановления костно-хрящевого каркаса грудной стенки, снижение технической сложности исполнения хирургических действий за счет стандартизации этапов установки и фиксации каркасных конструкций, улучшения интеграционных и антибактериальный свойств имплантата, повышение прочности материала и устойчивость к парапротезной инфекции.
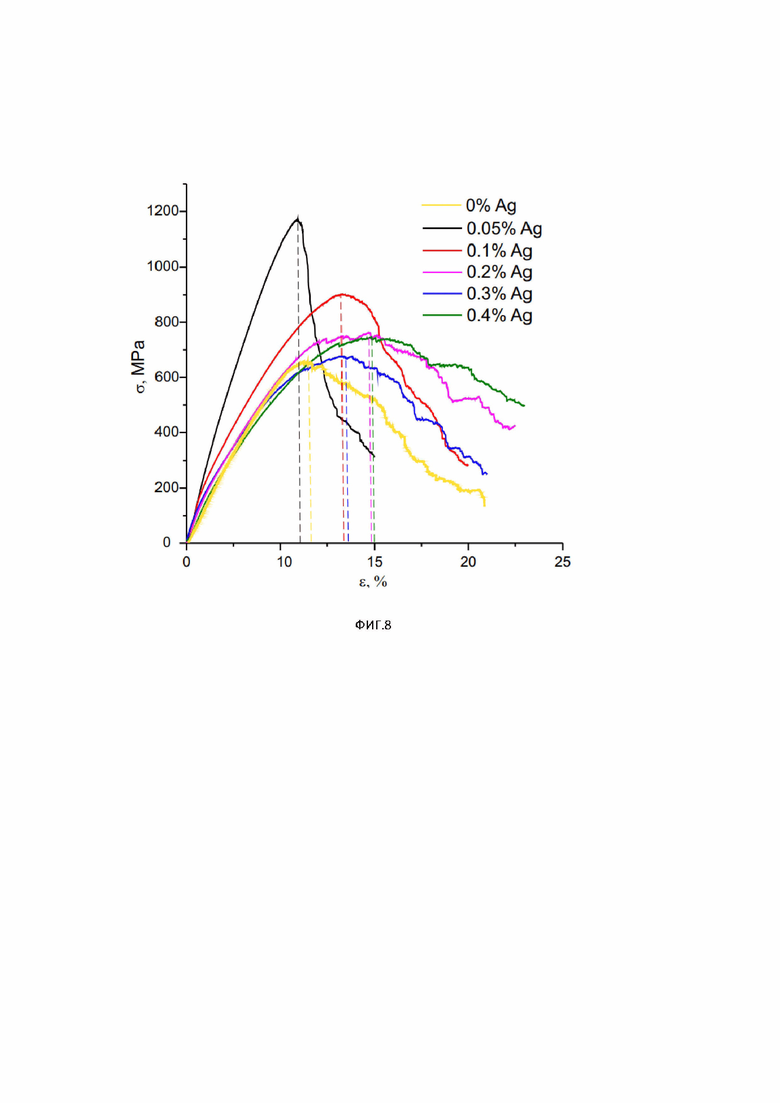
Указанный технический результат достигается добавок наночастиц серебра с концентрацией до 0,1 %, что приводит к кристаллизации наночастиц Ag в поверхностных слоях сплава размером 2±60 нм и выходу атомов Ag на поверхность, обеспечивая антибактериальный эффект и более быструю приживаемость, а также к растворению серебра в структуре В2 TiNi и как следствие к твердорастворному упрочнению и повышению прочности сплава с 620±3 МПа до 1180±3 МПа.
Указанный технический результат достигается тем, что заявлено устройство для замещения пострезекционных грудинно-реберных дефектов у пациентов при реконструкции каркаса грудной клетки, выполненное из сверхэластичного сплава, выполненное в виде повторяющихся модулей в виде проволочных структур, представляющих собой последовательно расположенные петлеобразные сегменты с толщиной проволочной структуры 1,7±0,1 мм, высотой сегмента 50 мм, шириной сегмента 30 мм, с возможностью соединения проволочных структур между собой посредством зажима, при этом сверхэластичный сплав, выполнен методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %:
никель 49,5-49,6;
наночастицы серебра 0,05-0,1;
титан –остальное.
Сегменты выполнены однопетельными или двухпетельными.
Зажим для соединения проволочных структур представляет собой двойной хомут выполненный из пластины никелида титана шириной 2,0± 0,5мм.
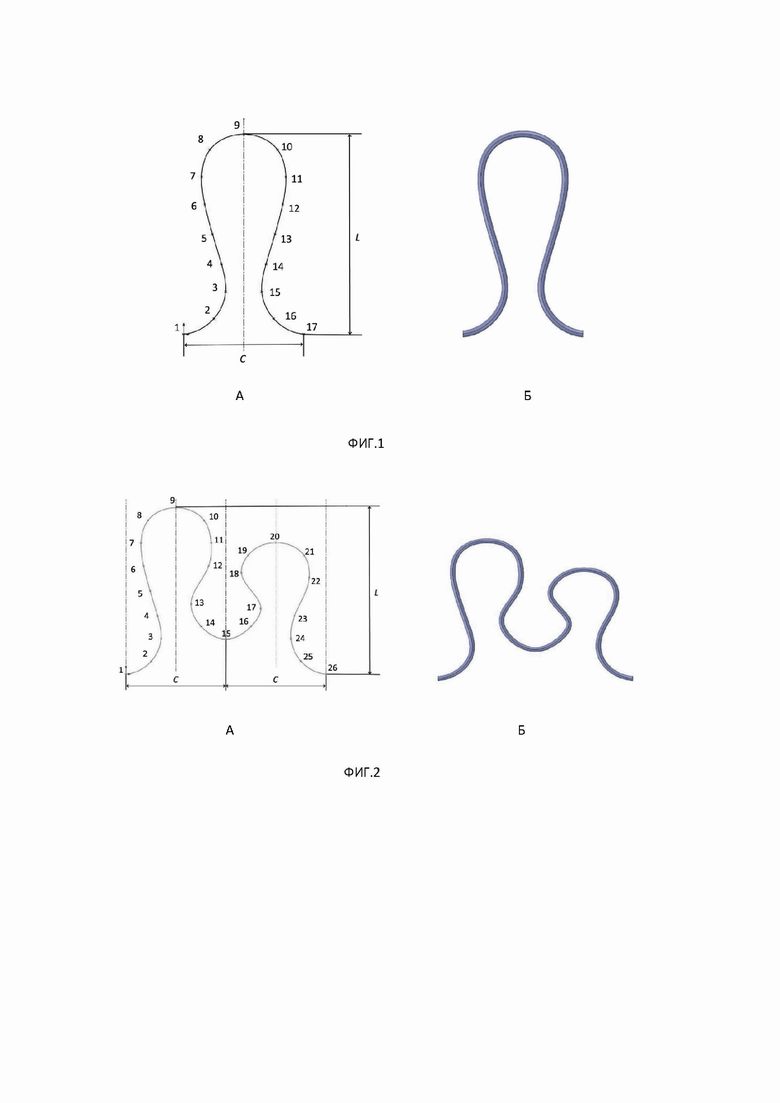
Петлеобразный сегмент (Фиг. 1 и 2), характеризуется структурными параметрами C и L, где C -ширина, L -высота сегмента. Петлеобразный сегмент – это изгибающаяся пространственная кривая, являющаяся образующей петли, вдоль которой экструдируется окружность диаметром D, совпадающим с диаметром используемой проволоки. Схемы образующих, представлены на (Фиг. 1а и 2а, на фиг. 1б и 2б представлены трехмерные изображения самих сегментов).
Этапу изготовления устройства каркаса грудной стенки предшествует этап проектирования, в этот момент планируются основные параметры изделия из чего закладывается конечная форма сегментов, моделей и каркаса.
При проектировании индивидуального устройства каркаса грудной стенки возможны вариации структурных параметров C, L и D. Образующая строится протягиванием сплайна на плоскости через ключевые точки. Ключевые точки распределены на плоскости по координатам в соответствии с установленными соотношениями со структурными параметрами, указанными в таблицах 1 и 2. Изделия, представленные на фигурах, имеют значения структурных параметров равные C = 30 мм, L= 50 мм и D=1,7 мм. В случае сегмента, представленного одиночной петлей (Фиг. 1), количество ключевых точек равно 17 (таблица 1). Петля симметрична относительно своей вертикальной оси, а при соединении сегментов последовательно образуется попеременная симметрия относительно продольной горизонтальной оси со смещением на ширину петли. В основе сегмента, представленного двойной петлей (Фиг. 2), лежит модифицированный метод изготовления одиночного петлеобразного сегмента путем соединения двух последовательно размещенных одиночных сегментов из промежуточной петлей обратной выпуклости. Характерный структурный параметр L соответствует высоте одного из образующих одиночных сегментов. Расстояние между вертикальными осями образующих сегментов равно C, а ширина сформированного ими нового сегмента равна 2C. Количество ключевых точек во этом случае составляет 26 (таблица 2). Промежуточная петля расположена симметрично малой петле сегмента относительно его горизонтальной оси на равноудаленном расстоянии между вертикальными осями промежуточной петли и образующих сегментов равном C/2. Каркас из модулей, сформированный сегментами в виде двойной петли (Фиг. 4Б), обладает дополнительной поперечной жесткостью вдоль вертикальной оси, по сравнению с каркасом (Фиг. 4А), сформированным модулями из сегментов в виде одиночной петли, обладающим только продольной жесткостью вдоль горизонтальной оси. Поперечная жесткость каркаса (Фиг. 4Б) формируется за счет соединения петель в рядах на двух разных уровнях. Выбор каркаса осуществляется лечащим врачом исходя из индивидуальных показателей операции.
Зажим для соединения проволочных структур представляет собой двойной хомут выполненный из пластины никелида титана шириной 2,0± 0,5мм.
Соединение модулей в каркас при формировании устройства каркаса грудной стенки проходит непосредственно во время операции по месту установки изделия путем использования специальных зажимов. Зажим (фиг. 5) для соединения проволочных структур представляет собой двойной хомут, выполненный из того же материала, что и проволока разработанного изделия – сверхэластичный никелид титана. В начальном состоянии хомут разогнут, во время установки две соединяющийся проволоки вставляются в разогнутые лапки зажима, после чего лапки смыкаются специальным ручным инструментом. Зажим устанавливается в места соприкосновения рядов друг с другом в крайних точках выпуклостей сегментов.
Достижимость технического результата обусловлена комплексным действием физико-механических свойств устройства, следующих из признаков формулы изобретения.
Использование сверхэластичного сплава на основе никелида титана с выраженным антибактериальным действием для заявленного устройства позволяет отвечать требованиям решения указанной задачи. Из обширного перечня таковых основными являются:
1. Биосовместимость. Она проявляется в быстрой и успешной интеграции имплантата как инородного тела с тканями грудной клетки. Бескапсулярный, бесконфликтный контакт инородного тела с живой тканью - главный признак биосовместимости никелида титана и залог согласованного функционирования получившейся композиции в акциях деформации стенки грудной клетки.
2. Механическая и циклическая прочность. Сплав никелида титана достаточно прочен даже для замещения экстремально нагруженных тканей организма. Циклостойкость за счет сверхэластичности (деформация без разрушения при нагрузке и разгрузке при удлинении до 10%) превосходит все известные металлические материалы медицинского назначения. Изготовленная из никелида титана проволока выдерживает без разрушения много миллионов циклов знакопеременной деформации. Это свойство существенно важно с учетом непрерывной дыхательной подвижности грудной клетки.
3. Коррозионная стойкость. Никелид титана в организме не корродирует и не резорбируется. Срок его целостного нахождения в тканях не ограничен. По этой причине нет необходимости удалять имплантат после реконвалесценции и, тем самым, дополнительно травмировать больного.
4. Наличие в структуре материала наночастиц серебра придает каркасу выраженные антибактериальные свойства к большинству патогенных бактерий. Полученные материалы на основе наночастиц серебра рассматриваются в качестве альтернативных агентов для преодоления антибиотикоустойчивости и представляют собой эффективную альтернативу применяемым в настоящее время антибактериальным препаратам. Малые концентрации серебра не будут оказывать токсический эффект от избытка и накопления в прилежащих тканях.
5. Каркас легок и податлив в формообразовании, формируется по длине и набору модулей во время операции персонально, т.е. адекватно образованному окончатому костно-хрящевому дефекту грудной стенки.
В качестве примера приводим клинические наблюдения:
Пример 1: Пациент Е., 37 лет поступил в хирургическое торакальное отделение ТОКБ с жалобами на повторяющиеся кровотечения из распадающегося гигантского новообразования передней поверхности грудной стенки. При комплексном обследовании установлен диагноз: Плеоморфная рабдомиосаркома мягких тканей грудной клетки с распространением на средостение, верхнюю и среднюю доли правого легкого T4G2-3N0M0, IIIB ст., осложненная распадом опухоли и вторичным нагноением, рецидивирующим аррозивным кровотечением. Мультидисциплинарным врачебным консилиумом выставлены абсолютные показания для проведения первоначально хирургического этапа в составе комбинированного противоопухолевого лечения. Под общей анестезией выполнена полнослойная комбинированно-расширенная резекция грудной стенки с резекцией правой большой грудной мышцы, костно-хрящевой части с 3 по 8 ребра справа, хрящевой части с 3 по 7 ребра слева, субтотальной резекцией грудины с мечевидным отростком, билатеральной резекцией медиастинальной плевры и удалением жировой клетчатки переднего средостения, атипичной резекцией верхней и средней долей правого легкого, грудинной части диафрагмы, краниальной части прямых мышц живота с апоневрозом передней брюшной стенки. Выполнена комбинированная реконструкция обширного полнослойного пострезекционного дефекта грудной стенки. Замещение костно-хрящевого дефекта выполнено 6 конгруэнтными к области дефекта по нормальной анатомической форме грудной стенки армирующими имплантами, в качестве которых использовалось заявляемое устройство, представленное на Фиг.4A с зажимами из пластины никелида титана шириной 2,0± 0,5мм, при этом проволочная структура представляет собой сверхэластичный сплав, полученный методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %:
никель 49,5,
наночастицы серебра 0,1,
титан – остальное.
Замещение мягкотканого дефекта встречными перемещенными несвободными билатеральными кожно-фасциальными лоскутами, слева кожно-мышечным лоскутом на основе большой грудной мышцы. Дренирование переднего средостения и билатерально подлоскутных пространств боковой поверхности грудной стенки. Послойно швы на операционные раны. Асептическая повязка. Больной экстубирован через 30 минут после окончания операции на операционном столе. Дыхание адекватное, нормальная сатурация. В раннем и отдаленном послеоперационном периоде признаков миграции или патологический подвижности конструкций не отмечено.
Пример 2: Пациент Р., 49 лет поступила в хирургическое торакальное отделение ТОКБ с диагнозом Одиночный метастаз в левую половину грудной стенки на уровне 6 межреберья аденокистозного рака вилочковой железы. В анамнезе комбинированное лечение: видеоасситированная комбинированно-расширенная тимэктомия, радикальный курс химиолучевой терапии. Прогрессирование. Состояние после трансстернальной экстирпации остаточной злокачественной опухоли переднего средостения с окончатой резекцией перикарда, левой медиастинальной плевры, левого диафрагмального нерва, левой внутренней грудной вены, атипичной резекцией верхней доли левого легкого. Прогрессирование 06.2024 г. МТС в грудную стенку слева. Мультидисциплинарным врачебным консилиумом выставлены абсолютные показания для проведения первоначально хирургического этапа в составе комбинированного противоопухолевого лечения. Выполнена в едином блоке резекция грудной стенки с резекцией боковых отрезков 6, 7 ребер слева, медиастинальной плевры диафрагмы и одномоментным восстановлением 2 конгруэнтными к области дефекта по нормальной анатомической форме грудной стенки армирующими имплантами в качестве которых использовалось заявляемое устройство, представленным на Фиг.4A с зажимами из пластины никелида титана шириной 2,0± 0,5мм, при этом проволочная структура представляет собой сверхэластичный сплав, полученный методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %:
никель 49,6,
наночастицы серебра 0,05,
титан – остальное.
Дренирование плевральной полости, швы на операционную рану. Больной экстубирован на операционном столе. Дыхание адекватное, нормальная сатурация. В раннем и отдаленном послеоперационном периоде признаков миграции или патологический подвижности конструкций не отмечено.
Пример 3: Пациент П., 69 лет поступила в хирургическое торакальное отделение ТОКБ с диагнозом Рак нижней доли левого легкого с инвазией боковые отрезки 8, 9 ребер слева, T4N0M0, IIIА ст., плоскоклеточный вариант, осложненный параканкрозной пневмонией с абсцедированием. По рекомендации мультидисциплинарного врачебного консилиума после комплексной предоперационной подготовки выполнена расширенная комбинированная нижняя лобэктомия левого легкого с резекцией язычковых сегментов верхней доле левого легкого, боковых отрезков 8, 9 ребер слева, с одномоментным восстановлением костно-хрящевого каркаса 3 конгруэнтными к области дефекта по нормальной анатомической форме грудной стенки армирующими имплантами, в качестве которых использовалось заявляемое устройство, представленное на Фиг.4Б с зажимами из пластины никелида титана шириной 2,0± 0,5мм, при этом проволочная структура представляет собой сверхэластичный сплав, полученный методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %:
никель 49,6,
наночастицы серебра 0,05,
титан – остальное.
Дренирование левой плевральной полости. Восстановление целостности мягких тканей. Больной экстубирован на операционном столе. Дыхание адекватное, нормальная сатурация. В раннем и отдаленном послеоперационном периоде признаков миграции или патологический подвижности конструкций не отмечено.
Пример 4: Пациент П., 56 лет поступила в хирургическое торакальное отделение ТОКБ с диагнозом Рак нижней доли правого легкого с инвазией боковые отрезки 7, 8 ребер справа, T3N1M0, IIIА ст., осложненный параканкрозной пневмонией с абсцедированием. Гистология: высокодифференная аденокарцинома легкого. По рекомендации мультидисциплинарного врачебного консилиума выполнена расширенная комбинированная нижняя лобэктомия правого легкого с резекцией боковых отрезков 7, 8 ребер справа, с одномоментным восстановлением костно-хрящевого каркаса 2 конгруэнтными к области дефекта по нормальной анатомической форме грудной стенки армирующими имплантами, в качестве которых использовалось заявляемое устройство, представленное на Фиг.4Б с зажимами из пластины никелида титана шириной 2,0± 0,5мм, при этом проволочная структура представляет собой сверхэластичный сплав, полученный методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %:
никель 49,6,
наночастицы серебра 0,05,
титан – остальное.
Дренирование левой плевральной полости. Восстановление целостности мягких тканей. Больной экстубирован на операционном столе. Дыхание адекватное, нормальная сатурация. В раннем и отдаленном послеоперационном периоде признаков миграции или патологический подвижности конструкций не отмечено.
На иллюстрациях представлено:
Фиг. 1. А-схема образующей и Б-трехмерная модель петли при значениях структурных параметров: C=30мм, L=50 мм.
Фиг. 2. А-схема образующей и Б- трехмерная модель двухпетельного сегмента при значениях структурных параметров: C=30мм, L=50 мм.
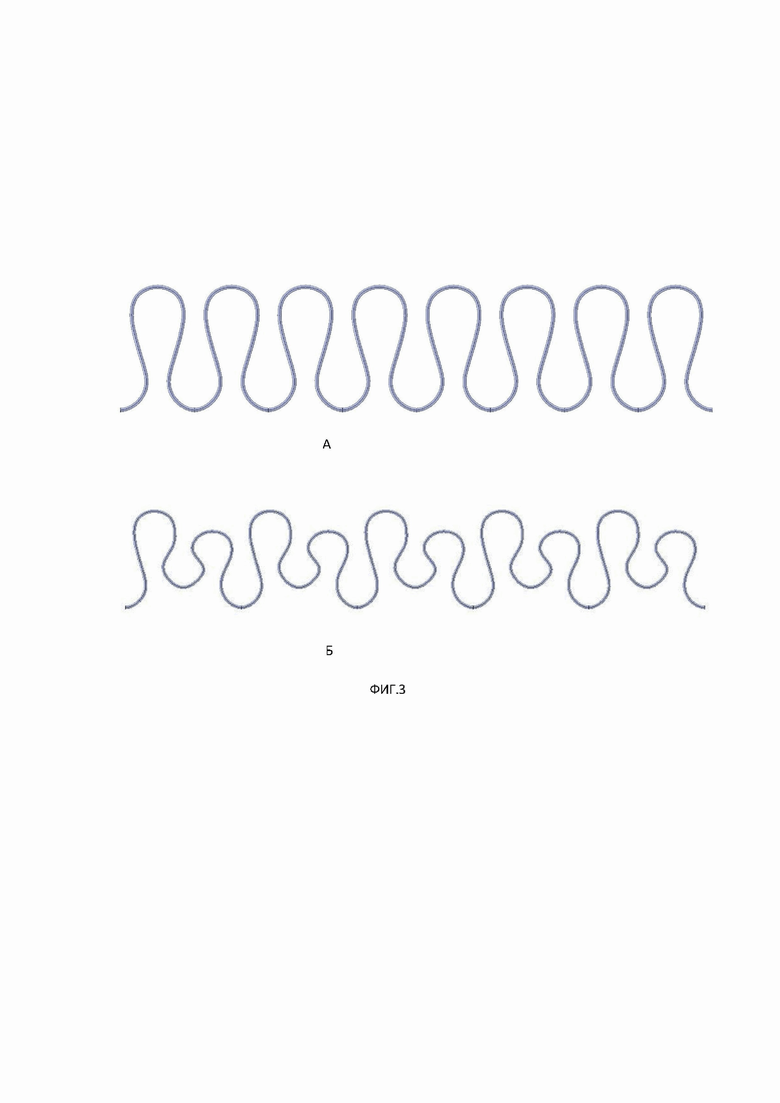
Фиг. 3. Внешний вид модуля для реконструкции стенки грудной клетки (А-модуль из одиночных петлеобразных сегментов, Б- модуль из двухпетельных петлеобразных сегментов) при значениях структурных параметров петлеобразного сегмента: C=30мм, L=50 мм.
Фиг 4. Внешний вид каркаса, состоящий из нескольких модулей для реконструкции стенки грудной клетки (А-модули из одиночных петлеобразных сегментов, Б- модули из двухпетельных петлеобразных сегментов) при значениях структурных параметров двояковыпуклого сегмента: C=30мм, L=50 мм
Фиг 5. Элемент крепления при использовании в устройстве (А-общий вид, Б-использование в устройстве)
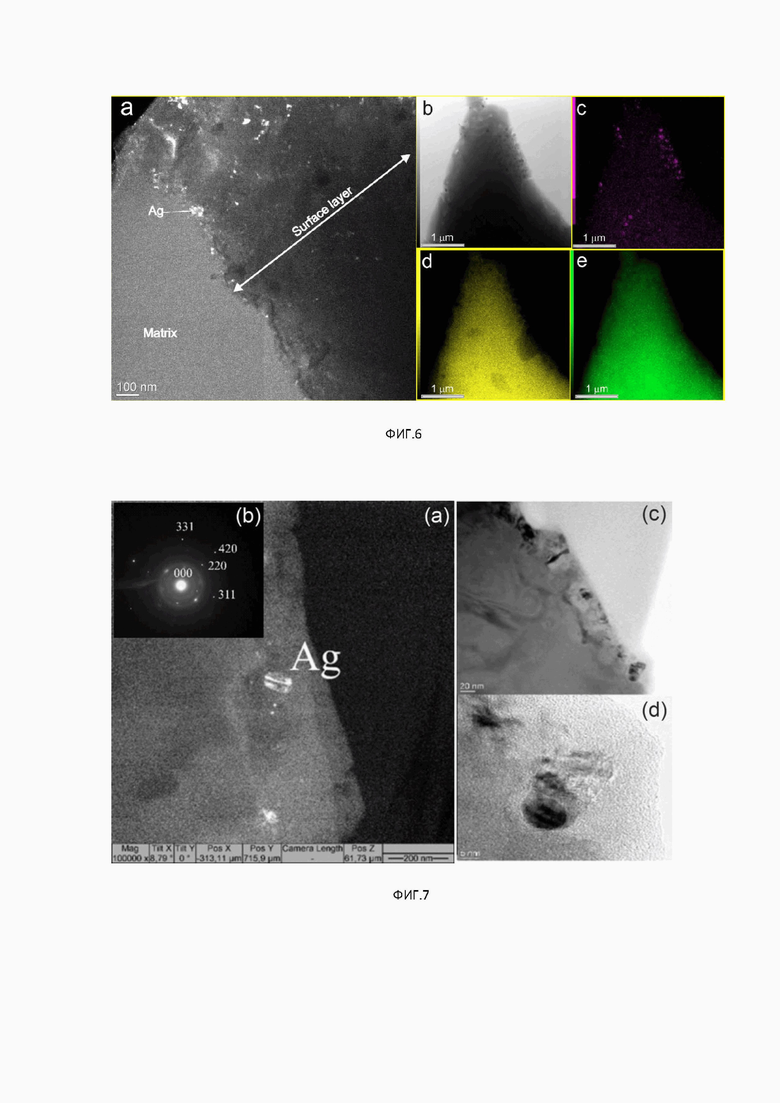
Фиг. 6. Распределение Ag в образце TiNi+0.05%Ag: TEM изображение и электронная микродифракция Ag (a); STEM–EDS элементное картирование (b, c, d, e), размер наночастиц серебра 2±20 нм.
Фиг. 7. Распределение Ag в образце TiNi 0.1 %Ag: TEM изображения и электронная микродифракция от наночастицы Ag, размер наночастиц серебра 5±60 нм.
Фиг. 8. Деформационные диаграммы до разрушения сплавов TiNi с разной концентрации серебра при квазистатическом растяжении.
В таблице 1 приведено соотношение между ключевыми точками образующей и структурными параметрами одиночного сегмента.
В таблице 2 приведено соотношение между ключевыми точками образующей и структурными параметрами двояковыпуклого сегмента.
Совокупность признаков, приводящих к достигаемому техническому результату, является новой, неизвестной из уровня техники и не вытекает явным образом из доступных для специалиста сведений, поскольку для медицины неприемлемы умозрительные выводы о результативности тех или иных приемов без экспериментального обоснования, что и было проделано. Данный способ прошел клинические испытания. Таким образом, он соответствует критериям изобретения: “новизна”, “изобретательский уровень”, “промышленная применимость”.
Таблица 1
Точки
Таблица 2
точки
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТА ГРУДНОЙ СТЕНКИ ИНДИВИДУАЛЬНЫМ 3D-ИМПЛАНТОМ | 2021 |
|
RU2760620C2 |
| МОДУЛЬ ДЛЯ КАРКАСНОЙ РЕКОНСТРУКЦИИ ГРУДНОЙ КЛЕТКИ | 2018 |
|
RU2694213C1 |
| Способ замещения дефекта грудной стенки индивидуальным 3D-имплантатом для замещения грудины | 2024 |
|
RU2836577C2 |
| СПОСОБ ПЛАСТИКИ ОБШИРНЫХ ПОСТРЕЗЕКЦИОННЫХ ОКОНЧАТЫХ ДЕФЕКТОВ СТЕНОК ГРУДНОЙ КЛЕТКИ И/ИЛИ СВОДА ЧЕРЕПА | 2009 |
|
RU2393808C1 |
| Способ хирургической реконструкции передней грудной стенки после обширной резекции грудины комбинированным имплантом, изготовленным путём дублирования трёхмерной стереолитографической модели | 2021 |
|
RU2770560C1 |
| Способ пластического замещения пострезекционных хрящевых дефектов на трахеогортанном сегменте | 2023 |
|
RU2801771C1 |
| Способ двухэтапной хирургической коррекции обширного трахеогортанного дефекта в сочетании с трахеомаляцией в грудном отделе трахеи | 2023 |
|
RU2816082C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ВОРОНКООБРАЗНОЙ ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ У ДЕТЕЙ | 2012 |
|
RU2480170C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ГОРТАНИ | 2011 |
|
RU2475194C1 |
| СПОСОБ УКРЫТИЯ ОБШИРНЫХ ОКОНЧАТЫХ ТОРАКОАБДОМИНАЛЬНЫХ ДЕФЕКТОВ | 2015 |
|
RU2600849C1 |


Изобретение относится к медицине. Устройство для замещении пострезекционных грудинно-реберных дефектов у пациентов при реконструкции каркаса грудной клетки выполнено из сверхэластичного сплава в виде повторяющихся модулей в виде проволочных структур, представляющих собой последовательно расположенные петлеобразные сегменты с толщиной проволочной структуры 1,7±0,1 мм, высотой сегмента 50 мм, шириной сегмента 30 мм, с возможностью соединения проволочных структур между собой посредством зажима. Сверхэластичный сплав, выполнен методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %: никель 49,5-49,6; наночастицы серебра 0,05-0,1; титан –остальное. Изобретение обеспечивает повышение безопасности и эффективности восстановления костно-хрящевого каркаса грудной стенки, снижение технической сложности исполнения хирургических действий за счет стандартизации этапов установки и фиксации каркасных конструкций, улучшения интеграционных и антибактериальный свойств имплантата, повышение прочности материала и устойчивость к парапротезной инфекции. 2 з.п. ф-лы, 8 ил., 2 табл., 4 пр.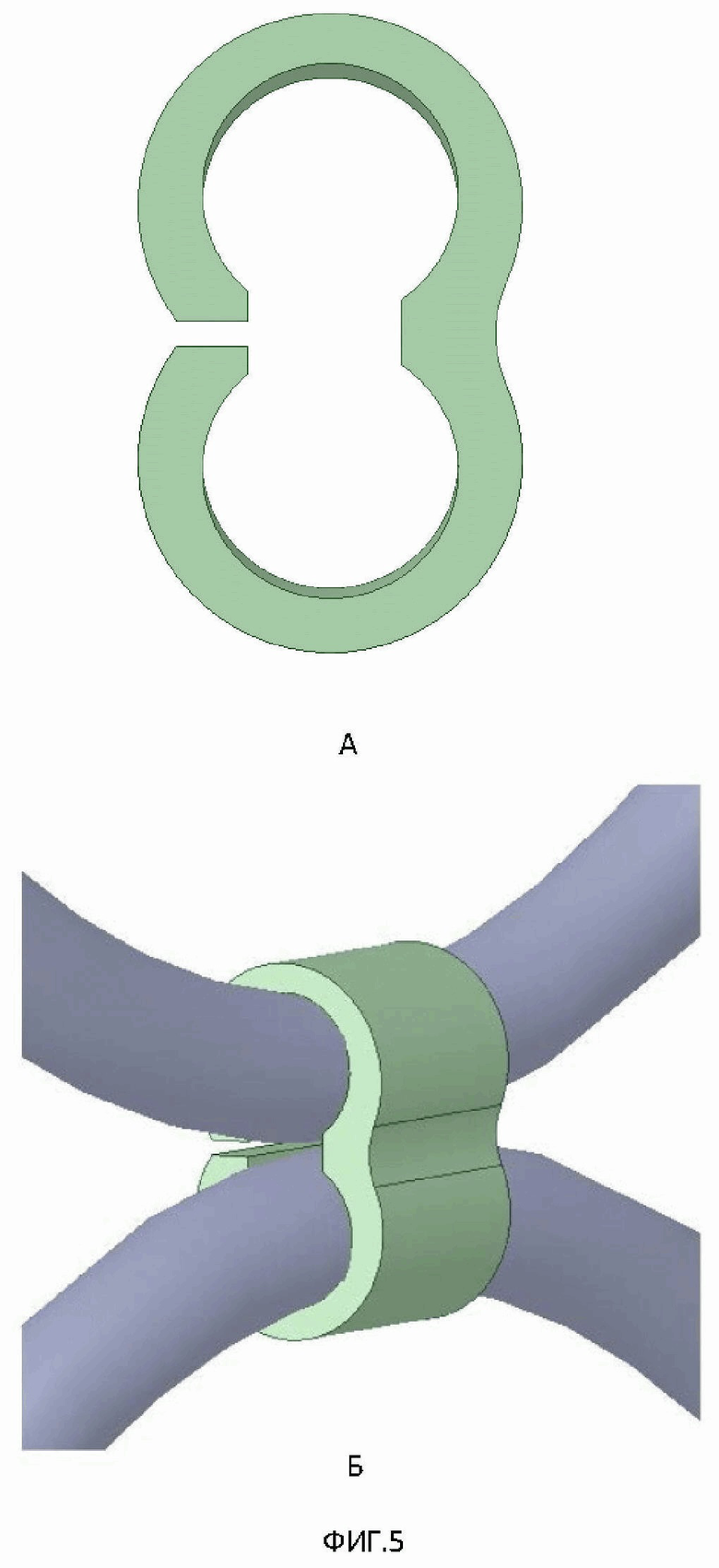
1. Устройство для замещении пострезекционных грудинно-реберных дефектов у пациентов при реконструкции каркаса грудной клетки, выполненное из сверхэластичного сплава, отличающееся тем, что оно выполнено в виде повторяющихся модулей в виде проволочных структур, представляющих собой последовательно расположенные петлеобразные сегменты с толщиной проволочной структуры 1,7±0,1 мм, высотой сегмента 50 мм, шириной сегмента 30 мм, с возможностью соединения проволочных структур между собой посредством зажима, при этом сверхэластичный сплав выполнен методом индукционной плавки в вакууме при следующем соотношении компонентов, ат %:
никель 49,5-49,6;
наночастицы серебра 0,05-0,1;
титан – остальное.
2. Устройство по п.1, отличающееся тем, что сегменты выполнены однопетельными или двухпетельными.
3. Устройство по п.1, отличающееся тем, что зажим для соединения проволочных структур представляет собой двойной хомут, выполненный из пластины никелида титана шириной 2,0±0,5 мм.
| МОДУЛЬ ДЛЯ КАРКАСНОЙ РЕКОНСТРУКЦИИ ГРУДНОЙ КЛЕТКИ | 2018 |
|
RU2694213C1 |
| СПОСОБ ПЛАСТИКИ ОБШИРНЫХ ПОСТРЕЗЕКЦИОННЫХ ОКОНЧАТЫХ ДЕФЕКТОВ СТЕНОК ГРУДНОЙ КЛЕТКИ И/ИЛИ СВОДА ЧЕРЕПА | 2009 |
|
RU2393808C1 |
| СПОСОБ УКРЫТИЯ ОБШИРНЫХ ОКОНЧАТЫХ ТОРАКОАБДОМИНАЛЬНЫХ ДЕФЕКТОВ | 2015 |
|
RU2600849C1 |
| КОСТНЫЙ ИМПЛАНТАТ | 1998 |
|
RU2157151C2 |
| 0 |
|
SU160899A1 | |
| Имплантат грудной клетки в части восстановления осколков ребер | 2023 |
|
RU2819510C1 |
| US 11160663 B2, 02.11.2021. | |||
Авторы
Даты
2025-04-01—Публикация
2024-10-03—Подача