Область техники
[0001] Настоящее изобретение относится к способу получения цитидин-5'-дифосфатного соединения.
Уровень техники
[0002] Способ промышленного производства цитидин-5'-дифосфатного соединения, включающий цитидин-5'-дифосфатхолин (далее также сокращенно ЦДФ-холин), включает способ химического синтеза, способ ферментации с применением микроорганизмов и энзиматический способ. В любом способе, поскольку способ протекает через реакцию, в которой цитидин-5'-монофосфат (далее также сокращенно 5'-ЦМФ) или его высокореакционноспособное производное конденсируется с фосфохолином или фосфоэтаноламином, 5'-ЦМФ, присутствующий в исходном сырье или получаемый как побочный продукт, присутствует в системе в виде примеси. Цитидин-5'-дифосфатное соединение гидролизуется при нагревании, и в качестве побочного продукта образуется 5'-ЦМФ.
[0003] На предшествующем уровне техники примеры общего способа очистки цитидин-5'-дифосфатного соединения из раствора, содержащего цитидин-5'-дифосфатное соединение, включают колоночную хроматографию с применением ионообменной смолы. Например, патентная литература 1-3 описывает способ, в котором неочищенный ЦДФ-холин адсорбируют на анионообменной смоле, и затем адсорбированный неочищенный ЦДФ-холин элюируется с применением сильно разбавленной муравьиной кислоты или соляной кислоты в концентрации приблизительно от 0,005 до 0,10 моль/л.
[0004] Патентная литература 4 описывает способ применения водного раствора хлорида натрия в качестве элюента. В качестве еще одного способа в патентной литературе 5 описан способ, в котором неочищенный ЦДФ-холин пропускают через слабоосновную анионообменную смолу, и только примесь 5'-ЦМП избирательно адсорбируется и удаляется.
Список цитирований
Патентная литература
[0005] Патентная литература 1: JPS48-86869A
Патентная литература 2: JPS47-18881A
Патентная литература 3: индийская опубликованная патентная заявка No. 2012MUM02534
Патентная литература 4: китайская опубликованная патентная заявка No. 101130797
Патентная литература 5: JPH6-31306B.
Сущность настоящего изобретения
Техническая проблема
[0006] В способе очистки цитидин-5'-дифосфатного соединения из раствора, содержащего цитидин-5'-дифосфатное соединение, трудно удалить примеси, особенно 5'-ЦМФ, который имеет аналогичные физико-химические свойства, из конечного продукта и при удалении 5'-ЦМФ колоночной хроматографией на предшествующем уровне техники цитидин-5'-дифосфатное соединение в растворе разбавляется, и последующее концентрирование требует много времени и средств. Также существует риск образования примесей, таких как 5'-ЦМФ, в результате разложения цитидин-5'-дифосфатного соединения вследствие нагревания на этапе концентрирования.
[0007] Таким образом, эффективное разделение цитидин-5'-дифосфатного соединения и примесей, особенно 5'-ЦМФ, из раствора, содержащего неочищенное цитидин-5'-дифосфатное соединение, и получение раствора, содержащего цитидин-5'-дифосфатное соединение с более высокой концентрация, чем до очистки, является важной проблемой при получении цитидин-5'-дифосфатного соединения высокой чистоты.
[0008] Однако в способах, описанных в патентных литературах 1-3, чтобы разделить, в частности, 5'-ЦМФ и цитидин-5'-дифосфатное соединение, необходимо собрать цитидин-5'-дифосфатное соединение, применяя большое количество элюата в условиях умеренного элюирования, и концентрация цитидин-5'-дифосфатного соединения в элюате снижается, так что для проведения кристаллизации или подобного необходима стадия концентрирования. В частности, когда элюирование осуществляется с применением летучей кислоты, такой как муравьиная кислота или соляная кислота, для удаления данного элюента упариванием концентрирование при пониженном давлении в основном осуществляют нагреванием, и в это время нагревание вызывает разложение цитидин-5'-дифосфатного соединения, и 5'-ЦМФ снова увеличивается, что представляет собой проблему для промышленного способа производства.
[0009] Способ, описанный в патентной литературе 4, не подходит в качестве способа промышленного производства, поскольку трудно окончательно удалить элюент, смешанный с фракцией, содержащей цитидин-5'-дифосфатное соединение. В способе, описанном в патентной литературе 5, необходимо промыть внутреннюю часть колонки со смолой водой после пропускания жидкости для сбора цитидин-5'-дифосфатного соединения. Аналогично способам, описанным в патентной литературе 1-3, концентрация цитидин-5'-дифосфатного соединения снижается по сравнению с тем, что было до прохождения через колонку, и, следовательно, применение в качестве способа промышленного производства ограничивается проходящей через колонку жидкостью, содержащей определенную концентрацию или более, и имеет низкую универсальность.
[0010] Как описано выше, о способе отделения 5'-ЦМФ от неочищенного цитидин-5'-дифосфатного соединения и концентрирования цитидин-5'-дифосфатного соединения до более высокой концентрации, чем до очистки, не сообщалось. Таким образом, целью настоящего изобретения является обеспечение способа получения цитидин-5'-дифосфатного соединения, с помощью которого 5'-ЦМФ можно эффективно удалить от неочищенного цитидин-5'-дифосфатного соединения, и цитидин-5'-дифосфатное соединение можно сконцентрировать до более высокой концентрации, чем до очистки.
Решение проблемы
[0011] Авторы настоящего изобретения обнаружили, что цитидин-5'-дифосфатное соединение можно эффективно очищать и концентрировать элюированием с применением раствора специфической органической кислоты, и обнаружили, что, в частности, цитидин-5'-дифосфатное соединение и 5'-ЦМФ можно эффективно разделяют, и можно получить элюат, содержащий цитидин-5'-дифосфатное соединение при более высокой концентрации, чем до очистки, тем самым завершив настоящее изобретение.
[0012] То есть, настоящее изобретение включает следующее.
1. Способ получения цитидин-5'-дифосфатного соединения, причем способ включает: следующие стадии (1) и (2):
(1) стадию приведения раствора, содержащего цитидин-5'-дифосфатное соединение, в контакт с основной ионообменной смолой для того, чтобы адсорбировать цитидин-5'-дифосфатное соединение на основной ионообменной смоле, и
(2) стадию получения элюата элюированием цитидин-5'-дифосфатное соединение, адсорбированного на основной ионообменной смоле, применяя водный раствор, содержащий органическую кислоту, содержащую 2 или более атомов углерода, в котором цитидин-5'-дифосфатное соединение представляет собой цитидин-5'-дифосфатное соединение, содержащее катионный заместитель.
2. Способ получения согласно 1 выше, в котором концентрация цитидин-5'-дифосфатного соединения, содержащегося в элюате на стадии (2), является равной или большей чем концентрация цитидин-5'-дифосфатного соединения в растворе, содержащем цитидин-5'-дифосфатное соединение на стадии (1).
3. Способ получения согласно 1 или 2 выше, в котором на стадии (2), температура, при которой цитидин-5'-дифосфатное соединение элюируют с основной ионообменной смолы, составляет 20°С или более.
4. Способ получения согласно любому 1-3 выше, в котором органическая кислота, содержащая 2 или более атомов углерода, представляет собой по меньшей мере одну органическую кислоту, выбранную из уксусной кислоты, пропионовой кислоты и масляной кислоты.
5. Способ получения согласно любому 1-4 выше, в котором на стадии (2), концентрация органической кислоты, содержащейся в водном растворе, составляет 0,1 моль/л или более.
6. Способ получения согласно любому 1-5 выше, в котором цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой соединение, в котором соединены цитидин-5'-дифосфат и катионный заместитель.
7. Способ получения согласно любому 1-6 выше, в котором цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой соединение, в котором катионный заместитель соединен с β-фосфатной группой цитидин-5'-дифосфата.
8. Способ получения согласно любому 1-7 выше, в котором органическая кислота, содержащая 2 или более атомов углерода, представляет собой карбоновую кислоту, содержащую 2 или более атомов углерода.
9. Способ получения согласно любому 1-8 выше, в котором цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой по меньшей мере одно, выбранное из цитидин-5'-дифосфатхолина и цитидин-5'-дифосфатэтаноламина.
Полезные свойства настоящего изобретения
[0013] Согласно способу получения настоящего изобретения, путем обеспечения стадии элюирования с применением раствора органической кислоты, содержащей 2 или более атомов, такой как уксусная кислота или пропионовая кислота, вместо муравьиной кислоты родственного уровня техники, можно обеспечить эффективное удаление 5'-ЦМФ и получение элюата, содержащего цитидин-5'-дифосфатное соединение с большей концентрацией, чем до очистки, и цитидин-5'-дифосфатное соединение высокой чистоты можно получить с высокой эффективностью.
Краткое описание чертежей
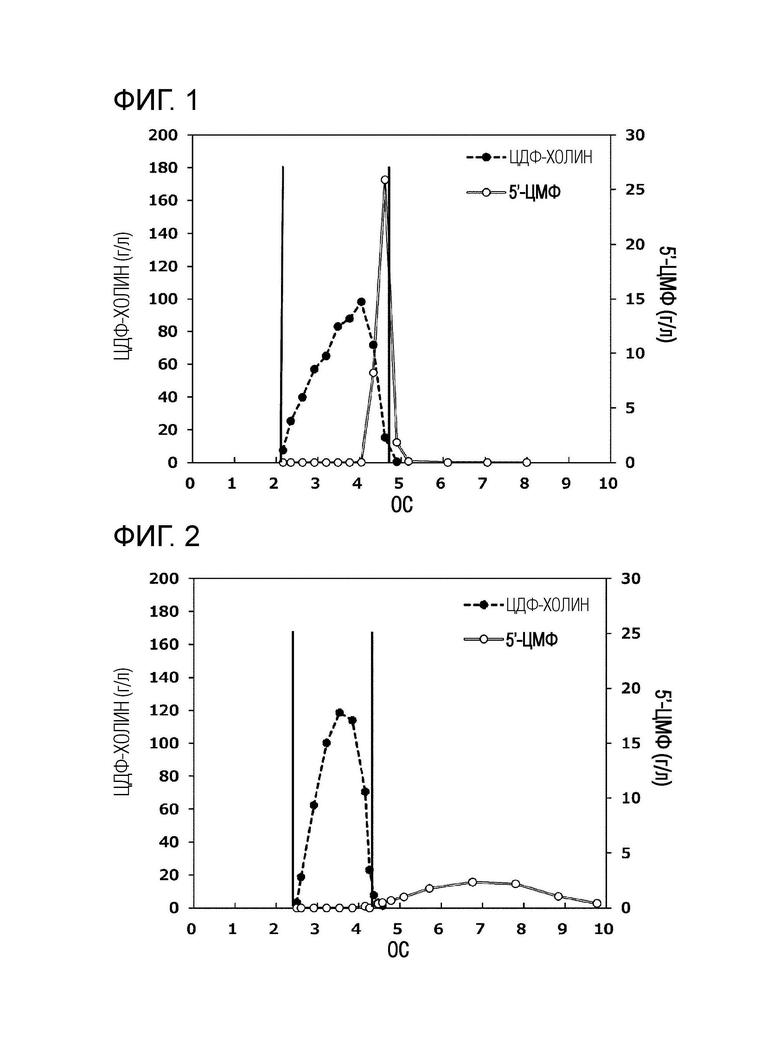
[0014] [Фиг. 1] Фиг. 1 представляет собой диаграмму, показывающую концентрацию ЦДФ-холина и концентрацию 5'-ЦМФ для каждой фракции элюирования в сравнительном примере 2, в котором RV на горизонтальной оси представляет собой аббревиатуру для объема смолы, и представляет собой объемное соотношение элюата, когда объем смолы составляет 1.
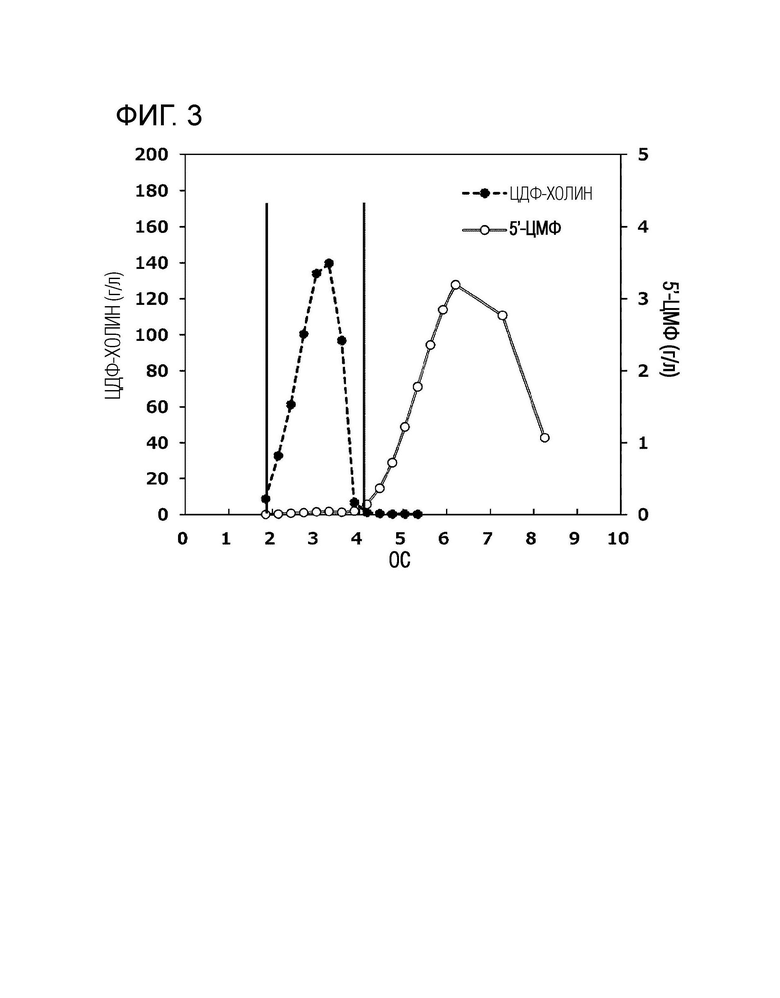
[Фиг. 2] Фиг. 2 представляет собой диаграмму, показывающую концентрацию ЦДФ-холина и концентрацию 5'-ЦМФ для каждой фракции элюирования в примере 2, в котором RV на горизонтальной оси представляет собой аббревиатуру для объема смолы, и представляет собой объемное соотношение элюата, когда объем смолы составляет 1.
[Фиг. 3] Фиг. 3 представляет собой диаграмму, показывающую концентрацию ЦДФ-холина и концентрацию 5'-ЦМФ для каждой фракции элюирования в сравнительном примере 4, в котором RV на горизонтальной оси представляет собой аббревиатуру для объема смолы, и представляет собой объемное соотношение элюата, когда объем смолы составляет 1.
Описание вариантов осуществления
[0015]<Способ получения>
Способ получения настоящего изобретения характеризуется включением следующих стадий (1) и (2).
(1) Стадия приведения раствора, содержащего цитидин-5'-дифосфатное соединение, в контакт с основной ионообменной смолой для того, чтобы адсорбировать цитидин-5'-дифосфатное соединение на основной ионообменной смоле.
(2) Стадия получения элюата элюированием цитидин-5'-дифосфатного соединения, адсорбированного на основной ионообменной смоле, применяя водный раствор, содержащий органическую кислоту, содержащую 2 или более атомов углерода.
[0016] (1) Стадия приведения раствора, содержащего цитидин-5'-дифосфатное соединение, в контакт с основной ионообменной смолой для того, чтобы адсорбировать цитидин-5'-дифосфатное соединение на основной ионообменной смоле.
[0017] В настоящем изобретении, цитидин-5'-дифосфатное соединение представляет собой цитидин-5'-дифосфатное соединение, содержащее катионный заместитель. Примеры цитидин-5'-дифосфатного соединения, содержащего катионный заместитель, включают соединение, в котором соединены цитидин-5'-дифосфат и катионный заместитель. Более конкретно, цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой соединение, в котором катионный заместитель соединен с β-фосфатной группой цитидин-5'-дифосфата. В настоящем изобретении, положения фосфатных групп в цитидин-5'-дифосфате представляют собой α-фосфатную группу и β-фосфатную группу в порядке от самой близкой к цитидину (Chemistry and Education, т. 46, No. 6, 1998, стр. 334-337). Примеры катионного заместителя включают заместитель, содержащий ониевый ион, такой как аммоний, оксоний, фосфоний, сульфоний, иминий, нитрилий, нитрозоний, диазоний, нитроний или диазений. Среди них предпочтительным является катионный заместитель, содержащий ион аммония. Примеры цитидин-5'-дифосфатного соединения, содержащего катионный заместитель, включают цитидин-5'-дифосфатхолин и цитидин-5'-дифосфатэтаноламин. Среди них с точки зрения эффективности очистки предпочтительными являются цитидин-5'-дифосфатхолин или цитидин-5'-дифосфатэтаноламин, и более предпочтительным является цитидин-5'-дифосфатхолин. Один из них может содержаться в растворе отдельно, или два или более из них могут содержаться в комбинации. Модификация цитидин-5'-дифосфатного соединения функциональной группой также допустима до тех пор, пока может поддерживаться отделение от 5'-ЦМФ.
[0018] На стадии (1) в способе получения настоящего изобретения, раствор, содержащий цитидин-5'-дифосфатное соединение, которое необходимо привести в контакт с основной ионообменной смолой, может представлять собой раствор, полученный любым способом, при условии, что он представляет собой раствор, содержащий цитидин-5'-дифосфатное соединение. Его примеры включают раствор, полученный способом химического синтеза, способом ферментации и способом с применением биокатализатора.
[0019] Примеры способа химического синтеза ЦДФ-холина включают способ, описанный в K. Kikugawa, М. Ichino, Chem. Pharm. Bull., 19, 1011, 1971. Примеры метода химического синтеза ЦДФ-этаноламина включают способы, описанные в Н. Ngo, М. F. Dunn et al. Biochemistry, 46, 7713, 2007.; Т. Tanaka yakugakuzasshi, 80, 439, 1959.; K. Oertell, С.E. McKenna, M. F. Goodman et al. Biochemistry, 53, 1842, 2014.; T. Tanaka et al. yakugakuzasshi, 85, 863, 1965.; и Т. Tanaka et al. yakugakuzasshi, 85, 863, 1965.
[0020] Примеры способа ферментации или способа с применением биокатализатора включают способы, описанные в патенте Японии №3369236; и Y. Liu et al. Appl. Microbiol. Biotechnol., 101, 1409, 2017. Раствор, содержащий цитидин-5'-дифосфатное соединение, применяемое на стадии (1) в способе получения настоящего изобретения предпочтительно представляет собой раствор, полученный путем удаления твердого содержимого из раствора, полученного способом ферментации или способом с применением биокатализатора.
[0021] В качестве раствора, содержащего цитидин-5'-дифосфатное соединение на стадии получения (1) в способе настоящего изобретения, можно применять раствор, полученный обработкой раствора, полученного способом химического синтеза, способом ферментации или способом с применением биокатализатора, сильной катионообменной смолой и заранее снижением или удалением примесей. При необходимости можно применять раствор, обработанный активированным углем или обесцвеченный с помощью неполярного пористого синтетического адсорбента типа Diaion серии HP (например, НР20 и НР21) производства Mitsubishi Chemical Corporation, серии Diaion SP800 (например, SP825 и SP850) производства Mitsubishi Chemical Corporation, серии Diaion SP200 (например, SP207) производства Mitsubishi Chemical Corporation и серии Amberlight XAD (например, XAD4, XAD7HP, XAD16HP, XAD1180 и XAD2000) производства Rohm and Haas.
[0022] Цитидин-5'-дифосфатное соединение и 5'-ЦМФ можно проанализировать обычным способом с применением высокоэффективной жидкостной хроматографии (УФ детектирование).
[0023] Концентрация цитидин-5'-дифосфатного соединения в растворе, содержащем цитидин-5'-дифосфатное соединение, на стадии (1) конкретно не ограничена, и предпочтительно составляет 100 или меньше, более предпочтительно 85 г/л или меньше, более предпочтительно 40 г/л или меньше, еще более предпочтительно 15 г/л или меньше и самое предпочтительное 13 г/л или меньше, с точки зрения эффективности очистки. Нижний предел концентрации цитидин-5'-дифосфатного соединения в растворе, содержащем цитидин-5'-дифосфатное соединение на стадии (1), конкретно не ограничен, и концентрация предпочтительно составляет 0,1 г/л или более, более предпочтительно 0,2 г/л или более, более предпочтительно 0,3 г/л или более и самое предпочтительное 0,4 г/л или более.
[0024] Отношение концентрации 5'-ЦМФ к концентрации цитидин-5'-дифосфатного соединения в растворе, содержащем цитидин-5'-дифосфатное соединение, на стадии (1) ("5'-ЦМФ концентрация (г/л)/концентрация цитидин-5'-дифосфатного соединения (г/л) × 100 (%)", в настоящем изобретении далее выражают как "5'-ЦМФ отношение (отношение в % 5'-ЦМФ к цитидин-5'-дифосфатному соединению)") конкретно не ограничено, и отношение предпочтительно составляет 150% или меньше, более предпочтительно 100% или меньше, более предпочтительно 50% или меньше и самое предпочтительное 15% или меньше, с точки зрения эффективности очистки.
[0025] Основная ионообменная смола настоящего изобретения конкретно не ограничена, и ее примеры включают ионообменные смолы, содержащие первичные или третичные амины или полиамины в качестве обменных групп в слабоосновной анионообменной смоле, и ионообменную смолу, содержащую четвертичный аммоний в качестве обменной группы в сильноосновной анионообменной смоле. В качестве ионообменной смолы, содержащей четвертичный аммоний, можно подходящим образом применять либо тип I, содержащий триметиламмониевую группу, либо триэтиламмониевую группу, либо тип II, содержащий диметилэтаноламмониевую группу. Примеры основного материала основной ионообменной смолы включают пористый тип, макропористый тип, гелевый тип, стирольный тип и акриловый тип.
[0026] Конкретные примеры основной ионообменной смолы включают серию Marathon (например, Marathon A, Marathon MSA и Marathon А2), изготовленную Dow Chemical Company, серию Monosphere (например, Monosphere 77 и Monosphere 550A), изготовленную Dow Chemical Company, 1×2, 1×4, 1×8, 22, 66 и MSA-2, изготовленные Dow Chemical Company, A400, A600, SGA550, A200, A300, A500, A501P, A502PS, A503, A510, A850, A860, A870, SSTA63, SSTA64, PFA520E, А100, A103S, A110, A111S, A133 S, A830W, A845 и A847, изготовленные Purolite, IRA400J, IRA402BL, IRA900J, IRA4580, SCAV4, HPR4002, IRA410J, IRA910CT, HPR4010, HPR4780, IRA67, IRA96SB и IRA98, изготовленные Organo Corporation, серию Diaion PA (например, PA306S, PA308, PA308L, PA312, PA312L, PA312LOH, PA312LTU, PA312LTUMB, PA316, PA316L, PA318L, PA318LOH, PA408, PA412, PA418, PA418 L, PA418LL, PAF308L, HPA25L, HPA25M, HPA512L и HPA716), изготовленную Mitsubishi Chemical Corporation (PA представляет собой торговое название), серию Diaion SA (например, SA10A, SA10AL, SA10ALLP, SA10AOH, SA10AP, SA10DL, SA11A, SA11AL, SA12A, SA12AL, SA12ALL, SA20A, SA20ALL, SA20ALLP, SA20AP, SA20AP2, SAF11AL, SANUPB, SAT10L и SAT20L), изготовленную Mitsubishi Chemical Corporation, Diaion серию UBA (например, UBA100, UBA100OH, UBA100OHUP, UBA120, UBA120OH, UBA12 OOHUP, UBA150 и UBA200), изготовленную Mitsubishi Chemical Corporation, и серию Diaion WA (например, WA10, WA20, WA21J, WA30, WA30C, WA30LL и WA55), изготовленную Mitsubishi Chemical Corporation.
[0027] В качестве основной ионообменной смолы настоящего изобретения, более предпочтительной является ионообменная смола, содержащая четвертичный аммоний в качестве обменной группы в сильноосновной анионообменной смоле. Конкретные примеры ионообменной смолы, содержащей четвертичный аммоний в качестве обменной группы в сильноосновной анионообменной смоле, включают 1×2, 1×4, 1×8, 22, MSA-2, Marathon A, Marathon А2, Marathon MSA, и Monosphere 550А, изготовленные Dow Chemical Company, A400, A600, SGA550, A200, A300, A500, A501P, A502PS, A503, A510, A850, A860, A870, SSTA63, SSTA64 и PFA520E, изготовленные Purolite, IRA400J, IRA402BL, IRA900J, IRA4580, SCAV4, HPR4002, IRA410J, IRA910CT и HPR4010, изготовленные Organo Corporation, серию Diaion PA (например, PA306S, PA308, PA308L, PA312, PA312L, PA312LOH, PA312LTU, PA312LTUMB, PA316, PA316L, PA318L, PA318LOH, PA408, PA412, PA418, PA418 L, PA418LL, PAF308L, HPA25L, HPA25M, HPA512L, и HPA716), изготовленную Mitsubishi Chemical Corporation (PA представляет собой торговое название), серию Diaion SA (например, SA10A, SA10AL, SA10ALLP, SA10AOH, SA10AP, SA10DL, SA11A, SA11AL, SA12A, SA12AL, SA12ALL, SA20A, SA20ALL, SA20ALLP, SA20AP, SA20AP2, SAF11AL, SANUPB, SAT10L и SAT20L), изготовленную Mitsubishi Chemical Corporation, и серию Diaion UBA (например, UBA100, UBA100OH, UBA100OHUP, UBA120, UBA120OH, UBA120OHUP, UBA150 и UBA200), изготовленную Mitsubishi Chemical Corporation.
[0028] Количество основной ионообменной смолы, подлежащей применению, может быть таким, чтобы количество катионов в растворе, содержащем цитидин-5'-дифосфатное соединение, то есть общее молярное количество примесей, таких как аминокислоты, органическая кислота, хлорид ион и подобные, содержащиеся в растворе в дополнение к цитидин-5'-дифосфатному соединению, находится в пределах общей обменной емкости основной ионообменной смолы. В качестве ионного типа основной ионообменной смолы можно применять либо гидроксид ион, либо ион, находящийся в состоянии связи с органической кислотой, содержащей 2 или более атомов, применяемой для элюирования, или их комбинацию.
[0029] Степень сшивки основной ионообменной смолы конкретно не ограничено при условии, что она представляет собой степень сшивки, способную разделить цитидин-5'-дифосфатное соединение и 5'-ЦМФ, и степень сшивки составляет 1% - 16%, более предпочтительно 2% - 12% и более предпочтительно 4% - 10%. Основную ионообменную смолу можно применять в способе, в котором раствор, содержащий цитидин-5'-дифосфатное соединение, может быть приведен в контакт с основной ионообменной смолой, и основную ионообменную смолу предпочтительно применяют в настоящем изобретении в заполняющей колонку форме, и в настоящем изобретении можно применять колонку любого типа.
[0030] Когда раствор, содержащий цитидин-5'-дифосфатное соединение, приводят в контакт с основной ионообменной смолой путем пропускания раствора через колонку, заполненную смолой, для адсорбции цитидин-5'-дифосфатного соединения на смоле, например, скорость прохождения через колонку при пропускании через колонку, заполненную основной ионообменной смолой со степенью сшивки 1%-16%, представляет собой объемную скорость (объемное соотношение (/час) раствора, прошедшего через колонку за час при объеме смолы ионообменной смолы равном 1, в дальнейшем именуемая «ОС»), и ОС предпочтительно=0,1-5, более определенное ОС=0,2-4, и более предпочтительно ОС=0,4-3.
[0031] (2) Стадия получения элюата элюированием цитидин-5'-дифосфатного соединения, адсорбированного на основной ионообменной смоле, применяя водный раствор, содержащий органическую кислоту, содержащую 2 или более атомов углерода. Стадия (2) представляет собой стадию получения элюата пропусканием водного раствора, содержащего органическую кислоту, содержащую 2 или более атомов углерода, через колонку с основной ионообменной смолой, на которой адсорбировано цитидин-5'-дифосфатное соединение на стадии (1), посредством этого элюируя цитидин-5'-дифосфатное соединение со смолы, отделяя и очищая цитидин-5'-дифосфатное соединение.
[0032] Органическая кислота, содержащая 2 или более атомов углерода, предпочтительно представляет собой карбоновую кислоту, содержащую 2 или более атомов углерода. Примеры органической кислоты, содержащей 2 или более атомов углерода, включают уксусную кислоту, пропионовую кислоту, масляную кислоту, валериановую кислоту, молочную кислоту, гликолевую кислоту, пировиноградную кислоту, глюконовую кислоту, винную кислоту, щавелевую кислоту, малоновую кислоту, янтарную кислоту, глутаровую кислоту, адипиновую кислоту, яблочную кислоту, фумаровую кислоту, малеиновую кислоту, лимонную кислоту, изолимонную кислоту и аскорбиновую кислоту. Среди них предпочтительными являются уксусная кислота, пропионовая кислота и масляная кислота, и более предпочтительными являются уксусная кислота и пропионовая кислота. Одну из органических кислот, содержащих 2 или более атомов, можно применять отдельно, или их множество можно применять в комбинации. Верхний предел количества атомов углерода в органической кислоте специально не ограничен, и с точки зрения растворимости в воде количество атомов углерода составляет 8 или меньше, более предпочтительно 6 или меньше, и более предпочтительно 3 или меньше. Органическая кислота, содержащая 2 или более атомов углерода, может представлять собой соль органической кислоты, содержащей 2 или более атомов углерода.
[0033] Концентрация органической кислоты, содержащей 2 или более атомов углерода, в водном растворе, содержащем органическую кислоту, содержащую 2 или более атомов углерода, предпочтительно составляет 0,1 моль/л или более, и более предпочтительно 0,35 моль/л или более, с точки зрения повышения эффективности очистки цитидин-5'-дифосфатного соединения. Верхний предел концентрации органической кислоты, содержащей 2 или более атомов углерода, в водном растворе, конкретно не ограничен, и концентрация предпочтительно составляет 2,0 моль/л или меньше, более предпочтительно 1,0 моль/л или меньше, более предпочтительно 0,6 моль/л или меньше и самое предпочтительное 0,45 моль/л или меньше, с точки зрения баланса между органической кислотой, которую применяют, и эффектом.
[0034] Элюат на стадии (2) (элюат, содержащий цитидин-5'-дифосфатное соединение, также называемый в настоящем изобретении элюатом, содержащим цитидин-5'-дифосфатное соединение) можно получить сбором жидкости, полученной пропусканием водного раствора, содержащего органическую кислоту, содержащую 2 или более атомов углерода, через колонку с основной ионообменной смолой в виде двух или более фракций для того, чтобы разделить примеси и цитидин-5'-дифосфатное соединение и также обеспечить концентрирование цитидин-5'-дифосфатного соединения, при необходимости. Полученные две или более фракций, содержащих цитидин-5'-дифосфатное соединение, можно смешивать, получая элюат, содержащий цитидин-5'-дифосфатное соединение. Жидкость можно собирать в виде более предпочтительно трех или более фракций, и более предпочтительно в виде четырех или более фракциях. Перед стадией смешивания фракций, содержащих цитидин-5'-дифосфатное соединение, можно включить стадию анализа цитидин-5'-дифосфатного соединения и примесей, таких как 5'-ЦМФ, которые содержатся в каждой фракции, с помощью ВЭЖХ. Цитидин-5'-дифосфатное соединение и примеси, такие как 5'-ЦМФ, можно анализировать, например, с помощью обычного способа с применением высокоэффективной жидкостной хроматографии (УФ-детектирование).
[0035] Концентрация цитидин-5'-дифосфатного соединения, содержащегося в элюате на стадии (2), предпочтительно является равной или большей, чем концентрация цитидин-5'-дифосфатного соединения в растворе, содержащем цитидин-5'-дифосфатное соединение на стадии (1). Конкретно, например, соотношение концентраций, то есть, концентрация (г/л) цитидин-5'-дифосфатного соединения, содержащегося в элюате на стадии (2)/концентрация (г/л) цитидин-5'-дифосфатного соединения в растворе, приводимом в контакт с основной ионообменной смолой на стадии (1) является предпочтительно 1,0 кратным или более, и более предпочтительно 1,1 кратным или более. Верхний предел соотношения концентраций конкретно не ограничен, и соотношение концентраций является, например, 160 кратным или меньше.
[0036] Отношение 5'-ЦМФ (отношение 5'-ЦМФ к цитидин-5'-дифосфатному соединению) элюата на стадии (2) предпочтительно составляет 1,00% или меньше, более предпочтительно 0,20% или меньше, и более предпочтительно 0,10% или меньше. Нижний предел отношения 5'-ЦМФ к цитидин-5'-дифосфатному соединению конкретно не ограничен, и отношение составляет, например, 0% или более.
[0037] Извлеченная доля (%) цитидин-5'-дифосфатного соединения на стадии (2), то есть, масса (г) цитидин-5'-дифосфатного соединения, содержащегося в элюате на стадии (2)/масса (г) цитидин-5'-дифосфатного соединения, содержащегося в растворе, содержащем цитидин-5'-дифосфатное соединение на стадии (1), × 100 (%) предпочтительно составляет 60% или более, более предпочтительно 80% или более и более предпочтительно 89% или более. Верхний предел извлеченной доли конкретно не ограничен, и извлеченная доля составляет, например, меньше чем 100%.
[0038] На стадии (2), температура, при которой цитидин-5'-дифосфатное соединение элюируют с основной ионообменной смолы, предпочтительно составляет 20°С или более, более предпочтительно 30°С или более, и более предпочтительно 40°С или более, с точки зрения повышения разделяющей способности цитидин-5'-дифосфатного соединения и 5'-ЦМФ при элюировании. Верхний предел температуры элюирования специально не ограничен, и температура элюирования предпочтительно равна 60°С или ниже с точки зрения предотвращения образования 5'-ЦМФ вследствие термического разложения цитидин-5'-дифосфатного соединения. В настоящем изобретении температура элюирования относится к температуре колонки и/или температуре водного раствора, содержащего органическую кислоту, содержащую 2 или более атомов.
[0039] С точки зрения повышения разделяющей способности цитидин-5'-дифосфатного соединения и 5'-ЦМФ, когда органическая кислота, применяемая для элюирования, представляет собой органическую кислоту, содержащую 2 атомов углерода (например, уксусную кислоту), температура элюирования предпочтительно составляет 30°С-60°С, и более предпочтительно 40°С-60°С. С другой стороны, когда органическая кислота, применяемая для элюирования, представляет собой органическую кислоту, содержащую 3 или более атомов углерода (например, пропионовую кислоту), температура элюирования предпочтительно составляет 20°С-60°С, более предпочтительно 30°С-60°С и более предпочтительно 40°С-60°С.
[0040] Известно, что при изменении температуры в реакции ионного обмена время удерживания соединения изменяется из-за изменений равновесия разделения, скорости диффузии, степени диссоциации, вязкости элюента и подобных. Хотя влияние температуры на реакцию ионного обмена варьируется в зависимости от соединения, а также варьируется в зависимости от носителя и элюента, авторы настоящего изобретения обнаружили, что способность к разделению цитидин-5'-дифосфатного соединения и 5'-ЦМФ имеет тенденцию увеличиваться при увеличении температуры элюирования. Кроме того, авторы настоящего изобретения подтвердили, что гидролиз цитидин-5'-дифосфатного соединения при нагревании протекает даже при 30°С, и при условии 40°С и более разложение прогрессирует значительно, причем более чем в 10 раз больше 5'-ЦМФ образуется в качестве побочного продукта по сравнению с условиями с 20°С, но авторы настоящего изобретения обнаружили, что эффект улучшения способности к разделению цитидин-5'-дифосфатного соединения и 5'-ЦМФ за счет увеличения температуры элюирования является более значительным, чем недостатки разложения при нагревании.
[0041] На стадии (2), скорость прохождения через колонку, при которой водный раствор, содержащий органическую кислоту, содержащую 2 или более атомов углерода, проходит через колонку с основной ионообменной смолой предпочтительно составляет ОС=0,1-2, более предпочтительно ОС=0,2-1,5, и более предпочтительно ОС=0,4-1.
[0042] Посредством вышеуказанных стадий (1) и (2) цитидин-5'-дифосфатное соединение и примеси, содержащиеся в растворе, такие как 5'-ЦМФ, УМФ, УДФ, УТФ, УДФ-холин, УДФ-этаноламин, ЦДФ, ЦТФ, неорганическая фосфорная кислота и полифосфорная кислота, можно эффективно разделить и получить цитидин-5'-дифосфатное соединение высокой чистоты. В частности, вышеуказанные стадии (1) и (2) позволяют эффективно разделить цитидин-5'-дифосфатное соединение и 5'-ЦМФ.
[0043] Элюат, содержащий цитидин-5'-дифосфатное соединение, полученный на стадии элюирования, можно обрабатывать активированным углем или, при необходимости, обесцвечивать с применением неполярного пористого синтетического адсорбента, такого как серию Diaion HP (например, НР20 и НР21), изготовленную Mitsubishi Chemical Corporation, серию Diaion SP800 (например, SP825 и SP850), изготовленную Mitsubishi Chemical Corporation, серию Diaion SP200 (например, SP207), изготовленную Mitsubishi Chemical Corporation, серию Amberlight XAD (например, XAD4, XAD7HP, XAD16HP, XAD1180 и XAD2000), изготовленную Rohm и Haas.
[0044] Кроме того, чтобы получить кристалл цитидин-5'-дифосфатного соединения в свободной форме, кристалл цитидин-5'-дифосфатного соединения можно получить путем регулирования рН элюата, содержащего цитидин-5'-дифосфатное соединение, или жидкости после обесцвечивающей обработки до предпочтительно 2,0-4,0 кислотой или щелочью при необходимости, выполняя концентрирование при необходимости, затем доводя концентрацию цитидин-5'-дифосфатного соединения до предпочтительно 50 г/л-800 г/л, более предпочтительно 100 г/л-700 г/л, и применяя органический растворитель предпочтительно гидрофильный органический растворитель, такой как ацетон, этанол, метанол или пропанол.
[0045] Для получения кристалла соли цитидин-5'-дифосфатного соединения, например, кристалла натриевой соли цитидин-5'-дифосфатного соединения, ее можно получить доведением рН элюата, содержащего цитидин-5'-дифосфатное соединение, до значения 5,0-9,5 гидроксидом натрия, при необходимости выполняя обесцвечивающую обработку и концентрационную обработку, затем доводя концентрацию цитидин-5'-дифосфатного соединения до предпочтительно 50 г/л-800 г/л и более предпочтительно 100 г/л-700 г/л, и применяя органический растворитель, предпочтительно гидрофильный органический растворитель, такой как ацетон, этанол, метанол или пропанол.
[0046] Примеры способа получения кристалла цитидин-5'-дифосфатного соединения с применением органического растворителя включают способ, в котором органический растворитель добавляют к раствору цитидин-5'-дифосфатного соединения для осаждения кристалла, и способ, в котором раствор цитидин-5'-дифосфатного соединения добавляют по каплям к большому количеству органического растворителя для осаждения кристаллов.
[0047] Далее настоящее изобретение будет дополнительно подробно описано со ссылкой на примеры, но настоящее изобретение не ограничивается данными примерами.
Примеры
[0048] [Пример анализа 1]
Количественный анализ ЦДФ-холина, 5'-ЦМФ и ЦДФ-этаноламина ВЭЖХ проводили в следующих условиях.
Применяемое устройство: контроллер системы (СВМ-20А), детектор (SPD-20A), насос (LC-20AT), автосэмплер (SIL-20ACXR), термостат колонки (СТО-10ASvp), программное обеспечение для анализа данных (LabSolutions версия 5,85) (все изготовлено Shimadzu Corporation).
Детектор: фотометр поглощения ультрафиолетовых лучей (измеряемая длина волны 254 нм).
Колонка: Shodex Asahipak NH2P-50 4Е 4,6×250 мм (изготовлена Showa Denko).
Подвижная фаза: 0,03 моль/л водный раствор дигидрофосфата калия, доведенный до рН 3,5 с помощью фосфорной кислоты (20,41 г дигидрофосфата калия растворяют в 5 л дистиллированной воды, и рН доводят до рН 3,5 добавлением фосфорной кислоты).
Температура колонки: 40°С.
Скорость потока: 0,50 мл/мин.
Вводимое количество образца: 10 мкл.
Время удерживания: ЦДФ-холин 7,3 мин, 5'-ЦМФ 16,0 мин ЦДФ-этаноламин 9,1 мин.
[0049] Каждую фракцию элюата на стадии (2) разводили в 100 раз или доводили до концентрации, близкой к концентрации стандартного образца, и применяли для анализа. Концентрации ЦДФ-холина, 5'-ЦМФ и ЦДФ-этаноламина, содержащихся в каждой фракции элюата, определяли, применяя 0,02 г/л ЦДФ-холина, 0,01 г/л 5'-ЦМФ и 0,018 г/л ЦДФ-этаноламина в качестве стандартных образцов соответственно, исходя из значений площадей пиков стандартных образцов способом одноточечной калибровочной кривой.
[0050] Например, для ЦДФ-холина, концентрацию можно рассчитать следующим образом: (концентрация ЦДФ-холина (г/л) фракции элюента) = 0,02×В/А×x, где А представляет собой величину площади пика стандарта ЦДФ-холина, и В представляет собой величину площади пика фракции элюента, разбавленной в x раз.
[0051] [Пример анализа 2]
Количественный анализ тринатриевой соли ЦДФ ВЭЖХ проводили в следующих условиях.
Применяемое устройство: контроллер системы (СВМ-20А), детектор (SPD-20A), насос (LC-20AD), автосэмплер (SIL-20AC), термостат колонки (СТО-20АС), программное обеспечение для анализа данных (LabSolutions версия 5,71) (все изготовлено Shimadzu Corporation).
Детектор: фотометр поглощения ультрафиолетовых лучей (измеряемая длина волны 254 нм).
Колонка: две Partisil 10 SAX 4,0×250 мм, соединенные последовательно (Hichrom).
Подвижная фаза: 0,06 моль/л водный раствор дигидрофосфата калия, доводенный до рН 3,5 с помощью фосфорной кислоты (40,83 г дигидрофосфата калия растворяют в 5 л дистиллированной воды, рН доводят до рН 3,5 добавлением фосфорной кислоты).
Температура колонки: 30°С.
Скорость потока: 0,45 мл/мин.
Вводимое количество образца: 10 мкл.
Время удерживания: тринатриевая соль ЦДФ 82,5 мин.
[0052] [Сравнительный пример 1]
Со ссылкой на опубликованную индийскую патентную заявку №2012MUM02534, эксперименты проводили, применяя 0,10 моль/л водный раствор муравьиной кислоты. В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 210 мл водного раствора, содержащего ЦДФ-холин (изготовленный Kyowa Hakko Bio Co., Ltd.) при концентрации 7,02 г/л и 5'-ЦМФ (изготовленный Tokyo Chemical Industry Co., Ltd.) при концентрации 0,37 г/л [отношение концентрации 5'-ЦМФ к концентрации ЦДФ-холина в растворе (далее в настоящем изобретении называют "отношение 5'-ЦМФ к ЦДФ-холину") составляет 5,3%], и водный раствор пропускали через колонку с 150 мл Marathon А ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции.
[0053] Затем температуру снаружи колонки доводили до 20°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 20°С, 3 л 0,10 моль/л водного раствора муравьиной кислоты (разбавленный реагент специальной чистоты, изготовленный FUJIFILM Wako Pure Chemical Corporation) пропускали через колонку при ОС=0,85, и получали 29,9 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 239 мл раствора, имеющего концентрацию ЦДФ-холина 6,08 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,40 г/л (отношение 5'-ЦМФ к ЦДФ-холину 6,6%). Извлеченная доля ЦДФ-холина составляла 98,6%.
[0054] [Сравнительный пример 2]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,20 л водного раствора, содержащего ЦДФ-холин при концентрации 7,11 г/л и 5'-ЦМФ при концентрации 0,36 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,1%), и водный раствор пропускали через колонку с 150 мл Marathon MSA ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки доводили до 20°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 20°С, 1350 мл 0,35 моль/л водного раствора муравьиной кислоты пропускали через колонку при ОС=0,85, и получали 14,1 мл каждого элюата. Рисунок 1 показывает результат количественной оценки концентрации ЦДФ-холина и концентрации 5'-ЦМФ по ВЭЖХ для каждой элюируемой фракции.
[0055] Фракции, содержащие ЦДФ-холин, смешивали, и в результате, получали 381 мл раствора, имеющего концентрацию ЦДФ-холина 59,7 г/л. Концентрация 5'-ЦМФ в растворе составляла 2,7 г/л (отношение 5'-ЦМФ к ЦДФ-холину 4,5%). Извлеченная доля ЦДФ-холина составляла 100%.
[0056] [Пример 1]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,20 л водного раствора, содержащего ЦДФ-холин при концентрации 7,11 г/л и 5'-ЦМФ при концентрации 0,36 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,1%), и водный раствор пропускали через колонку с 150 мл Marathon MSA ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки доводили до 20°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 20°С, 1350 мл 0,35 моль/л водного раствора уксусной кислоты (разбавленный реагент специальной степени чистоты, изготовленный FUJIFILM Wako Pure Chemical Corporation) пропускали через колонку при ОС=0,85, и получали 14,6 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 351 мл раствора, имеющего концентрацию ЦДФ-холина 65,3 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,10 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,15%). Извлеченная доля ЦДФ-холина составляла 100%.
[0057] [Пример 2]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,21 л водного раствора, содержащего ЦДФ-холин при концентрации 7,13 г/л и 5'-ЦМФ при концентрации 0,38 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,3%), и водный раствор пропускали через колонку с 150 мл Marathon MSA ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки доводили до 20°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 20°С, 1350 мл 0,35 моль/л водного раствора пропионовой кислоты (разбавленный реагент Wako специальной степени чистоты, изготовленный FUJIFILM Wako Pure Chemical Corporation) пропускали через колонку при ОС=0,85, и получали 15,6 мл каждого элюата. Рисунок 2 показывает результат количественной оценки концентрации ЦДФ-холина и концентрации 5'-ЦМФ по ВЭЖХ для каждой элюируемой фракции.
[0058] Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 281 мл раствора, имеющего концентрацию ЦДФ-холина 78,2 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,03 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,04%). Извлеченная доля ЦДФ-холина составляла 96,0%.
[0059] [Пример 3]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,64 л водного раствора, содержащего ЦДФ-холин при концентрации 7,12 г/л и 5'-ЦМФ при концентрации 0,41 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,8%), и водный раствор пропускали через колонку с 150 мл Marathon А ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки доводили до 20°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 20°С, 1350 мл 0,45 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали 14,8 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 415 мл раствора, имеющего концентрацию ЦДФ-холина 63,2 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,32 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,51%). Извлеченная доля ЦДФ-холина составляла 100%.
[0060] [Пример 4]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,64 л водного раствора, содержащего ЦДФ-холин при концентрации 7,12 г/л и 5'-ЦМФ при концентрации 0,41 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,8%), и водный раствор пропускали через колонку с 150 мл Marathon А ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки доводили до 30°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 30°С, 1350 мл 0,45 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали 14,6 мл каждого элюата. Рисунок 3 показывает результат количественного определения концентрации ЦДФ-холина и концентрации 5'-ЦМФ ВЭЖХ для каждой элюируемой фракции. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 34 9 мл раствора, имеющего концентрацию ЦДФ-холина 71,4 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,03 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,04%). Извлеченная доля ЦДФ-холина составляла 96,1%.
[0061] [Пример 5]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,64 л водного раствора, содержащего ЦДФ-холин при концентрации 7,13 г/л и 5'-ЦМФ при концентрации 0,38 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,3%), и водный раствор пропускали через колонку с 150 мл Marathon А ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 60°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 60°С, 1350 мл 0,45 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали 14,8 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 354 мл раствора, имеющего концентрацию ЦДФ-холина 71,2 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,01 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,01%). Извлеченная доля ЦДФ-холина составляла 97,1%.
[0062] [Сравнительный пример 3]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,20 л водного раствора, содержащего ЦДФ-холин при концентрации 7,10 г/л и 5'-ЦМФ при концентрации 0,38 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,4%), и водный раствор пропускали через колонку с 150 мл Marathon MSA ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 40°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 1350 мл 0,45 моль/л водного раствора муравьиной кислоты пропускали через колонку при ОС=0,85, и получали 14,7 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 323 мл раствора, имеющего концентрацию ЦДФ-холина 67,4 г/л. Концентрация 5'-ЦМФ в растворе составляла 3,5 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,2%). Извлеченная доля ЦДФ-холина составляла 95,8%.
[0063] [Пример 6]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 3,20 л водного раствора, содержащего ЦДФ-холин при концентрации 7,10 г/л и 5'-ЦМФ при концентрации 0,38 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,4%), и водный раствор пропускали через колонку с 150 мл Marathon MSA ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 40°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 1350 мл 0,45 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали 15,2 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 305 мл раствора, имеющего концентрацию ЦДФ-холина 70,8 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,05 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,07%). Извлеченная доля ЦДФ-холина составляла 95,0%.
[0064] [Пример 7]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 2,90 л водного раствора, содержащего ЦДФ-холин при концентрации 7,05 г/л и 5'-ЦМФ при концентрации 0,37 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,2%), и водный раствор пропускали через колонку с 150 мл Marathon А ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 40°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 3 л 0,10 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали 26,8 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 885 мл раствора, имеющего концентрацию ЦДФ-холина 22,6 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,003 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,01%). Извлеченная доля ЦДФ-холина составляла 97,8%.
[0065] [Пример 8]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 2,15 Л водного раствора, содержащего ЦДФ-холин при концентрации 7,24 г/л и 5'-ЦМФ при концентрации 0,38 г/л (отношение 5'-ЦМФ к ЦДФ-холину 5,2%), и водный раствор пропускали через колонку с 139 мл PFA520E ОН- типа (изготовленной Purolite) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 40°С, и 209 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 1500 мл 0,10 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали 13,9 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали, и в результате получали 487 мл раствора, имеющего концентрацию ЦДФ-холина 31,0 г/л. Концентрация 5'-ЦМФ в растворе составляла 0,005 г/л (отношение 5'-ЦМФ к ЦДФ-холину 0,02%). Извлеченная доля ЦДФ-холина составляла 97,0%.
[0066] [Пример 9]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 1,00 л водного раствора, содержащего ЦДФ-холин при концентрации 7,04 г/л и 5'-ЦМФ при концентрации 0,37 г/л (соотношение 5'-ЦМФ к ЦДФ-холину 5,3%), и водный раствор пропускали через колонку со 100 мл Monosphere 77 ОН- типа (изготовленной Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 40°С, и 150 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 1500 мл 0,40 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали по 15,0 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали и в результате получали 285 мл раствора, имеющего концентрацию ЦДФ-холина 24,4 г/л. Концентрация 5'-ЦМФ в растворе составила 0,005 г/л (соотношение 5'-ЦМФ к ЦДФ-холину 0,02%). Извлеченная доля ЦДФ-холина составила 98,8%.
[0067] В таблице 1 показаны результаты, полученные выше.
[0068] [Таблица 1]
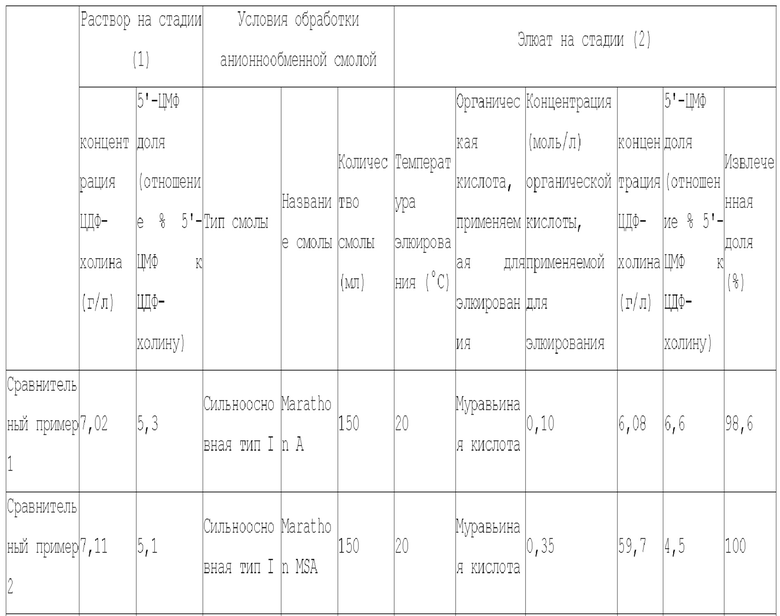
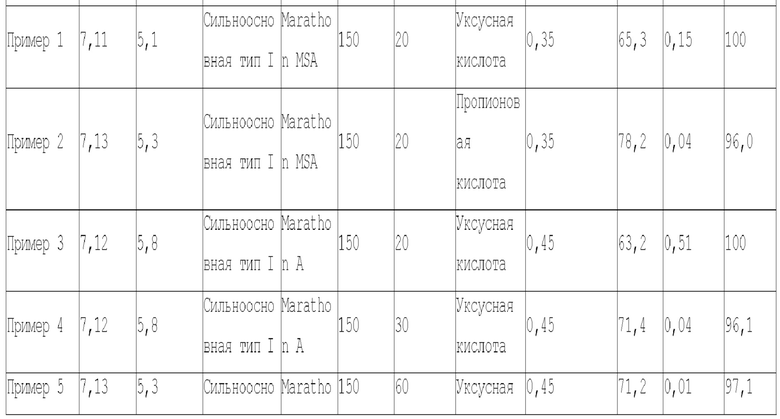
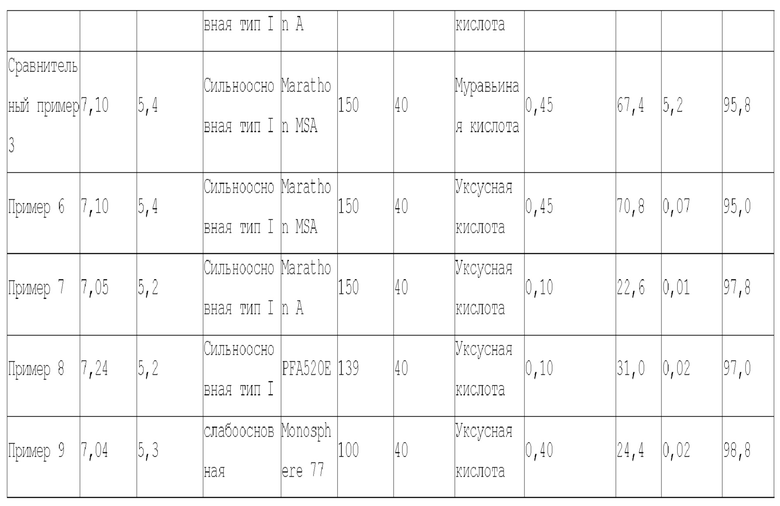
[0069] Как видно в таблице 1, находили, что в примерах 1-9, в которых элюат получали приведением раствора, содержащего цитидин-5'-дифосфатное соединение, в контакт с основной ионообменной смолой, адсорбируя цитидин-5'-дифосфатное соединение на основной ионообменной смоле, и затем элюированием цитидин-5'-дифосфатного соединения, адсорбированного на основной ионообменной смоле, применяя водный раствор, содержащий органическую кислоту, содержащую два или более атомов углерода, цитидин-5'-дифосфатное соединение высокой чистоты получали с высокой эффективностью по сравнению с сравнительными примерами 1-3, в которых цитидин-5'-дифосфатное соединение элюировали, применяя водный раствор, содержащий органическую кислоту, содержащую один атом углерода.
[0070] [Пример 10]
Органохимический синтез ЦДФ-холина проводили по известному способу (K. Kikugawa, М. Ichino, Chem. Pharm. Bull., 19, 1011, 1971.). К 20 мл воды добавляли 6,6 г тетрагидрата кальциевой соли хлорида фосфохолина (изготовленного Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием при 80°С до растворения. К раствору добавляли 2,52 г дигидрата щавелевой кислоты (реагент специальной чистоты, изготовленный FUJIFILM Wako Pure Chemical Corporation) с последующим перемешиванием в течение 10 минут.
[0071] Образовавшийся белый осадок собирали фильтрованием, и полученный фильтрат концентрировали при 50°С и пониженном давлении. Затем, к нему добавляли 16 мл ДМФ (изготовленного FUJIFILM Wako Pure Chemical Corporation, для органического синтеза) с последующим концентрированием при 70°С и пониженном давлении. После охлаждения до 0°С к нему по каплям добавляли раствор, полученный растворением 4,4 г п-толуолсульфонилхлорида (изготовленного Nacalai Tesgue, Inc.) в 6 мл ДМФ, с последующим перемешиванием до однородности. К нему добавляли 2,0 г цитидин-5'-монофосфата с последующим перемешиванием в течение ночи при комнатной температуре. После повторного охлаждения до 0°С к нему добавляли 250 мл воды и доводили рН до 3,5, применяя 28 мас. % аммиачную воду (реагент специального сорта, изготовленный FUJIFILM Wako Pure Chemical Corporation). Две из вышеперечисленных операций выполняли одновременно, и после смешивания обоих добавляли воду для получения 5050 мл раствора, содержащего цитидин-5'-дифосфатное соединение. На данный момент, раствор, содержащий цитидин-5'-дифосфатное соединение, содержал ЦДФ-холин при концентрации 0,486 г/л и 5'-ЦМФ при концентрации 0,0717 г/л (соотношение 5'-ЦМФ к ЦДФ-холину 14,8%).
[0072] Таким образом, полученные 2450 мл раствора, содержащего цитидин-5'-дифосфатное соединение, пропускали через колонку с 150 мл РА412 ОН- типа (изготовленной Mitsubishi Chemical Corporation) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 60°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 60°С, 1350 мл водного раствора с 0,50 моль/л пропионовой кислоты пропускали через колонку при ОС=0,85, и получали 15,2 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали и в результате получали 106 мл раствора с концентрацией ЦДФ-холина 10,7 г/л. Концентрация 5'-ЦМФ в растворе составила 0,003 г/л (соотношение 5'-ЦМФ к ЦДФ-холину 0,03%). Извлеченная доля ЦДФ-холина составила 95,3%. Из данных результатов находили, что способ получения настоящего изобретения также можно применять к раствору, содержащему цитидин-5'-дифосфатное соединение, полученное способом органического синтеза.
[0073] [Пример 11]
Культуральный раствор, имеющий концентрацию ЦДФ-холина 30,8 г/л, получали способом, описанным в патенте Японии №3369236, и рН доводили до 3,0 серной кислотой. Затем бактериальные клетки отделяли центрифугированием (8000 об/мин, 10 минут) и к полученному супернатанту добавляли воду с получением 10,9 л водного раствора, содержащего ЦДФ-холин при концентрации 12,2 г/л в качестве раствора, содержащего цитидин-5'-дифосфатное соединение.
[0074] Раствор, содержащий цитидин-5'-дифосфатное соединение, пропускали через колонку с 8,4 л сильнокислой катионнообменной смолы Н+ типа при ОС=0,26 для адсорбции, при этом внешнюю температуру колонки поддерживали на уровне 10°С. Затем, холодную воду с температурой 10°С пропускали через колонку, и когда начиналось элюирование ЦДФ-холина, раствор непрерывно пропускали через колонку с 900 мл РА412 ОН- типа для адсорбции. Затем температуру снаружи колонки ПА412 повышали до 40°С, и через колонку пропускали 2,7 л воды при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 5,4 л 0,47 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85 и получали по 61 мл каждого элюата.
[0075] Фракции, содержащие ЦДФ-холин, смешивали и в результате получали 2,85 л раствора, имеющего концентрацию ЦДФ-холина 42,8 г/л. Концентрация 5'-ЦМФ раствора составляла 0,01 г/л или меньше (соотношение 5'-ЦМФ к ЦДФ-холину 0,02% или меньше). Извлеченная доля ЦДФ-холина составила 91,7%. Из данных результатов находили, что способ получения настоящего изобретения также можно применять к раствору, содержащему цитидин-5'-дифосфатное соединение, полученное культуральным способом.
[0076] [Пример 12]
Схема органического синтеза ЦДФ-этаноламина приведена ниже. На приведенной ниже схеме реакций «кт» относится к комнатной температуре.
[0077] [Схема 1]
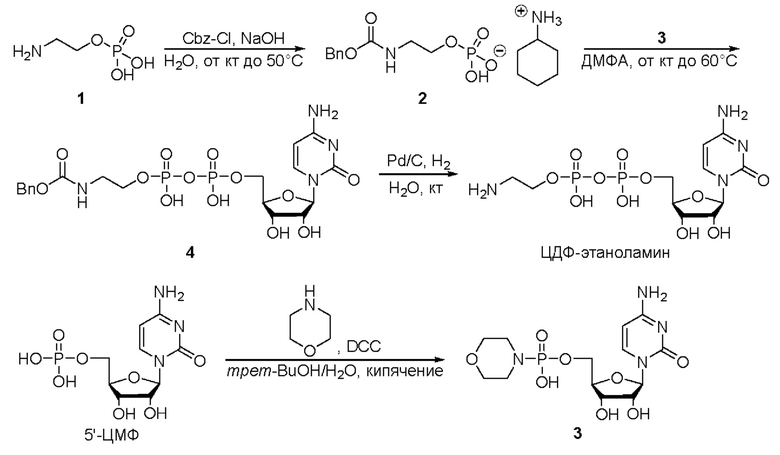
[0078] Синтез соединения 2 осуществляли со ссылкой на известную литературу (H.Ngo, M.F.Dunn et al. Biochemistry, 46, 7713, 2007; Т. Tanaka yakugakuzasshi, 80, 439, 1959.). К 18,9 мл воды добавляли 6,80 г гидроксида натрия (реагент специальной чистоты, изготовленный FUJIFILM Wako Pure Chemical Corporation) с последующим перемешиванием до полного растворения. После охлаждения раствора до 0°С добавляли 8,00 г фосфоэтаноламина (изготовленный Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием до растворения. К данному раствору по каплям добавляли 7,99 мл Z-хлорида (изготовленного Tokyo Chemical Industry Co., Ltd.) с последующим перемешиванием при комнатной температуре в течение 2 часов. Смесь дополнительно перемешивали при 50°С в течение 1 часа, и затем перемешивали в течение ночи при комнатной температуре. Жидкость, полученную добавлением к ней 1 л воды, пропускали через колонку с 850 мл сильнокислотной катионообменной смолы типа Н+. После прохождения через колонку проводили промывку водой для получения всего 5 л элюата. Жидкость концентрировали при пониженном давлении с получением 500 мл неочищенной жидкости с продуктом.
[0079] Неочищенную жидкость с продуктом нейтрализовали циклогексиламином (специальный сорт Wako, изготовленный FUJIFILM Wako Pure Chemical Corporation) до тех пор, пока рН не достигала 4,5, и затем растворитель полностью отгоняли при пониженном давлении. К выпавшему в осадок белому твердому веществу добавляли 98 мл воды и 28 мл этанола (реагент специальной чистоты, изготовленный FUJIFILM Wako Pure Chemical Corporation) и полностью растворяли при 66°С.Жидкость медленно охлаждали до комнатной температуры и оставляли на ночь. Осажденные белые кристаллы получали фильтрованием с отсасыванием и сушили в течение ночи при пониженном давлении. Выход составил 12,2 г.
[0080] Синтез соединения 3 осуществляли со ссылкой на известную литературу (K. Oertell, С.Е. McKenna, MF Goodman et al. Biochemistry, 53, 1842, 2014). К смешанному растворителю, состоящему из 16,8 мл трет-BuOH (изготовленному FUJIFILM Wako Pure Chemical Corporation) и 16,8 мл воды, добавляли 953 мг цитидин-5'-монофосфата и 0,77 мл морфолина (изготовленного FUJIFILM Wako Pure Chemical Corporation) и полностью растворяли при перемешивании при кипячении с обратным холодильником. 1,83 г N,N'-дициклогексилкарбодиимида (первичный сорт Wako, изготовленный FUJIFILM Wako Pure Chemical Corporation) растворяли в 19,3 мл трет-BuOH.
[0081] Одну восьмую раствора непрерывно добавляли к раствору цитидин-5'-монофосфата один раз каждые 15 минут. После добавления всего количества смесь дополнительно кипятили с обратным холодильником в течение 2,5 часов. После добавления приблизительно 50 мл воды к неочищенной жидкости с продуктом, охлажденной до комнатной температуры, образовавшееся белое твердое вещество удаляли фильтрацией с отсасыванием. Далее фильтрацию проводили с помощью мембранного фильтра с диаметром пор 0,45 мкм до тех пор, пока фильтрат не стал прозрачным. После отгонки растворителя при пониженном давлении добавляли ДМФ и снова отгоняли, и затем применяли полученный продукт в следующей реакции без очистки.
[0082] Синтез соединения 4 проводили со ссылкой на известную литературу. (Т. Tanaka et al. yakugakuzasshi, 85, 863, 1965). Добавляли 2,00 г ранее синтезированного соединения 2 и растворяли в 17 8 мл воды. Раствор пропускали через колонку с сильнокислотной катионообменной смолой типа Н+ для удаления циклогексиламина с последующей промывкой водой с получением в общей сложности 300 мл элюата. Затем воду отгоняли при пониженном давлении, добавляли к ней соответствующее количество ДМФ и снова отгоняли. ДМФ снова добавляли для растворения. Далее отдельно синтезированное соединение 3 растворяли в ДМФ, и затем оба соединения смешивали и перемешивали в течение ночи при комнатной температуре. На данной стадии применяли 16,2 мл ДМФ, включая тот, который применяли для промывки. На следующий день температуру повышали до 60°С, и смесь перемешивали в течение 5 часов для завершения реакции. После отгонки растворителя при пониженном давлении добавляли воду и снова отгоняли, и полученный продукт применяли для последующей реакции без очистки.
[0083] Синтез ЦДФ-этаноламина проводили со ссылкой на известную литературу (Т. Tanaka et al. yakugakuzasshi, 85, 863, 1965). К ранее синтезированному соединению 4 для растворения добавляли 11,2 мл воды. После замены атмосферы азотом добавляли 636 мг 5 мас. % Pd/C (тип STD для органического синтеза, изготовленный N.E. СНЕМСАТ) с последующим перемешиванием. Затем атмосферу заменяли водородом с последующим сильным перемешиванием при комнатной температуре в течение 4 часов. После того как атмосферу снова заменили азотом, Pd/C удаляли из реакционного раствора фильтрованием с отсасыванием. Далее оставшийся Pd/C удаляли с помощью мембранного фильтра с диаметром пор 0,45 мкм. К полученному таким образом фильтрату добавляли воду с получением 1020 мл раствора, содержащего цитидин-5'-дифосфатное соединение. В это время раствор, содержащий цитидин-5'-дифосфатное соединение, содержал ЦДФ-этаноламин при концентрации 1,17 г/л и 5'-ЦМФ при концентрации 0,0334 г/л (соотношение 5'-ЦМФ к ЦДФ-этаноламину 2,9%).
[0084] 1000 мл раствора, содержащего цитидин-5'-дифосфатное соединение, полученного как описано выше, пропускали через колонку со 150 мл РА412 ОН- типа при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 60°С, и 225 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 60°С, 1500 мл 0,5 моль/л водного раствора пропиновой кислоты пропускали через колонку при ОС=0,85, и получали 15,1 мл каждого элюата. Фракции, содержащие ЦДФ-этаноламин, смешивали и в результате получали 151 мл раствора с концентрацией ЦДФ-этаноламин 7,50 г/л. Концентрация 5'-ЦМФ раствора составляла 0,008 г/л (соотношение 5'-ЦМФ к ЦДФ-этаноламину 0,11%). Извлеченная доля ЦДФ-этаноламина составила 96,8%. Из данных результатов находили, что способ получения настоящего изобретения также можно применять к раствору ЦДФ-этаноламина, полученному способом синтеза.
[0085] [Сравнительный пример 4]
Получали 140 мл водного раствора, содержащего тринатриевую соль ЦДФ (Lot: В12560, изготовленная Combi-Blocks) при концентрации 6,67 г/л и 5'-ЦМФ при концентрации 0,43 г/л, и водный раствор пропускали через колонку со 100 мл ОН- типа Marathon А (изготовленная Dow Chemical Company) при ОС=1,25 для адсорбции. Затем, температуру снаружи колонки повышали до 40°С, и 150 мл воды пропускали через колонку при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, 1500 мл 0,50 моль/л водного раствора уксусной кислоты пропускали через колонку при ОС=0,85, и получали по 15,0 мл каждого элюата. Тринатривая соль ЦДФ не содержалась в любой фракции. Из данных результатов, находили, что способ получения настоящего изобретения нельзя применять для тринатриевой соли ЦДФ.
[0086] [Пример 13]
В качестве раствора, содержащего цитидин-5'-дифосфатное соединение, получали 140 мл водный раствор, содержащий ЦДФ-холин при концентрации 7,09 г/л и 5'-ЦМФ при концентрации 0,45 г/л (соотношение 5'-ЦМФ к ЦДФ-холину 6,3%), и водный раствор пропускали через колонку со 100 мл ОН-типа Marathon А (изготовленного Dow Chemical Company) при ОС=1,25 для адсорбции. Далее температуру снаружи колонки повышали до 40°С и пропускали через колонку 150 мл воды при ОС=1,10. Наконец, пока колонка поддерживалась при 40°С, через колонку пропускали 1000 мл 0,50 моль/л водного раствора уксусной кислоты при ОС=0,85 и получали по 10,0 мл каждого элюата. Фракции, содержащие ЦДФ-холин, смешивали и в результате получали 110 мл раствора с концентрацией ЦДФ-холина 8,06 г/л. Раствор не содержал 5'-ЦМФ, и извлеченная доля ЦДФ-холина составляла 89,3%.
[0087] Хотя настоящее изобретение было подробно описано со ссылкой на конкретные варианты осуществления, специалистам в данной области техники будет очевидно, что различные изменения и модификации можно вводить без отступления от сущности и объема настоящего изобретения. Настоящая заявка основана на международной заявке (РСТ/JP2021/031429), поданной 26 августа 2021 г., все содержание которой включено в настоящее изобретение посредством ссылки. Все ссылки, цитируемые в настоящем изобретении, включены в полном объеме.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ ДЛЯ НОРМАЛИЗАЦИИ ЦИКЛА СНА/БОДРСТВОВАНИЯ | 2003 |
|
RU2366428C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОЛОЧНОЙ КИСЛОТЫ | 2013 |
|
RU2643147C2 |
| БЛОК-СОПОЛИМЕР С ПОНИЖЕННЫМ СОДЕРЖАНИЕМ ПРИМЕСЕЙ, ПОЛИМЕРНЫЙ НОСИТЕЛЬ, ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ В ПОЛИМЕРНОЙ ФОРМЕ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2282641C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-A-ГЛИЦЕРОФОСФОРИЛХОЛИНА ФАРМАКОПЕЙНОГО КАЧЕСТВА | 2017 |
|
RU2635665C1 |
| ПИЩЕВЫЕ ИНГРЕДИЕНТЫ ИЗ STEVIA REBAUDIANA | 2017 |
|
RU2772126C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ Ga ВЫСОКОЙ ЧИСТОТЫ | 2011 |
|
RU2464043C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ПОДОБНЫХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2000 |
|
RU2234509C2 |
| СПОСОБ РЕГЕНЕРАЦИИ ФТОРИРОВАННЫХ АЛКАНОВЫХ КИСЛОТ ИЗ ОТРАБОТАННЫХ ВОД | 1999 |
|
RU2226186C2 |
| ИЗВЛЕЧЕНИЕ НИКЕЛЯ И КОБАЛЬТА С ИСПОЛЬЗОВАНИЕМ НЕПРЕРЫВНОГО ИОННОГО ОБМЕНА | 2013 |
|
RU2621504C2 |
| СПОСОБ РЕГЕНЕРАЦИИ ОСНОВНОЙ АНИОНООБМЕННОЙ СМОЛЫ | 2006 |
|
RU2388537C2 |
Настоящее изобретение относится к области органической химии, конкретно к технологии очистки цитидин-5'-дифосфатного соединения и его разделения от цитидин-5'-монофосфата (5'-ЦМФ). Способ получения цитидин-5'-дифосфатного соединения (5'-ЦДФ) с катионным заместителем включает стадию адсорбции путем контактирования раствора, содержащего 5'-ЦДФ с основной ионообменной смолой, и стадию получения элюата элюированием адсорбированного 5'-ЦДФ водным раствором органической кислоты, содержащей 2 или более атомов углерода. Техническим результатом изобретения является обеспечение способом получения 5'-ЦДФ, позволяющим эффективно удалять примеси нежелательного 5'-ЦМФ и концентрировать целевой продукт. 8 з.п. ф-лы, 3 ил., 1 табл., 13 пр.
1. Способ получения цитидин-5'-дифосфатного соединения, причем способ включает: следующие стадии (1) и (2):
(1) стадию приведения раствора, содержащего цитидин-5'-дифосфатное соединение, в контакт с основной ионообменной смолой для того, чтобы адсорбировать цитидин-5'-дифосфатное соединение на основной ионообменной смоле, и
(2) стадию получения элюата элюированием цитидин-5'-дифосфатного соединения, адсорбированного на основной ионообменной смоле, применяя водный раствор, содержащий органическую кислоту, содержащую 2 или более атомов углерода, где цитидин-5'-дифосфатное соединение представляет собой цитидин-5'-дифосфатное соединение, содержащее катионный заместитель.
2. Способ получения по п. 1, где концентрация цитидин-5'-дифосфатного соединения, содержащегося в элюате на стадии (2), является равной или большей, чем концентрация цитидин-5'-дифосфатного соединения в растворе, содержащем цитидин-5'-дифосфатное соединение на стадии (1).
3. Способ получения по п. 1 или 2, где на стадии (2), температура, при которой цитидин-5'-дифосфатное соединение элюируют с основной ионообменной смолы, составляет 20°С или более.
4. Способ получения по любому из пп. 1-3, где органическая кислота, содержащая 2 или более атомов углерода, представляет собой по меньшей мере одну органическую кислоту, выбранную из уксусной кислоты, пропионовой кислоты и масляной кислоты.
5. Способ получения по любому из пп. 1-4, где на стадии (2) концентрация органической кислоты, содержащейся в водном растворе, составляет 0,1 моль/л или более.
6. Способ получения по любому из пп. 1-5, где цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой соединение, в котором соединены цитидин-5'-дифосфат и катионный заместитель.
7. Способ получения по любому из пп. 1-6, где цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой соединение, в котором катионный заместитель соединен с β-фосфатной группой цитидин-5'-дифосфата.
8. Способ получения по любому из пп. 1-7, где органическая кислота, содержащая 2 или более атомов углерода, представляет собой карбоновую кислоту, содержащую 2 или более атомов углерода.
9. Способ получения по любому из пп. 1-8, где цитидин-5'-дифосфатное соединение, содержащее катионный заместитель, представляет собой по меньшей мере одно, выбранное из цитидин-5'-дифосфатхолина и цитидин-5'-дифосфатэтаноламина.
| Kennedy E | |||
| THE SYNTHESIS OF CYTIDINE DIPHOSPHATE CHOLINE, CYTIDINE DIPHOSPHATE ETHANOLAMINE, AND RELATED COMPOUNDS | |||
| J | |||
| Biol Chem., 222(1), Sep | |||
| Приспособление для строгания деревянных полов, устраняющее работу на коленях | 1925 |
|
SU1956A1 |
| Способ укрепления под покрышкой пневматической шины предохранительного слоя или манжеты | 1917 |
|
SU185A1 |
| Koerner J.F | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Jor | |||
| OF BIOLOGICAL CHEMISTRY, v | |||
| Упругая металлическая шина для велосипедных колес | 1921 |
|
SU235A1 |
| Котел для игрушек | 1922 |
|
SU2688A1 |
Авторы
Даты
2025-04-01—Публикация
2022-08-26—Подача