Группа изобретений относится к органической химии, а именно к новому химическому соединению [4-(диметиламинофенил)(2-хлорэтокси)фосфонил]ме-тангидразиду (ДМАФМГ), обладающему биологической активностью, и способу его получения.
Заявляемое химическое соединение является гидразидом фосфорилированной муравьиной кислоты и по окружению атома фосфора относится к ряду фосфонатов.
Из уровня техники известен дифенилфосфинилметангидразид (ДФФМГ) формулы Ph2P(0)C(0)NHNH2, также являющийся гидразидом муравьиной кислоты, но относящийся к ряду оксидов третичных фосфинов, и обладающий биологической активностью, которая включает анксиолитическую и противовоспалительную активность и способность корригировать нарушенное поведение при аутизме (патент RU 2783121, С07С 243/26, C07F 9/50, А61К 31/662, А61Р 29/00, А61Р 25/00, опубл. 2022 г.).
ДФФМГ имеет узкий спектр биологической активности, в частности, не обладает способностью улучшать процессы памяти и когнитивные функции.
Способ получения ДФФМГ заключается в том, что ведут взаимодействие этилдифенилфосфинита с этилхлорметаноатом при температуре 70°С до прекращения выделения этилхлорида, полученный этилдифенилфосфинилметаноат при температуре 50°С вводят в реакцию в этаноле с гидразин-гидратом, взятым в избытке, с последующим удалением легколетучих компонентов в вакууме и перекристаллизацией из диоксана (патент RU 2783121, С07С 243/26, C07F 9/50, А61К 31/662, А61Р 29/00, А61Р 25/00, опуб. 2022 г.).
Недостатками метода являются необходимость предварительного синтеза промежуточного этилдифенилфосфинита в инертной атмосфере с использованием основания и большого объема растворителя, а также последующая утилизация соли амина.
Наиболее близким к [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангид-разиду (ДМАФМГ) по технической сущности является [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]этангидразид фосфинатного строения - гидразид [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]уксусной кислоты, называемый «САРАН» или «КАПАХ» формулы
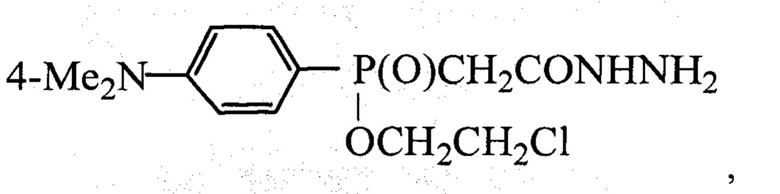
обладающий ноотропным, антидепрессивным действием (патент RU 2141961, C07F 9/32, А61К 31/66, 31/675, опубл. 1999 г.).
Недостатком известного химического соединения является узкий спектр нейропсихотропной активности, в частности отсутствие способности улучшать когнитивные функции в состоянии стресса.
Аналоги «КАПАХ», которые являются гидразидами муравьиной кислоты, ранее не были описаны в литературе.
[(4-Диметиламинофенил)(2-хлорэтокси)фосфонил]этангидразид («КАПАХ») получают взаимодействием (4-диметиламинофенил)дихлорфосфина с этиленоксидом и последующей обработкой промежуточного фосфонита этилхлорацетатом и образовавшегося прекурсора гидразин-гидратом. Этот процесс основывается на сведениях, описанных в патенте РФ №2141961 (1999), по получению соединения, и реализуется по следующей реакционной схеме:
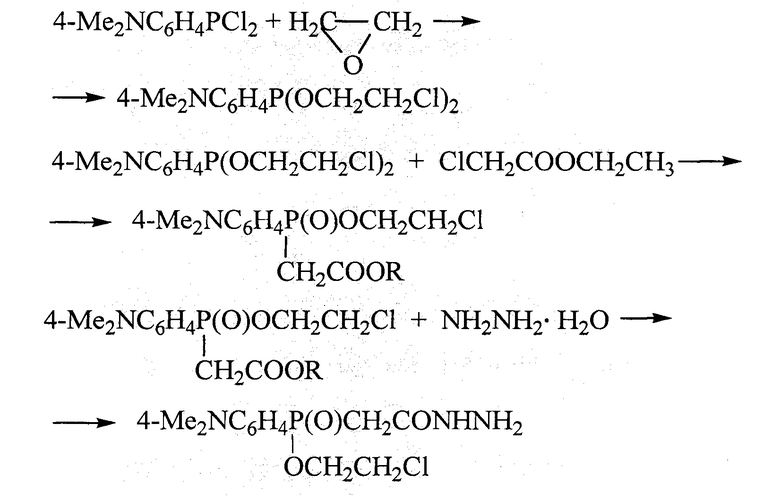
Недостатком указанного способа является использование в качестве источника 2-хлорэтоксильной группы оксида этилена в газообразном или в жидком виде, который представляет опасность в связи с его высокой летучестью, взрыво-, пожароопасностью и сильной специфической ядовитостью [A.J. Spezialle, R. С.Freeman, J. Org. Chem., 1958, 23, 1883].
Технической проблемой является разработка нового химического соединения, обладающего высокой биологической активностью для коррекции нарушений неврологических и психических функций мозга.
Техническая проблема решается новым химическим соединением - [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразидом (ДМАФМГ) формулы
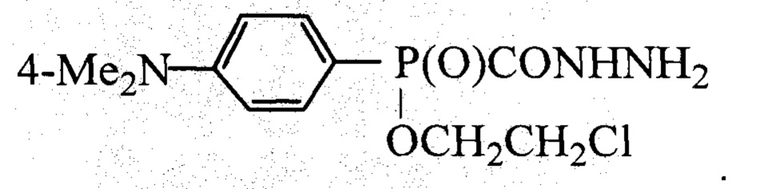
Техническая проблема решается способом получения [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразида, в котором сначала взаимодействием (4-диметиламинофенил)дихлорфосфина, 1,1-(2-хлорэтокси)этоксиэтана и метилхлорметаноата в толуоле при комнатной температуре получают метил [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метаноат, который затем вводят в реакцию с избытком гидразин-гидрата в диоксане при температуре 15-20°С с последующим удалением легколетучих компонентов в вакууме и перекристаллизацией полученного [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразида из диоксана.
Решение технической проблемы позволяет получить ДМАФМГ обладающий высокой биологической активностью безопасным способом. [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразид с токсичностью, сопоставимой с таковой у «КАПАХ» (прототип), обладает более высокой эффективностью, улучшая когнитивные функции, в том числе, и в состоянии стресса. По сравнению с «КАПАХ» и эталонными препаратами ДМАФМГ имеет более широкий спектр нейропсихотропной активности. Биологическая активность ДМАФМГ включает способность улучшать когнитивные функции и память, снижать состояние тревоги при нарушении функций мозга, а также корригировать дефицит социального и устранять симптомы стереотипного поведения при аутизме.
Краткая характеристика веществ, используемых для синтеза заявленного вещества:
[4-(Диметиламино)фенил]дихлорфосфин 4-Ме2NC6Н4РСl2 - кристаллическое вещество с температурой плавления 66°С и температурой кипения 185-186°С при давлении 15 мм рт.ст.
1,1-(2-Хлорэтокси)этоксиэтан - бесцветная прозрачная жидкость с температурой кипения 46-47°С при давлении 10 мм рт.ст.
Метилхлорметаноат - бесцветная жидкость, смешивается с бензолом, хлороформом, диэтиловым эфиром, этанолом. Нерастворим в воде. Молярная масса: 94,49 г/моль. Плотность: 1,236 г/см. Температура кипения 71,4°С.
Гидразин NH2NH2 - бесцветная, сильно гигроскопичная жидкость, с неприятным запахом. Смешивается в любых соотношениях с водой, жидким аммиаком, этанолом; плохо растворяется в неполярных растворителях. Плотность - 1,01 г/см3, температура кипения 114°С, температура плавления 2°С.
Синтез [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразида реализуется по следующей схеме:
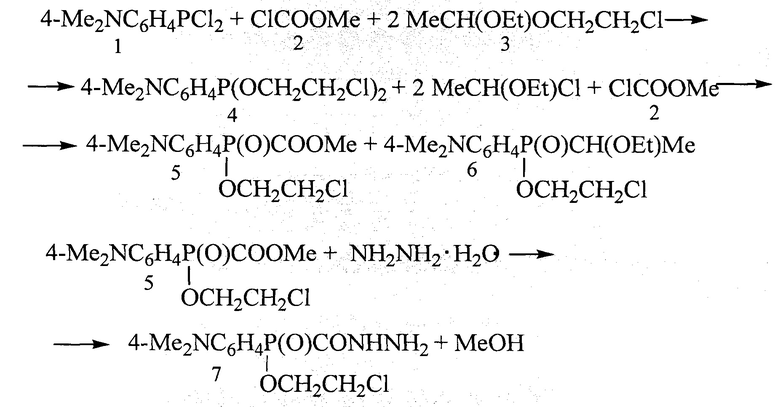
При взаимодействии (4-диметиламинофенил)дихлорфосфина 1 с 1,1-(2-хлорэтокси)этоксиэтаном 3-новым (2-хлорэтокси)лирующим реагентом, образуется промежуточный фосфонит 4, реакция которого с метилхлорметаноатом 2 приводит к образованию метил[(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метаноата 5. Далее при взаимодействии соединения 5 с гидразин-гидратом образуется ДМАФМГ 7.
Данное изобретение иллюстрирует следующий пример конкретного выполнения.
В колбу загружали 15 мл толуола, 3,31 г (14,9 ммоль) (4-диметиламинофенил)дихлорфосфина 1 и 2,83 г (30 ммоль) метилхлорметаноата 2, к полученной смеси при перемешивании добавляли по каплям 4,58 г (30 ммоль) 1,1-(2-хлорэтокси)этоксиэтана 3, поддерживая температуру реакционной смеси 20°С. Для завершения реакции реакционную смесь выдерживали при комнатной температуре в течение 28 часов до полного израсходования (4-диметиламинофенил)дихлорфосфина 1, что определяли по исчезновению в спектре ЯМР 31Р реакционной массы резонансного сигнала атома фосфора исходного дихлорфосфина 1 при δP 166.7 м.д. По окончании реакции растворитель и другие легколетучие компоненты удаляли в вакууме (10 мм рт.ст.). В спектре ЯМР 31Р кристаллического остатка обнаруживали резонансный сигнал при δP 19.07 м.д. (соединение 5, 85%) и δP 42.03, 41.1 м.д. (соединение 6, 6%). Для удаления последнего кристаллический остаток промывали горячим гексаном и фильтрованием получали 3.9 г метил[(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метаноата 5. Белые кристаллы с температурой плавления 112-113°С. Выход продукта составил 86%.
Структуру соединения 5 подтверждали спектрами ЯМР на ядрах 1H и 31Р и элементным анализом.
Спектры ЯМР 1Н регистрировали на спектрометрах «Tesla BS-567A» (рабочая частота 100 МГц) и «Вruker AVANCE 400 WB» (рабочая частота 400.13 МГц). Спектры ЯМР 31Р регистрировали на приборе «Вгикег MSL-400» с рабочей частотой 162 МГц. Химические сдвиги ядер водорода и углерода указаны относительно ТМС, фосфора - 85%-ной Н2РO4. Спектры ЯМР записывали при 20°С.
Температуры плавления определяли в стеклянных капиллярах на приборе «StuartSMP10».
Элементный анализ проводили на анализаторе «Еuro ЕА3000 CHNS-О» («EuroVectorS.p.A.», Милан, Италия).
Содержание фосфора определяли методом пиролиза на несерийном приборе.
Спектр ЯМР 1Н соединения 5 (100 МГц, CDCl3, δ, м.д., J/Гц): 2,87 с (6Н, Me2N); 3.61 с (3Н, ОМе); 3.58 дт (2Н, СН2Сl, 3JHH 6.0, 4JPH 2.4); 4.23 дт (2Н. РОСН2, 3JHH 6.0, 3JPH 8.0); 6.58 дд (2Н, м-СНAr, 3JHH 8.8); 7.55 дд (2Н, о-СНAr, 3JHH 8.8, 3JPH 12.0). Спектр ЯМР 31Р (CDCl3, δ, м.д.): 18.5.
Элементный анализ. Найдено, %: Р 9.88; N 4.72. C12H17NClO4P. Вычислено, %: Р 10.13; N4.58.
Затем 2.9 г (9.5 ммоль) метил[(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метаноата 5 растворяли в 15 мл диоксана при температуре 15-20°С и при перемешивании добавляли по каплям 0.75 г (15 ммоль) гидразин-гидрата. Для завершения реакции реакционную смесь выдерживали при комнатной температуре в течение 24 часов. Завершение реакции определяли по исчезновению в спектре ЯМР 31Р реакционной массы резонансного сигнала атома фосфора при δP 18.5 м.д.. Растворитель и другие легколетучие компоненты удаляли в вакууме. Остаток перекристаллизовывали из диоксана.
Получали 2.3 г [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразида 7 с температурой плавления 127-128°С. Выход продукта составил 81%.
Структуру ДМАФМГ подтверждали спектрами ЯМР на ядрах 1Н, 31Р и элементным анализом.
Спектр ЯМР 'Н ДМАФМГ (CDCl3, δ, м.д., J/Гц): 3,02 с (6Н, NMe2); 3,72 д.т. (2Н, СН2Сl, 3JHH 6,2; %, 2,0); 4,07 уш. с (2Н, NH2); 4,26 м (2Н, ОСН2); 6,70 д.д. (2Н, мета-СНAr, 3JHH 8.9, 3JPH 3.3); 7,75 д.д. (2H, орто-СНAr, 3J™ 8.9, 3Jpн 11.7); 9,1 уш.с (1H, NH). Спектр ЯМР31Р: δр 17,67 м.д.
Элементный анализ. Найдено, %: Р 9.90; N 13.89. C11H17N3CIO3P. Вычислено, %: Р 10.13; N 13.75.
Полученный ДМАФМГ исследовали на биологическую активность.
Токсичность и наличие у [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метан-гидразида биологической активности, включающей способность улучшать процессы обучения, а также корригировать нарушенное поведение при аутизме, были выявлены при проведении экспериментальных исследований, выполненных на кафедре фармакологии ФГБОУ ВО «Казанского государственного медицинского университета» Министерства здравоохранения Российской Федерации.
Полученные результаты обрабатывали статистически по стандартной методике с использованием t-критерия Стьюдента (доверительная вероятность составляла 0,95 (р<0,05), после проверки полученных данных на нормальность распределения в сравниваемых группах при помощи программы Graph Pad Prism 8.0.1.
Острая токсичность ЛД50(мг/кг) ДМАФМГ и препарата сравнения КАПАХ была оценена при внутрибрюшинном введении их белым нелинейным мышам-самцам массой 18-22 г, которые вводили в виде водного раствора из расчета 0,1 мл на 10 г массы животного в возрастающих дозах.

Средние смертельные дозы (ЛД50) ДМАФМГ и КАПАХ практически не различаются и для крыс, и для мышей.
Общая картина при определении «острой» токсичности в летальных дозах - общее угнетение, частое поверхностное дыхание, снижение двигательной активности.
Исследование биологической активности проводили в дозах, составляющих 1/100 от ДЛ50 (10 мг/кг) при многократном применении (количество дней указано в таблицах). Препараты сравнения (рефренс-препараты) исследовали в стандартных дозах, описанных в научной литературе.
Для выявления способности соединений улучшать память, обучаемость и когнитивные функции были использованы следующие тесты:
А) Тест «Водный лабиринт Морриса» использовали для исследования процессов памяти и когнитивных функций. Установка представляет собой круглый бассейн (диаметр 1,5 м, глубина - 0,6 м), заполненный водой (+25°С). В одном из секторов бассейна на глубине 1,5-2 см под водой находится скрытая платформа (10 × 10 см), расположение которой на этапе обучения неизменно. Воду перед началом эксперимента подкрашивали обезжиренным молочным порошком, чтобы животное не видело установленную платформу и полагалось только на память. Метод основан на том, что животное должно найти кратчайший путь в бассейне с водой до спрятанной спасательной платформы на основании знаний о ее местонахождении, полученных в процессе обучения. Для ориентации животных в бассейне использовали 4 черно-белых визуальных ориентира, которые устанавливали на борта бассейна на равноудаленном расстоянии по сторонам света - север, юг, запад, восток. Таким образом, расстояние от точки старта до спасительной платформы было приблизительно равным. Тест состоит из двух этапов.
Первый этап (обучения) необходим для формирования и закрепления у животных понимания расположения спасительной платформы в пространстве. Для этого в течение 3-х последовательных дней, по 3 сессии в день исследуемое животное осторожно опускали в воду поочередно возле каждого из 3 ориентиров (мордочкой к данному ориентиру) и в течение 60 секунд позволяли самостоятельно искать платформу. Если в течение этого времени крыса ее не находила, то была аккуратно туда направлена. Когда животное забиралось на платформу, ему позволяли посидеть на ней 15 с, после ее чего перемещали клетку для просушки.
Второй этап (тестирование) был проведен на 4 день (после этапа обучения) и служит способом проверки показателей памяти. Для этого спасительную платформу убирали из установки и течение 1 минуты регистрировали время нахождения животного в зоне, где ранее располагалась платформа. При нормальном состоянии процессов памяти и когнитивных функций животное больше времени пребывало в зоне прежнего расположения платформы.
Б) Тест «Экстраполяционное избавление» позволяет оценить когнитивные функции в состоянии стресса. Установка (НПК «Открытая наука», Россия) представляет собой емкость (высотой 35 см, диаметром 23 см) наполненную водой с прозрачным сосудом в центре (диаметр 9,2 см), который не касается стенок и погружен в воду (21°С) на 2 см. Суть методики заключается в помещении испытуемого животного в стрессовые условия (ограниченное водное пространством центрального цилиндра), из которых нужно найти верный выход - т.е. поднырнуть под его край. Чем быстрее животное это понимает, тем лучше ее когнитивные функции. Кроме того, данная методика позволяет выявить расположенность к тревожному поведению - безуспешные попытки выпрыгнуть или вскарабкаться на верхний край цилиндра наблюдаются исключительно у крыс с повышенным уровнем эмоциональной реактивности. За 2 минуты теста учитывали:
1. Количество прыжков животного, что отражает общий уровень стресса, т.е. чем больше прыжков - тем больше уровень стресса;
2. Латентный период двигательной активности (с) - время с момента начала эксперимента до первого движения, что отражает общее состояние когнитивных функций в стресогенных условиях;
3. Продолжительность времени до подныривания - увеличение данного показателя отражает снижение когнитивных функций в стрессовых условиях.
Для регистрации поведенческих реакций использовали систему «EthoVisionXT» (Noldus, Нидерланды) с автоматическим способом анализа треков.
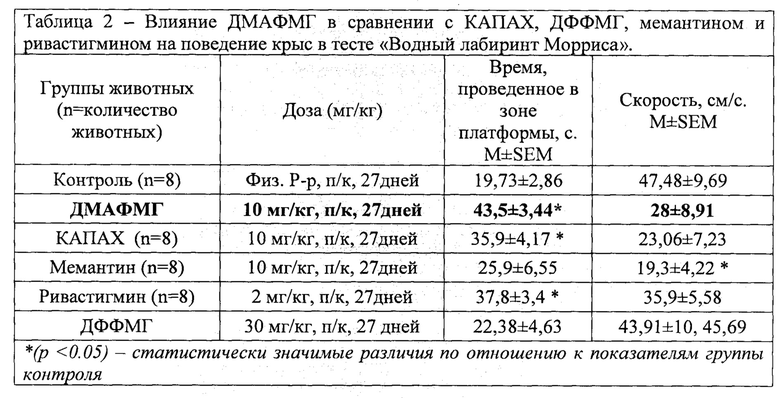
Результаты исследования ДМАФМГ в тесте «Водный лабиринт Морриса» в сравнении со структурными аналогами КАПАХ и ДФФМГ (патент RU 2783121, С07С 243/26, C07F 9/50, А61К 31/662, А61Р 29/00, А61Р 25/00, опуб. 2022 г.), а также рефренс-препаратами, применяемыми в клинике для улучшения когнитивных функций, представлены в табл. 2. Улучшение когнитивных функций выражалось в увеличении времени плавания крыс в зоне платформы. Как видно из таблицы, самые высокие показатели отмечены после 27-дневного введения ДМАФМГ (увеличение времени плавания в зоне платформы в 2,3 раза, р<0,05, по сравнению с группой контроля; КАПАХ - в 1,8 раза, р<0,05). ДФФМГ не проявил активности.
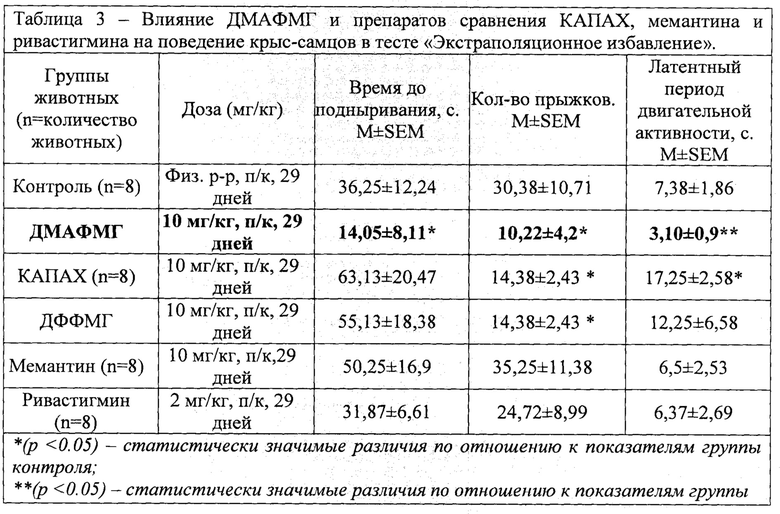
Результаты изучения когнитивных функций в состоянии стресса показали преимущества ДМАФМГ как перед КАПАХ, так и перед препаратами сравнения (табл. 3). Только ДМАФМГ уменьшал продолжительность времени до подныривания, что свидетельствует об улучшении ими когнитивных функций у крыс, оказавшихся в состоянии стресса (замкнутый цилиндр в воде). Кроме того, ДМАФМГ также как КАПАХ и ДФФМГ, снижал и состояние тревожности при стрессе - уменьшение количества прыжков.
В качестве модели расстройств аутистического спектра (РАС) была использована вальпроатная модель аутизма (ВМА) у крыс. В качестве препаратов сравнения использовали КАПАХ, а также препараты, применяемые для коррекции поведения в клинике - антидепрессант амитриптилин и нейролептик рисперидон.
Для изучения способности ДМАФМГ корригировать нарушенное поведение при аутизме использовали несколько методов.
Основным нарушением поведения при аутизме является дефицит социального поведения. «Трехкамерный социальный тест» считается оптимальным вариантом для изучения социального поведения грызунов и основан на их естественном стремлении контактировать с другими особями, или же проявлять интерес к новому объекту. Установка «Трехкамерный социальный тест» представляет собой бокс из 2 боковых (20×40 см) и 1 центрального (20×60) отсеков. В каждом боковом отсеке имеются пластиковые контейнеры - ограждения с отверстиями, ограничивающие передвижение животных, не позволяющие проявлять агрессию, но предполагающие социальный интерес (обнюхивания и тактильный контакт). Тест состоит из 3 последовательных сессий. В 1 сессию испытуемое животное помещается в центральный отсек и в течение 10 минут мог свободно исследовать установку (адаптация), после его забирали для очищения модели. Во 2 сессию в ограждение одного из боковых отсеков помещали незнакомое животное того же возраста и пола, ранее никогда не контактировавшее с испытуемым животным, а в центральный осек возвращали исследуемую крысу. В течение последующих 10 минут регистрировали время (с) нахождения животного в камере с социальным (крысой) или несоциальным объектом (элементом сетчатого заграждения). По окончанию 2 сессии испытуемое животное отсаживали, проводили уборку камер. Далее, следовала 3 сессия эксперимента, в ходе которой в оставшийся боковой отсек помещали новое «незнакомое» животное, а животное из 2 сессии становилось «знакомым» и после возвращения исследуемого грызуна в центральный отсек регистрировали время, проведенное в камере то с тем или иным животным. Считается, что уровень тревожности и асоциальное™ будет обратно пропорционален времени, проведенного испытуемого животного с ранее не знакомым несоциальным (2 сессия) или социальным (3 сессия) объектом.
Результаты экспериментов второй сессии представлены в табл. 4. Крысы должны выбирать между социальным объектом (незнакомая крыса) и несоциальным (неодушевленный предмет). Нормальные животные, с ненарушенным социальным поведением, предпочитают больше времени проводить с социальным объектом, т.е., с незнакомой крысой. Крысы в модели аутизма статистически меньше времени проводили с социальным объектом. Следует подчеркнуть, что в этой серии из всех применяемых веществ только ДМАФМГ корригировало дефицит социального поведения до уровня контрольных значений.
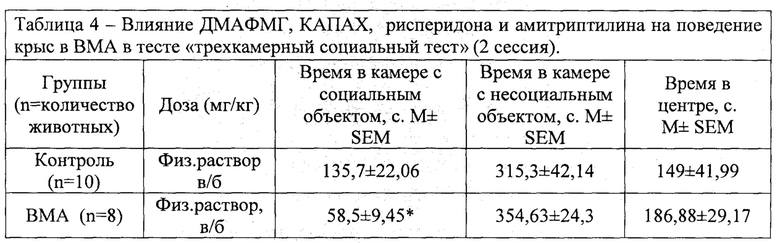

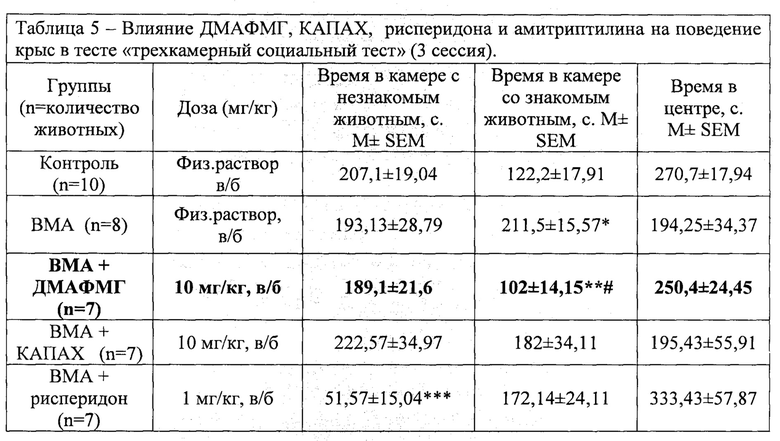
Результаты показателей социального поведения в 3-ю сессию опыта (табл. 5) выявили нарушения у крыс в модели аутизма - последние предпочитали больше времени находиться в отсеке со знакомым животным (в норме - крысы должны больше контактировать со незнакомым). Все исследуемые вещества корригировали продолжительность контакта со знакомой крысой до уровня контрольных животных. Что касается ДМАФМГ - его эффективность в этой сессии значительно выше, чем у других препаратов, поскольку продолжительность контакта со знакомым животным статистически значимо (в 2,1 раза, р<0,05) выше, чем у нелеченых крыс с аутизмом.

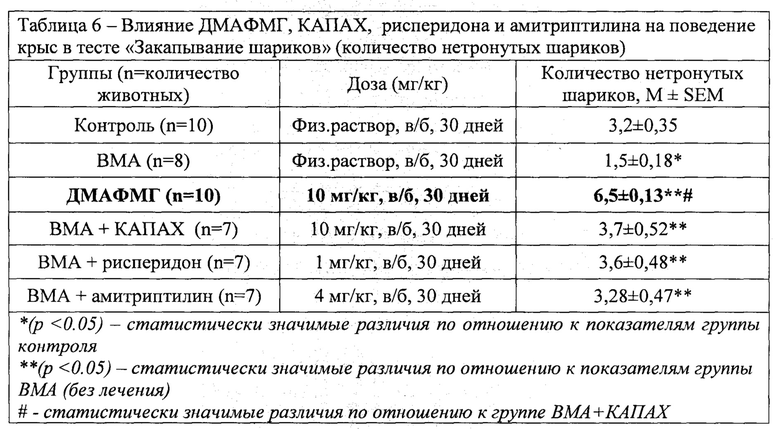
Метод оценки обсессивно-компульсивного расстройства у крыс, связанного с навязчивыми идеями и действиями, является еще одним показателем нарушения поведения при аутизме. Это расстройство у крыс позволяет оценить тест «Закапывание шариков». Животное помещали в подготовленную клетку с шариками и оставляли на 30 мин., после чего аккуратно извлекали и проводили подсчет шариков, закопанных более чем на 2/3. Количество закопанных шариков отражает выраженность стереотипного поведения животного - чем больше закопанных шариков, тем выше уровень стереотипности.
Результаты эксперимента представлены в табл. 6. При введении ДМАФМГ наблюдалось уменьшение количества закопанных шариков по сравнению с крысами группы без лечения. Следует отметить, что этот показатель эффективности превышал результаты у КАПАХ и других веществ. Это свидетельствует о наличии у ДМАФМГ положительного влияния на один из основных симптомов аутизма - стереотипное поведение.
Учитывая, что одним из основных факторов нарушения социального поведения при аутизме является тревожность, была проведена оценка поведения крыс в модели аутизма с использованием теста «Приподнятый крестообразный лабиринт» (ПКЛ), который позиционируется как наиболее чувствительный при исследовании тревожного поведения грызунов.
Тест является информативной методикой, позволяющей адекватно оценивать биологическое действие потенциальных лекарственных средств и позиционируется как одна из наиболее чувствительных моделей для исследования тревожности животного. В этом тесте оценивают степень выраженности эмоциональной реакции страха и тревоги.
К регистрируемым в "Приподнятом крестообразном лабиринте" показателям уровня тревожности относят длительность пребывания животных в «открытых» и «закрытых» рукавах лабиринта. Чем меньше у животного выражена реакция тревоги, тем больший период времени наблюдения оно проводит в открытых рукавах и реже посещает закрытые. Увеличение времени нахождения в открытых рукавах характеризует о наличии анксиолитической активности у исследуемых соединений.

Результаты оценки уровня тревожности крыс в ВМА демонстрируют ее повышенный уровень. КАПАХ корригирует этот уровень до значений контрольной группы, а ДМАФМГ превосходит анксиолитическое действие КАПАХ, статистически значимо повышая длительность нахождения в ОР по сравнению с «нелечеными» крысами.
Таким образом, сравнительная оценка биологической активности ДМАФМГ с ближайшим аналогом - [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]-этангидразидом (КАПАХ), представленная экспериментальными результатами, свидетельствует о его преимуществах: имея токсичность, сопоставимую с таковой у КАПАХ и структурным аналогом ДФФМГ, обладает более высокой эффективностью, улучшая когнитивные функции, в том числе, и в состоянии стресса. По сравнению со структурными аналогами и эталонными препаратами заявленное вещество имеет более широкий спектр нейропсихотропной активности, в том числе, при коррекции поведения крыс в модели аутизма, что позволяет позиционировать ДМАФМГ как потенциальное лекарственное средство для улучшения когнитивных функций и памяти, снижения состояния тревоги при нарушении функций мозга, а также коррекции дефицита социального и устранения симптомов стереотипного поведения при аутизме.
| название | год | авторы | номер документа |
|---|---|---|---|
| Дифенилфосфинилметангидразид, обладающий биологической активностью, и способ его получения | 2021 |
|
RU2783121C1 |
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ РАССТРОЙСТВ АУТИСТИЧЕСКОГО СПЕКТРА | 2017 |
|
RU2666598C1 |
| АНТИДЕПРЕССАНТНОЕ СРЕДСТВО ДЛЯ КОРРЕКЦИИ НЕЖЕЛАТЕЛЬНЫХ ПОБОЧНЫХ ЭФФЕКТОВ НЕЙРОЛЕПТИКОВ | 2019 |
|
RU2746012C2 |
| СПОСОБ ТЕСТИРОВАНИЯ ПРЕПАРАТОВ С ПРЕДПОЛАГАЕМЫМ ПСИХОТРОПНЫМ ИЛИ АКТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2015 |
|
RU2601376C1 |
| ПРОИЗВОДНОЕ 4-ФЕНИЛПИРРОЛИДИНОНА-2, СОДЕРЖАЩАЯ ЕГО КОМПОЗИЦИЯ С НООТРОПНОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ НАРУШЕНИЙ НЕРВНОЙ СИСТЕМЫ | 2015 |
|
RU2611623C2 |
| Способ моделирования энцефалопатии у потомства при воздействии нетоксичных доз марганца в пренатальный период | 2022 |
|
RU2794816C1 |
| Состав для изготовления драже | 2017 |
|
RU2650548C1 |
| СПОСОБ КОРРЕКЦИИ АГРЕССИВНОГО ПОВЕДЕНИЯ, ВЫЗВАННОГО ХРОНИЧЕСКИМ УМЕРЕННЫМ СТРЕССОМ | 2019 |
|
RU2714934C1 |
| 11-(4-трет-Бутилбензил)- и фенацилзамещённые 2, 3, 4, 5-тетрагидро[1, 3]диазепино [1, 2-а]бензимидазола, обладающие анксиолитической активностью | 2016 |
|
RU2629022C1 |
| ЛИТИЯ БЕТА-ФЕНИЛ-ГАММА-АМИНОБУТИРАТ КАК НОРМОТИМИЧЕСКОЕ СРЕДСТВО | 2017 |
|
RU2677879C1 |
Изобретение относится к соединению [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразиду формулы 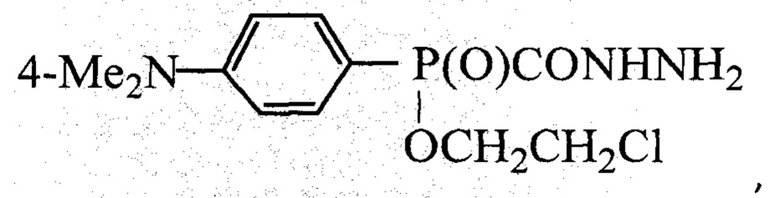 а также к способу его получения для улучшения когнитивных функций и памяти, снижения состояния тревоги при нарушении функций мозга, а также для корригирования дефицита социального и устранения симптомов стереотипного поведения при аутизме. Технический результат: получено новое соединение, обладающее биологической активностью для коррекции нарушений неврологических и психических функций мозга. 2 н. и 1 з.п. ф-лы, 7 табл., 1 пр.
а также к способу его получения для улучшения когнитивных функций и памяти, снижения состояния тревоги при нарушении функций мозга, а также для корригирования дефицита социального и устранения симптомов стереотипного поведения при аутизме. Технический результат: получено новое соединение, обладающее биологической активностью для коррекции нарушений неврологических и психических функций мозга. 2 н. и 1 з.п. ф-лы, 7 табл., 1 пр.
1. [4-(Диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразид формулы
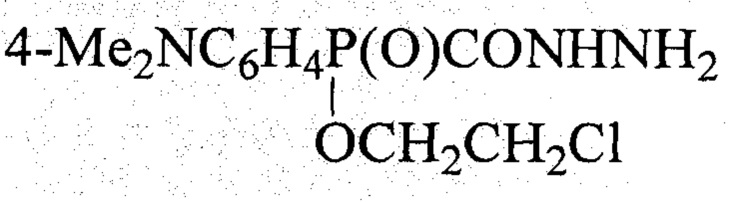
2. [4-(Диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразид по п. 1, обладающий биологической активностью, включающей способность улучшать когнитивные функции и память, проявлять противотревожное действие при нарушении функций мозга, корригировать поведенческий дефицит при аутизме.
3. Способ получения [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразида по п. 1, характеризующийся тем, что сначала взаимодействием (4-диметиламинофенил)дихлорфосфина, 1,1-(2-хлорэтокси)этоксиэтана и метилхлорметаноата в толуоле при комнатной температуре получают метил[(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метаноат, который затем вводят в реакцию с избытком гидразин-гидрата в диоксане при температуре 15-20°С с последующим удалением легколетучих компонентов в вакууме и перекристаллизацией полученного [(4-диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразида из диоксана.
| Дифенилфосфинилметангидразид, обладающий биологической активностью, и способ его получения | 2021 |
|
RU2783121C1 |
| Способ получения дифенилфосфинилметангидразида | 2023 |
|
RU2799966C1 |
| ЭФИРЫ ФОСФИНОВЫХ КИСЛОТ ИЛИ ИХ ФИЗИОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ ОБМЕННЫХ ПРОЦЕССОВ МОЗГА | 1994 |
|
RU2141961C1 |
| US 4162311 A, 24.07.1979 | |||
| US 5679663 A, 21.10.1997. | |||
Авторы
Даты
2025-04-11—Публикация
2024-06-17—Подача