Изобретение касается гидразидов фосфорилированных карбоновых кислот, обладающих терапевтической активностью, в частности при лечении депрессии и при коррекции врожденных и приобретенных неврологических дефицитов, например при нарушениях памяти, обучения, внимания, интегративных функций мозга.
Известны гидразиды фосфорилированных карбоновых кислот со структурой R1R2P(O)CH2C(O)NHNH2, где радикалы R1 и R2 могут быть фенильной, п-толильной, этильной, этоксисодержащей и бутоксисодержащей группами или их N-замещенными производными (Разумов А.И., Позняк Р.Л., Брудная К.Б., Берим М.Г., Слепова Р. И. , Туктарова Ш.З., Ржевская Г.Ф. //Журн. общей химии, 1967, т. 37, с. 421 - 424). Эти гидразиды характеризуются низким уровнем противомикробной активности. Описан также гидразид дифенилфосфинилуксусной кислоты дифенилфосфинилацетогидразид, далее называемй ДФАГ, (C6H5)2P(O)CH2C(O)NHNH2,
который обладает вегетотропным, противоэпилептическим и антисеротониновым свойствами (Разумов А.И., Тарасова Р.И., Николаева В.Г., Яфарова Р.Л. //A.с. СССР N 467593, кл. C 07 F 9/50; БИ 1976, N 14), (Разумов А.И., Заиконникова И.В. и др. //A.с. СССР N 741876, кл. A 61 K 32/42; БИ 1980, N 23). Некоторые гидразиды фосфорилированных уксусных кислот показали низкий уровень нейротропной активности (Журавлева Г.Г., Исмагилов Р.К., Колла В.Э. //Хим.-фарм. журнал, 1978, т.12, c. 79 - 83; Исмагилов Р.К., Разумов А.И., Журавлева Г.Г. , Зыкова Т.В., Яфарова Р.Л., Безбородова Т.А. //Хим.-фарм. журнал, 1982, т. 16, с. 296 - 300).
Хорошо известно, что пациенты, страдающие нейродегенеративными заболеваниями, например болезнью Альцгеймера и болезнью Паркинсона или страдающие нарушениями умственной деятельности вследствие черепно-мозговых травм, нейроинфекций, отравлений, или страдающие расстройствами мозгового кровообращения различного генеза, часто характеризуются также наличием различной степени астенических и депрессивных состояний в пределах от слабой тревоги до сильной депрессии. Такие пациенты реагируют на терапию нейротропными препаратами и, в частности, на терапию ноотропными препаратами и антидепрессантами.
Задачей настоящего изобретения является расширение арсенала лекарственных средств, пригодных для использования в этих областях; установлено, например, что ранее неизвестное соединение (2-хлорэтокси) (4'-N,N-диметиламинофенил)фосфинилацетогидразида формулы I, где X - 4-(CH3)2N, Y-Cl, n = 1, n' = 2, R1 = R2 = H и R3 = R4 = H) является сильнодействующим нейротропным веществом и, в частности, обнаруживает антидепрессантную и ноотропную активность.
Поставленная задача решается синтезом соединений со следующей общей формулой I: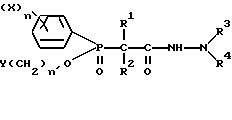
в которой каждый радикал X отдельно представляет собой галогенсодержащую группу, гидроксигруппу, C1-4-алкильную группу, C1-4-алкоксигруппу, нитрогруппу, незамещенную или замещенную аминогруппу NRR', в которой радикалы R и R' независимо могут быть водородом, C1-4-алкильными группами и C2-4-галогенированными алкильными группами;
Y - галогенсодержащая группа, гидроксигруппа, C1-4-алкоксигруппа, незамещенная или замещенная аминогруппа NRR', в которой радикалы R и R' являются такими же, как определено выше;
n = 0 - 3 и n' = 1 - 4;
каждый из радикалов R1 и R2 отдельно представляют собой водород, галогенсодержащую группу, фенильную группу или C1-4-алкильную группу или совместно представляют собой группу = NOR'', в которой R'' представляет собой водород или группу ZC(O)- или (ZO)2P(O)-, где Z - C1-4-алкильная группа;
R3 и R4 независимо представляют собой водород, ацетильную, фенильную, 2,2,2-трихлор-1-гидроксиэтильную группу, C1-4-алкильную группу или они совместно представляют собой группу =CHR''', в которой R''' представляет собой C1-4-алкильную, C1-4-галогенированную алкильную или фенильную группу; или группу = CH-CH= CHR''', в которой радикал R''' является таким же, как и определенный выше, причем каждая фенильная группа, присутствующая в радикалах R3 и R4 или в суммарной группе (R3 + R4), состоящей из радикалов R3 и R4, в целом может быть замещенной одной-тремя группами из ряда галогенсодержащих групп, гидроксигруппы, C1-4-алкильных групп, C1-4-алкоксигрупп, нитрогруппы и незамещенных или замещенных аминогрупп NRR', в которых радикалы R и R' являются такими же, как и определенные выше; соединение как один из вариантов может находиться в форме физиологически приемлемой соли.
В соединениях с формулой I галогенсодержащие группы могут представлять собой иодсодержащую, бромсодержащую или, что особенно предпочтительно, хлорсодержащую группы, C1-4-алкильная группа и алкоксигруппа могут включать в себя алкильные группы, которые являются разветвленными или, что более предпочтительно, неразветвленными, такими как метильная, этильная, пропильная, изопропильная, бутильная и изобутильная группы, причем особый интерес представляют группы меньшего размера, такие как метильная группа. Галогенированные алкильные группы могут состоять из таких галогенсодержащих и алкильных групп, которые преимущественно содержат один атом галогена, а C2-4-галогенированные алкильные группы предпочтительно должны быть замещены не у α-углеродного атома, как, например, в случае 2-хлорэтильной группы.
Что касается группы (X)n, то n может представлять собой либо 0, в случае чего фенильная группа у соединения I является незамещенной, либо чаще n = 1. Когда величина n является отличной от 0, например равняется 1, то тогда радикал X может представлять собой галогенсодержащую группу или в особенности группу NRR'. Предпочтение следует отдавать дизамещенным аминогруппам NRR', например диалкиламиногруппам, таким как диметиламиногруппа. Хотя заместитель (или заместители) X может находиться в различных положениях кольца, желательно, чтобы заместитель или, когда их присутствует несколько, один из заместителей находился в параположении бензольного кольца в отношении фосфорсодержащей группировки.
Что касается группы Y, то она предпочтительно представляет собой галогенсодержащую группу, и число n' может принимать значения 4, 3 или, что особенно предпочтительно, 2 (соединения, у которых число n' равно 1, представляют меньший интерес, причем особенно тогда, когда группа Y является отличной от галогенсодержащей группы), в силу чего предпочтительной группировкой Y(CH2)n'-O представляется 2-хлорэтоксигруппа. Каждая из групп R1 и R2 предпочтительно представляет собой водород, хотя интерес представляют также и соединения, у которых каждая из групп R1 и R2 является галогенсодержащей или одна группа является водородом, а другая представляет собой галогенсодержащую, фенильную или алкильную группу, например метильную группу, а также группы вида =NOR''.
Что касается групп R3 и R4, то группа R3 предпочтительно представляет собой водород или совместно с группой R4 является двухвалентной группой. Примерами различных специфических групп NR3R4 являются такие группы, у которых R3 и R4 - водород, R3 - водород и R4 - радикалы COCH3, C6H5, CH(OH)CCl3 или, что особенно предпочтительно, CH3 и C2H5, или группа R3 совместно с группой R4 (R3 + R4) представляют собой радикалы CHCH3, CHCH2Cl, CHCH= CHCH3, CHCH= CHC6H5 или CHC6H5, а также группы R4 и совместные группы (R3 + R4) могут содержать бензольное кольцо с одним или более заместителем из ряда галогенсодержащих групп, гидроксигрупп, C1-4-алкильных групп, C1-4-алкоксигрупп, нитрогрупп и незамещенных или замещенных аминогрупп NRR'. Например, группа R4 или группа R3 совместно с группой R4 (R3 + R4) содержат группировки 2-HOC6H4, 2,4-(HO)2C6H3, 4-CH3OC6H4, 2,4-(CH3O)2-C6H3, 4-(CH3)2NC6H4, 4-ClC6H4, 2,4-Cl2C6H3, 2-NO2C6H4, 3-NO2C6H4 или 4-NO2C6H4.
Примерами специфических типов соединения I являются соединения, у которых группа NR3R4 представляет собой NHCH(OH)CCl3, N=CH-CH=CHCH3, N=CH-CH= CHC6H5, N=CH-C6H4-NO2-3, N=CH-C6H4-OH-2 или, что особенно предпочтительно, NH2. У предпочтительных соединений с формулой I такие группы NR3R4 сочетаются с группами R1 и R2, представляющими собой водород, причем число n равно 0 или X представляет собой диметиламиногруппу с величиной n, равной единице, особенно при нахождении в параположении, и группой Y(CH2)n'-O, представляющей собой галогеналкоксигруппу, особенно когда величина n' равна двум, такую как 2-хлорэтоксигруппа.
Наиболее предпочтительным соединением является 2-хлорэтокси-(4'-N,N-диметиламинофенил)фосфинилацетогидразид, называемый далее САРАН, и его физиологически приемлемые соли, такие как гидрохлорид.
Соединения с формулой I, у которых каждая из групп R3 и R4 представляет собой водород, могут быть синтезированы взаимодействием гидразина, обычно в виде гидрата, с соответствующим сложным эфиром фосфорилуксусной кислоты. У предпочтительных сложных эфиров группировка -COORIV, превращающаяся затем в группировку - CONHNR3R4 соединения с формулой I содержит группу RIV, которая представляет собой C1-4-алкильную группу, например, метильную или этильную группу. Такие промежуточные сложные эфиры удобно получать, используя общий метод, описанный Арбузовым и др. (Арбузов Б.А., Ризположенский Н.И. //Изв. АН СССР, ОХН, 1952, с. 854 - 859) и Henning и др. (Henning H.J., Hilgetag I. // J. Prakt. Chem., 1965, B. 29 (1-2), S. 86-92), по которому сложный эфир соответствующей фенилфосфонистой кислоты взаимодействует с надлежащим алкилгалогенацетатом. Соединения с формулой I, у которых один или оба радикала R3 и R4 не являются водородом, могут быть получены путем последующей реакции соединения I, у которого каждая из групп R3 и R4 представляет собой водород, с надлежащим реагентом.
Так, например, группировка NR3R4, со структурой NHCH(OH)CCl3, может быть получена с использованием трихлорацетальдегида, а группы N=CH-CH=CHCH3 и N-CH-CH= CHC6H5, например, могут быть получены с использованием кротонового альдегида и коричного альдегида соответственно.
По другой методике САРАН и его аналоги, у которых группа Y(CH2)n, -O представляет собой галогенэтоксигруппу, могут быть получены в одну стадию взаимодействием 4-N, N-диметилфенилдихлорфосфина с этиленоксидом и последующей обработкой продукта реакции этилхлорацетатом и гидразингидратом. Вместо этилхлорацетата можно использовать другой сложный эфир XCH2COOR, у которого заместитель X представляет собой галогенсодержащую группу и R-алкильную группу, например с 1 - 4 атомами углерода. Этот процесс основывается на сведениях, описанных в патенте США N 4162264 или a.с. СССР N 467593 (Разумов А.И. , Тарасова Р.И., Николаева В.Г., Яфарова Р.Л. //А.c. СССР N 467593, кл. C 07 F 9/59; БИ 1976, N 14), по получению соединения (C6H5)2P(O)CH2C(O)NHNH2, и реализуется по следующей реакционной схеме A.
Реакционная сxема A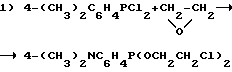
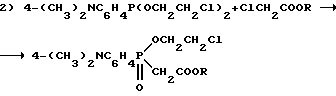
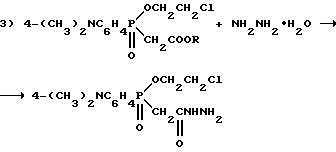
Исходный реагент, представляющий собой 4-N,N-диметиламинофенилдихлорфосфин, получают известным способом (Кормачев В.В., Чалых С.Н., Павлов В.П., Кухтин В. А. /Синтез на основе 4-N,N-диметиламинофенилдихлорфосфина //Сб. статей "Фосфорорганические соединения и полимеры", Чувашский государств. ун-т, Чебоксары, 1976, с. 119).
Другие методики, известные специалистам, работающим в этой области химического синтеза, могут быть также распространены на синтез соединений, используемых в настоящем изобретении.
Во-первых, соединения, у которых заместитель Y представляет собой группу, отличную от галогенсодержащей группы, такую как незамещенная и замещенная аминогруппа, могут быть получены с использованием методики, показанной на реакционной схеме B, по получению (2-N,N-диметиламиноэтокси)(4'-N, N-диметиламинофенил) фосфинилацетогидразида.
Реакционная схема B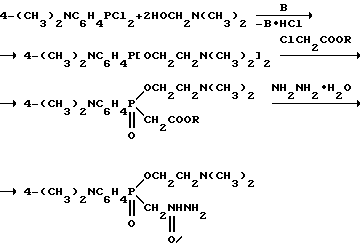
По схеме B могут быть получены также другие соединения формулы I, у которых заместитель Y может быть другой функциональной группой, включая галогеногруппу и, в частности, хлор. Эти же соединения формулы I можно получать по несколько видоизмененной схеме B', используя в качестве исходного реагента вместо замещенного фенилдихлорфосфина соответствующий бис(диалкил)амид фенилфосфонистой кислоты.
Реакционная схема B'
4-(CH3)2NC6H4P [N(C2H5)2] 2 + 2HOCH2CH2N(CH3)2 ---> 4-(CH3)2NC6H4P [OCH2CH2N(CH3)2]2
Последующие стадии процесса аналогичны описанным в схеме B.
Во-вторых, соединения, у которых заместители R1 и R2 совместно представляют собой группу =NOH, могут быть получены с использованием методики, показанной на реакционной схеме C по получению (2-хлорэтокси)(4'-толил)фосфинил (гидроксиимино)-ацетoгидразида.
Реакционная схема C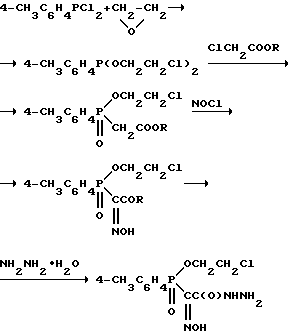
Как cказано выше, соединения, отвечающие настоящему изобретению, обладают ценным терапевтическим действием как антидепрессанты и ноотропы.
В соответствии со сказанным изобретение включает в себя также соединения формулы I, которые предназначены для использования в терапии.
Изобретение касается также фармацевтических рецептур, включающих в себя в качестве активного компонента соединение с формулой I, как это было описано выше, совместно с физиологически приемлемым разбавителем или носителем.
Как уже отмечалось, соединения могут быть приготовлены в виде солей при использовании физиологически приемлемых неорганических или органических кислот, причем особый интерес представляют соли соединений, у которых группы R1 и R2 являются водородом. Ими, например, могут быть соли галоидоводородных кислот, таких как хлористоводородная кислота; однако в случае солей приемлемым может оказаться использование метансульфоновой кислоты, изотионовой кислоты, винной кислоты или какой-либо другой растворимой кислоты.
Соединения с формулой I могут применяться в виде индивидуального соединения или в виде смеси двух или нескольких соединений, пригодных для использования в фармацевтической рецептуре разнообразными способами.
Фармацевтическая рецептура, отвечающая настоящему изобретению, может иметь форму, пригодную для орального использования, например, форму таблетки, капсулы, водного или маслянистого раствора, суспензии или эмульсии; форму, пригодную для назального использования, например, форму порошка для вдыхания через нос, форму препарата, предназначенного для распыления в нос, или форму капель, предназначенных для закапывания в нос; форму, пригодную для вагинального или ректального использования, например, форму суппозитория; форму препарата, предназначенного для введения посредством ингаляции, например, форму тонкодисперсного порошка или жидкого аэрозоля; форму, пригодную для подъязычного или трансбуккального использования, например, форму таблетки или капсулы; или форму, пригодную для парентерального использования (включая внутривенное, подкожное, внутримышечное, интраваскулярное введение или инфузию), например форму стерильного водного или маслянистого раствора или супсензии. В общем случае указанные выше составы могут быть приготовлены обычным способом с использованием обычных наполнителей и при использовании стандартных методик, хорошо известных специалистам, работающим в области фармации.
Соединения, отвечающие настоящему изобретению, находят применение как ноотропы при различных заболеваниях нервной системы, связанных с сосудистыми заболеваниями и нарушениями обменных процессов мозга, при заболеваниях с явлениями хронической церебрально-сосудистой недостаточности, проявляющейся в нарушении памяти, внимания, речи, а также после травм головного мозга и интоксикаций и в период восстановительной терапии после таких состояний. Применяют эти соединения также при заболеваниях нервной системы, сопровождающихся снижением интеллектуально-мнемонических функций.
Соединения, отвечающие настоящему изобретению, находят также применение в лечении клинической депрессии, в частности, реактивной депрессии, хотя они могут найти использование и в лечении маниакальной депрессии и шизофрении, а также в лечении индивидуумов с нарушенной памятью. Особым преимуществом соединений, отвечающих настоящему изобретению, является то, что они обладают как ноотропными свойствами, так и свойствами антидепрессанта. Следовательно, фармацевтический состав, отвечающий настоящему изобретению, является особенно полезным для пациентов, страдающих обоими типами симптомов. Таким образом, одна конкретная область использования сводится к применению вещества одновременно в качестве ноотропа, в том числе для улучшения памяти, в качестве антидепрессанта и в качестве препарата, устраняющего беспокойство, в частности после ишемической болезни, тогда как вторая область использования сводится исключительно к применению вещества в качестве антидепрессанта с возможным сопутствующим анксиолитическим эффектом. Дополнительное потенциально возможное использование, о котором следует упомянуть, сводится к коррекции седативных эффектов от применения бензодиазепиновых транквилизаторов и к лечению осложнений, вызванных применением нейролептических средств.
Следует сказать, что дозировка может изменяться в широких пределах, что зависит от активности данного используемого препарата, от индивидуальных характеристики пациента, который получает препарат, и от состояния, которое подвергается воздействию. Для ориентации, однако, можно указать, что в случае любого из этих лечений соединения, отвечающие настоящему изобретению, часто вводят в суммарной дозе в расчете на человека весом в 70 кг в количестве от 1 до 1000 мг ежедневно, особенно в пределах от 10 до 300 мг ежедневно, хотя точная доза будет зависеть от частных особенностей пациента и может иногда уменьшаться, выходя за этот диапазон. Если соединение используют только в качестве антидепрессанта, а не в сочетании с ноотропным эффектом, то тогда дозы, вероятно, должны быть несколько выше, чем те, которые применяются при получении совместного эффекта.
Настоящее изобретение тем самым включает способ лечения пациента, страдающего депрессией или нуждающегося в коррекции нарушений обменных процессов мозга, который включает в себя введение упомянутому пациенту терапевтически эффективного количества соединения формулы I, как это было определено выше.
Далее изобретение включает использование соединения формулы I для производства медицинского препарата, предназначенного для лечение депрессии и (одновременно или по отдельности) в качестве ноотропного средства.
Изобретение иллюстрируется также следующими диаграммами:
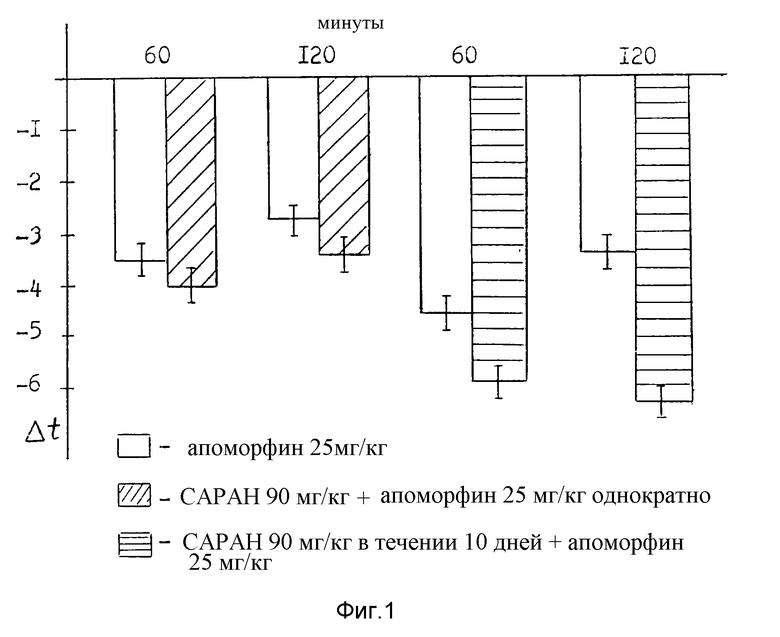
- фиг. 1 характеризует эффект от воздействия САРАН на индуцированную апоморфином гипотермию у мышей;
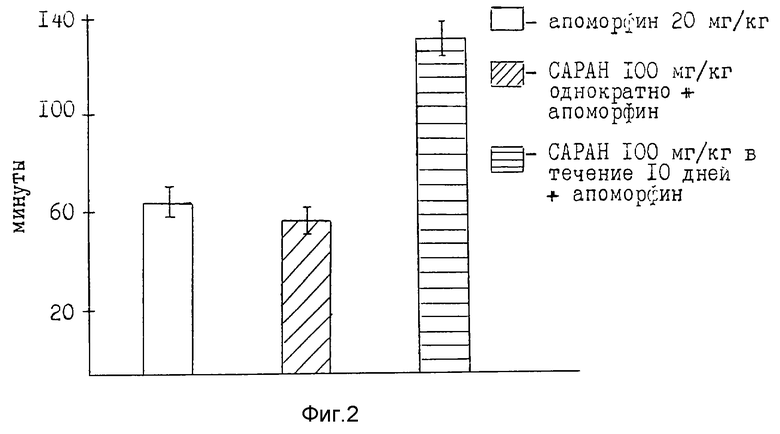
- фиг. 2 характеризует эффект от воздействия САРАН на индуцированную апоморфином стереотипию у крыс;
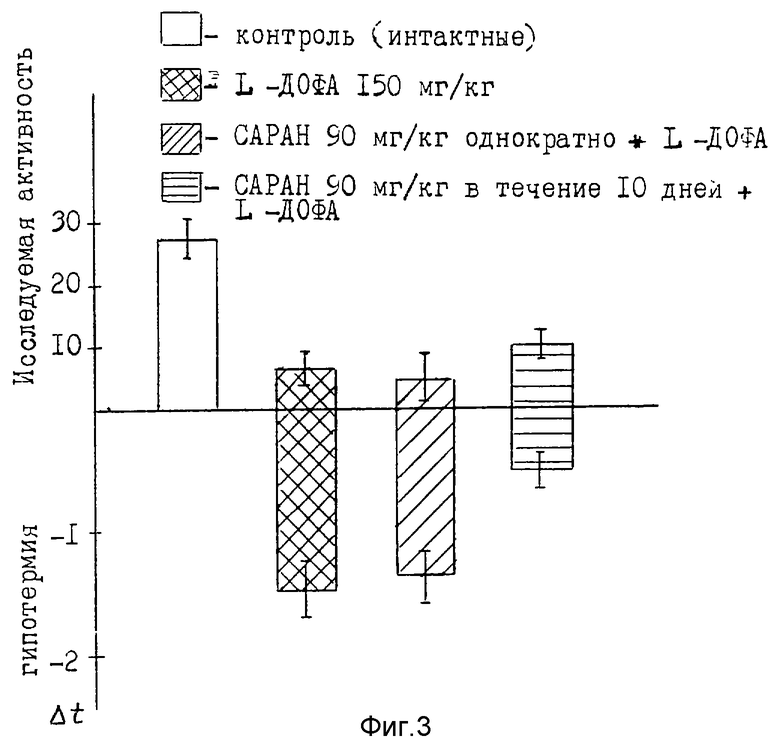
- фиг. 3 характеризует эффект от воздействия САРАН на индуцированную L-ДОФА гипотермию и двигательную активность;
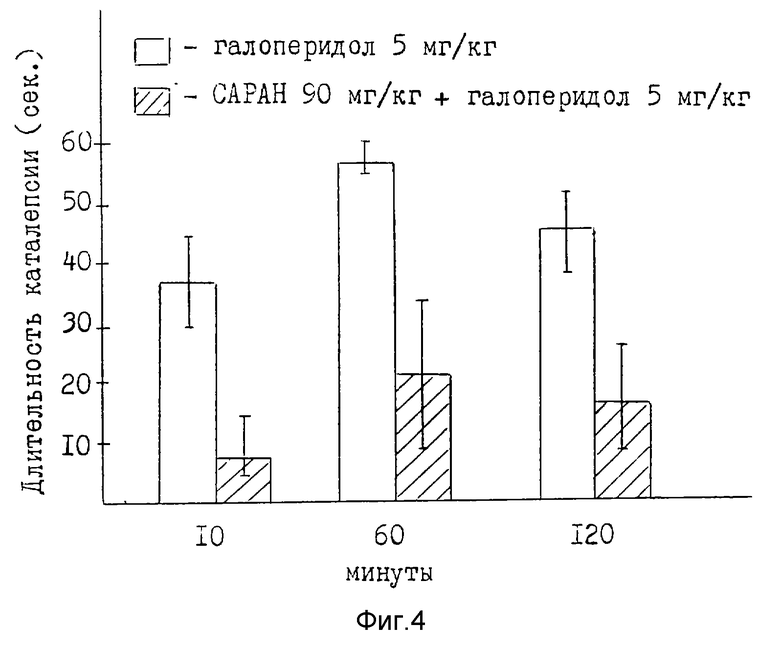
- фиг. 4 характеризует эффект от воздействия САРАН на индуцированную галопериодолом каталепсию.
Пример 1. Синтез 2-хлорэтокси(фенил)фосфинилацетогидразида.
A. К перемешиваемому этил-2-хлорэтокси(фенил)фосфинилацетату (1) (0,1 моль) добавляют гидразингидрат (0,3 моль) при комнатной температуре. Реакционную смесь затем держат при комнатной температуре в течение 12 - 24 ч, после чего образовавшееся твердое вещество отфильтровывают, промывают смесью этанола с простым эфиром (взятыми по объему в соотношении 1:1) и перекристаллизовывают из этанола, в результате чего получают названное соединение с выходом 56% в виде белых кристаллов с температурой плавления 159 - 160oC.
Найдено: P - 11,13%, N - 9,84%; вычислено для формулы C10H14ClN2O3P: P - 11,21%, N - 10,12%.
δ31P(диметилсульфоксид) составляет 40,5 м.д.
1. Этил-2-хлорэтокси(фенил)фосфинилацетат получают по общей методике Арбузова и др., по которой проводят взаимодействие соответствующего сложного эфира фенилфосфонистой кислоты с надлежащим алкилгалогенацетатом.
B. Методика по п. A может быть применена при использовании промежуточных соединений, полученных так, как это описано в пункте A(1), для получения различных соединений формулы I, например п-хлорзамещенных, п-метилзамещенных и п-диметиламинозамещенных соединений.
Пример 2. Синтез (2-хлорэтокси)(4'-N,N-диметиламинофенил)фосфинилацетогидразида
1. Четырехгорлую колбу, снабженную термометром, трубкой для подачи газа, мешалкой и обратным холодильником, наполняют, вводя 30,6 г (0,137 моль) 4-N, N-диметиламинофенилдихлорфосфина и 22,3 г (0,206 моль) метилхлорацетата. После растворения 4-N,N-диметиламинофенилдихлорфосфина содержимое колбы охлаждают до 0oC, и при температуре 0-10o подают 12,05 г (0,274 моль) этиленоксида. После окончания реакции реакционную смесь нагревают до комнатной температуры, перемешивают в течение 0,5 ч, и избыточный этиленоксид удаляют в вакууме водоструйного насоса. Обратный холодильник затем заменяют на нисходящий, и реакционную смесь медленно нагревают при энергичном перемешивании. Взаимодействие протекает при 100 - 110oC и завершается по истечении 3 - 4 ч. В конце взаимодействия температуру повышают до 120oC и поддерживают в течение 15 - 20 мин. Реакционную смесь затем охлаждают до 100oC, дихлорэтан и непрореагировавший метилхлорацетат отгоняют в вакууме при остаточном давлении 10 - 15 мм рт.ст. К образовавшейся смеси небольшими порциями при комнатной температуре добавляют 6,84 г (0,274 моль) гидразингидрата при перемешивании. За 2 ч реакционная масса закристаллизовалась. Кристаллы отфильтровывают, промывают сначала спиртом, затем эфиром и сушат на воздухе. Получен целевой продукт - САРАН (28,0 г, выход 63%) в виде белых кристаллов с температурой плавления 143 - 148oС. После перекристаллизации из хлороформа получили 24,6 г (выход 55%) чистого САРАН с температурой плавления 155 - 156oC.
Найдено: P - 9,20, 9,31%; N - 13,50, 13,31%; вычислено для формулы C12H19ClN3O3P: P - 9,70%, N - 13,14%.
Частота νmax (KBr, табл.) составила 1197 (P=O); 1650 (NH), 1695 (C=O), 3220 - 3315 (NH) см-1.
δ31P (диметилсульфоксид) составил 40,0 м.д.
2. В первом варианте методики, описанной по п. 1 4-N,N-диметиламинофенилдихлорфосфин заменяют эквимолярным количеством 4-хлорфенилдихлорфосфина или 4-трлилдихлорфосфина для получения (2-хлорэтокси)(4'-хлорфенил)фосфинилацетогидразида или (2-хлорэтокси)(4'-толил)фосфинилацетогидразида.
3. Во втором варианте методики, описанной по п. 1, гидразид заменяют на эквимолярное количество фенилгидразина для получения Nβ (фенил)-(2-хлорэтокси)(4'-N,N-диметиламинофенил)-фосфинилацетогидразида.
Пример 3. Синтез гидрохлорида (2-хлорэтокси)(4'-N, N-диметиламинофенил)фосфинилацетогидразида.
К раствору, содержащему 0,005 моль САРАН в 10 мл этанола, добавляют один эквивалент хлористого водорода, растворенного в этаноле (8% по весу на объем). Этанол удаляют под вакуумом при комнатной температуре, образовавшаяся маслянистая жидкость кристаллизовалась. Кристаллы отфильтровывают и промывают эфиром, в результате чего получают гидрохлорид САРАН с выходом 8% в виде белых кристаллов с температурой плавления 171oC, хорошо растворимых в воде.
Найдено: P - 8,75, 8,85%; N - 11,50, 11,75%; Cl - 19,99, 20,34%; вычислено для формулы C19H20Cl2N3O3P: P - 8,72%, N - 11,78%; Cl - 19,94%.
δ31P (H2O) 33,8 м.д.
Пример 4. Синтез Nβ (2,2,2-трихлор-1-гидрокси)(2'-хлорэтокси)-(4''-N, N-диметиламинофенил) фосфинилацетогидразида.
К суспензии, состоящей из 0,005 моль САРАН в 5 мл сухого хлороформа, порциями при перемешивании добавляют при комнатной температуре 0,007 моль трихлорацетальдегида. Температура реакционной смеси повышалась до 35oC к концу реакции. По завершении взаимодействия реакционную смесь перемешивают при комнатной температуре в течение 3 ч, и растворитель затем удаляют под вакуумом. Образовавшуюся маслянистую жидкость очищают, проводя несколько раз осаждение из гексана, в результате чего получают названное соединение с выходом 52% в виде бледно-желтых кристаллов с температурой плавления 115 - 116oC.
Найдено: P - 6,25, 6,35%; N - 8,80, 8,62%; вычислено для формулы C14H20Cl4N3O4P: P - 6,66%, N - 9,00%;
δ31P (диметилсульфоксид) 36,7 м.д.
Пример 5. Синтез Nβ (бут-2-енилиден)-(2-хлорэтокси)(4'-N,N-диметиламинофенил) фосфинилацетогидразида и родственных соединений.
A. К суспензии, состоящей из 0,005 моль САРАН в 5 мл сухого хлороформа, при комнатной температуре добавляют раствор 0,007 моль кротонового альдегида в 2 мл хлороформа при перемешивании. По мере протекания реакции температура реакционной смеси повышалась до 26 - 30oC, при этом САРАН полностью растворялся. Реакционную смесь поддерживают при комнатной температуре в течение 6 - 12 ч, и растворитель затем удаляют под вакуумом. Образовавшуюся маслянистую жидкость очищают, проводя несколько раз осаждение из гексана, в результате чего получают названное соединение в виде желтого порошка с температурой плавления 145 - 146oC, выход 67%.
Найдено: P - 8,20%; N - 11,57%; вычислено для формулы C16H24ClN3O3P: P - 8,36%; N - 11,30%.
δ31P (диметилсульфоксид) 37,5; 38,5 м.д.
Соединение труднорастворимо в большинстве органических растворителей и в воде, растворимо в диметилсульфоксиде и других апротонных полярных растворителях. Наличие двух сигналов ЯМР 31P свидетельствует о присутствии двух изомерных форм с син- и антиположениями.
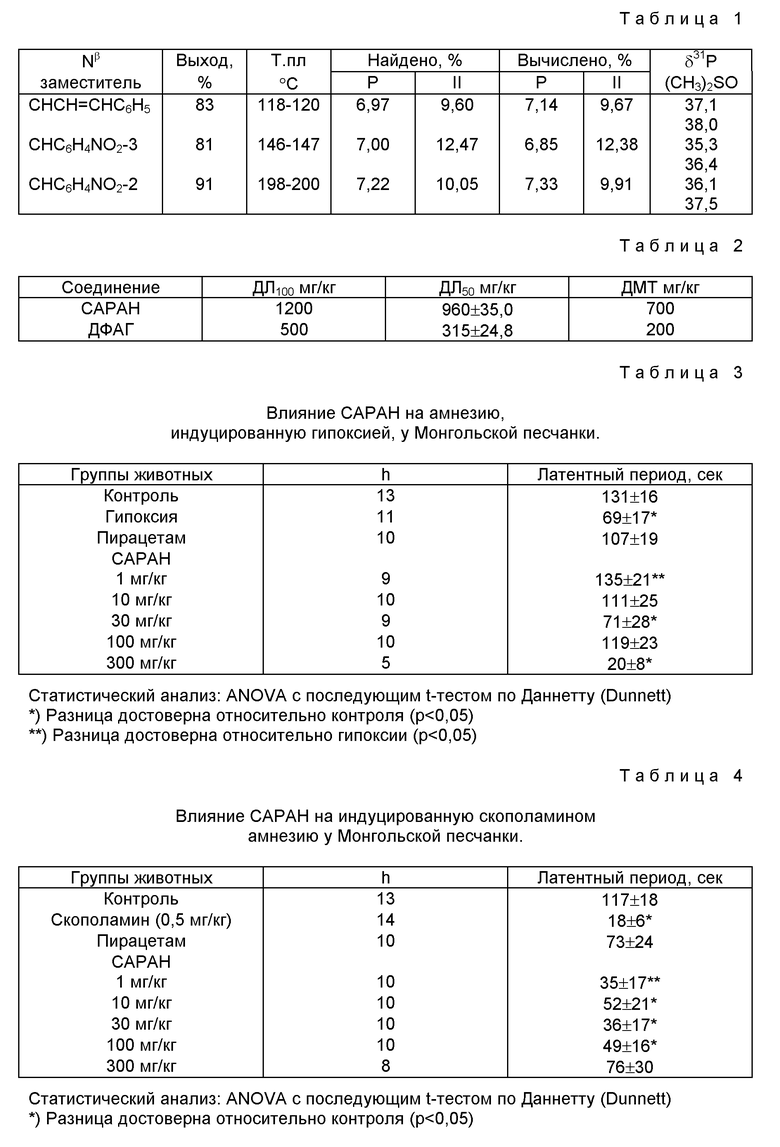
B. Методика, описанная выше по п. A, была использована в реакциях с коричным альдегидом, м-нитробензальдегидом или салициловым альдегидом вместо кротонового альдегида с целью получения Nβ-фенилпропенилиденового, Nβ-м-нитробензилиденoвого и Nβ-o-гидроксибензилиденового производных, характеристика которых представлена в табл. 1. Растворимость этих соединений аналогична бутенилиденовому аналогу, описанному по п. A.
Пример 6. Синтез (2-N, N-диметиламиноэтокси)(4'-N, N-диметиламинофенил)фосфинилацетогидразида.
Реакционную схему B, описанную выше, использовали для проведения синтеза названного в примере 6 соединения на основе 4-N,N-диметиламинофенилдихлорфосфина и 2-N,N-диметиламиноэтанола.
Пример 7. Синтез [(2-хлорэтокси)(4'-толил)фосфинил] (гидроксиимино)ацетогидразида.
Реакционную схему C, описанную выше, использовали для проведения синтеза названного в примере 7 соединения на основе 4-хлорфенилдихлорфосфина и этиленоксида.
Пример 8. Токсичность САРАН.
В ходе проведения фармакологического исследования было установлено, что 2-хлорэтокси (4'-N, N-диметиламинофенил)фосфенилацетогидразид (САРАН) является биологически активным соединением, которое избирательно действует на центральную нервную систему. Из сравнения предложенного соединения с его ближайшим аналогом по строению и цели дифенилфосфинилацетогидразидом (ДФАГ) следует, что САРАН является менее токсичным соединением со значительно большим интервалом между максимально толерантной дозой (ДМТ) и летальной дозой LD100, чем у дифенилфосфинилацетогидразида (табл. 2).
Пример 9. Воздействие САРАН на дофаминергическую систему.
1. Взаимодействие с апоморфином.
Оценивали эффект от воздействия САРАН на индуцированную апоморфином гипотермию и стереотипию. Гипотермию индуцировали подкожной инъекцией мышам 25 мг/кг апоморфина. Изменение температуры кожи регистрировали термометром типа ТПЕМ-1 сразу перед инъекцией апоморфина и также через 60 и 120 мин после введения. Стереотипию у крыс индуцировали подкожным введением апоморфина в дозе 20 мг/кг. Оценивали общую продолжительность периода стереотипии, а также интенсивность проявления отдельных ее составляющих (вылизывание, грызение, вынюхивание). САРАН вводили за 40 мин до введения апоморфина при однократном введении и через 24 ч после последней инъекции при 10-дневном применении. Доза препарата для мышей составляла 90 мг/кг и 100 мг/кг крысам. Результаты представлены на фиг. 1 и 2.
Из полученных результатов следует, что однократное введение САРАН не влияет на индуцированные апоморфином эффекты, в то время как 10-дневное применение САРАН усиливает гипотермическое действие апомофрина у мышей и увеличивает длительность стереотипии у крыс.
2. Взаимодействие с L-ДОФА.
Соединение L-3,4-дигидроксифенилаланин (L-ДОФА) вводили в дозе 150 мг/кг, чем индуцировали гипотермию, депрессию и понижение двигательной активности. САРАН вводили мышам в дозе 100 мг/кг однократно и в течение 10 дней. Однократное применение препарата не показало активности; 10-дневное введение усиливало эффекты L-ДОФА, активируя исследовательскую активность и повышая температуру тела мышей (фиг. 3).
3. Воздействие на каталeпсию, вызванную галоперидолом.
Галоперидол, находящийся в ампуле, вводили подкожно в дозе 5 мг/кг через 40 мин после введения САРАН (90 мг/кг).
Каталепсию оценивали по способности животного удерживать неудобную позу (задние ноги находятся на подставке высотой 30 мм, а передние - на уступе) в течение 60 с интервалами в 10, 60 и 120 мин после последнего введения галоперидола.
Результаты показаны на фиг. 4.
Пример 10. Антиамнестические свойства САРАН.
В этих примерах изучалось защитное действие САРАН при амнезии, индуцированной скополамином, и гипоксии у песчанок в тесте по пассивному избеганию.
Методы.
Методика тренировки.
Песчанок тренировали по программе "пассивного избегания", т.е. их обучали не входить в темное отделение, где они получали удар.
Индуцированная скополамином амнезия.
Песчанкам делали внутрибрюшинную инъекцию скополамина (0,5 мг/кг) за 30 мин до реализации тренировочной методики. Определяли способность СПАРАН, введенного до скополамина, предотвращать индуцированную амнезию.
Амнезия, индуцированная гипоксией.
Песчанок тренировали так, как это описано выше. Для получения гипоксической среды вдували газовую смесь (4% кислорода и 96% азота) через пластиковый бокс (12 л/мин). Сразу после периода тренировки песчанку помещали в эту гипоксическую среду, и удаляли оттуда, когда проявлялись признаки удушья (максимальная продолжительность пребывания в гипоксическом боксе составляла 40 с).
Тест на пассивное избегание.
Песчанок тренировали, как это было описано выше, используя типичное устройство для пассивного избегания сходового типа (модель E13-08, фирма "Коулборн инструментс", Лехай-Валли, США), разделенное на безопасную часть и решетчатую опасную часть (решетку). Экспериментальная камера (размером 16х16х20 см) содержала платформу безопасности (размером 6х16х3 см) и пол, изготовленный из стержней, выполненных из нержавеющей стали. Тренировка на пассивное избегание осуществлялась в течение 5 мин. Песчанки были помещены на платформу безопасности и получали серии слабых электрических ударов с током 0,12-0,2 нА в течение 3 с каждые 6 с, когда они сходили на решетку (чувствительность к току определялась для каждой партии песчанок). Песчанок возвращали в устройство для испытания через 24 ч, и регистрировали (максимально в течение 60 с) время их вхождения на решетку, то есть латентный период - скрытую способность помнить о сходе на решетчатый пол. Контрольные животные имели высокий латентный период.
При проведении обеих серий экспериментов в качестве контрольного вещества использовали пирацетам.
Результаты
Результаты приведены в табл. 3 и 4.
В этом тесте САРАН был активным в дозах 1, 10, 100 мг/кг. Активность отсутствует в дозах 30, 300 мг/кг. Доза в 300 мг/кг (1/3 LD50) является токсичной. Возможно, что механизм положительного САРАН в дозах 1, 10 и 100 мг/кг является различным. В дозе 100 мг/кг САРАН обнаруживает дофаминергическую активность. Эта доза соединения подавляет каталепсию, индуцированную галоперидолом (подкожная инъекция в дозе 5 мг/кг).
Активность САРАН при малых дозах (1 и 10 мг/кг) может быть обусловлена действием иного механизма.
Статистически значимое обратное изменение у индуцированной скополамином амнезии наблюдали в дозе 300 мг/кг, хотя тенденция к улучшению памяти просматривалась и при меньших дозах.
Ноотропная активность САРАН. Сочетание у САРАН противогипоксических свойств и способности положительно влиять на процессы памяти у крыс свидетельствуeт о ноотропном компоненте в спектре психотропного действия препарата.
Пример 11. Изучение влияния на процессы памяти у крыс.
Изучение влияния САРАН на сохранение памятного следа у крыс с использованием методики пассивного избегания. Условная реакция пассивного избегания (УРПИ) вырабатывалась в камере, которая состояла из двух отсеков: светлого (30х30 см) и темного (30х30 см), снабженного электродным полом. В первый день опыта животное при заходе в темный отсек получало удар током (1 мА, 50 Гц). САРАН вводили сразу же после извлечения животного из камеры в первый день опыта. Во 2, 7, 14-й дни, а при хроническом введении и на 21-й день в течение 3 мин оценивали латентный период захода в темный отсек, т.е. оценивали способность животных воспроизводить ранее выработанный навык (получение однократного болевого раздражения в темной камере). САРАН вводили в дозах 300, 100, 50, 30 мг/кг внутрибрюшно однократно сразу после обучения, а также на фоне хронического введения 50 мг/кг (1/20 ДЛ50), которое продолжалось до 21-го дня тестирования. Выявлено, что животные, обучавшиеся рефлексу на фоне однократного введения САРАН, сохраняли навык пассивного избегания при воспроизведении УРПИ на 2, 7, 14-й дни, тогда как в контроле рефлекс исчезал уже после 7 суток. Наиболее эффективной дозой являлось 50 мг/кг. В длительном эксперименте, когда обучение рефлексу пассивного избегания проводилось на фоне хронического введения препарата, памятный след сохранялся значительно лучше. Большинство животных не заходило в темный отсек даже на 21-й день тестирования, а на 7 и 14-й дни процент животных, зашедших в темный отсек, был равен 0.
Эксперименты проведены на беспородных крысах-самцах весом 150-180 г. В каждой группе было по 8 животных.
Результаты представлены в табл. 5.
Пример 12. Изучение антигипоксических свойств САРАН.
Наличие антигипоксического свойства у САРАН изучали на мышах на двух моделях гипоксии: гиперкапнической гипоксии в гермокамере емкостью 100 мл и гемической.
Гипоксию с гиперкапнией в гермообъеме моделировали, помещая мышей в банки объемом 100 мл с герметически закрывающимися крышками. Регистрировали продолжительность жизни животных в гермокамере. САРАН вводили в дозах 90, 45, 30 мг/кг, составляющих соответственно 1/10, 1/20, 1/30 от ДЛ50. Эксперименты были проведены на линейных белых мышах весом 18 г. В каждой группе было по 6 животных (табл. 6).
Гемическую гипоксию вызывали подкожным введением нитрита натрия - 300 мг/кг. Регистрировали продолжительность жизни животных. Эксперименты проведены на белых мышах весом 18-21 г. В каждой группе было по 8 животных. САРАН вводили внутрибрюшинно в дозе 90 мг/кг (табл. 7).
Пример 13. Влияние препарата САРАН на концентрацию РНК и ДНК в коре головного мозга крыс при длительной невротизации.
Неизбегаемое болевое раздражение переменным током 50 Гц, 25 В (что соответствует 12-14 мА) подавалось на лапы животных одновременно в четырех камерах, соединенных общим металлическим полом. Ток подавался в сочетании с 10-секундными световыми вспышками, начиная с 6 с; эти сочетания чередовались в постоянно меняющемся порядке с изолированными вспышками (по 6 в опыте). При таком режиме выработка оборонительного рефлекса чрезвычайно затруднена, а вегетативные показатели (давление) повышены, что приводит к нарушению показателей психосоматического характера (гипертония), рассматриваемых в качестве проявлений экспериментального невроза.
Как тест-метод использовали "открытое поле".
"Открытое поле" квадратной формы 120х120 см разделено на квадраты (длина стороны 15 см) и три концентрические зоны, на пересечении квадратов имелись отверстия диаметром 2,5 см. Освещение осуществлялось лампой 150 Вт. За 3 мин тестирования регистрировали:
1) число пересеченных линий и число вертикальных стоек;
2) число обследованных отверстий как показатель исследовательской активности животного;
3) число фекальных болюсов.
Препарат вводили в режиме "лечения" в течение 7 дней после окончания 15-дневного курса невротизации. Тестирование проводилось через 24 ч после последнего введения веществ. Затем животных забивали декапитацией и определяли содержание ДНК и РНК в мозговой ткани крыс.
Проводилось определение количества ДНК и РНК в ткани головного мозга крыс.
Для исследования бралась навеска коры в лобно-теменной области мозга крыс. Измерение проводили на спектрофотометре. СФ-26 в области 260 и 285 нм для РНК и 2368 и 282,5 нм для ДНК. Результаты выражали в мг% фосфора на сырой вес ткани.
Эксперименты проведены на 80 крысах-самцах линии Вистар весом 150-200 г.
После 15 дней невротизации у животных возникли стойкие изменения поведения в "открытом поле": резко уменьшалась исследовательская активность (число обследованных отверстий, горизонтальная и вертикальная активность). Стрессированные животные значительно теряли в весе, в них отмечалась гипертрофия надпочечников. Произошли изменения в обменных процессах: возросла концентрация продуктов перекисного окисления липидов - малонового диальдегида в коре головного мозга крыс, снизился уровень нуклеиновых кислот (РНК и ДНК).
Применение САРАН при лечении невротизированных животных восстанавливало сниженный процедурой стрессирования уровень ДНК и РНК (табл. 8).
Пример 14. Оценка антидепрессивной активности САРАН.
Для оценки антидепрессивной активности САРАН были использованы модель "поведенческого отчаяния" и тест "выученной беспомощности".
а) Метод "поведенческого отчаяния". Тест основан на том, что мыши, принужденные плавать в ограниченном пространстве, которое представляет собой цилиндрический сосуд высотой 15 см и с уровнем воды 6 см, замирают. Считается, что замирание отражает состояние пониженного настроения и безысходности, которое уменьшается антидепрессантами. САРАН изучался при остром и хроническом введении (в течение 10 дней). Оценивали в секундах общую длительность неподвижности животных в течение 6 мин наблюдения. Температура воды в сосуде поддерживалась на уровне 21oC. Эксперименты проведены на 30 мышах-тетрагибридах CBWA. САРАН вводили в дозе 90 мг/кг за 40 мин до начала эксперимента. Результаты эксперимента показали, что САРАН при многократном применении уменьшает длительность периодов "замирания", что указывает на наличие антидепрессивного компонента (табл. 9).
б) Метод "выученной беспомощности". Предварительное неизбегаемое аверсивное воздействие проводили в темных камерах (30х15х15 см) с электродным полом. Мышей индивидуально помещали в камеры, где они получали серии стимулов (150 мкА, 60 Гц) в течение 6 с с интервалом 30 с. Экспозиция 40 мин. Через 24 ч животных тестировали в "челночной" камере, которая состояла из двух отсеков с электродным полом, соединенных отверстием, расположенном на 1 см от основания с выступом, находящимся постоянно под напряжением электрического тока. Доступ в соседний отсек преграждала автоматически управляемая заслонка. Поочередно с интервалом 30 с в каждый отсек подавали раздражение (150 мкА) и с отстаиванием в 4 с заслонку закрывали, и подачу тока прекращали. За сеанс животное получало 10 предъявлений. Оценивали среднее суммарное время латенции избегания, а также общее число невыполненных реакций.
Эксперименты проведены на 40 мышах-самцах беспородных весом 18-20 г. В качестве эталонного препарата использовали мелипрамин. Препараты вводили внутрибрюшинно в дозах: САРАН - 90 мг/кг; мелипрамин - 7 мг/кг. Контрольные животные получали равное количество бидистилированной воды. В 1-й контрольной группе (контроль 1) мыши не подвергались неизбегаемому раздражению; во 2-й контрольной группе (контроль 2) животные подвергались предварительному неизбегаемому аверсивному воздействию, но не получали препаратов. Животные, предварительно помещенные в ситуацию неизбегаемого стресса, при последующем (через 24 ч) тестировании в "челночной камере" проявляли достоверный дефицит поведения, сохранявшийся при повторном тестировании на 6 и 12-й дни (табл. 10).
Как видно из табл. 10, САРАН (90 мг/кг) демонстрировал заметные антидепрессантные эффекты как при однократном, так и при длительном воздействии.
Пример 15.
Композиция в виде таблетки стандартного размера:
Активное вещество 2-хлорэтокси-п-N-диметиламинофенилфосфонилуксусной кислоты), г - 0,05
Наполнитель (картофельный крахмал), г - 0,012
Связующее (стеарат кальция), г - 0,065
Общий вес, г - 0,127
Изучение антидепрессивной активности некоторых аналогов САРАН.
Антидепрессивную активность препаратов изучали на модели "поведенческого отчаяния" у мышей (1, 2). В экспериментах использовано 50 беспородных мышей-самцов массой 18-20 г. Препараты (KSTU-1, KSTU-2, KSTU-3595, 3598) вводили в дозах 10 мг/кг внутрибрюшинно за 40 мин до тестирования.
Результаты экспериментов показали наличие антидепрессивной активности у соединения KSTU-1 (время иммобилизации мышей 58% по отношению к контролю), тенденцию к достоверности у соединения KSTU-2. Соединения KSTU-3595 и KSTU-3598 были неактивны (табл. 11).
Изучение антигипоксической активности некоторых аналогов САРАН.
Методика исследования. Антигипоксическую активность соединения изучали на модели гипобарической гипоксии, которую моделировали в барокамере путем создания разреженной среды, имитирующей подъем на высоту 10 000 м со скоростью 85 м/с. Эксперименты проведены на мышах-самцах массой 20-22 г. Регистрировали продолжительность жизни животных c момента "подъема" до последнего вздоха. Соединения (KSTU-1, KSTU-2, KSTU-3595, KSTU-3598) вводили в дозах 100 и 10 мг/кг внутрибрюшинно за 40 мин до начала эксперимента.
Результаты экспериментов. Исследования показали наличие антигипоксической активности у соединения KSTU-1 в обеих исследуемых дозах. При введении этого препарата продолжительность жизни мышей составляла соответственно 169 и 182% по отношению к контролю. Антигипоксическая активность соединения KSTU-2 проявилась лишь в большой (100 мг/кг) дозе. Противогипоксическая активность выявлена также у препарата KSTU-3598 (табл. 12).
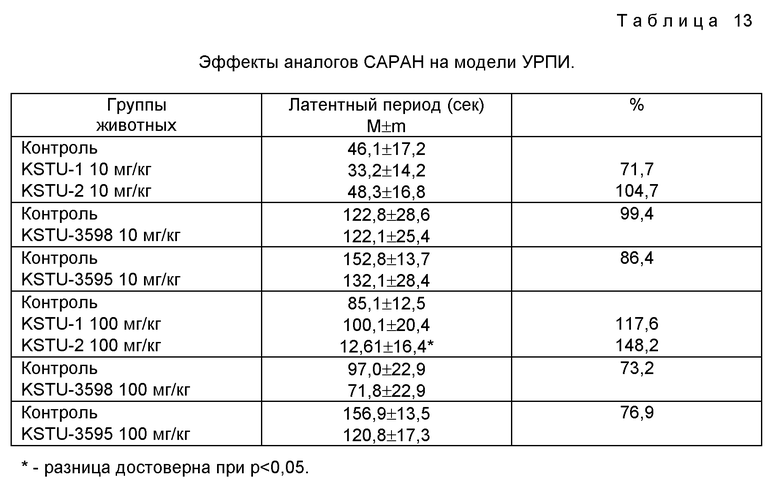
Изучение активности некоторых аналогов САРАН на модели УРПИ.
Методика исследования. Эксперименты проведены на 100 беспородных мышах-самцах массой 18-20 г. Выработку УРПИ осуществляли в камере, состоящей из двух отсеков: светлого и темного, снабженного электродным полом. В первый день опыта животное, заходя в темный отсек, получало электроболевое раздражение. Во второй день опыта оценивали в течение 3 мин латентный период захода в темный отсек. Препараты (KSTU-1, KSTU-2, KSTU-3595, KSTU-3598) вводили в дозах 10 и 100 мг/кг за 40 мин до обучения в первый день опыта.
Результаты экспериментов. На данной модели эффект в улучшении процессов памяти оказал лишь препарат KSTU-2. Остальные соединения данной модели были малоэффективными (табл. 13).
| название | год | авторы | номер документа |
|---|---|---|---|
| [(4-Диметиламинофенил)(2-хлорэтокси)фосфонил]метангидразид, обладающий биологической активностью, и способ его получения | 2024 |
|
RU2838153C1 |
| ЗАМЕЩЕННЫЕ 3-АРИЛСУЛЬФОНИЛ-ПИРАЗОЛО[1,5-a]ПИРИМИДИН-2,6-ДИАМИНЫ, АНТАГОНИСТЫ СЕРОТОНИНОВЫХ 5-НТ РЕЦЕПТОРОВ, СПОСОБЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2421456C1 |
| ДИЛИТИЕВАЯ СОЛЬ N-САЛИЦИЛОИЛГЛИЦИНА, ОБЛАДАЮЩАЯ НООТРОПНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2495867C1 |
| ВОДОРАСТВОРИМОЕ ПРОИЗВОДНОЕ САЛИЦИЛМОРФОЛИДА, ОБЛАДАЮЩЕЕ НООТРОПНОЙ АКТИВНОСТЬЮ В СОЧЕТАНИИ С АНТИДЕПРЕССИВНЫМ ДЕЙСТВИЕМ | 2012 |
|
RU2495032C1 |
| ПРОИЗВОДНОЕ ГАММА-АМИНОМАСЛЯНОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ НООТРОПНОЙ АКТИВНОСТЬЮ В СОЧЕТАНИИ С ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 2012 |
|
RU2495866C1 |
| ТЕТРАГИДРО-ПИРАЗОЛО[1,5-a]ПИРИДО-ПИРИМИДИНЫ - АНТАГОНИСТЫ СЕРОТОНИНОВЫХ 5-HT РЕЦЕПТОРОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2008 |
|
RU2391343C1 |
| ГИДРОХЛОРИД ДИМЕТИЛГИДРАЗОНА ДИИЗОПРОПОКСИФОСФОРИЛУКСУСНОГО АЛЬДЕГИДА, ПРОЯВЛЯЮЩИЙ НЕЙРОТРОПНУЮ АКТИВНОСТЬ | 1988 |
|
RU1577317C |
| N-МОНО- И N,N-ДИТИЕТАНСОДЕРЖАЩИЕ 5-БРОМ-2,4-ДИГИДРО-1,2,4-ТРИАЗОЛ-3-ОНЫ, ПРОЯВЛЯЮЩИЕ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2024 |
|
RU2826999C1 |
| ЗАМЕЩЕННЫЕ 2-АЛКИЛСУЛЬФАНИЛ-3-СУЛЬФОНИЛ-ПИРАЗОЛО[1,5-а]-ПИРИМИДИНЫ, АНТАГОНИСТЫ СЕРОТОНИНОВЫХ 5-HT РЕЦЕПТОРОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2008 |
|
RU2393159C1 |
| 4(3Н)-ПИРИМИДОНЫ, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1978 |
|
SU772122A1 |




Изобретение относится к новым эфирам фосфиновых кислот соединения формулы I, где Х - галоген, С1-С4-алкил, С1-С4-диалкиламиногруппа; n - от 0 до 3; Y - галоген или С1-С4-диалкиламиногруппа; n' - от 1 до 4; R1 и R2 - водород или вместе представляют группу =NOH; R3 и R4 - водород, необязательно замещенный С1-С4-алкокси, 2,2,2-трихлор-1-гидроксиэтил, ацетил или вместе представляют группу =CHR''' или =СН-СН=СНR''', где R''' - С1-С4-алкил или фенил, который может быть замещен ОН, СООН или NO2 - группой, или к их физиологически приемлемым солям. Соединения формулы I получают взаимодействием гидразина с эфиром фосфорилуксусной кислоты. Соединения формулы I обладают ноотропной и антидепрессивной активностью. Изобретение также относится к фармацевтической композиции, обладающей ноотропной и антидепрессивной активностью и содержащей в качестве активного начала соединение формулы I в эффективном количестве. Изобретение относится также к способу коррекции нарушений обменных процессов мозга, который заключается во введении терапевтически эффективной дозы соединения по п.1. 3 с. и 16 з.п. ф-лы, 13 табл., 4 ил.
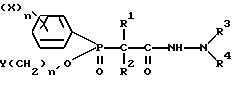
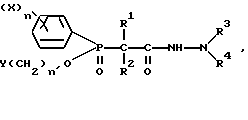
где X - галоген, C1 - C4-алкил, C1 - C4-диалкиламиногруппа;
n = 0 - 3;
Y - галоген или C1 - C4-диалкиламиногруппа;
n' = 1 - 4;
R1 и R2 - водород или вместе представляют группу =N-OH;
R3 и R4 - водород, необязательно замещенный C1 - C4-алкокси, 2,2,2-трихлор-1-гидроксиэтил, ацетил или вместе представляют группу =CHRIII или = CH-CH=CHRIII, где RIII - C1 - C4-алкил или фенил, который может быть замещен OH, COOH или NO2-группой,
или их физиологически приемлемые соли.
| Средство для лечения нервно-психических заболеваний | 1972 |
|
SU741876A1 |
| US 4162311 A, 1979 | |||
| Журнал общей химии | |||
| Запальная свеча для двигателей | 1924 |
|
SU1967A1 |
| Химико-фармацевтический журнал | |||
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
Авторы
Даты
1999-11-27—Публикация
1994-01-11—Подача