ПРАВА ПРАВИТЕЛЬСТВА
[1] Данное изобретение было создано при государственной поддержке в рамках грантов №№ DK099803, DK072517, DK101373, EY013574 и DK089502, предоставленных Национальными институтами здравоохранения. Правительство имеет определенные права на данное изобретение.
ОБЛАСТЬ ТЕХНИКИ
[2] Настоящее изобретение относится к способам лечения хологенной диареи путем введения ингибитора хлоридных каналов CFTR.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[3] Хологенная диарея (bile acid diarrhea - BAD) обычно наблюдается после резекции подвздошной кишки и при болезни Крона и, как полагают, встречается более чем у одной трети пациентов с синдромом раздраженного кишечника с преобладанием диареи (IBS-D) или хронической функциональной диареи, с оценкой общей распространенности до 1% в западных странах. BAD может быть вызвана нарушениями синтеза желчных кислот в печени или энтерогепатической циркуляции, что приводит к доставке избытка желчных кислот в толстую кишку, где они вызывают секрецию жидкости и увеличивают моторику.
[4] Современные методы лечения первичной BAD или BAD, вызванной резекцией подвздошной кишки или болезнью Крона, включают вещества, связывающие желчные кислоты, такие как холестирамин, колестипол и колесевелам, и в стадии разработки находятся агонисты рецептора фарнезоида X (FXR), такие как обетихолевая кислота. Для лечения IBS-D, при котором BAD, вероятно, участвует в патогенезе более чем одной трети пациентов, одобренные FDA методы лечения включают антагонист 5-HT3 алосетрон, смешанный агонист опиоидных рецепторов элюксадолин и специфический для кишечника антибиотик широкого спектра действия рифаксимин. Другие широко используемые методы лечения IBS-D включают лоперамид, секвестранты желчных кислот, спазмолитики и трициклические антидепрессанты. Некоторые из этих методов лечения связаны со значительными побочными эффектами, такими как ишемический колит при лечении алосетроном и панкреатит при лечении элюксадолином.
[5] Сохраняется неудовлетворенная потребность в улучшенных и альтернативных терапевтических средствах для лечения BAD.
[6] Белок трансмембранного регулятора проводимости при муковисцидозе (CFTR) представляет собой хлоридный канал, экспрессируемый в некоторых эпителиальных клетках млекопитающих, включая эпителиальные клетки кишечника. Функция хлоридного канала CFTR была связана с секреторной диареей.
[7] Ингибиторы CFTR находят клиническое применение в терапии секреторной диареи. Секреторная диарея, вызванная энтеротоксинами, такая как холера и диарея путешественников (энтеропатогенная кишечная палочка), требует функционального CFTR для первичной секреции хлоридов в просвет кишечника, что вторично стимулирует секрецию натрия и воды (смотри, например, Kunzelmann et al., Physiol. Rev. 82:245-89 (2002); Thiagarajah et al., Curr. Opin. Pharmacol. 3:594-9 (2003)). На культурах клеток и на животных моделях показано, что кишечная секреция хлорида при секреторной диарее, опосредованной энтеротоксином, происходит в основном посредством CFTR (смотри, например, Clarke et al., Science 257: 1125-28 (1992); Gabriel et al., Science 266:107-109 (1994); KunzelmannandMall, Physiol. Rev. 82:245-89 (2002); Field, 15 J. Clin. Invest. 111:931-43 (2003); и Thiagarajah et al., Gastroenterology 126:511-519 (2003)). Несколько классов низкомолекулярных ингибиторов CFTR были описаны ранее (смотри, например, Verkman et al., Nat. Rev. Drug Discov. 8:153-71 (2009)).
[8] В патенте США № 9062073 описан ряд соединений бензопиримидопирролооксазиндиона (BPO) и некоторых соединений пиримидопирролохиноксалиндиона (PPQ), которые могут использоваться в качестве ингибиторов хлоридных каналов CFTR. Соединения BPO имеют общую формулу:
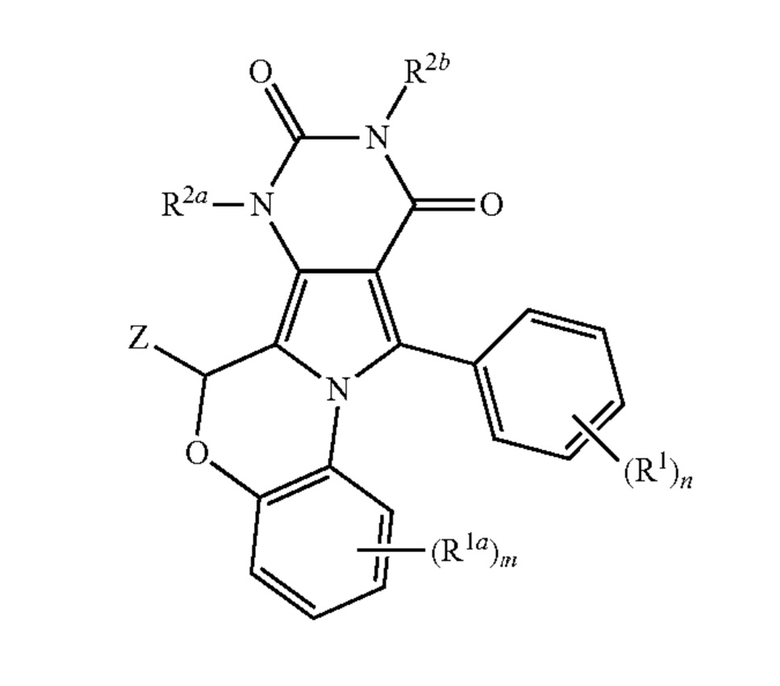
где:
m равно 1, 2, 3 или 4;
n равно 1, 2, 3, 4 или 5;
p равно целому числу от 0 до 4;
q равно целому числу от 1 до 4;
R1 в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-C6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R1a в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-C6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R2a и R2b, каждый, являются одинаковыми или различными и, независимо, представляют собой H или C1-C6 алкил;
R4a представляет собой -OR7, -NR7R8, -O(CH2)q-OC(O)R7 или остаток аминокислоты;
R7 и R8, каждый, являются одинаковыми или различными и, независимо, представляют собой H, C1-C20 алкил, сахарид или остаток аминокислоты; и
Z представляет собой арил или гетероарил,
где остаток аминокислоты выбран из остатков аланина, аргинина, аспарагина, аспарагиновой кислоты, цистеина, глутамина, глутаминовой кислоты, глицина, гистидина, изолейцина, лейцина, лизина, метионина, фенилаланина, пролина, серина, треонина, триптофана, тирозина, валина, фосфосерина, фосфотреонина, фосфотирозина, 4-гидроксипролина, гидроксилизина, демозина, изодемозина, гамма-карбоксиглутамата, гиппуровой кислоты, октагидроиндол-2-карбоновой кислоты, статина, 1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты, пеницилламина, орнитина, 3-метилгистидина, норвалина, бета-аланина, гамма-аминомасляной кислоты, циртуллина, гомоцистеина, гомосерина, метилаланина, пара-бензоилфенилаланина, фенилглицина, пропаргилглицина, саркозина, метионинсульфона, трет-бутилглицина, 3,5-дибромтирозина, 3,5-дииодтирозина, гликозилированного треонина, гликлозилированного серина и гликозилированного аспарагина.
[9] Соединения PPQ имеют общую формулу:
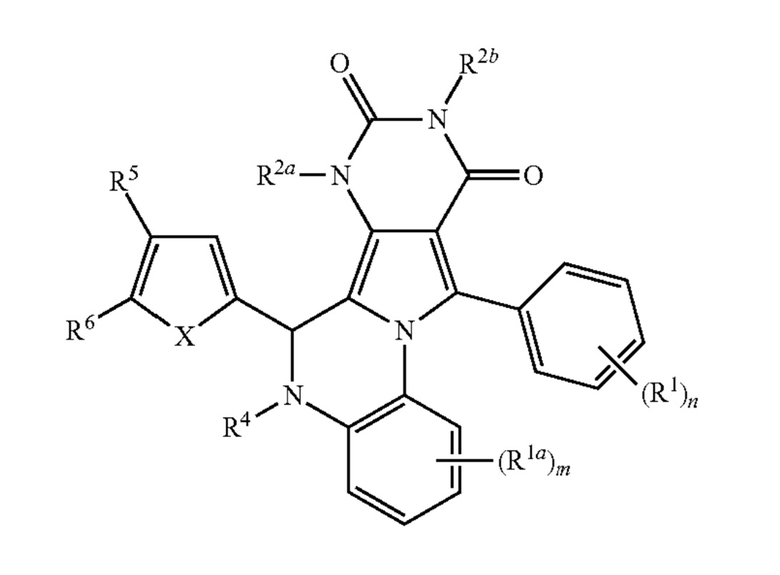
где:
m равно 1, 2, 3 или 4;
n равно 1, 2, 3, 4 или 5;
p равно целому числу от 0 до 4;
q равно целому числу от 1 до 4;
X представляет собой O или S;
R1 в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R1a в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R2a и R2b, каждый, являются одинаковыми или различными и, независимо, представляют собой H или C1-6 алкил;
R4a представляет собой -OR7, -NR7R8, -O(CH2)q-OC(O)R7, остаток аминокислоты или пептид;
R4 представляет собой H, -N(═O), C1-6 алкил или галогеналкил;
R5 представляет собой H, галоген или C1-6 алкил;
R6 представляет собой галоген, C1-6 алкил или C1-6 галогеналкил; и
R7 и R8, каждый, являются одинаковыми или различными и, независимо, представляют собой H, C1-20 алкил, сахарид, остаток аминокислоты или пептид.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[10] Аспекты настоящего изобретения относятся к способам лечения субъекта, страдающего хологенной диарей, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для лечения хологенной диареи.
[11] Другие аспекты изобретения относятся к способам лечения субъекта, страдающего хологенной диареей, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридных каналов CFTR, эффективное для лечения хологенной диареи.
[12] Кроме того, аспекты настоящего изобретения также относятся к способам снижения секреции кишечного сока, происходящей в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой, в кишечном эпителии у нуждающегося в этом субъекта, включающих введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для снижения указанной секреции кишечного сока, происходящей в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой.
[13] Другие аспекты изобретения относятся к способам снижения секреции кишечного сока, происходящей в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой, в кишечном эпителии у субъекта, нуждающегося в этом, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридных каналов CFTR, эффективное для снижения указанной секреции кишечного сока, происходящей в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой.
[14] Дополнительные аспекты настоящего изобретения относятся к способам снижения потока апикального хлоридного канала CFTR, индуцированного желчной кислотой, в кишечном эпителии субъекта, нуждающегося в этом, включающим введение субъекту количества ингибитора хлоридного канала CFTR, эффективного для снижения потока апикального хлоридного канала CFTR, индуцированного желчной кислотой.
[15] Другие аспекты изобретения относятся к способам снижения потока апикального хлоридного канала CFTR, индуцированного желчной кислотой, в кишечном эпителии субъекта, нуждающегося в этом, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридного канала CFTR, эффективного для снижения указанного потока апикального хлоридного канала CFTR, индуцированного желчной кислотой.
[16] В некоторых аспектах изобретение относится к способам лечения диареи или облегчения симптомов, связанных с диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающих введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для лечения указанной диареи или для облегчения симптомов указанной диареи.
[17] Другие аспекты изобретения относятся к способам лечения диареи или облегчения симптомов, связанных с диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающим введение субъекту фармацевтической композиции, содержащей некоторое количество хлоридного канала CFTR, эффективное для лечения указанной диареи или для облегчения симптомов указанной диареи.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[18] Фигура 1. Ингибиторы CFTR блокируют индуцированный желчной кислотой секреторный поток в клетках T84 (A.) Ток короткого замыкания (Isc), показывающий реакцию на указанные желчные кислоты, добавленные как в апикальные, так и в базолатеральные отмывочные растворы. (R)-BPO-27 добавляют в количестве 10 мкМ (представитель 3 фильтров, исследованных на холевую кислоту, урсодезоксихолевую кислоту и литохолевую кислоту; и 5 фильтров на дезоксихолевую кислоту, хенодезоксихолевую кислоту и их тауроконъюгатов). (B.) CDCA (0,75 мМ) добавляют к обоим отмывочным растворам, с добавлением (R)-BPO-27 (10 мкМ) или CFTRinh-172 (10 мкМ), как указано. (C.) Сводная информация о пиковом потоке, индуцированном CDCA, и снижении потока после (R)-BPO-27 или CFTRinh-172 (△Isc, среднее±SEM, n=7-8 фильтров на условие). (D.) Ток короткого замыкания в толстой кишке мышей демонстрирует эффекты CDCA (1 мМ), добавленного к базолатеральным или апикальным отмывочным растворам, с добавлением (R)-BPO-27 (10 мкМ), как указано.
[19] Фигура 2. CDCA действует с апикальной стороны в монослоях клеток T84, активируя апикальный CFTR. (A.) CDCA добавляется к базолатеральным или апикальным отмывочным растворам. (верху) Типичные кривые тока короткого замыкания с добавлением (R)-BPO-27 в концентрации 10 мкМ. (внизу) Сводка пиковых потоков, индуцированных CDCA (Isc, среднее±SEM, n=-8, ** p <0,01, ns, несущественно по сравнению с нулевым эффектом)). (B.) К базолатеральному отмывочному раствору добавляют CDCA с увеличением от 0,75 до 2 мМ, затем форсколин (по 10 мкМ с обеих сторон) и (R)-BPO-27 (10 мкМ). (C.) К апикальному базолатеральному отмывочному раствору добавляют ток короткого замыкания в клетках T84 после пермеабилизации базолатеральной мембраны с 250 мкг/мл амфотерицина B в присутствии градиента Cl- базолатерального к апикальному отмывочному раствору (базолатеральный [Cl-] 120 мМ, апикальный [Cl-] 5 мМ). CDCA градиента (0,75 или 1 мМ), затем (R)-BPO-27 (10 мкМ).
[20] Фигура 3. CDCA оказывает минимальное влияние на передачу сигналов cAMP в клетках T84. (A.) Ток короткого замыкания, демонстрирующий влияние указанной концентрации CDCA, затем форсколина (10 мкМ) и затем (R)-BPO-27 (10 мкМ) (B.) Сводка пикового потока, индуцированного форсколином (ΔIsc, среднее±SEM, n=4-6, ** p <0,01, ns, несущественно по сравнению с ответом на форсколин с 0 мМ CDCA). (C.) cAMP в клетках Т84, измеренный через 30 мин после инкубации с указанной концентрацией CDCA с 10 мкМ форсколина или без него (среднее±SEM, n=3-6, ** p <0,01, ns, не значимо).
[21] Фигура 4. Действие CDCA в клетках T84 связано с передачей сигналов Ca2+. (A.) Ток короткого замыкания, показывающий эффект CDCA (1 мМ) после предварительной обработки BAPTA-AM (30 мкМ) в течение 25 мин, а затем (R)-BPO-27 (10 мкМ). (B.) Сводка пикового потока, индуцированного CDCA, с предварительной обработкой BAPTA-AM или без нее (Isc, среднее±SEM, n=4-5, ** p<0,01). (C.) Цитоплазматическая концентрация Ca2+, измеренная с помощью флуоресценции Fluo-4. CDCA (0,75, 1 мМ), ATP (100 мкМ) или карбахол (100 мкМ) добавляли к апикальному отмывочному раствору с предварительной обработкой BAPTA-AM (30 мкМ) или без нее в течение 30 минут. (D.) Пиковое увеличение флуоресценции Fluo-4 (среднее±SEM, n=3-6, ** p <0,01, ns, несущественно).
[22] Фигура 5. Секреторный ответ CDCA в первичных культурах эпителиальных клеток толстой кишки человека, состоящих из планарных монослойных культур, полученных из колоноидов. (A.) (вверху) Ток короткого замыкания, демонстрирующий влияние указанной концентрации CDCA, добавленной к апикальным или базолатеральным отмывочным растворам, с последующим добавлением форсколина (10 мкМ) и (R)-BPO-27 (5 мкМ). (B.) Сводка пиковых потоков, индуцированных CDCA (ΔIsc, среднее±SEM, n=9-13). (C.) Ток короткого замыкания показывает эффект CDCA (0,5 мМ) после предварительной обработки BAPTA-AM (30 мкМ) в течение 20 мин, затем форсколином (10 мкМ) и (R)-BPO-27 (5 мкМ). (D.) Измерение флуоресценции цитоплазматической концентрации Ca2+ с добавлением CDCA (0,75 мМ) или ATP (100 мкМ).
[23] Фигура 6. CDCA-индуцированная секреция жидкости в закрытых петлях кишечника у мышей. (A.) Динамика секреции жидкости, вызванной CDCA. 100 мкл CDCA в PBS (10 мМ) или PBS вводили в замкнутые петли средней части тощей кишки, и петли вырезали в разное время для измерения веса и длины петли (среднее±SEM, n=5-9 петель на группу, ** p <0,01). (B.) Концентрационная зависимость эффекта CDCA в замкнутых петлях тощей кишки. 100 мкл CDCA или PBS вводили в замкнутые петли средней части тощей кишки (среднее±SEM, n=3-14 петель на группу, ** p <0,01, ns, несущественно). (C.) Концентрационная зависимость эффекта CDCA в замкнутых петлях толстой кишки. 100 мкл CDCA или PBS вводили в замкнутые петли толстой кишки (среднее±SEM, n=3-5 петель на группу, ** p <0,01, ns, несущественно).
[24] Фигура 7. (R)-BPO-27 ингибирует секрецию жидкости, индуцированную CDCA, в замкнутых петлях кишечника мышей. (A.) Протокол эксперимента. (B.) (слева) Отношение веса/длины петель средней части тощей кишки, инъецированной CDCA (10 мМ) или PBS с или без BPO-27 (R- или S-энантиомеры)) (среднее±SEM, n=6-7 петель на группу, ** p <0,01, ns, несущественно). (справа) Репрезентативные фотографии петель с введением CDCA и PBS с или без BPO-27. (C.) (слева) Отношение веса к длине петель толстой кишки, инъецированной CDCA (2,5, 10 мМ) или PBS с или без (R)-BPO-27 (среднее±SEM, n=4-7 петель на группу, ** p <0,01, ns, несущественно). (справа) Репрезентативные фотографии CDCA и PBS петель с инъекцией с или без (R)-BPO-27. (D.) Отношение веса к длине петель средней кишки или толстой кишки мышей с муковисцидозом (CFTR-дефицит), которым вводили CDCA (2,5, 10 мМ) (среднее±SEM, n=4 петель на группу, ** p <0,01, ns, несущественно).
[25] Фигура 8. (R)-BPO-27 снижает увеличение содержания воды в стуле в модели хологенной диареи у крыс. (A.) Протокол эксперимента (вверху) и фотографии (снизу), сделанные через 10 минут после инфузии в середину толстой кишки 500 мкл PBS, содержащего синий краситель Эвана. (B.) Четырехчасовое выделение стула (сырой вес) после инфузии в середину толстой кишки у крыс с предварительной обработкой (R)-BPO-27 или без нее (среднее±SEM, n=4 крысы в группе, обработанной PBS, n=8 крыс в группе, обработанной CDCA, * p <0,05, ns, несущественно). (C.) (слева) Содержание воды в стуле (процент воды при измерении сырого/сухого веса) в стуле, собранном в B (** p <0,01, ns, несущественно). (справа) Парный анализ, показывающий увеличение содержания воды в стуле у отдельных крыс (вода в стуле через 0-4 часа минус вода в стуле перед инфузией у тех же крыс) (* p<0,05, ** p <0,01, ns, несущественно).
ПОДРОБНОЕ ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[26] Настоящее изобретение можно понять со ссылкой на следующее подробное описание, которое составляет часть данного изобретения. Изобретение не ограничивается конкретными способами, условиями или параметрами, описанными и/или показанными в настоящем документе, а терминология, используемая в настоящем документе, предназначена для описания конкретных вариантов осуществления изобретения только в качестве примера и не предназначена для ограничения заявленного изобретения.
[27] Научные и технические термины, используемые в связи с настоящей заявкой, имеют значения, которые обычно понимаются специалистами в данной области, если иное не определено в настоящем документе.
[28] В настоящем документе, термины «композиция», «соединение», «лекарственное средство», «фармакологически активный агент», «активный агент» или «медицинский препарат» используются в настоящем документе взаимозаменяемо для обозначения соединения или соединений или композиций вещества, которые при введении субъекту (человеку или млекопитающему) вызывает желаемый фармакологический и/или физиологический эффект за счет местного и/или системного действия.
[29] В настоящем документе, термины «лечение» или «терапия» (а также их различные формы) включают предупреждающее (например, профилактическое), лечебное или паллиативное лечение. Как используется в настоящем документе, термин «лечение» включает облегчение или уменьшение по меньшей мере одного неблагоприятного или отрицательного эффекта или симптома состояния, заболевания или расстройства.
[30] Термин «введение» означает прямое введение соединения или композиции по настоящему изобретению.
[31] Термин «субъект» используется в настоящем документе для обозначения человека или домашнего млекопитающего (например, собаки, кошки), которому предоставляется лечение, включая профилактическое лечение, соединениями по настоящему изобретению.
[32] В рамках настоящего изобретения описанные соединения могут быть получены в виде фармацевтически приемлемых солей. «Фармацевтически приемлемые соли» относятся к производным описанных соединений, в которых исходное соединение модифицировано путем получения его кислотных или основных солей. Примеры фармацевтически приемлемых солей включают, но не ограничиваются ими, соли минеральных или органических кислот с основными остатками, такими как амины; щелочные или органические соли кислотных остатков, таких как карбоновые кислоты; и тому подобное. Фармацевтически приемлемые соли включают обычные нетоксичные соли или соли четвертичного аммония исходного соединения, образованные, например, из нетоксичных неорганических или органических кислот. Например, такие обычные нетоксичные соли включают соли, полученные из неорганических кислот, таких как хлористоводородная, бромистоводородная, серная, сульфаминовая, фосфорная, азотная и тому подобные; и соли, полученные из органических кислот, таких как уксусная, пропионовая, янтарная, гликолевая, стеариновая, молочная, яблочная, винная, лимонная, аскорбиновая, памоиновая, малеиновая, гидроксималеиновая, фенилуксусная, глутаминовая, бензойная, салициловая, сульфаниловая, 2-ацетоксибензойная, фумаровая, толуолсульфоновая, метансульфоновая, этан-дисульфоновая, щавелевая, изетионовая и тому подобные. Эти фармацевтически приемлемые соли получают способами, известными в данной области, например, растворением свободных оснований амина с избытком кислоты в водном спирте или нейтрализацией свободной карбоновой кислоты основанием щелочного металла, таким как гидроксид, или амином.
[33] Настоящее изобретение относится к способам лечения субъекта, страдающего хологенной диареей, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для лечения хологенной диареи.
[34] В некоторых аспектах настоящее изобретение относится к способам лечения субъекта, страдающего хологенной диареей. Хологенная диарея (BAD) представляет собой клинически диагностируемое состояние, при котором считается, что диарея является результатом мальабсорбции или нарушения регуляции желчных кислот. Смотри, например, M. Camilleri, Advances in understanding of bile acid diarrhea, Expert Rev Gastroenterol Hepatol. 2014 January ; 8(1): 49-61. Способы диагностики BAD известны в данной области. Смотри, например, ссылку выше.
[35] В некоторых аспектах способов, описанных в настоящем документе, субъекту вводят некоторое количество ингибитора хлоридных каналов CFTR (CFTR-CCI). Как используется в настоящем документе, хлоридный канал CFTR относится к регулятору трансмембранной проводимости при муковисцидозе (CFTR), хлоридному каналу, активированному cAMP, экспрессированному в эпителии легких, кишечника, поджелудочной железы, семенников и других тканей. Термин «ингибитор хлоридного канала CFTR» (или «CFTR-CCI»), как используется в настоящем документе, относится к ингибиторам хлоридного канала регулятора трансмембранной проводимости при муковисцидозе, описанным в предшествующем уровне техники как используемые для одной или нескольких медицинских целей, включая те, которые описаны в патентах США №№ 9062073, 7235573, 7638543, 7414037 и 7888332; в публикации заявки США № 2009/0253799; в публикациях международных патентных заявок №№ WO 09/120803 и WO 09/146144; и Ma T, et al. Thiazolidinone CFTR inhibitor identified by high-throughput screening blocks cholera toxin-induced intestinal fluid secretion. J. Clin. Invest. 2002;110:1651-1658; Sonawane N, Verkman AS. Thiazolidinone CFTR inhibitors with improved water solubility identified by structure-activity analysis. Bioorg. Med. Chem. 2008;16:8187-8195, и Muanprasat C, et al. Discovery of glycine hydrazide pore-occluding CFTR inhibitors: mechanism, structure-activity analysis, and in vivo efficacy. J. Gen. Physiol. 2004;124:125-137 Каждая из этих ссылок полностью включена в настоящий документ посредством ссылки.
[36] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой ингибитор хлоридных каналов BPO CFTR (BPO-CFTR-CCI). BPO-CFTR-CCI представляют собой соединения, охватываемые общей структурой
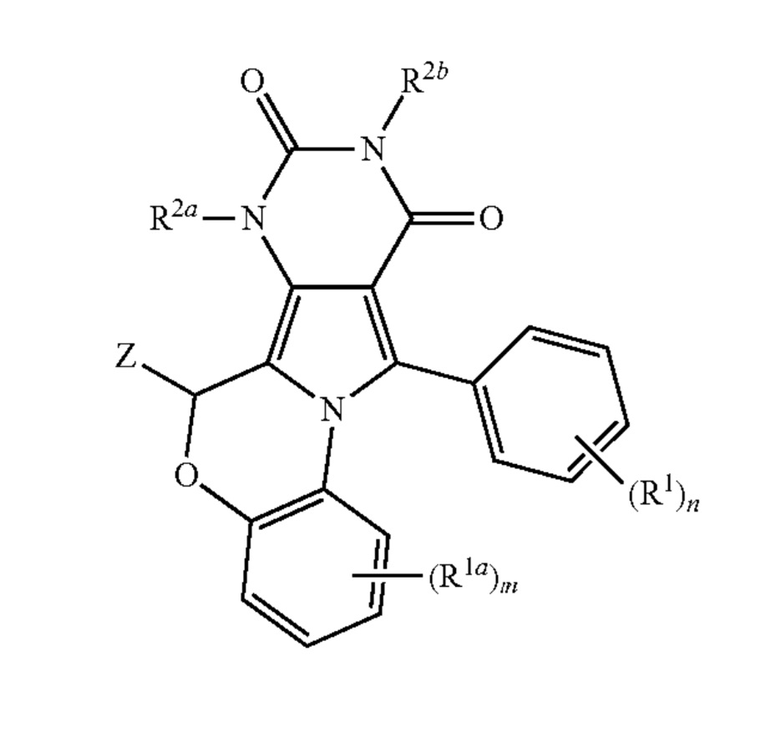
где:
m равно 1, 2, 3 или 4;
n равно 1, 2, 3, 4 или 5;
p равно целому числу от 0 до 4;
q равно целому числу от 1 до 4;
R1 в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-C6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R1a в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-C6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R2a и R2b, каждый, являются одинаковыми или различными и, независимо, представляют собой H или C1-C6 алкил;
R4a представляет собой -OR7, -NR7R8, -O(CH2)q-OC(O)R7 или остаток аминокислоты;
R7 и R8, каждый, являются одинаковыми или различными и, независимо, представляют собой H, C1-C20 алкил, сахарид или остаток аминокислоты; и
Z представляет собой арил или гетероарил,
где остаток аминокислоты выбран из остатков аланина, аргинина, аспарагина, аспарагиновой кислоты, цистеина, глутамина, глутаминовой кислоты, глицина, гистидина, изолейцина, лейцина, лизина, метионина, фенилаланина, пролина, серина, треонина, триптофана, тирозина, валина, фосфосерина, фосфотреонина, фосфотирозина, 4-гидроксипролина, гидроксилизина, демозина, изодемозина, гамма-карбоксиглутамата, гиппуровой кислоты, октагидроиндол-2-карбоновой кислоты, статина, 1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты, пеницилламина, орнитина, 3-метилгистидина, норвалина, бета-аланина, гамма-аминомасляной кислоты, циртуллина, гомоцистеина, гомосерина, метилаланина, пара-бензоилфенилаланина, фенилглицина, пропаргилглицина, саркозина, метионинсульфона, трет-бутилглицина, 3,5-дибромтирозина, 3,5-дииодтирозина, гликозилированного треонина, гликлозилированного серина и гликозилированного аспарагина.
[37] В некоторых вариантах осуществления изобретения BPO-CFTR-CCI представляет собой соединение формулы
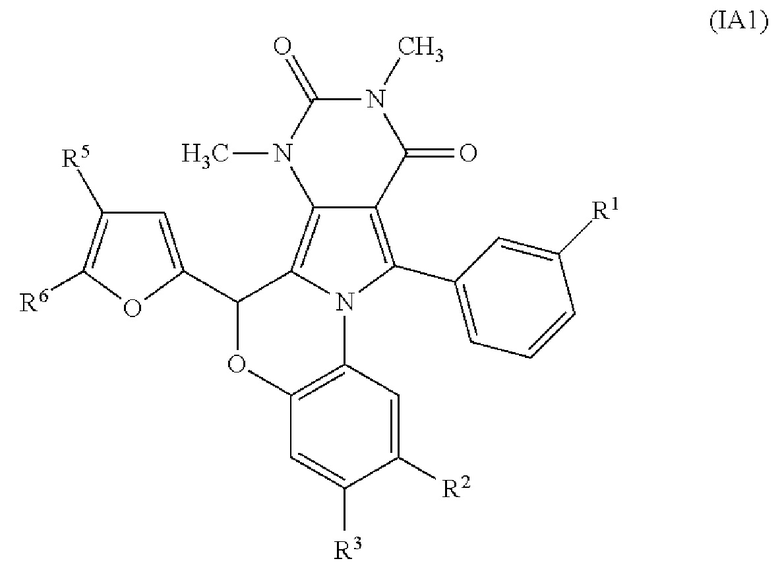
где:
R1 представляет собой H, галоген или C1-6 алкил;
R2 и R3, каждый, являются одинаковыми или различными и, независимо, представляют собой H, галоген, -NO2, C1-6 алкил, тетразолил, -S(O)2OR7 или -C(═O)OR7;
R5 представляет собой H, галоген или C1-6 алкил;
R6 представляет собой галоген, C1-6 алкил или C1-6 галогеналкил; и
R7 представляет собой H, C1-6 алкил, сахарид, остаток аминокислоты или пептид.
[38] BPO-CFTR-CCI описаны в патенте США № 9062073, который полностью включен в настоящий документ посредством ссылки.
[39] В некоторых вариантах осуществления изобретения BPO-CFTR-CCI представляет собой (R)-BPO-27, соединение, имеющее структуру:
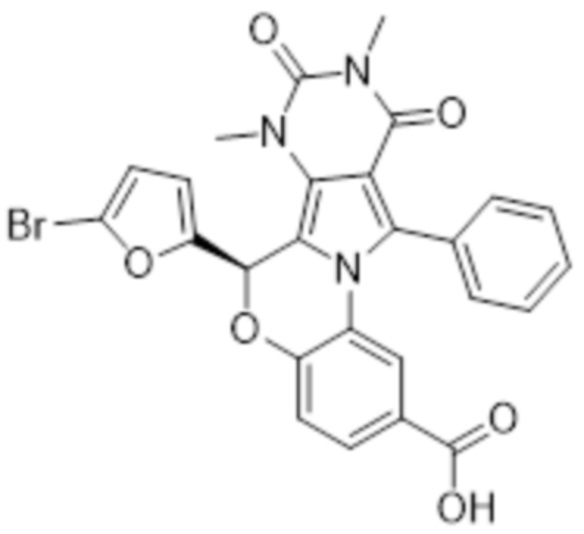
[40] В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой ингибитор хлоридных каналов PPQ CFTR (PPQ-CFTR-CCI). PPQ-CFTR-CCI представляют собой соединения, охватываемые общей структурой
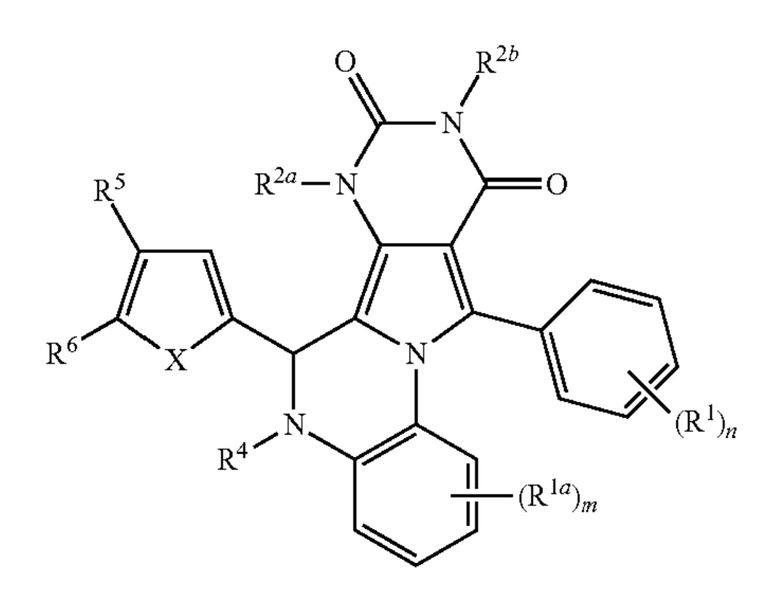
где:
m равно 1, 2, 3, или 4;
n равно 1, 2, 3, 4 или 5;
p равно целому числу от 0 до 4;
q равно целому числу от 1 до 4;
X представляет собой O или S;
R1 в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R1a в каждом случае является одинаковым или различным и, независимо, представляет собой H, галоген, галогеналкил, C1-6 алкил, -(CH2)p-C(O)-R4a, -S(O)2R4a, -NO2 или тетразолил;
R2a и R2b, каждый, являются одинаковыми или различными и, независимо, представляют собой H или C1-6 алкил;
R4a представляет собой -OR7, -NR7R8, -O(CH2)q-OC(O)R7, остаток аминокислоты или пептид;
R4 представляет собой H, -N(═O), C1-6 алкил или галогеналкил;
R5 представляет собой H, галоген или C1-6 алкил;
R6 представляет собой галоген, C1-6 алкил или C1-6 галогеналкил; и
R7 и R8, каждый, являются одинаковыми или различными и, независимо, представляют собой H, C1-20 алкил, сахарид, остаток аминокислоты или пептид.
[41] PPQ-CFTR-CCI описаны в патенте США № 9062073, который полностью включен в настоящий документ посредством ссылки.
[42] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой ингибитор тиазолидиноновых хлоридных каналов CFTR (TD-CFTR-CCI). TD-CFTR-CCI представляют собой соединения, охватываемые общей структурой:
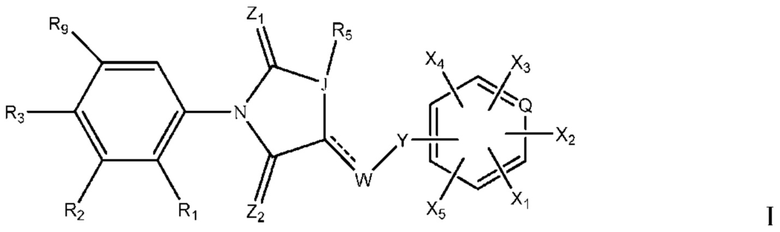
или их фармацевтически приемлемые соли, пролекарства или стереоизомеры,
где
Y представляет собой -NH- или отсутствует;
W представляет собой =CH-, -S-, -O-, -C(=S)- или -C(=O)-;
Z1, Z2, Z3, Z4 и Z5, каждый, независимо, представляют собой O или S;
J представляет собой C, S, O или N;
Q представляет собой C или N;
R1, R2, R3 и R9, каждый. независимо, представляют собой H, C1-6 алкил, алкокси, галоген, -CF3, -CF2CF3 или -OCF3;
R5 представляет собой H, галоген, C1-6 алкил или отсутствует;
X1, X2, X3 и X4, каждый, независимо, представляют собой H, -OH, -SH, галоген, тетразоло, -P(=O)(OH)2, -C(=Z3)Z4H, -Z5-C(=Z3) Z4H или -Z5-CH2-C(=Z3)Z4H; и
X5 представляет собой -O-, тетразоло, -C(=O)OH, -O-C(=O)OH или отсутствует.
[43] TD-CFTR-CCI также представляют собой соединения, охватываемые общей структурой:
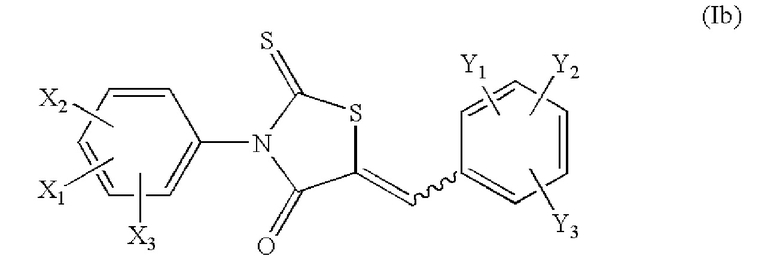
где X1 представляет собой трифторметил;
X2 и X3 независимо выбраны из водорода и группы галогенов;
Y1, Y2 и Y3 независимо выбраны из водорода, C1-C8 алкила, C1-C7 алкокси, карбоната, карбамата, карбоксила, группы галогенов, нитро группы, азо группы, гидроксильной группы и меркапто группы.
[44] TD-CFTR-CCI также представляют собой соединения, описанные Ma T, et al. Thiazolidinone CFTR inhibitor identified by high-throughput screening blocks cholera toxin-induced intestinal fluid secretion. J. Clin. Invest. 2002;110:1651-1658; и Sonawane N, Verkman AS. Thiazolidinone CFTR inhibitors with improved water solubility identified by structure-activity analysis. Bioorg. Med. Chem. 2008;16:8187-8195; в патентах США №№ 7235573, 7638543, и публикации международной патентной заявки № WO 09/120803. Полностью каждая из этих ссылок включена в качестве ссылки в настоящий документ.
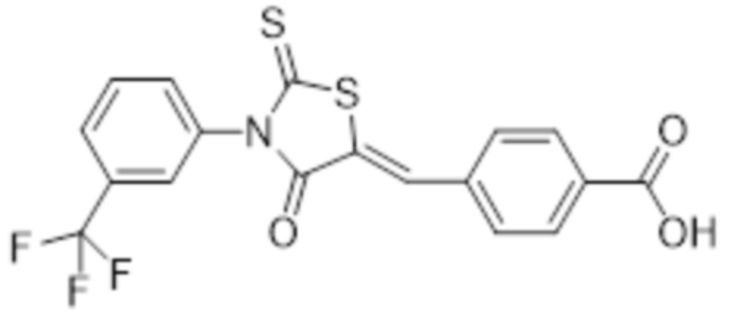
[45] В некоторых вариантах осуществления изобретения TD-CFTR-CCI представляет собой CFTRinh-172, который имеет структуру:
[46] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой ингибитор хлоридных каналов глицингидразид CFTR (GH-CFTR-CCI). GH-CFTR-CCI представляют собой соединения, охватываемые структурой:
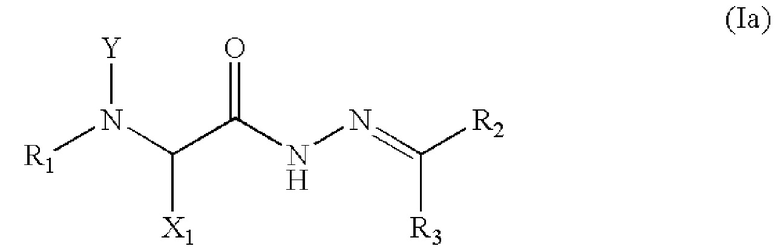
или их фармацевтически приемлемые соли или стереоизомеры,
где X1 представляет собой водород или замещенный или незамещенный насыщенный прямой или разветвленный алкил;
Y представляет собой водород или замещенный или незамещенный, насыщенный прямой или разветвленный алкил;
R1 представляет собой незамещенный фенил,
замещенный фенил где фенил замещен одним или несколькими гидрокси, алкилами и галогенами,
замещенный или незамещенный хинолинил,
замещенный или незамещенный антраценил или
замещенный или незамещенный нафаленил;
R2 представляет собой незамещенный фенил,
замещенный фенил, где фенил замещен бромом или карбокси,
ди(гидрокси)фенил,
моно(галоген)-моно(гидрокси)фенил,
моно(галоген)-ди(гидрокси)фенил,
моно(галоген)-три(гидрокси)фенил,
ди(галоген)-моно(гидрокси)фенил,
ди(галоген)-ди(гидрокси)фенил,
ди(галоген)-три(гидрокси)фенил,
моно(галоген)-моно(гидрокси)-моно(алкокси)фенил,
моно(галоген)-ди(гидрокси)-моно(алкокси)фенил,
моно(галоген)-моно(гидрокси)-ди(алкокси)фенил,
моно(галоген)-ди(гидрокси)-ди(алкокси)фенил,
ди(галоген)-моно(гидрокси)-моно(алкокси)фенил,
ди(галоген)-ди(гидрокси)-моно(алкокси)фенил,
ди(галоген)-моно(гидрокси)-ди(алкокси)фенил, и
R3 представляет собой водород или замещенный или незамещенный алкил.
[47] GH-CFTR-CCI также представляют собой соединения, охватываемые общей формулой:
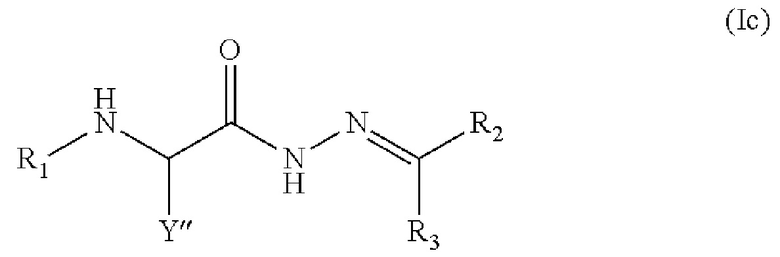
или их фармацевтически приемлемые соли или стереоизомеры,
где Yʺ представляет собой замещенный или незамещенный насыщенный прямой или разветвленный алкил; или амид или эфирный линкер, присоединенный к полярной молекуле, где полярная молекула выбрана из замещенной или незамещенной фенильной группы, простого полиоксиалкилполиэфира, полиэтиленимина, дисахарида, трисахарида, полиалкилимина и небольшого аминодекстрана;
R1 представляет собой незамещенный или замещенный фенил, замещенный или незамещенный хинолинил, замещенный или незамещенный антраценил, или замещенный или незамещенный нафаленил;
R2 представляет собой незамещенный или замещенный фенил; и
R3 представляет собой водород или замещенный или незамещенный алкил, тем самым ингибируя CFTR.
[48] GH-CFTR-CCI также представляют собой соединения, охватываемые общей формулой:
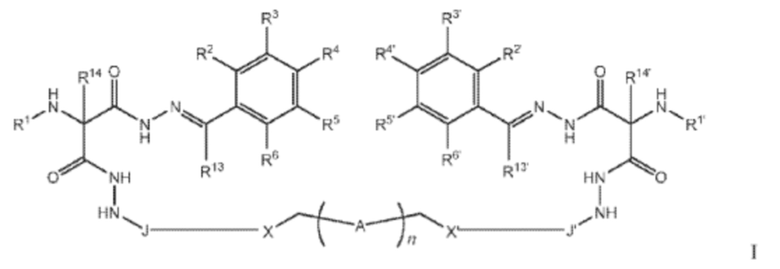
или их фармацевтически приемлемые соли, пролекарства или стереоизомеры,
где:
R1 и R1 являются одинаковыми или различными и, независимо, представляют собой необязательно замещенный фенил, необязательно замещенный гетероарил, необязательно замещенный хинолинил, необязательно замещенный антраценил, или необязательно замещенный нафаленил;
R2, R2ʼ, R3, R3ʼ, R4, R4ʼ, R5, R5ʼ, R6 и R6ʼ, каждый, являются одинаковыми или различными и, независимо, представляют собой водород, гидрокси, Ci g алкил, Ci g алкокси, карбокси, галоген, нитро, циано, -SO3H, -S(=O)2NH2, арил и гетероарил;
R13, R13, R14 и R14, каждый, являются одинаковыми или различными и, независимо, представляют собой водород или C1-8 алкил;
X и Xʼ представляют собой одинаковые или разные линкерные фрагменты;
J и Jʼ, каждый, являются одинаковыми или различными спейсерными фрагментами;
A представляет собой полимерную субъединицу; и n обозначает целое числом между 0 и 2500.
[49] GH-CFTR-CCI также представляют собой соединения, описанные Muanprasat C, et al. Discovery of glycine hydrazide pore-occluding CFTR inhibitors: mechanism, structure-activity analysis, and in vivo efficacy. J. Gen. Physiol. 2004;124:125-137; в патентах США №№ 7414037 и 7888332; в публикации заявки на патент США № 2009/0253799; в публикации международной патентной заявки № WO 09/146144. Полностью каждая из этих ссылок включена в настоящий документ в качестве ссылки.
[50] В некоторых вариантах осуществления изобретения GH-CFTR-CCI представляет собой GlyH-101, который имеет структуру
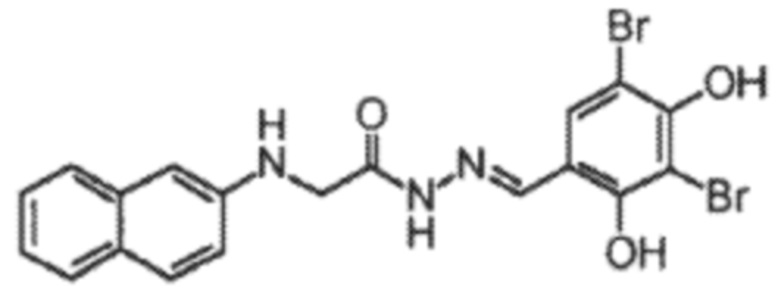 .
.
[51]
[52] Другими ингибиторами хлоридных каналов CFTR являются глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат и нифлумовая кислота.
[53] В некоторых вариантах осуществления способов, описанных в настоящем документе, субъекту вводят ингибитор хлоридных каналов CFTR, который представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI.
[54] В некоторых вариантах осуществления способов, описанных в настоящем документе, субъекту вводят (R)-BPO-27, CFTRinh-172, GlyH-101, глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию.
[55] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI.
[56] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI.
[57] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения TD-CFTR-CCI представляет собой CFTRinh-172.
[58] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения GH-CFTR-CCI представляет собой GlyH-101.
[59] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой дифениламин-2-карбоксилат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой 5-нитро-2-(3-фенилпропиламино)бензоат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой нифлумовую кислоту.
[60] В некоторых вариантах осуществления способов по настоящему описанию субъекту вводят фармацевтическую композицию, содержащую фармацевтический наполнитель и некоторое количество ингибитора хлоридных каналов CFTR.
[61] В некоторых аспектах изобретение относится к способам лечения субъекта, страдающего хологенной диареей, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридных каналов CFTR, эффективное для лечения хологенной диареи. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения BPO-CFTR-CCI представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения фармацевтическая композиция дополнительно содержит (S)-BPO-27. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения TD-CFTR-CCI представляет собой CFTRinh-172. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения GH-CFTR-CCI представляет собой GlyH-101. В еще других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию.
[62] В таких вариантах осуществления изобретения, когда субъекту вводят фармацевтическую композицию, содержащую ингибитор хлоридных каналов CFTR, который представляет собой (R)-BPO-27, фармацевтическая композиция также может включать (S)-BPO-27. В этих вариантах осуществления изобретения количество (R)-BPO-27 в фармацевтической композиции будет по существу равно или больше чем количество (S)-BPO-27, присутствующего в фармацевтической композиции. Например, в некоторых вариантах осуществления изобретения фармацевтическая композиция может включать рацемическую смесь (R/S)-BPO-27. В некоторых аспектах (R)-BPO-27 будет присутствовать в энантиомерном избытке (эи) по сравнению с (S)-BPO-27. Например, (R)-BPO-27 может присутствовать примерно в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 99% эи. В некоторых вариантах осуществления изобретения фармацевтическая композиция будет включать (R)-BPO-27, где % эи составляет более 99%.
[63] Количество вводимого ингибитора хлоридных каналов CFTR является эффективным для лечения хологенной диареи. Количество, которое эффективно в этом отношении, будет варьироваться в зависимости от характеристик и состояния пациента.
[64] В некоторых аспектах описанных способов количество ингибитора хлоридных каналов CFTR является эффективным для снижения секреции кишечного сока, происходящей в результате хологенной диареи.
[65] В других аспектах описанных способов количество ингибитора хлоридных каналов CFTR является эффективным для снижения вызванной желчной кислотой активации апикальных хлоридных каналов CFTR.
[66] В некоторых аспектах описанных способов субъекту также вводят некоторое количество второго агента, эффективного для лечения хологенной диареи. В некоторых вариантах осуществления изобретения второй агент представляет собой вещество, связывающее желчные кислоты, агонист рецептора фарнезоида X (FXR), антагонист 5-HT3, агонист опиоидного рецептора, смешанный агонист опиоидного μ-рецептора, кишечно-специфический антибиотик широкого спектра действия или кишечно-специфический антибиотик широкого спектра действия. В некоторых вариантах осуществления изобретения второй агент представляет собой вещество, связывающее желчные кислоты, предпочтительно, холестирамин, колестипол или колесевелам. В других вариантах осуществления изобретения второй агент представляет собой агонист рецептора фарнезоида X (FXR), предпочтительно, обетихолевую кислоту. В других вариантах осуществления изобретения второй агент представляет собой антагонист 5-HT3, предпочтительно, алозетрон. В других вариантах осуществления изобретения второй агент представляет собой агонист опиоидных рецепторов, предпочтительно, лоперамид. В других вариантах осуществления изобретения второй агент представляет собой смешанный агонист опиоидного μ-рецептора, предпочтительно, элюксадолин. В других вариантах осуществления изобретения второй агент представляет собой кишечно-специфический антибиотик широкого спектра действия, предпочтительно, рифаксимин.
[67] В некоторых аспектах настоящее изобретение относится к способам снижения секреции кишечного сока, происходящей в результате индуцированной желчной кислотой активации хлоридных каналов CFTR, в кишечном эпителии у субъекта, нуждающегося в этом, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для снижения секреции кишечного сока, происходящей в результате индуцированной желчной кислотой активации хлоридных каналов CFTR.
[68] Как используется в настоящем документе, секреция кишечного сока относится к секреции кишечного сока из кишечного эпителия в просвет кишечника.
[69] В некоторых вариантах осуществления изобретения секреция кишечного сока является результатом индуцированной желчной кислотой активации хлоридных каналов CFTR в кишечном эпителии. В других вариантах осуществления изобретения хлоридные каналы CFTR представляют собой апикальные хлоридные каналы CFTR в кишечном эпителии. Апикальные хлоридные каналы CFTR представляют собой хлоридные каналы CFTR, расположенные в апикальной клеточной мембране (то есть в клеточной мембране, обращенной к просвету кишечника). Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способам снижения секреции кишечного сока, происходящей в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой, в кишечном эпителии у субъекта, нуждающегося в этом, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для снижения секреции кишечного сока, происходящей в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой.
[70] В некоторых аспектах секреция кишечного сока снижается путем введения количества ингибитора хлоридных каналов CFTR, эффективного для снижения указанной секреции кишечного сока. Как используется в настоящем документе, уменьшение секреции кишечного сока относится к уменьшению количества жидкости, которая секретируется в просвет кишечника, по сравнению с количеством жидкости, которая секретируется в просвет кишечника при отсутствии введения ингибитора хлоридных каналов CFTR. Способы измерения уменьшения секреции жидкости известны специалистам в данной области и включают измерение содержания воды в содержимом просвета кишечника и диареи.
[71] В некоторых вариантах осуществления изобретения секреция кишечного сока снижается путем введения ингибитора хлоридных каналов CFTR, который представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения секреция кишечного сока снижается путем введения ингибитора хлоридных каналов CFTR, который представляет собой (R)-BPO-27, CFTRinh-172, GlyH-101, глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой CFTRinh-172. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GlyH-101. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой дифениламин-2-карбоксилат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой 5-нитро-2-(3-фенилпропиламино)бензоат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой нифлумовую кислоту.
[72] В этом аспекте изобретения количество вводимого ингибитора хлоридных каналов CFTR является количеством, которое эффективно для снижения указанной секреции кишечного сока, происходящей в результате индуцированной желчной кислотой активации хлоридных каналов CFTR (например, апикальных хлоридных каналов CFTR). Количество, которое эффективно в этом отношении, будет варьироваться в зависимости от характеристик и состояния пациента.
[73] В некоторых аспектах настоящее изобретение относится к способам снижения секреции кишечного сока, происходящей в результате индуцированной желчной кислотой активации хлоридных каналов CFTR, в кишечном эпителии у субъекта, нуждающегося в этом, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридных каналов CFTR, эффективного для снижения секреции кишечного сока, происходящей в результате индуцированной желчной кислотой активации хлоридных каналов CFTR. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения BPO-CFTR-CCI представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения фармацевтическая композиция дополнительно содержит (S)-BPO-27. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения TD-CFTR-CCI представляет собой CFTRinh-172. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения GH-CFTR-CCI представляет собой GlyH-101. В еще других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию.
[74] В других аспектах изобретение относится к способам снижения индуцированного желчной кислотой потока хлоридного канала CFTR в кишечном эпителии субъекта, нуждающегося в этом, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для снижения указанного индуцированного желчной кислотой потока хлоридных каналов CFTR.
[75] Как используется в настоящем документе, термин «поток» относится к прохождению ионов через канал. Таким образом, поток хлоридного канала CFTR относится к прохождению хлорид-ионов через хлоридный канал CFTR.
[76] В некоторых вариантах осуществления изобретения поток хлоридного канала CFTR возникает в результате активации апикальных хлоридных каналов CFTR, индуцированной желчной кислотой, в кишечном эпителии. Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способам снижения потока апикального хлоридного канала CFTR, вызванного желчной кислотой, в кишечном эпителии субъекта, нуждающегося в этом, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для снижения указанного потока апикального хлоридного канала CFTR, вызванного желчной кислотой.
[77] В некоторых вариантах осуществления изобретения поток индуцированного желчной кислотой потока хлоридного канала CFTR в кишечном эпителии снижается путем введения ингибитора хлоридных каналов CFTR, который представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения поток индуцированного желчной кислотой потока хлоридного канала CFTR в кишечном эпителии снижается путем введения ингибитора хлоридных каналов CFTR, который представляет собой (R)-BPO-27, CFTRinh-172, GlyH-101, глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию.
[78] В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой CFTRinh-172. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GlyH-101. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой дифениламин-2-карбоксилат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой 5-нитро-2-(3-фенилпропиламино)бензоат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой нифлумовую кислоту.
[79] В этом аспекте изобретения количество вводимого ингибитора хлоридных каналов CFTR представляет собой количество, которое эффективно для снижения потока индуцированного желчной кислотой хлоридного канала CFTR (например, апикальных хлоридных каналов CFTR). Количество, которое эффективно в этом отношении, будет варьироваться в зависимости от характеристик и состояния пациента.
[80] В некоторых аспектах, настоящее изобретение относится к способам снижения индуцированного желчной кислотой потока хлоридного канала CFTR в кишечном эпителии субъекта, нуждающегося в этом, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридных каналов CFTR, эффективного для снижения указанного индуцированного желчной кислотой потока хлоридных каналов CFTR. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения BPO-CFTR-CCI представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения фармацевтическая композиция дополнительно содержит (S)-BPO-27. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения TD-CFTR-CCI представляет собой CFTRinh-172. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения GH-CFTR-CCI представляет собой GlyH-101. В еще других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию.
[81] В некоторых аспектах изобретение относится к способам лечения диареи или облегчения симптомов, связанных с диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающим введение субъекту количества ингибитора хлоридных каналов CFTR, эффективного для лечения указанной диареи или для облегчения симптомов указанной диареи. Как используется в настоящем документе симптомы диареи включают один или несколько из следующего: (1) повышенное содержание воды в стуле, (2) повышенная частота дефекации; (3) увеличение количества стула; (4) боль в животе; (5) вздутие живота и (6) тошнота.
[82] В некоторых вариантах осуществления изобретения способы лечения диареи или облегчения симптомов, связанных с диареей, у субъекта, перенесшего резекцию подвздошной кишки, включают введение субъекту ингибитора хлоридных каналов CFTR, который представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI.
[83] В некоторых вариантах осуществления изобретения способы лечения диареи или облегчения симптомов, связанных с диареей, у субъекта, перенесшего резекцию подвздошной кишки, включают введение субъекту ингибитора хлоридных каналов CFTR, который представляет собой (R)-BPO-27, CFTRinh-172, GlyH-101, глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой CFTRinh-172. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GlyH-101. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой дифениламин-2-карбоксилат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой 5-нитро-2-(3-фенилпропиламино)бензоат. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой нифлумовую кислоту.
[84] В этом аспекте изобретения количество вводимого ингибитора хлоридных каналов CFTR является эффективным для лечения диареи у субъекта или облегчения симптомов, связанных с диареей у субъекта. Количество, которое эффективно в этом отношении, будет варьироваться в зависимости от характеристик и состояния пациента.
[85] В некоторых аспектах изобретение относится к способам лечения диареи или облегчения симптомов, связанных с диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающим введение субъекту фармацевтической композиции, содержащей количество ингибитора хлоридных каналов CFTR, эффективное для лечения указанной диареи или для облегчения симптомов указанной диареи. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI, PPQ-CFTR-CCI, TD-CFTR-CCI или GH-CFTR-CCI. В некоторых вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой BPO-CFTR-CCI. В некоторых вариантах осуществления изобретения BPO-CFTR-CCI представляет собой (R)-BPO-27. В некоторых вариантах осуществления изобретения фармацевтическая композиция дополнительно содержит (S)-BPO-27. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой PPQ-CFTR-CCI. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой TD-CFTR-CCI. В некоторых вариантах осуществления изобретения TD-CFTR-CCI представляет собой CFTRinh-172. В других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой GH-CFTR-CCI. В некоторых вариантах осуществления изобретения GH-CFTR-CCI представляет собой GlyH-101. В еще других вариантах осуществления изобретения ингибитор хлоридных каналов CFTR представляет собой глибенкламид, дифениламин-2-карбоксилат, 5-нитро-2-(3-фенилпропиламино)бензоат или нифлумовую кислоту или их комбинацию.
[86] Во всех способах изобретения субъекту вводят ингибитор хлоридных каналов CFTR. В некоторых вариантах осуществления изобретения субъектом является млекопитающее. В других вариантах осуществления изобретения субъектом является человек.
[87] В некоторых вариантах осуществления изобретения у субъекта диагностирована болезнь Крона.
[88] В других вариантах осуществления изобретения у субъекта диагностирован IBS-D.
[89] В еще других вариантах осуществления изобретения у субъекта диагностирована функциональная диарея.
[90] В некоторых аспектах способы по настоящему изобретению приводят к снижению содержания воды в стуле субъекта. Степень уменьшения количества воды может быть определена путем измерения количества воды в стуле субъекта перед введением ингибитора хлоридных каналов CFTR и сравнения этого количества с количеством воды в стуле субъекта после введения ингибитора хлоридных каналов CFTR.
[91] В некоторых вариантах осуществления изобретения снижение содержания воды в стуле субъекта демонстрируется путем измерения с использованием клинического инструмента, такого как, например, Бристольская шкала формы стула (BSFS). BSFS, которая известна в данной области, присваивает стулу субъекта оценку консистенции от 1 (твердый) до 7 (водянистый). Таким образом, в некоторых вариантах осуществления изобретения снижение содержания воды в стуле субъекта с использованием настоящих способов демонстрируется снижением количества баллов по Бристольской шкале формы стула. В некоторых вариантах осуществления изобретения снижение содержания воды в стуле субъекта с использованием настоящих способов демонстрируется уменьшением на 1 балл (например, с 7 до 6, с 6 до 5, с 5 до 4, с 4 до 3, с 3 до 2, с 2 до 1) по Бристольской шкале формы стула. В других вариантах осуществления изобретения снижение содержания воды в стуле субъекта с использованием настоящих способов демонстрируется уменьшением на 2 балла (например, с 7 до 5, с 6 до 4, с 5 до 3, с 4 до 2, с 3 до 1) по Бристольской шкале формы стула. В других вариантах осуществления изобретения снижение содержания воды в стуле субъекта с использованием настоящих способов демонстрируется уменьшением на 3 балла (например, с 7 до 4, с 6 до 3, с 5 до 2, с 4 до 1) по Бристольской шкале формы стула. В других вариантах осуществления изобретения снижение содержания воды в стуле субъекта с использованием настоящих способов демонстрируется уменьшением более чем на 3 пункта по Бристольской шкале формы стула.
[92] Специалистам в данной области будет понятно, что снижение содержания воды в стуле субъекта может быть продемонстрировано с использованием других клинических шкал, известных в данной области.
[93] В некоторых аспектах способы по настоящему изобретению приводят к снижению частоты дефекации у субъекта. Степень снижения частоты дефекации может быть определена путем сравнения частоты дефекации у субъекта перед введением ингибитора хлоридных каналов CFTR с частотой дефекации у субъекта после введения ингибитора хлоридных каналов CFTR. В настоящем документе частота дефекации может быть определена, например, путем опроса субъекта или введения субъекту инструмента, предназначенного для получения этой информации. Способы определения частоты дефекации известны специалистам в данной области.
[94] В других аспектах способы по настоящему изобретению приводят к уменьшению выделения стула у субъекта. Степень снижения выделения стула может быть определена путем измерения количества стула пациента перед введением ингибитора хлоридных каналов CFTR и сравнения этого количества с количеством стула пациента после введения ингибитора хлоридных каналов CFTR. В настоящем документе количество может быть измерено по весу или по объему. Способы измерения диуреза известны специалистам в данной области.
[95] В других аспектах способы по настоящему изобретению приводят к уменьшению боли в животе у субъекта. Степень уменьшения боли в животе может быть определена путем сравнения боли в животе субъекта перед введением ингибитора хлоридных каналов CFTR с болью в животе субъекта после введения ингибитора хлоридных каналов CFTR. В настоящем документе боль в животе может быть оценена, например, путем опроса субъекта или введения субъекту инструмента, предназначенного для получения этой информации. Способы определения боли в животе известны специалистам.
[96] В других аспектах способы по настоящему изобретению приводят к уменьшению вздутия живота у субъекта. Степень уменьшения вздутия живота может быть определена путем сравнения вздутия живота у субъекта перед введением ингибитора хлоридного канала CFTR со вздутием живота у субъекта после введения ингибитора хлоридного канала CFTR. В настоящем документе вздутие живота может быть оценено, например, путем опроса субъекта или введения субъекту инструмента, предназначенного для получения этой информации. Способы определения вздутия живота известны специалистам.
[97] В других аспектах способы по настоящему изобретению приводят к уменьшению тошноты у субъекта. Степень уменьшения тошноты может быть определена путем сравнения тошноты у субъекта перед введением ингибитора хлоридных каналов CFTR с тошнотой у субъекта после введения ингибитора хлоридных каналов CFTR. В настоящем документе тошнота может быть оценена, например, путем опроса субъекта или введения субъекту инструмента, предназначенного для получения этой информации, такого как анкета для определения тошноты. Способы измерения тошноты известны специалистам.
Примеры
[98] Следующие далее примеры представлены для лучшего понимания объекта изобретения, описанного в настоящем документе. Эти примеры не следует рассматривать как ограничивающие описанный объект изобретения. Понятно, что примеры и варианты осуществления, описанные в настоящем документе, предназначены только для иллюстративных целей, и что различные модификации или изменения в этом свете будут очевидны специалистам в данной области техники и должны быть включены в объем, а также могут быть выполнены без отклонения от объема настоящего изобретения.
Сокращения
[99] BAD: хологенная диарея
[100] BAPTA-AM: тетракис(ацетоксиметиловый эфир) 1,2-бис(2-аминофенокси)этан-N, N,Nʼ,Nʼ-тетрауксусной кислоты
[101] BPO-27: 6-(5-бромфуран-2-ил)-7,9-диметил-8,10-диоксо-11-фенил-7,8,9,10-тетрагидро-6H-бензо[b]пиримидо[4ʼ,5ʼ:3,4]-пирроло[1,2-d][1,4]оксазин-2-карбоновая кислота
[102] CaCC: хлоридный канал, активируемый кальцием
[103] CDCA: хенодезоксихолевая кислота
[104] CFTR: регулятор трансмембранной проводимости при муковисцидозе
[105] CFTRinh-172: 4-[[4-оксо-2-тиоксо-3-[3-(трифторметил)-фенил]-5-тиазолидинилиден]метил]бензойная кислота
[106] DCA: дезоксихолевая кислота
[107] DRA: пониженная регуляция при аденоме
[108] ENaC: эпителиальный натриевый канал
[109] FGF-19: фактор роста фибробластов 19
[110] FXR: рецептор фарнезоида X
[111] GlyH-101: N-2-нафталенил-[(3,5-дибром-2,4-дигидроксифенил)метилен]глицингидразид
[112] IBS-D: синдром раздраженного кишечника с преобладанием диареи
[113] IC50: полумаксимальная ингибирующая концентрация
Химические вещества
[114] Если не указано иное, все химические вещества были приобретены у компании Sigma-Aldrich (St. Louis, MO). Натриевые соли таурохенодезоксихолевой кислоты и тауродезоксихолевой кислоты были приобретены у компании Spectrum Chemicals (Gardena, CA). Все растворы желчных кислот готовили в PBS, за исключением литохолевой кислоты, которую растворяли в ДМСО. BAPTA-AM был приобретен у компании EMD Millipore (Billerica, MA). Форсколин был приобретены у компании Lc Laboratories (Woburn, MA). CFTRinh-172 и (R)-BPO-27 были синтезированы и очищены, как описано. Смотри, например, Snyder, D. S., Tradtrantip, L., Yao, C., Kurth, M. J., and Verkman, A. S. (2011) Potent, metabolically stable benzopyrimido-pyrrolo-oxazine-dione (BPO) CFTR inhibitors for polycystic kidney disease. J Med Chem 54, 5468-5477; Snyder, D. S., Tradtrantip, L., Battula, S., Yao, C., Phuan, P. W., Fettinger, J. C., Kurth, M. J., and Verkman, A. S. (2013) Absolute configuration and biological properties of enantiomers of CFTR inhibitor BPO-27. ACS Med Chem Lett 4, 456-459; Ma, T., Thiagarajah, J. R., Yang, H., Sonawane, N. D., Folli, C., Galietta, L. J., and Verkman, A. S. (2002) Thiazolidinone CFTR inhibitor identified by high-throughput screening blocks cholera toxin-induced intestinal fluid secretion. J Clin Invest 110, 1651-1658.
Пример 1. Культура клеток Т84
[115] Клетки T84 (ATCC CCL-248) культивируют в смеси 1:1 среды DMEM/Hamʼs F-12 с добавлением 10% FBS, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина. Клетки выращивают на вкладышах Snapwell (Costar Corning, Horseheads, NY) при температуре 37ºC в атмосфере 5% CO2/95% воздуха и используют через 7-14 дней после посева.
Пример 2. Культуры колоноидов человека
[116] Культуры колоноидов человека получают из неидентифицированных образцов тканей (кроме возраста и пола), полученных в результате эндоскопических или хирургических процедур у трех разных субъектов. Человеческие культуры генерируют из изолированных кишечных крипт, встроенных в матригель (Corning, Tewksbury, MA) в 24-луночных планшетах, и культивируют в присутствии Wnt3A, R-spondin-1 и Noggin, содержащих недифференцированные среды (UDM), как описано Zachos, N. C. et. al (2016) Human enteroids/colonoids и intestinal organoids functionally recapitulate normal intestinal physiology and pathophysiology. J Biol Chem 291, 3759-3766; In, J., et al. (2016) Enterohemorrhagic escherichia coli reduce mucus and intermicrovillar bridges in human stem cell-derived colonoids. Cell Mol Gastroenterol Hepatol 2, 48-62. Культуры матригеля в среде UDM используются для размножения колоноидов. Для создания однослойных культур колоноиды растирают в растворе для сбора органоидов Cultrex (Trevigen, Gaithersburg, MD), и фрагменты собирают центрифугированием и ресуспендируют в UDM. Фрагменты колоний (100 мкл) высевают на вставки для 24-луночных культур клеток из полиэфирной мембраны с порами 0,4 мкм (Transwell; Corning, Tewksbury, MA), предварительно покрытые человеческим коллагеном IV (34 мкг/мл; Millipore Sigma). Монослои культивируют в UDM при температуре 37ºC, 5% CO2. В этих условиях культуры достигают слияния через 7-14 дней, что контролируется трансэпителиальной резистентностью.
Пример 3. Измерение тока короткого замыкания
[117] Клетки T84 помещают в камеры Уссинга и погружают в симметричный буферный раствор HCO3-, содержащий (в мМ): 120 NaCl, 5 KCl, 1 MgCl2, 1 CaCl2, 10 D-глюкозы, 5 HEPES и 25 NaHCO3 (pH 7,4). Растворы аэрируют 95% O2/5% CO2 и поддерживают при температуре 37ºC. В одном исследовании для измерения апикальной проводимости Cl- применяется базолатеральный к апикальному градиенту Cl-, в котором базолатеральная полукамера содержит (в мМ): 120 NaCl, 1 MgCl2, 1 CaCl2, 10 D-глюкозы, 5 HEPES и 25 NaHCO3 (pH 7,4); в апикальном растворе 120 мМ NaCl заменяется на 5 мМ NaCl и 115 мМ Na-глюконата, а базолатеральная мембрана делается проницаемой с помощью 250 мкг/мл амфотерицина В. Ток короткого замыкания измеряется с помощью многоканальных зажимов для измерения напряжения EVC4000 (World Precision Instruments, Sarasota, FL).
[118] Для измерения тока короткого замыкания в кишечнике мышей CD1 анестезируют изофлураном. Толстую кишку удаляют, промывают ледяным буфером Кребса, вскрывают по границе брыжейки и помещают полноразмерный фрагмент в камеру micro-Ussing (площадь 0,7 см2, World Precision Instruments). Полукамеры заполнены кислородсодержащим раствором бикарбоната Кребса.
[119] Измерения в культурах колоний человека выполняются, как описано (18). Апикальные и базолатеральные полукамеры заполняются бикарбонатным буфером Кребса-Рингера (KBR), который насыщается газом 95% O2/5% CO2 при температуре 37ºC. В базолатеральную половую камеру добавляли 10 мМ глюкозы, а в апикальную полукамеру 10 мМ маннита для поддержания осмотического баланса.
Пример 4. Измерения внутриклеточного Ca2+ и cAMP
[120] Клетки Т84 помещают в 96-луночные микропланшеты с черными стенками. Конфлюэнтные клетки загружают Fluo-4 NW (Invitrogen, Carlsbad, CA) через 72 часа после посева. Для измерения Ca2+ флуоресценцию Fluo-4 измеряют с помощью считывателя флуоресцентных пластин FluoStar (BMG Lab Technologies, Durham, North Carolina) при длинах волн возбуждения/испускания 485/538 нм. В некоторых исследованиях клетки предварительно обрабатывают BAPTA-AM в течение 30 минут. Измерение Ca2+ в культурах колоноидов человека выполняется в монослоях, которые трансдуцируются флуоресцентным датчиком Ca2+ Adeno-GCsMP6s. Для анализа cAMP клетки Т84 выращивают в 24-луночных планшетах, обрабатывают в течение 30 мин CDCA и/или форсколином, лизируют повторным замораживанием/оттаиванием, центрифугируют для удаления остатков клеток, и супернатант анализируют на cAMP с использованием набора для иммуноанализа Parameter cAMP в соответствии с инструкциями производителя (R&D Systems, Minneapolis, NM).
Пример 5. Секреция кишечного сока в замкнутых петлях кишечника у мышей
[121] Мышам CD1 (возраст 8-10 недель) дают доступ к воде с 5%-ной декстрозой, но не к твердой пище в течение 24 часов перед экспериментами. Мышам вводят (R)-BPO-27 (5 мг/кг) или носитель (5% ДМСО, 10% Kolliphor HS в физиологическом растворе) внутрибрюшинно за 60 минут до создания замкнутых петель кишечника (средней части тощей кишки или дистального отдела толстой кишки) и инъекции CDCA или носитель PBS. Ранее было показано, что эта доза (R)-BPO-27 дает терапевтические уровни в сыворотке крови в течение нескольких часов у мышей. См. Cil, O., et al. (2017) Benzopyrimido-pyrrolo-oxazine-dione CFTR inhibitor (R)-BPO-27 for antisecretory therapy of diarrheas caused by bacterial enterotoxins. FASEB J 31, 751-760. Для создания петель мышей анестезируют изофлураном, и температуру тела во время операции поддерживают на уровне 36-38ºC с помощью грелки. Делается небольшой разрез брюшной полости, чтобы обнажить кишечник. Для модели с замкнутой петлей средней части тощей кишки наложением швов создают петли на 2-3 см. В петли вводят 100 мкл PBS, содержащего CDCA, или носитель PBS. Разрез брюшной полости закрывают швами, и мышам дают оправиться от анестезии. В модели с замкнутым контуром толстой кишки мышам делают клизму (500 мкл минерального масла) за 12 часов до операции, чтобы очистить толстую кишку от твердых веществ, как сообщалось ранее (Haggie, P. M., et al. (2018) SLC26A3 inhibitor identified in small molecule screen blocks colonic fluid absorption and reduces constipation. JCI Insight 3, e121370) и создают замкнутую петлю 1-2 см наложением швов. Кишечные петли удаляются хирургическим путем в определенное время, и длина и вес петли измеряются для количественной оценки секреции жидкости. В некоторых экспериментах используют мышей CF (гомозиготные ΔF508, возраст 8-10 недель).
Пример 6. Модель хологенной диареи
[122] Самкам крыс Sprague-Dawley (возраст 8-10 недель) вводят 500 мкл CDCA (10 мМ в PBS) или носитель PBS путем инфузии в середину толстой кишки с использованием гибкой пластиковой трубки (размер 15, длина 78 мм, Instech Laboratories, Plymouth Meeting, PA). Крысам внутрибрюшинно вводят (R)-BPO-27 (10 мг/кг) (или контрольный носитель) за 30 минут до инфузии. (R)-BPO-27 растворяют в физиологическом растворе, содержащем 5% ДМСО и 10% Kolliphor HS. После инфузии крыс по отдельности помещают в метаболические клетки и предоставляют свободный доступ к воде и пище. Образцы стула собирают до инфузии (для определения исходного содержания воды в стуле) и через 4 часа после инфузии. Стул взвешивается сразу после визуализации для определения сырого веса. Для определения содержания воды в стуле образцы стула сушат при температуре 70ºC в течение 24 часов, и содержание воды рассчитывается как (влажный вес-сухой вес)/влажный вес.
Пример 7. Статистика
[123] Данные представлены как среднее±SEM. Статистический анализ выполняется с использованием пакета программного обеспечения (San Diego, CA). Статистические сравнения выполняются с использованием t-критерия Стьюдента при наличии двух групп или одностороннего дисперсионного анализа при наличии трех или более групп. Значение p<0,05 считается статистически значимым.
Ингибирование CFTR блокирует секреторный ответ, индуцированный желчной кислотой, в клетках T84
[124] В первоначальных исследованиях ряд желчных кислот отбирают путем измерения тока короткого замыкания на предмет их способности вызывать просекреторный ответ в линии эпителиальных клеток толстой кишки Т84. См. пример 3. При добавлении в апикальные (слизистые) и базолатеральные (серозные) отмывочные растворы желчные кислоты CDCA и DCA и их тауриновые конъюгаты создают устойчивый секреторный поток, который блокируется (R)-BPO-27 (фигура 1A). Для холевой кислоты и урсодезоксихолевой кислоты увеличения тока короткого замыкания не наблюдается, а для литохолевой кислоты наблюдается только небольшая переходная реакция.
[125] Увеличение тока короткого замыкания после применения CDCA полностью блокируется селективными и химически неродственными ингибиторами (R)-BPO-27 и CFTRinh-172 (фигура 1B, C). Исследования зависимости от концентрации показывают, что IC50 для ингибирования (R)-BPO-27 в этой модели составляет <1 мкМ (данные не показаны). Измерения тока короткого замыкания в дистальном отделе толстой кишки мыши показывают увеличение тока на 5,2±1,4 мкА/см2 (среднее±SEM, n=3) с добавлением CDCA к апикальному отмывочному раствору, которое полностью отменяется (R)-BPO-27 (-5,2±1,7 мкА/см2) (фигура 1D). После добавления CDCA к базолатеральному отмывочному раствору увеличения тока короткого замыкания не наблюдается.
[126] Чтобы исследовать односторонность действия CDCA в клетках T84, CDCA добавляют либо в апикальные, либо в базолатеральные отмывочные растворы. На фигуре 2А показан устойчивый отклик по потоку при добавлении 0,75 или 1 мМ CDCA к апикальному раствору, без эффекта 1 мМ CDCA, добавленного к базолатеральному раствору. Небольшой эффект наблюдается при добавлении до 2 мМ CDCA к базолатеральному раствору (фигура 2B) с добавлением форсколина в конце исследования в качестве положительного контроля для демонстрации целостности монослоя клеток Т84. Действие CDCA на апикальный CFTR и ингибирование (R)-BPO-27 подтверждается измерениями тока короткого замыкания в монослоях базолатеральных мембран проницаемых клеток T84 в присутствии апикально-базолатерального градиента концентрации Cl-, в котором короткое замыкание контурного тока обеспечивает прямое измерение апикального потока CFTR Cl- (фигура 2C).
[127] Изучаются возможные действия CDCA на сигнальные пути cAMP и Ca2+ в клетках T84. См. пример 4. CDCA до 0,75 мМ не оказывает значительного влияния на реакцию короткого замыкания на добавление форсколина, агониста cAMP, но небольшое снижение форсколин-индуцированного потока наблюдается с 1 мМ CDCA (фигура 3A, B). В каждом случае повышенный поток полностью блокировался (R)-BPO-27. Измерение внутриклеточного cAMP показывает, что CDCA до 1 мМ сам по себе не увеличивает cAMP. Однако, 0,75 и 1 мМ CDCA увеличивает cAMP в ответ на максимальный (10 мкМ) форсколин (фигура 3C).
[128] CDCA-индуцированное увеличение тока короткого замыкания в клетках T84 в значительной степени блокируется предварительной обработкой хелатором Ca2+ BAPTA-AM (фигура 4A, B). Измерения внутриклеточной концентрации Ca2+ с использованием флуоресцентного датчика Fluo-4 показывают устойчивое повышение Ca2+ после 0,75 или 1 мМ CDCA, с сопоставимой величиной с пиковым повышением Ca2+, наблюдаемым с холинергическим агонистом карбахолом или пуринергическим агонистом ATP (фигура 4C, D). Повышение Ca2+ в значительной степени блокируется предварительной обработкой BAPTA-AM. Эти эксперименты подтверждают участие передачи сигналов Ca2+ в просекреторном ответе на CDCA в клетках T84, что было неожиданным, поскольку секреторный ответ, по-видимому, полностью опосредован CFTR, cAMP-активированным Cl- каналом, а не Ca2+-активированными Cl- каналами.
Исследования в первичных культурах колоноидов человека
[129] Основные результаты, полученные с использованием клеток T84, включая секреторный ответ CFTR Cl- на апикальную CDCA и участие Ca2+ сигнализации, исследованы на первичных культурах колоноидов человека. См. пример 2. Как видно на примере клеток T84, CDCA вызывает зависящее от концентрации увеличение тока короткого замыкания при добавлении к апикальному, но не базолатеральному отмывочному раствору, который отменяется (R)-BPO-27 (фигура 5A, B). Кроме того, увеличение тока короткого замыкания значительно снижается предварительной обработкой BAPTA-AM (фигура 5C), и CDCA вызывает повышение цитоплазматической концентрации Ca2+ с пиковой величиной, сравнимой с пиковой величиной, производимой ATP (фигура 5D), хотя и более кратковременной, чем наблюдается в клетках Т84.
BPO-27 подавляет секрецию жидкости в замкнутых петлях кишечника мышей
[130] Модель замкнутой кишечной петли создана на мышах для исследования просекреторного действия CDCA in vivo. См. пример 5. Первоначальные исследования выполняются в средней части петель тощей кишки из-за технической простоты получения нескольких петель у одного животного и их широкого использования ранее при изучении секреции кишечного сока на моделях холеры и диареи путешественников. На фигуре 6A показано, что инъекция 10 мМ CDCA в петли средней части тощей кишки вызывает устойчивое накопление жидкости к 1 часу. Исследование зависимости концентрации CDCA с петлевой жидкостью, измеренной через 2 часа, показывает значительное увеличение накопления петлевой жидкости с 5 и 10 мМ CDCA (фигура 6B). Подобные эксперименты в закрытых петлях дистального отдела толстой кишки показывают значительное накопление жидкости петли с 2,5 мМ CDCA (фигура 6C).
[131] Чтобы изучить эффекты ингибирования CFTR, (R)-BPO-27 вводят за 60 минут до создания замкнутых петель кишечника и инъекции CDCA (или контрольного носителя PBS) (фигура 7A). В замкнутых петлях средней части тощей кишки активный энантиомер BPO-27, (R)-BPO-27, вызывает значительное снижение накопления жидкости в петле на 55%, в то время как неактивный энантиомер (S)-BPO-27 не оказывает значительного влияния (фигура 7B). Более значительное снижение накопления жидкости в петле с (R)-BPO-27 на ~70% было обнаружено в закрытых петлях толстой кишки (фигура 7C).
[132] Поскольку ингибирование CFTR в значительной степени, но не полностью, блокирует накопление жидкости в петле, исследуется, могут ли CFTR-независимые механизмы частично быть ответственными за эффект CDCA. Для этих экспериментов исследования по замкнутому циклу выполняются на мышах с муковисцидозом, лишенных функционального CFTR. Замкнутые петли средней части тощей кишки и дистального отдела толстой кишки, в которые вводили 10 мМ CDCA, показывают небольшое, но значительно большее содержание жидкости в петле по сравнению с контрольными петлями, в которые вводили носитель PBS, что указывает на другие механизмы, помимо CFTR, которые также играют роль в накоплении жидкости, индуцированном CDCA, которые, основываясь на предыдущих исследованиях, могут включать ингибирование обменников Na+/H+ и Cl-/HCO3- (про-абсорбционные процессы), повышенную межклеточную проницаемость или стимуляцию секреции слизи. См. Alrefai, W. A., et al. (2007) Taurodeoxycholate modulates apical Cl-/OH- exchange activity in Caco2 cells. Dig Dis Sci 52, 1270-1278; Pallagi-Kunstar, E., et al. (2015) Bile acids inhibit Na+/H+ exchanger and Cl-/HCO3- exchanger activities via cellular energy breakdown and Ca2+ overload in human colonic crypts. Pflugers Arch 467, 1277-1290; Sarathy, J., et al. (2017) The yin and yang of bile acid action on tight junctions in a model colonic epithelium. Physiol Rep 5, e13294; Barcelo, A., et al. (2001) Effect of bile salts on colonic mucus secretion in isolated vascularly perfused rat colon. Dig Dis Sci 46, 1223-1231.
BPO-27 снижает содержание воды в стуле у крыс с диареей желчной кислоты
[133] Создана модель для исследования эффекта (R)-BPO-27, в которой CDCA (или контрольный носитель) вводят крысам в виде инфузии в середину толстой кишки, при этом в течение 4 часов собирают стул для измерения массы стула и содержания воды (по массовому соотношению влажного и сухого) (фигура 8A, вверху). См. пример 6. Жидкость, введенная в этой модели, быстро распределяется по просвету толстой кишки, что видно с использованием синего красителя Эванса (фигура 8A, внизу). За 4 часа у крыс, которым вводили CDCA, собирается большее количество стула, а содержание воды в стуле значительно увеличивается на ~25% (фигура 8B, C). Хотя предварительная обработка (R)-BPO-27 не влияет на количество стула или содержание воды у крыс, которые получают инфузию PBS в середину толстой кишки, увеличение содержания воды в стуле у крыс, получавших инфузию CDCA, ингибируется на ~55% (фигура 8C).
[134] Не ограничиваясь теорией, данные настоящего документа подтверждают полезность ингибирования CFTR ингибиторами CFTR, в частности, (R)-BPO-27, при лечении диареи, связанной с желчными кислотами. Измерения тока короткого замыкания в клетках Т84 и культурах колоноидов человека показывают просекреторный поток в ответ на воздействие CDCA на апикальную поверхность клетки, который полностью отменяется ингибированием CFTR. Полное ингибирование секреторного потока с помощью (R)-BPO-27 также наблюдается в ткани толстой кишки мышей, подвергшейся воздействию CDCA, ex vivo. Системное введение (R)-BPO-27 в значительной степени предотвращает накопление жидкости в замкнутых петлях толстой кишки у мышей in vivo и предотвращает увеличение количества воды в стуле после внутритолстокишечной инфузии раствора, содержащего CDCA. Эти результаты указывают на участие CFTR в качестве основного просекреторного ионного канала в CDCA-индуцированной диарее в культурах клеток толстой кишки человека и грызунов.
[135] По настоящей заявке испрашивается приоритет по предварительной заявке США № 62/860539, поданной 12 июня 2019 г., которая полностью включена в настоящий документ посредством ссылки.
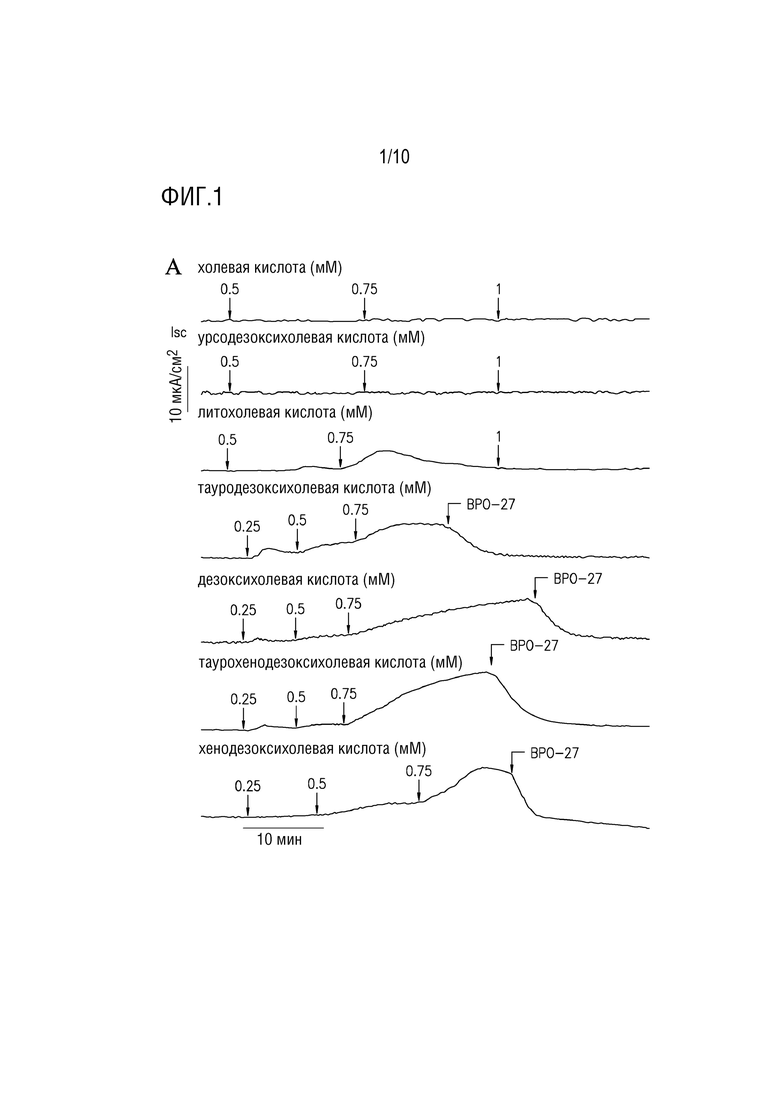
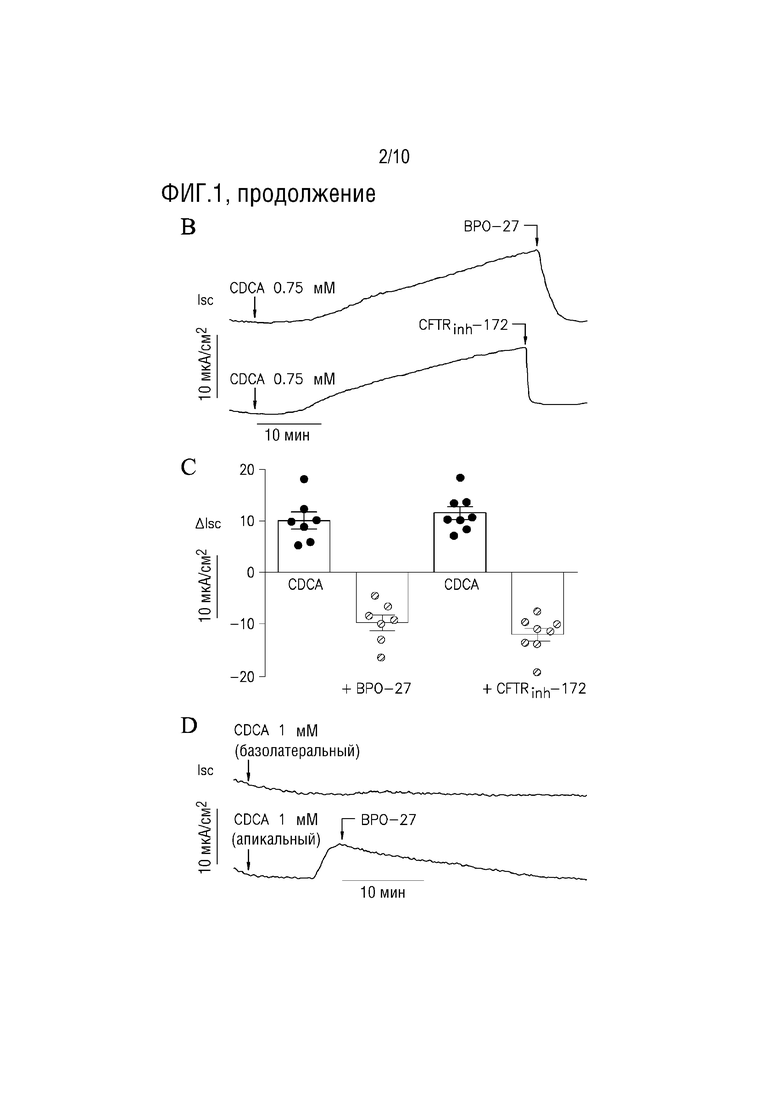
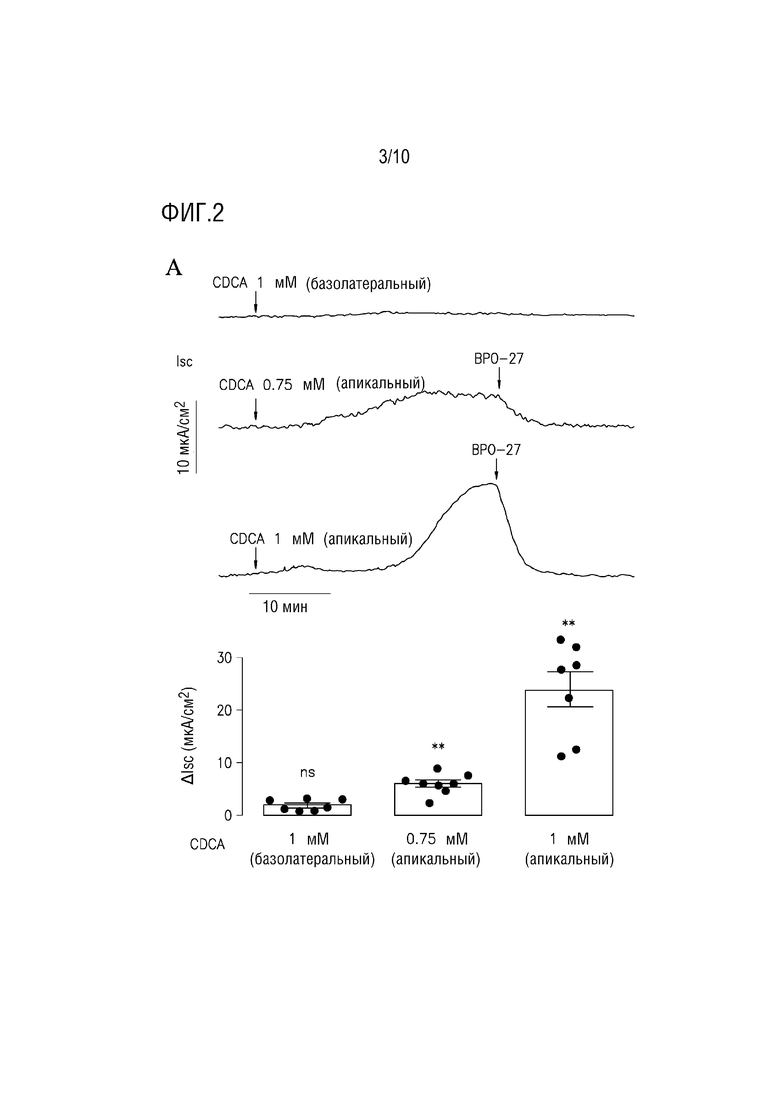
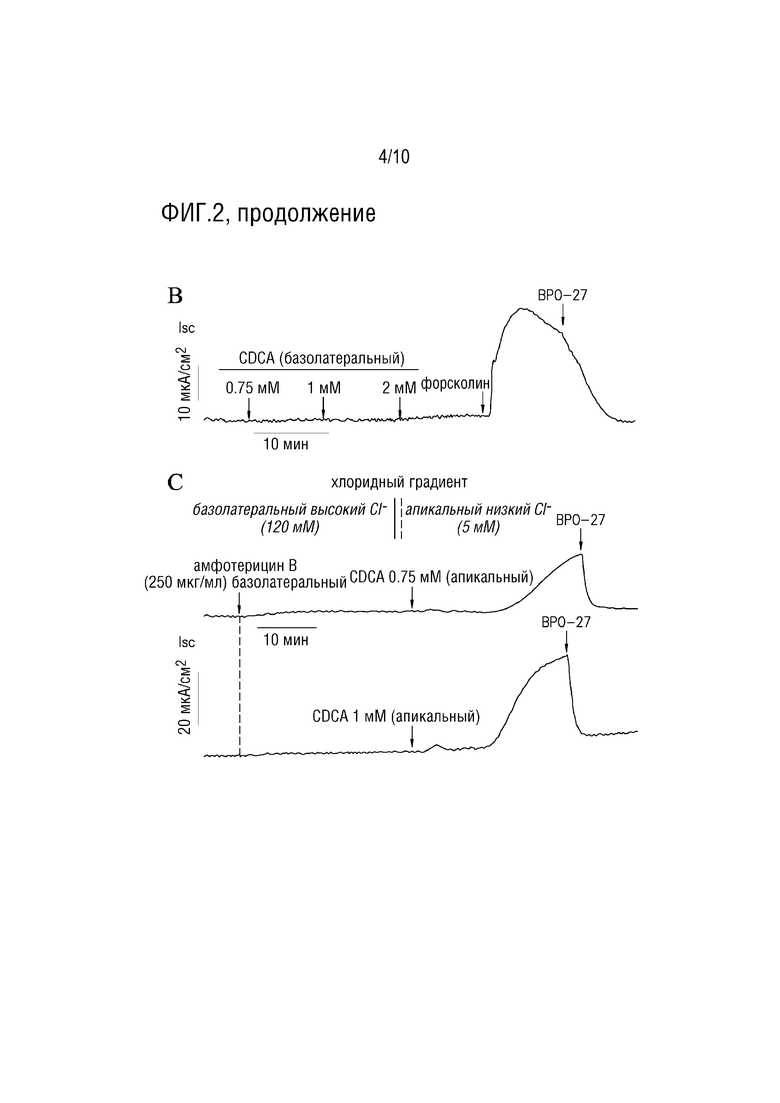
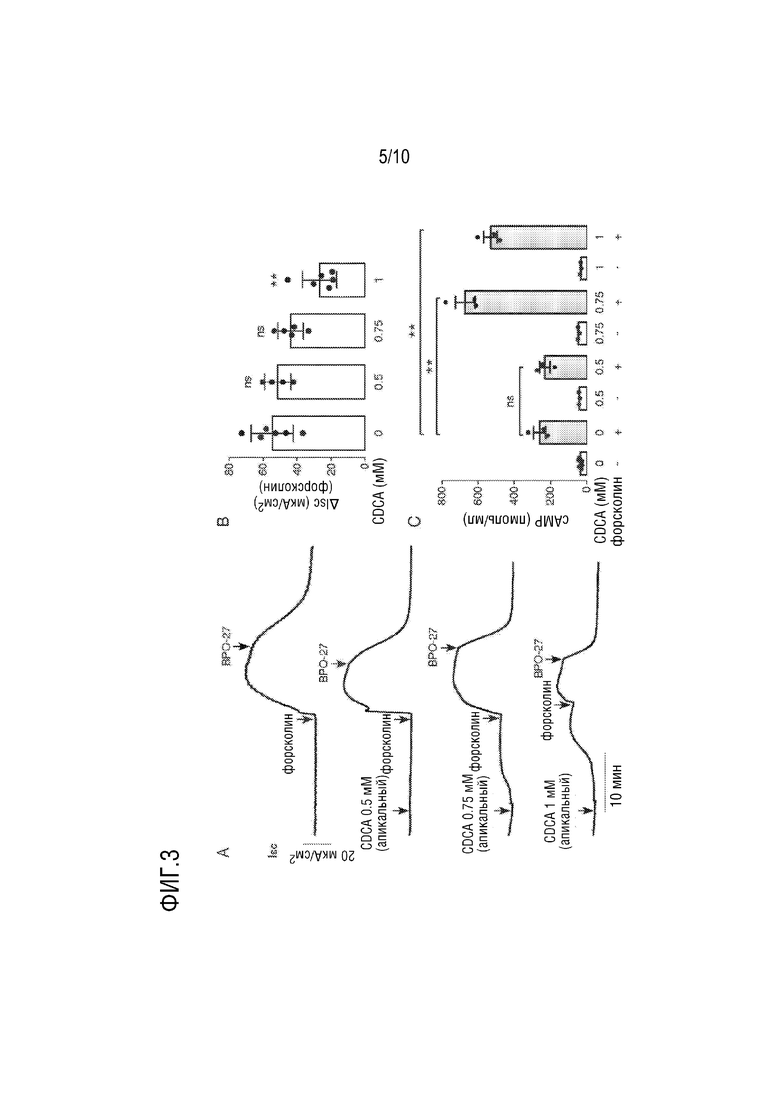
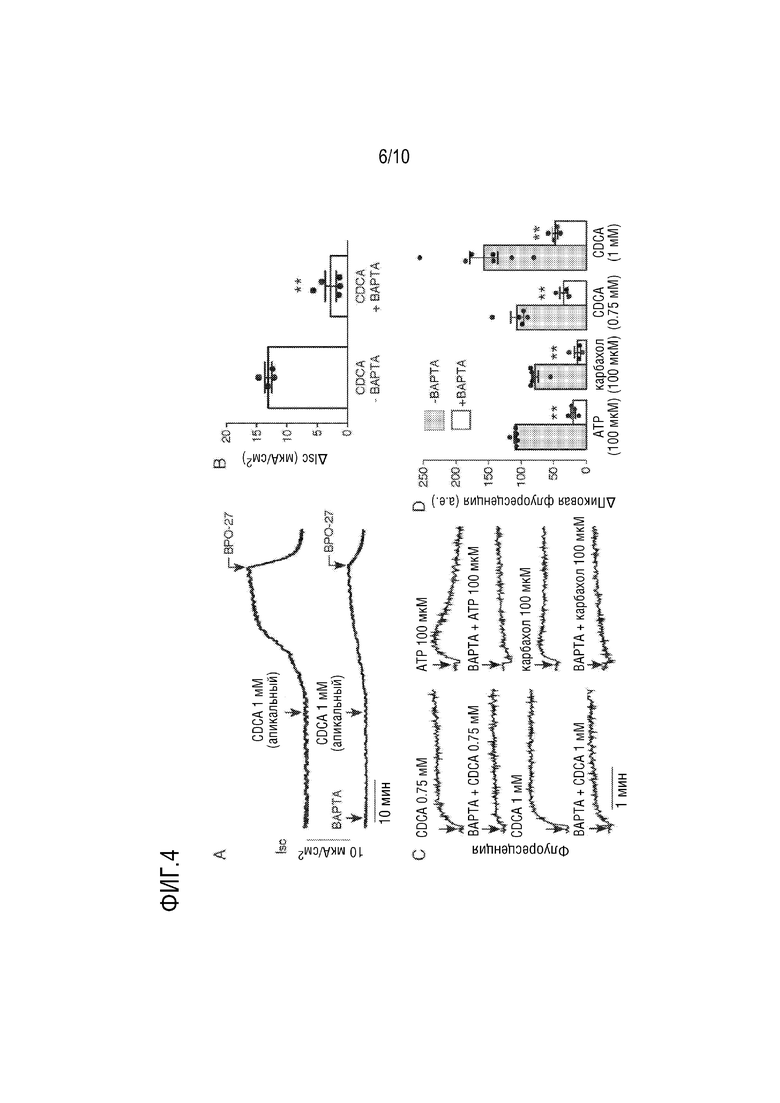
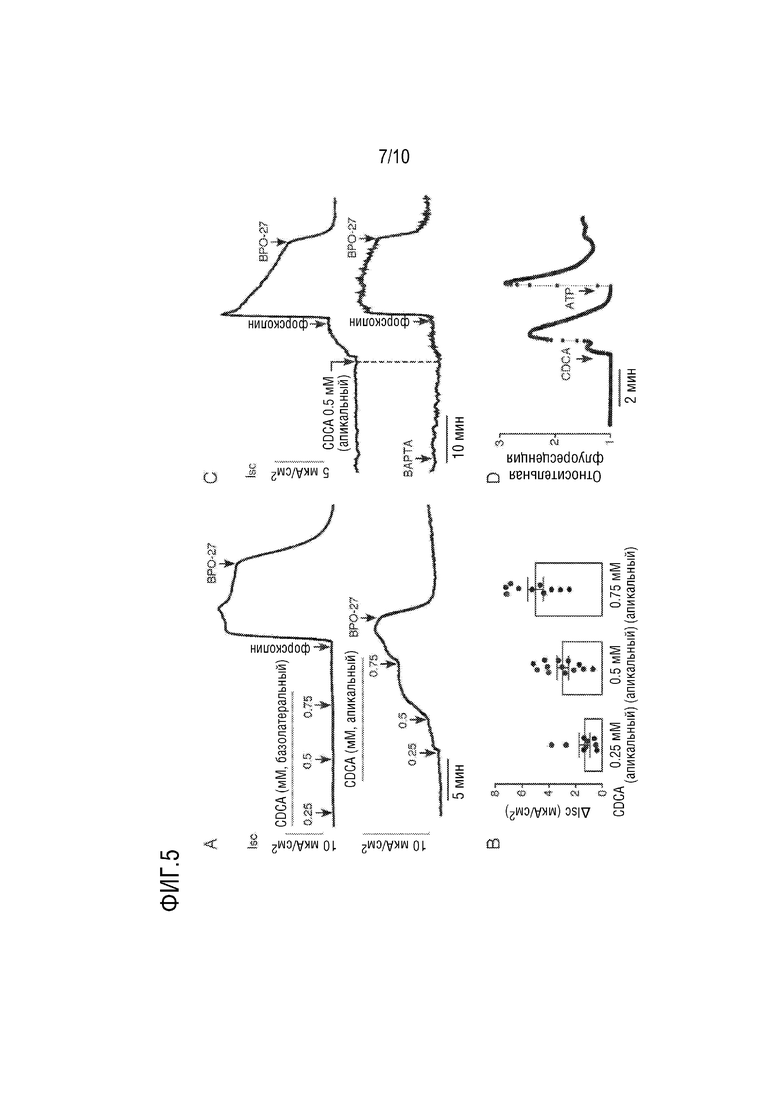
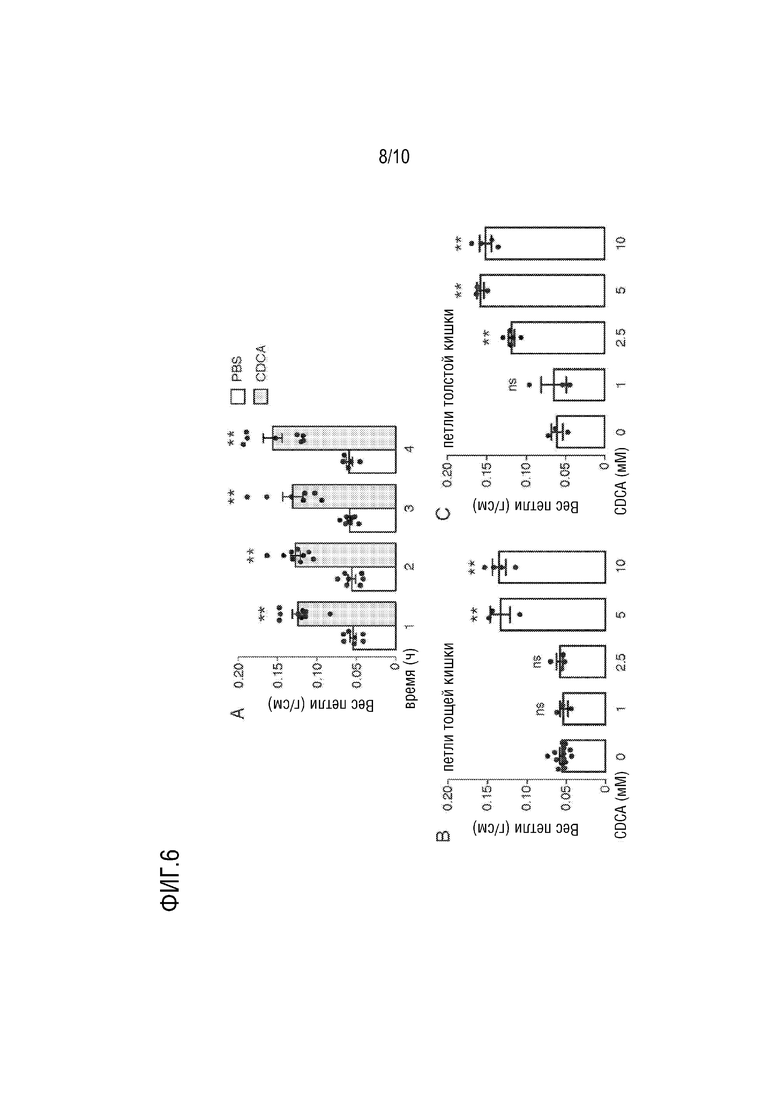
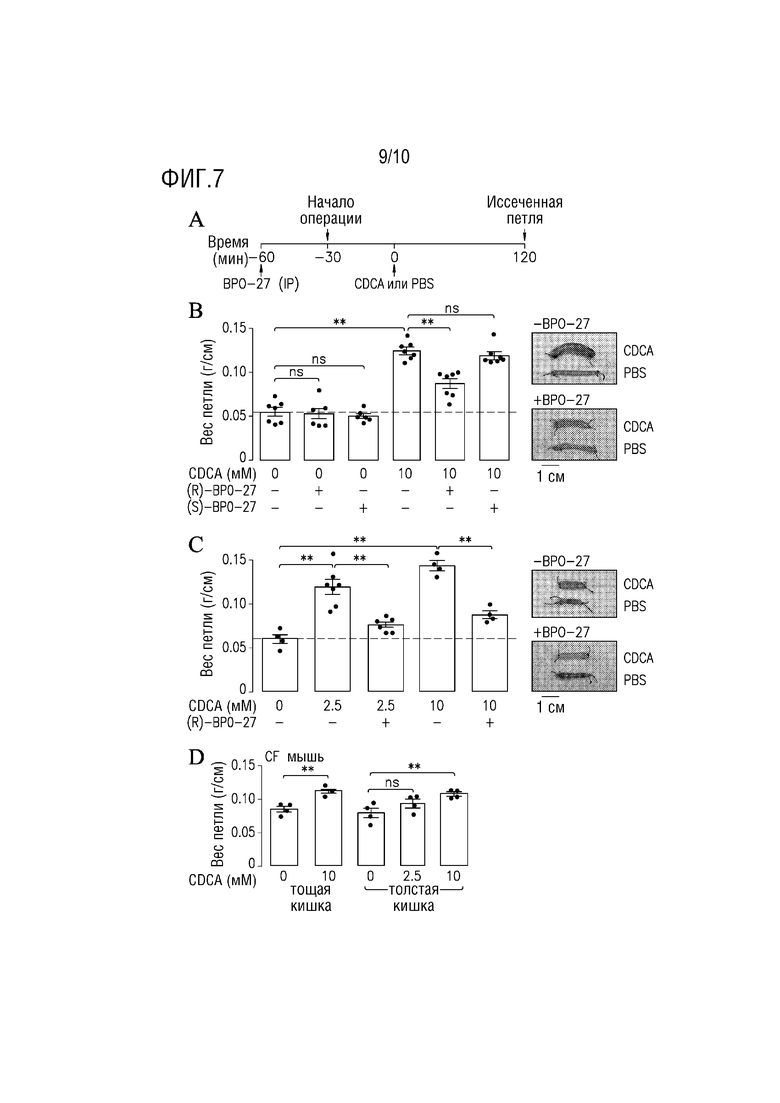
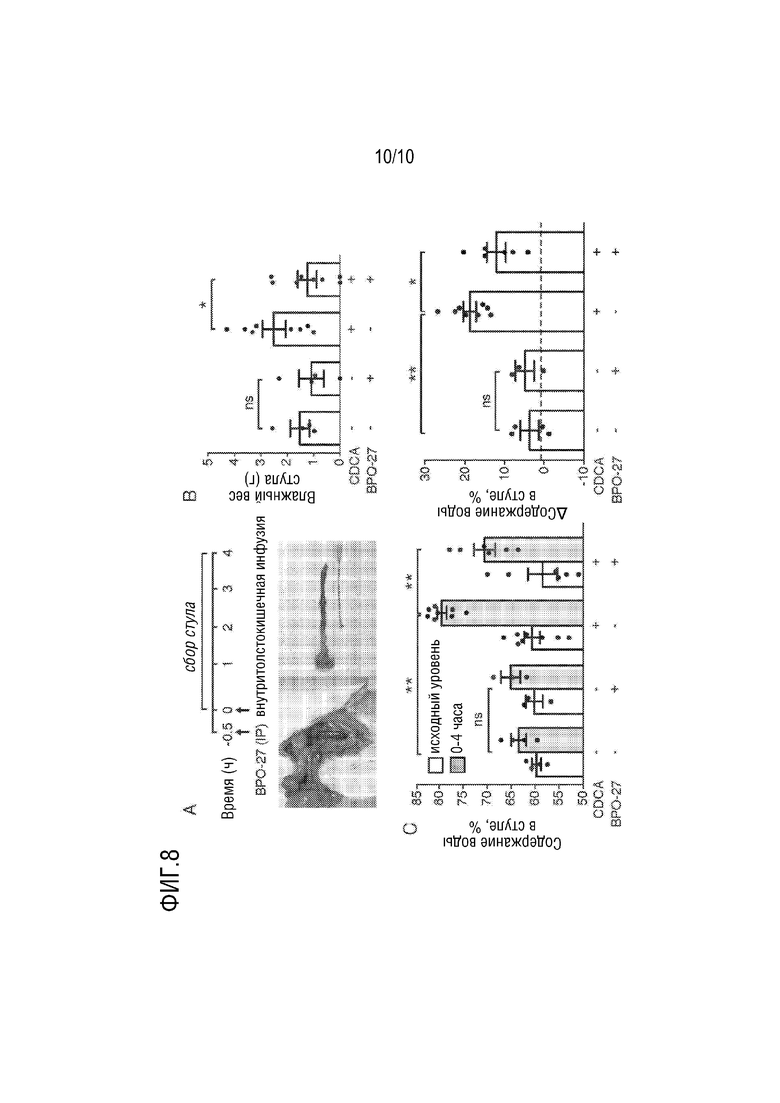
Группа изобретений относится к медицине, а именно к лечению хологенной диареи. Предложен способ лечения субъекта, страдающего хологенной диареей, включающий введение субъекту количества BPO-27, эффективного для лечения хологенной диареи, или фармацевтической композиции, содержащей количество BPO-27, эффективное для лечения хологенной диареи. Также группа изобретений относится к способам лечения хологенной диареи или облегчения симптомов, связанных с хологенной диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающим введение субъекту BPO-27 или содержащей BPO-27 фармацевтической композиции в количестве, эффективном для лечения указанной хологенной диареи или для облегчения симптомов указанной хологенной диареи. Способы обеспечивают эффективное лечение хологенной диареи за счет подавления секреции жидкости в замкнутых петлях кишечника и снижения содержания воды в стуле. 4 н. и 17 з.п. ф-лы, 8 ил., 7 пр.
1. Способ лечения субъекта, страдающего хологенной диареей, включающий введение субъекту количества BPO-27, эффективного для лечения хологенной диареи.
2. Способ по п.1, где указанный BPO-27 представляет собой (R)-BPO-27.
3. Способ лечения субъекта, страдающего хологенной диареей, включающий введение субъекту фармацевтической композиции, содержащей количество BPO-27, эффективное для лечения хологенной диареи.
4. Способ по п.3, где указанный BPO-27 представляет собой (R)-BPO-27.
5. Способ по любому из предшествующих пунктов, где указанное количество BPO-27 является эффективным для снижения секреции кишечного сока, происходящей в результате хологенной диареи.
6. Способ по любому из предшествующих пунктов, где указанное количество BPO-27 является эффективным для снижения вызванной желчной кислотой активации апикальных хлоридных каналов CFTR.
7. Способ по любому из предшествующих пунктов, дополнительно включающий введение субъекту второго агента, эффективного для лечения хологенной диареи, где указанный второй агент представляет собой вещество, связывающее желчные кислоты, агонист рецептора фарнезоида X (FXR), антагонист 5-HT3, агонист опиоидного рецептора, смешанный агонист опиоидного μ-рецептора, кишечно-специфический антибиотик широкого спектра действия, спазмолитик или трициклический антидепрессант.
8. Способ по п.7, где указанный второй агент представляет собой вещество, связывающее желчные кислоты, предпочтительно холестирамин, колестипол или колесевелам.
9. Способ по п.7, где указанный второй агент представляет собой агонист рецептора фарнезоида X (FXR), предпочтительно обетихолевую кислоту.
10. Способ по п.7, где указанный второй агент представляет собой антагонист 5-HT3, предпочтительно алозетрон.
11. Способ по п.7, где указанный второй агент представляет собой агонист опиоидных рецепторов, предпочтительно лоперамид.
12. Способ по п.7, где указанный второй агент представляет собой смешанный агонист опиоидного μ-рецептора, предпочтительно элюксадолин.
13. Способ по п.7, где указанный второй агент представляет собой кишечно-специфический антибиотик широкого спектра действия, предпочтительно рифаксимин.
14. Способ лечения хологенной диареи или облегчения симптомов, связанных с хологенной диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающий введение субъекту количества BPO-27, эффективного для лечения указанной хологенной диареи или для облегчения симптомов указанной хологенной диареи.
15. Способ по п.14, где указанный BPO-27 представляет собой (R)-BPO-27.
16. Способ лечения хологенной диареи или облегчения симптомов, связанных с хологенной диареей, у субъекта, перенесшего резекцию подвздошной кишки, включающий введение субъекту фармацевтической композиции, содержащей количество BPO-27, эффективное для лечения указанной хологенной диареи или для облегчения симптомов указанной хологенной диареи.
17. Способ по п.16, где указанный BPO-27 представляет собой (R)-BPO-27.
18. Способ по любому из предшествующих пунктов, где субъектом является человек.
19. Способ по любому из предшествующих пунктов, где у субъекта диагностирована болезнь Крона.
20. Способ по любому из пп.1-18, где у субъекта диагностирован IBS-D.
21. Способ по любому из пп.1-18, где субъект страдает функциональной диареей.
| WO 2018222921 A1, 06.12.2018 | |||
| US 20140080821 A1, 20.03.2014 | |||
| Аппарат для выпаривания | 1924 |
|
SU9847A1 |
| Предохранительная трубка для сосудов с огнеопасными жидкостями | 1927 |
|
SU11074A1 |
| US 20070254050 A1, 01.11.2007 | |||
| US 20170224721 A1, 10.08.2017 | |||
| WO 2015195509 A2, 23.12.2015 | |||
| US 20180099011 A1, 12.04.2018. | |||
Авторы
Даты
2025-04-25—Публикация
2020-06-08—Подача