Изобретение относится к аналитической химии, в частности к способу количественного определения гидроксида тетраметиламмония (ТМАГ) в концентрированном водном растворе, который может быть использован в исследовательской практике, а также в качестве концентрата для производства безметальных проявителей, применяемых при разработке и изготовлении интегральных схем (ИС) в микроэлектронном производстве и производстве радиоэлектронной аппаратуры.
Производство ИС с нанометровыми топологическими нормами требует освоения новых материалов и повышения их уровня качества. Одной из наиболее важных технологических операций производства ИС является фотолитографический процесс формирования рельефных покрытий на функциональных поверхностях подложек для ИС, в которой используются безметальные проявители.
Технология получения концентрированных водных растворов гидроксида тетраметиламмония с концентрацией от 24,5 до 25,5%, используемых для получения безметальных проявителей, применяемых в производстве ИС, заключается в мембранном электролизе водных растворов хлорида или бикарбоната тетраметиламмония. Чрезвычайно важным требованием, предъявляемым к качеству концентрированного водного раствора гидроксида тетраметиламммония, является точная концентрация в нем ТМАГ, которая должна быть в пределах от 24,5 до 25,5%. Так как при концентрациях гидроксида тетраметиламмония в концентрированном водном растворе за пределами указанного интервала будет происходить нарушение технологического процесса получения безметального проявителя. Кроме того, регистрация концентрации ТМАГ в нормируемом диапазоне от 24,5 до 25,5% с использованием метода прямого кондуктометрического определения концентрации гидроксида тетраметиламмония в процессе получения концентрированного водного раствора ТМАГ позволяет оптимизировать технологию синтеза ТМАГ в целом, так как этот интервал концентраций ТМАГ в растворе является контрольной точкой прекращения синтеза целевого продукта.
Данный метод исключает нецелесообразный перерасход электроэнергии, и уменьшает длительность процесса синтеза ТМАГ на 30÷40 мин.
Поскольку ТМАГ является сильным органическим основанием, как гидроксиды натрия или калия, то его содержание в водном растворе можно определять методом нейтрализации с применением индикатора - фенолфталеина аналогично неорганическим щелочам [Левин А.И. Теоретические основы электрохимии. М.: Металлургиздат.1963, - 430 с; Бародулина Е.К., Ильичева И.А., Шрайбман С.С. Технический анализ и контроль электрохимических производств неорганических веществ. М:. Химия. 1979. 231 с]. При титровании водного раствора ТМАГ 0,1 н раствором соляной кислоты в отсутствии карбонатов, протекает реакция:
[(CH3)4N]OH+НСl → [(CH3)4N]Cl+Н2O (1)
Однако, как показали наши исследования [Конарев А.А., Варламов Д.А., Грибов Б.Г. // Электронная техника. Сер. 3. Микроэлектроника. 2019. Вып. 3(175). С.25-37], использование визуального титриметрического метода для анализа концентрации ТМАГ в концентрированном водном растворе, полученном электролизом водных растворов хлорида тетраметиламмония, приводит к снижению точности определения ТМАГ из-за субъективной ошибки нахождения точки эквивалентности титрования. Кроме того, возникают трудности в исключении поглощения углекислого газа раствором ТМАГ из атмосферы анализируемым раствором ТМАГ при проведении анализа, что требует применения дорогостоящих приборов.
Для более точного определения содержания ТМАГ в водном растворе может применяться потенциометрический метод титрования, в котором точку эквивалентности определяют по скачку потенциала электрода, погруженного в анализируемый раствор [Крешков А.П. Основы аналитической химии, М:. Химия. 1970. 471 с]. Несмотря на то, что потенциометрический метод титрования более точен, по сравнению с титриметрическим, (исключает субъективную ошибку определения конечной точки титрования), однако, этот метод невозможно использовать при непрерывном контроле концентрации ТМАГ при его производстве, поскольку данный метод не позволяет проводить прямые измерения, а он может быть применен лишь при периодическом отборе пробы раствора ТМАГ и ее анализе титрованием кислотой.
Поэтому возникает острая необходимость в разработке высокочувствительного, простого, точного, легко реализуемого в производственных условиях непрерывного способа количественного анализа концентрации ТМАГ в концентрированном водном растворе в процессе синтеза, приводящего к обеспечению требуемого его качества и к оптимизации процесса его производства.
Наиболее близкий к предлагаемому способу по технической сущности и достигаемому результату является способ определения содержания ТМАГ в концентрате кондуктометрическим титрованием 0,1 н раствором соляной кислоты [Конарев А.А., Варламов Д.А., Грибов Б.Г. //Электронная техника. Серия 3. Микроэлектроника. 2019. Выпуск 3(175). С. 25-37]. Кондуктометрическая методика определения содержания ТМАГ в концентрате основывается на титровании раствора ТМАГ 0,1 н раствором соляной кислоты без индикатора и с регистрацией при этом величины удельной электропроводности с последующим построением простой по форме кондуктометрической кривой на компьютере, расчетом эквивалентных точек и определением концентрации ТМАГ в водном растворе.
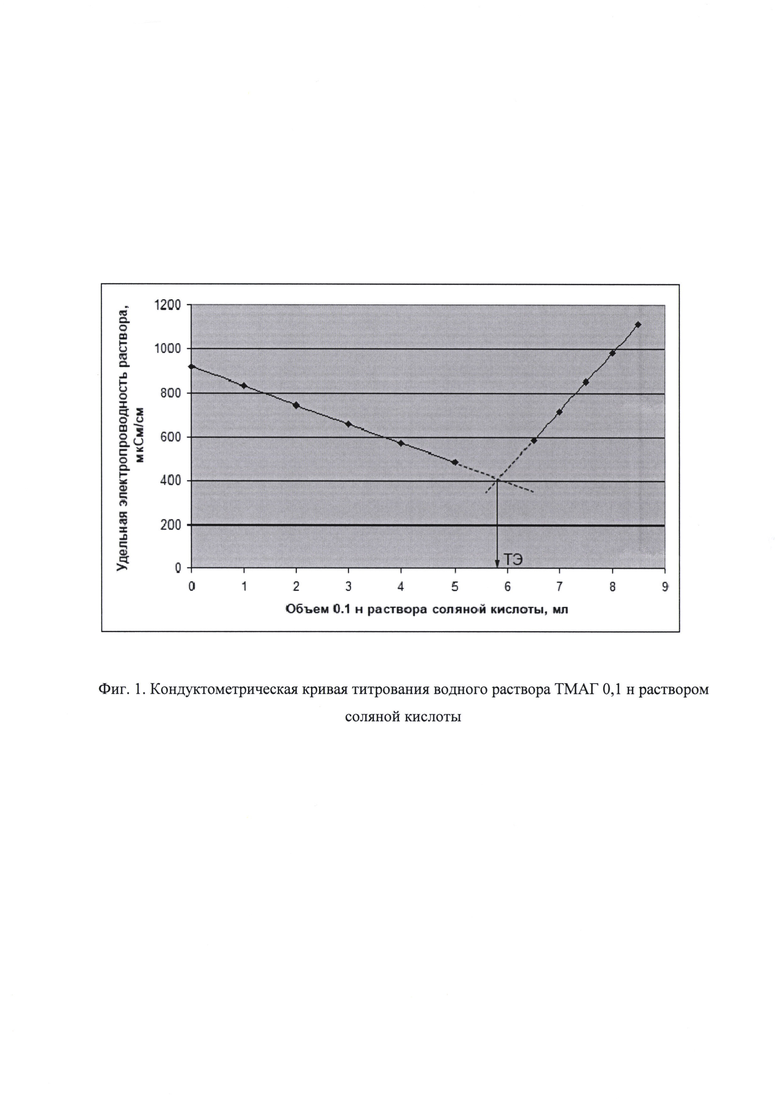
Типичная кондуктометрическая кривая титрования ТМАГ 0,1 н раствором соляной кислоты в водном растворе приведена на фиг. 1.
Из фиг. 1 видно, что при титровании ТМАГ, содержащегося в водном растворе, раствором соляной кислоты, удельная электропроводность этого раствора до точки эквивалентности резко понижается, так как подвижность ОН- (λOH-=198,3 Ом-1⋅см2⋅моль-1 при 25°С) выше подвижности заменяющих их хлорид-ионов (λCl-=76,4 Ом-1⋅см2⋅моль-1 при 25°С). Избыток титранта вызывает резкое повышение величины удельной электропроводности раствора (λн+=349,8 Ом-1 см2 моль-1 при 25°С) [Девис С, Джеймс А. Электрохимический словарь. М.: Мир. 1979. 281 с]. По полученным экспериментальным данным строят прямолинейные участки кривой кондуктометрического титрования в координатах χ (мкСм/см) - V (мл). Первый линейный участок описывается уравнением χ1=-b1V+С1 а второй - χ2=b2V - С2. Точка пересечения этих прямых является точкой эквивалентности (ТЭ) титрования, которая определяется решением этих уравнений при χ1=χ2, что увеличивает точность ее определения, а, следовательно, точность определения концентрации ТМАГ в водном растворе. Затем проводят расчет концентрации ТМАГ (С1) в водном растворе по формуле:
С1 (%) - (0,009115⋅К⋅VHCl⋅100)/ g, (2)
где С1 - концентрация ТМАГ в анализируемом растворе, %;
g - навеска анализируемого раствора ТМАГ, г;
VHCI - объем 0,1 н раствора соляной кислоты, пошедший на титрование образца раствора ТМАГ, мл;
0,009115 г, соответствующее 1 мл точно 0,1 н раствора соляной кислоты, г;
К - поправочный коэффициент 0,1 н раствора соляной кислоты.
Кондуктометрический метод определения концентрации ТМАГ в водном растворе более предпочтительный по сравнению с потенциометрическим, так как более прост в реализации и не требует тщательности при титровании, в особенности в близи точки эквивалентности. К тому же, он обеспечивает более точный результат определения концентрации ТМАГ (табл.1).
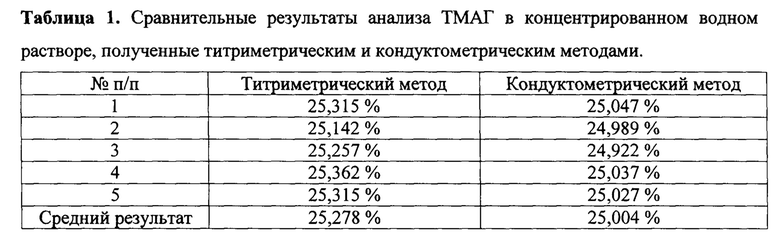
Несмотря на простоту исполнения этого способа и точность определения концентрации ТМАГ в водном растворе, этот метод является продолжительным из-за процесса титрования пробы и построения кондуктометрической кривой титрования (40-50 мин.). Кроме того, этот метод определения концентрации ТМАГ в водном растворе, как и потенциометрический не представляется возможным применять для непрерывного контроля концентрации ТМАГ в ходе его производства.
Задачей предлагаемого изобретения является разработка точного, простого и быстрого способа количественного определения концентрации ТМАГ в концентрированном водном растворе, обеспечивающего непрерывный контроль концентрации ТМАГ при его производстве, требуемое качество продукта и оптимизацию технологии его получения. А также, прямой оперативный контроль концентрации ТМАГ в отобранной пробе.
Для решения этой задачи предложен способ кондуктометрического количественного определения концентрации ТМАГ в концентрированном водном растворе, заключающийся в прямом измерении величины его удельной электропроводности при температуре 20°С непосредственно в технологической схеме или в отобранной пробе раствора ТМАГ и последующем расчете концентрации ТМАГ (С2) в водном растворе по следующей формуле:
С2(%)=(χ- 70,897)/6,3095, (3)
где χ - величина удельной электропроводности анализируемого раствора ТМАГ, измеренная при температуре 20°С, мСм/см;
70,897 - коэффициент смещения по оси проводимости, мСм/см;6,3095 - тангенс угла наклона прямой зависимости удельной электропроводности от концентрации ТМАГ, мСм/(см %).
Предлагаемый способ осуществляют прямым измерением величины удельной электропроводности концентрированного водного раствора ТМАГ с помощью цифрового кондуктометра серийного производства, в частности, серии Анион 4100 (или другой конструкции с аналогичными параметрами) при его производстве. Для этого в технологическую схему производства концентрированного водного раствора ТМАГ или в отобранную его пробу помещают датчик кондуктометра и измеряют им удельную электропроводность полученного продукта при температуре 20°С. Для обеспечения нормативной концентрации ТМАГ в водном растворе от 24,5 до 25,5% величина удельной электропроводности раствора ТМАГ, измеренная при 20°С, должна быть в диапазоне от 225,5 до 231,8 мСм/см.
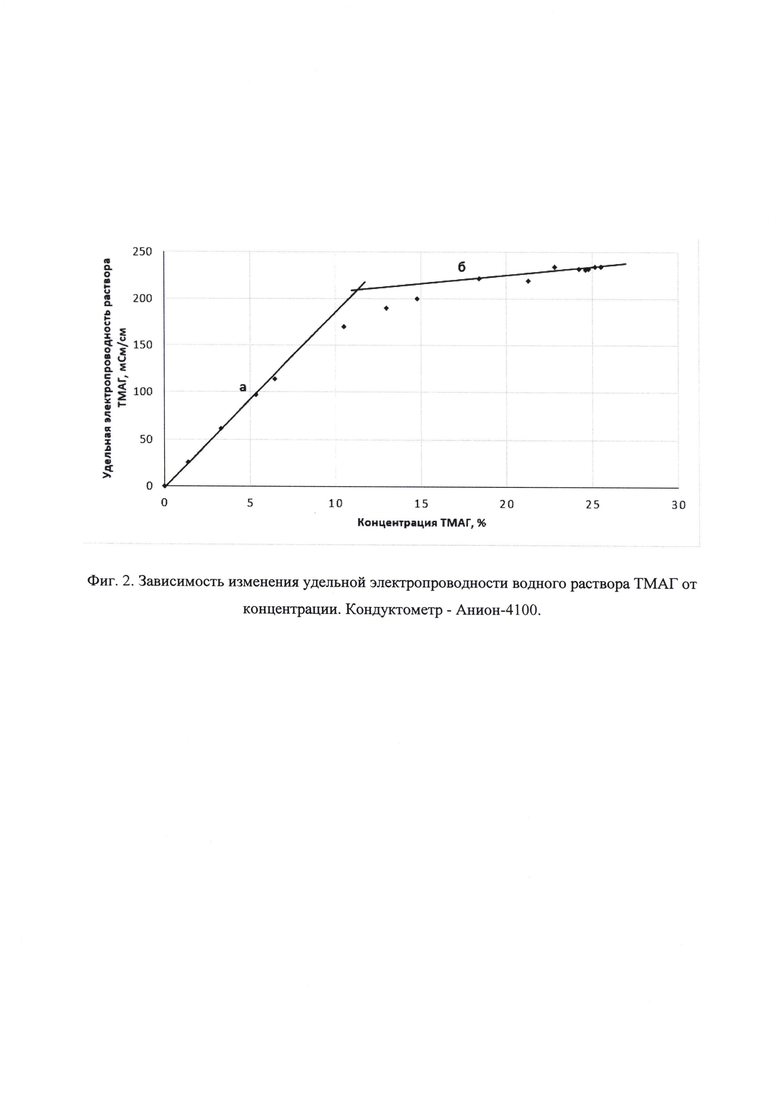
Для обоснования предлагаемого способа контроля концентрации ТМАГ при его производстве исследовано влияние концентрации ТМАГ на удельную электропроводность водного раствора, так как в научной литературе эти данные не приводятся, а имеются лишь сведения по влиянию концентрации неорганических щелочей: КОН и NaOH на удельную электропроводность их растворов [Сваровская Н.А., Колесников И.М., Винокуров В.А. Электрохимия растворов электролитов. 2017, М.: Издательский центр нефти и газов им. И.М Губкина. - 66 с]. Как видно из фиг. 2, зависимость удельной электропроводности водного раствора ТМАГ от концентрации органической щелочи имеет сложный характер, как и в случае неорганических щелочей [Антропов Л.И. Теоретическая электрохимия. М: Высшая школа, 1969. 510 с]. Однако в интервале концентраций от 1 до 26% на кондуктометрической кривой можно выделить два линейных отрезка с различным углом наклона: первый линейный отрезок (а) наблюдается в диапазоне концентраций ТМАГ от 1 до 10%, а второй (б) - от 18 до 26%. При увеличении концентрации ТМАГ до 10% удельная электропроводность раствора более резко возрастает, что объясняется увеличением числа ионов (носителей заряда) в водном растворе. Однако при дальнейшем увеличении концентрации ТМАГ в растворе от 18 до 26% влияние концентрации ТМАГ на удельную электропроводность замедляется, что объясняется электростатическим взаимодействием между ионами. Чем больше ионов в растворе, тем меньше расстояние между ионами и сильнее взаимодействие, таким образом, ионы мешают друг другу перемещаться (электрофоретическое торможение) [Щербаков В.В. Электрохимия, 2009. Т. 45. №11. С. 1394]. Однако, как видно из фиг. 2, линейность изменения удельной электропроводности раствора ТМАГ при этом еще сохраняется. Поэтому второй отрезок (б) может быть использован для контроля концентрации ТМАГ и окончания синтеза концентрата ТМАГ при достижении нормируемой концентрации ТМАГ в растворе от 24,5 до 25,5%, что позволяет оптимизировать технологический процесс производства ТМАГ в целом, так как при этом обеспечивается нормативная концентрация продукта и исключается нерациональный расход электроэнергии, а также уменьшается длительность процесса синтеза ТМАГ на 30-40 мин.
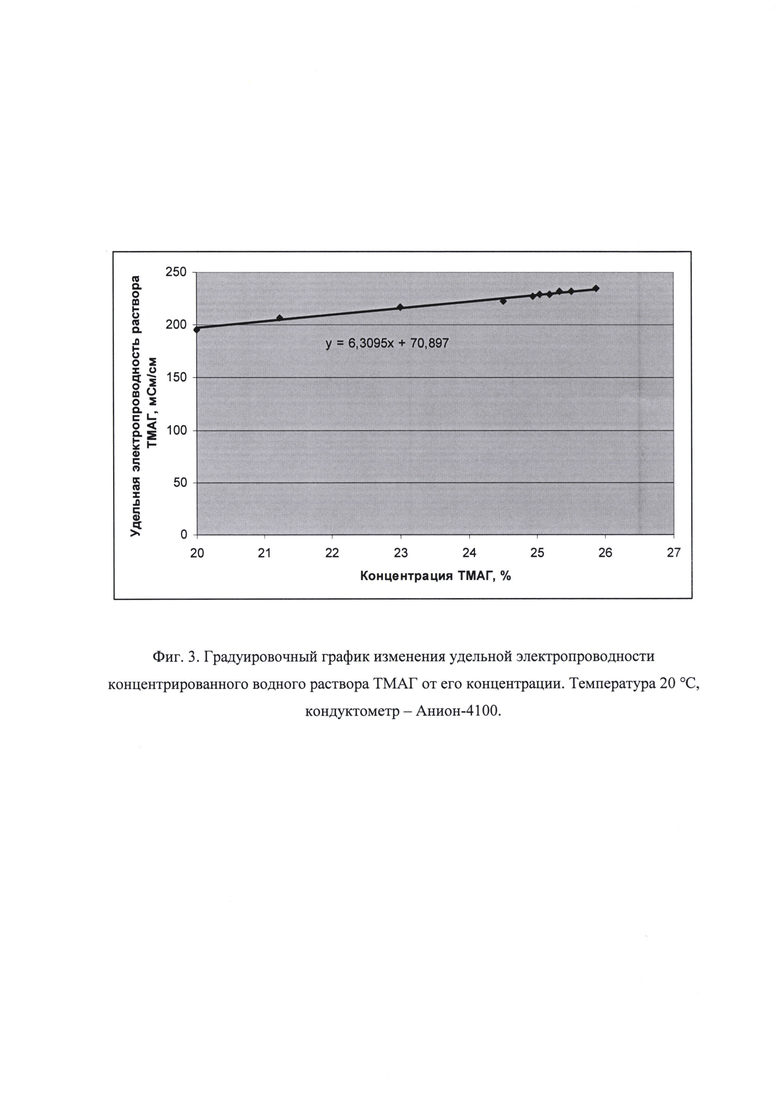
Для определения концентрации ТМАГ в концентрированном водном растворе предварительно строят градуировочный график зависимости удельной электропроводности раствора от концентрации ТМАГ в растворе от 20,0 до 26,0% (фиг. 3), а концентрацию ТМАГ в анализируемой пробе концентрата ТМАГ рассчитывают по формуле, приведенной выше.
Для построения градуировочного графика готовят шкалу стандартных растворов ТМАГ согласно (табл. 2).
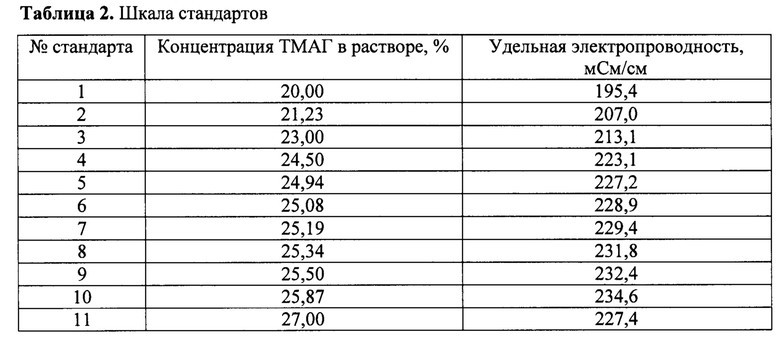
Для приготовления стандартного раствора ТМАГ взвешивают точную навеску ТМАГ с концентрацией 25-27% масс, и растворяют ее в деионизованной воде с удельным сопротивлением не менее 18 МОм⋅см в мерной колбе вместимостью 100 см3, а затем доводят объем раствора деионизованной водой до метки, определяют концентрацию ТМАГ в полученном растворе по формуле (2) и измеряют величину удельной электропроводности данного стандарта при температуре 20°С. Для построения градуировочного графика используют программу «Microsoft Excel» (фиг. 3.).
В растворе с концентрацией ТМАГ от 20,0 до 26,0% (фиг. 3) наблюдается линейная зависимость изменения удельной электропроводности от концентрации органической щелочи, что является основой количественного определения концентрации ТМАГ в водном растворе. Дальнейшее увеличение диапазона концентраций ТМАГ в растворе нецелесообразно, так как нормативный интервал концентраций ТМАГ в растворе находится в исследованном диапазоне концентраций ТМАГ (фиг. 3). Кроме того, при концентрации ТМАГ в растворе 27,0% нарушается линейная зависимость удельной электропроводности от концентрации щелочи, о чем свидетельствует уменьшение величины удельной электропроводности до 227,4 мСм/см.
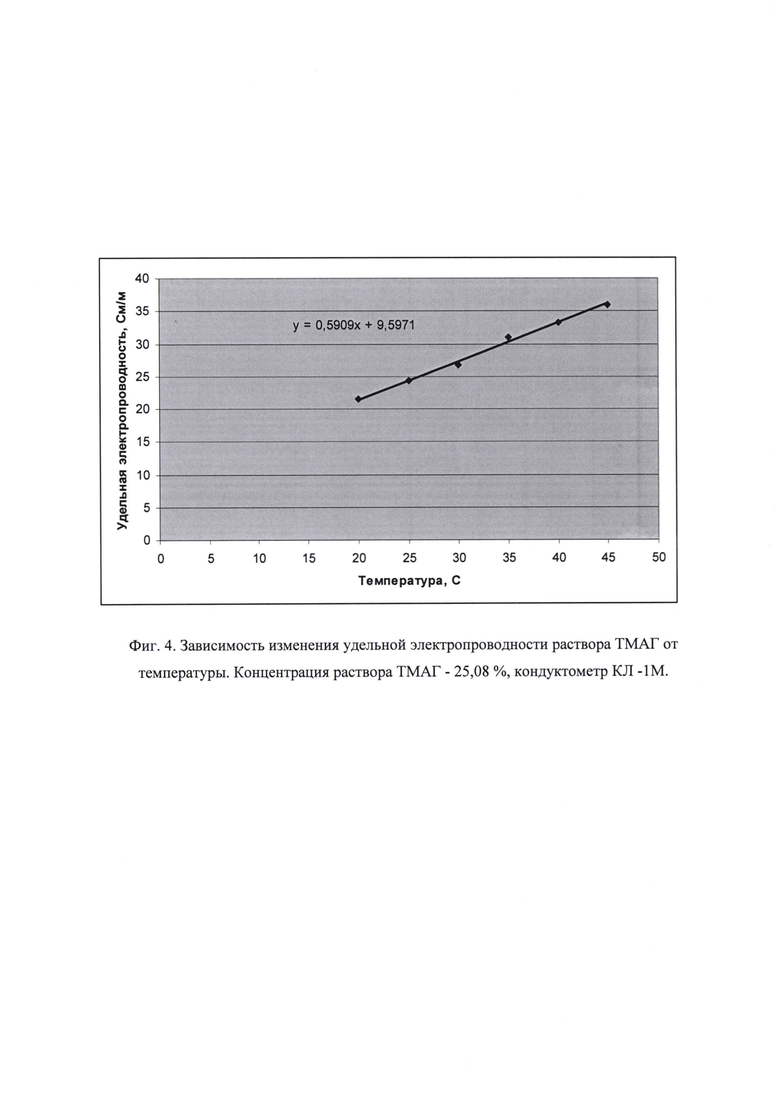
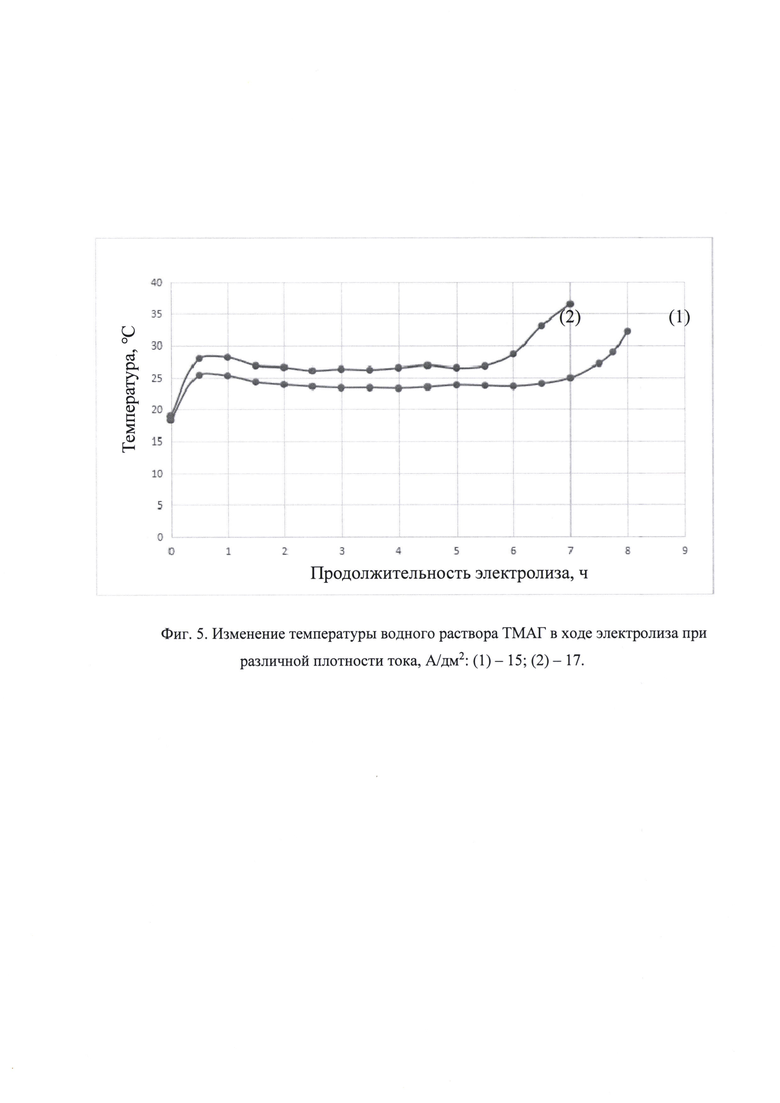
Как показали наши исследования, удельная электропроводность раствора ТМАГ существенно увеличивается с повышением температуры вследствие увеличения скорости движения ионов и уменьшения вязкости среды (фиг. 4). Поскольку температура раствора ТМАГ при его производстве в ходе электролиза может изменяться от 20 до 35°С в результате изменения удельной электропроводности как исходного бикарбоната тетраметиламмония, так и раствора образующегося ТМАГ (фиг. 5), поэтому измерение удельной электропроводности раствора ТМАГ должно проводиться в режиме автоматической температурной компенсации (АТК), который имеется в современных кондуктометрах. Для измерения величины удельной электропроводности анализируемого образца раствора ТМАГ рекомендуется температура 20°С.
При производстве раствора ТМАГ предпочтительнее датчик кондуктометра размещать в технологической схеме получения продукта, чем периодически отбирать его пробы, так как при этом достигается непрерывный контроль удельной электропроводности раствора, а, следовательно, концентрации ТМАГ в нем. При достижении нормируемой концентрации ТМАГ в растворе от 24,5 до 25,5% синтез целевого продукта прекращается.
При прямом кондуктометрическом определении концентрации ТМАГ в растворе исключается процесс титрования пробы раствора ТМАГ и построение кривой титрования, что упрощает и ускоряет анализ концентрации ТМАГ при его производстве, а также повышает эффективность процесса синтеза ТМАГ в целом.
Выбор прямого кондуктометрического определения концентрации ТМАГ в концентрированном водном растворе обусловлен низкими концентрациями карбонатов (не более 0,05% масс.) и хлоридов (не более 0,0001% масс.) при концентрации ТМАГ в растворе от 24,5 до 25,5%, что не оказывает влияния на величину удельной электропроводности анализируемого раствора.
Данные, касающиеся количественного определения концентрации ТМАГ в растворе прямой кондуктометрией, в научной и патентной литературе не приводятся. В то же время, в справочной литературе [Справочник по электрохимии, под ред. A.M. Сухотина. Л.: Химия, 1981. - 488 с; Добош Д. Электрохимические константы, М.: Мир, 1980. - 365 с] приводятся величины удельной электропроводности гидроксида натрия или калия в растворах с концентрацией от 1 до 40%, а в монографиях [Ротинян А.Л., Тихонов К.И., Шошина И.А. Теоретическая электрохимия. Л.: Химия, 1981, - 424 с; Левин А.И. Теоретические основы электрохимии. М.: Металлургиздат.1963, - 430 с; Дамаскин Б.Б., Петрий О.А. Основы теоретической электрохимии. М.: «Высшая школа». 1978, 239 с] представлены зависимости изменения удельной электропроводности от концентрации гидроксидов натрия или калия в том же интервале. Приведенные кривые χ=f(C) имеют сложный характер, связанный с изменением подвижности ионов с увеличением концентрации соли, и проходят через максимум, специфичный для данной неорганической щелочи и растворителя. К тому же, в работах [Конарев А.А. Тезисы доклада. 11 Международная научно-техническая конференция «Современные методы в теоретической и экспериментальной электрохимии», Плес, 2010, с. 164; Конарев А.А., Захарова И.В., Райнфарт В.В. и др. Патент РФ 2634789, 2017] приводятся лишь сведения об использовании прямой кондуктометрии только для анализа хлоридов в промывных водах, используемых для очистки фармацевтических субстанций карбамазепина и ферроцина соответственно.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Раствор ТМАГ производят на опытно-промышленной установке, приведенной на фиг. 6.
Для производства раствора ТМАГ с концентрацией от 24,5 до 25,5% готовят раствор исходного бикарбоната тетраметиламмония в емкости, поз. Р-2. Для приготовления исходного раствора бикарбоната тетраметиламмония с концентрацией 28-30%, в емкость, поз. Р-2 заливают деионизованную воду, а затем в нее загружают исходное сырье. Полученный водный раствор бикарбоната тетраметиламмония тщательно перемешивают принудительной циркуляцией с помощью насоса, поз. Н-6 по анодному контуру в течение 10-15 минут, затем останавливают насос, поз. Н-6.
В емкость, поз. Р-1 заливают деионизованную воду, а затем добавляют навеску из 20 г 25,0%-ного водного раствора гидроксида тетраметиламмония.
Приготовленный раствор бикарбоната тетраметиламмония из емкости, поз. Р-2 насосом, поз. Н-6 подают в анодные камеры электролизера, поз. Э-1, обеспечив его циркуляцию по замкнутому контуру, а приготовленный разбавленный раствор тетраметиламмония гидроксида из емкости, поз. Р-1 подают насосом, поз. Н-5 в катодные камеры электролизера, поз. Э-1, обеспечив его циркуляцию по замкнутому контуру. Для охлаждения рабочих растворов в змеевики емкостей, поз. Р-1 и Р-2 подают охлаждающую воду из водопроводной системы. Обеспечив циркуляцию растворов через электродиализатор, поз. Э-1, включают выпрямительный агрегат, поз. ВА-9 и устанавливают на нем по амперметру заданную силу тока 400 А.
На опытно-промышленной электрохимической установке в ходе электролиза поддерживают следующие параметры: силу тока - 400 А, температуру растворов от 20 до 35°С подачей холодной воды в змеевики аппаратов, поз. Р-1, Р-2 из водопроводной системы, контролируют удельную электропроводность образующегося раствора ТМАГ по показаниям кондуктометра, датчик которого помещен в емкость, поз. Р-1. При достижении величины значений удельной электропроводности образующегося раствора ТМАГ от 225,5 до 231,8 мСм/см электролиз прекращают, отключив подачу напряжения на электролизер, поз. Э-1.
Расчет концентрации ТМАГ в полученном растворе проводят по формуле (3), приведенной выше. При удельной электропроводности раствора ТМАГ, составляющей 228,34 мСм/см, концентрация ТМАГ в растворе - 24,95%, что соответствует технологическому интервалу концентрации ТМАГ от 24,5 до 25,5%.
Пример 2.
Раствор ТМАГ производят аналогично примеру 1.
Измеренная величина удельной электропроводности раствора ТМАГ составляет 229,72 мСм/см, а концентрация ТМАГ в растворе - 25,17%, что соответствует технологическому интервалу концентрации ТМАГ от 24,5 до 25,5%.
Пример 3.
Раствор ТМАГ производят аналогично примеру 1 и отбирают пробу.
В отобранную пробу помещают датчик кондуктометра и измеряют им удельную электропроводность полученного продукта, расчет концентрации ТМАГ в анализируемой пробе раствора ТМАГ проводят по формуле (3), приведенной выше. Измеренная величина удельной электропроводности раствора составляет 228,16 мСм/см, а концентрация ТМАГ в анализируемой пробе раствора - 24,92%.
Предлагаемый способ прямого кондуктометрического количественного определения концентрации ТМАГ в концентрированном водном растворе, используемом для производства безметальных проявителей при изготовлении интегральных схем в микроэлектронном производстве, повышает точность его анализа, упрощает и ускоряет его проведение, что обеспечивает его реализацию в производственных условиях, оптимизацию технологического процесса получения концентрированного водного раствора ТМАГ (исключает нецелесообразный перерасход электроэнергии и уменьшает длительность процесса синтеза ТМАГ на 30÷40 мин.).
Таким образом, задача изобретения решена.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРЯМОГО КОНДУКТОМЕТРИЧЕСКОГО КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ХЛОРИДОВ | 2016 |
|
RU2634789C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГИДРОХЛОРИДА 5-АМИНОЛЕВУЛИНОВОЙ (5-АМИНО-4-ОКСОПЕНТАНОВОЙ) КИСЛОТЫ | 2010 |
|
RU2413209C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГИДРОХЛОРИДА 5-АМИНОЛЕВУЛИНОВОЙ (5-АМИНО-4-ОКСОПЕНТАНОВОЙ) КИСЛОТЫ И ЕЕ СЛОЖНЫХ ЭФИРОВ | 2011 |
|
RU2442979C1 |
| Кондуктометрический способ определения концентрации хлорида натрия в стерильных растворах | 2023 |
|
RU2818483C1 |
| Способ количественного определения хлоридов в концентрате тетраметиламмония гидроксида | 2018 |
|
RU2707580C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ pH МАЛОБУФЕРНЫХ ПРЕДЕЛЬНО РАЗБАВЛЕННЫХ ВОДНЫХ РАСТВОРОВ ТИПА КОНДЕНСАТА | 2014 |
|
RU2573453C1 |
| Устройство для определения концентрации компонентов смеси сильных электролитов | 2016 |
|
RU2626297C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЧИЩЕННОГО КРАСИТЕЛЯ КИСЛОТНОГО ЯРКО-ГОЛУБОГО З | 2022 |
|
RU2787434C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ КИСЛЫХ ПРОДУКТОВ ТЕРМОЛИЗА ОРГАНИЧЕСКИХ ПРИМЕСЕЙ В ПАРЕ ПРЯМОТОЧНЫХ ЭНЕРГЕТИЧЕСКИХ КОТЛОВ | 2007 |
|
RU2329500C1 |
| СПОСОБ КОНТРОЛЯ СТЕПЕНИ ОТРАБОТКИ ЭЛЕКТРОЛИТА В СИСТЕМАХ ЭЛЕКТРОХИМИЧЕСКОЙ РЕГЕНЕРАЦИИ ВОЗДУХА СОВМЕЩЕННОГО ТИПА ПОДВОДНЫХ ЛОДОК | 2012 |
|
RU2499622C1 |

Изобретение относится к области аналитической химии. Раскрыт способ кондуктометрического количественного определения концентрации гидроксида тетраметиламмония в растворе, включающий отбор и подготовку проб анализируемого раствора гидроксида тетраметиламмония, построение градуировочного графика, измерение удельной электропроводности раствора гидроксида тераметиламммония и расчет его концентрации. При этом количественное определение концентрации гидроксида тетраметиламмония осуществляют прямым измерением удельной электропроводности концентрированного водного раствора гидроксида тетраметиламмония при температуре 20°С непосредственно в технологической схеме его производства или в отобранной пробе. Изобретение обеспечивает создание точного, простого и быстрого способа контроля концентрации гидроксида тетраметиламмония в водном растворе при его синтезе. 6 ил., 2 табл., 3 пр.
Способ кондуктометрического количественного определения концентрации гидроксида тетраметиламмония в растворе, включающий отбор и подготовку проб анализируемого раствора гидроксида тетраметиламмония, построение градуировочного графика, измерение удельной электропроводности раствора гидроксида тераметиламммония и расчет его концентрации, отличающийся тем, что количественное определение концентрации гидроксида тетраметиламмония осуществляют прямым измерением удельной электропроводности концентрированного водного раствора гидроксида тетраметиламмония при температуре 20°С непосредственно в технологической схеме его производства или в отобранной пробе, а расчет концентрации гидроксида тетраметиламмония (С2) в растворе проводят по следующей формуле:
С2 (%)=(χ - 70,897)/6,3095,
где χ _ величина удельной электропроводности анализируемого раствора ТМАГ, измеренная при температуре 20°С, мСм/см;
70,897 - коэффициент смещения по оси проводимости, мСм/см;
6,3095 - тангенс угла наклона прямой зависимости удельной электропроводности от концентрации ТМАГ, мСм/(см %).
| КОНАРЕВ А.А | |||
| и др | |||
| Получение концентрата тетраметиламмония гидроксида мембранным электролизом раствора хлорида тетраметиламмония //ЭЛЕКТРОННАЯ ТЕХНИКА | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| МИКРОЭЛЕКТРОНИКА, 2019, Выпуск 3(175), стр.25-37 | |||
| СПОСОБ ПРЯМОГО КОНДУКТОМЕТРИЧЕСКОГО КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ХЛОРИДОВ | 2016 |
|
RU2634789C2 |
| JP 2002257809 A, 11.09.2002 | |||
| Determination of alkaline component in photoresist remover solution // HIRANUMA | |||
Авторы
Даты
2025-05-12—Публикация
2024-09-25—Подача