Изобретение относится к медицине, а именно к нейрохирургии и онкологии, и может быть использовало для снижения числа повторного развития менингиом.
Менингиомы являются первичной опухолью центральной нервной системы (ЦНС), которые составляют 38.3% от общего числа случаев опухолей ЦНС (Ostrom Q.T., Patil N., Cioffi G., Waite K., Kruchko C., Barnholtz-Sloan J.S. CBTRUS Statistical Report: Primary Brain and Other Central Nervous System Tumors Diagnosed in the United States in 2013-2017. Neuro Oncol. 2020 Oct 30; 22 (12 Suppl 2): iv1-iv96. https://doi: 10.1093/neuonc/noaa200). В настоящее время стандартными лечебными процедурами у пациентов с менингиомами являются хирургия, радиотерапия, противоопухолевая лекарственная терапия. Также в процессе лечения регулярно проводится контроль его эффективности посредством МРТ с контрастным усилением и без него (Клинические рекомендации «Первичные опухоли центральной нервной системы», 2020, одобрены Научным советом Минздрава России в 20.12.2019).
Известно, что менингиомы имеют тенденцию к рецидиву. В современной клинической практике основными прогностическими факторами в отношении возникновения рецидивов, согласно клиническим рекомендациям, утвержденным Минздравом РФ, являются степень радикальности удаления опухоли, оцениваемая по шкале D. Simpson, и гистологический диагноз с определением степени анаплазии (Grade) (Клинические рекомендации «Первичные опухоли центральной нервной системы», 2020, одобрены Научным советом Минздрава России в 20.12.2019).
По степени анаплазии выделяют Grade 1-3. К Grade 1 относят доброкачественные или типические менингиомы, к Grade 2 - проявляющие переходные качества между доброкачественными и анапластическими менингиомами, к Grade 3 - анапластические менингиомы или злокачественные менингиомы. Известно, что менингиомы Grade 1 рецидивируют в 7-23% случаев, Grade 2 - в 41-55%, Grade 3 - в 72-78% (Ostrom Q.T., Patil N., Cioffi G., Waite K., Kruchko C., Barnholtz- Sloan J.S. CBTRUS StatisticalReport: Primary Brain and Other Central Nervous System Tumors Diagnosed in the United States in2013-2017. Neuro Oncol. 2020; 22. doi: 10.1093/neuonc/noaa200; Violaris K., Katsarides V., Sakellariou P. The Recurrence Rate in Meningiomas: Analysis of Tumor Location, Histological Grading, and Extent of Resection. Open J Modern Neurosurg. 2012; 2: 6-10. doi: 10.4236/ojmn.2012.21002; Rogers L., Barani I., Chamberlain M., Kaley T.J., McDermott M., Raizer J., Schiff D., Weber D.C., Wen P.Y., Vogelbaum M.A. Meningiomas: knowledge base, treatment outcomes, and uncertainties. A RANO review. J Neurosurg. 2015; 122 (1): 4-23. doi: 10.3171/2014.7. JNS131644). Продолженный рост и рецидив опухоли часто ведут к повторному оперативному вмешательству, что влияет не только на качество жизни, но и на выживаемость больных.
Зачастую радикальное удаление всего объема менингиомы невозможно, особенно при рецидивирующем течении неопластического процесса или в непосредственной близости и инвазии опухоли в функционально значимые зоны головного мозга, соответственно в таких случаях часть опухоли не может быть удалена. Стефани Сшипманн с соавторами в 2018 году показали, что остаточная часть опухоли должна рассматриваться как основа для продолженного роста менингиом, а соответственно разработка новых технологий воздействия на эту остаточную часть опухоли и зону ее исходного роста является перспективным направлением увеличения степени локального контроля за опухолевым процессом (Schipmann S., Schwake M, Sporns P.B. et al. Is the Simpson Grading System Applicable to Estimate the Risk of Tumor Progression After Microsurgery for Recurrent Intracranial Meningioma? World Neurosurg. 2018; 119:e589-e597. https://doi:10.1016/j.wneu.2018.07.215).
Одной из технологий воздействия на остаточную часть опухоли и зону ее исходного роста является фотодинамическая терапия (ФДТ). Лечебное действие ФДТ основано на локальной активации видимым красным светом накопившегося в опухолевой ткани фотосенсибилизатора, приводящей к развитию фотохимической реакции и разрушению опухолевых клеток. Основную роль в ФДТ играет синглетный, или активный, кислород, который образуется в молекулах липидов и белков мембран клеток и внутриклеточных органелл при воздействии на них кванта света. При этом синглетный кислород разрывает атомарные связи с другими атомами в составе молекулы из-за чего происходит разрыв цепочки молекулы и ее разрушение с образованием свободных радикалов и повреждением клеточных мембран. Молекула фотосенсибилизатора при поглощении кванта света также переходит в синглетное и в более долгоживущее триплетное состояние. При этом наблюдается резонанс, усиливающий фотодинамическую реакцию, или находящаяся в триплетном состоянии молекула фотосенсибилизатора передает энергию молекуле кислорода, переводя ее в синглетное состояние (Красновский А.А. Фотодинамическое действие и синглетный кислород // Биофизика. 2004. Т. 49. №2. С. 305-321). Возбужденные молекулы кислорода и фотосенсибилизатора возвращаются в исходное состояние и способны вступать в химические реакции. Весь цикл может быть запущен заново после поступления нового кванта световой энергии. После нескольких циклов фотосенсибилизатор «выгорает», т.е. теряет способность участвовать в фотодинамической реакции. Этот эффект называется фотобличингом (McCaughan Jr. J.S. Photodynamic therapy // Drugs and Aging. 1999. Vol. 15 (1). P. 49-68).
На сегодняшний день вопрос про происхождение клеток менингиом не решен. Хотя в конце 20 века рядом ученых высказывалось предположение, что менингиомы образуются из клеток арахноэндотелия грануляций паутинной оболочки головного мозга (ГМ), основанное на гистологическом сходстве клеток менингиомы с арахноэндотелием (Yamashima T., Kida S., Yamamoto S. Ultrastructural comparison of arachnoid villi and meningiomas in man. Mod Pathol. 1988; 1 (3): 224-234. https://DOI: 10.1007/BF02903517), роль арахноидэндотелия грануляций паутинной оболочки ГМ при изучении вопросов рецидивирования менингиом в литературе не рассматривалась. Соответственно на данный момент это не учитывается в клинической практике при определении тактики комплексного лечения и при постановке заключительного патоморфологического диагноза после проведения лечения.
Из опубликованных литературных источников известно, что грануляции паутинной оболочки имеют парасагиттальную, конвекситальную локализацию вблизи синусов твердой мозговой оболочки (ТМО), в области крыльев клиновидной кости, в области фалькса (Buetow M.P., Buetow P.C., Smirniotopoulos J.G. Typical, atypical, and misleading features in meningioma. Radiographics. 1991; 11 (6): 1087 1106. https://doi.org/10.1148/radiographics.11.6.1749851; Kunimatsu A., Kunimatsu N., Kamiya K., Katsura M., Mori H., Ohtomo K. Variants of meningiomas: a review of imaging findings and clinical features. Jpn J Radiol. 2016; 34 (7): 459-469. https://doi.org/10.1007/s11604-016-0550-6; Grzybowski, D.M., Herderick, E.E., Kapoor, K.G., Holman, D.W., & Katz, S.E. (2007). Human arachnoid granulations Part I: a technique for quantifying area and distribution on the superior surface of the cerebral cortex. Cerebrospinal fluid research, 4, 6. https://doi.org/10.1186/1743-8454-4-6). Грануляции паутинной оболочки имеют характерную макроскопическую структуру, что позволяет идентифицировать эти области, в особенности, если они представлены гипертрофированным вариантом развития, то есть увеличенным в размере (Фиг. 1) (Ogul, H., Guven, F., Izgi, E., & Kantarci, M. (2019). Evaluation of giant arachnoid granulations with high-resolution 3D-volumetric MR sequences at 3T. European journal of radiology, 121, 108722. https://doi.org/10.1016/j.ejrad.2019.108722).
Наличие рецидива опухоли, в том числе и после ее радикального хирургического удаления, свидетельствует о несовершенстве существующих способов лечения.
Известен патент №2756868 «Способ профилактики рецидивов менингиом», заключающийся в том, что во время операции по удалению опухоли производят иссечение ТМО в радиусе 2,5 см вокруг зоны роста опухоли. Способ обеспечивает повышение радикальности удаления менингиомы, профилактику рецидива за счет удаления стыка зоны роста менингиомы и ТМО.
Недостатком данного способа является тот факт, что он не учитывает возможный рост опухоли в области контакта грануляций паутинной оболочки ГМ и ТМО, а соответственно риск рецидива менингиомы сохраняется. Также данный способ не применим при локализации менингиомы в области основания черепа, в области верхнего сагиттального синуса или при инвазивном типе роста опухоли в окружающие ткани.
Известен патент №2211057 «Способ предотвращения рецидива гиперостозной менингиомы головного мозга», заключающийся в том, что поверхность гиперостоза, то есть области, где произошло избыточное образование новой кости или утолщение уже существующей, обрабатывают сканирующим лучом Nd-YAG-лазера мощностью не более 20 Вт, диаметром не более 3 мм в течение 15-20 мин до полной абляции и обугливания гиперостоза на всей его площади. Способ позволяет уменьшить травматизацию головного мозга при удалении опухоли.
Недостатком данного способа является применимость его только для менингиом с гиперостозом и не возможность применить его для мягкотканных менинигиом, при локализации менингиомы в непосредственной близости от магистральных артерий и вен мозга или его функциональных зон, а также бесконтрольное неселективное воздействие излучения на окружающие ткани, что может привести к их повреждению и ухудшению неврологического статуса пациента.
Известен патент №2689795 «Способ прогнозирования рецидивов менингиом в послеоперационном периоде». Этот способ заключается в том, что фрагмент опухоли замораживают и получают гистологические срезы менингиомы, затем проводят иммуногистохимическое исследование, обработав срез реактивом с антителами к белку Циклин-D1. Затем полученный̆ препарат исследуют в световом микроскопе для определения экспрессии белка Циклин-D1, выраженного в процентах. При наличии экспрессии белка Циклин-D1 менее 3% прогнозируют безрецидивное течение менингиомы. При экспрессии белка Циклин-D1 свыше 3% прогнозируют высокую вероятность рецидива менингиомы.
Недостатком данного способа является тот факт, что он не учитывает распространенность менингиомы за пределами прооперированной области. Также необходимость проведения дополнительного иммуногистохимического исследования, наличия необходимых реактивов, что удорожает и удлиняет процесс прогнозирования рецидивов.
Известен патент №2214293 «Способ лечения злокачественных опухолей головного мозга с использованием фотодинамической лазерной терапии». Этот способ заключается в том, что спустя 10-12 суток с момента проведения операции (удаление опухоли) проводят принудительную локорегиональную доставку фотосенсибилизатора (ФС) в ликворные пространства головного мозга дважды через 24 ч. Через 2 ч после второго введения ФС осуществляют 2 последовательных сеанса чрескожной транскраниальной фотодинамической лазерной терапии ложа удаленной опухоли посредством сканирующего облучения расфокусированным лучом лазера с длиной волны 675 нм и мощностью 0,15-0,20 Вт в течение 20 мин. При этом перед проведением фотодинамической лазерной терапии эвакуируют 15-20 мл ликвора (из которых 2-4 мл удаленного ликвора исследуют спектроскопически и хроматографически для регистрации ФС в ликворе и определения его концентрации) для предупреждения внутричерепной гипертензии. Сеансы чрескожной транскраниальной фотодинамической лазерной терапии проводят с интервалом в 24 ч. Предлагаемый способ позволяет улучшить результаты лечения посредством предотвращения процедива в зоне удаленной опухоли.
Недостатком данного способа является отсутствие подтверждения накопления ФС в тканях опухоли, так как ФС вводят в полость ликворной кисты в зоне удаления опухоли, а не в сами клетки опухоли. Также при такой реализации изобретения нельзя определить была ли получена терапевтическая дозировка при облучении из-за отсутствия измеримого контроля проводимой терапии, что снижает эффективность лечения. Вместе с тем проводимые повторные инвазивные вмешательства в головной мозг пациентов увеличивают риск появления осложнений и ухудшения неврологического статуса пациента.
Технической задачей изобретения является снижение частоты повторного развития менингиомы.
Техническим результатом изобретения является создание эффективного способа профилактики и прогнозирования рецидивов интракраниальльной менингиомы после хирургического лечения, что позволяет увеличивать без рецидивный период у больных и качество их жизни.
Технический результат достигается за счет удаления опухоли под интраоперационным флуоресцентным контролем, с последующим проведением профилактики рецидивов с помощью ФДТ и гистологического исследования материала ткани грануляций паутинной оболочки, близлежащей к области опухоли, на наличие опухолевых клеток.
Способ осуществляют, например, следующим образом.
Способ реализуется как часть выполнения хирургического лечения интракраниальных менингиом любой локализации в несколько этапов.
I этап
Пациенту за 6 часов до предполагаемой операции перорально вводят фотосенсибилизатор (ФС) 5-аминолевулиновую кислоту (5-АЛА) в дозировке 20 мг/кг, либо в течение 30 минут после введения наркоза вводят через капельницу внутривенно - хлорин Е6 в дозировке 1мг/кг. Операция включает в себя выполнение широкой костно-пластической трепанации черепа, чтобы визуализировать как опухоль, так области расположения грануляций паутинной оболочки для последующего забора материала оттуда.
II этап
Визуализацию локализации опухоли проводят интраоперационно с помощью биспоктроскопии и визуальной оценки интенсивности флуоресцентного эффекта. Область опухоли является зоной с интенсивностью флуоресценции и индексом флуоресценции (ИФ) выше, чем в здоровых тканях.
Биоспектроскопия позволяет оценить степень накопления ФС в тканях пациента в области операции посредством высчитывания ИФ, равного отношению интенсивности флуоресценции ФС к интенсивности отраженного лазерного сигнала. Выражается в условных единицах (У. Е.). Биоспектроскопия проводится, например, с помощью лазерной электронно-спектральной установки ЛЭСА-01-Биоспек (Биоспек, Россия) с использованием волоконно-оптического зонда и программного обеспечения, например, Uno (Биоспек, Россия).
Для визуальной оценки интенсивности флуоресцентного эффекта используется 4-балльная шкала: 0 - отсутствие видимой флуоресценции, 1 - слабое свечение, 2 - умеренное свечение, 3 - яркое свечение. Оценка по шкале производится хирургом самостоятельно в зависимости от контраста флуоресценции опухоль/здоровая ткань. Для визуализации флуоресценции от 5-АЛА используется источник излучения света с длиной волны 400 нм, например, операционный микроскоп Leica, (Германия), от хлорина Е6 - источник излучения света с длиной волны 405 нм, например, операционный микроскоп LEICA M720 OH5 (Германия) с модификацией источника света путем подключения специализированного лампового осветителя синего света «ECO bright» (SOI-Korea Center).
III этап
Хирургическое удаление менингиомы выполняют под интраоперационным флуоресцентным контролем, основываясь на данных биоспектроскопии и визуальной оценке флуоресценции. После максимально возможного удаления менингиомы с учетом физиологической и функциональной дозволенности в ложе удаленной опухоли достигается тщательный гомеостаз. После чего проводится визуализация зон с высоким ИФ и высокой интенсивностью флуоресценции посредством биоспектроскопии и визуальной оценки флуоресценции. Если такие зоны были выявлены, то далее они подвергаются фотодинамической терапии (ФДТ); если таких зон выявлено не было, то ФДТ не проводится, а следующий этап пропускается.
IV этап
Облучение ложа опухоли проводят с помощью лазерных аппаратов. Выбор аппарата зависит от использованного ФС.
При применении 5-АК в качестве ФС используется, например, лазерная установка ЛФТ-02-Биоспек (Биоспек, Россия) с мощностью 2 Вт и длинной волны излучения 635 нм с моноволоконными гибкими световодами с цилиндрическим концевым излучателем или торцевым концевым излучателем. При использовании хлорина Е6 в качестве ФС используется, например, лазерная установка «Латус-2,5» (ООО «Полупроводниковые приборы», Санкт-Петербург) мощностью до 2,5 Вт и длиной волны излучения 662 нм с моноволоконным гибким световодом с насадками в форме цилиндра или шара. Выбор насадки зависит от геометрии облучаемого участка.
Общая длительность терапии разделяется на сеансы по 2-5 минут с перерывами 1-2 минуты для выполнения биоспектроскопического контроля, с помощь которого определяется продолжительность ФДТ. ФДТ заканчивают тогда, когда происходит полная фотодеградация молекулы фотосенсибилизатора, то есть наблюдается эффект фотобличинга.
Также после завершения ФДТ рассчитывается полученная световая доза (Дж/см2) по формуле:
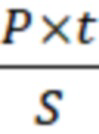 , где
, где
Р - мощность лазерного излучения, Вт,
t - длительность ФДТ, сек,
S - площадь облучаемого участка, см2.
V этап
Далее производят забор грануляций паутинной оболочки, близлежащей к области опухоли, с использованием следующих хирургических инструментов: ножницы, хирургический пинцет, биполярная коагуляция. При выполнении забора материала грануляций паутинной оболочки важно не допустить излишней коагуляции забираемой ткани, что может ухудшить качество операционного материала и затруднить последующее гистологическое исследование врачом-патологоанатомом. При возникновении кровотечения применяются стандартные методы остановки кровотечения.
Полученный материал исследуют в лабораторных условиях, при этом данный материал проходит те же этапы подготовки препарата для гистологического исследования, что и материал опухоли, в том числе применяется стандартная технология по приготовлению парафиновых блоков. После пробоподготовки материал в виде гистологических стекол исследуется врачом-патологоанатомом. В случае определении опухолевых клеток в материале грануляций паутинной оболочки прогнозируется высокий риск рецидива опухоли, что является дополнительным обоснованием для назначения дополнительного курса лучевой терапии.
Заявленное изобретение поясняется чертежами:
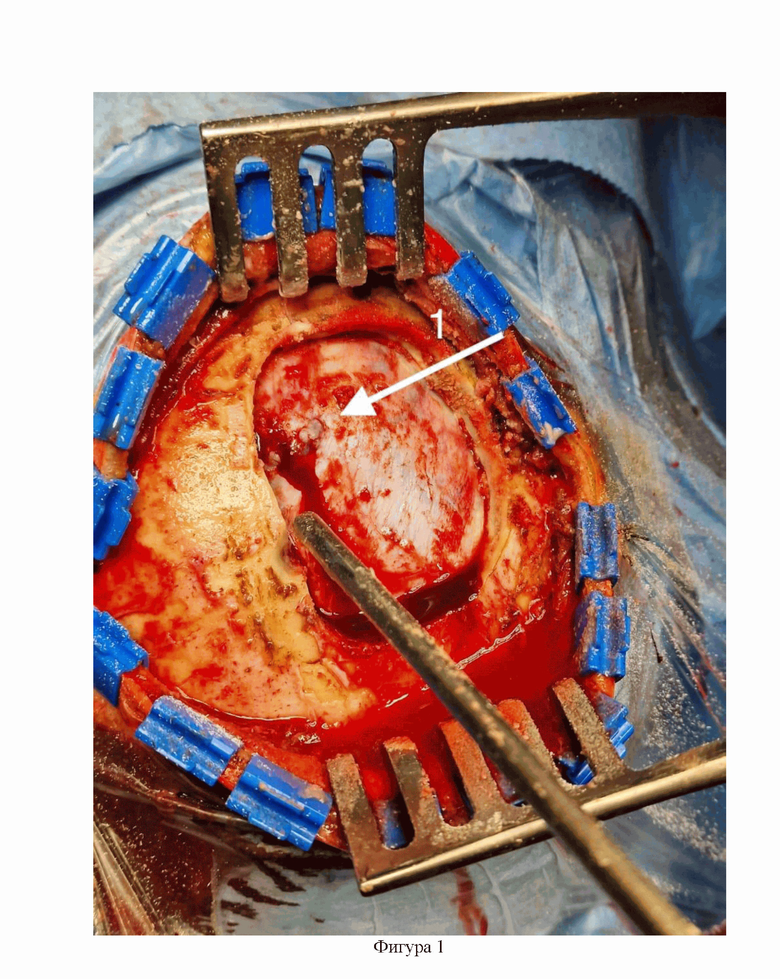
Фигура 1 - интраоперационная картина гипертрофированной грануляции паутинной оболочки головного мозга.
1 - грануляция паутинной оболочки.
Фигура 2 - МРТ-картина менингиом пациента А. из примера №1.
А - аксиальная проекция, размеры менингиомы - 1,6*1,7*1,9 см.
2 - конвекситальная менингиома.
Б - сагиттальная проекция, размеры опухоли - 4,29*5,20*5,76 см.
2 - конвекситальная менингиома.
В - коронарная проекция, размеры опухоли - 1,6*1,7*1,9 см.
2 - конвекситальная менингиома, 3 - фалькс-менингиома.
Фигура 3 - гистологическая картина участка папиллярной злокачественной менингиомы Grade 3 пациента А. из примера №1. Окраска гематоксилином и эозином, увеличение х200.
Фигура 4 - гистологическая картина участка грануляции паутинной оболочки головного мозга со структурами менингиомы пациента А. из примера №1. Окраска гематоксилином и эозином, увеличение х100.
4 - структура грануляции паутинной оболочки, 5 - менингиома.
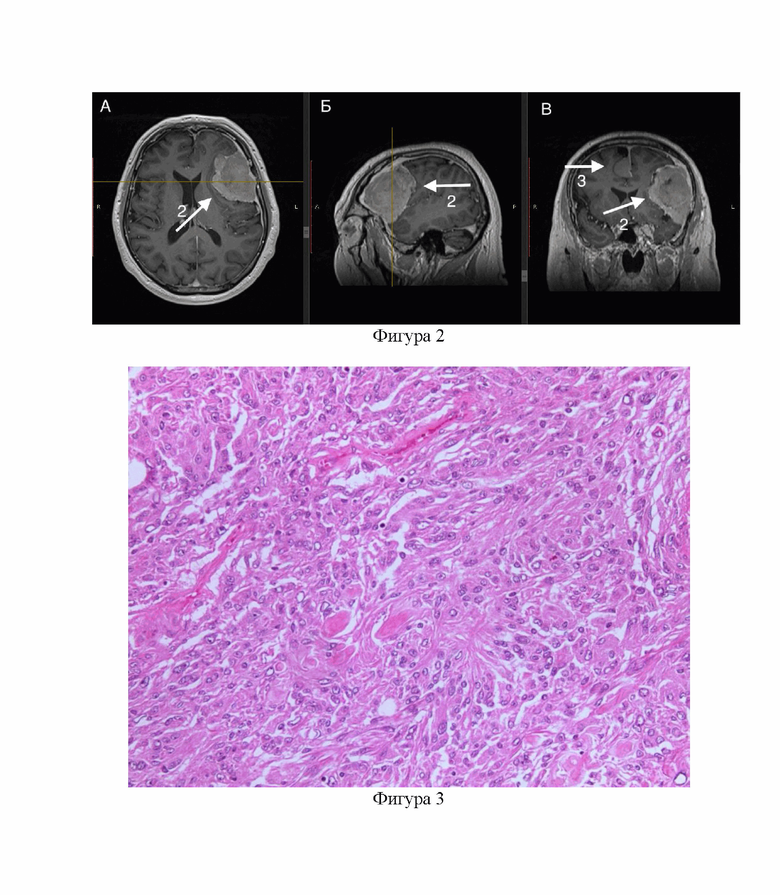
Фигура 5 - МРТ-картина менингиомы размера 4,5*4,4*4,4 см пациента Е. из примера №2.
А - сагиттальная проекция.
6 - парасагиттальная менингиома.
Б - аксиальная проекция.
6 - парасагиттальная менингиома.
В - коронарная проекция.
6 - парасагиттальная менингиома.
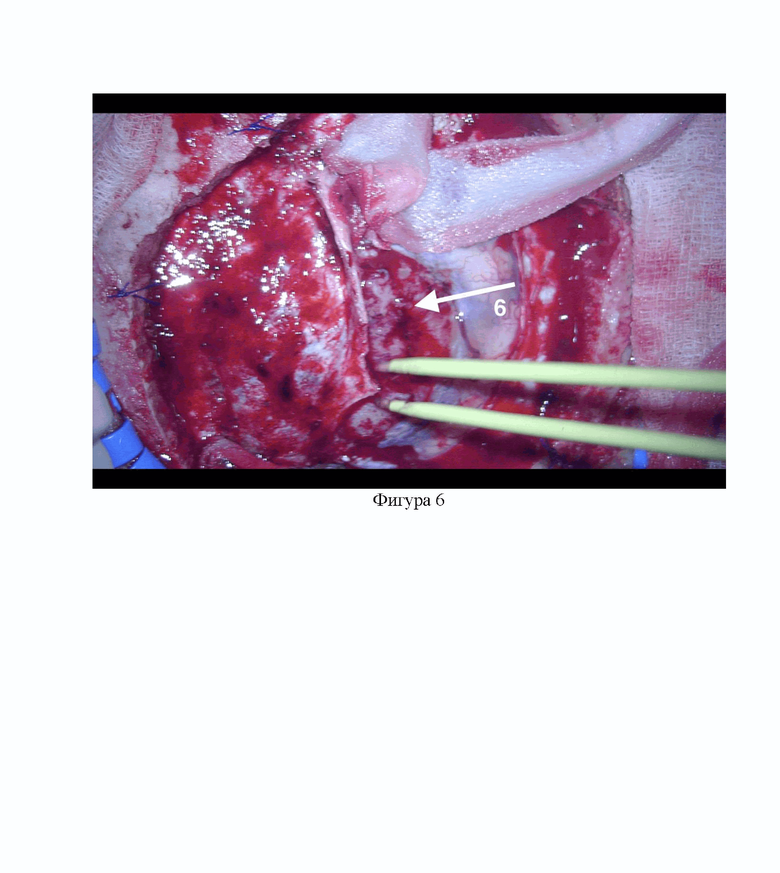
Фигура 6 - интраоперационная картина парасагиттальной менингиомы у пациента Е. из примера №2.
6 - парасагиттальная менингиома.
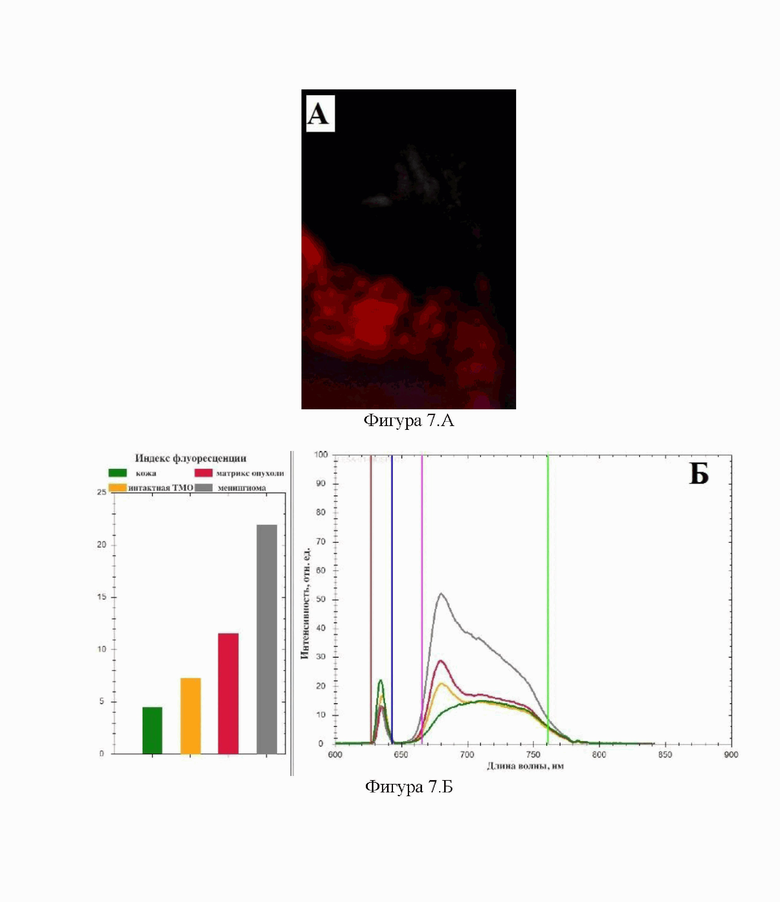
Фигура 7 - флюоресцентная визуализация и биоспектроскопия менингиомы пациента Е. из примера №2.
А - интраоперационная визуализация флуоресценции, степень контрастности флуоресценции опухоль/здоровая ткань равна 3.
Б - данные биоспектроскопического исследования до проведения ФДТ: ИФ кожи равно 4,8; ИФ интактной ТМО - 7; ИФ матрикса опухоли - 12; ИФ менингиомы - 22.
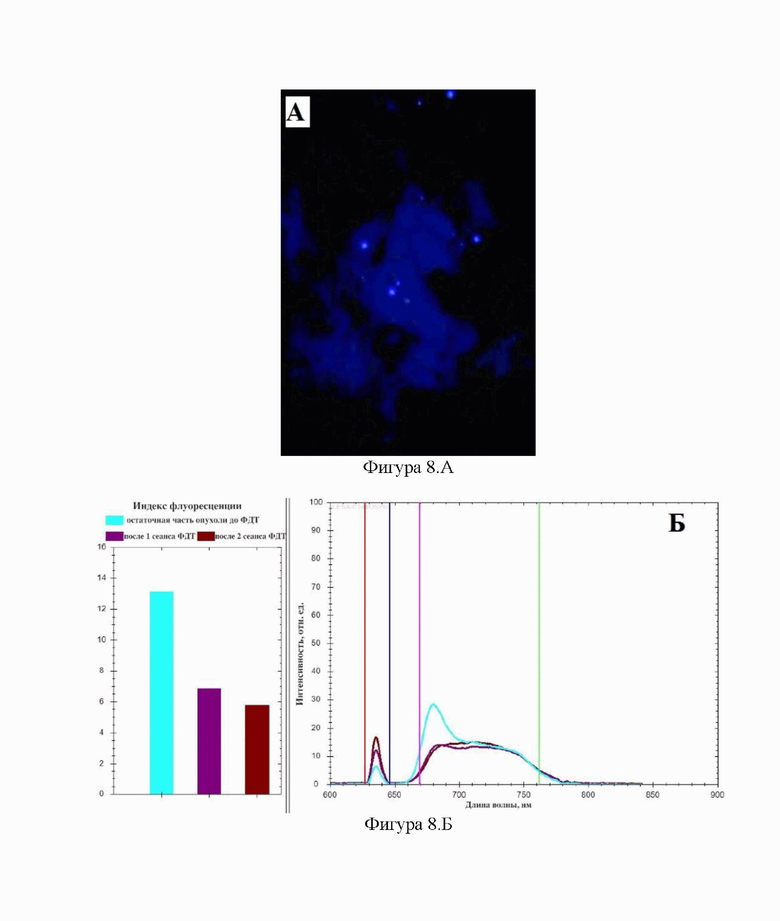
Фигура 8 - флюоресцентная визуализация и биоспектроскопия менингиомы пациента Е. из примера №2.
А - интраоперационная визуализация флуоресценции, степень контрастности флуоресценции опухоль/здоровая ткань равна 0.
Б - данные биоспектроскопического исследования: ИФ остаточной части опухоли до начала ФДТ равен 13, после первого сеанса ФДТ - ИФ равен 7, после второго сеанса ФДТ - ИФ равен 6.
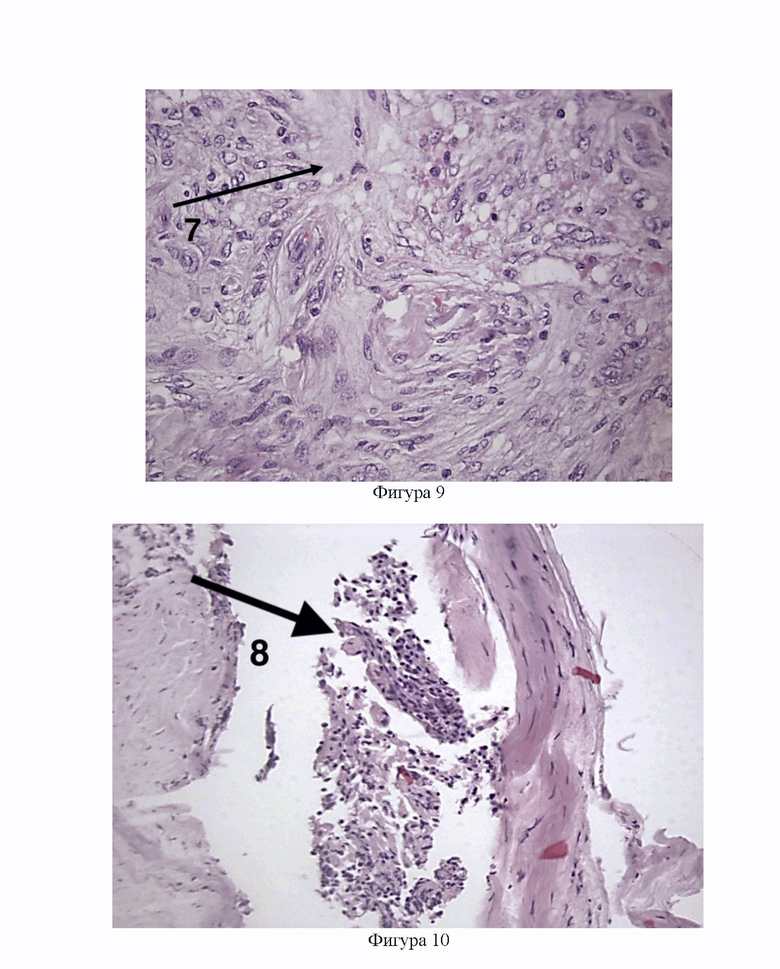
Фигура 9 - Микропрепарат менингиомы Grade 2 с клеточным и ядерным полиморфизмом пациентки Е. из примера №2. Окраска гематоксилином и эозином, увеличение х400.
7 - микронекроз.
Фигура 10 - Микропрепарат грануляции паутинной оболочки с наличием опухолевой ткани атипической менингиомы пациентки Е. из примера №2. Окраска гематоксилином и эозином, увеличение х200.
8 - менингиома.
Способ подтверждается следующими клиническими примерами.
Клинический пример №1
Пациент А. 71 год с клинической картиной судорожного синдрома по типу генерализованного клонико-тонического приступа, а также умеренной общемозговой симптоматикой был госпитализирован в отделение нейрохирургии №6 ФГБУ НМИЦ им. В.А. Алмазова МЗ РФ.
По данным МРТ головного мозга с внутривенным контрастированием были выявлены множественные внемозговые объемные новообразования в левой лобно-височной области (2), в области фалькса (3) с распространением вправо с равномерным распределением контрастного вещества, перифокальный отек не был выражен, нейровизуализационная картина соответствовала менингиоме. У опухоли в левой лобно-височной области был отмечен крупный размер, а также гетерогенность структуры (Фигура 2). Оперативное вмешательство по удалению опухоли левой лобно-височной области проводилось в условиях гибридной операционной с использованием интраоперационного нейрофизиологиечского мониторинга, а также интраоперационного флуоресцентного контроля с применением 5-аминолевуленовой кислоты в качестве фотосенсибилизатора (ФС). Интраоперационно макроскопически картина опухоли соответствовала менингиоме, в режиме флюоресценции свечение было расценено как яркое (степень визуальной интенсивности флуоресценции равна была 3). Выполнено радикальное удаление опухоли, степень радикальности соответствовала I степени по D. Simpson, после удаления опухоли при проведении измерения ИФ и визуальной оценки интенсивности флуоресценции не было выявлено зон с более яркой интенсивностью флуоресценции и высоким ИФ, чем в здоровых тканях, соответственно ФДТ не проводилась.
На морфологическое исследование был направлен материал патологической ткани опухоли, а также гипертрофированная ткань грануляции паутинной оболочки, обнаруженной на расстоянии около 3 см от узла опухоли. Гистологическое исследование опухолевого узла выявило менингиому Grade 3 преимущественно папиллярного строения, инфильтрирующую твердую мозговую оболочку в зоне матрикса (Фигура 3). Опухолевая ткань представлена арахноидэндотелием с выраженным клеточным и ядерным полиморфизмом, содержащая разнообразные структуры, напоминающие розетки и сосочки, простынное разрастание клеток; выявлялись очаги декомплексированных крупных эпителиоидных и рабдоидных клеток с обильной эозинофильной цитоплазмой с крупными ядрами. Митозов и некрозов нет. В прилегающих к опухолевому узлу грануляциях паутинной оболочки (4) обнаружены структуры менингиомы (5) с признаками анаплазии, выраженным клеточным и ядерным полиморфизмом (Фигура 4).
С учетом проведенного патоморфологического исследования и выявления опухолевой ткани в структуре грануляции паутинной оболочки - отмечен высокий риск рецидива опухоли. Пациенту дана рекомендация - проведение лучевой терапии с последующим динамическим наблюдением в объеме регулярных МРТ-исследований головного мозга с внутривенным контрастированием. Лучевая терапия была проведена на линейном ускорителе, СОД 60 Гр. На контрольной интраскопии (МРТ головного мозга с внутривенным контрастированием) через 14 месяцев - данных, подтверждающих наличие рецидива опухоли, не было получено.
Клинический пример №2
Пациент Е. 61 год с клинической картиной судорожного синдрома по типу частых фокальных приступов с трансформацией в билатеральные тонико-клонические приступы; левостороннего спастического нижнего монопареза, атаксии, а также общемозговой симптоматики был госпитализирован в отделение нейрохирургии №6 ФГБУ НМИЦ им. В.А. Алмазова МЗ РФ.
По данным МРТ головного мозга с внутривенным контрастированием было выявлено внемозговое образование в области средней трети верхнего сагиттального синуса (ВСС) с двусторонним распространением, преимущественно вправо, с развитием перифокального отека, нейровизуализационная картина соответствовала парасагиттальной менингиоме (6) (Фигура 5). Оперативное вмешательство по удалению опухоли области средней трети ВСС проводилось в условиях гибридной операционной с использованием интраоперационного нейрофизиологиечского мониторинга интраоперационной флюоресцентной навигацией с применением Хлорина Е6 в качестве ФС. Интраоперационно макроскопически картина опухоли соответствовала парасагиттальной менингиоме (6) (Фигура 6). Далее провели биспоктроскопию и визуальную оценку интенсивности флуоресцентного эффекта. Степень визуальной интенсивности флуоресценции опухоль/здоровая ткань равна была 3 (Фигура 7. А), а индекс ИФ менингиомы (6) был равен 22 (Фигура 7. Б). Выполнено микрохирургическое удаление опухоли: выполнена внутриопухолевая декомпрессия, затем отделение опухолевой ткани от окружающей ткани головного мозга. При удалении отмечена спаянность менингиомы с тканью головного мозга, прорастание стенки ВСС. Учитывая высокий риск геморрагических осложнений и ухудшения по неврологическому статусу в послеоперационном периоде, было принято решение закончить хирургическое удаление. Степень радикальности соответствовала III степени по D. Simpson.
После удаления опухоли было произведено измерение ИФ и интенсивности флуоресценции в области операционного поля. Оставленный фрагмент опухоли в полости ВСС равномерно флюоресцировал с ИФ равным 13, после 1 сеанса ФДТ ИФ снизился до 7, после 2 сеанса - до 6 (Фигура 8. Б), степень визуальной интенсивности флуоресценции равна 0 (Фигура 8. А). Параметры ФДТ были следующие: доза ФС 80 мг, режим обучения - 2 сеанса по 5 мин, итоговая световая доза составила 159 Дж/см3, а плотность мощности 265 мВт/см2.
На морфологическое исследование был направлен материал патологической ткани опухоли, перифокальной зоны, а также ткань грануляции паутинной оболочки, обнаруженной на расстоянии до 3 см от узла опухоли. Гистологическое исследование выявило атипическую менингиому Grade 2 с инвазией в ткань головного мозга, твердую мозговую оболочку. Опухоль из арахноидэндотелия с умеренным клеточным и ядерным полиморфизмом, обнаружены апоптозные тельца, очаги организованных микронекрозов (7) (Фигура 9). В грануляциях паутинной оболочки обнаружены пролифераты опухолевой ткани атипической менингиомы (8) (Фигура 10).
Ранний послеоперационный период протекал без осложнений. За время наблюдения в условиях профильного отделения отмечено увеличение мышечной силы, сохраняется легкий парез в левой стопе; вертикализирована, ходьба отработана; иктальных событий не зафиксировано. Функциональная активность по шкале Карновского 80. С учетом проведенного патоморфологического исследования и выявления опухолевой ткани в структуре грануляции паутинной оболочки - отмечен высокий риск рецидива опухоли. Пациенту дана рекомендация - проведение лучевой терапии с последующим динамическим наблюдением в объеме регулярных МРТ-исследований головного мозга с внутривенным контрастированием. Радиохирургическое лечение (вариант лучевой терапии) было проведено. На контрольной интраскопии (МРТ головного мозга с внутривенным контрастированием) через 9 месяцев - данных, подтверждающих наличие рецидива опухоли, не было получено.
Предложенный способ позволяет повысить эффективность хирургического лечения интракраниальной менингиомы путем снижения частоты возникновения рецидивов, при этом выявление опухолевых клеток в материалах грануляций паутинной оболочки должно является дополнительным показанием к проведению курса адъювантной терапии с последующим динамическим наблюдением в объеме регулярных (каждые 6-12 месяцев) МРТ-исследований головного мозга с внутривенным контрастированием. Данный способ позволяет увеличить безрецидивный период, продолжительность жизни больных и улучшить ее качество.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ комбинированного лечения немышечно-инвазивного рака мочевого пузыря T1-T2 N0+M0 | 2022 |
|
RU2787917C1 |
| Способ профилактики рецидивов менингиом | 2021 |
|
RU2756868C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВОВ МЕНИНГИОМ В ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД | 2018 |
|
RU2689795C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛУБИННЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА, РАСПОЛОЖЕННЫХ ВБЛИЗИ КОРТИКОСПИНАЛЬНОГО И КОРТИКОБУЛЬБАРНОГО ТРАКТОВ, С ПРИМЕНЕНИЕМ СТЕРЕОТАКСИЧЕСКОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПОД СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНЫМ И НЕЙРОФИЗИОЛОГИЧЕСКИМ МОНИТОРИНГОМ | 2023 |
|
RU2830942C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВОВ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ОРГАНОВ МАЛОГО ТАЗА ИЛИ НЕОРГАННЫХ ОПУХОЛЕЙ ЗАБРЮШИННОГО ПРОСТРАНСТВА | 2011 |
|
RU2486933C1 |
| СПОСОБ УДАЛЕНИЯ МЕНИНГИОМЫ, ВРАСТАЮЩЕЙ В ПОЛОСТЬ ВЕРХНЕГО САГИТТАЛЬНОГО СИНУСА В СРЕДНЕЙ/ЗАДНЕЙ ТРЕТИ | 2006 |
|
RU2316284C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2014 |
|
RU2552032C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОПУХОЛЕЙ | 2012 |
|
RU2519936C2 |
| УСТРОЙСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РЕЗИДУАЛЬНЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА С ФЛУОРЕСЦЕНТНЫМ КОНТРОЛЕМ ФОТООБЕСЦВЕЧИВАНИЯ ФОТОСЕНСИБИЛИЗАТОРА | 2021 |
|
RU2801893C2 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ В КОМБИНИРОВАННОМ ЛЕЧЕНИИ МЕСТНО-РАСПРОСТРАНЕННЫХ САРКОМ МЯГКИХ ТКАНЕЙ | 2020 |
|
RU2737704C2 |
Изобретение относится к медицине, а именно к нейрохирургии. До начала операции или после введения больного в наркоз вводят больному фотосенсибилизатор. Выполняют костно-пластическую трепанацию черепа. Визуализируют опухоль. Удаляют опухоль под интраоперационным флуоресцентным контролем. Далее проводят флуоресцентную диагностику и биоспектроскопию для выявления участков матрикса и остатков капсулы опухоли. Проводят профилактику рецидивов, а именно продолженного роста выявленных участков матрикса и остатков капсулы опухоли с помощью фотодинамической терапии (ФДТ). При этом ФДТ разделена на сеансы по 2-5 минут с перерывами 1-2 минуты для выполнения биоспектроскопического контроля. В случае, если не было выявлено участков матрикса и остатков капсулы опухоли с продолженным ростом, ФДТ не проводится. Способ позволяет провести профилактику рецидивов интракраниальной менингиомы после хирургического лечения, увеличивать безрецидивный период у больных, повысить качество их жизни. 6 з.п. ф-лы, 10 ил., 2 пр.
1. Способ профилактики рецидивов интракраниальльных менингиом после хирургического лечения, включающий выполнение костно-пластической трепанации черепа, визуализацию локализации опухоли, удаление опухоли, проведение профилактики рецидивов, отличающийся тем, что до начала операции или после введения больного в наркоз вводят больному фотосенсибилизатор, удаляют опухоль под интраоперационным флуоресцентным контролем, далее проводят флуоресцентную диагностику и биоспектроскопию для выявления участков матрикса и остатков капсулы опухоли; проводят профилактику рецидивов, а именно продолженного роста выявленных участков матрикса и остатков капсулы опухоли, с помощью фотодинамической терапии (ФДТ), при этом ФДТ разделена на сеансы по 2-5 минут с перерывами 1-2 минуты для выполнения биоспектроскопического контроля; если не было выявлено участков матрикса и остатков капсулы опухоли с продолженным ростом, ФДТ не проводится.
2. Способ по п. 1, отличающийся тем, что в качестве фотосенсибилизатора используется 5-аминолевулиновая кислота в дозировке 20 мг/кг, которая вводится перорально за 6 часов до предполагаемой резекции опухоли.
3. Способ по п. 1, отличающийся тем, что в качестве фотосенсибилизатора используется хлорин Е6 в дозировке 1мг/кг, который вводится внутривенно через капельницу в течение 30 минут после введения наркоза при осуществлении предполагаемой резекции опухоли.
4. Способ по п. 1, отличающийся тем, что флуоресцентную диагностику проводят с помощью источника излучения света с длиной волны в диапазоне 400-405 нм.
5. Способ по п. 1, отличающийся тем, что при ФДТ используют лазерную установку с мощностью 2-2,5 Вт и длиной волны 635-662 нм.
6. Способ по п. 1, отличающийся тем, что определение продолжительности ФДТ осуществляют с помощью биоспектроскопического контроля.
7. Способ по п. 1, отличающийся тем, что ФДТ заканчивают в момент фотодеградации молекулы фотосенсибилизатора.
| Ушанов В.В | |||
| и др | |||
| Роль грануляций паутинной оболочки в рецидивировании менингиом | |||
| Российский нейрохирургический журнал им | |||
| проф | |||
| А.Л | |||
| Поленова | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| Потапов А.А | |||
| и др | |||
| Приспособление для записи звуковых явлений на светочувствительной поверхности | 1919 |
|
SU101A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Олюшин В.Е | |||
Авторы
Даты
2025-05-26—Публикация
2024-06-27—Подача