Настоящее изобретение относится к фармацевтическим упаковкам, содержащим определенные полипропиленовые контейнеры и упакованные в них водные препараты NGF.
Упаковка является одним из важных аспектов фармацевтической промышленности, обеспечивающим защиту и сохранность лекарственного средства при транспортировке, хранении, продаже и использовании.
Первичная упаковка имеет большое значение, так как она находится в непосредственном контакте с лекарственным средством, поэтому она должна быть инертной и не вызывать каких-либо изменений в ее составе.
Вид первичной упаковки зависит от лекарственной формы и химического состава препарата. Для жидких лекарственных форм обычно используются высококачественные стеклянные или пластмассовые материалы. Стекло является широко используемым материалом, потому что оно химически инертно и позволяет очень легко проверять содержимое контейнера. Однако стекло хрупкое и дорогое.
Что касается пластика, то его преимущество заключается в гибкости, малом весе и экономичности, но в некоторых случаях возникают проблемы из-за того, что некоторые лекарства могут реагировать с контейнером.
Для фармацевтической первичной упаковки материалы на основе полипропилена были одобрены Фармакопеями и широко используются.
Фактор роста нервов (NGF) представляет собой сложный белок, регулирующий выживание, развитие и функцию нейронов как на центральном, так и на периферическом уровне.
Предполагается, что NGF эффективен для лечения некоторых дегенеративных заболеваний как периферической, так и центральной нервной системы, включая наследственные сенсорные и двигательные невропатии, наследственную и спорадически возникающую системную дегенерацию, боковой амиотрофический склероз, болезнь Паркинсона и болезнь Альцгеймера. В настоящее время NGF также находит специфическое терапевтическое применение при лечении заболеваний роговицы, таких как нейротрофический кератит. NGF, используемый в настоящее время в терапии, экстратируется из подчелюстных желез мыши, или его получают с помощью рекомбинантных технологий.
Использование NGF в терапии связано с некоторыми проблемами, поскольку его биоактивность, которая зависит от его вторичной и третичной структуры, может изменяться в процессе производства, очистки или хранения. Растворы NGF могут подвергаться агрегации белков, что может привести к изменчивости титра.
В дополнение к проблемам со стабильностью, как и многие другие белки, NGF неспецифически связывается с поверхностями и различными материалами, включая стекло и пластик, с которыми NGF может контактировать во время производства, хранения или введения. Это явление может привести к снижению концентрации активного вещества в растворе и, следовательно, к непостоянным или недостаточным количествам NGF, окончательно вводимым пациенту.
NGF в настоящее время продается либо в лиофилизированной форме для восстановления во время использования, либо в виде водного препарата, требующего хранения при низких температурах, обычно -20°C, чтобы свести к минимуму деградацию и адгезию водных препаратов NGF. Кроме того, чтобы уменьшить адгезию NGF к первичной упаковке, внутренняя контактная поверхность NGF, продаваемых в настоящее время в стеклянных флаконах, покрыта покрытием, уменьшающим адсорбцию белков.
В WO 95/05845 A1 описаны препараты NGF и иллюстрирует недостатки недостаточной стабильности и нежелательной адгезии к различным поверхностям этого белка. Для уменьшения или предотвращения адгезии NGF в этом документе предлагается использовать стабилизирующие добавки для водных препаратов NGF, такие как поверхностно-активные вещества, такие как полисорбаты, например, Tween® 80, полоксамеры, такие как Pluronic® F68, или белки, такие как альбумин. Примеры 5 и 6 описывают исследования стабильности водных препаратов NGF, упакованных в полипропиленовые флаконы с капельным наконечником. Полипропилен этих флаконов представляет собой обычный нехарактерный материал.
В JP 2012001588 A описан лист на основе пропилена, обладающий превосходной прозрачностью, ударопрочностью, формуемостью и устойчивостью к скручиванию, для упаковки твердых препаратов.
В WO 2016153663 A1 описаны распыляемые клеи-расплавы на основе олефинов.
В свете вышеизложенного по-прежнему существует необходимость поддерживать активность и титр водных препаратов NGF при обращении и хранении, не прибегая к комбинированному использованию добавок в растворе, к низким температурам на всем протяжении производства и хранения и к сложным и дорогим контейнерам для первичной упаковки.
Сущность настоящего изобретения
Заявитель провел исследования, направленные на эффективное предотвращение или сведение к минимуму адгезии NGF из водных препаратов к внутренней контактной поверхности контейнеров, в которых они хранятся, и неожиданно обнаружил, что определенные полипропилены (PP), характеризующиеся определенными термическими свойствами и кристалличностью, показывают адгезию NGF значительно ниже, чем у силиконизированного стекла или других полипропиленов.
Таким образом, с помощью этих конкретных РР можно хранить водные препараты NGF в менее жестких условиях, даже при комнатной температуре, преимущественно избегая дополнительных обработок покрытия контейнеров и стабилизирующих добавок в препарате, сохраняя при этом титр NGF постоянным.
Таким образом, целью настоящего изобретения является фармацевтическая упаковка, содержащая пластиковый контейнер в качестве первичной упаковки и упакованный в него водный препарат NGF, при этом пластиковый контейнер имеет внутреннюю поверхность, контактирующую с водным препаратом NGF, и внешнюю поверхность, причем, по меньшей мере, указанная внутренняя контактная поверхность по существу состоит, предпочтительно, указанная внутренняя контактная поверхность более чем на 80 мас.% состоит, по меньшей мере, из сополимера пропилена и этилена, имеющего энтальпию плавления ΔHm менее 95 Дж/г и более 35 Дж/г при измерении с помощью DSC в соответствии со способом, приведенным в описании.
Еще одной целью настоящего изобретения является способ выбора сополимера пропилена и этилена, подходящего для изготовления по меньшей мере внутренней контактной поверхности пластикового контейнера фармацевтической упаковки согласно изобретению, который включает:
- предоставление по меньшей мере образца сополимера пропилена и этилена,
- измерение энтальпии плавления ΔHm образца сополимера пропилена и этилена с помощью DSC в соответствии со способом, приведенным в описании,
- выбор подходящего сополимера пропилена и этилена, если его энтальпия плавления ΔHm меньше 95 Дж/г и больше 35 Дж/г.
Еще одной целью изобретения является использование определенного выше пластикового контейнера для упаковки водного препарата NGF.
Определения
Под термином «полипропилен» подразумеваются как гомополимеры, так и сополимеры пропилена.
Под аббревиатурой «PP» подразумевается полипропилен.
Под термином «материал на основе пропилена» подразумевается материал, содержащий более 50% мономерных звеньев пропилена.
Под термином «сополимер пропилена и этилена» подразумевается сополимер пропилена с этиленом, в котором мономер пропилена является основным мономером. Термин «сополимер пропилена и этилена» в данном документе также включает терполимеры пропилена и этилена, в которых пропиленовый мономер является основным мономером, и присутствует дополнительный олефиновый мономер.
Термин «основной мономер» означает мономер, присутствующий в полимере в количестве, превышающем 50 мол.%.
Под термином «мономерное звено» подразумевается повторяющаяся единичная часть полимера.
Аббревиатура «NGF» означает фактор роста нервов.
Под термином «по существу изготовленный из» подразумевается процентное содержание компонента выше 80 мас.%.
Под термином «жидкая лекарственная форма» подразумевается жидкий препарат, в котором лекарственный продукт производится и предоставляется для использования, такой как раствор, эмульсия, суспензия, лосьон и т.п.
Под термином «первичная упаковка» или «первичный контейнер» подразумевается упаковка, непосредственно контактирующая с жидкой лекарственной формой.
Под термином «однодозовая упаковка» подразумевается упаковка, содержащая одну дозу лекарственного средства.
Термин «многодозовая упаковка» означает упаковку, содержащую более одной дозы лекарственного средства.
Термин «контактная поверхность» означает поверхность пластикового контейнера, используемого в контакте с водным препаратом NGF.
Если не указано иное, в данном документе все проценты являются массовыми процентами.
Краткое описание чертежей
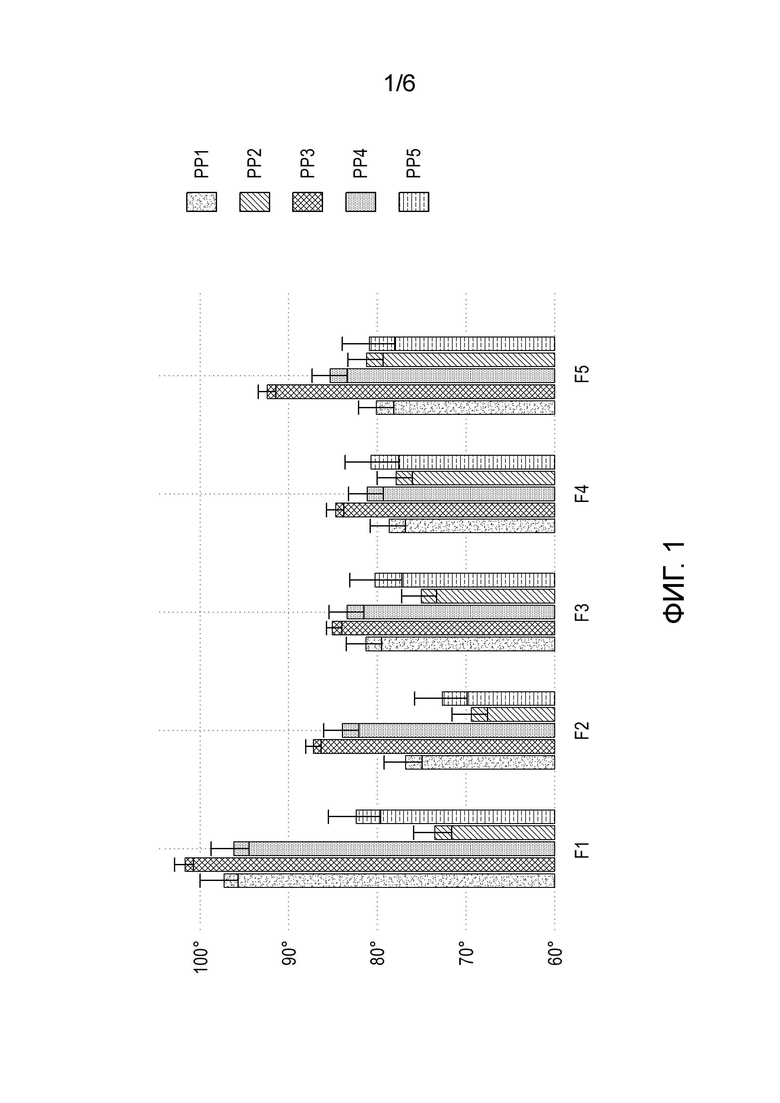
- На фиг. 1 показаны гистограммы углов контакта препаратов от F1 до F5 на испытанных PP материалах от PP1 до PP5;
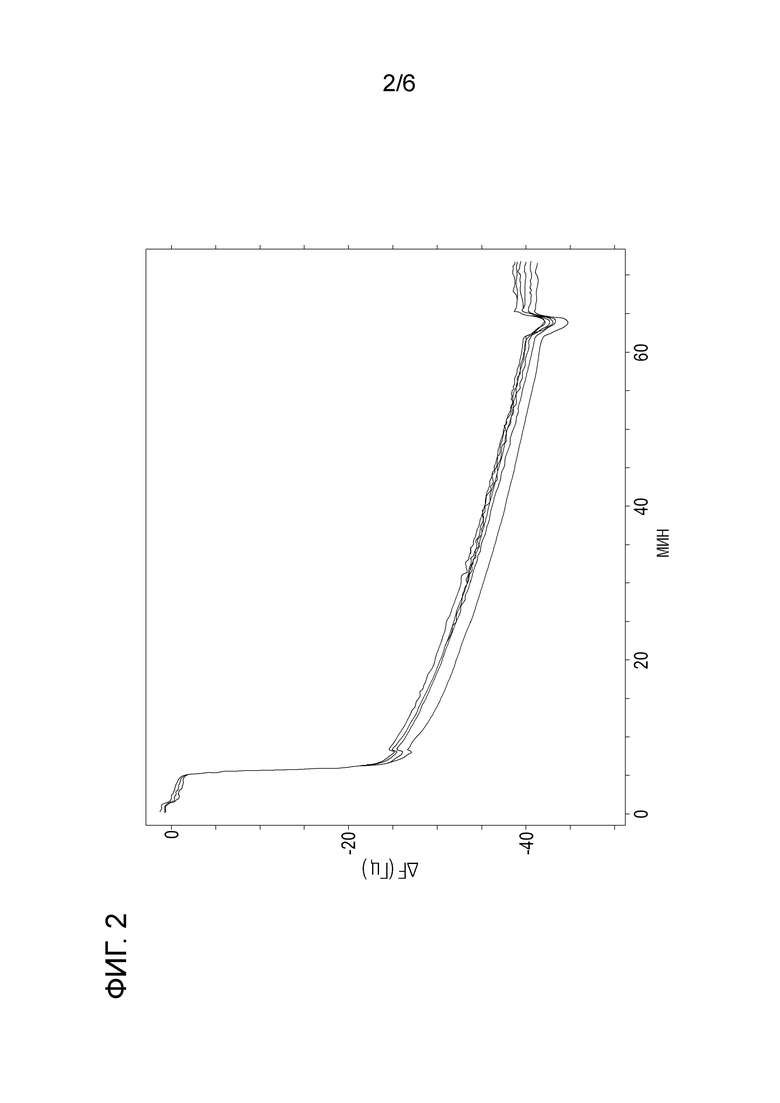
- на фиг. 2 показан график зависимости частоты колебаний электрода от времени при измерении на микровесах на кристалле кварца (ΔF - Гц от времени - мин, 6 повторов), в эксперименте по адсорбции rhNGF из препарата F1 на пленку из материала PP2;
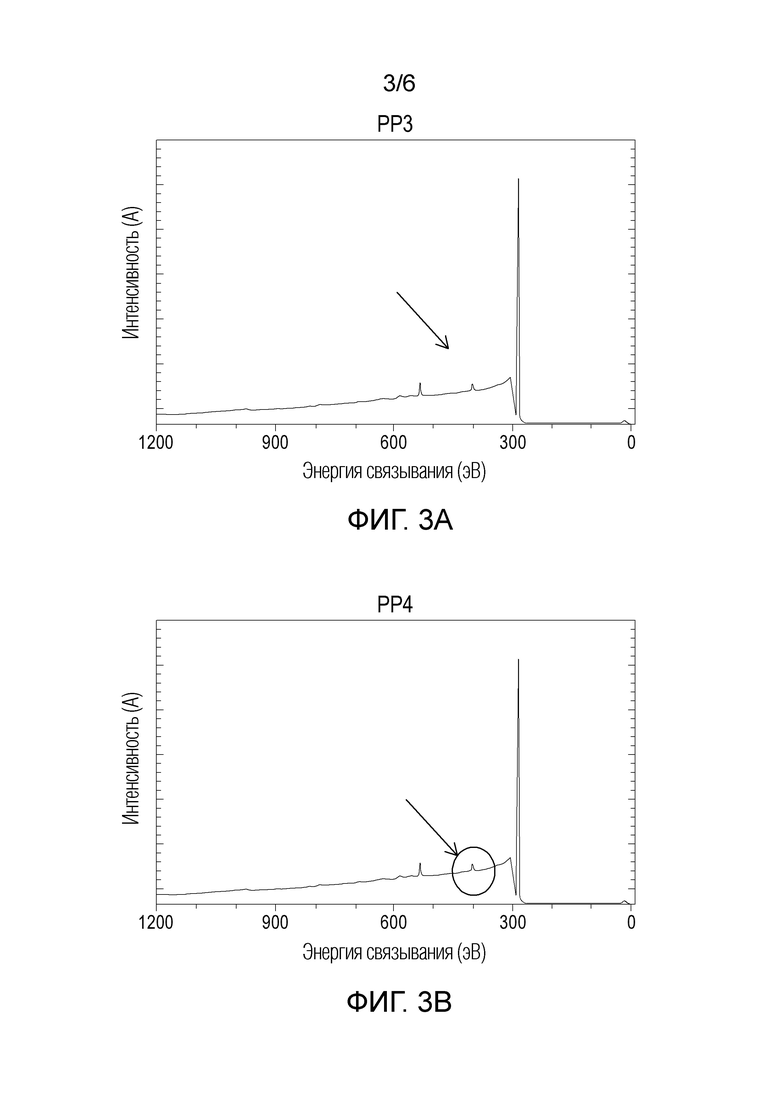
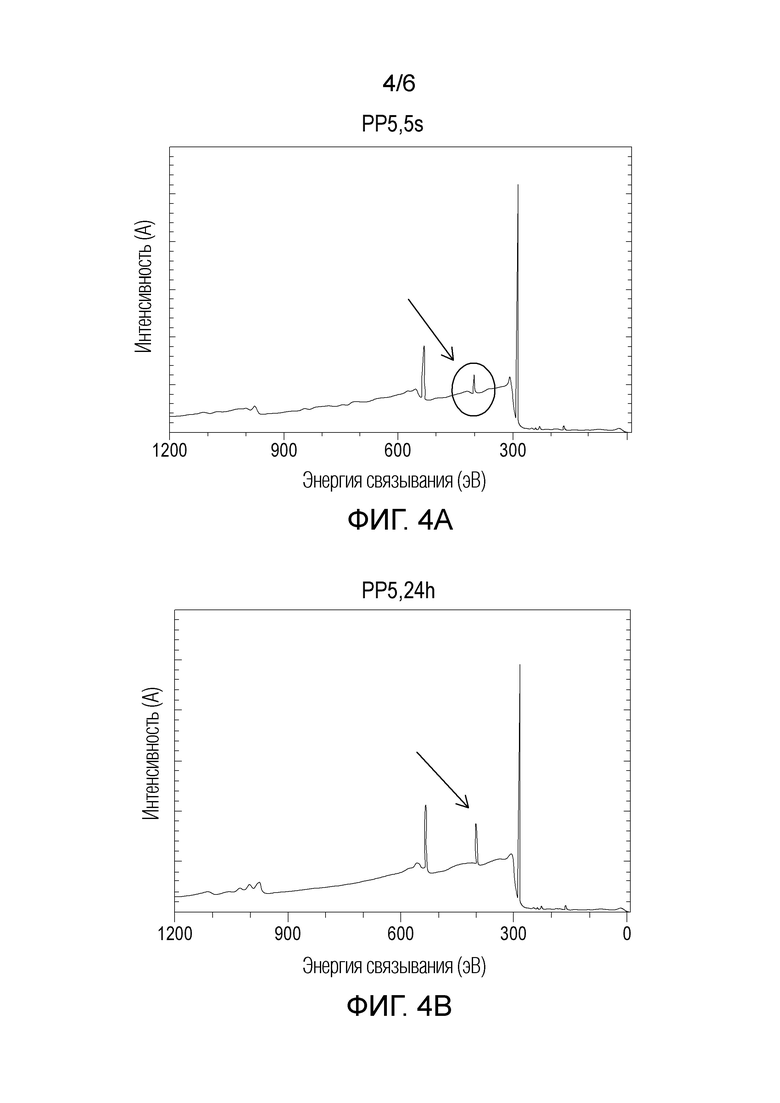
- на фиг. 3 и 4 представлены графики фотоэлектронной эмиссии NGF, адсорбированного на поверхности образцов PP3, PP4 и PP5 из препарата F6;
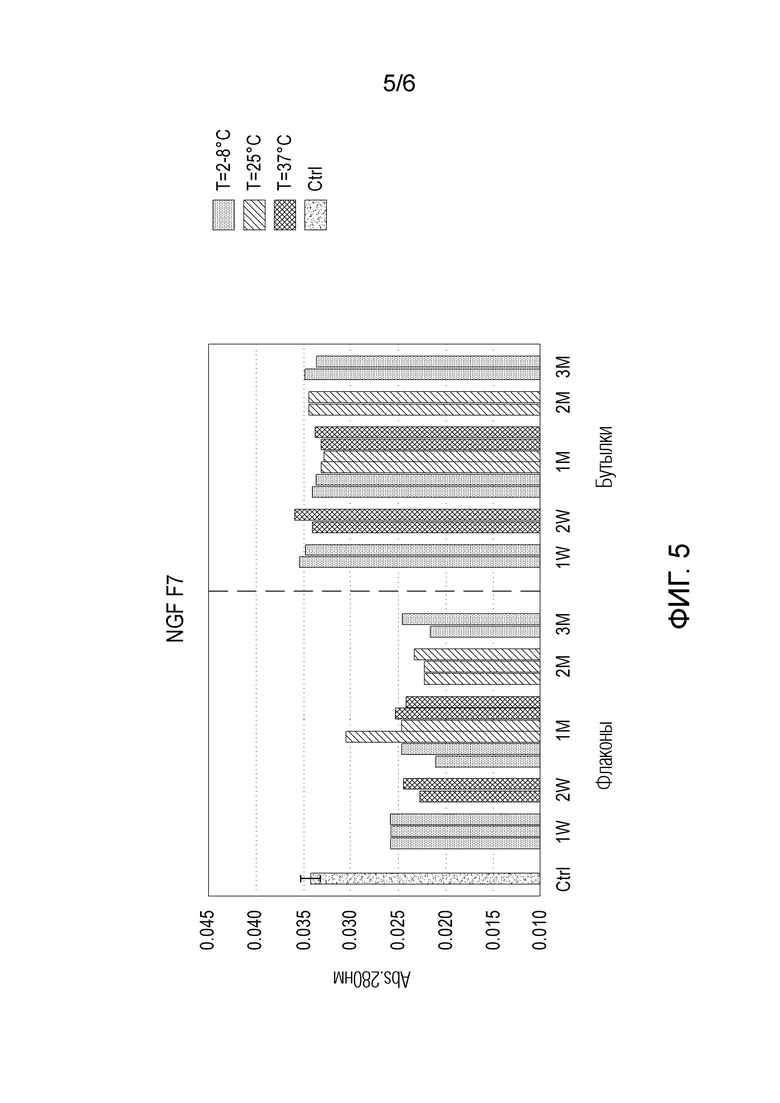
- на фиг. 5 показаны гистограммы поглощения (при 280 нм) препарата F7 по сравнению с контрольным препаратом (Ctrl), препарат F7 упакован в двойные силиконизированные стеклянные флаконы или в бутылки из РР3 и хранится при температуре 2-8°C, 25°C и 37°C; абсорбцию измеряли в моменты времени 1 неделя, 2 недели, 1 месяц, 2 месяца и 3 месяца (тест на стабильность 3 месяца);
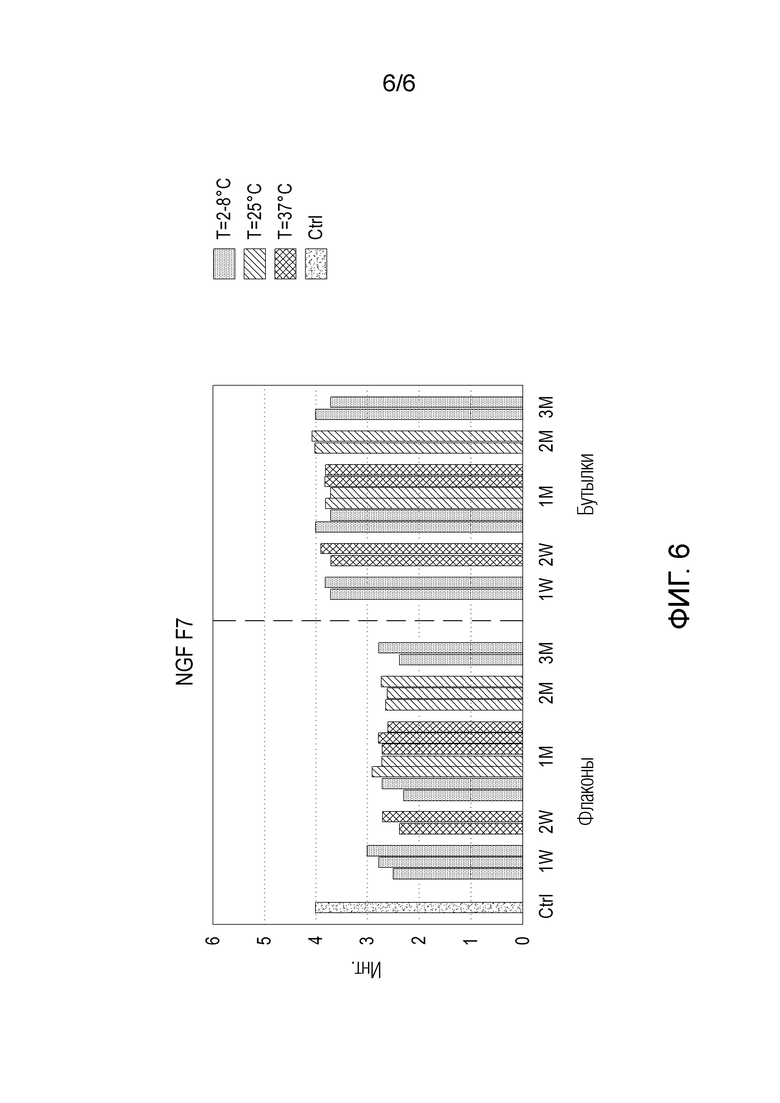
- на фиг. 6 показаны гистограммы флуоресценции триптофана (интенсивность при λ max - x 107 имп/с) препарата F7 по сравнению с контрольным препаратом (Ctrl), препарат F7 упакован в двойные силиконизированные стеклянные флаконы или бутылки из РР3 и хранится при температуре 2-8°C, 25°C и 37°C; флуоресценцию измеряли в моменты времени 1 неделя, 2 недели, 1 месяц, 2 месяца и 3 месяца (тест на стабильность 3 месяца).
Если не указано иное, все проценты выражены в процентах по массе.
Подробное раскрытие настоящего изобретения
Объектом настоящего изобретения является фармацевтическая упаковка, содержащая пластиковый контейнер и упакованный в него водный препарат NGF, при этом пластиковый контейнер имеет внутреннюю поверхность, контактирующую с водным препаратом NGF, и внешнюю поверхность, при этом, по меньшей мере, указанная внутренняя контактная поверхность по существу изготовлена, предпочтительно, указанная внутренняя контактная поверхность состоит более чем на 80 мас.%, по меньшей мере, из сополимера пропилена и этилена, имеющего энтальпию плавления ΔHm менее 95 Дж/г и более 35 Дж/г, измеренную с помощью DSC в соответствии с способом, приведенным в описании.
Пластиковый контейнер упаковки согласно изобретению представляет собой пластиковый контейнер, пригодный для первичной упаковки водного препарата NGF.
Пластиковый контейнер упаковки согласно изобретению может быть жестким или гибким контейнером.
Контейнер упаковки согласно изобретению может представлять собой ампулу, флакон, бутылку, банку, пакет или мешок.
Предпочтительно настоящий контейнер представляет собой бутылку или флакон.
Пластиковый контейнер упаковки согласно изобретению может иметь однослойную или многослойную структуру, предпочтительно имеет однослойную структуру.
В случае однослойной структуры пластиковый контейнер по существу изготовлен из сополимера пропилена и этилена, как определено в данном документе, предпочтительно он содержит по меньшей мере 90%, более предпочтительно по меньшей мере 95%, еще более предпочтительно по меньшей мере 99% по меньшей мере сополимера пропилена и этилена, как определено в данном документе.
В случае многослойной структуры, по меньшей мере, контактный поверхностный слой состоит из по меньшей мере сополимера пропилена и этилена, как определено в данном документе, предпочтительно, чтобы он составлял по меньшей мере 90%, более предпочтительно, по меньшей мере 95%, еще более предпочтительно, по меньшей мере 99%. по меньшей мере сополимера пропилена и этилена, как определено в данном документе.
В одном варианте осуществления весь контейнер по существу изготовлен из по меньшей мере сополимера пропилена и этилена, как определено в данном документе, предпочтительно он содержит по меньшей мере 90%, более предпочтительно по меньшей мере 95%, еще более предпочтительно по меньшей мере 99% по меньшей мере сополимера пропилена и этилена или их смеси, как определено в данном документе.
Дополнение до 100% контактного поверхностного слоя или всего контейнера может быть представлено другими предпочтительно смешиваемыми термопластичными полимерами, такими как, например, сополимер этилена и винилацетата и т.п.
Настоящий пластиковый контейнер характеризуется, по меньшей мере, сополимером пропилена и этилена, образующим, по меньшей мере, контактный поверхностный слой, причем указанный сополимер пропилена и этилена имеет энтальпию плавления ΔHm менее 95 Дж/г и более 35 Дж/г, измеренную с помощью DSC в соответствии со способом, приведенным в описании.
Предпочтительно сополимер пропилена и этилена имеет энтальпию плавления ΔHm менее 90 Дж/г, более предпочтительно менее 80 Дж/г.
Предпочтительно сополимер пропилена и этилена имеет энтальпию плавления ΔHm более 40 Дж/г.
Предпочтительно энтальпия плавления ΔHm сополимера пропилена и этилена составляет от 90 Дж/г до 35 Дж/г, более предпочтительно от 80 Дж/г до 40 Дж/г.
100% кристаллический гомополимер пропилена, который не подходит для изготовления контейнера настоящей упаковки, имеет энтальпию плавления ΔHm примерно 207 Дж/г (Thermal Application Note - Polymer Heats of Fusion - Roger L. Blaine, TA Inctruments,109 Lukens Drive, New Castle DE 19720, USA).
Предпочтительно сополимер пропилена и этилена имеет температуру плавления Tm ниже 160°C, более предпочтительно ниже 155°C, измеренную в соответствии со способом DSC, приведенным в описании.
Предпочтительно сополимер пропилена и этилена имеет температуру плавления Tm выше 130°C, более предпочтительно выше 140°C, измеренную в соответствии со способом DSC, приведенным в описании.
Предпочтительно сополимер пропилена и этилена имеет температуру плавления Tm от 160°C до 130°C, более предпочтительно от 155°C до 140°C, измеренную в соответствии со способом DSC, приведенным в описании.
Предпочтительно сополимер пропилена и этилена имеет индекс текучести расплава менее 10 г/10 мин, более предпочтительно менее 9 г/10 мин, измеренный в соответствии с ISO 1133 при 230°C и 2,16 кг.
Предпочтительно сополимер пропилена и этилена имеет индекс текучести расплава от 1 до 20 г/10 мин, измеренный в соответствии с ISO 1133 при 230°C и 2,16 кг.
Предпочтительно сополимер пропилена и этилена представляет собой статистический сополимер пропилена и этилена.
Предпочтительно сополимер пропилена и этилена является полукристаллическим.
Предпочтительно содержание мономера этилена в сополимере пропилена и этилена составляет менее 40%, более предпочтительно менее 30% и по меньшей мере 5%.
В одном варианте осуществления сополимер пропилена и этилена представляет собой терполимер пропилена, этилена и альфа-олефина, предпочтительно бутена.
Предпочтительно поверхность контакта сополимера пропилена и этилена, которая в конечном контейнере находится в контакте с водным препаратом NGF, характеризуется шероховатостью поверхности Sa до инкубации NGF менее 25 нм, более предпочтительно менее 20 нм, еще более предпочтительно менее 15 нм при измерении согласно ISO 4287 (1997).
Предпочтительно поверхность сополимера пропилена и этилена, которая в конечном контейнере находится в контакте с водным препаратом NGF, характеризуется углом контакта более 90°, предпочтительно более 95° при измерении относительно раствора F1, как описано в экспериментальной части.
Предпочтительно сополимер пропилена и этилена одобрен по меньшей мере в фармакопее.
Примерами сополимеров пропилена и этилена, подходящих для изготовления контейнера упаковки согласно изобретению, являются сополимеры серии BormedTM компании Borealis, в частности сополимеры пропилена и этилена BormedTM RD808CF, BormedTM SB815MO и BormedTM SC876CF.
Настоящий пластиковый контейнер может содержать один сополимер пропилена и этилена или смесь двух или более сополимеров пропилена и этилена.
В случае примеси сополимеров пропилена и этилена они смешиваются с образованием однофазной гомогенной смеси с одним пиком плавления и одной энтальпией плавления ΔHm в соответствии с предпочтениями, выраженными выше.
В настоящем пластиковом контейнере, помимо пластиковых полимеров, могут присутствовать незначительные количества добавок, обычно используемых в этой области.
В зависимости от контейнера могут использоваться различные известные технологии изготовления, в которых настоящие сополимеры пропилена и этилена являются материалом для всей стенки контейнера или, по меньшей мере, для контактного поверхностного слоя.
Например, жесткие более толстые контейнеры (например бутылки или флаконы) могут быть изготовлены путем литья под давлением из выбранных полимеров, в то время как гибкие тонкие контейнеры (например пакеты или мешки) путем вырезания подходящим образом и самозапечатывания моно- или многослойных пленок, как это известно в области упаковки.
Преимущественно, фармацевтическая упаковка согласно изобретению обеспечивает хранение водных препаратов NGF в более легких условиях хранения, в то же время сводя к минимуму адгезию NGF на контактной поверхности контейнера и сохраняя титр NGF.
В частности, фармацевтическая упаковка согласно изобретению позволяет сохранять водные препараты NGF при температурах выше 4°C, даже при комнатной температуре, без использования стабилизирующих добавок к препарату, например, предотвращающих адгезию или агрегацию NGF.
Предпочтительно контейнер представляет собой флакон или бутылку, которая, по меньшей мере, на внутренней контактной поверхности содержит, предпочтительно состоит из сополимера пропилена и этилена, как определено выше.
Настоящая фармацевтическая упаковка содержит водные препараты NGF, такие как водный раствор, эмульсия, суспензия, лосьон и т.п., предпочтительно водный раствор NGF, более предпочтительно водный раствор NGF для офтальмологического применения.
Водный препарат NGF содержит NGF в терапевтически эффективных количествах. Предпочтительно, в водном препарате, NGF присутствует в количестве от примерно 0,0001% до примерно 0,5% м/о, более предпочтительно от примерно 0,001% до примерно 0,1% м/о, наиболее предпочтительно примерно 0,002% м/о водного препарата.
Водный препарат NGF может содержать достаточное количество биологически приемлемых солей для обеспечения надлежащей тоничности жидкости и поддержания NGF в растворе.
Предпочтительно, водный препарат NGF содержит достаточное количество соли, чтобы быть изотоническим в физиологически приемлемых пределах с глазными жидкостями, человеческой кровью или спинномозговой жидкостью, в зависимости от терапевтического применения.
Предпочтительной солью является хлорид натрия (NaCl), но можно использовать и другие биологически приемлемые соли, такие как, например, хлорид калия (KCl), хлорид кальция (CaCl2) и хлорид магния (MgCl2) и их смеси.
Водный препарат NGF дополнительно содержит биологически приемлемый буфер для обеспечения и поддержания правильного pH во время хранения.
Водный препарат NGF забуферен биологически приемлемым буфером до pH от примерно 6,8 до примерно 7,5, более предпочтительно до pH примерно 7,2.
Предпочтительным буфером является фосфатный буфер, но также включены другие буферы, способные поддерживать рН в нужном диапазоне, особенно буферы, подходящие для офтальмологического применения. Предпочтительное количество буфера будет варьироваться в зависимости от типа используемого буфера и его буферной емкости.
Водный препарат NGF может необязательно содержать добавки, которые дополнительно снижают или предотвращают адсорбцию NGF на различных поверхностях, предпочтительно поверхностно-активные вещества, такие как, например, полисорбаты, такие как Tweeny 80, полоксамеры, такие как Pluronics F68, или белки, такие как сывороточный альбумин.
В одном варианте осуществления водный препарат NGF не содержит каких-либо добавок, снижающих адсорбцию, предпочтительно не содержит поверхностно-активных веществ.
В водном препарате NGF могут присутствовать эксципиенты, обычно используемые в фармацевтических водных препаратах и известные техническим специалистам, такие как сахара, сахарные спирты, аминокислоты, производные целлюлозы, полиэтиленгликоли.
Водный препарат NGF содержит воду в количестве, достаточном для достижения соответствующей концентрации компонентов препарата.
В данном документе NGF включает любую форму фактора роста нервов из любого источника, при условии, что он проявляет биологическую активность и связывается с рецепторами NGF.
NGF также включает модифицированные формы NGF, которые сохраняют биологическую активность NGF и связывание с рецептором, включая слитые белки, фрагменты NGF и мутанты, в которых определенные аминокислоты были удалены или заменены, при сохранении достаточной биологической активности NGF и связывания с рецептором для обеспечения терапевтической активности.
В одном варианте осуществления NGF имеет мышиное происхождение.
Предпочтительно NGF представляет собой NGF человека (hNGF), более предпочтительно он представляет собой рекомбинантный hNGF (rhNGF).
Способы получения rhNGF, пригодных для использования в настоящем водном препарате, известны специалистам в данной области, например, способы их получения описаны в WO 9505845 A1, WO 0022119 A1 и WO 2013092776 A1.
NGF водного препарата согласно настоящему изобретению предпочтительно имеет чистоту выше 70%, более предпочтительно выше 80%, еще более предпочтительно выше 90% и наиболее предпочтительно выше 95%. Чистота выделенного NGF для использования в представленных водных препаратах может быть определена обычными способами, известными специалистам в данной области.
Представленные водные препараты NGF предпочтительно готовят заранее, а затем упаковывают и хранят в контейнере согласно изобретению.
Однако в одном варианте осуществления препарат NGF упаковывают в контейнер в виде порошка, например, в лиофилизированной форме, затем после восстановления водным восстанавливающим носителем хранят в виде водного препарата NGF до введения пациентам, нуждающимся в терапии.
Контейнер упаковки согласно изобретению после обычного заполнения препаратом NGF необходимо закрыть.
Крышки, используемые для закрывания контейнеров с лекарственными средствами после процесса заполнения, должны быть максимально инертными. Они не должны вызывать нежелательных взаимодействий между содержимым и внешней средой и должны обеспечивать полную герметизацию. Помимо своей защитной функции крышки также должны позволять легко и безопасно вводить лекарство.
Примерами крышек, подходящих для данного контейнера, являются простые эластомерные колпачки, или они являются частью более сложных систем доставки, таких как, например, система Novelia® от Nemera или офтальмологический выжимной диспенсер (OSD) от APTAR.
Преимущественно настоящая упаковка, если она обладает достаточными газонепроницаемыми свойствами, может содержать модифицированную атмосферу, такую как бескислородная атмосфера, с целью улучшения стабильности при хранении.
В таком случае упаковка должна быть газонепроницаемой, возможно, с использованием подходящих газонепроницаемых материалов, известных в области упаковки.
Предпочтительно, водный препарат NGF представляет собой водный раствор NGF для офтальмологического применения в форме глазных капель, вводимых глазным путем.
Особенно предпочтительный водный препарат NGF в дополнение к NGF, предпочтительно rhNGF, содержит трегалозу, маннит, метоцел, ПЭГ 6000, L-метионин, фосфатный буфер, воду и имеет рН примерно 7,2.
Настоящая фармацевтическая упаковка может быть однодозовой или многодозовой.
В одном варианте осуществления фармацевтическая упаковка согласно изобретению представляет собой упаковку с одной дозой, а именно предварительно загруженный стерильный пластиковый аппликатор, содержащий контейнер, как определено ранее, и водный раствор NGF, предпочтительно без стабилизирующих добавок, упакованный в него, для однократного введения.
В одном варианте осуществления фармацевтическая упаковка согласно изобретению представляет собой многодозовую упаковку, содержащую многодозовый стерильный контейнер, как определено ранее, и водный раствор NGF, предпочтительно не содержащий стабилизаторы, для многократного введения, предпочтительно с использованием систем доставки.
Водные препараты NGF применимы для лечения пациентов с состояниями, чувствительными к терапии NGF.
Обычно такие препараты стерильны и подходят для офтальмологического, внутривенного, внутримышечного, парентерального или интрацеребровентрикулярного введения, предпочтительно для офтальмологического введения.
Такая терапия может быть полезна для лечения заболеваний роговицы, таких как нейротрофический кератит или дисфункция нейронов, включая повреждение нейронов или дегенерацию нейронов, чувствительных к NGF, например, при болезни Альцгеймера.
Водный препарат NGF для лечения нейротрофического кератита обычно вводят глазным путем.
Водный препарат NGF для лечения деменции можно вводить любым из множества способов в зависимости от конкретного конечного применения.
Чтобы преодолеть возможные трудности при преодолении гематоэнцефалического барьера, NGF можно вводить в ЦНС путем прямых внутрижелудочковых инъекций или с помощью имплантатов или насосов, пропитанных лекарственным средством. Другой путь введения - непрерывная инфузия через интрацеребровентрикулярную канюлю.
Преимущественно, по меньшей мере, поверхность пластиковых контейнеров (т.е. шприцев, трубок, внутренних камер и т.д.), которая вступает в контакт с водным препаратом NGF во время этих введений, по существу изготовлена из сополимера пропилена и этилена, как определено ранее.
Точная доза и схема введения будут зависеть от многих факторов, таких как путь введения и степень заболевания индивидуума, получающего лечение.
Настоящее изобретение лучше проиллюстрировано в следующем экспериментальном разделе.
Экспериментальная часть
В этом экспериментальном разделе взаимодействие между белком (rhNGF) и пластиковым материалом (полипропилен PP) оценивали как в качественном, так и в количественном отношении.
Для прямого и косвенного определения адсорбции rhNGF на полипропиленовом упаковочном материале использовали различные аналитические методики.
Неожиданно было обнаружено, что различные степени кристалличности полипропиленового материала приводят к различным уровням адсорбции NGF и что испытанные аналитические методики дали согласованные и надежные взаимосвязанные результаты.
В этих испытаниях авторы использовали полипропиленовые материалы фармацевтического качества, перечисленные в таблице 1, уже одобренные для изготовления первичных контейнеров для лекарственных средств:
Таблица 1: PP
Испытания на литье под давлением показали, что все полипропиленовые материалы легко поддаются механической обработке и соответствуют требованиям, предъявляемым к процессам экструзии и литья с точки зрения формуемости и механики.
Образцы для проведения испытаний были изготовлены для каждого материала методом литья под давлением. Образцы представляли собой лепешки длиной 15 см, шириной 2 см, высотой 1 см.
Пример 1
Измерение энтальпии плавления (ΔHm) и температуры плавления (Tm) PP методом дифференциального сканирующего калориметрического (DSC) анализа
С целью оценки термических свойств различных PP был проведен дифференциальный сканирующий калориметрический анализ на приборе DSC TA 2010, работающем по принципу двойного термосканирования (первый нагрев от 0°C до 200°C со скоростью 20°C/ мин, промежуточное охлаждение от 200°C до 0°C со скоростью 20°C/мин и второй нагрев от 0°C до 200°C со скоростью 20°C/мин). Испытывали по два образца для каждого материала.
Средние результаты анализа DSC представлены в следующей таблице 2:
Таблица 2: Тепловые свойства PP
начало (°C)
пик (°C)
начало (°C)
пик (°C)
Соответствующие энтальпия плавления ΔHm (Дж/г) и температура плавления (Tm пик °C) были измерены при втором нагревании.
Поскольку степень кристалличности пластмасс пропорциональна соответствующей энтальпии плавления ΔHm (Дж/г), испытанные PP можно расположить по степени кристалличности, как показано ниже (слева направо, от наиболее к наименее кристаллическому):
PP2 > PP5 > PP1 > PP3 > PP4
Пример 2
Измерение угла контакта
Для этого теста использовали пять препаратов rhNGF на водной основе (F1-F5). Препараты F1 - F5 показаны в Таблице 3 ниже:
Таблица 3: Препараты
qs сколько нужно; поверхностно-активным веществом был полоксамер, пригодный для офтальмологического применения.
Препараты F1-F5 готовили, как описано ниже:
В химический стакан на 150 мл вносили 70 мл воды для инъекций (WFI), затем добавляли все ингредиенты, кроме rhNGF, и выдерживали при магнитном перемешивании до полного растворения. Добавляли точное количество rhNGF, и раствор доводили до объема (100 мл) с помощью WFI при перемешивании. Измеряли рН раствора и, в случае необходимости, корректировали гидроксидом натрия или соляной кислотой.
Ожидалось, что препарат F1 покажет наибольшее отложение rhNGF, поскольку он не содержал поверхностно-активных веществ или других стабилизирующих добавок.
Измерения угла контакта были выполнены с помощью прибора Dataphysics - Contact Angle System OCA 200 с программным обеспечением электронного управления с автоматическим выравниванием. Для каждого материала было выполнено десять измерений угла контакта, а затем рассчитаны среднее значение и стандартное отклонение. Чтобы свести к минимуму ошибку, вызванную разной шероховатостью поверхности образца, полученной в процессе литья под давлением, было проведено пять измерений на передней поверхности и пять измерений на задней поверхности каждого образца.
Для каждого препарата F1-F5 на каждый образец PP наносили в общей сложности 10 капель по 3 мкл (по 5 капель на каждую поверхность образца). Осажденные капли не были стабильными во времени, так как имели тенденцию растекаться по поверхности подложки. Следовательно, изображение капли для получения углов контакта было получено в течение 10 секунд после осаждения капли.
Средние углы контакта и значения стандартного отклонения были зарегистрированы для каждого препарата F1-F5 для материалов PP1-PP5 и представлены в Таблице 4 ниже:
Таблица 4: Углы контакта (°)
По значениям углов контакта испытанные полипропиленовые материалы характеризовались следующим порядком смачиваемости (слева направо, от наиболее смачиваемых к наименее смачиваемым):
PP2 > PP5 > PP1 > PP4 > PP3
Тенденция среднего угла контакта в зависимости от препарата F1-F5 и материала образца представлена на фиг. 1.
Что касается таблицы 4 и фиг. 1, авторы наблюдали подобное поведение для некоторых полипропиленовых материалов. В частности, PP3 и PP4 имели наименьшую смачиваемость (наибольший угол контакта), особенно с препаратом F1 (rhNGF в буферном составе с pH 7,2 - определяющий наибольшие различия состав, не содержащий поверхностно-активных веществ и других добавок). Согласно анализу DSC, PP3 и PP4 имели самую низкую кристалличность (т.е. самое низкое Δ Hm, см. Таблицу 2).
С другой стороны, материалы PP5 и PP2 имели более высокую смачиваемость, а именно более гидрофильную поверхность, и более высокую кристалличность, чем первые.
В заключение, этот тест показал, что существует корреляция между, с одной стороны, кристалличностью и ΔHm PP, а с другой стороны, их смачиваемостью и углом контакта. Больший угол контакта указывал на более низкую смачиваемость поверхности пластика, что, в свою очередь, спрогнозировало меньшую адсорбцию NGF, что подтверждается следующими тестами адсорбции.
Пример 3
Измерение адсорбции rhNGF на образцах PP
В методике, принятой для этого теста, использовали микровесах на кристалле кварца (QCM) и обеспечивали прямой и количественный анализ степени адсорбции rhNGF на материале.
Испытываемый полипропиленовый материал (от PP1 до PP5) сначала растворяли в декалине (2% м/о) при встряхивании при температуре 150°C в течение 1 часа, а затем наносили методом электропрядения в виде тонкой пленки на кварцевый кристаллический электрод (нанесение покрытия методом центрифугирования при 3500 об/мин). Оборудование для переноса растворенного полимера в центрифугу предварительно нагревали до 120-150°C. Толщина PP пленок указана в следующей таблице 5:
Таблица 5: Толщина PP пленок
Электроды с покрытием инкубировали в течение ночи в PBS перед экспериментами по адсорбции белка. Для инкубации использовали следующий препарат F6, приготовленный как препараты F1-F5:
Таблица 6: Препарат rhNGF
Препарат нагнетали высокоточным многоканальным перистальтическим насосом через тефлоновую трубку с внутренним диаметром 0,75 мм и наносили на электрод с покрытием при скорости потока 50 мкл/с.
Прикладывали разность потенциалов ΔV к двум сторонам электрода, который начинал вибрировать с определенной частотой.
Частота колебаний электрода уменьшалась по мере увеличения осажденной на нем пленки rhNGF до плато адсорбции примерно через 60 минут, как показано на графике фиг. 2, относящемся к материалу PP2.
В приведенных ниже таблицах 7 и 8 показана адсорбция rhNGF до и после промывания электрода фосфатно-солевым буфером (PBS), измеренная как масса (нг/см2) после достижения плато адсорбции примерно через 60 мин.
Таблица 7: Адсорбированный rhNGF перед промывкой PBS
Электрод промывали PBS для проверки стабильности адсорбции rhNGF на поверхности различных PP.
Таблица 8: Адсорбированный rhNGF после промывания PBS
Из приведенного выше анализа авторы заметили, что наиболее кристаллические и гидрофильные полипропиленовые материалы (PP5 и PP2) имели более высокую массу rhNGF, адсорбированного на поверхности, по сравнению с наиболее гидрофобными полипропиленовыми материалами с более низкой кристалличностью (PP3, PP4 и PP1).
Результаты после промывки показывают, что адсорбированный rhNGF достаточно стабилен на пластиковой поверхности и что на всех поверхностях процент десорбированного rhNGF после промывки был довольно низким.
В заключение, результаты теста на адсорбцию хорошо коррелируют с данными об угле контакта и кристалличности, показывая более низкую адсорбцию NGF на менее кристаллических, более гидрофобных материалах.
Пример 4
Измерение шероховатости поверхности методом атомно-силовой микроскопии (AFM)
Атомно-силовая микроскопия - это метод, который позволяет измерять посредством отклонения небольшого рычага, называемого «кантилевер», минимальные силы, действующие на поверхность, и обеспечивать трехмерное изображение той же поверхности с разрешением от 1 до 10 нм.
Детектор AFM измеряет отклонение кантилевера и преобразует его в электрический сигнал. Интенсивность этого сигнала пропорциональна смещению кантилевера.
Часть 1
Каплю препарата F6, содержащего белок (rhNGF), наносили на поверхность образцов PP1-PP5 в виде лепешек (по одному образцу на каждый PP) и инкубировали в течение 1 недели при 4°C.
После инкубации образцы промывали и погружали в первый химический стакан, содержащий 200 мл воды Milli-Q, на 5 минут, а затем переносили во второй стакан, также содержащий 200 мл воды Milli-Q, еще на 5 минут. Затем поверхность обезвоживали в слабом потоке азота. Эта процедура была необходима для удаления NGF, не адсорбированного, но присутствующего в растворе, захваченного на поверхности полипропилена, и солей, которые могли бы вызывать артефакты после высыхания на образце.
Шероховатость поверхности измеряли до и после инкубации с композицией rhNGF в соответствии с ISO 4287 (1997). Образцы анализировали путем получения изображений сканирования поверхности с помощью атомно-силового микроскопа (Bruker), работающего в динамическом режиме. Использовали рычаги TESPA (Bruker, USA) с упругой константой 40 Н/м и резонансной частотой 300 кГц. Радиус кривизны кончика составлял примерно 10 нм.
Изображения были получены в различных масштабах, от 50 до 2 мкм.
Результаты, выраженные как Sa, среднее арифметическое абсолютного значения ординат в пределах области определения (A), показаны в следующей Таблице 9:
Таблица 9: Шероховатость по AFM
Sa - это продолжение Ra (средняя арифметическая высота линии) на поверхность. Он выражает в виде абсолютной величины разницу высоты каждой точки по сравнению со средним арифметическим значением поверхности.
По значениям Sa в таблице 9 авторы заметили, что только для двух материалов - PP5 и PP2 - шероховатость значительно увеличилась после инкубации с NGF (см. дельта Sa - разница до и после 1 недели инкубации NGF).
Эти данные о шероховатости хорошо коррелируют с данными по адсорбции, измеренными на микровесах на кристалле кварца из таблиц 7 и 8, и с углами контакта из таблицы 4, поскольку PP2 и PP5 являются наиболее гидрофильными материалами, имеющими самую шероховатую поверхность и вызывающими самую высокую адсорбцию NGF.
Другие материалы PP1, PP3 и PP4, по-видимому, плохо адсорбировали NGF, и нельзя было оценить увеличение шероховатости поверхности после инкубации. На самом деле материал PP3, по-видимому, даже уменьшал шероховатость своей поверхности после инкубации с NGF.
Часть 2
Во второй части эксперимента авторы отбросили менее интересные гидрофильные материалы (PP5 и PP2) и повторно рассмотрели только наиболее перспективные гидрофобные материалы (PP3, PP1 и PP4).
Авторы также внесли изменения в методологию подготовки образцов. Препарат rhNGF F6 на этот раз инкубировали в течение 48 часов вместо 1 недели. Данные о шероховатости показаны в Таблице 10 ниже:
Таблица 10: Шероховатость по AFM
Данные подтвердили, что среди наиболее перспективных, гидрофобных, низкокристаллических полипропиленов PP1, PP3 и PP4, PP3 и PP4 показали постоянную или даже более низкую шероховатость после инкубации с NGF.
Пример 5
Измерение азота на поверхности образцов PP методом рентгеновской фотоэлектронной спектроскопии (XPS)
Рентгеновская фотоэлектронная спектроскопия - это метод спектроскопии, используемый для исследования поверхностей материалов. Он позволяет оценить химические элементы, составляющие поверхность материала, а иногда и определить их связующее состояние.
Электроны, испускаемые материалом, подвергшимся воздействию монохроматического рентгеновского луча, выбрасываются с кинетической энергией, пропорциональной энергии связи, что указывает на химический элемент.
В этом случае авторы проанализировали лучшие гидрофобные материалы PP3 и PP4, ранее изученные с точки зрения угла контакта, AFM и QCM, сравнив их с PP5, худшим материалом с точки зрения адсорбции NGF.
Часть 1
Каплю (примерно 45 мкл) препарата F6 наносили на поверхность полипропиленового материала и оставляли на 5 секунд, затем поверхность промывали водой, сушили в токе азота и анализировали, как описано ниже.
Все спектры XPS были измерены на спектрометре S-Probe компании Surface Science Instruments. Этот прибор имеет монохроматическое рентгеновское излучение A1 Ka и низкоэнергетическую электронную пушку для нейтрализации заряда непроводящих образцов. Образцы были закреплены на двустороннем скотче и использованы в качестве изоляторов. Зона рентгенологического анализа для этих снимков составляла примерно 800 мкм в диаметре. Давление в аналитической камере во время регистрации спектра было менее 5×10-9 торр. Энергия пропуска была установлена равной 150 эВ. Угол выхода составлял 0° (угол выхода 0°=глубина отбора проб 100 А).
Графики на фиг. 3 и 4 показывают фотоэлектронную эмиссию и, в частности, они выделяют пиковую эмиссию азота, указывающую на присутствие rh NGF на поверхности.
Следует отметить, что для более гидрофобных пластиков с низкой кристалличностью (PP3 и PP4, фиг. 3A и 3B) пиковая эмиссия атома азота имела значительно меньшую интенсивность (интенсивность 0,4-0,5 А) по сравнению с пиком, связанным с более гидрофильным материалом с высокой степенью кристалличности (PP5) (интенсивность 2 А) на фиг. 4А.
Эти результаты, которые демонстрируют более низкое отложение NGF для образцов PP3 и PP4, очень хорошо коррелируют с результатами других предыдущих методов, описанных выше.
Часть 2
Авторы хотели подчеркнуть высокие адсорбционные свойства материала PP5, инкубируя NGF в течение более длительного периода времени (24 часа) и оценивая интенсивность эмиссии электронов, связанную с пиком азота.
Как видно из графиков на фиг. 4, rhNGF продолжал адсорбироваться на поверхности пластика в течение 24 часов, обеспечивая пик с интенсивностью излучения примерно 4 А (фиг. 4В), что в два раза выше, чем начальные 2 А, измеренные через 5 секунд инкубации (фиг. 4А).
В конце этой первой экспериментальной фазы авторы пришли к выводу, что:
1) Полипропилены с более высокой степенью кристалличности, такие как гомополимеры пропилена (PP2 и PP5), были связаны с повышенной адсорбцией NGF на поверхности.
2) Полипропилены с более низкой степенью кристалличности, такие как сополимеры пропилена и этилена РР1, РР3 и РР4, приводили к более низкой поверхностной адсорбции NGF.
3) Адсорбция была довольно стабильной и необратимой: после того, как NGF адсорбировался на поверхности пластика, десорбция происходила с большим трудом.
Сводка основных результатов, полученных в вышеуказанных тестах, представлена в Таблице 11 ниже.
Таблица 11: Сводная таблица
(Дж/г)§
против F1
Адсорбированная масса (нг/см2)
Шероховатость* Sa (нм)
эмисся азота*
Примечания: § измерено с помощью DSC при втором нагревании, * разница до и после 1 недели инкубации NGF, +++ минимальное взаимодействие rhNGF-PP, --- максимальное взаимодействие rhNGF-PP.
Из данных, представленных в Таблице 11, авторы пришли к выводу, что наиболее подходящими полипропиленовыми материалами для производства контейнеров для водных растворов NGF являются PP1, PP3 и PP4, а именно те, которые характеризуются одним или несколькими из следующих свойств:
- ΔHm менее 95 Дж/г, предпочтительно менее 90 Дж/г, более предпочтительно менее 80 Дж/г и ΔHm более 35 Дж/г, предпочтительно более 40 Дж/г,
- угол контакта с водой препарата F1 более 90°(±2), предпочтительно более 95°(±2),
- дельта Sa шероховатости по AFM (нм), до инкубации NGF, менее 10 нм, предпочтительно менее 5 нм,
- интенсивность фотоэлектронной эмиссии азота от 0,2 до 0,5 А, предпочтительно от 0,2 до 0,4 А,
свойства, измеренные в соответствии с ранее описанными методами.
Пример 6
Измерение адсорбции rhNGF из водных препаратов, расфасованных в бутылки из полипропилена, по сравнению с флаконами из силиконизированного стекла (исследования стабильности в течение 3 месяцев)
Авторы провели 3-месячный сравнительный тест на стабильность препарата rhNGF F7, упакованного в двойные флаконы из силиконизированного стекла 2R (2 мл, закрытые эластомерной крышкой, производства Soffieria Bertolini SpA) (V) или в полипропиленовые бутылки (10 мл, закрытые системой Novelia® производства Nemera) (B).
Состав препарата F7, приготовленного как препараты F1-F5, представлен в Таблице 12 ниже:
Таблица 12: Препарат F7
Полипропиленовые бутылки (В) были изготовлены из PP3, одного из лучших PP по результатам предыдущих испытаний.
В этом тесте на стабильность закрытые стеклянные флаконы (V) и полипропиленовые флаконы (B), содержащие препарат F7, хранили при температуре 2-8°C, 25°C или 37°C и анализировали на адсорбцию NGF в определенные моменты времени через 1 неделю (1Н), через 2 недели (2Н), 1 месяц (1М), 2 месяца (2М) и 3 месяца (3М) по сравнению с контрольным препаратом (Ctrl), а именно препаратом F7, но свежеприготовленным и проанализированным немедленно.
В каждый момент времени анализировали содержание NGF по меньшей мере в двух флаконах и двух бутылях для некоторых или всех температур. PP бутыли Novelia® прессовали вручную и собирали капли для анализа. Образцы препаратов перед измерением оставляли для уравновешивания по меньшей мере на 30 минут при комнатной температуре.
Содержание NGF в растворах определяли спектрофлуориметрическим анализом на спектрофлуориметре Fluoromax (FluoroMax-4) (автофлуоресцентная эмиссия).
Для определения концентрации белка в различных образцах NGF были построены калибровочные кривые по поглощению в УФ-видимой области и измерению эмиссии собственной флуоресценции. rhNGF разводили в растворе, содержащем фосфатный буфер (50 мМ), метионин 0,020 мг/мл, NaCl 100 мМ, воду q.s. при рН 6,2, в диапазоне концентраций 5-40 мкг/мл; для каждой концентрации проводили три разведения.
Содержание NGF в образцах (препарат F7 по сравнению с CTRL), оцененное с помощью спектроскопического анализа, показано на фиг. 5, а с помощью спектрофлуориметрического анализа - на фиг. 6.
Значения поглощения УФ-видимого света при 280 нм были скорректированы с учетом фона светорассеяния (LS).
Столбцы с одинаковыми водяными знаками относятся к дубликатам для одного и того же момента времени.
Из этих данных авторы заметили, что:
- для препарата F7, который содержал только фосфатный буфер, а не поверхностно-активное вещество, препятствующее адсорбции, было очевидно, что NGF адсорбировался больше в контейнере из силиконизированного стекла, чем в пластиковом контейнере. Это различие было особенно очевидно из графиков автофлуоресцентной эмиссии триптофана: для F7 адсорбция в контейнере из силиконизированного стекла первоначально была очень быстрой по сравнению с CTRL, а затем стабилизировалась в течение следующих 3 месяцев (фиг. 6);
- как для контейнеров из силиконизированного стекла, так и для контейнеров из полипропилена содержание NGF было постоянным в течение трех месяцев при всех условиях стабильности. Как самофлуоресценция триптофана, так и измерения поглощения показали, что в ходе теста не было падения титра NGF в растворе, а именно, что NGF был стабилен в условиях теста; в частности при анализе длины волны флуоресцентного излучения триптофана, даже в контейнере, где NGF адсорбируется больше всего (V, флакон из двойного силиконизированного стекла) и с определяющим наибольшее различие препаратом (препарат F7 без поверхностно-активного вещества), авторы не заметили какого-либо процесса разворачивания или неправильного сворачивания NGF, что свидетельствует о сохранении биологической активности белка.
В заключение, приведенные выше анализы позволили различить полипропиленовые материалы с точки зрения адсорбции белка. Неожиданно с помощью вышеописанных методик было показано, что полипропиленовые пластики, которые адсорбируют меньше белка на своей поверхности, являются гидрофобными материалами, с низкой степенью сополимеризации с полиэтиленом и низкой кристалличностью. Выбранный пластиковый материал PP3 адсорбировал меньше белка на границе твердое тело-жидкость, чем силиконизированное стекло.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИПРОПИЛЕНА С ВЫСОКОЙ ПОЛИДИСПЕРСНОСТЬЮ | 2014 |
|
RU2648672C2 |
| ПОЛИПРОПИЛЕН С ЧРЕЗВЫЧАЙНО ШИРОКИМ РАСПРЕДЕЛЕНИЕМ МОЛЕКУЛЯРНОЙ МАССЫ | 2014 |
|
RU2673339C2 |
| СОПОЛИМЕР ПРОПИЛЕНА ДЛЯ ТОНКОСТЕННЫХ УПАКОВОК | 2014 |
|
RU2652110C2 |
| ГЕТЕРОФАЗНЫЙ СОПОЛИМЕР ПРОПИЛЕНА С ВЫСОКОЙ ТЕМПЕРАТУРОЙ ПЛАВЛЕНИЯ | 2015 |
|
RU2654696C2 |
| КОМПОЗИЦИЯ ВСПЕНЕННОГО ПОЛИПРОПИЛЕНА, СОДЕРЖАЩАЯ ПОЛИМЕРНЫЕ ВОЛОКНА | 2019 |
|
RU2764244C1 |
| ИЗДЕЛИЕ, ИЗГОТОВЛЕННОЕ ЛИТЬЕМ С РАЗДУВОМ И ОБЛАДАЮЩЕЕ ХОРОШИМИ МЕХАНИЧЕСКИМИ И ОПТИЧЕСКИМИ СВОЙСТВАМИ | 2014 |
|
RU2648674C2 |
| СОПОЛИМЕР ПРОПИЛЕНА ДЛЯ БУТЫЛОК, ИЗГОТАВЛИВАЕМЫХ ПНЕВМОФОРМОВАНИЕМ С ЭКСТРУЗИЕЙ | 2014 |
|
RU2637930C2 |
| МЯГКИЕ И ПРОЗРАЧНЫЕ СОПОЛИМЕРЫ ПРОПИЛЕНА | 2017 |
|
RU2698721C1 |
| СТАТИСТИЧЕСКИЙ СОПОЛИМЕР ПРОПИЛЕНА ДЛЯ ПРИМЕНЕНИЯ В ПЛЕНКАХ | 2015 |
|
RU2668797C2 |
| ОБОЛОЧКА КАБЕЛЯ | 2018 |
|
RU2746595C1 |
Группа изобретений относится к химии и фармацевтике, а именно к фармацевтической упаковке; к способу выбора сополимера пропилена и этилена, подходящего для изготовления внутренней контактной поверхности пластикового контейнера указанной упаковки; к применению пластикового контейнера в качестве первичной упаковки водного препарата фактора роста нервов (NGF). Предложенная упаковка содержит пластиковый контейнер в качестве первичной упаковки и упакованный в него водный препарат NGF, где пластиковый контейнер имеет внешнюю поверхность и внутреннюю контактную поверхность, контактирующую с водным препаратом NGF и выполненную более чем на 80 мас.% из сополимера пропилена и этилена, содержащего более 50 мол.% звеньев пропилена и имеющего энтальпию плавления ΔHm менее 95 Дж/г и более 35 Дж/г, измеренную с помощью дифференциальной сканирующей калориметрии (DSC) путем двойного термосканирования (первый нагрев от 0°C до 200°C со скоростью 20°C/мин, промежуточное охлаждение от 200°C до 0°C со скоростью 20°C/мин и второй нагрев от 0°C до 200°C со скоростью 20°C/мин). Группа изобретений обеспечивает снижение адгезии NGF из водных препаратов к внутренней контактной поверхности пластиковых контейнеров. 3 н. и 14 з.п. ф-лы, 8 ил., 12 табл., 6 пр.
1. Фармацевтическая упаковка, содержащая пластиковый контейнер в качестве первичной упаковки и упакованный в него водный препарат фактора роста нервов (NGF), при этом пластиковый контейнер имеет внутреннюю контактную поверхность, контактирующую с водным препаратом NGF, и внешнюю поверхность, при этом, по меньшей мере, указанная внутренняя контактная поверхность выполнена более чем на 80 мас.% из сополимера пропилена и этилена, содержащего более 50 мол.% мономерных звеньев пропилена и имеющего энтальпию плавления ΔHm менее 95 Дж/г и более 35 Дж/г, измеренную с помощью дифференциальной сканирующей калориметрии (DSC) путем двойного термосканирования, включающего первый нагрев от 0°C до 200°C со скоростью 20°C/мин, промежуточное охлаждение от 200°C до 0°C со скоростью 20°C/мин и второй нагрев от 0°C до 200°C со скоростью 20°C/мин.
2. Упаковка по п.1, в которой сополимер пропилена и этилена имеет энтальпию плавления ΔHm менее 90 Дж/г, предпочтительно менее 80 Дж/г, измеренную с помощью DSC путем указанного двойного термосканирования.
3. Упаковка по п.2, в которой сополимер пропилена и этилена имеет энтальпию плавления ΔHm более 40 Дж/г, измеренную с помощью DSC путем указанного двойного термосканирования.
4. Упаковка по любому из предыдущих пунктов, в которой сополимер пропилена и этилена имеет температуру плавления Tm ниже 160°C, предпочтительно ниже 155°C, измеренную в соответствии со способом DSC путем указанного двойного термосканирования.
5. Упаковка по п.4, в которой сополимер пропилена и этилена имеет температуру плавления Tm выше 130°C, более предпочтительно выше 140°C, измеренную в соответствии со способом DSC путем указанного двойного термосканирования.
6. Упаковка по любому из предшествующих пунктов, в которой сополимер пропилена и этилена представляет собой статистический сополимер пропилена и этилена.
7. Упаковка по любому из предшествующих пунктов, в которой содержание мономера этилена в сополимере пропилена и этилена составляет менее 40 мас.%, предпочтительно менее 30 мас.% и по меньшей мере 5 мас.%.
8. Упаковка по любому из предыдущих пунктов, в которой пластиковый контейнер состоит из указанного сополимера пропилена и этилена.
9. Упаковка по любому из предшествующих пунктов, в которой пластиковый контейнер представляет собой ампулу, флакон, бутылку, банку, пакет или мешок, предпочтительно флакон или бутылку.
10. Упаковка по любому из предшествующих пунктов, в которой водный препарат NGF представляет собой водный раствор, эмульсию, суспензию или лосьон NGF, предпочтительно представляет собой водный раствор NGF, более предпочтительно офтальмологический водный раствор NGF.
11. Упаковка по любому из предыдущих пунктов, в которой в водном препарате NGF NGF присутствует в количестве от 0,0001% до 0,5% м/о, предпочтительно от 0,001% до 0,10% м/о, наиболее предпочтительно 0,002% м/о водного препарата.
12. Упаковка по любому из предшествующих пунктов, в которой в водном препарате NGF NGF представляет собой рекомбинантный человеческий NGF (rhNGF).
13. Упаковка по любому из предшествующих пунктов, в которой водный препарат NGF забуферен биологически приемлемым буфером до рН от 6,8 до 7,5, предпочтительно до рН 7,2.
14. Упаковка по любому из предыдущих пунктов, в которой водный препарат NGF в дополнение к rhNGF содержит трегалозу, маннит, метоцел, ПЭГ 6000, L-метионин, фосфатный буфер, воду и имеет pH 7,2.
15. Упаковка по любому из предшествующих пунктов, которая представляет собой упаковку с одной или несколькими дозами.
16. Способ выбора сополимера пропилена и этилена, подходящего для изготовления по меньшей мере внутренней контактной поверхности пластикового контейнера фармацевтической упаковки по любому из пп.1-15, который включает:
- предоставление по меньшей мере образца сополимера пропилена и этилена, содержащего более 50 мол.% мономерных звеньев пропилена,
- измерение энтальпии плавления ΔHm образца сополимера пропилена и этилена с помощью DSC путем двойного термосканирования, включающего первый нагрев от 0°C до 200°C со скоростью 20°C/мин, промежуточное охлаждение от 200°C до 0°C со скоростью 20°C/мин и второй нагрев от 0°C до 200°C со скоростью 20°C/мин,
- выбор подходящего сополимера пропилена и этилена, если его энтальпия плавления ΔHm меньше 95 Дж/г и больше 35 Дж/г.
17. Применение пластикового контейнера в качестве первичной упаковки водного препарата NGF, при этом пластиковый контейнер имеет внутреннюю контактную поверхность, контактирующую с водным препаратом NGF, и внешнюю поверхность, при этом, по меньшей мере, указанная внутренняя контактная поверхность изготовлена более чем на 80 мас.% из сополимера пропилена и этилена, содержащего более 50 мол.% мономерных звеньев пропилена и имеющего энтальпию плавления ΔHm менее 95 Дж/г и более 35 Дж/г, измеренную с помощью DSC путем двойного термосканирования, включающего первый нагрев от 0°C до 200°C со скоростью 20°C/мин, промежуточное охлаждение от 200°C до 0°C со скоростью 20°C/мин и второй нагрев от 0°C до 200°C со скоростью 20°C/мин.
| WO 2017087871 A1, 26.05.2017 | |||
| WO 9717087 A1, 15.05.1997 | |||
| JP 2012001588 A, 05.01.2012 | |||
| КОНТЕЙНЕР ДЛЯ ХРАНЕНИЯ ФАРМАЦЕВТИЧЕСКИХ РЕЦЕПТУР | 2005 |
|
RU2360853C2 |
| WO 2019241063 A1, 19.12.2019 | |||
| WO 9505845 A1, 02.03.1995 | |||
| КОМПОЗИЦИЯ ТЕРМОПЛАВКОГО АДГЕЗИВА И ЕЕ ИСПОЛЬЗОВАНИЕ | 2016 |
|
RU2709356C2 |
Авторы
Даты
2025-06-06—Публикация
2021-10-27—Подача