: со со Изобретение относится к физико-хи мическому анализу, в частности к потенциометрическим методам количественного непрерывного контроля активности ионов фтора в различных средах и веществах, и мояет быть испольэова но в черной, цветной, нефтехимической и нефтеперерабатывающей, стеколь ной промышленности, промышленности строительных материалов, а также в практике научных исследочаний в области химии. Известны потенциометрические датчики для определения активности ионо фтора, содержащие i opnyc, индикаторный и сравнительный электроды и изме рительную схему. Принцип потенциомет ричесКого измерения активности ионов в известных случаях основан на измерении разности электрических потенци алов индикаторного и сравнительного электродов, помещенных в ана1лизируемый раствор, причем сравнительный электрод в процессе изменения должен иметь постоянный потенциал 1 и 2 Недостатками известных датчиков являются непостоянство потенциала электрода сравнения, например, из-за измерения диффузионного потенциала на границе раздела фаз: электрод сравнения - анализиру(эмый раствор, сложность и недостаточная надежность высокоомных измерительных преобразователей, а следовательно, значительная ошибка измерения (15-20%) и ошиб ка воспроизводимости результатов измерений (10%) . Наиболее близким к предлагаемому по технической сущности является ч потенциометрический датчик для измерения активности ионов фтора, содержащий корпус, заполненный анализируемым раствором, в который погружен индикаторный фтороселективный электрод, на чувствительный элемент которого нанесен твердый внутренний контакт, состоящий из слоев AgF и &, и измерительную схему 3. Основным источником ошибок при из мерении ЭДС является электрод сравне ния. Место контакта измеряемый раствор/солевой мостик существенно влияет на воспроизводимость измерения ЭДС, так как здесь возникает нестабильный диффузионный потенциал, колеблящийся в пределах 2-10 mV. С точки зрения воспроизводимости и надежности измерений контактная зона сравнения электрода является самым уязвимым местом датчика. Наличие температурного гистерезиса электрода сравнения приводит к из менению показаний датчика на i5 mV. Поляризация внутренних контактов на границе раздела фаз индикаторного электрода приводит к изменению тока рассеяния и тока обмена, а следовательно, увеличению погрешности измерения. Электрическое сопротивление индикаторного фтореелектинного электрода порндка 1 мОм требует применения выг coKOOMHbix измерительных преобразователей. У высокоомных измерительных преобразователей высокого класса уровень шумов составляет 25 MV,следовательно, увеличение сопротивления преобразователя ведет к увеличению уровня шумов и дополнительным флуктуациям показаний. Необходимо высокое сопротивление изоляции по всейудлине измерительного кабеля, включая и разъем, также как и входного сопротивления измерительного преобразователя, которое должно быть на несколько порядков выше внутреннего сопротивления электроДа.. Таким образом, точность анализа при учете всех погрешностей работы известного датчика составляет 15-20% Цель изобретения - повьт1ение.точJHOCT4 и, надежности измерений. Поставленная цель достигается тем, что в потенциометрическом датчике для измерения активности ионов фтора, содержащем корпус, заполненный анализируемым раствором, в который погружен индикаторный фторселективный электрод, на чувствительный элемент которого нанесен твердый внутренний контакт, состоящий из слоев AgF и Ад, и измерительную схему, твердый внутренний контакт дополнительно содержит слой Agl , расположенный между слоями AgF .и Ад, и внутр.енние металлические контакты, один из которых прикреплен к слою AgF, а другой - к слою Ад, включенные в измерительную схему, состоящую из источника стабилизированного, напряжения и измерителя тока. Первый слой AgF готовят по следующей методике, Поликристалический порошок фтористой соли AgF тщательно перемешивают путем истирания и нагревают с целью гомогенизации в течение 1 ч в вакуумной печи при . Обработанную таким образом массу после дополнительного измельчения прессуют, применяя вакуумное горячее прессование при , давлении 120 кг/ем- и вакуу-ме .рт.ст. в течение 2 ч. Для изготовления второго слоя Agl берут твердую основу, например керамическую, пропитывают раствором азотнокислого серебра, затем сушат. Керамическую основу- после просушки пропитывают раствором иодида натрия, а после этого проводят повторную про мывку и просушку, при этом происходит реакция .j-(-No(3 /l J-t-NaNO. Промьшку производят водой до полного отсутствия иона NO в керамиче кой основе. Полученные слои AgF и Agl, а такж Ад и чувствительный элемент в виде мембраны соединяют, применяя вакуумное горячее прессования при , давлении 120 кг/см2 и вакууме 10 рт.ст. в течение 1 ч. Металлические контакты, например платиновые, соединяют со слояМи AgF и Ад, применяя тйкже вакуумное горячее прессование, в готовый электрод, который затем помещают в корпус На фиг. 1 изображен предлагаемый потенцирметрический датчик; на фиг. 2 - кривые зависимости выход-, ного сигнала датчика от времени; на фиг. 3 - температурные кривые датчики; ни фиг. 4 - зависимость тока датчика от концентрации ионов, полученных в растворах NaF с постоянной ионной СИЛОЙ; на фиг. 5 - калибровочная кривая зависимости выходного сигнала потендиометрического датчи-т; ка от концентрации; на фиг. б - гра; фическая схема переноса зарядов при работе датчика. Предлагаемый потенциометрическйй датчик содержит корпус 1, заполнейны анализируемым раствором 2, в который /погружен измерительный Фторселектив- ный электрод 3 с твердым внутренним контактом, представ л якядий собой последовательно нанесенные на чувстви-. тельный элемент в виде мембраны-4 твердоэлектролитные слои 5-7 AgF, . Agl и Ад соответственно, и внутренние металлические контакты 8 и 9, например платиновые, один из которьо (контакт 8) прикреплен к слою 5 AgF/ а другой - к слою 7 Ад, соединенные с источником 10 стабилизированного напряжения и измерителем 11 тока. Изоляцию от окружающей среды и фикса цию внутреннего электрохимически ак тивного элемента электрода 3 обеспечивёиот, например, инертным эпоксидным или силиконовым компаун- , дом 12.. Предлагаемый датчик представляет собой электрохимическую цепь, cpcTajB ленную следуквдим образом: инертый электрод Mie/MeX ;,/МеХл / /инертный электрод; мембрана раствор где Me - металл; , соли металла; Х - ,анализируемый ион. Для такой электрохимической цепи, в которой МеХл существует с небольшим отклонением от идеального сте-. хиометрического состава,-можно вывес ти следующее уравнение для ЭДС цепи (Vtli Aiez j (), Лх где Е - электродвижущая сила цепи;t , t2 числа переноса катионов и анионов; Z, Zn- значения зарядов катионов и анионов; (ие химический потенциал Me со стороны Me; химический потенциал Me со стороны X; Cjj - химический потенциал X со стороны Me; химический потенциал X , со стороны X (мембраны); F - постоянная Фарадея. Таким образом, имеется непосредственная возможность измерения ЭДС цепи при систематическом изменении значения fjiy , При использовании мембраны в качестве чувствительного элемента значение на границе разде- ла фаз мембрана/МеХ2 изменяется при изменении концентрации ионов Х2 во внешнем анализируемом растворе в соответствии с уравнением Нернста ./ j :const + |lenc,, f2) где Cj( - концентрация ионов в анали2 зируемом растворе; Т - температура; R - ;универсальная газовая постоянная . Воздействуя на ЭДС цепи путём изменения химического потенциала уи на внутренней стороне мембраны, как следствие можно измерять изменение тока цепи, величина которого будет служить концентрации анализируемого компонента во внешнем раств.оре. Принцип действия датчика заключается в следующем. При положении напряжения от стабилизированного источника питания к электрохимической цепи датчика в AgF начинается движение ионов серебра- в -направлении согласно электрическому, полю. Это приводит к возникновению дефицита ионов серебра на граничной поверхности AgF / инертный электрод, в результате чего ионы серебра диффундируют слева направо из слоя Ад в слой AgF При достижении стационарного состояния диффузия ионов серебра компенсируется электролитическим движением за счет приложенного напряжения, при этом перенос тока во внешней цепи осуществляется за счет , электронсв без химических изменений на электродах. На фиг. 2 представлены кривые заBHQ.KMOCTH выходного сигнала датчика от времени при различных значениях поляризующего напряжения и концентра ции измеряемого компонента. Из .анали за кривых следует, что злектрохимические процессы на инертных токоотво ДЯ1ДИХ электродах практически не идут Стабильность показаний датчика соста ляет t 5%. При изменении активности или концентрации ионов фтора во внешнем растворе изменяется потенциал на фазовой границе мембрана/AgF, что ведет к изменению тока в злектрохимической цепи датчика. Величина изменения тока в свою очередь служит мерой измеряемой концентрации ионов в анализируемом растворе. Промежуточный слой твердого элект рбпита Agl необходим для осуществлениА процесса снятия изменения концен рации анализируемых ионов во внешнем растворе. Электропроводность Agl составляет 1,3-2,6 (Ом-см) , коэффициент диффузии ионов Ад имеет такой же порядок как в расплавленных или жидких солях Таким образом, можно считать, что пр водимость Agl носит униполярный характер и обеспечивается движением ионов Agt Слой Agl служит также для предотвращения образования металлических мостов, а следовательно, короткого замыкания цепи и является как бы защитным слоем с .ионной проводимостью. На металлические контакты 8 и 9 подается поляризующее, напряжение от стабилизированного источника питания обеспечивающее определенный начальный ток цепи, а также последующее его измерение за счет изменения потенциала на фазовой границе мембрана/ AgF . Величина поляризующего напряжения определяется из условия недиссоциации электролитов цепи, . не прохождением процесса электролиза-, а также величиной измеряемой концентра ции анализируемых ионов, и равна 10-50 MV. При этом ток, протекающий через ячейку, является функцией приложенного напряжения и свойств внутренних элементов и определяется урав нением dX /3) Е - величина приложенного поляризующего напряжения; электронная и ионная проводимость цепи F - постоянная Фараден. В процессе поляризации ток ионной проводимости вызывает градиент химического потенциала электронов вдоль цепи, обуславливающий образование электрического поля с направлением, противоположным направлению первоначального поля. По мере возрастания поляризации общее электрическое поле, а следовательно, и ионный ток, уменьшаются, в результате чего достигает-ся стационарное состояние. Знак поляризующего напряжения следующий; плюс от источника стабилизированного напряжения приложен к.электрод ному слою из Ад Диапазон измеряемых концентраций зависит, с одной стороны, от произведения растворимости материала мембраны, а с другой, от величины начального тока, который определяется величиной поляризующего напряжения. При значительной величине поляризующего напряжения малые значения возникающего потенциала будут вызывать малое измейение ЭДС цепи, а при малых величинах поляризующего напряжения имеется возможность зафиксировать изменения ЭДС, соизмеримые с величиной возникающего потенциала. Таким образом, имеется прямая возможность изменения диапазона измеряемых концентраций в соответствии с оптимальной величиной чувствительности датчика за счет изменения величины поляризукщего напряжения (ст, табл. 1). Таблица 1 Знак и величина поляризующего напряжения, подаваемого от стабилизированного источника питания, во время процесса измерения остаются постоянной. Изменяется потенциал, возникающий на границе мембрана / AgF. Изменение величины тока, служащее мерой изменения концентраций измеряе1 /1ых ионов в анализируемом растворе в соответствии с уравнениями (1) и (2), фиксируетизмеритель 11 тока с нулевой отметкой посредине шкалы, так как изменение может быть как отрицательно, так и положительно в зависимости от соотношения возникающего потенциала и величины поляризующего напряжения . Таким образом, првдлагаёйый датчик реалиэуетсзя с помощью электрохимической цепи вида: инертный электрод /Ag/Agl/AgF/ , инертный электрод мембрана рас ТВ ор и позволяет производить непрерывный количественный контроль анализируемого компонента без применения злект рода сравнения и высокоомного измери тельного оборудования. Точность изме рения и надежность датчика значитель но возрастают из-эа отсутствия диф- фузионного потенциала и других допол нительных погрешностей, связанньос с наличием контактной зоны электрода сравнения. Отсутствие тока на фазовой границе мембрана / AgF приводит к отсутст вию поляризационных явлений в.предла гаемом датчике; что позволяет непос редственно подключить выводы контак тов 8 и 9 к простому и надежному и&мерительному прибору с магнитоэлектрической системой, например к широко распространенному- универсальному измерительному прибору без электрического усиления - миллиамперметру. Достоинством предлагаемого потендиометрического датчика является воз можность прямого непрерывного преобр зования активности или концентрации измеряемых ионов в пропорциональные им электрические сигналы без сложиог превращения сигналов.Логарифмическая связь между активностью измеряемых ионов и выходным сигналом датчика позволяет работать на нескольких диа, пазонах концентраций с неизменной от носительной точностью. Эта динамическая область работы вместе с простой и надежной конструк цией датчика, а также простотой обслуживания позволит применять предла гаемый датчик непосредственно для , . непрерывных измерений в процессе контроля технологических растворов или в качестве контрольного прибора при исследовании окружающей среды. Датчик может быть использован з широком диапазоне рН 2-12, при температурах окружающей среды 5 - 50 С На фиг. 3 представлены температурные кривые предлагаемого датчика при различных значениях измеряемого параметра. Оптимальная рабочая температура в процессе измерения cocxaf ляет 40± 5°С. Время установления стационарных значений измеряемой величины даже s разбсшленньос растворах не превышает 5-10 с. Сопротивление,предлагаемого Дс1тчика составляет 1 кОм. В табл. 2 представлены данные за висимости выходного сигнсша от концентрации измеряемого компонента Для трех различных датчиков. Многократное проведениеопытов позволяет утверждать, что воспроизводимость показаний потенциометрического датчика составляет 4%. Таблица2 Точность определения концентрации фтор-иона предлагаемым датчиком с применением калибровочной кривой coc-t тавляет t 5%. Датчик можно использовать для потенциометрического титрования ионов фтора по стандартным методикам. Точность определения при этом составляет 0,4-0,6%. Пример. Определение концентрации ионов фтора прямым потенциометрическим методом с помощью калибровочной кривой. Крив-ая зависимости изменения тока датчика ох концентрации ионов фтора в чистых растворах NaF, а также зависимость, полученная в растворах с постоянной ионной силой ЗМ, создаваемой буферным раствором цитрата натрия, представлены на фиг. 4. (Кривая 13 - чистый раствор NaF, кривая 14 - раствор NaF с .постоянной ИОННОЙ силой ЗМ). Пример2. Определение концентрации ионов фтора методом потенциометрического титрования. Кривая потенциометрического титрования представлена на фиг. 5. Взято для анали;за 50 мл 0,5 М раствора NaF. На титрование пошло 249 мл 0,1 н.раствора ТН(м6э)4. Найдено, что концентрация фторида натрия в исходнрм растворе составляет 0,498 М. Ошибка определения составляет 0,4%. Предлагаемый датчик может быть выполнен в виде различных модификаций: обычный погружной с горизонтально
расположенной мембраной; погруженной с мембраной, расположенной вертикально, для улучшения конвективного обмена у поверхности мембраны; в виде таблетки, которую можно вводить в труднодоступные полости.
использование предлагаемого датчика позволит проводить технологические процессы, связанные с наличием
ионов фтора, например с приготовлением солей данного иона, очисткой отходящих газов от фтористых соединений, в условиях, близких.к оптимальным. Так как предлагаемый датчик обладает хорошими метрологическими и эксплуатационными характеристиками, это позволит изготовлять его-в промышленном масштабе.
60 .60
Jff
го го
/57 fff /у- /
1- L-r
; Фtfг.J



| название | год | авторы | номер документа |
|---|---|---|---|
| Проточная потенциометрическая ячейка | 1985 |
|
SU1318902A1 |
| СПОСОБ ИЗМЕРЕНИЯ АКТИВНОСТИ ИОНОВ В РАСТВОРАХ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2003 |
|
RU2244917C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ ДАТЧИК ДЛЯ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ ГАЗОВ И СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ГАЗОВ С ПОМОЩЬЮ ДАННОГО ДАТЧИКА | 1994 |
|
RU2106621C1 |
| ТВЕРДОЭЛЕКТРОЛИТНЫЙ ДАТЧИК ДЛЯ ПОТЕНЦИОМЕТРИЧЕСКОГО ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ ВОДОРОДА В ГАЗОВЫХ СМЕСЯХ | 2012 |
|
RU2490623C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ФТОРИД-ИОНОВ В ВОДЕ (ВАРИАНТЫ) | 2006 |
|
RU2331873C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧУВСТВИТЕЛЬНЫХ ПОТЕНЦИОМЕТРИЧЕСКИХ ДАТЧИКОВ | 2002 |
|
RU2301997C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ДИОКСИДА КРЕМНИЯ НА ПОВЕРХНОСТИ КРЕМНИЯ | 2011 |
|
RU2469303C1 |
| Способ индикации точки эквивалентности в кулонометрическом анализе | 1980 |
|
SU934343A1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ ДЕТЕКТОР ДЛЯ ИССЛЕДОВАНИЯ ЖИДКОСТИ СЛОЖНОГО СОЛЕВОГО И ХИМИЧЕСКОГО СОСТАВА | 2008 |
|
RU2370759C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО МУЛЬТИСЕНСОРНОГО ОБНАРУЖЕНИЯ И ИДЕНТИФИКАЦИИ АЛКАЛОИДОВ | 2008 |
|
RU2375705C1 |

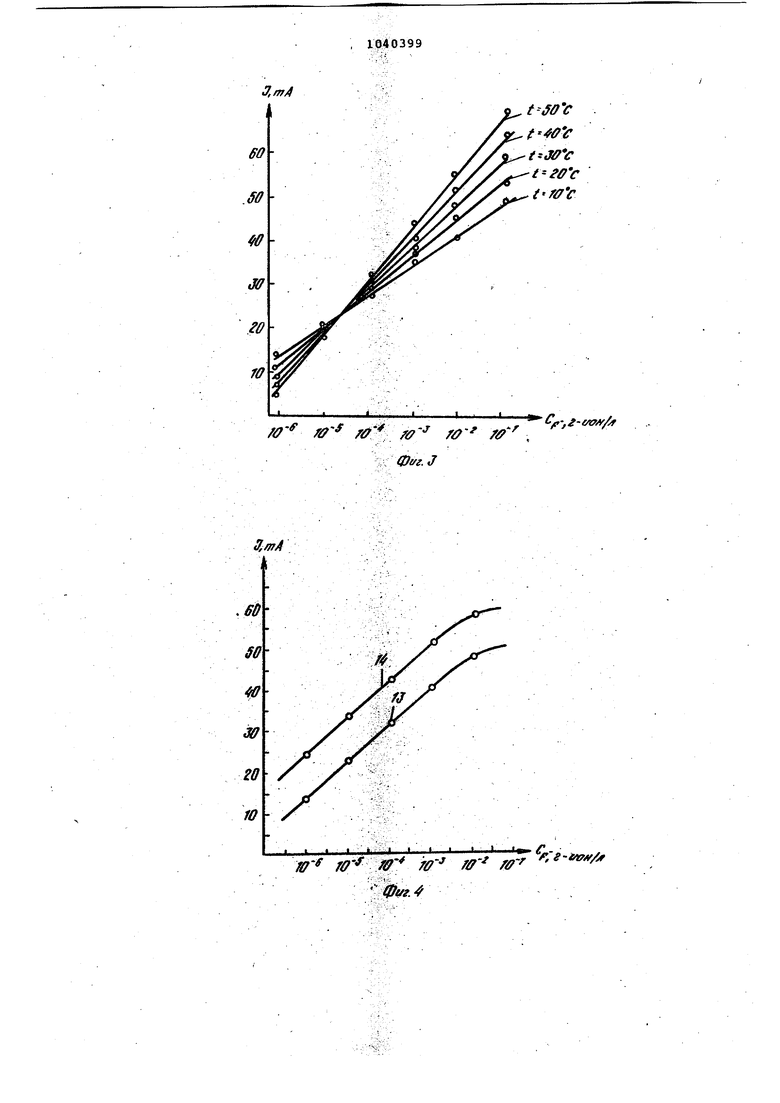
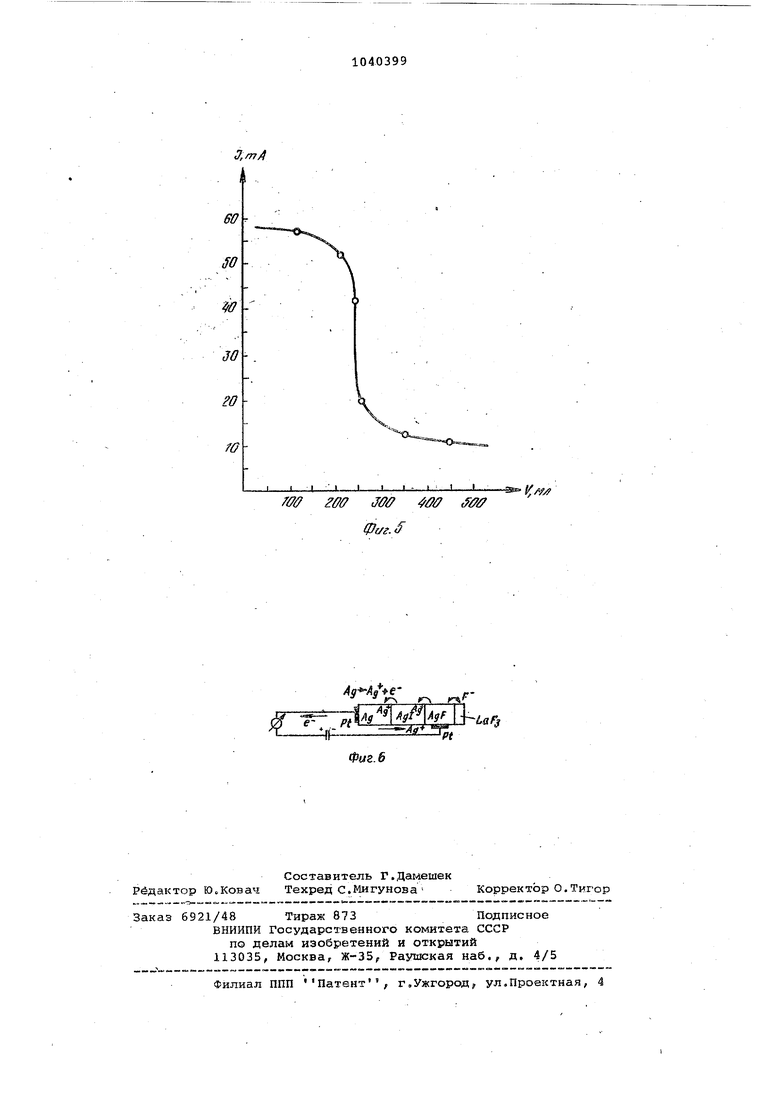
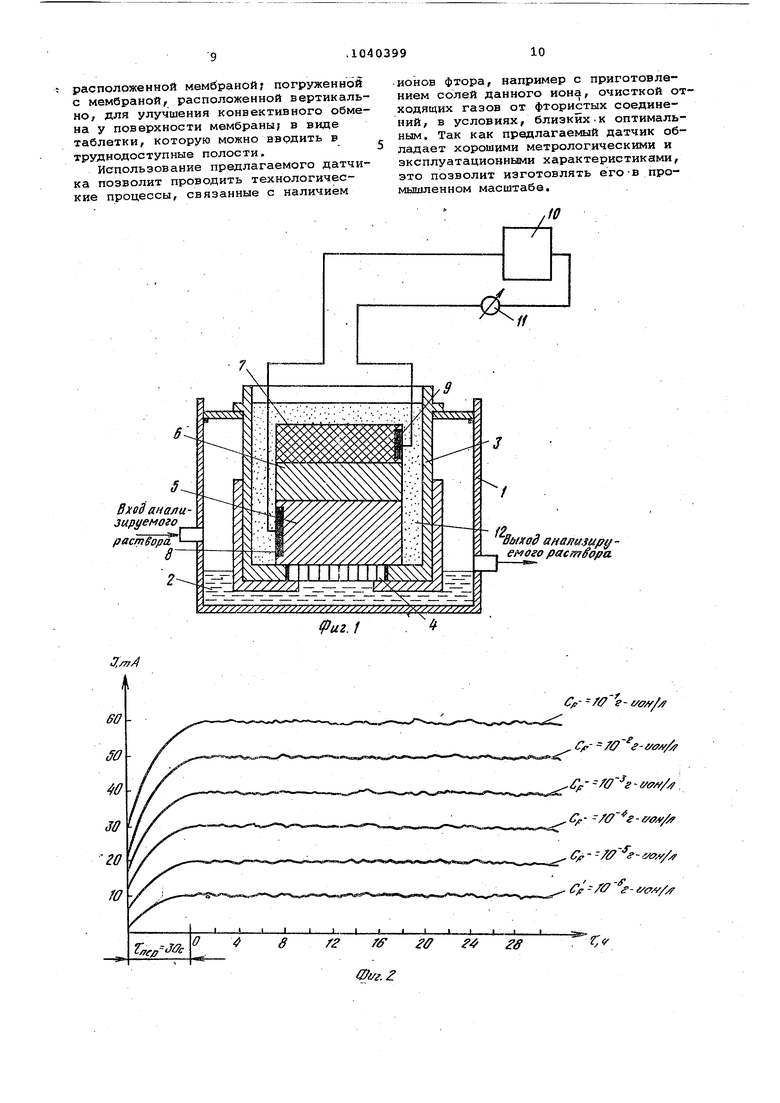
ПОТЕНЦИОМЕТРЙЧЕСКИЙ ДАТЧИК ДЛЯ ИЗМЕРЕНИЯ АКТИВНОСТИ ИОНОВ ФТОРА содержащий корпус, заполненный анали: зируегфвд раствором,в который погружениндикаторный фторселетивный элект- род, на чувствительный элемент которого нанесен твердый внутренний контакт, состоящий из слоев AgF и Ад, .и измерительную схему, о т л и ч а ю щ и и с я тем, что, с целью повышения точности и надежности измерений, твердый внутренний контакт дополнительно содержит слой Agl, расположен.; ный между слоями AgF и Ад, и внутрен/:ние металлические контакты, один из -.которых прикреплен к слою AgF, а друQ . , гой - к слою Ад, включенные в измериS тельную схему,: состоящую из источнисо iка стабилизированного напряжения и iизмерителя тока..
SO SO
Зв
20 10
rf rof - 7ff- Фиг.4
3,mA
60 SO W
го fff
I II I I I I . 1 II
ffff Jffff ffff ffff
p.
, - f#Г/й
Ф1/г. f
3iLl3
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Лайт Т | |||
| Использование ионоселективных электродов для производственного анализа и контроля технологических процессов | |||
| кн | |||
| j Ионоселективные.электроды | |||
| Под ред | |||
| Р.Дарста, М., Мир, 19729 с | |||
| Приспособление для записи звуковых явлений на светочувствительной поверхности | 1919 |
|
SU101A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗДЕЛИЙ ИЗ СЛОЖНОЛЕГИРОВАННЫХ ЖАРОПРОЧНЫХ НИКЕЛЕВЫХ СПЛАВОВ | 2011 |
|
RU2457924C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Стенина Н.И,, Лапшанова Н.С., Швецов.В.В, Определение Фтора с йс- поль9бваяие селективцого фторнйного электрода | |||
| Труды Уральского научно-; / исследовательского института, , вып | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| : | |||
Авторы
Даты
1983-09-07—Публикация
1981-12-01—Подача