Изобретение относится к новым хи мическим соединениям, а именно 2-фС карбокси- -меркаптоэтилимино)-пирро лидинам, -пиперидинам, -гексагидроазепинам общей формулы I соон R 2 Л-, I SH R . при ,3 R.,R - каждый атом водород ,2 R атом водорода; R-мети . .,2,3 R - метил; R- атом вод рода, метил, обладающим антигипертензивной актив ностью. Структурными аналогами указанных соединений являются соединения общей формулы А НзС V СООСНз о p -C K-CH-R пзС ffie R означает Н, -CgHij, ,,-, CHj. SCHj, СН7.И соединение формулы Б (CH2)5-COOH . Н. . Однако о биологической активности этих соединений сведений в литер туре нет. Известно использование в качеств антигипертензивных препаратов D-пени цилламина и цистеина ГН го/СООН НзС, нг-сн ::с-сн SH цистеинD-пеницилламин Цель изобретения - новые соединения, проявляющие антигипертензивную активность в ряду амидинов, содержа1чИх в боковой цепи карбоксильную и меркаптогруппы. Цель достигается соединениями I, способ получения которых, заключается в том, что диэтилацеталь N-метиллактама общей формулы II со где п 1-3, или лактимньй эфир общей формулы III ICHoinш-I где п 1-3, подвергают взаимодействию c -aMiHoР-меркаптокислотой общей формулы IV. СООН R H2N-CH-C-R (iv SH где R - атом водорода, метил, в среде низшего спирта при 20-25 С. Строение полученных соединений общей формулы I подтверждено данными элементного анализа, ИК- и масс-спектров. В ИК-спектрах полученных соединеС0 иний имеются полосы поглощения 1600-1700 см C N-групп в области В масс-спектрах имеются пики молекулярных ионов, основные пути фрагментации которых связаны с отрывом SH-, СООН и Н2.8-групп. Пример 1. Получение 2-(N-lкарбокси-2-меркаптоэтилимино)-пирролидина. К 1,09 г (10 ммоль) цистеина в 25 мл метанола прибавляют по. каплям 1,19 г (12 ммоль) 0 метил.бутиролактима в 5 мл метанола при 20-25С. Смесь выдерживают при этой же температуре и перемешивании в течение 16 ч, метанол упаривают, к остатку добавляют абсолютньй эфир ( мп), выпавший осадок отфильтровывают. Получают 1,6А г (87%) 2-(N-l-Kapбокси-2-меркаптоэтилимино)-пирролидина в виде белого кристаллического порошка; т.пл. 175-176 С (из изопропанола). Найдено,%: С 44,21; Н 6,56; 14,80; S 16,89. СгЕ,, ,S. Вычислено,%: С 44,68; Н 6,38; N 14,89; S 17,02. В условиях, аналогичных примеру 1, получают соединения 3, 6 и 10. Физические константы, условия реакции, выходы и аналитические характеристики указанных соединений приведены в таблице I. Пример 2. Получения 1-метил2-(N-l-кapбoкcи-2-мepкaптoэтилиминo)-пиppoлидинa , К 0,7 г (6 ммоль) цистёина в 25 м метанола прибавляют по каплям 1,3 г (9 ммоль) диэтилацеталя N-метилпирролидона в 5 мл метанола при 10-15° размешивают 4 ч при 20-2fС, отфиль ровывают, фильтрат упаривают, остаток промывают 2-3 раза абсолютным эфиром (по 30 мл), затирают в абсолютном эфире (30 мл), отфильтровывают . Получают 0,51 г (43%) 1-метил-2(N-1-карбокси-2-меркаптоэтилимино)пирролидина в виде белого кристалли ческого порошка; т.пл. 183-186 С (из этанола). Найдено,%: С 45,09; Н 6,53; 12,94; S 15,05; НгО 6,34. I HjO. , Вычислено,%: С 44,86; Н 7,01; N 13,08; S 14,95; НаО 5,61. В условиях, аналогичных примеру получают соединения 4, 5, 6 и 7. Фи зические константы, условия реакции выходы и аналитические характеристи ки указанных соединений приведены в таблице 1. П р и м е р 3. Получение 1-метил . 2- (N-1 -карбокси-2-метил-2-меркаптопропилимино)-пиперидина. К 0,75 г (5 ммоль) В-пенициллами на в 25 мл абсолютного этанола прибавляют по каплям 1,0 г (5,3 ммоль) диэтилацеталя N-метилпиперидона в 5 мл абсолютного этанола при 20-25 смесь выдерживают при этой температ ре 5 ч, этанол упаривают, к остатку добавляют абсолютный эфир (50 мл), выпавший осадок отфильтровывают. Получают 1,1 г (90%) 1-метил-2(Ы-1-карбокси-.2-метил-2-меркаптопро пилимино)-пиперидина в виде белого кристаллического порошка, т.Ш1.178180 С (из этанола). Найдено,%: С 53,70; Н 8,50; N11,12; S 12,93. . Вычислено,%: С 54.10; Н 8,20; N 11,48; S 13,11. Указанные биологические свойства определяются химическим строением со динений I. Существенным фактором, определяю щим активность соединений 1, являет ся наличие в молекуле находящихся при соседних углеродных атомах карбоксильной и меркаптогрупп, а также преобразование аминогруппы соответс вующейЛ -аминокислоты в амидиновую группировку. Соединения общей формулы 1 представляют собой кристаллические вещества белого цвета, имеющие температуру плавления в пределах 150-186 С, хорошо растворимые в воде, низших спиртах при Нагревании, трудно растворимые в органических растворителях, устойчивые при хранении. Изучение биологической активности соединений 1 проводилось на очищенном ферменте дипептидил-карбокси пептидазы (ДКП), на животных с различными формами гипертонических-состояний. Дипептидил - карбоксипептидаза (ДКП) является ключевым ферментом ренин-ангиотензин-альдостероновой . , и калликреин-кининовой систем: .образует прессорный пептид ангиотензин II и разрушает депрессорный пептид браднкинин, контролируя, таким образом, их концентрацию в крови. ДКП участвует в регуляции кровяного дав ления. В присутствии различных концентраций предлагаемых соединений (1х10, 0,5x10, 1x10 , 1x10 М) фермент выдерживают при 37 С в течение 30 мин,, затем добавляют субстрат и через 30 мин останавливают ферментативную реакцию. Активности фермента определяют высокочувствительным флюориметрическим методом. В качестве эталона для сравнения действия соединений I на этот фермент использук1т лекарственные препараты - Вгпенициллаьин и цистенн в тех же концентрациях, обладающие ингибирующим действием на фермент ДКП. Результаты исследования представлены в табл.2. Как видно из представленных . данных, все соединения оказывают ингибирующее влияние на фермент ДКП, наиболее активными из них ока зались соединения № 2, Зи 10 Исследование антигипертензивной активности соединений I проводилось: а)на спонтанно гипертензивных крысах-самцах массой 250-300 г, б)на модели рено-васкулярной гипертогши у крыс-самок массой 180250 г, вызванной сужением левой почечной артерии спиралью из нихромовой проволоки при одновременном удалении правой почки;
в) на модели гипертензии у крыссамцов массой 150-200 г, вызванной подкожным введением дезоксикортикостерона ацетата (4 мг/кг, подкожно, через день в течение 6 недель) и питьем 1% раствора хлористого натрия.
Активность соединений изучают в дозах, составляющих 10% от ЛДд, которую определяют на мышах-самцах массой 16-17 г при введении внутрь и расчитывали по известному методу.
Результаты исследования антигипертензивной активности и острой токсичности (ЛД 50) соединений общей формуры1 представлены в табл.3,
В результате исследования установлено , что соединения 1j 2, 3, 4, 5, 6, 7,9, 10 в указанных дозах понижают на 17-51 мм рт.ст, артериальное давление АД) у спонтанно гипертензивных крыс, соединения 1, 3, 4,
5, 7, 8, 9, 10 - на 8-55 мм рт.ст. понижают АД у животных с рено-васкулярной моделью гипертонии и соединения 1, 2, 3, 4, 5, 6, 8, 9, 10 - понижают на 4-32 мм рт.ст. АД у крыс с Д01СА-солевой моделью гипертонии.
Как видно из представленных данных, уровень активности соединений 1 по антигипертензивному действию близек к лекарственным препаратам 1 -пеницилламину и цистеину.
Наиболее выражены антигипертензивные свойства у соединений 4, 5 и 6, которые на различных моделях гипертензии по активности Превосходят 2 -пеницилламин и цистеин.
Токсичность соединений (ЛД5о), изученная на мьшах-самцах массой 16-17 г при введении внутрь, невелика (более 1000 мг/кг), что позволяет отнести их к разряду малотоксичных соединений.
I
104557312
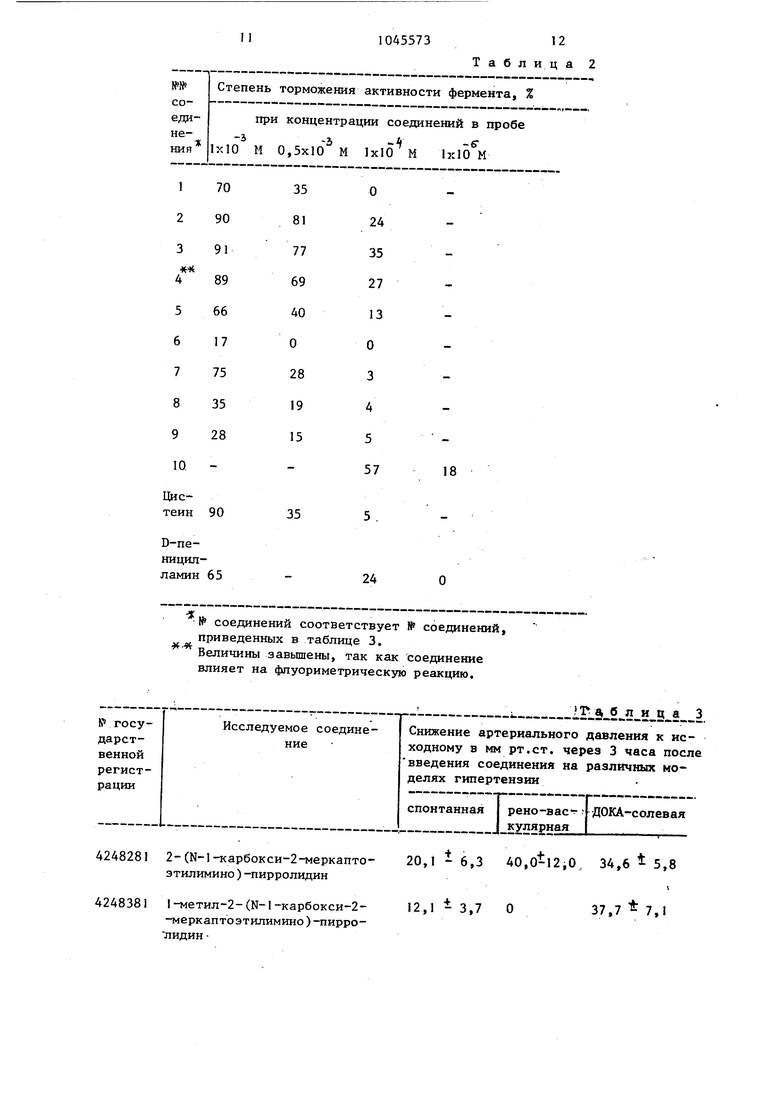
Таблица 2





| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ АНТРА[2,1-d]ИЗОТИАЗОЛ-3,6,11-ТРИОНА | 2002 |
|
RU2213744C1 |
| ДИПЕПТИДЫ, СОДЕРЖАЩИЕ НА N-КОНЦЕВОМ АМИНОКИСЛОТНОМ ОСТАТКЕ 2-ТИОАЦИЛЬНУЮ ГРУППУ, В КАЧЕСТВЕ ИНГИБИТОРОВ ВАЗОПЕПТИДАЗЫ | 2002 |
|
RU2298559C2 |
| ПРОИЗВОДНЫЕ КАРБОКСАМИДИНА И ИХ ИСПОЛЬЗОВАНИЕ ПРИ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ СОСУДОВ | 2003 |
|
RU2320330C2 |
| ПРОИЗВОДНЫЕ АМИДИНОФЕНИЛАЛАНИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРОИЗВОДНЫЕ АМИДИНОФЕНИЛАЛАНИНА, ОБЛАДАЮЩИЕ АНТИКОАГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1992 |
|
RU2088591C1 |
| ЗАМЕЩЕННЫЕ БЕНЗИЛАМИНЫ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ДЕПРЕССИИ | 1997 |
|
RU2179553C2 |
| СЕРУСОДЕРЖАЩИЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ НА ИХ ОСНОВЕ | 2000 |
|
RU2244708C2 |
| ЗАМЕЩЕННЫЕ 8,8A-ДИГИДРО-3AH-ИНДЕНО [1,2-D] ТИАЗОЛЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2001 |
|
RU2263669C2 |
| НОВЫЕ СОЕДИНЕНИЯ С АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 2004 |
|
RU2397982C2 |
| АНТИБАКТЕРИАЛЬНЫЕ АГЕНТЫ | 2000 |
|
RU2269525C2 |
| ПРОИЗВОДНЫЕ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ И ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2001 |
|
RU2265011C2 |
2-(о -Карбокси- меркаптоэтилимино)-1шрролидины,-пиперидины- или -гексагидроазепины общей формулы 1 ,„ sj-I N-eH-C R иNH где при ,3 К,Е-каждый атом водо- о S to рода; ,2 атом водорода; (Л R - метил; ,2,3 R - метил; R - атом водорода, метил. обладающие антигипертензивной активностью. 1 сл СП ч| со
JT
№ соединений соответствует 8 соединений, приведенных в таблице 3.
-9t
Величины завьпаены, так как соединение влияет на фпуориметрическую реакцию.
2- (N-1-карбокси-2-меркаптоэтилимино)-пирролнднн
|-метил-2-(Ы-1-карбокси-2-меркаптоэтилимино)-пирро лидин
20,1 - 6,3 40,0-12,0, 34,6 5,8
37,7 7,1
12,1 - 3,7 О
13 104557314
Продолжение табл.3
| Fitt J.J | |||
| Gschwend H.W.o -ALkyLation and Michael Addition of Amino Ocids-a Practical Method-, J.Org.Chem, 1977, V 42, N 15, s 2639-41 | |||
| Kbrosi J | |||
| Neue Peptidsynthese unter Ver vrendlung von semicyclischen Amidin - Casbonsauren I | |||
| HersteLLung von N-(E-Amino-Caproyl)-E-AminoCapronsaure und PaLycenproLactam | |||
| Neue Daten z.iim Mechanismus der PoLycaprelactam - BiLdung in Gegenwart von Wasses, Amino-Carbonsaureh und AmisaLzen | |||
| S | |||
| P.Chem, 1964, v.23, S.212. |
Авторы
Даты
1986-06-23—Публикация
1981-12-29—Подача