Изобретение относится к металлур гии легких металлов, а нменно к кон тролю технологического процесса электролиза алюминия. При работе электролизера в условиях возникновения анодных эффектов расход углерода анода повышается,од нако до настоящего времени не бьш разработан способ, позволяющий определить расход углерода анода при анодном эффекте. Известен способ определения COg и CF4 в условиях герметизации шторных укрытий электролизера (при определенной степени герметизации электролизера) Pj . Недостатком данного способа явля ется то, что не учитывается расход углерода анода при анодном эффекте. Наиболее близким по технической сущности к предлагаемому является способ определения удельного расхода углерода анода, включающий определение концентрации СО в условиях герметичной работы электролизера и концентраций СО, СО-и дрступ воздуха в электролизер. Согласно этому способу определяю концентрацию С02 в анодных газах пр работе электролизера в герметичных условиях и концентрации COg, СО и Nj при доступе воздуха в электролизер, а величину удельного расхода углерода рассчитывают по уравнению ,,,,, 8(-6) °(2A.6)(.Nco,,) 3(,,J где Р - удельный расхода углерод анода, кг/кг А6 / СО - концентрация С02 в услоВИЯХ герметичной работы электролизера,ед; А,В,В - содержание С02, СО и N условиях доступа воздуха в электролизер, ед. 2j. Недостатком прототипа является то, что он не учитывает дополнител ные потери углерода, связанные с возникновением анодного . Цель изобретения - повышение точности измерения удельного расхо углерода анода. Поставленная цель достигается тем, что в способе определения удельного расхода углерода анода, включающем определение концентрации СО в условиях Герметичной работы электролизера и концентраций CO/J, СО и N при доступе воздуха в электролизер, что согласно изобретению дополнительно определяют концентрации С02И CF в условиях герметичной работы Электролизера при анодном эффекте, а величину удельного расхода определяют по уравне-нию3(1-0,03744tk)(H-Nco2) 0,352В(А+Б) (1-0,03744tk)(2A+B)- (l + Nco 0, 1 (1-0,03744tk) 1-Ncoa) где Р - удельный расход угг лерода анода в кг/кг АИ , Ncoj- содержание СО при работе электролизера в герметичных условиях ед; А,Б,8- содержание СО, СО и N2 в анодных газах при наличии доступа воздуха в электролизер, ед. П(;д ,П(;р - содержание CF4 в условиях герметич. ной работы электролизера при анодном эффекте ед/ К -коэффициент анодного эффекта, шт./сутки;С - продолжительность анодного эффекта, ч. Допустим, что коэффициент вспьшки (анодного эффекта), который показывает число вспьшки в сутки, равняется К, а продолжительность вспышки в часах равняется о ТОГда в интервале времени равном 1 ч относительная п1Л должительность (т.е. время, при котором можно считать,что ванна работает при анодном эффекте) & будет равняться: л 0,0416Dk. Обозначив продолжительность нормального электролизера буквой д1 и зная, что . 1 получим: йЦ 1-0,416 Ck Теперь, для нормального электрол за определим теоретическое часовое количество кислорода, которое, входи в состав СО и СО по формуле, вытек ющей из закона Фарадея: 5,6J 26,840 где и - сила тока электролиза, А. Вследствие обратной реакции электродных продуктов: 2 АЬ + 3 С02 Ае.Оз + 3 СО за один час теряется лт (кг), металла:дт 0,336-10 П (1-) Согласно этой реакции потери кислорода, связанного в С02, соста vS b|:|Mo,336no-3r(iгде; 1 - величина выхода по току в период нормальной работы ванн. Практическое же количество кислорода VQ. выходящего б состав ко нечного анодного газа, будет равня Подставляя соответствзпопр е знат „ ,,,С07 получим: .0 0,2074-10-3 (l Одному кубическому метру анодног - / 11N со 1 газа соответствует ( NCO у л, я кислорода, а Vq количеству кисло рода будет соответствовать количество анодного газа: Vfj 4СО 0,415-10-3 1 - N сог Допустим, что вследствие парази тических процессов (а) частичньй разряд ионов алюминия и натрия на катоде и их окисление на аноде, б) анодное растворение водорода и катодный его разряд, в) электролиз растворенных анодных газов и т.д.) одинаково снижающих анодные и като ные выхода по току (М) не вступи в реакцию с анодными газами 0,337103 iq количество металла Тогда вследствие паразитических процессов и в соответствии с обрат ной реакцией за один час не получитсяSJ - Ь522,4 ю-з, 2 количество кислорода. Согласно обратной реакции потери кислорода, входящие в состав С02, при наличии паразитических лроцессов составляют: & 227 ° Практическое же количество кисорода, согласно уравнению: , .1,5«22,4 ..п 5,610-з .Vo 2/27 26,8 КО,336-10-3 Ь522,4 КО,336ИО-з 1 - (2 + biZ) получится равным: NJg 0,2074-10h Такому количеству кислорода также будет соответствовать: Wco 0.415.10-3... Мсог количество анодного газа. Из этого следует, что общее часовое количество анодного газа не зависит от паразитических процессов. Это значит, что электрохимически недополученное количество кислорода компенсируется тем его эквивалентным количеством, которое не теряется из-за уменьшения величины потерь металла (й12) обусловленной обратной реакцией. Из-за паразитических процессов потери кислорода эквивалентны не (1-) количеству металла,а 1-(2-)-Ь) количеству металла.Так . как уменьшение потерь кислорода равняется количеству недополученного на аноде кислорода (в виде СОл), то величина VQQ .Q оказывается независимой от паразитических процессов. Ясно, что зная часовое количество анодного газа и его состав, легко можно определить и часовой расход углерода анода: 0,415МО 5,6 - - 1+NC02 . Если за одинчас расходуется йР количество углерода, то за время, равное Д1,2 1 - 0,0416lj-k будет расходоваться uPut2 (1 - 0,0416D-k). Определяем часовой расход углеро да анода при работе ванн в режиме анодного эффекта. Как известно при анодном эффекте происходит резкое повышение содержания окиси углерода которое и является основным показателем повьшения расхода анода. Кром этого в анодном газе появляется новый компонент CF. Обозначив концентрации этих компонентов П.С02 Псо чтоПсо- + П и зная, GF4 г СО количество определим часовое анодно го газа. Так при анодном эффекте частична замена разряда ионов кислорода на разрядионов фтора иобразование CFij. в конечном итоге не приводит к изменению теоретического объема газа (при исчезновении каждого грамм-моля кислорода (или С02) обра зуется 1 г-моль четьфехфтористого углерода), то и в этом случае объем газа окажется равным „Т 5,6 Ъ,+ Ср4 2678-ГО-з Вследствие обра;тной реакции элек тродных продуктов 2 Аб + 3 СОд + 3 СО кг метал час теряется за один ла: 0,33640-3:) (1-I2J,) выход по току при вспыш ке, ед. Согласно этой реакции потери кислорода, связанного в СО, составляют H °336.to-3.3( Практическое же количество кислорода (входящего в состав конечно ;го СО2 и СО) и четьфехфтористого углерода окажется равным V -V -лУ ги i 02 Voa+cF4 0 2074 10 Одному кубическому метру анодно газа соответствует ( смеси кислорода и четырехфтористого углерода, а Уо + сГД./ количеству Oj и CF4 будет соответствовать количество анодного гаC0i4 СО + СЦ 0,.CO.CF4 0 510-3. ,ср, , Зная часовое количество анодного газа и его состав, легко можно определит. и часовой расход углерода анода при работе ванн в режиме анодного эффекта.. . 0,415-10 3 Псог-ьПср Бсли за один час расходуется &Р количество углерода, то за время, равное u.ij 0,04162-k будет расходоваться 0,04l6.k 0,445-10з Таким образом, действительный часовой расход углерода анода равняется не величине ьР а сумме +uPbt2 или ьР, (1-0,0416 ) 0,0416Ck-- x 0,41510-5 :. + И- NCO КО,415- 10-3 co. Вследствие пульсирующего выхода анодных газов под корку электролита подсасывается немалое количество воздуха, кислород которого, дополнительно окисляя-углерод анода, меняет расход углерода. Это положение доказано отсутствием азота (наличием равенства Nco -t-Nco и присутствием N,2 (существованием неравенства AtB) в пробах газов, взятых при отсутствии и наличии доступа воздуха под корку электролита.Так как (;Q А)-Б. то ИЗ ЭТОГО СЛВДует, что вследствие подсоса воздуха соотношение COj и СО не изменяется в сторону его повышения (т.е. концентрация COg в газовоздушной смеси не увеличивается). Концентрация COg повысилась бы в случае наличия реакцииI
2СО + Og (воздуха) 2 CO и отсутствия или незначительной ст пени развития вторичного процесс;а COri + С (неполяризованньй) 2 С Высокая же концентрация азота. (В 0,173) свидетельствует о дост большого количества воздуха под ко ку электролита. Отсутствие же следов кислорода в газовоздушной смес является доказательством полного его взаимодействия с углеродом ано и анодными газами. При входе с электролизер воздух вместе с В количеством азота вноси и определенное количество кислород ( Д.о,2 ). Зная .состав воздуха и со держание азота (в) в отобранном объеме анодного газа, получим iVo,. 0. /2 0,79 Согласно приведенной формуле и реакции С + 0 С02 количество вн будет равнятьс образованного СОл кг/моль: г - 0.21В С02 22,4О,79 Если принять, что из со2. количества углекислого газа его количество вступает в реакцию с углеродом, то тогда, количество непрореагировавшего СО, окажется равным со са 0,2Ь.В , 0,79-22,4 . 02 Количество же вновь образованно окиси углерода будет равным А Зная отношение (COj: СО) (-) сос тавим равенство (0.21 В t ) 2Ссо2 0,79-22,4 СОг Из этого равенства получаем С02 О,7922,4 2А+Б В переводе на кубические метры .количества дополнительно образова ных СО- bVco и СОл fri ока и ,жутся равными
8 2.0,266&V
bVco
и
COj
вУ 2-°266( В(А+Б) со, 2-0,266 12А+Б) Как доказано вьш1е, при нормальной работе электролизера часовое количество анодных- газов выражается формулой+ СО 0,415-10-3 При работе алюминиевого электролизера с открытыми огоньками N СО-, + N со Т количество первоначального анодного газа разбавляется В количеством азота n(i(VQ-(-JxVAo ) количеством COg и СО образованных при окислении углерода анода кислородом воздуха. В новой смеси (Nco7 Со) Vcoil количество газа соответствует (А+б), а количеству газа ( N со + N со ) соответствует NCO Отсюда полу-, чаем. XN .1, (А+Б) (2А+Б) л (2А+Б)4-20,266-В(А+Б) Суммарная концентрация COg и СО, образованных вследствие реакции углерода с кислородом воздуха, будет + со U X fsn + U X 20,266В (Ач-Б)г 20,266«В(А+Б) + (2А+Б) Соответствующим образом АХсоя XQQ окажутся равными .у2-0,266БВ (А+Б) ал,-- 2- 0,266-в(А+Б) + (2А+Б) ЛХ - 2-0,266АВ(А+Б) СОл о.п ; 7 ,266 В(А+Б) + (2А+Б) Долевой концентрации | соответствует X со со колиjiecTBo газа, а концентрации йХсол Л.Хсо будет соответствовать дополнительное количество COg и СО, образованных при окислении углерода анода кислородом воздуха. Зная это, получим: 0,22«10-5 ( (UNcbJ Vco .0,22 (2A+B) (l+Ncoa) Ha основании этих данных легко можно определить часовой расход |( углерода, вызванный окисле нием его кислородом воздуха 5Т6. Т2 щТта; -« Если за один час расходуется кол честно углерода, то за время, равно 2 -0,416Jk будет расходоватьсяuPuil -,-.л. X -3 (1-0,04t6i;k) В(А+Б) но,22.10-3 (2А+Б) ( Из этого факта следует независимость соотношения СО и СО, возникших от окисления углерода анода кис лородом воздуха, от состава анодног газа. Кроме этого это означает,что смесь С02 и СО, образованных при окислении углерода анода кисло1 одом воздуха, значительно богаче окисью углерода. На участке входа воздуха под корку электролита вследствие резкого уменьшения скорости перехода анодно образованного СО, создаются условия для более полного протекания реак1щи углерода анода с углекислым газом, образованию за счет кислорода воздуха. Tak как при анодном эффекте условия подсоса воз духа не изменяются, то часовой расх углерода и в этом окажется равным Р -57 °- -°;2Л°втнсо Если за один час расходуется а Р количество углерода, то за время, равное ut, 0,0416Ck будет расходоваться
3
0,0416tkЬР
Ai-;
5.6
1 9-J. in-3 ит HA+I
° (2Ач-Б 1 Нсо.;)
0, Таким образом часовой расход углерода анода, обусловленный под- сосом воздуха, равняется не вели.чина Р а:
,ошг)o.22-io 3 X
определяется по соотношению - 2 . В(А+Б)
3(1 + Nc02) (2А-ьБ)(НМсо„)
1
1
0,0276Ck(
-)
1- -Псо/ ПСР
HN
С02
Эта формула получается при допущении равенства выходов по току при нормальном режиме и при вспьш1ке.
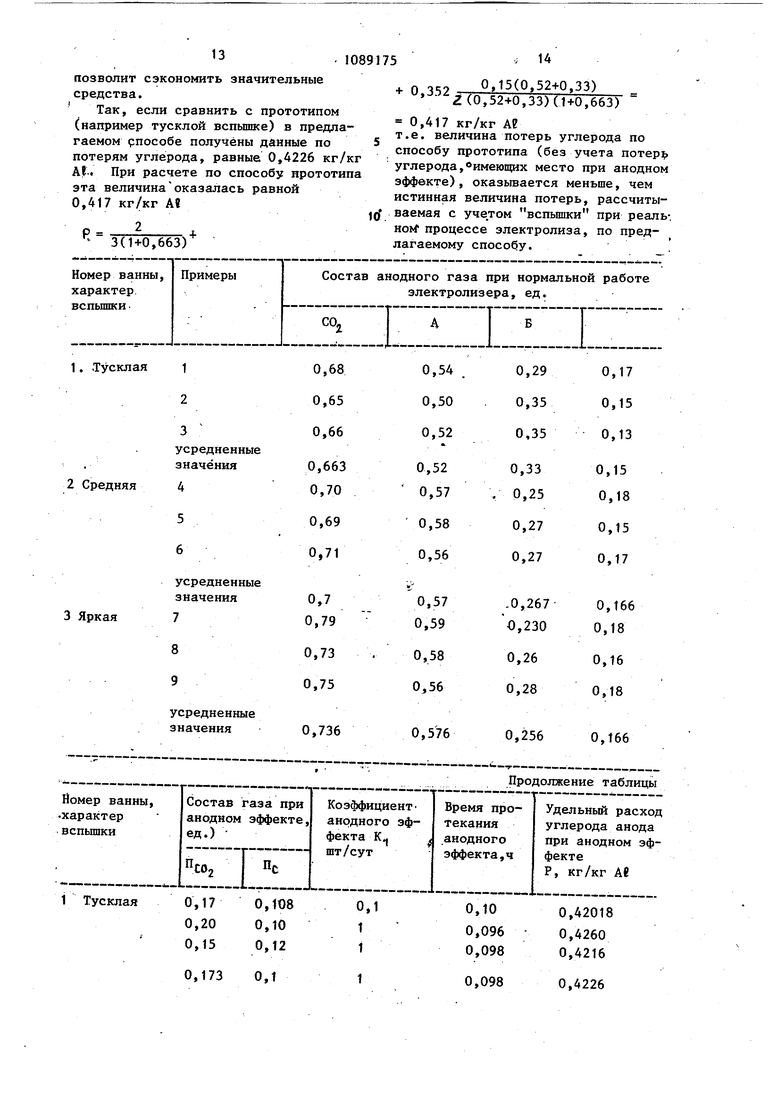
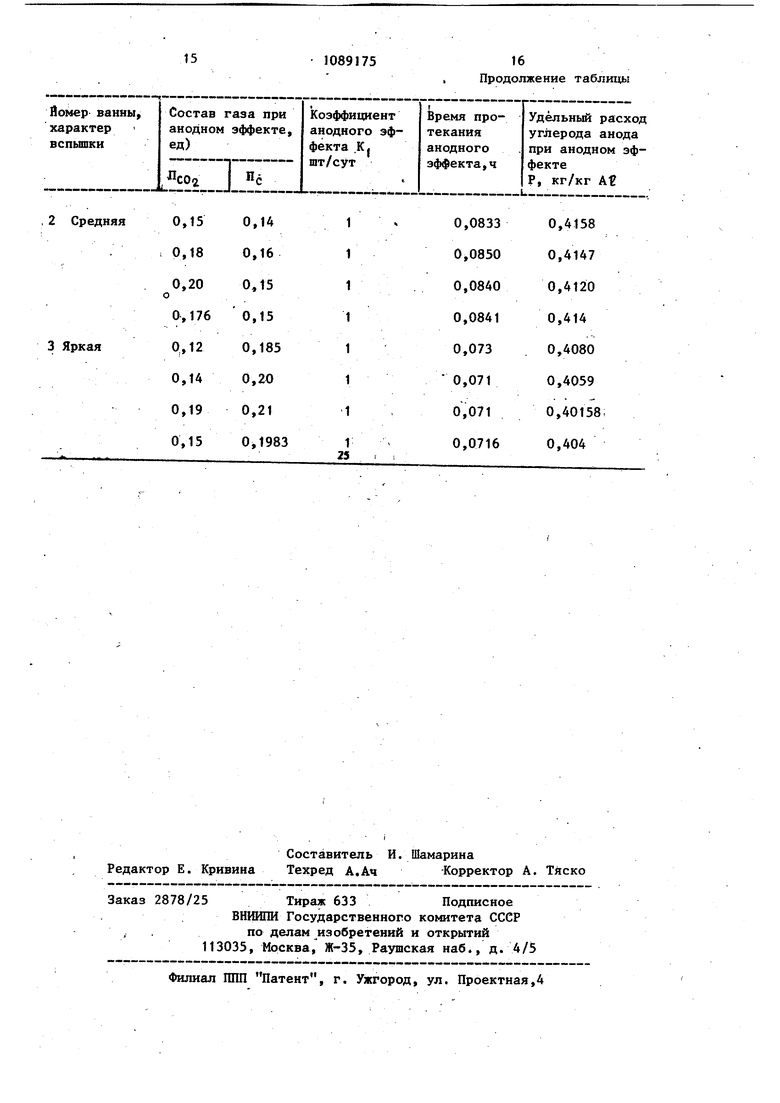
В действительности часовая производительность алюминиевого электролизера равняется сумме количеств (.Н . ) (2A-h6)(ffNcoJ Ар - 3 ,4 ,, 1П-п1 JiAlE} ьРг - 57б-022 10 73 (),) Йбщий часовой расход углерода, ключающий дополнительные потери угерода, связанные с возникновением анодного эффект-а, окажется равным . ЛР йР1+ДР2 КР (t-0,0416tk)x+ 0,.kK ,415 10-.3 гз 2:1 3 (,415И(Г.гггГ п 5,0 Пс02 сР4 -J-.0 22-10-3 .ВО+И 5,6 (l + NCOg) (2А+Б) После соответствующих преобразоаний получим .,, --.0,415 10 l + Ncoa j,o (А-нБ) X о,22-10- Nco,j)(2A+B) -1- 0,041бе.. 110,415.10- К 1+nco2+ncF4 -) 1+Nco При часовой производительности лектролизера, равной п 0,33610 1ч (кг) удельные поери (расход) углерода в кг на кг актическим полученного металла. металла, образованных за время нор мальной работы &i2 m-, 0,33 I,- .3-(1-0,04l62k) и за время, равное iti когда ванна находится на вспьш1ке т2 т2-0,,4(бТ те 2 О.заЪ ,336-fo -0,04-f6x (.х-Н) где 12 -ВЫХОД оо току (в долях еди ницы) во время анодного эффекта. Принимая 1 Г1 находим, что Zk После соответствующих преобразований получаем .tirtg 0.6iO 3tl-0,0416uk(l-k,) , Величина kj определяется по соотношению потерь металла в нормальной работы HV при вспьшке со -строго известной поверхности катодного металла известным методом. Непосредственные замеры, проведенные на промьшшенном электролизере,, -показывают, что среднее значение 1( для нормально работающего электролизера равняется k 0,9. Подставляя значение k в формул дпя т получаем Wg 0,33640-31 :1 (1-0,03744irk) Подставляя значение 1 j г k;, i 0,9 в приведённую выше формулу общего часового расхода углерода анода, по лучаем ,р. 0.45,10-. + 0,04l60k 0,415.10-3 И-Псог-ьПс 1 . 3 -.3 l-tZB (А+Б) 5, (1 + Nco4)(2Ar-B) Определяя удельные потери (расхо углерода в кг на кг фактически полу ченного металла ( Р г« (Г получаем з( 1-0,037441: Ч (I + NCO) + о 352 B(A-t-B) 1-0,03744tK (2A+B)(H-Nce При коэффициенте вспьш1ки, равном нулю (), получаем расчетную формулу прототипа S 2 „.„ В(А-«-Б) Р SXI+NCO) (2А+Б)(1+Мсо2) а при значениях и получаем общеизвестную формулу М.А. Коробог за Р 3TiTN) Известно, что анодные эффекты бывают тусклые, средние и яркие. Поэтому для лучшего понимания данного изобретения приводятся примеры для каждого из случаев. В каждом случае в течение первых десяти минут отбирали пробы анодных газов при работе электролизера в герметичных условиях, т.е. при наличии . одного огонька. В течение вторых десяти минут отбирают пробы анодных газов при доступе воздуха в электролизер, . когда на ванне существует два огонька. Затем отбирают пробы при.анодном эффекте при герметичных условиях работы электролизера. Результаты анализов проб анодных газов и расчетов удельного расхода углерода анода при тусклом, среднем и ярком анодных эффектах приведены в таблице. Использование предлагаемого способа определения удельного расхода углерода анода при анодном эффекте наряду с известным способом определения расхода углерода анода при . нормальных условиях работы электролизера позволяет более точно определить истинный расход углерода в процессе электролизера. Это дает возможность усилить контроль за технологическими параметрами процесса элвkтpanизa и разработать мероприятия по снижению потерь углерода анода. Учитывая большой масштаб производства алюминия и дороговизну углеродистого материала анода, даже небольшое снижение потерь углерода
позволит сэкономить значительные средства.
Так, если сравнить с прототипом (например тусклой вспышке) в предлагаемом рпособе получены данные по потерям углерода, равные 0,4226 кг/кг At.f При расчете по способу прототипа эта величинаоказалась равной 0,417 кг/кг At
3(1-i-0,663)
+ о 3-52 0.15(0,52-ю,33) Z(О,52+0,33)(1+0,663)
0,417 кг/кг лг
т.е. величина потерь углерода по
способу прототипа (без учета потер, углерода,имеющих место при анодном эффекте), оказьтается меньше, чем истинная величина потерь, рассчитываемая с уче.том вспышки при реаль-. Hott процессе электролиза, по предлагаемому способу..





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения удельного расхода углерода анода | 1980 |
|
SU922183A1 |
| Способ определения потерь фтора при электролизе алюминия | 1980 |
|
SU922182A1 |
| Способ определения потерь фтора при электролизе алюминия | 1981 |
|
SU947228A1 |
| Способ определения выхода по току при получении алюминия в электролизере | 1979 |
|
SU933807A1 |
| Способ электролитического получения алюминия в электролизерах с самообжигающимся анодом | 1992 |
|
SU1836495A3 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УДЕЛЬНОГО РАСХОДА АНОДНОЙ МАССЫ | 2002 |
|
RU2281988C2 |
| СПОСОБ ПЕРИОДИЧЕСКОГО КОНТРОЛЯ ПРОЦЕССА | 1967 |
|
SU199417A1 |
| Электролизер для получения алюминия | 1980 |
|
SU943326A1 |
| Способ производства анода для алюминиевого электролизера | 2024 |
|
RU2835295C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОДНОЙ МАССЫ ДЛЯ АЛЮМИНИЕВЫХ ЭЛЕКТРОЛИЗЕРОВ | 1994 |
|
RU2073749C1 |
СПОСОБ ОПРЕДЕЛЕНИЯ УДЕЛЬНОГО РАСХОДА УГЛЕРОДА АНОДА,включающий определение концентрации СО в условиях герметичной рабрты электролизера и концентраций СО, СО и Ng при доступе воздуха в электролизер, о тл и ч ающийс я тем, что, с целью повышения точности измерения расхода.углерода анода, дополнительно определяют концентрации С02 и CF в условиях герметичной работы электролизера при анодном эффекте, а величину удельного расхода определяют, по уравнению . 2 3
0,173 0,1
0,098
0,4226
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Цветные металлы | |||
| Прибор для заливки свинцом стыковых рельсовых зазоров | 1925 |
|
SU1964A1 |
| с | |||
| Способ изготовления звездочек для французской бороны-катка | 1922 |
|
SU46A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ определения удельного расхода углерода анода | 1980 |
|
SU922183A1 |
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
1984-04-30—Публикация
1982-10-18—Подача