ьэ о
Сл Изобретение относится к химическому меднению аысокодисперсных электропроводных материалов (порошков графитов различных марок, порошков каталитически неактивных металлов и т.д.) и может быть использовано в порошковой металлургии, электротехнической, радиотехнической, машиностроительной промышленности. Цель изобретения - снижение электросопротивления медного покрытия. Пример 1. 50 г гидроокиси натрия растворяют в 800 мл дистиллированной воды. После охлаждения раствора до 20°С в него вводят 50 г сорбита. После растворения сорбита к раствору добавляют 50 мл пентагидрата сернокислой меди и 30 мл изопропилового спирта. Обьем раствора доводят дистиллированной водой до 1 л и перемешивают до полного перехода ионов меди в комплексы с сорбитом, о чем свидетельствует растворение осадка гидроокисей меди. Далее в раствор вводят 18.8 г каталитически неактивного порошка никеля. К смеси раствор-порошок никеля после перемешивания в течение 5 мин добавляют 80 мл формалина, в котором предварительно растворяют 0,8 г MgS04 7Н20, что соответствует 1 г MgS04 ТНаО на 1 л формалина. Процесс химического меднения продолжается 35 мин. Порошок полностью покрыт медью. Выпадения меди в объеме растЕюра не наблюдается. Пример 2. 100 г гидроокиси натрия растворяют в 800 мл дистиллированной воды. Поспе охлаждения раствора до в него вводят 70 г оттека - отходов промышленного производства ксилита. После растворения оттека добавляют 8(3 г пентагидрата сернокислой меди и 40 мл изопропилового спирта, и объем раствора доводят дистиллированной водой до 1 л. Раствор перемешивают до полного перехода ионов меди в комплексы с оттеком. Далее в раствор вводят 20 г порошка графита марки ГАК-2. К смеси раствор-графит после перемешивания в течение 7 мин добавляют 110 мл формалина, в котором предварительно растворяют 0,55 г MgChx x&HzO, что соответствует 5 г 6Н20 на 1 л формалина. Процесс химического меднения продолжается 22 мин. Порошок полностью покрыт медью. Выпадения меди в объеме раствора не наблюдается. Пример 2. 150 г гидроокиси натрия растворяют в 800 мл дистиллированной воды. Поспе охлаждения раствора до 20°С в него вводят 90 г ксилита, После растворения ксилита добавляют 120 г пентагидрата сернокислой меди и 50 мл этилового спирта. Объем раствора доводят до 1 л дистиллированной водой. Раствор перемешивают до полного перехода ионов меди в комплексы с ксилитом. Далее в раствор вводят 70 г графита марки ГК-3 и перемешивают смесь в течение 10 мин. К смеси раствор-графит добавляют 150 мл формалина, в котором растворено 1,2 г Мд(К1Оз)2 НаО, что соответствует 8 г Mg(N03)2 N20 на 1 л формалина. Процесс химического меднения продолжается в течение 14 мин. Порошок полностью покрыт медью. Выпадения меди в объеме раствора не наблюдается. Пример 4. Процесс химического меднения осуществляют по примеру 2, но 1 ЛдС12 6Н20 берут 0,7 г на 1 л формалина. Процесс химического меднения продолжается в течение 28 мин. Порошок медью не покрыт - большая часть меди выделяется в объеме раствора. Пример 5. Процесс химического меднения осуществляют по примеру 2, но 6H2Q берут 10 г на 1 л формалина. Процесс химического меднения осуществляют в течение 19 мин, но выпавшая в осадок часть гидроокиси магния, резко увеличивает время фильтрования омедненного порошка, а включение гидроокиси магния в состав осадка меди повышает электросопротивление омедненного графита. Свойства порошков, омедненных по примерам 1-5, представлены в табл.1. Таким образом, из данных тзбл.1 видно, что поставленная цель - снижение электросопротивления медного покрытия - достигается. Описанный 8 примерах 1-5 порядок проведения процесса необходим по следующим причинам. Введение формалина в раствор химического меднения без предварительного внесения порошка вызывает разложение раствора с выпадением порошка меди в его объеме. Если в раствор химического меднения внести сначала соль магния, а затем порошок и формалин, то порошок не покрывается полностью и плохо фильтруется в результате выпадения в растворе химического меднения гидроокиси магния. Содержание соли магния в формалине менее 1 г/л приводит к непокрытию частиц медью и к выпадению меди в объеме раствора. Содержание соли магния в формалине свыше 8 г/л приводит к выпадению части ионое магния в растворе химического меднения в виде гидроокиси, что увеличивает электросопротивление покрытия и затрудняет процесс фильтрования омедненного порошка.
В качестве соли магния можно использовать MgCl26H20-MgS047H20, Мд(ЫОз)2х
Х6Н20.
Введение соли магния в формалин в процессе химического меднения снижает содержание СогО в покрытии и тем самым уменьшает его сопротивление.
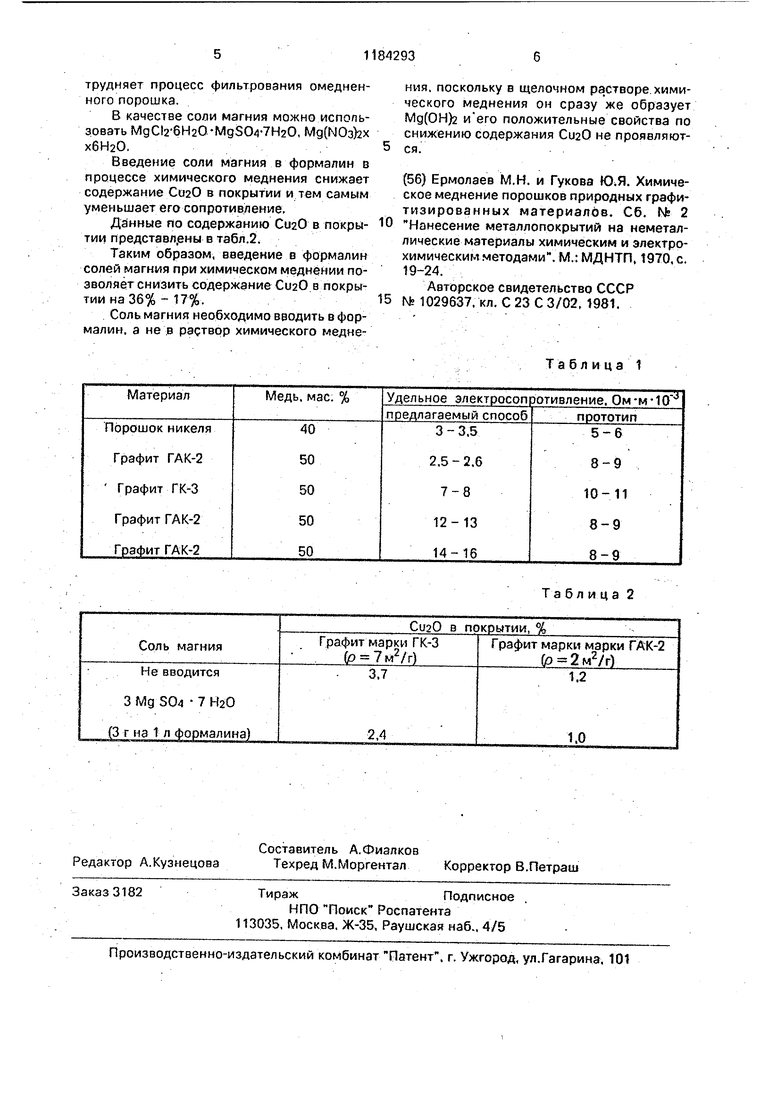
Данные nto содержанию СиаО в покрытии представл.ены в табл.2.
Таким образом, введение в формалин солей магния при химическом меднении позволяет снизить содержание СигО в покрытии на 36% - 17%.
Соль магния необходимо вводить в формалин, а не .в раствор химического меднения, поскольку в щелочном растворе, химического меднения он сразу же образует Мд(ОН)2 иего положительные свойства по снижению содержания СиаО не проявляются.
(56) Ермолаев М.Н. и Гукова Ю.Я. Химическое меднение порошков природных графитизированных материалов. Сб. № 2
Нанесение металлопокрытий на неметаллические материалы химическим и электрохимическим методами. М.: МДНТП, 1970, с. 19-24.
Авторское свидетельство СССР
№ 1029637. кл, С 23 С 3/02, 1981.
Таблица 1
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ меднения порошкообразных материалов | 1985 |
|
SU1279747A1 |
| Способ получения электропроводящегопОлиКАпРОАМидА | 1978 |
|
SU794045A1 |
| Способ получения медных покрытий на неметаллических материалах | 1981 |
|
SU1029637A1 |
| СПОСОБ МЕДНЕНИЯ ЛАВСАНОВЫХ НИТЕЙ С НЕДЕСТРУКТИРУЮЩЕЙ АКТИВАЦИЕЙ ПОВЕРХНОСТИ | 2018 |
|
RU2682577C1 |
| СПОСОБ МЕДНЕНИЯ ЛАВСАНОВЫХ НИТЕЙ | 2018 |
|
RU2701829C1 |
| РАСТВОР ХИМИЧЕСКОГО МЕДНЕНИЯ | 1992 |
|
RU2069457C1 |
| Раствор для химического меднения диэлектриков | 1973 |
|
SU497359A1 |
| ВЫСОКОЧАСТОТНЫЙ ДИЭЛЕКТРИЧЕСКИЙ РЕЗОНАТОР И РАСТВОР ДЛЯ ЕГО ХИМИЧЕСКОГО МЕДНЕНИЯ | 1992 |
|
RU2091926C1 |
| Способ химического меднения углеродных материалов | 1988 |
|
SU1604862A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОЙ МЕДИ | 1990 |
|
RU1777289C |

Та бл и ц а 2
| Ермодаев М.Н, и Гукова Ю.Я | |||
| Химическое меднение порошков природных графитизированных материалов | |||
| Сб | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ получения медных покрытий на неметаллических материалах | 1981 |
|
SU1029637A1 |
| кл, С 23 С 3/02.1981. | |||
Авторы
Даты
1993-10-15—Публикация
1984-01-05—Подача