Изобретение относится к усовершенствованному способу получения известных производных 17 α-гидрокси-3-оксоандрост- 4-ен-17 β-карбоновой кислоты общей формулы I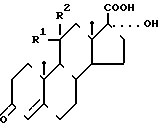
 где R1, R2 - атомы водорода (Iа), или R1, R2 - вместе означают оксогруппу (Iб).
где R1, R2 - атомы водорода (Iа), или R1, R2 - вместе означают оксогруппу (Iб).
Соединения общей формулы I обладают противовоспалительной активностью при местном применении и, кроме того, могут известными способами превращены в 17 α-гидроксиандростан-17 β-карбоновой кислоты, замещенные в положениях 6, 9, 11, 16, которые обладают высокой противовоспалительной активностью и сильным тимолитическим действием.
Целью изобретения является упрощение процесса за счет сокращения числа стадий и повышение выхода целевых продуктов.
Выход для соединения Ia составляет 66%, считая на соединение IIа, а соединения Iб - 70%, считая на соединение IIб.
Исходные соединения 17 α-гидрокси-17 β -цианоандрост-4-ен-3-он(IIa) и 17 α -гидрокси-17 β-цианоандрост-4- ен-3,11-дион(IIб) являются доступными, их получают в одну стадию с выходом 85-90% из продуктов микробиологического окисления ситостерина.
П р и м е р 1. Получение 17 α-гидрокси-3-оксоандрост- 4-ен-17 β-карбоновой кислоты (Iа) (с выделением натриевой соли Ia).
5 г (0,016 моль) 17 α-гидрокси-17 β -цианандрост-4-ен- 3-она(IIa) кипятят в 300 мл смеси конц.соляной и уксусной (Х4) кислот (1:1) по объему в течение 12-14 ч. Раствор упаривают до 25 мл, разбавляют 100 мл воды и экстрагируют 30 мл хлороформа, промывают водой до нейтральной реакции. Экстракт обрабатывают углем, уголь отфильтровывают и к экстракту при перемешивании прибавляют 10 мл 10% раствора соды. Перемешивание продолжают при комнатной температуре в течение 1 ч. Выпавший осадок отфильтровывают, промывают 10 мл хлороформа, сушат.
Получают 4,05 г (71,7%) натриевой соли 17 α-гидрокси-3- оксоандрост-4-ен-17 β -карбоновой кислоты в виде белого кристаллического порошка, растворимого в воде при нагревании, нерастворимого в органических растворителях хлороформе, бензоле, эфире т.пл. > 300оС.
По данным ТСХ содержит 1,5% посторонних стероидов.
ИК-спектр, см-1: 3500-3300, 1690-1650.
4,05 г натриевой соли кислоты Iа растворяют в 50 мл воды при нагревании (70-80оС), добавляют 10 мл соляной кислоты (рН 2), выпавший осадок отфильтровывают, промывают водой до нейтральной среды, сушат и растирают с 10 мл эфира.
Получают 3,5 г (92,5%) 17 α-гидрокси-3-оксоандрост-4- ен-17 β -карбоновой кислоты; т. пл. 233-235оС (по литературным данным; т.пл. 233-234оС.).
По данным ТСХ содержит 1% андрост-4-ен-3,17-диона и 2% 3-оксоандроста-4,16-диен-17 β -карбоновой кислоты.
М+ 332.
ИК-спектр, см-1: 3490, 3260, 1710, 1640.
ПМР-спектр, м.д.: 0,83,1,2,3,5,5,76, 7,27.
Данные ИК, ПМР, масс-спектров в литературе не приведены.
Выход Ia, считая на исходный IIa, составляет 66%.
П р и м е р 2. Получение 17 α-гидрокси-3-оксоандрост-4- ен-17 β -карбоновой кислоты (Iа) (без выделения натриевой соли Iа).
2 г (0,006 моль) 17 α-гидрокси-17 β -цианоандрост-4-ен-3- она(IIа) кипятят в 120 мл смеси соляной и уксусной кислот (1:1) по объему в течение 12-14 ч. Раствор упаривают до 10 мл, разбавляют 20 мл воды, экстрагируют 10 мл хлороформа. Экстракт промывают водой до нейтральной среды, обрабатывают углем, уголь отфильтровывают и раствор экстрагируют 10%-ным раствором соды (50 мл х 3) при 40оС. К охлажденному раствору прибавляют 3 мл соляной кислоты и обрабатывают, как указано в примере 1.
Получают 1,4 г (66,5%) 17 α-гидрокси-3-оксоандрост-4 -ен-17 β -карбоновой кислоты (Iа); т. пл. 232-234оС.
П р и м е р 3. Получение 17 α-гидрокси-3,11-диоксоандрост -4-ен-17 β -карбоновой кислоты (Iб).
1 г (0,003 моль) 17 α-гидрокси-17 β -цианоандрост-4-ен-3,11-диона (IIб) кипятят 14 ч в 40 мл смеси соляной и уксусной кислот (1:1) по объему, упаривают раствор до 5 мл и экстрагируют 10 мл хлороформа. Экстракт промывают водой до нейтральной среды, экстрагируют 10%-ным водным раствором воды (10 мл х 3). Содовый раствор подкисляют соляной кислотой до рН 2, экстрагируют хлороформом (2 х 10 мл) и упаривают досуха.
Получают 0,83 г (79%) соединения формулы Iб, считая на IIб, который по данным ТСХ содержит 1,5% посторонних стероидов, из них 0,5е% исходного IIб. Осадок растирают с 5 мл эфира, отфильтровывают, промывают 3 мл эфира.
Получают 0,74 г 17 α-гидрокси-3,11-диоксоандрост-4-ен-17 β-карбоновой кислоты (по данным ТСХ 0,5% посторонних стероидов); т.пл. 271-273оС (по литературным данным 273-277оС).
Масс-спектр: М+ 346.
ИК-спектр, см-1: 3480, 1730, 1705, 1640.
ПМР-спектр, м.д.: 0,71, 1,43, 2,15, 3,3, 5,71.
Данные ИК, ПМР, масс-спектров в литературе не приведены.
Выход 70,4%, считая на исходное IIб.
П р и м е р 4. Получение 17 α-гидрокси-3-оксоандрост-4-ен-17 β-карбоновой кислоты (Iа).
1,35 г (0,004 моль) амида 17 α-гидрокси-3-оксоандрост-4-ен-17 β-карбоновой кислоты кипятят 6 ч в 80 мл смеси соляной и уксусной кислот (1:1) по объему и далее обрабатывают, как в примере 1.
Получают 1,32 г натриевой соли кислоты (Iа) с выходом 91,5%, считая на исходный амид.
Кислоту (Iа) получают согласно примеру 1.
Получают 1,12 г кислоты (Iа), т.пл. 232-234оС. Выход составляет 83%, считая на амид.
П р и м е р 5. Объемное соотношение НСl:CH3COOH 0,5:1.
1 г (0,003 моль) 17 α-гидрокси-17 β -цианандрост-4-ен-3-она (IIа) кипятят в 45 мл смеси концентрированной соляной и уксусной кислот (1:2) в течение 12 ч. После обработки, описанной в примере 1, получают 0,65 г (57,5%) натриевой соли 17α -гидрокси-3-оксоандрост- 4-ен-17 β-карбоновой кислоты, из которой указанным способом получают 0,64 г кислоты (53%), от теор., считая на IIа).
П р и м е р 6. Объемное соотношение НСl:CH3COOH 1,2:1.
0,55 г (0,00165 моль) 17 α-гидрокси-17 β-цианандрост-4-ен-3-она (IIа) кипятят в 11 мл смеси концентрированной соляной и уксусной кислот (1,2:1) в течение 10 ч.
После обработки описанной в примере 1, получают 0,38 г (61,5%) натриевой соли Iа и из нее 0,34 г (56,8% от теор. в пересчете на IIа) 17 α-гидрокси-3-оксоандрост-4-ен-17 β-карбоновой кислоты (Iа).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КОРТИКОСТЕРОИДОВ | 1999 |
|
RU2156256C1 |
| СПОСОБ ПОЛУЧЕНИЯ 17β-ГИДРОКСИ-11β-[4-(ДИМЕТИЛАМИНО)ФЕНИЛ]-17α-(ПРОП-1-ИНИЛ)-ЭСТРА-4,9 -ДИЕН-3-ОНА | 2000 |
|
RU2165938C1 |
| СПОСОБ ПОЛУЧЕНИЯ 11БЕТА, 17АЛЬФА, 21-ТРИГИДРОКСИ-16АЛЬФА-МЕТИЛ-9АЛЬФА-ФТОРПРЕГНА-1,4-ДИЕН-3,20-ДИОНА (ДЕКСАМЕТАЗОНА) ИЗ ФИТОСТЕРИНА | 2013 |
|
RU2532902C1 |
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ 3β-АЦЕТОКСИ-17α-ГИДРОПЕРОКСИ-16α-МЕТИЛПРЕГНАНОВ ИЗ Δ-20-КЕТОСТЕРОИДОВ И СПОСОБ ПОЛУЧЕНИЯ 3β-АЦЕТОКСИ-17α-ГИДРОКСИ-16α-МЕТИЛПРЕГНАНОВ С ИСПОЛЬЗОВАНИЕМ 3β-АЦЕТОКСИ-17α-ГИДРОПЕРОКСИ-16α-МЕТИЛПРЕГНАНОВ | 2009 |
|
RU2418805C1 |
| СПОСОБ ПОЛУЧЕНИЯ 17-(3-ГИДРОКСИПРОПИЛ)-17-ГИДРОКСИСТЕРОИДОВ | 2008 |
|
RU2466137C2 |
| ПРОИЗВОДНЫЕ АНДРОСТЕНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2194053C2 |
| СПОСОБ ПОЛУЧЕНИЯ О-АРИЛГЛИКОЛЕВЫХ КИСЛОТ | 2002 |
|
RU2214995C1 |
| СПОСОБ ЭТЕРИФИКАЦИИ ТИОКАРБОНОВОЙ КИСЛОТЫ | 2004 |
|
RU2351605C2 |
| 3-ЦИАНОАНДРОСТА-3,5-ДИЕН-1717β-КАРБОНОВАЯ КИСЛОТА В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА, СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЯ | 1993 |
|
RU2114861C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ОКСОСПИРО- 17β -ОКСИРАНИЛАНДРОСТ-5-ЕНА | 1987 |
|
RU1438188C |
Изобретение относится к стероидным соединениям, в частности к производным 17α -гидрокси-3-оксоандрост-4-ен- 17β -карбоновых кислот формулы 1 (см. рисунок), где R1 и R2 - водород, или вместе означают оксогруппу, применяющихся в медицине как противовоспалительные средства. Для упрощения процесса и повышения выхода 1 в способе используют другое исходное, которое превращают в целевой продукт. Синтез ведут из 17α -гидрокси- 17β -циано-3-оксоандрост-4-ена обработкой смесью концентрированных HCl и CH3 COOH, взятых в объемном соотношении, равном (0,5 - 1,2) : 1 при кипячении реакционной массы с последующим выделением 1 в виде натриевой соли. Способ обеспечивает повышение выхода 1 до 66 - 70% и сокращение стадий процесса с 5 до 2.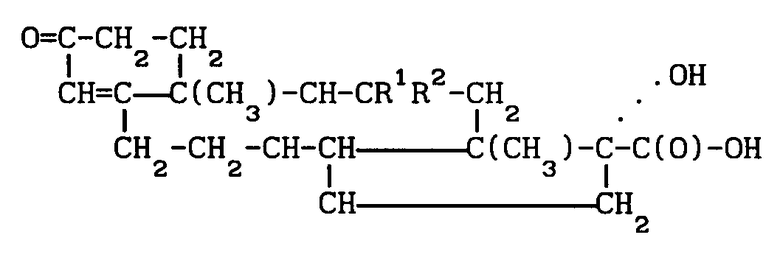
СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 17α -ГИДРОКСИ-3-ОКСОАНДРОСТ-4-ЕН- 17β -КАРБОНОВЫХ КИСЛОТ общей формулы 1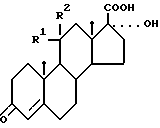
где R1, R2 - атомы водорода (1а) или вместе означают оксогруппу (1б), исходя из 17α - гидрокси- 17β -циано-3-оксоандрост-4-ена общей формулы II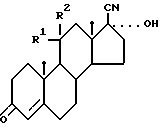
где R1 и R2 имеют вышеуказанные значения,
отличающийся тем, что, с целью упрощения процесса и повышения выхода целевых продуктов, соединенные общей формулы II обрабатывают смесью концентрированной соляной и уксусной кислот, взятых в объемном соотношении (0,5-1,2) : 1, при кипячении реакционной массы и целевой продукт выделяют через соответствующую натриевую соль.
| Радиомаяк с двойной и тройной модуляцией | 1934 |
|
SU42606A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-03-20—Публикация
1985-05-27—Подача