Изобретение относится к способам подготовки воды для нужд теплоэнергетики, а именно к способам получения обессоленной воды для электрических станпдй.
Цель Изобретения - уменьшение количества образующихся в процессе обессоливания сточных вод и снижение расхода реагентов при сохранении высокой степени обессоливания воды.
Исходную природную воду подвергают известкованию, коагуляции и осветлению, после чего нейтрализуют угольной кислотой и подают на аниокирование ка
слабоосновном анионите в НСО -форме. После повторного известкования и осветления воды ее подвергают катиони- рованию на слабокислотном катионите регенерируемом угольной кислотой,, и декарбонизируют. Содержащий бикар- бонат натрия раствор после регенерации катионита используют для регенерации анионита. При необходимости глубокого обескремнивания воды, после декарбонизации ее дополнительно подвергают анионированию на высоко- :основном анионите, регенерируемом ед- :ким натром, а отработанный регенераtC
i
циоиньй раствор присоеллп;яют к мсхо; ной воде.
Иейтрс 1лиза1щя осветлен}юй водь: угольной кислотой с последуклцга ее аннонированием на сЛабоосновном ани- оните, регенер -груемом бякарб(11{атом натрия, обеспечивает перевод всех анионов, оставшихся в воде после из- весткования, в бикарбонсчты, что позволяет провести повторное известкование, при котором из воды выводятся в осадок оставшиеся соединения каль- 1ЩЯО В известном способе эти соединения задерживаются катионитом,, после регенерации которого сильными минеральными кислотами образуются сточные воды, В воде после повторного известкования и осветлен.ия остается практически только бикарбонат натрия который задерживается на катио}гате и после регенерации угольной кислотой выделяется в виде более концентррованного раствора, используемого дл регенерации анионита. В результате исключается образование сточньк вод (при регенера11;ии катионита), а также использование дорогих и агрессивных реагентов (минеральные к слоты щелочь),для регенерАпзяи ионитов,
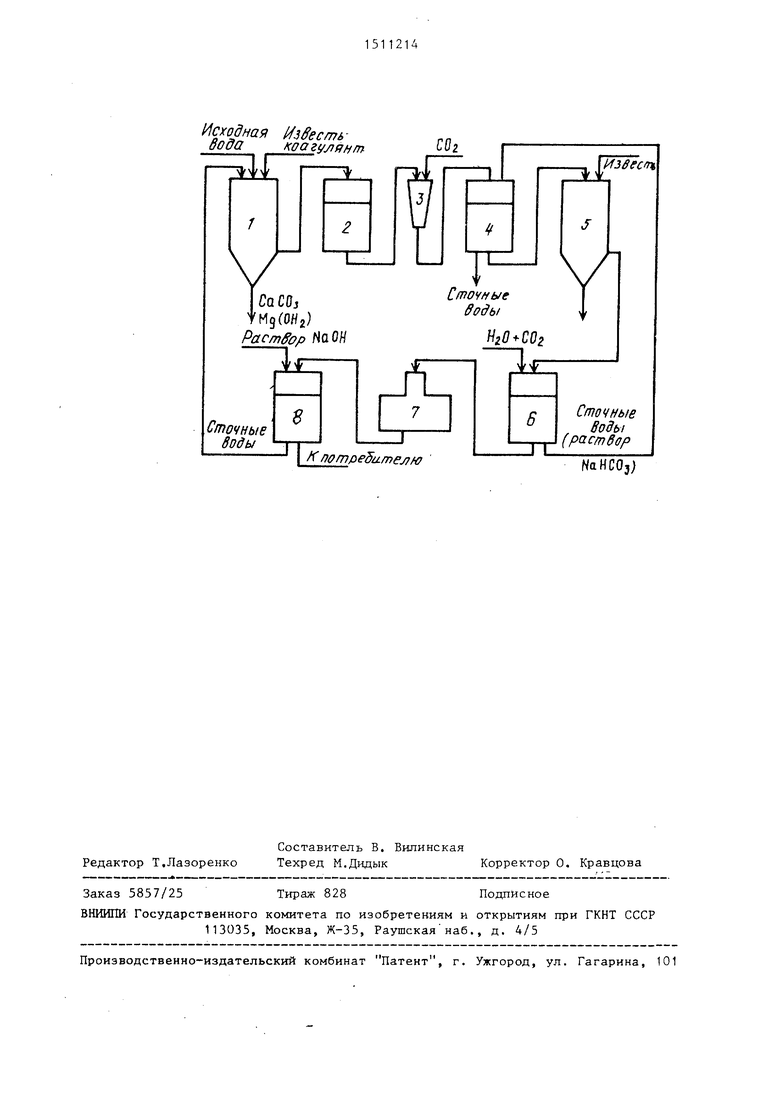
На чертеже представлена схема тановки для реализшщи претщагаено- го способа.
Установка содержит еккость 1 ;1ля известкования и коагулящги исходной воды, механический фильтт) 2 для ее осветления на предварительной ступени очистки, карбонизатор 3, анионит- ный фильтр А со слабоосновным аниони том в HCOj-форме, емкость 5 для повторного известкования и осветления воды, катионитный фильтт 6 со слабокислотным катионитом в Н -формеj де- карбонизатор 7, анионитньш фильтр 8 с высокоосновным ан онитом в ОН -фор ме.
Способ реализуют образом.
Исходную воду подвергают известкованию и коагуляции путем добавления в емкость 1 извести и солей железа или алюминия. При этом происходит удаление в осадок всего магния в виде гидроокиси, части кальция в виде карбоната, а также кремниевой кислоты и органических примесей, соосаждающихся с гидроксидом магния и коагулянтом. Этот oca;i;oK сбрасывают в отходы. Основные реакции, про12U
Г(ка о|| ие что; стади в i-iosiiiOH форме),, быть onHcaifhi следующи- ai У }а;1 еииями:
+ Oil
4,0,
с; а
- +
.
bfofOH) i
0
Иззестковаиную ноду пропускают через мехаш1ческие (осветлительные) фильтры 2 и подвергают нейтрализацией тлекислотой дымовых газов в карбо- низаторе 3, При нейтрализации остав- пиеся в воде известь и карбонат каль- 1ЩЯ переводятся в бикарбонат ггялыц я, концентрап 1я которого (остаточная щелочность) в зависимости от условий известкования и состава исходной воды не превышает 0,5-1,0 мг-экв/л:
СаСО , + С05 + Са(ИСО, ) 25Ca(OH),. + 200,, Ca(HCOj).,
0
Нейтралияа:11;ия воды гюсле известкования необходима потомл 5 что она позволяет исключить возможность образования осадка карбоната кальция при акионировапии, производимом на следу- щей стадии обработки в анионитном фильтре ч, заполнет{ -1ом слабоосновным аш-юпитом в нею -форме „ К результате алЧионированяя присутств топще в исходной анионь сильных кислот (хло- ppvV -s сульфат;.) заменяются на бикарбонат м:
АнНСО} + С1 АнС1 + НСО:, АнНСО, + Ан80 + 2НСО:
5
0
5
Солесодержание анионированнои воды определяется присутствием в ней бикарбоната натрия в количестве, эквивалентном концентрации натрия в исходной воде, и.бикарбоната кальция, концентрация которого эквивалентна постоянной некарбонатной жесткости исходной воды и оста- Тчочной щелочности посгсе известкова- Н.ЧЯ, Регенерап те истощенного анионита ведут раствором бикарбоната натрия 5 полу-ченным на одной из послед У5шщх стадий при регенерации катионита „ Количество бикарбоната натрия я растворе после регенерации катионита определяется концентрацией натрия и исходной воде. В то же время необ51
ходлмое для рег енсрации аниоютта количество NaHCO с учетом запаса долно быть примерно вдвое больше сумманой концентрации в исходной воде анионов сильных кислот. Поэтом., если в исходной воде имеет место соотношение , необходимо добавить соответствуюгцее колш1ество NaHCOj к раствору д/1я регенерации анионита. При этом следует иметь ввиду, что концентра11;ия натрия в воде перед обессоливанием в том случа если в нее добавляется отработанный регенерахщонный раствор после высо- коосновного анионита, используемого для глубокого обескремнивання, может выше, чем в исходной воде,
На следующей стадии обработки анионированную воду подвергают пов- торному известкованию, при котором бикарбонат кальция, образовавшийся на стадиях нейтрализации угольной кислотой и анионирования переводится в CaCOj, которьй выпадает в оса- док и сбрасывается в отходы без образования сточных вод. В результате в обработанной воде остается 1юль- ко гидроксид натрия и остаточное количество карбоната и гидроксида каль ция (также как после первой стадии известкования) NaHCOj + Са(ОН)2. NaOH + СаСО +
Ca(HCOj)2.+ Са(ОН)2 2СаСО +
Нейтрализации воды после второго известкования не требуется, так как опасность образования осадка СаСОз на следующей стадии отсутствует.
Вода после повторного известкова- ния в осветлителе 5 поступает на фильтр 6, заполненный слабокислотным катионитом в Н -форме, регенерируемым раствором угольной кислоты, также полученной из дымовых газов.
НКат + NaOH МаКат +
NaKaT + + СО НКат + NaHCO,,
К полученному после регенерации катионита раствору бикарбоната натрия добавляют, если необходимо, еще некоторое количество этого реагента и используют для регенерации анионита.
Воду после Н-катионирования подвергают декарбонизации (удалению свободной угольной кислоты) в обыч
- 10 15
20 25 30
40 дз
35
0
5
146
ном декарбонияаторе 7. Допустимо /также удаление СО. вместе с раство- ренньп в воде кислородом при обычной термической деаэрации.
При обессоливан1ш чистых природных вод, не требуюп1гос предварительного известкования, коагулятщи и осветления, предлагаемьш способ может быть начат сразу по стадии ионирова- ния (в данном НСО -анионирова- ния). При необходимости глубокого обескремнивания воды осуществляют ее обработку в анионитном фильтре 8, заполненном высокоосновным аниони- том в ОН -форме, регенерируемым едким натром. Однако, если в известном способе обессоливания отработанный регенерационный раствор целиком направляется в сточные воды, то в предлагаемом способе этот раствор присоединяют к исходной воде. Содержащаяся в нем кремниевая кислота удаляется при предварительном известковании, а гидроксид натрий в итоге в виде бикарбоната попадает в раствор после регенерации Н-катионита и снижает количество NaHCO, которое необходимо добавить в раствор для регенерации анионита. Одновременно попадание в исходную воду гидроксида натрия позволяет снизить (на эквивалентное количество) дозу извести для известкования.
Пример 1. Обессоливание воды проводят на лабораторной установке о Солесодержание исходной воды характеризуется след тацими показателями, мг-экв/л:
Жесткость (содержание
Р1елочность (содержание НСОр5 Содержание магния 4 Содержание натрия 3 Сумма хлоридов и сульфатов 8
Исходную воду подвергают известкованию с расходом извести на первой стадии известкования 5,5 мг-экв/л. Воду после фильтрования нейтрализуют угольной кислотой пропусканием из баллона до рН 6,5-7,0. После нейтрализации воду пропускают через фильтр, заполненный О,Л л слабоосновного анионита в НСО -форме, отрегенериро- ванного раствором бикарбоната натрия. К моменту истощения фильтра бьио
1
nponyineno Ю л исходной йоды. Обтаем направленного в сто пгые води регене- ранд онного раствора (без отмывочных вод) составляет 1,5 л. В аниоршрован ной воде в среднем содержится 8 мг-экв/л бикарбонатов натрия и кальция. Расход извести на второй стадии известкования составляет 8,5 мг экв/л, В воде после извест- кования и фильтрования содержится 4 мг-экв/л гидроксида натрия и 0,5 мг-экв/л ги/фоксида и карбоната кальи я. После катионирования на катионите, регенерируемом раствором угольной кислоты, жесткость обработанной воды не преньтает 10 мкг-экв содержание натрия менее 1 мг/л. В р генерационном растворе (1 л) содержится около 8 г бикарбоната натрия, В этот раствор добавляют еще 37 г NaHCOj и используют для регенерации анионита.
Количество сточных вод, ньсх при обессоливании того же количества воды известньм способом составляет А л.
Пример 2, Обессоливлиие пр водят, как описано в прютере 1, но
в качестве дополнительной стадии применяют глубокое обескремнивание воды на высокоосновном анионите, регенерируемом гидроксидом натрия. Получены аналогичные результаты по количеству сточных вод (1,5 л), ю в раствор д/гя регенерации анионита бикарбонат натрия не добавляют. При глубоком обескремнивании воды, обессоленной способом, выбранном в качесве прототипа, кол1тчество сточных вод возрастает до 6,5 л, что составляет 30% от расхода исходной воды,
Предлагаемый способ позволяет з 3-А раза снизить количество образу- кщихся в процессе обессолива1тик сточ- ных вод и исключить применение /тля
8
регепет) ионито дороп-гх и серной или соляной 1цслоть и гидхюокиси натрия, заменив их дегле- вой углекислотойi, полл аемой из дымс)- вых газов, и бикарбонатом натрия, основное количество которого возьшкает в процессе обессол 1вания в качестве побочного продукта.
Формула изобретения
1, Способ обессоливания природных вод, включающж ее известкование, коагулятщю, осветление, анионирование и катионирование с регенерап ей иони- тов, декарбонизацию, о т л и ч а кг- щ и и с я тем, что, с целью меньше- ния количества образующихся в процессе обессоливания сточных вод и снижения расхода реагентов при сохранении высокой степени обессоливания воды, после осветления обрабатываемую воду нейтрализуют угольной кислотой и подвергают сначала анионированию на слабоосновном анионите в НСО -Лорме, а затем повторному известкованию и ос- ветлсмшю с последующим катионировани- ем водгы на слабо1сислотном катионите в Н -форме; 5 регенерируемом угольной кислотой, я декарбонизап;ии, при этом отработанный раствор после регене- рап;ии катионита используют для регенерации слабоосновного анионита.
2о Способ по п. 1, о т л и ч а- ю a и и с я тем, что при необходимости глубокого обескремнивания при- ;зод«ой воды после декарбонизащи во- пу дополнительно подвергают аниониро- ваншо на высокоосновном аниог-гите в ОН -форме, регенерируемом гидроксидом натрия, а отработанны регенера- ;ионньй раствор направляют в исходную воду.
Исходная Изеест&- Вода / оагулянт
Jii.
CaCOj MgfOWz) Pacmffop Na OW
Сточные воды
/f f)ompedii.
C/noyffb/e воды
Сточные
Воды (растбор
NaHCOj)



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ глубокого ионообменного обессоливания воды | 1989 |
|
SU1682322A1 |
| Способ глубокого химобессоливанияВОды | 1979 |
|
SU812726A1 |
| СПОСОБ ОБЕССОЛИВАНИЯ ВОДЫ | 1991 |
|
RU2072325C1 |
| СПОСОБ ОБЕССОЛИВАНИЯ ВОДЫ | 1991 |
|
RU2072326C1 |
| Способ химического обессоливания воды | 1988 |
|
SU1703622A1 |
| Способ опреснения воды (варианты) | 2017 |
|
RU2655995C1 |
| Способ водоподготовки | 1991 |
|
SU1830052A3 |
| СПОСОБ ОБРАБОТКИ ВОДЫ | 1994 |
|
RU2089510C1 |
| СПОСОБ ГЛУБОКОГО ОБЕССОЛИВАНИЯ ВОДЫ | 2009 |
|
RU2411189C1 |
| СПОСОБ ОБЕССОЛИВАНИЯ ВОДЫ | 1991 |
|
RU2036160C1 |
Изобретение относится к способам подготовки воды для нужд теплоэнергетики. Цель изобретения - уменьшение количества образующихся в процессе обессоливания сточных вод и снижение расхода реагентов при сохранении высокой степени обессоливания воды. Способ включает обработку воды путем известкования, коагуляции и осветления воды, затем нейтрализации угольной кислотой, анионирования на слабоосновном анионите в HCO3 - форме, повторного известкования и осветления с последующим катионированием на слабокислотном катионите в H+ - форме, регенерируемом угольной кислотой и использование отработанного после регенерации катионита раствора для регенерации слабоосновного анионита. При необходимости глубокого обескремнивания воды после декарбонизации воду дополнительно подвергают анионированию на высокоосновном анионите в OH- форме, регенерируемом гидроксидом натрия, а отработанный регенерационный раствор направляют в исходную воду. 1 з.п. ф-лы, 1 ил.

| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Голубцева, Энергия, 1966, с | |||
| Ручная тележка для реклам | 1923 |
|
SU407A1 |
Авторы
Даты
1989-09-30—Публикация
1987-10-22—Подача