Изобретение относится к способу получения п-замещенных α-феноксипропионовой кислоты формулы I
R - O  O
O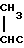 OOH ,
OOH ,
где R 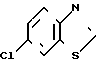 C- ,
C- , 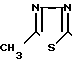 ,
,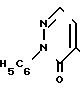 которые могут найти применение в качестве промежуточных продуктов в синтезе гербицидов.
которые могут найти применение в качестве промежуточных продуктов в синтезе гербицидов.
Целью предлагаемого изобретения является упрощение технологии процесса.
П р и м е р 1. 20,4 г (0,1 моль) 2,6-дихлорбензотиазола в 58,1 мл диоксана смешивают с 18,2 г (0,1 моль) параоксифеноксипропионовой кислоты и 11,2 г (0,2 моль) гидроксида калия в 120 мл воды. Массовое соотношение диоксан-вода 1: 2. Реакционную массу нагревают 6 ч с перемешиванием при температуре кипения (87оС), после этого обратный холодильник заменяют на прямой и отгоняют азеотрон диоксан-вода до тех пор, пока температура в парах не поднимется до 100оС. Отогнанный азеотрон без очистки используется для проведения следующего синтеза. Кубовый остаток охлаждают до 0-5оС и по каплям приливают концентрированную соляную кислоту, пока не будет достигнуто рН среды 1, при этом температура реакционной массы не должна подниматься выше 5оС. Выпавший осадок серого или светло-коричневого цвета отфильтровывают, промывают на фильтре водой и сушат. Получают 32,8 г 2-[4-(6-хлорбензотиазолилокси)-фенокси]-пропионовой кислоты (т.пл. 90-93оС), содержание основного вещества, определяемое методом высокоэффективной жидкостной хроматографии составляет 98%.
Строение синтезированного соединения подтверждается данными спектроскопии ядерного магнитного резонанса. Спектр ЯМР13С данного соединения характеризуется химическими сдвигами: 172,8 (S, SC(N)O); 147,4S; 133,2S; 128,2S; 126,6d; 121,8d - бензотиазольный фрагмент; 155,8S; 147,9S; 121,8d; 116,0d - ароматическое ядро; 172,9 (S, COOH), 72,62 (d, OCH), 18,7 (K, CH3) - оксипропионат. ИК-спектр данного соединения характеризуется следующими полосами поглощения: 3400 (νOH), 1715 ( ν C=O), 1608, 1540, 1510 (ν C=O ароматич.).
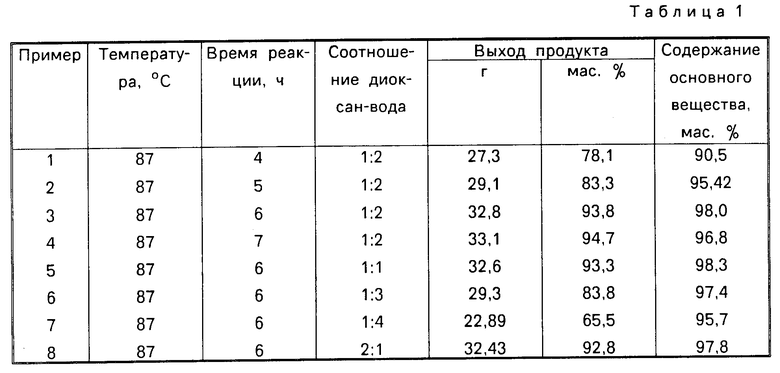
П р и м е р ы 2-8, иллюстрирующие получение 2-[4-(6-хлорбензотиазолилокси)-фенокси]-пропионовой кислоты представлены в табл.1.
При снижении температуры реакции наблюдается значительное увеличение времени реакции и снижение качества целевого продукта.
П р и м е р 9. Синтез проводят аналогично примеру 1, но в качестве исходных реагентов берут 18,2 г (0,1 моль) 2-(4-оксифенокси)-пропионовой кислоты и 13,45 г (0,1 моль) 2-хлор-5-метил-1,3,4-тиадиазола. Соотношение диоксан-вода 1: 2. В результате проведенного опыта получено 27,4 г 2-[4-(5-метил-1,3,4-тиадизолил-2-окси)-фенокси]-пропионовой кислоты.
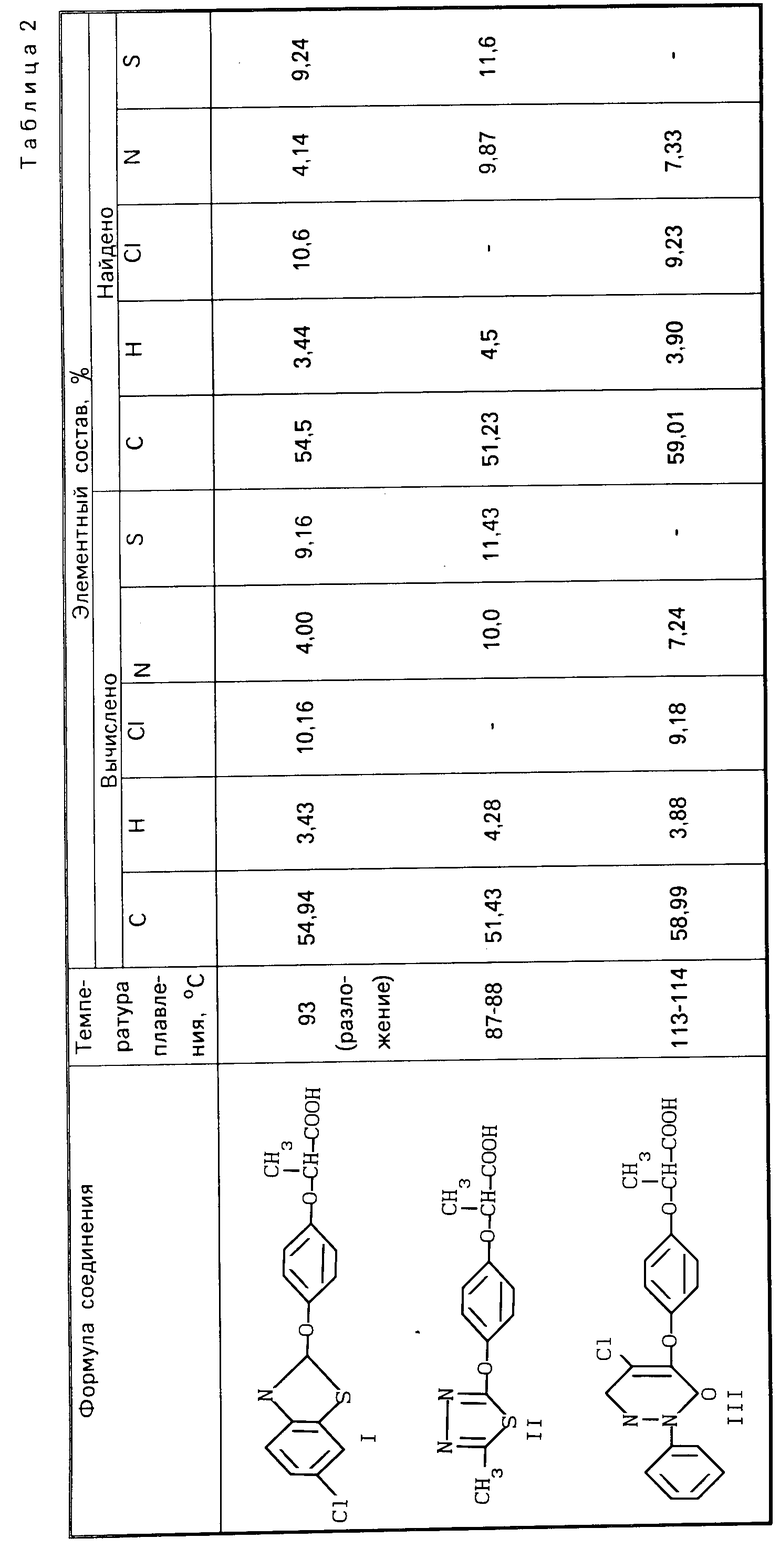
2-[4-(5-метил-1,3,4-тиадиазолил-2-окси)-фенокси] -пропионовая кислота представляет собой кристаллический продукт коричневого цвета, т.пл. 80-83оС. В результате повторной очистки получен продукт, характеристика которого приведена в табл.2.
Строение синтезированного соединения подтверждается данными спектроскопии ядерного магнитного резонанса. Спектр ЯМР13С данного соединения характеризуется химическими сдвигами: 175,0S; 160,6S; 16,63 (K, CH3)-тиадиазольный фрагмент; 155,4S; 149,5S; 121,1d; 116,3d - ароматическое ядро; 172,6 (S; COOH), 72,36d (d, OCH); 18,64 (K, CH3) - оксипропионат.
ИК-спектр данного соединения характеризуется следующими полюсами поглощения: 3300, 3400 (ν OH); 1730 (ν C=O); 1660 (ν C=N); 1610, 1510 (ν C=C).
Содержание основного вещества распределялось методом высокоэффективной жидкостной хроматографии и составило 95,3%, выход 97,8%.
П р и м е р 10. Синтез проводят аналогично описанному в примере 1. В качестве исходных реагентов взято 24,1 г (0,1 моль) 1-фенил-4,5-дихлорпиридазона-6 и 18,2 г (0,1 моль) оксифеноксипропионовой кислоты. Соотношение диоксан: вода равнялось 1:2. В результате опыта получено 36,3 г 2-[4-(1-фенил-5-хлорпиридазон-6-илокси)-фено- кси] -пропионовой кислоты, кристаллического продукта кремового цвета, т.пл. 110-115оС. Содержание основного вещества в целевом продукте 90%. Выход составляет 93,9%. В результате повторной очистки получен продукт, характеристика которого приведена в табл.2.
Строение синтезированного соединения подтверждается данными спектроскопии ядерного магнитного резонанса. Спектр ЯМР13С данного соединения характеризуется химическими сдвигами: 157,4 (S, CO); 153,1S, 130,2 (d, CH); 118,7S - гетероцикл; 141,1S; 128,6d; 128,1d; 125,7d - ароматическое кольцо при атоме азота; 155,0S; 147,1S; 120,7d; 116,5d - ароматическое ядро; 172,7 (S, COOH); 72,43 (d, OCH); 18,64 (K, CH3) - оксипропионат.
ИК-спектр данного соединения характеризуется следующими полосами поглощения: 3480, 3420, 3300 (ν OH); 1738 (ν C=O); 1660 (ν C=N); 1620, 1608, 1518 (ν С=С - ароматические).
Настоящий способ позволяет получить 2-[4-(5-метил-1,3,4-тиадиазолил-2-окси)-фенокси] -пропионовую и 2-[4-(1-фенил-5-хлорпиридазонил-6-окси)-фенокси] -пропионо- вую кислоты, которые являются новыми соединениями и могут быть использованы в синтезе гербицидов.
Кроме того, преимущество при использовании этих кислот как промежуточных полупродуктов заключается в возможности расширения спектра синтеза других производных кислот (хлорангидриды, амиды и др.), которые могут найти широкое применение в качестве биологически активных соединений, в частности гербицидов.
Изобретение относится к гетероциклическим соединениям, в частности к получению п-замещенных a феноксипропионовой кислоты формулы (см. чертеж), которые используют в синтезе гербицидов. Цель - упрощение технологии процесса. Получение ведут реакцией соответствующего хлорпроизводного гетероциклического соединения с п-оксифеноксипропионовой кислотой при нагревании в воднодиоксановом растворе при массовом соотношении диоксан - вода 1 : 1 - 2. 2 табл.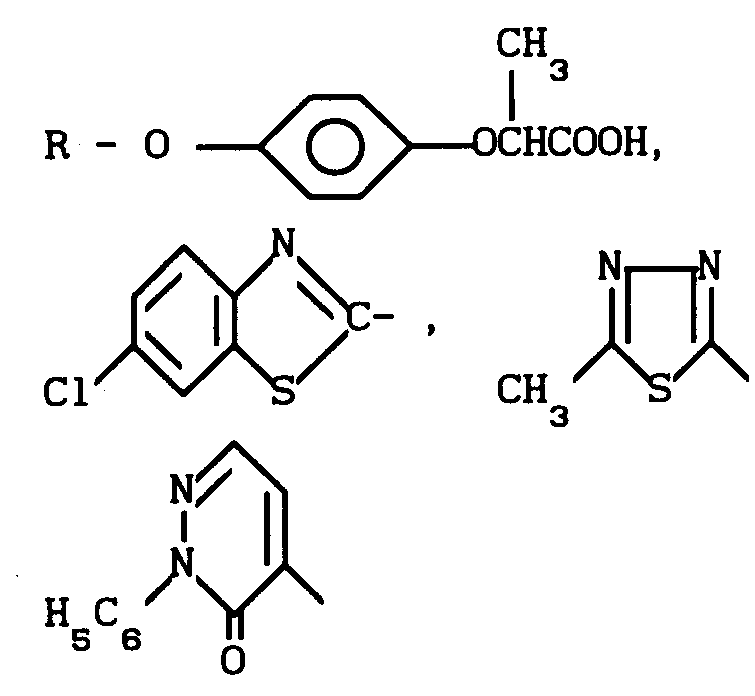
СПОСОБ ПОЛУЧЕНИЯ П-ЗАМЕЩЕННЫХ α -ФЕНОКСИПРОПИОНОВОЙ КИСЛОТЫ общей формулы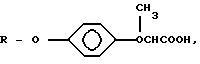
где R -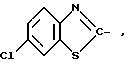
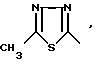

отличающийся тем, что, с целью упрощения технологии процесса, соответствующее хлорпроизводное гетероциклического соединения подвергают взаимодействию с п-оксифеноксипропионовой кислотой при нагревании в водно-диоксановом растворе при массовом соотношении диоксан - вода 1 : 1 - 2.
| ЭФИРЫ ГИДРОХИНОНА, ОБЛАДАЮЩИЕ ГЕРБИЦИДНОЙ АКТИВНОСТЬЮ | 1988 |
|
RU1630255C |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-03-27—Публикация
1989-04-18—Подача