Изобретение относится к водной токсикологии и может быть использовано для биологического контроля за токсичными водорастворимыми веществами с использованием в качестве тест-объекта простейпшх в системе мониторинга и контроля качества воды, в том числе при сбросе сточных вод промышленных предприятий, поверхностного стока при мелиорации и других областях, где требуется оперативный контроль качества водной среды
Проблема -биотестирования является одной из важных в области охраны природы, в частности при контроле химического загрязнения водной среды. При этом особую актуальность принимают все методы оперативного контроля, т.е. методы оценки физиологического состояния биологических тест-объектов в краткосрочных опытах. Учитывая большую информативность оценок по подвижности микроорганизмов, последние находят большое развитие для задач биотестирования,,
Известен способ определения средней скорости движения совокупности однородных биологических объектов, согласно которому регистрируют следы
О 00
00
оэ
лвижения изображении на пндрО1Крано,
Т рИ -ЭТОМ СКОРОСТЬ ВЫЧМСЛЯО Г ПО г юрМУ 0
V
- fSl -
П I0/t,
n
с ,
г де Sn - суммарная ПЛШЧРДЬ изображений СЛедОП 1 50КОВ В МОМСНТ
времени t(3;
суммарная тощэд изображений спс/юл тоекон в момент времени tf ;
fc ц - го;
1 - характерная ллшы сетки
экрана.
Данный способ ягшяется усовершенствованием известного метода регистрации скорости дш-гкенчя микрооргания Мои в воде. Однако гш i обоих ттпх способов характерна большая о чиС5ка Измерения, которая СРтзана как го значительной систематической ошибкой ( опыты ведут с помощью микроскопа), так и с субъективизмом опенки, так как оператор на экране наблюдает лиш движения в одной плоскости. При этом все вращательные движения, кувыркаПия
движения в ларг ондикулярнои
плоскости на видео экране не отражаются. Очевидно, что зкпяд движений в суммарную скорость может быть существенным. Кроме ioro явления фототаксиса накладывают дополнительные эффекты, которые пргктическн учесть невозможно. Jaicoro типа ошибки присущи всем мегоггм контроля подвижности с помопью MI кроскопного наблюдения Кроме того, при движении клеток в поггшяцич обычк наблюдается Следующий зААект, Подвижные клетки т Своем движении вовлекают в поток не- иодпижнне или мерттыс точки, которые оператор принимает за подвижные, что
Известен способ определения то ности водорастворимых веществ, со ласно которому токсичность вещест определяют путем оценки их влияни на двигательную активность инфузо Теtгапутепa pynformis путем дисп гирования инфузорий в культуральн среде и регистрации изменения вел
также вносит большую ошибку в нзмере Пия, особенно при налччии пристеночных .5 ны светопропускания -культуры до и
явлений Последнее связано с ограничением рабочего объема покрывным стек- Лом.
Разделение подвижных и неподвижные клеток в популяции - это сложная задача, которую, напоим ар, решают путем фракционирования с помощью специальных сефадексколоно.
Кроме того, в анализах состояния популяции движущихся клеток обычно измеряют только скорость движения, так как неподвижные клетки не всегда отражают мертвое состтямие« Организмы могут на некоторое время остановиться,
50
55
после экспозиции с исследуемъгм ве ством. При этом культуру Tetrahyn pyriformis культивпр/ют на амичоп тидной среде (0,6%-ный раствор ам пептида и 0,%-ный раствор дрожже экстракта) при 27 С и содержащую в 1 мл 40-60 тыс, особей помещают в кювету с расстоянием между рабочи гранями 20 мл. Кювету устанавливаю в правый кюветодержатель колориме неЛелометра ЭК-ЗбМ с освещением светом длиной волны ( А 582 мм) В левый кюветодержатель устанавлив ют кювету с аминопеп иднои средой
0
5
0
5
0
а атем снопа начинают двигаться. По- задача идентификации н поднилных клеток - ото проблема, которую необходимо решить при анализе состояния популяции движущихся микроорганизмов.
При оценке токсического воздействия химических веществ на движущиеся биологические тест-объекты все недостатки, присущие визуальной микроскопии, не позволяют обеспечить высокую точность и достоверность анализа, так как ошибка оператора в измерении истинной скорости движения и процента подвижных клеток обпчно достигает для подвижности на малых скоростях 10-20% в сторону увеличения результатов измерения, а на больших - до 307 в сторону занижения результатов.
Известен способ оценки токсичности с использованием простейших, согласно которому токсическое действие в экспериментах оценивается по интенсивности роста и подвижности, определяемой поп микроскопом При этом степень ин- гибирования оценивают в процентах за определенный период времени путем построения пробит-графика и определения LC50.
/ лнному способу присущи все вышеперечисленные недостатки, к которым добавляются еще длитепьность анализа до 12 ч и отсутствие учета влияния температурных эффектов и циркадных ритмов Функционирования организмов.
I
Известен способ определения токсичности водорастворимых веществ, согласно которому токсичность веществ определяют путем оценки их влияния на двигательную активность инфузории Теtгапутепa pynformis путем диспергирования инфузорий в культуральной среде и регистрации изменения величи0
5
после экспозиции с исследуемъгм веществом. При этом культуру Tetrahynena pyriformis культивпр/ют на амичопеп- тидной среде (0,6%-ный раствор амино- пептида и 0,%-ный раствор дрожжевого экстракта) при 27 С и содержащую в 1 мл 40-60 тыс, особей помещают в кювету с расстоянием между рабочими гранями 20 мл. Кювету устанавливают в правый кюветодержатель колориметра- неЛелометра ЭК-ЗбМ с освещением светом длиной волны ( А 582 мм)„ В левый кюветодержатель устанавливают кювету с аминопеп иднои средой.
16
Инфузории перемешиванием диспергируют в кювете (контроль) и, вращая левпй барабан неЛелометра, в течение 3 мин после прекращения перемешивания поддерживают стрелку измерительного прибора на О, регистрируя каждые 10 с значения на шкале светопропус- кания вращаемого барабана.
Затем (опыт) в кювету вводят ис- пытуемое вещество заданной концентрации и аналогично проводят измерения так, как и в контроле.
Двигательную активность инфузорий определяют по сумме разниц (Д) между соседними значениями светопропускания с последующим вычислением относительного измерения в процентах
й-2:/ п/-2:/ рит/.
S- OKOHT /
При этом графическим путем методом пробит-анализа определяют концентра- цию LC „, при которой двигательная активность уменьшается на 50%.
К недостаткам данного способа относится следующее.
В сути известного способа лежит явление отрицательного фототаксиса инфузорий, при котором клетки уходят из зоны наблюдения (сканирования световым пучком), а о токсическом действии судят по снижению двигательной активности,, Однако для фототаксиса присуща суточная ритмика, при этом токсический эффект будет иметь существенную зависимость от времени анализа в сутках, что обуславливает низкую точность оценки токсичности и воспроизводимость анализа.
Низкая точность определения токсичности связана также и с тем, что данному способу присуща большая динамическая ошибка в проведении опыта, которая связана с изменением скорости ухода клеток из зоны наблюдения в зависимости от седиментационных и коагу ляционных характеристик культуры. Очевидно, этот показатель может изменяться от Аизико-химических свойств испытываемых вешеств, особенно от сложного их комплекса, например, сточных воде, Этот факт в известном способе практически не поддается учету.
Измеряемый признак не отражает физиологической характеристики движения отдельных клеток, что не позволяет корректно оценивать биологическую реакцию тест-объекта (инфузорий),
0
1
Q
5
5
0 0
5 0
616
тяк как с помощью нефелометра по сути измеряется концентрация клеток в зо- че наблюдения,- При действии токсиканта могут развиваться реакции разрушения клеток (что вепет к увеличению концентрации микроагрегатов в суспензии) , стресса, которые развиваются в сторону уменьшения параметрической чувствительности, в частности, к фототаксисе (что ведет также к увеличению концентрации клеток в зоне наблюдения) и т„п. Кроме того, измерение модуля изменения параметра контроля вносит дополнительную ошибку в процесс оценки фототаксиса, так как при этом учитываются все изменения концентрации клеток, которые связаны с перемешиванием, флотацией, седиментацией и другими процессами не физиологической природы для тест-объектов.
Следовательно, данному способу присуща низкая достоверность определения токсичности химических веществ„
Большой объем камеры (порядка 1C см3) требует с учетом испытания как минимум пяти-шести концентраций вещества и трех повторностей как минимум 150 мл культуральной среды„ Испытываемые вещества могут быть различной цен- нгсти (впервые полученные или препаративно выделенные, как правило, очень дорогие), поэтому данный способ очень неэкономичен„
Наиболее близким по технической сущности к предлагаемому является способ определения токсического воздействия химических веществ, сопержащихся в водной среде, на культуру планктонных гидробионтов - мнкровогорослей„
Дэпчый способ предусматривает культивирование водорослей в опытных и контрольных камерах, введение в опыт- пые камеры исследуемой среды, выдерживание водорослей в присутствии исследуемой среды, измерение в этот период времени средней скорости движения по ансамблю клеток водорослей в опыте и контроле методом корреляцион- но доплеровской спектроскопии, оценку отношения числа подвижных клеток в культуре к числу неподвижных соответственно в опыте и контроле, оценку по полученным данным величины энергозатрат гидробионтов на движение и суждение о токсическом воздействии исследуемой среды по величине энергозатрат на движение в опыте.
К недостаткам способа можно отнести невысокую точность опенки ввиду невозможности определения урои- ней токсического поз:сйствия, большой расход исследуемой средь и культуры водорослей.
Целью изобретения ннляется повышение точности оценки ,а счет определения уровней токсическогс воздействие исследуемого вещества и сокращение расхода исследуемой среды и культуры гкдробионтов.
Способ осуществллпт следующим образом.
Через 30-60 мин после начала инкубации среду с гипробионтами подвергают фиксированному воздействию в вi
де температурного скачка с 22 до 28 облучают когерентным светом с длиной волны в красном диапазоне, например, 632,8 им с измерением Флуктуаци рассеянного движущимися клетками света и оценивают „скорость и число подвижных клеток„ а относительную величину энергозатрат на движение клеток Е популяции гычиспяют по формуле
2.
Icon С(о),)П
Г Ч
}
Qn; ionL
- v ,.-сГо7Г
где ; , v средняя скорость по ансамблю клеток микроорганизмов в зоне наблюдения соответст- венно ь опыте и контроле, мкг /с;
ton F X отношение числа подвижных клеток в популяции
к числу неподвижных
соответственно в опыте и контроле, отн,ад„;
G(° значение корреляционно Функции при времени задержки, равном нупю, соответственно в опьте и контроле, уел сед при этом нижнюю границу токсического
действия вещества огределяют по первому пику параметрической чувствитель
ности энергозатрат -а движение клеток в популяции, а максимально допустиую концентрацию химического вещества - п второму пику параметрической чувствительности.
Проведение инкубации биологического тест-объекта с химическим веществом в течение 1JO-()0 УИН обаспечьяа-- ет реализацию крлтк срсчного опыте
контроля химического ночдепстпия при анализе токсичности, Т.Р оперативность анализа. 1а это время организмы тест-объекта изменяют только энергетические характеристики своего состояния, а параметры, отражающие информационные потоки (в генетическом аппарате и др,), не успевают отреагиро- пать. Требования на длительность повреждающего воздействия в этом аспекте можно представить в следующем виде:
л. on -ч сорг )
20 25
30
35
где
Л
. ог) - длительность опыта; -орг
полного никла жизнедеятельности тест-объекта (для инфузорий что время составляет 4-5 ч К,
Данное ограничение обеспечивает повышение точности и воспроизводимости анализ, так как позволяет исключить влияние не только медленных циклоп жизнедеятельности организма в реакции на химическое воздействие, но и суточных ритмов параметров движения инфузорий. При длительностях, сравнимых или больших характерных времени, необходимо обязательно учитывать все параметры жизнедеятельности микроорганизмов, а это на практике обычно осуществить очень сложн-о, так как требуется проведение хронических опытов с привлечением помимо всего прочего и Лурье-анализа временных рядов данных.
То, что после инкубации суспензию микроорганизмов подвергают фиксированному воздействию в виде температурного скачка заданной величины, обеспечивает высокую точность оценки реакции живых организмов на токсическое воздействие, так как при этом изучается параметрическая чувствительность (в данном случае термочувствительность), при которой извлекается наибольшее количество информации о состоянии тест- объекта. ,ггля расчета информации в случае неравномерностью событий Шено- ном предложено уравнение энтропии информации
-Sv rгде Р, ,Р2, . . ,Рт
ТИП 1 ,,... ,ТЧ
рроятности собыПредложим, что одно из событий дотоверно, т.о. вероятность его равна единице. В этом случае имеем i -(1 + 0 + ... + 0) 0, т.е. система не содержит никакой неопределенности и сообщение о ее испытании не содержит никакой информации (при отсутствии температурного скачка состояние тест-объекта не изменяется в опыте), так как i -0 0.
Наибольшее количество информации несут равновероятные события (при температурном скачке в популяции все клетки адекватно реагируют на темпе- ратурное воздействие), т.е. когда Р 1/2, поскольку i -(1/2 Iog21/2 f + 1/2 lop 2 1/2) 1 .
Вот почему прием температурного скачка, при котором не происходят необратимые сдвиги в клетках, является наиболее оффективным методом оценки реакции популяции клеток на воздействие, в частности, токсикантом
Облучение когерентным светом с длиной волны в красном диапазоне, например, 632,8 нм обеспечивает повышение точности оценки скорости движения клеток микроорганизмов (инфузорий) методом доплеровской cneKtpocKonHH.
Измерение флуктуации рассеянного движущимися клетками света обеспечивает измерение скорости движения микроорганизмов методом доплеровской спектроскопии при низких требованиях к стабильности параметров как источника излучения, так и измерительного тракта. Для этого достаточно, чтобы характерные времена изменения параметров системы были не соизмеримы с характерными временами доплеровского сдвига на микроорганизмах.
Таким образом, прием измерения корреляционной функции при доплеровской спектроскопии в целом повышает точность оценки состояния биологического тест-объекта.
То, что из корреляционной функции получают скорость и долю подвижных клеток, обеспечивает объективный ана- лиз состояния популяции подвижных клеток. Корреляционная функция имеет быстро- и медленноепадающие компоненты. Параметры быстроспадающего слагаемого связаны с величиной средней по ансамблю скорости движения микроорганизмов, а относительный вес мед- ленноспадающего компонента определяет относительное количество неподвиж-
Q
5
0
5 0
0
5
9
5
5
ных клеток. Эти параметры движения извпекаются, например, путем подгонки по методу наименьших квадратов.
Таким образом, при анализе состоя-, ния популяции микроорганизмов методом коррепяционно-доплеровской спектроскопии в условиях автоматизации съема и обработки информации о скорости и подвижности клеток исключается субъективизм оценки, причем величину погрешности можно угтенышть путем увеличения объема выборки (количества экспериментов). Реальное время съема и обсчета информации в одном опыте составляет 1,5-2,0 мин.
То, что при анализе состояния популяции подвижных микроорганизмов используется показатель в виде (o) обеспечивает оценку энергозатрат на движение клеток и энергия, расходуемая на трение, пропорциональна v2, а (о) пропорциональна количеству движущихся клеток в зоне наблюдения, так как J7 - это подвижность, а G(o) - пропорциональна числу клеток в момент съема информации в зоне наблюдения. Последний параметр по сути учитывает процесс изменения концентрации клеток в зоне съема, которая может быть связана с процессом фототаксиса, гибели клеток с осаждением их и др. Следует отметить, что ранее в исследованиях при анализе по- катателей движения, например, инЛузо- рий, нигде этот признак не использовался .
Величина энергозатрат отражает свойство популяции энергообъема с внешней средой, и в этом проявляется фундаментальность оценки биосистемы, по данному признаку. Это связано с тем. что в популяции подвижных микроорганизмов функция движения клетки является результирующим проявлением жизненно важных процессов. Так, известно, что трофические реакции, изменения таксического характера (фототаксис, хемотаксис, термотаксис и т.д.) и даже функции размножения популяции имеют непосредственную связь с показателями движения клетки. В этом проявляется фундаментальность оценки состояния популяции подвижных микроорганизмов по изменению средних по популяции параметров движения„ То, что в качестве основного критерия оценки взят параметр двигательных энергозатрат, связано с тем, что в этом показателе учитывается как относительное количество подвижных кпеток в популяции, так ч средняя по ансамблю микроорганизмов скорость перемещения, т+е. в этом проявляется универсальность измеряемого параметра.
Исследования показывают, что именно показатель энергозатрат наиболее информативен по сравнению как с характер ристикой скорости, так и с подвижностью клеток, по крайней мере,, в опытах по исследованию термочувствитель- ности„
В качестве примера целесообразно рассмотреть результаты (таблицу) экспериментов , в которых изучалась реакция на температурный скачок в течение 5 мин с измерением скорости, подвижности клеток и энергозатрат на движение клеток через 1,5 мин после начала воздействия температуры (скачок от 22 до 28°С). Нее результаты нормированы в виде fj, М, где fj - значение измеряемой Функции; У сред нее значение по выборке из 7 опытов.
Используя критерий информационной значимости испытываемого признака в виде
i P.,
j
имеем для скорости ветичину 0,985,для подвижности - , а для энергозатрат - 1,95. Из этого следует, что с Точки зрения информационной значимости показатель энергозатрат отражает в большей степени переходный процесс и популяции на температурный скачок, чем другие,
Таким образом, использование показателя энергозатрат при оценке токсического действия химических веществ На популяцию движущихся клеток является принципиально новым признаком,
который ранее в таком вице нигде не рассматривался,
То, что относительную величину энергозатрат на движение клеток в популяции вычисляют по формуле
} У2оп Pon G(o)on
П G(«V
обеспечивает воспроизводимость результатов оценки, так как при этом в относительном показателе энергозатрат учитываются возможные изменения физиологического состояния исхо.г,
о 5
0
5
0
5
0
5
ной культуры микроорганизмов, имеющие характерные изменения при развитии популяции в процессе их культивирования или в результате суточной динамики функционирования организмов, при этом также повышается точность измерения,
То, что нижнюю границу токсического действия вещества определяют по первому типу параметрической чувствительности энергозатрат на движение клеток в популяции, а максимально допустимую концентрацию химического вещества - по второму циклу параметрической чувствительности,, обеспечивает точность оценки токсического действия вещества в краткосрочных опытах. Это связано с тем, что характер реакции популяции движущихся организмов при действии повреждающего фактора (температурные и химические воздействия) изменяется в зависимости от интенсивности воздействия„ При этом наблюдаются первая фаза стимуляции, которая проявляется увеличением параметрической чувствительности, фаза стресса с ми- нимапьной чувствительностью к дейстт вию внешнего фактора, после которой снова повышается (вторично) параметрическая чувствительность, причем энергозатраты относительно увеличиваются. Однако, если на- первой фазе снять воздействие, то биосистема возвращается в свое нормальное состояние, из стресса популяции также восстанавливает свои характеристики, а вот при наличии второй фазы увеличения термочувствительности энергозатрат снятие воздействия не сопровождается переходом биосистемы в норму. Обычно наблюдали либо значительный гистерезис переходного процесса, либо последующую раскачку параметров популяции и ее реградацию (по крайней мере, при тех временах наблюдения, которые исследовались в опытах). Учитывая стохастичиость реакции тест-объекта (популяции) на токсическое воздействие, необходимо в исследованиях не только контролировать средние параметры тест-объекта, но и стохастические характеристики например вериабилъность которая отражает системные свойства Объекта анализа. Установлено, что j (Ъазность реакции проявляется и в ва- риабильности характеристик движения клеток в популяции. Данный Феномен
реакции биосистемы наблюдали и на других подвижных объектах (простейшие, микроводоросли, активный ил очистных сооружений, сперма).
Учет состояния исходной популяции микроорганизмов осуществляют по вари- абильности отклика популяции на токсическое воздействие в зависимости от фазы робта. Это обеспечивает установ- ,Q ление наиболее оптимальных условий для проведения опытов, с точки зрения выбора фазы роста популяции Вполне естественная ситуация, когда в опытах используют старую культуру, а в этом 5 случае и необходим критерий отбраковки культуры. Все это повышает воспроизводимость результатов, что особенно важно при сопоставлении токсикантов.
Величину температурного скачка 20 определяют по минимуму вариабильности температурного отклика популяции микроорганизмов, например для инфузорий Tetrahymena pyriformis температурный
скачок устанавливается в пределах от
22 до 28°С0
Данный признак повышает воспроизводимость реакции тест-объекта, обеспечивает принципиальную возможность измерения с высокой точностью парамет-30 рической чувствительности реакции подвижных организмов на токсикант, т.е. именно в этом температурном диапазоне происходит однонаправленное изменение энергозатрат на движение клеток з по- зг пуляции, с минимальной вариабильностью в точке 28°С.
На фиг. 1 представлена блок-схема устройства для измерения энергозатрат популяции на движения инфузорий в ре- 40 альном масштабе времени методом кор- реляционно-доплеровской спектроскопии; на фиг. 2 - температурные зависимости энергозатрат популяции на движение инфузорий и вариабильности их ответа; 45 на фиг. 3 - динамика реакции популяций инфузорий на температурный скачок; на фиг, 4 - суточные изменения параметров движения инфузорий T.pyrifonnis; на фиг о 5 - кинетика изменения энерго о затрат популяции на движение инфузорий при различной концентрации токсиканта; на фиг, 6 - дозовые зависимости реакции биологического тест-объекта на действие меди в краткосрочном опыте ее на различных стадиях развития популяции; на фиг. 7 - дозовые зависимости реакции инфузорий на действие этилового спирта в краткосрочных опытах.
,Q 5
0 5
0 г
0 5 о е
Устройство для реализации предлагаемого способа содержит источник 1 когерентного излучения в диапазоне красного света, в качестве которого ис- , пользован ЛГ-105 с источником 2 питания. На выходе лазера 1 установлены диафрагма 3 и линза 4, Излучение падает перпендикулярно на измерительную камеру 5, снабженную термо- статирующей рубашкой, которая соединена с термостатом 6. Рассеянный свет от суспензии и блик от передней стенки кюветы регистрируются фотоприемником 7, в качестве которого использован фотоэлектрический умножитель ФЭУ-79, установленный под углом 16- 20 и снабженный диафрагмой 8, которая реализует собой камеру обскура. Питание ФЭУ осуществляют блоком 9 высоковольтного питания типа Б5-24 или ВС-220 Выход фотоприемника 7 соединен с входом усилителя 10 типа У 4-28, выход которого соединен с входом коррелятора 11, типа Хб-4. Цифровой выход коррелятора 11 соединен с входом микроЭВМ 12 типа CMO-40U С мик- роЭВМ 12 идут сигналы управления работой коррелятора 11, при этом интервалы между съемами информации задаются таймером 13„ Выход микроЭВМ 12 соединен с цифропечатающим устройством 14 типа Искра 001-45.
Культуру простейших - инфузорий Tetrahymena pyrifornis использовали в качестве тест-объекта., Преимуществом этого организма является высокая чувствительность и возможность его выращивания в чистых средах без бактерий, в отличие от культур других простейших, для которых бактерии служат в качестве пищи.
После предварительного культивирования инфузорий на питательной среде составом, включающим, пептон 20 г, глюкозу - 5 н. NaCl - 1 г, дрожжевой экстракт 1 мл, дистиллированную воду 1 л, при рН 7,1, которое осуществляют путем пересева на 5 мл среды 2 капли из 1 мл пипетки Мора суспензии клеток при температуре 21+2°С в течение времени, на которое популяция переходит в ту или иную фазу роста (экспоненциальную или стационарную), пробу микроорганизмов вводят в сосуд для инкубации, куда вводят химическое вещество с заданной концентрацией. Если исследуемая вода с токсикантом имеет неизвестный COCTSP, что характерно
дл° исследования токснче кого доисг- пия, например стпч ы пол, то гото- рял проб воды чядаинои краппо- I-1 ью разбавления , ытимер 1:1, I:, 1:5, 1: 1П, 1 :20, 1 , IOO, , 1:600, 1 : 1000, 1 : 10(4100.
Инкубацию суспензии осуществляют в условиях мягкого режима освещенности так, чтобы не тг талан прямой солнечный свет Однако затемнени нежелательно, так как в этом ГЛУЧЧС после облучения л з. черным снегом при намерениях проявляются явления гЬото- таксиса в большей мере, чем при све- тоном режиме инкубации. Температуру инкубации устанавлир -от ч пределах от 20 до 22 С, прелпочтнгельно 21°Г со стабильностью + 0,Ь С „ Длительность инкубации выбирают в пределах 30 60 мин в зависимости of ребований оперативного контроля и характера действия токсиканта„
После инкубации суспензию микроорганизмов помещают С Фиг. 1) в ичме- рительную камеру ri, котопую термоста- тирук Г до выбранной температуры, например ,2 С с помощью термостата 3. Пучок когерентного снега с длиной волны, например, 632,8 им от па iepa 1Г-105 сформируют с помощью диамря мь 3 и фокусируют в центр измерительной камеры 5 с помощью линзы А.
Через 1,5-,О мин снег, рассеянный движущимися клеткам7, и б ик от переп- ien стенки камеры Ь регистрируют фото лриемником 7, на выходе которого получают ча счет гетрродшшрования моду- пиронанный электрический сигнал, пос- гупающий на вход низкочастотного уси- Кителя 10, где происходит усиление iKriVKTViUTnoHHoro сигнала до уровня 2- 3В. Ич сигнача с помощью коррелятора 11 строят корреляционную функцию рассеянного света в реальном масштабе Времени при временах задержки 1 00 | с л величинот выборки (стсиистики) 2 , ..., 2 ъ Корреляционная функция в виде цифрового сигнала поступает в оперативную память мнкро ЗВМ 12. Из корреляционной функции по методу наименьших квадратов извлекают величину скорости и числа подвижных клеток в популяции микроорганизмов, информация о которых выводится, например, на циф ропечать 14. Время между сч.смами информации определяется с помошью таймера 13„ Время между съамами составляет 28 с. Поэтому при усреднении измеряемых параметров но 10 посчедова- гельным сптьп ам общее время анализа с оставляет 280 с.
Относительную величину энергозатрат на пнижеште клетж в популяции с учетом текущей плотности и организмов в зоне наблюдения вычисляют по формуле
Zsc:
п соп
оп
f:(o) :
где v
оп;
f
П
i on I i. к
средняя скорость по ансамблю клеток микроорганизмов в оне наблюдения соответственно в опыте и контроте, мкм/с;
отиошсние числа подвижных клеток в популяции к числу неподвижных соответственно в опыте и конт роле , отн ед . ;
С(о) ,г(о)к - значение корреляционной функции при времени за- держки, равном нулю соответственно в опыте и контроле, усл.ед
Результаты энергозатрат на движени клеток в популяции при различных концентрациях химических веществ представляют в виде графика, при этом нижнюю границу токсического действия определяют по первому пику параметрической чувствительности энергозатрат на движение клеток в популяции, а максимально допустимую концентрацию химического вещества - по второму пику параметрической чувствительности,
Рели необходимо уточнить состояние исходной популяции микроорганизмов, то по результатам токсикологических опытов для каждой концентрации химического вещества вычисляют величину вариабильности отклика популяции на воздействие химического вещества. При этом полученные значения наносят на тот же график и в результате сравнительного анализа осуществляют учет текущего состояния ПОПУЛЯЦИИ. i
Пример 1 о По обоснованию выбора величины температурного скачка для изучения термочувствительности инфузорий Т. pyriformis в опытах биотестирования.
Исследовали температурную зависимость энергозатрат популяции ча движение инфузорий и вариабильности их
OTWTOH Н lIonVniUHH В ЧК ТЮШ МШИе ЭЛЬ -
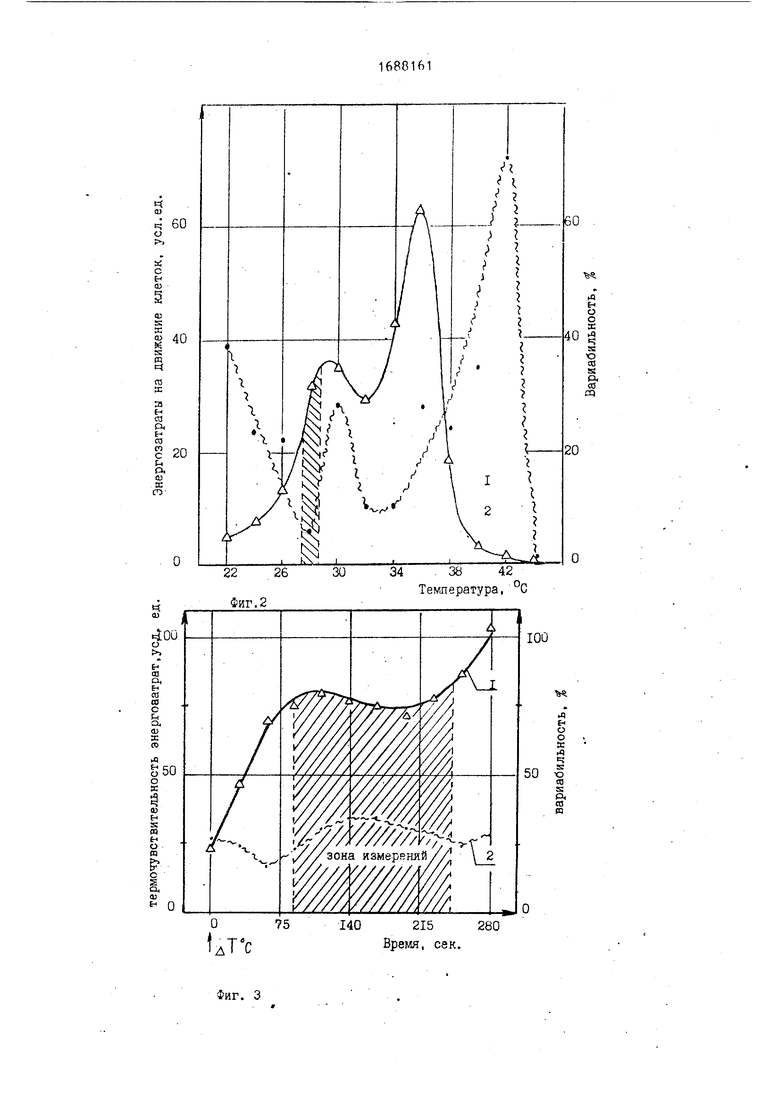
поп (Ьачг ростл ля -ттого пробу культуры инфузории помещали п и-змеритель- ную Kawc pv, которую термостатировали при заданной температуре в пределах от 22 до 42°С с изменением температуры на 2°С с точностью 0,1 С При этом микроорганизмы выдерживали для каждой температуры в течение 4,0 - 4,5 мин. Контроль скорости, подвижности клеток и энергозатраты популяци проводили в 3-кратной повторности при статистике 2 . Установлено, что не только показатели движения имеют тем- пературную зависимость, но и вариа- билъность имела сложную температурную зависимость. На фиг 2 представлены экспериментальные результаты этих опы roii, где график 1 - зависимость энер- гозатрат на движение клеток к популяции, график 2 - вариабильность их ответа.
Как видно из температурных зависи- (мостей, именно в диапазоне физиологи- ческих температур от 22 до 30°С наблюдается арениусовский характер изменения параметра движения клеток, при этом в температуре вариабильность имеет минимальное значение, что указы вает на устойчивое состояние популяции в этих условиях. Поэтому, если взять температурный скачок величиной 6 Г от 22 до 28°С, то температурная чувствительность для контроля будет иметь минимальную динамическую ошибку Экспериментально установлено, что при температурах выше 28°С в реакции тест- объекта возникают неустойчивые колебания параметров движения, что связано с повреждающим воздействием температурного фактора. При меньиГих температурах от величины 28° увеличивается вариабильность, что также повышает ошибку измерений показателя термочув- ствительности.
Таким образом, установление величины температурного скачка до 20+5°С обеспечивает достаточный уровень чув- ствительности тест-объекта с ошибкой не хуже 4,5%.
Пример 2. По обоснованию выбора длительности измерения показателей движения инфузорий, в частное- ти термочувствительности, при наличии явлений фототаксиса и динамических процессов на температурный скачок до 28°С.
Q Q
5 о Q 5
5
Суспензию микроорганизмов помещают в камеру, термостатированную с темпе- р-ятурой 28°С, облучают лазерным светом в красном диапазоне и регистрируют в течение 5 мин через каждые 28,4с энергозатраты на движение клеток в популяции. По девяти опытам вычисляли средние значения в каждой точке измерения и вариабильность этого показателя, Результаты экспериментов представлены на фиг„ 3, где график 1 - термочувствите.льность, график 2 - вариабильность. Популяция находилась в экспоненциальной фазе роста.
Из графиков на фиг. 3 видно, что энергозатраты после температурного скачка, начиная с 1,5 мин вплоть до 4 мин, практически не изменяется, при этом вариабильность за это время изменяется в пределах от 24 до 34%, т.е. динамическая ошибка измерения оценки состояния по термочурствитель- ности энергозатрат на движение клеток в популяции составляет менее 3,2%, что вполне удовлетворяет требованиям проведения опытов анализа текущего состояния тест-объекта в условиях специальных воздействий (температурного скачка) и случайных факторов (например, связанных с фототаксисом). Вот почему в опытах по биотестированию использовали длительность измерения параметров движения инфузорий в нтервалах от 1,5 до 4,5 мин. Пример 3. По обоснованию |выбора времени проведения опытов оценки токсического действия химичес- ких веществ в течение суток.
Данные исследования были проведены в связи с тем, что было известно о существенной суточной зависимости показателей жизнедеятельности инфузорий о
Опыты проводили следующим образом.
Суспензию инфузорий помещали в камеру, воздействовали температурным скачком до 28°С с измерением в течение 5 мин термочувствительности энергозатрат на движение клеток в популяции в различное время суток. Результаты приведены на фиг„ 4, где график 1 - термочувствительность энергозатрат, а график 2 - вариабильность. Популяция находилась в экспоненциальной фазе роста.
Учитывая длительность проведения токсикологического анализа, которая включает собственно время инкубации 30-60 мик и время измерения параметров движения клеток в популяции (для десяти концентраций оно составляет X мин,, где 5 - премя оценки одной пробы), что з общем составляет Порядка 80-110 минут, необходимо, например, проводить испедования в период между 14 ч. 30f и 16 ч 30 суточного времени, так как именно в это время в меньшей степени сказываются суточные влияния на параметр термочувствительности энергозатрат на движение клеток в популяции. На фиг, 4 эта область заштрихована, в которой наблюдается состояние устойчивого равновесия с Если же г технологических позиций требуется проводить оценку токсичности в другое время, то необходимо учитывать суточную динамику реакции тест-объекта в виде соответствующих поправок, что, в свою очередь, обеспечит воспроизводимость и сопоставимость оценок токсического действия в опытах биотестирования.
Пример 4„ По обоснованию длительности проведения опыта (инкубации) при оценке токсического действия химических веществ на инфузории.
Пробы микроорганизмов инкубировали при 21-22°С в присутствии заданной концентрации токсикантов, после чего измеряли энергозатраты на движение клеток в популяции. На фиг. 5
представлены в качестве примера результаты экспериментов действия токсикантов при 22°С„ где график 1 - с концентрацией 0,3 мг/л Си+5 , график 2-е концентрацией |,5 мг/л , до график 3-е концентрацией 7,5 мг/л , Все значения достоверны с величиной 99,9.
Как видно из фиг. 5, в интерва- 45 лах 30-60 мин инфузории изменяют свои параметры движения достаточно, чтобы . сделать вывод о токсическом действии. Длительность инкубирования более 60 мин ограничивается требованием экспресс- „ ности контроля, а менее 30 мин - величиной ошибки в динамике и требованием завершения фазы переотройки стимуляции.
Пример 5. По обоснованию к-зи- терия токсического эффекта по анализу ., параметрической чувствительности в краткосрочных опыта} с использованием подвижных микроорганизмов - инфузорий Tetrahymena pyriformis.
Q 0 5
0
5
о
5 „ .
.,
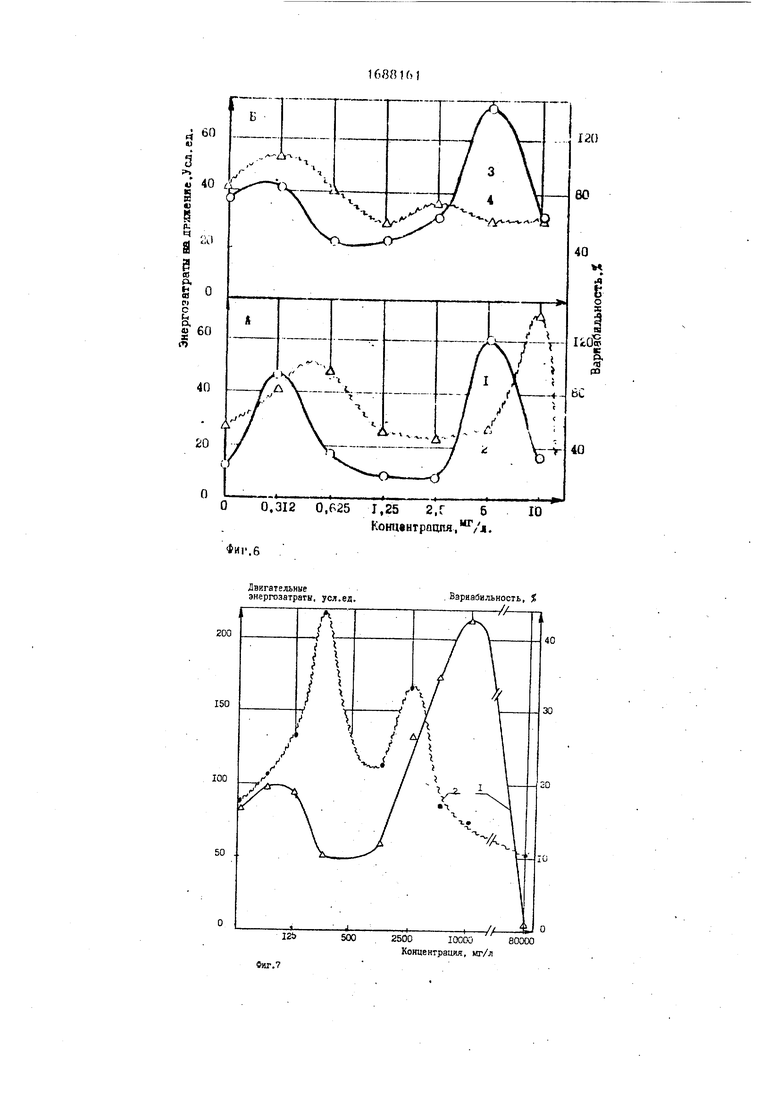
Инкубацию инфузорий с химическим веществом проводили при температуре 21-22 С в течение 60 мин, скячок температуры устанавливали равным 6°С от 22 до 28 С и измеряли параметр термочувствительности энергозатрат на движение клеток в популяции в течение 4 мин. Результаты действия ионов меди представлены на фиг. 6, где график 1 и 2 соответствуют энергозатратам и вариабильности для популяции в экспоненциальной фазе роста, а график 3 и 4 - соответственно для популяции в стационарной фазе роста. Экспоненциальную фазу роста наблюдали для 4-5- дневной культуры.
Из фазовой зависимости видно, что термочувствительность энергозатрат имеет два явно выраженных максимума - первый при 0,312 мг/л Си+ и второй - при 5 мг/л (для экспоненциальной и стационарной фазы роста культуры). При этом параметр вариабильности для экспоненциальной фазы имеет также два ярко выраженных пика при 0,6 мг/л и 10 мг/л , а для стационарной фазы наблюдается один пик при концентрации 0,312 мг/л, причем второй пик не наблюдали при концентрации 10 мг/л , а лишь наблюдали некоторую тенденцию увеличения вариабильности в зоне концентраций 2,5 мг/л . Из этого следует, что по вариабильности можно оценивать состояние исходной популяции Этот показатель отражает внутренние свойства популяции в плане возможности перестройки своих энергетических характеристик. Для опытов биотестирования предпочтительно использовать популяцию, находящуюся в экспоненциальной фазе роста, так как наличие второго пика варнлбильности в зоне токсического воздействия химического вещества отражает более выраженную картину гибели организмов, С другой стороны разрешимость пиков чувствительности, которая определяется по формуле
К М/2/Т,;
где Д1/2 - ширина пика на полувысоте;
L - расстояние между пиками, для популяции в экспоненциальной фазе роста намного выше, А именно, первый пик в экспоненциальной базе имеет размытость 33,0%, второй - 28,8%, а в стационарной - соответственно 56,3 и 46,3%.
В качестве другого примера действия химического вещества на фиг 7 приведены результаты реакции инфузори на этиловый спирт, где график 1 - чув ствительность энергозатрат инфузорий, а график 2 - вариабильность их отклика Популяция в экспоненциальной фазе роста.
Из фиг. 6 и 7 следует, что нижнюю границу токсического действия вещества определяют по первому пику параметрической чувствительности энергозатрат на движение клеток в популяции а максимально допустимую концентрацию химического вещества - по второму пику параметрической чувствительности
Сопоставляя значения соответствующих концентраций, делаем вывод, что для меди диапазон концентрации имеет значение 0,312 и 10 мг/л, а для этилового спирта - 62,5 и 10000 мг/л.
Таким образом, использование данно го критерия определения уровня токсического воздействия позволяет количе- ственно оценивать токсический эффект и биологическую активность испытываемых веществ в краткосрочных опытах при высокой объективности, достоверности и воспроизводимости анализа.
Предлагаемый способ может быть реализован на любой другой установке, которая позволяет получать информацию о скорости движения, подвижности клеток в популяции в реальном масштабе времени методом корреляционно-допле- ровской спектроскопии с анализом температурной чувствительности параметров движения.
Использование способа наиболее эф- фек-тивно в задачах оперативного контроля качества водной среды методом биотестирования в связи с особой важ- ностью решения проблемы охраны окружающей среды Кроме того, его целесо- образно использовать при скрининге вновь синтезируемых химических веществ, например в медицине, ветеринарии, сельском хозяйстве, пищевой, химической и парфюмерной промышленнос- тях.Особое значение использование данного способа имеет при биомониторинге и оценке состояния водных систем в экстремальных ситуациях воздействия, например, в особый период.
Таким образом, измерение параметрической чувствительности параметров движения клеток в популяции путем контроля флуктуации рассеянного света
,.
jg 5
0
5 0
.Q г
5
0
рвиж гщимися клетками микроорганизмов метолом корреляционно-доплеровской спектроскопии позволяет с боттьшой точностью оценить реакцию тест-объекта в реальном масштабе времени в условиях краткосрочных опытов. При этом получают объективную информацию о движении клеток с получением количественных характеристик энергозатрат-популяции на движение клеток.
Выбор режимов измерения практически исключает влияние на результаты эффектов фототаксиса, суточного ритма, кинетики переходных процессов на температурный скачок с учетом фазы развития популяциио
Наличие большой статистики выборки ,при анализе рассеянного света движущимися организмами позволяет Получать статистически достоверные сдвиги энергозатрат на популяционном уровне при исследованиях токсических эффектов на подвижных микроорганизмах (гидробион- тах) .
Формула изобретения
1. Способ определения токсического воздействия химических веществ, содержащихся в водной среде, на культуру пла-нктонных гидробионтов, предусматривающий культивирование планктонных гидробионтов в опытных и контрольных термостатируемых камерах, введение в опытные камеры исследуемой среды, выдерживание культуры гидробионтов в присутствии исследуемой среды, измерение при выдерживании средней скорости движения по ансамблю гидробионтов в опыте и контроле методом корре- ляционно-доплеровской спектроскопии, оценку отношения числа подвижных гидробионтов в культуре к числу неподвижных соответственно п опыте и контроле, оценку по полученным данным величины энергозатрат гидробионтов на движение и суждение о токсическом воздействии исследуемой среды по величине энергозатрат гидробионтов на движение в опыте, отличающийся тем, что, с целью повышения точности оценки за счет определения уровней токсического воздействия исследуемого вещества и сокращения расхода исследуемой среды и культуры гидробионтов, во время выдерживания культуры гидробионтов в присутствии исследуемой среды осуществляют изменение температуры среды содержания гндробиотп ов н опыте и контроле, а и процессе измерения дополнительно оценивают концентрацию гилро- бионтов в зоне наблюдения, строят гра фик зависимости пепичнны энергозатрат гидробионтов от концентрации исследуемого вещества в исследуемой среде, величину энергозатрат гидробионтов на движение Q) оценивают но формупе
У)
d s VV о.п; с(о)рп N v| г; . сГо),, ;
де v
ол
J
( ОП
v - средняя скорость движения по ансамблю гидробионтов ч зоне наблюдения в опыте н контроле,мкм/с;
15
ц - отношение числа подвижных
гидробионтов к числу не- 2 до 28°С.
2„ Спосо щийся туры содерж вляют путем
5
подвижных в опыте и контроле, отн. ед ; с;(о) ,г(о) - концентрация гидробионО) К
тов в зоне наблюдения,
уел .ед..,
при этом нижнюю границу токсического действия исследуемого вещества в среде определяют по первому пику величины энергозатрат гидробионтов на движение в культуре по графику, а максимально допустимую концентрацию исследуемого вещества в среде - по второму пику величины энергозатрат.
2„ Способ по п„ 1, отличающийся тем, что изменение температуры содержания гидробионтов осуществляют путем повышения температуры с
термочувствительность энергозатрат,усд, ед
ел оо
е п
со
вариабильность, %
Энергозатраты на движение клеток, усл.ед.











| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки токсического действия химических веществ, содержащихся в водной среде | 1987 |
|
SU1482887A1 |
| СПОСОБ ОЦЕНКИ ТОКСИЧНОСТИ ЗАГРЯЗНИТЕЛЕЙ ВОД ДАЛЬНЕВОСТОЧНЫХ МОРЕЙ | 2001 |
|
RU2215290C2 |
| СПОСОБ ОЦЕНКИ ТОКСИЧНОСТИ ЗАГРЯЗНИТЕЛЕЙ ВОД ДАЛЬНЕВОСТОЧНЫХ МОРЕЙ | 2001 |
|
RU2220415C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БЕЗОПАСНОСТИ ПИЩЕВЫХ ИНГРЕДИЕНТОВ С ПОМОЩЬЮ КЛЕТОЧНЫХ ТЕСТ-СИСТЕМ | 2015 |
|
RU2604802C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БЕЗОПАСНОСТИ ПРОБИОТИЧЕСКИХ МИКРООРГАНИЗМОВ С ПОМОЩЬЮ КЛЕТОЧНЫХ ТЕСТ-СИСТЕМ | 2015 |
|
RU2604804C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦИТОТОКСИЧНОСТИ АНТИГЕНОВ Burkholderia pseudomallei in vitro | 2011 |
|
RU2465592C1 |
| СПОСОБ БИОЛОГИЧЕСКОГО ОБЕЗЗАРАЖИВАНИЯ НЕПРОТОЧНЫХ ВОДОЕМОВ ОТ ПАТОГЕННОЙ И УСЛОВНО-ПАТОГЕННОЙ МИКРОФЛОРЫ | 2001 |
|
RU2193531C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ПОЧВЫ МЕТОДОМ БИОТЕСТИРОВАНИЯ С ИСПОЛЬЗОВАНИЕМ РАВНОРЕСНИЧНЫХ ИНФУЗОРИЙ PARAMECIUM CAUDATUM EHRENBERG | 2011 |
|
RU2482478C2 |
| СПОСОБ ОЦЕНКИ ТОКСИЧНОСТИ БАКТЕРИАЛЬНЫХ АНТИГЕНОВ | 2004 |
|
RU2281507C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ СРЕДЫ ПО СТЕПЕНИ УГНЕТЕНИЯ РОСТА ТЕСТ-КУЛЬТУР МИКРООРГАНИЗМОВ | 2014 |
|
RU2570637C1 |

Изобретение относится к водной токсикологии и может быть использовано для биологического контроля качества сточных вод и вод в водоемах. Целью изобретения является повышение точности оценки за счет определения уровней токсического воздействия исследуемого вещества и сокращения расхода исследуемой среды и культуры гид- робионтов. Методом корреляционно- доплеровской спектроскопии оценивают величину энергозатрат планкто нных гидробионтов на движение в период температурного скачка среды их содер - жания с 22 до 28°С. Строят график зависимости величины энергозатрат от концентрации исследуемого вещества в исследуемой среде. Нижнюю границу токсического действия исследуемого вещества определяют по первому пику ве- с личины энергозатрат гидробионтов на движение, а по второму пику - максимально допустимую концентрацию исследуемого вещества. 1 з.п. Л-лы, 7 ил., 1 табл,, (Л
Вариабильность, %
1688161
Мигательные энергозатраты, усл.ед.
О о 2 4 б 8 ю 11 ь is IB го гг и
Вретсдток,час Фиг. U
и
и
s
к о н
&
о
а
1,0
90
Время, мин
8
S
«
sc
O
Варяайильность.$
| Способ оценки токсического действия химических веществ, содержащихся в водной среде | 1987 |
|
SU1482887A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1991-10-30—Публикация
1987-12-11—Подача