Известен способ получения кортикоидных соединений, исходя из 17α-оксипрегненолона, который после формилирования бромируют и дегидробромируют с последующими окислением по Оппенауэру и омылением.
С целью упрощения процесса и повышения выхода продуктов, предложен способ получения кортикоидных соединений общей формулы:
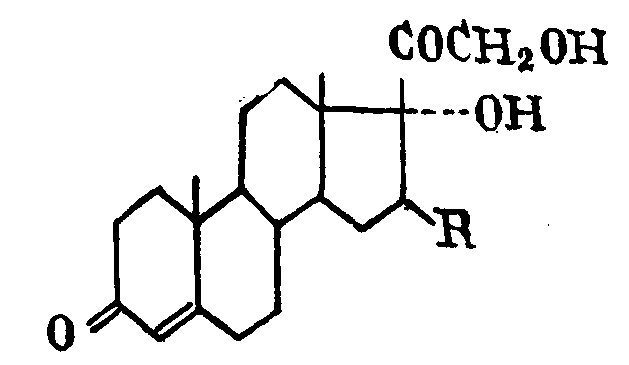
где R=H, α=СН3, β=СН3, α=ОН и др., заключающийся в том, что 17α-оксипрегненолоны подвергают взаимодействию с одним молем брома при охлаждении в смеси хлористого метилена и пиридина, затем еще с одним молем брома при нагревании до 30° в смеси метанола и хлористого метилена в присутствии газообразного хлористого водорода. Образовавшийся трибромхлористоводородный комплекс обрабатывают бикарбонатом натрия.
Полученную смесь изомерных 5,6,21-трибромидов разделяют. Выделенный 5α,6β,21-три-бромид подвергают взаимодействию с йодистым натрием и ацетатом калия в среде ацетона, а затем с уксусной кислотой и на полученный 21-ацетат Δ5-прегнен-3β,17α,21-триол-20-она действуют бромом в среде хлористого метилена, ацетона и пиридина при охлаждении. Реакционную массу обрабатывают хромовой кислотой в водном растворе серной кислоты при 20°С, цинковой пылью в уксусной кислоте и соляной кислотой. Выход I (R=H) достигает 88%, считая на использованный 21-ацетокси-17α-оксилрегненолон. Окисление проводят также ферментативно.
Выделенный на первой стадии изомерный 5β,6α,21-трибромид 3β,17α-прегнандиол-3-она действием цинковой пыли в уксусной кислоте или хлоридом двухвалентного хрома превращают в исходный 17α-оксипрегненолон.
Пример 1. Смесь, состоящую из 66,4 кг 17α-оксипрегненолона, 498 г хлористого метилена и 3,32 л пиридина, охлаждают до 8°С и добавляют 33,2 кг брома в 33,2 л хлористого метилена. После кратковременного перемешивания реакционную массу нагревают примерно до 30°С и при перемешивании добавляют 33,2 л метилового спирта, а затем часть раствора 34,7 кг брома в 33,2 л хлористого метилена. Через полученную смесь барботируют безводный хлористый водород до начала бромирования в 21-м положении после быстрого добавления остатка раствора брома, а затем медленного добавления метилового спирта (66,4 л) и раствора 12,03 кг бикарбоната натрия в 498 л воды. Реакционную смесь охлаждают в течение 2 час до 0°С. Образовавшийся осадок промывают и высушивают, в результате чего получают 90-95 кг трибромида.
Маточный раствор собирают и выдерживают в спокойном состоянии до расслоения. Органический слой отделяют разбавляют метиловым спиртом уксусной кислотой и дебромируют цинковой пылью. Однако органический слой можно дебромировать и хлористым хромом (2) обычным способом. Регенерированный исходный продукт выделяют из реакционной смеси обычным способом.
Полученный трибромид (90-95 кг) суспендируют в 380 л ацетона совместно с 57 кг йодистого натрия и к суспензии добавляют часть (9,5 кг) всего предназначенного количества (135 кг) ацетата калия. После перемешивания в течение 1 час к суспензии добавляют 570 л ацетона, остаток (125,5 кг) ацетата калия и 9 кг уксусной кислоты. Всю эту смесь нагревают с обратным холодильником в течение 3 час, концентрируют и разбавляют 900 л воды. После последующего выделения и сушки получают 61-65 кг 21-ацетата 5-прегнен-3β,17α,21-триод-20-она, который можно при желании перскристаллизовать.
40 кг сухого ацетата прегнентриолона в 160 л хлористого метилена охлаждают до 5-8°С и добавляют 1,6 л. пиридина. Затем добавляют раствор 18 кг брома в 20 л хлористого метилена и ацетон (480 л) и раствор снова охлаждают до 0-5°С. К охлажденному раствору добавляют как можно быстрее раствор, состоящий из 15,77 кг хромовой кислоты, 16,0 л воды и 13,545 л серной кислоты (реагент Джонса), поддерживая температуру ниже 23°С. Продолжительность добавления должна быть около 10-15 мин. Перемешивание продолжают еще в течение 30 мин, после добавления всего реагента Джонса.
После этого добавляют 280 л хлористого метилена и 70 л воды, смесь перемешивают, нагревают до 30°С и выдерживают в спокойном состоянии до отделения слоя хлористого метилена. Этот слой промывают водой, 120 л метилового спирта, добавляют к нему 20 л уксусной кислоты и дебромируют 13 кг цинковой пыли обычным способом. После декантации растворителя с цинка устанавливают температуру, равную 30°С, добавляют 16 л концентрированной соляной кислоты, раствор перемешивают в течение 30 мин и добавляют к нему 700 л воды. Отделившийся при стоянии слой хлористого метилена отделяют и промывают 10%-ным раствором едкого натра, а затем водой до нейтральности. Раствор, содержащий хлористый метилен, упаривают до образования очень густой пасты, добавляют к нему 280 л ацетона и концентрируют до объема, равного примерно 120 л. Эту массу охлаждают до 0°С и при этой температуре перемешивают в течение 2 час, а затем профильтровывают и получают ацетат соединения с выходом 92-88% по весу в пересчете на примененный в качестве исходного 21-ацетокси-17α-окси-прегненолон, т. пл. 228-236°С.
Пример 2. Смесь, состоящая из 1 ч. 16α-метил-Δ5-прегнен-3β,17α-диол-20-она (т. пл. 245-250°С), 7 ч. хлористого метилена и 0,05 ч. пиридина при температуре около 8°С, реагирует с 0,5 ч. брома в 0,5 ч. хлористого метилена. После кратковременного перемешивания смесь нагревают до 35-38°С и добавляют к ней 0,2 ч. метилового спирта и некоторое количество 0,48 ч. брома. Эту реакционную смесь барботируют газообразным хлористым водородом до начала бромирования у С21 после добавления остального брома. После кратковременного перемешивания смесь охлаждают примерно до 10°С и осторожно добавляют к ней 0,365 ч. бикарбоната натрия к 1 ч. воды. Трибромид выливают при перемешивании в течение 1 час при 0-5°С, после чего его отделяют при фильтровании и промывают водой, в результате чего получают 16α-метил-5α,6β,21-трибромпрегнан-3β,17α-диол-20-она.
Выделенный 5α,6β-транс-трибромид (1 ч.) в 4 ч. ацетона и 0,1 ч. ацетата калия перемешивают при последующем добавлении 0,76 ч. йодистого натрия, а затем перемешивают еще в течение 1 час примерно при комнатной температуре. После этого добавляют ацетон (6 ч.), ацетат калия (1,6 ч.) и 0,1 ч. метилового спирта. Эту реакционную смесь нагревают с обратным холодильником в течение 3 час и концентрируют до удаления 6 ч. растворителя для повторного использования. К концентрату добавляют 2 ч. воды и перегоняют под вакуумом до удаления остатков ацетона. После добавления воды, охлаждения и фильтрования получают 21-ацетат 16α-метил-Δ5-прегнен-3β,17α,21-триол-20-она, ацетат 16-метилмонака, т. пл. 170-180°С. После очистки активированным углем в ацетоне т. пл. 180-185°С.
16α-метил-17α-оксилрегненолон - исходный продукт отделяют от цис- и 6β,5α-транс-бромидов стадии, вышеописанной бромирования следующим способом.
Экстракты, полученные с помощью хлористого метилена, и маточные растворы со стадии бромирования промывают до нейтральности, смешивают с метиловым спиртом и уксусной кислотой, смешанной с цинковой пылью, при температуре кипения. После перемешивания в течение 20-30 мин смесь нагревают с обратным холодильником, отстаивают и декантируют надосадочный раствор. Этот раствор концентрируют и охлаждают, в результате чего получают 16α-метил-17α-оксипрегненолон, который бромируют.
20 кг ацетата 16α-метилмонака в 80 л хлористого метилена охлаждают до 5°С и к раствору добавляют пиридин (0,8 л), а затем раствор 9 кг брома в 10 л хлористого метилена. После добавления ацетона (240 л) смесь охлаждают до 0-5°С и добавляют к ней раствор, состоящий из 7,88 кг хромовой кислоты, 8 л воды и 6,77 л серной кислоты, поддерживая температуру ниже 23°С. Всю смесь кратковременно перемешивают.
К реакционной смеси добавляют хлористый метилен (140 л) л 350 л воды, перемешивают и нагревают до 30°С. Отделенный после отстаивания органический слой промывают водой, разбавляют 60 л метилового спирта и 10 л уксусной кислотой и дебромируют после добавления 6,5 кг цинковой пыли. Отстоявшийся растворитель отделяют декантацией or цинка и при 30°С добавляют к нему 8,1 л концентрированной соляной кислоты. После перемешивания в течение 30 мин добавляют 350 л воды и отделяют слой хлористого метилена, который промывают 10%-ным раствором едкого натра, а затем водой до нейтральности. Раствор, содержавший хлористый метилен, упаривают до очень густой пасты, добавляют к ней 140 л ацетона и полученную смесь концентрируют. При охлаждении получают ацетат 16α-метилсоединения с хорошим выходом, т.пл. 98-103°С.
Пример 3. Смесь 35 г 5-прегнен-3β,16α,17α-триол-20-она (т. пл. 242-246°С) в 350 мл хлористого метилена я 9 мл пиридина перемешивают при медленном добавлении 16,8 г брома в 35 мл хлористого метилена. Затем добавляют 15 мл метилового спирта и продолжают перемешивание еще в течение 0,5 час. После этого добавляют еще одну порцию брома, эквивалентную 2 мл, и газообразный хлористый водород в количестве, достаточном для нейтрализации пиридина, и начинают бромирование у C21. При обесцвечивании смеси к ней добавляют остаток раствора брома по мере его потребления. Затем при перемешивании добавляют 20 мл метилового спирта и раствор 21 г бикарбоната натрия в 350 мл воды. После перемешивания выделяется 5α,6β,21-трибром-прегнан-3β,16α,17α-триол-20-он (35-40 г), т. пл. 120-130°С. [α]D=-29° (диоксан).
Из этой массы отделяют путем фильтрования хлористый метилен, который смешивают с 18 мл уксусной кислоты и 70 мл метилового спирта, а затем добавляют цинковую пыль. После перемешивания и нагревания с обратным холодильником в течение 15 мин выделяют 12 г триола, применяющегося в качестве исходного продукта.
К суспензии 15,8 г трибромида в 75 мл метилового спирта добавляют 8 г йодида натрия. Смесь перемешивают в течение 2 час при 35-40°С, разбавляют 50 мл воды и 75 мл хлористого метилена, а затем взбалтывают с раствором 7,5 г тиосульфата натрия в 15 мл воды. Органический слой отделяют и соединяют с экстрактом, полученным из водного слоя с помощью хлористого метилена, и эту смесь промывают в 50 мл теплой воды. Органический слой быстро отделяют, концентрируют и охлаждают, в результате чего выделяют 21-бром-5-прегнен-3β,16α,17α-триол-20-он (7,5-8,0 г); т. пл. 125-130°С. [α]D=-12° (диоксан).
При обработке фильтрата цинковой пылью, метиловым спиртом и уксусной кислотой выделяют 3 г 16α-оксипрегненолона.
Смесь 12 г 21-бромпроизводного, 18 г ацетата калия и 100 мл ацетона перемешивают и нагревают с обратным холодильником в течение 4 час; при этом большая часть ацетона перегоняется. При обработке продукта водой получают 10,5 г 21-ацетата-5-прегнен-3β,16α, 17α-21-тетрол-20-она (16α-оксимонак, т. пл. 186-188°С) [α]D=-30° (хлороформ).
Смесь, состоящую из 10 г 16α-оксимонака, 200 мг йода и 40 мл ацетона, нагревают с обратным холодильником в течение 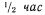 , концентрируют и разбавляют 50 мл воды, а затем к ней добавляют водный раствор 500 мг тиосульфата натрия. При разбавлении до 150 мл водой получают 10,5 г 16,17-ацетонида 16α-оксимонака; т.пл. 213-215°С, [α]D=+11° (хлороформ).
, концентрируют и разбавляют 50 мл воды, а затем к ней добавляют водный раствор 500 мг тиосульфата натрия. При разбавлении до 150 мл водой получают 10,5 г 16,17-ацетонида 16α-оксимонака; т.пл. 213-215°С, [α]D=+11° (хлороформ).
Смесь, состоящую из 8 г ацетонида и 4 мл пиридина в 50 мл хлористого метилена, охлаждают до 0-5°С и добавляют к ней раствор 3,4 г брома в 10 мл хлористого метилена, а также 100 мл ацетона. При 0-5°С быстро добавляют раствор 3,1 г хромовой кислоты, 5 мл воды и 2,7 мл серной кислоты при температуре ниже комнатной. После перемешивания в течение 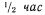 час добавляют 60 мл хлористого метилена, а затем 140 мл воды. Органический слой отделяют и дебромируют 25 мл метилового спирта, 4 мл уксусной кислоты и 2,8 г цинковой пыли. После добавления соляной кислоты и выдержки раствора при кратковременном перемешивании добавляют 150 мл воды. Органический слой концентрируют разбавляют ацетоном и еще раз концентрируют. После охлаждения получают 21-ацетат, 16,17-ацетонид 21-ацетата 4 прегнен 16α,17α,21-триол-3,20-диона.
час добавляют 60 мл хлористого метилена, а затем 140 мл воды. Органический слой отделяют и дебромируют 25 мл метилового спирта, 4 мл уксусной кислоты и 2,8 г цинковой пыли. После добавления соляной кислоты и выдержки раствора при кратковременном перемешивании добавляют 150 мл воды. Органический слой концентрируют разбавляют ацетоном и еще раз концентрируют. После охлаждения получают 21-ацетат, 16,17-ацетонид 21-ацетата 4 прегнен 16α,17α,21-триол-3,20-диона.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ 3β-АЦЕТОКСИ-17α-ГИДРОПЕРОКСИ-16α-МЕТИЛПРЕГНАНОВ ИЗ Δ-20-КЕТОСТЕРОИДОВ И СПОСОБ ПОЛУЧЕНИЯ 3β-АЦЕТОКСИ-17α-ГИДРОКСИ-16α-МЕТИЛПРЕГНАНОВ С ИСПОЛЬЗОВАНИЕМ 3β-АЦЕТОКСИ-17α-ГИДРОПЕРОКСИ-16α-МЕТИЛПРЕГНАНОВ | 2009 |
|
RU2418805C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТАТА 16α,17α-ЦИКЛОГЕКСАНО-5α,6α-ЭПОКСИПРЕГН-3β-ОЛ-20-ОНА | 2011 |
|
RU2480477C1 |
| 6-ОКСИМЫ 16А,17А-ЦИКЛОГЕКСАНОПРЕГНЕНОВ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ОПУХОЛЕВЫМ КЛЕТКАМ ЧЕЛОВЕКА | 2013 |
|
RU2534995C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНО-16α,17α-ЦИКЛОГЕКСАНОПРЕГН-4-ЕН-3,20-ДИОНА | 2014 |
|
RU2566366C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНГИДРОКОРТИЗОНА ИЛИ ЕГО ЭФИРОВ ИЗ 21-АЦЕТАТА ГИДРОКОРТИЗОНА | 2017 |
|
RU2664101C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТАТА 16α,17α-ЦИКЛОГЕКС-3',4'-ЕНОПРЕГН-5-ЕН-3β-ОЛ-20-ОНА | 2011 |
|
RU2480476C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6α-МЕТИЛГИДРОКОРТИЗОНА ИЛИ ЕГО ЭФИРОВ ИЗ 21-АЦЕТАТА ГИДРОКОРТИЗОНА | 2017 |
|
RU2663484C1 |
| СПОСОБ ПОЛУЧЕНИЯ 17-(3-ГИДРОКСИПРОПИЛ)-17-ГИДРОКСИСТЕРОИДОВ | 2008 |
|
RU2466137C2 |
| 18-МЕТИЛ-19-НОРАНДРОСТ-4-ЕН-17,17-СПИРОЭФИР (18-МЕТИЛ-19-НОР-20-СПИРОКС-4-ЕН-3-ОН) И ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ, КОТОРЫЕ ЕГО СОДЕРЖАТ | 2007 |
|
RU2440365C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТАТА 16α,17α-ЦИКЛОГЕКС-3',4'-ЕНОПРЕГН-5-ЕН-3β-ОЛ-20-ОНА | 2011 |
|
RU2472802C1 |
1. Способ получения кортикоидных соединений общей формулы (I)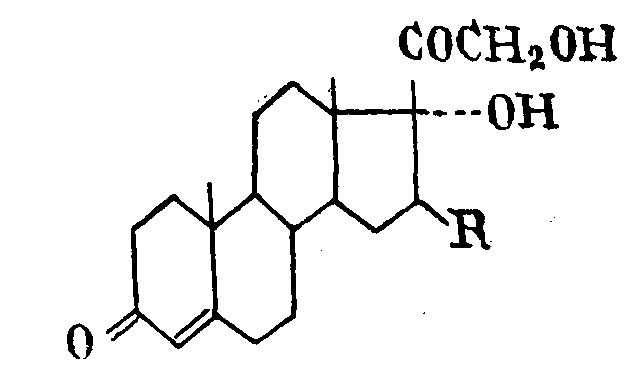
где R=H, α=СН3, β=СН3, α=ОН и др., на основе 17α-оксипрегненолонов с применением реакций бромирования и дегидробромирования в присутствии йодистого натрия и ацетата щелочного металла в среде органического растворителя, например ацетона, отличающийся тем, что, с целью упрощения процесса и повышения выхода продуктов, 17α-оксипрегненолоны непосредственно подвергают взаимодействию с бромом, полученный при этом трибромид разделяют на изомеры, из которых 5α,6β,21-трибромизомер подвергают взаимодействию с йодидом щелочного металла в присутствии ацетата щелочного металла с последующим микробиологическим или химическим окислением а изомерный 5β,6α,21-трибромид обрабатывают цинком и кислотой или хлористым хромом.
2. Способ по п. 1, отличающийся тем, что в качестве химического окислителя используют реагент Джонса.
Авторы
Даты
1968-11-19—Публикация
1964-07-08—Подача