Некоторые самосадочные озера Арало-Каспийского района, как например, озера Куули, Джаксы-Клыч, Чумыш-Куль содержат помимо поваренной соли, эксплоатируемой на товарную продукцию, весьма значительные запасы, измеряемые миллионами тонн, минерала астраханита, залегающего более или менее мощным пластом под поваренной солью.
Астраханит (Na2SO4MgSO4·4H2O), содержит сульфаты магния и натрия в виде двойной соли. Каждый из этих сульфатов в отдельности представляет ценный продукт - первый в стеклоделии, второй - для производства фибролитов, магнезиальных цементов и др., не говоря уже о ряде других химических производств.
До сих пор, однако, запасы астраханита не находят применения за неимением технологически осуществимого и экономически приемлемого метода выделения из него составных частей.
Согласно настоящему изобретению, предлагается способ раздельного получения сульфатов магния и натрия из астраханита путем нагревания раствора астраханита до 180-200°.
Этот способ основан на уменьшении растворимости сернокислого магния при нагревании его раствора, начиная от 90°. Растворимость MgSO4 по данным Robson′a следующая: при 90° - 34,5%, при 150° - 19,3%, при 180° - 5% и при 195° - 1,9%. В то же время растворимость сульфата натрия в этих пределах температуры даже несколько растет и остается во всяком случае в границах 30-31,5%.
При совместном присутствии растворимость обеих солей в данных температурных условиях должна несколько измениться, тем более, что в природном астраханите имеется примесь поваренной соли.
Насыщенный раствор сульфатов: магния и натрия содержит:
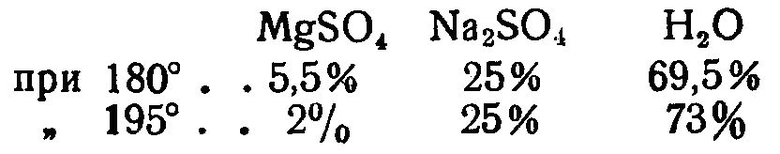
Первой операцией в предлагаемом процессе является прибавление к астраханиту такого количества воды, которое растворило бы весь сульфат натрия и оставило бы сульфат магния в твердой фазе в виде MgSO4·H2O (согласно его растворимости, определяемой указанными выше цифрами). На тонну астраханита (чистого) при 195° надо добавить 1065 кг воды, причем выделится 375 кг кизерита (MgSO4·H2O), содержащего 326 кг сульфата магния. Это составляет ~90%-й выход сульфата магния по отношению к количеству его 360 кг, содержащемуся в тонне астраханита. Оставшийся маточник можно переработать по двум вариантам.
По первому варианту после предварительного испарения воды в количестве 680 кг при охлаждении до 10° должно выделиться около 935 кг глауберовой соли с выходом около 97% сульфата натрия от содержания его в тонне астраханита.
Второй вариант заключается в прибавлении к маточнику поваренной соли (которая на астраханитовых озерах имеется всегда не только в виде товарной продукции, но и в виде отбросов) для высаливания серно-кислого натрия. Вместе с тем необходима выпарка для удаления излишка воды с тем, чтобы после охлаждения до 55-60° получить маточник близкий к насыщению.
Расчет показывает, что к маточнику после выделения кизерита надо прибавить на 1 т обрабатываемого астраханита около 100 кг хлористого натрия (а если он имеется в составе астраханита, то соответственно меньше) и испарить около 940 кг воды. При этом должно получиться около 430 кг безводного сульфата натрия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СИЛИКОКИЗЕРИТОВОГО ВЯЖУЩЕГО | 2006 |
|
RU2375323C2 |
| УСОВЕРШЕНСТВОВАННЫЕ УДОБРЕНИЯ С ПОЛИМЕРНЫМИ ВСПОМОГАТЕЛЬНЫМИ ВЕЩЕСТВАМИ | 2010 |
|
RU2551538C2 |
| Способ выделения бишофита из хлормагниевых рассолов | 1980 |
|
SU963954A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОРСКОЙ СОЛИ | 1997 |
|
RU2111167C1 |
| ГРАНУЛИРОВАННОЕ УДОБРЕНИЕ, СОДЕРЖАЩЕЕ ВОДОРАСТВОРИМЫЕ ФОРМЫ АЗОТА, МАГНИЯ И СЕРЫ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2455270C2 |
| СПОСОБ ОБЕЗВРЕЖИВАНИЯ ТОКСИЧНЫХ ПРОМЫШЛЕННЫХ ОТХОДОВ | 2009 |
|
RU2394659C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЙОДИРОВАННОЙ ПОВАРЕННОЙ СОЛИ | 1999 |
|
RU2179147C2 |
| СПОСОБ ВЫЩЕЛАЧИВАНИЯ ЦЕННЫХ МЕТАЛЛОВ ИЗ РУДЫ В ПРИСУТСТВИИ ХЛОРИСТОВОДОРОДНОЙ КИСЛОТЫ | 2005 |
|
RU2423534C2 |
| Способ переработки карналлитовых минеральных солей | 1958 |
|
SU129558A1 |
| СПОСОБ ВЫЩЕЛАЧИВАНИЯ ЦЕННЫХ МЕТАЛЛОВ ИЗ РУДЫ В ПРИСУТСТВИИ ХЛОРИСТОВОДОРОДНОЙ КИСЛОТЫ | 2005 |
|
RU2395594C2 |
Способ разложения астраханита водой, отличающийся тем, что, с целью, раздельного получения сульфата магния и натрия, астраханит обрабатывают при 180-200° водой в количестве, достаточном только для полного растворения сульфата натрия, раствор которого отделяют от твердого сульфата магния известными приемами.
Авторы
Даты
1939-09-30—Публикация
1938-04-05—Подача