сурьмой .0,4-1:1 и 0,03-0,3:1 соответственно.
1,1,1,3-Тетрафтор-3,3-дихлорпропан представляет собой бесцветную прозрачную жидкость с не резко вглраженным специфическим запахом,мол.вес 185,т.кип.64°С,удельный вес 1,51 г/с упругость пара при 215,4 мм рт.ст. Хорошо смегиивается со спиртом, эфиром, маслами. Предлагаемое соединение не горит, не образует взрывоопасных смесей с воздухом, химически инертно, не разлагается под действием света, кислорода воздуха, при. нагревании до ,не гидролизуется водой даже при температуре кипения. Благодаря высокой химической стойкости соединение согласно изобретению сохраняется длительное время без добавления стабилизатора .(в отличие от фторотана) 2.
Проведенные токсикологические исследования и расчеты показали, что 1,1,1,3-тетрафтор-З,3-дихлорпропан имеет относительно невысокую токсичность LCyo 175,0 мг/л. Это соединение обладает высокой наркотической активностью (средненаркотическая концентрация ЕС-г; 0,88 об.%), а широта наркотизирующего действия (терапевтический индекс) на 30% больше,- чем у известного наркотического средства фторотана. Коэффициент возможности ингаляционного отравления у предлагаемого соединения в 2,8 раза , чем у фторотана, поэтому оно менее опасно для лиц, находящихся в операционной.
Клиническая картина наркотическо-го действия 1,1,1,3-тетрафтор-З,3-дихлорпропана для белых крыс и мышей характеризуется быстрым периодом (1,5-2 мин) вхождения в наркоз без видимого периода возбуждения и быстрым пробуждением с восстановлением исходного состояния после прекращения подачи анестетика. При изучении характера воздействия на сердечнососудистую систему установлено, что предлагаемое соединение в концентрациях, применяемых для вводного наркоза (2,5-3,0 об.%), не оказывает существенного влияния на уровень артериального давления и. электрокардиограмму подопытных животных. Его действие на ультраструктуру печеночных клеток белых мышей незначительно.
Пример 1. В стеклянный барботер емкостью 2,5 л загружают 1200 1,1,1-трифтор-З-хлорпропана, затем добавляют50 мл дистиллированной воды в качестве катализатора и начинают подачу газообразного хлора. Скорость подачи хлора регулируют таким образом,чтобы не было проскока его на выходе из барботера. Реакционную зону освещают лампой накаливания мощностью 300 Вт. Температуру в барботере постепенно повышают от (в начале синтеза) до 45-50 С (в конце) . Образующийся хлористый водород отводят с верха барботера и нейтрализуют раствором щелочи. По окончании хлорирования реакционную смесь промывают 5%-ным раствором щелочи и высушивают над прокаленным хлористым кальцием. Всего пропускают 1352 хлора. Получают 1810 г 1,1,1-трифтор3,3,3-трихлорпропана сырца (см.состав в табл. 1).
Таблица 1




Чистый продукт выделяют ректификацией. Фторирование проводят в стеклянной колбе емкостью 1,5 л, снабженной месдалкой и обратным возду1лным холодильником..
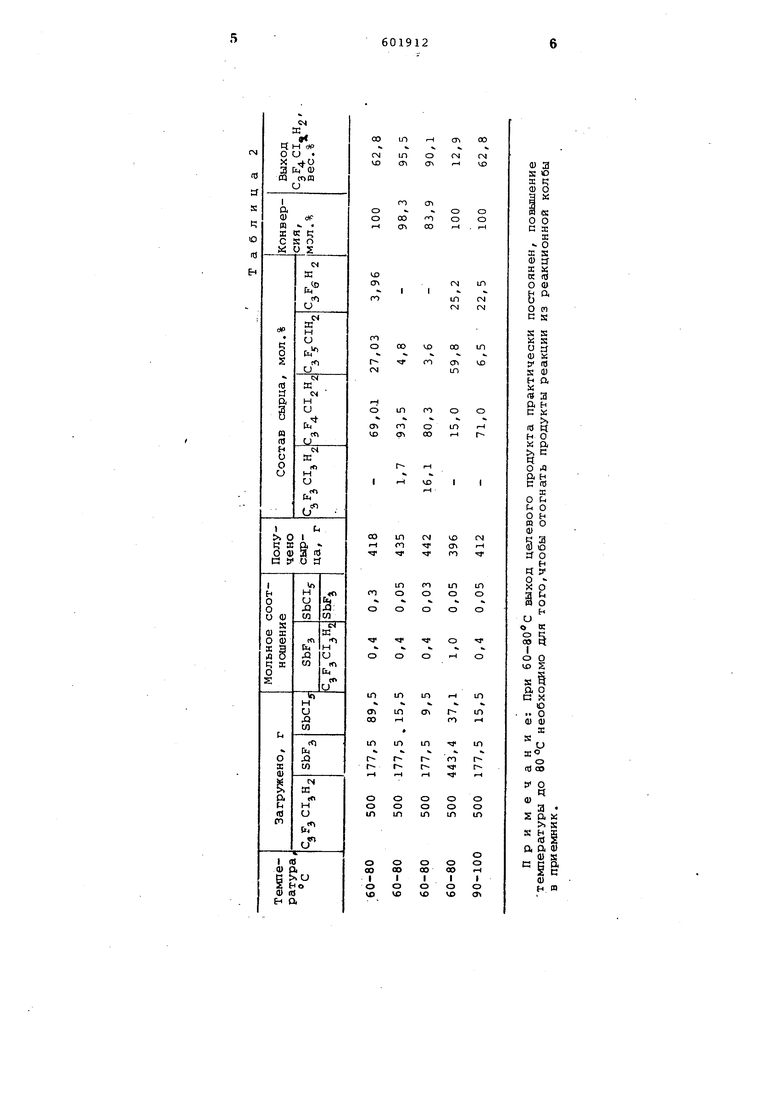
В колбу загружают 177,5 г трехфтористой сурьмы, добавляют. 15,5 г пятихлористой сурьмы и 500 г 1,1,1-трифтор-3,3,3-трихлорпропана. Смесь нагревают при постоянном перемешивании до 60-80С и эту температуру поддерживают в течение .всего опыта. Продукты фторирования через воздуишый холодильник отгоняют в два последовательно соединенных приемника, первый из которых охлаждается до , второй - до -70с. По окончании отгонки реакционную смесь, собранную в приемниках, промывают соляной кислотой (1:4), затем 5%-ным раствором щелочи и высушивают над прокаленным хлористым кальцием.
Получают 435 г сырца, %: 1,1,1-трифтор-3, 3, 3-трихлорпропан 1,7; 1,1,1,З-тетрафтор-З,3-дихлорпропан 93,5; 1,1,1,3,3-пентафтор-З-хлорпропан 4,8, Целевой продукт выделяют из смеси ректификацией. Дополнительные данные стадии фторирования приведены в табл. 2.
Для обоснования возможности применения 1,1,1,3-тетрафтор-З,3-дихлорпропана в качестве ингаляционного анестетика изучены,его наркотические свойства.
Наркотическую активность и токсичность предлагаемого соединения- изучают в острых экспериментах длительностью 30 и 120 мин на белых мышах и крысах при статической и динамической затравке в специальных камерах емкостью 30 и 100 л по общепринятым
1,1,1,3-Тетрафтор-3,3-дихлорпропан152,5 175(165-185,5) 192,0 12,8
65,0 83(65,4-103,7) 106,0 37,0
Фторотан
Сравнение наркотизирующей активности, токсичности и терапевтического индекса соединения согласно изоб0,88(0,66-1,22) 3,6(3,2-3,8) 4,1 0,89(0,71-1,11) 2,84(2,3-3,46) 3,2
fl р и м е р 2. Изучено влияние 1,1,1,3-тетрафтор-З,3-дихлорпропана на артериальное давление (АД) и электрокардиограмму (ЭКГ) белых крыс. АД измеряют ртутным манометром на левой сонной артерии, ЭКГ регистрируют на чернильно-пишущем электрокардиографе (модель 061) в трех стандартных отведениях. Животных готовят к эксперименту под легким гексеналовым наркозом. Изучаемые показатели регистрируют через каждые 10 мин. Исходный уровень кровяного давления в опытах 120-125 мм рт.ст. В период .введения животного в состояние наркоза давление практически не изменяется, через 10 мин оно равчо 115 мм рт. ст. и через 30-45 мин - то же. К концу эксперимента АД снижается до 105 мм рт.ст. Дальнейшее понижение АД (ниже 100 мм рт.ст.) не наблюдается. В то же время при воздействии-фторотана А уже через 10 мин снижается до 88,
в фармакологии и токсикологии методам. Критериями при сравнительной оценке служат, величины средненаркотических (ECjo) и среднесмертепьных (CLj концентраций,терапевтический индекс.и коэффициент возможности ингаляционного отравления (КВИО).
Сравнение токсичности 1,1,1,3-тетрафтор-3,3-дихлорпропана и фторотана в острых опытах при ингаляционной затравке в течение 2 ч дано в табл. 3.
Таблица
ретению и фторотана при ингаляционном воздействии в течении ЗО мин дано в табл. 4,
Таблица 4
iepes 30 мин до 70 и в конце опыта равно 60 мм рт.ст. Наркоз 1,1,1 3тетрафтор-3,3-дихлорпропаном сопровождается .умеренно выраженной бради- кардией. Нарушение ритма и другие явления изучаемого соединения на ЭКГ не выявлены.Прекращение подачи анестетика приводит к быстрому (в течение 5-10 мин) восстановлению АД и исчезновению брадикардии в течении 10-15 мин.
. Примерз. 1,1,1,3-Тетрафторт -3,3-дихлорпропан оказывает значительно меньшее токсическое влияние на печень/ чем Фторотан. В оцытах на белых мышах изучено действие предлагаемого соединения на структуру и функцию печеночных клеток. После однократного ингаляционного воздействия 1,1,1,3-тетрафтор-З,3-дихлорпропана в концентрации 2,5-3,0 об% животные были забиты декапитацией через 1, 4, 5 2.4 ч, 3 и 6 суток. В качестве основных методов исследования используют электронную микроскопию и гистоавторадиографию (введение меченой аминокислоты - -метионина). Полученные данные сравнивают с результатами воздействия на печеночную паренхиму известного анестетика - фторотана, проведенного в аналогичных условиях.
В первые 4 ч после ингаляции фторотана в печени подопытных-животных наряду с гепатоцитами, имеюрдами нормальную ультраструктуру, имеется значительное число клеток с выраженной редукцией гранулярной цитоплазматической сети (ответственной за синтез экспортного белка) и деформацией митохондрий . Уменьшается число зерен гликогена. Через 24 ч от начала опыta определяют гибнущие гипатоциты. Йа автографах в цитоплазме неповрежденных печеночных клеток выявлено увеличение включения s -метионина, что расценивают как компенсаторную реакцию в ответ на повреждение. К первым суткам (в момент наиболее выраженной деструкции) количество радиоактивной аминокислоты в гепатоцитах снижается по сравнению с печенью Интактных животных. В последующие сроки (3-6 сутки) отмечается нормализация ультраструктуры печеночных клеток, однако уровень белкового обмена не возвращается к контрольному уровню вплоть до конца опыта.
По сравнению с фторотаном ингаляция 1,1,1,3-тетрафтор-З,3-дихлорпропана вызывает значительно меньшие нарушения ультраструктуры гепатоцитов. Редукция гранулярной цитоплазматической сети и повреждение митохондрий выявлены в немногих печеночных клетках и менее выражены, чем пр фторотане. Как правило, в таких клетках сохраняется гликоген. В первые сутки гепатоциты с необратимыми повреждениями клеточных органелл не выявлены. В дальнейшем (3-6 сутки) развиваются репаративные процессы, которые приводят к восстановлению субмикроскопической организации печеночных клеток. При авторадиографическом изучении бел кового обмена, в течение всех сроков опыта количество треков меченого предшественника над цитоплазмой гепатоцитов не отличается от контрольных значений.
Следовательно 1,1,1,3-тетрафтор-3,3-дихлорпропан оказывает по сравнению с фторотаном слабо выраженное действие на ультраструктуру печеночных клеток белых мышей. Наблюдаемые изменения клеточных органелл (гранулярЯОй цитоплазматической сети и митохондрий) обратимы и не оказывают заметного воздействия на уровень белкового обмена печеночной ткани.
Формула изобретения
CFj - CHg - CFCIg , проявляющий наркотическую активность,
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1979-05-15—Публикация
1976-04-21—Подача