Изобретение относится к области аналитической.химии, в частности, к спектрофотометрическому методу oripeделения ультра малых количеств железа посредством экстракции органическим растворителем ионного ассоциата анионного комплекса железа с органическим катионом с последующим образованием роданидного комплекса в органической фазе и может быть приме нено для контроля качества сырьевых продуктов для оптического стекловарения, волоконной оптики, монокриста лов, непосредственно оптических сред а также других химических веществ высокой очистки. Известен способ фотометрического определения железа, вк.шочающий экстракцию внутрикомплексного соединения железа из 0,1 н. раствора соляной кислоты раствором (2-этилгексил)фосфорной .кислоты в циклогексане. Для образования окрашенного комплекса в экстракт вводят спиртовый раствор роданида калия. Метод применен для определения О,1-0,5 мг железа. Применение спиртового-раствора роданида калия затрудняет очистку препарата роданида, что приводит к высокому холостому опыту. Для определения долей микрограмма железа метод не применим l. Известен экстракционно-фотометрический способ определения железа в виде его смешанных {комплексов с роданид-ионом и монооктиланилинбензидфосфоновой кислотой (МОАБФ) . Способ основан на экстракции хлорофоменным раствором МОАБФ смешанного комплекса железа из водного раствора, содержащего 0,3 М роданида калия и 0,15 М по соляной кислоте. Кислотность в методике строго фиксирована. Оптическую плотность экстракта измеряют при Я-450 нм, молярный коэффициент погашения - 5200, относительное стандартное отклонение 0,2-1,8, Определению мешает уран, молибден и оксалат-ион. Образование окрашенного роданидно-МОАБФ-комплекса железа происходит в водной фазе в присутствии элементов-матрицы, маскирукнцих агентов и т.д. Недостатком способа является . невысокая чувствительность f 5200, закон Бугера Ламберта-Бера выполняется в интервале 5-1000 мкг/10 мл экстракта, открываеьвлй минимум 0,5 мкг/мл. Наиболее близким по технической сущности и достигаемому результату
является способ экстракционно-фотометрического определения железа, основанный на экстракции комплексной кислоты или ее соли железа из семинормального раствора соляной кислоты или хлорида лития гексоном. К экстракту добавляют 0,5 г роданида аммония и определяют железо по интенсивности окраски роданидного комплекса.. Чувствительность метЬда 5 мкг железа. К недостаткам метода следует отнести низкую чувствительность метода, узкий интервал концентраций соляной кислоты или хлорида лития, применение дорогого и сложноочищаемого растворителя. Экспериментальная проверка этого метода показала,что окраска органической фазы не устойчива как за счет образования стойких эмульсий,так и за счет разложения роданидного соединения железа. Метод обладает низкой воспроизводимостью
Сз.
Недостатки названных методов объясняются тем, что во всех случаях применяются растворители с высокой координационной способностью и недоста/гочно высокой полярностью. Эти свойства растворителей, являющихся средой для образования роданидной формы соединения железа, препятствую образованию роданидной гексаформы железа, обладающей наиболее глубокой окраской. Поэтому ни один иэ выше названных методов не применим для определения 10 железа, что . необходимо для решения поставленной задачи.
Цель изобретения - повьаиение чувствительности и селективности определения железа в кислотно-солевы растворах.
Поставленная цель достигается предложенным экстрационно-спеКтрофотометрическим способом определения микроколичёств железа, основанным на экстракции железа из растворов соляной кислоты, хлоридов металлов или смешанных кислотно-солевых растворов с общей концентрацией хлорид-ионов от 1,5 до 8 г«ион/л раствором тетрафенилфосфоний хлорида в апротонном полярном органическом растворителе. В качестве, полярного растворителя используют дизслорэтан, или нитробензол или хлороформ. Полученный экстракт, содержащий ионный ассоциат тетрафенилфосфония с анионрым хлоридным комплексом железа, обрабатывают водным/роданидным раствором.
При этом происходит замещение хлорид-ионов в анионной части ассоциата и образование гексароданоферрит-иона, являкнцегося наиболее интенОивно окрашенным из всех роданидных /форм железа. Окраска развивается почти мгновенно и остается неизменно IB течение нескольких часов.
светопоглощения экстракта лежит при длине волны 505 им. Закон БугераЛамберта-Бера выполняется в интервал концентрации железа от 0,2 до 10 мкг в 4 мл экстракта. Состав комплекса, определенный экспериментально, можно выразить следукхцим соотношением: тетрафенилфосфоний, железо, роданидион-2,4-1,6. Открываемый минимум :при толщине поглощаемого слоя 10 мм соответствует 0,05 мкг/мл железа. Коэффициент молярного погашения равен 3,8-10 . Пpимeняe vIый раствор тетрафенилфосфония хлорида после анализа может быть регенерирован отмывкой водой и слабым раствором соляной кислоты и применяется многократно.
Таким образом, замена экстракции компле.ксного соединения железа кислородсодержащими растворителями с вы.сокой донорной активностью на экстракцию ионного ассоциата с тетрафенилфосфонием в апротонном полярном растворителе приводит к расширению области экстракции железа, повышению чувствительности на порядок, высокой стабильности окраски экстракта, допустимости всех применяемых реактивов. Предпочтительно использовать в качестве растворителей дихлорэтан, нитробензол, хлороформ. Выполненное исследование показало, что определе нию железа предлагаемым методом сопутствующие примеси не мешают.
Пример. Определение примеси железа в оксиде лантана для оптических целей.
Навеску препарата (2 г) помещают в делительную воронку, в которую предварительно напито 6 мл воды, 3-5 капель перекиси .водорода и добавляют 7 мл 7,5 н;раствора соляной кислоты, содержимое воронки перемешивают до полного растворения, дают раствору остыть и экстрагируют железо 4 мл 0,015 М раствора тетрафенилфосфония хлорида в дихлорэтане в течение 2-3 мин. После расслаивания фаз, органическую тщательно отделяют и переносят в делительную воронку меньшего размера, в которую предварительно прилито 2 МП 1-2 М раствора роданида аммония, и встряхивают воронку в течение 1 мин. Органическую фазу отделяют, переносят в 1 см кюве и измеряют оптическую плотность на. спектрофотометре при Л 505 нм с экстрактом холостого опыта в качеств раствора сравнения. Количество железа находят по калибровочному графику построенному в тех же условиях.
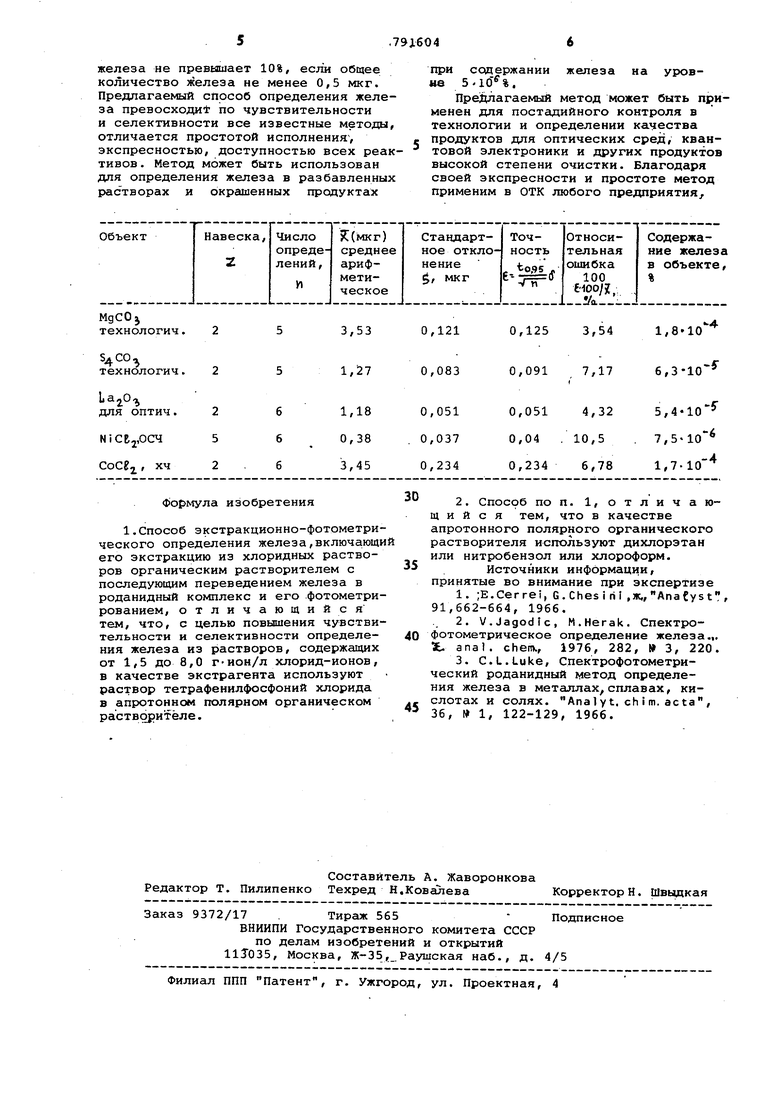
По аналогичной схеме эыполйяется анализ большой группы солей и оксидо в том числе карбоната магния, карбонта стронция, хлоридов никеля и кобальта. Результаты анализов приведен в таблице. Ошибка определения
железа не превьяшает 10%, если общее количество железа не менее 0,5 мкг. Предлагаемый способ определения железа превосходи по чувствительности и селективности все известные методы, отличается простотой исполнения экспресностью, доступностью всех реактивов. Метод может быть использован для определения железа в разбавленных растворах и окрашенных продуктах
при содержании железа на уровне 5..
Предлагаемый метод может быть применен для постадийного контроля в технологии и определении качества продуктов для оптических сред, квантовой электроники и других продуктов высокой степени очистки. Благодаря своей экспресности и простоте метод применим в ОТК любого предприятия

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения палладия | 1982 |
|
SU1087889A1 |
| Способ концентрирования примесей металлов из растворов солей никеля | 1979 |
|
SU861323A1 |
| Способ определения ванадия (У) | 1989 |
|
SU1714501A1 |
| Способ определения меди | 1991 |
|
SU1797024A1 |
| Способ определения германия | 1990 |
|
SU1734010A1 |
| Способ экстракционно-фотометрического определения перхлорат-ионов | 1978 |
|
SU710917A1 |
| Способ определения цинка | 1990 |
|
SU1758550A1 |
| Способ определения мышьяка (III) | 1990 |
|
SU1734009A1 |
| Способ спектрофотометрического определения титана | 1982 |
|
SU1018909A1 |
| Способ определения цинка | 1981 |
|
SU960124A1 |

Формула изобретения
а ющ и и с я тем, что в качестве апротонного полярного органического растворителя используют дихлорэтан или нитробензол или хлороформ.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1980-12-30—Публикация
1979-01-08—Подача