Изобретение относится к способу получения новых производных урацила обладающих противоопухолевым действием, которые могут найти применени в медицине. 1йзвестен способ получения замещенных 5-фторурацила путем ацилиров ния 5-фторурацила соответствующими галоидпроизводными 1. Целью изобретения является спосо получения новых биологически активных производных 5-фторурацила.. Поставленная цель достигается описываемым способом получения производных урацила общей формулы О ЯИ „л/ где R.,R и R, - каждый представляе собой атом водорода или метильную группу, R - представляет собой насьаценную или ненасыщенную алкильную группу с прямой или разветвленной цепью. Способ заключается в том,что соединение формулы (II): где R , R.TljH Кц имеют указанные выше значения, X - представляет собой атом галогена или низшую алкоксигруппу, подвергают взаимодействию с 5-фторурацилом. Исходный реагент - 5-фторурацил может быть использован в виде соли щелочного металла. Реакцию можно проводить с использованием таких органических растворителей, как диметилформамид, диметилацетамид и т.п. Реакция протекает эквимолярно и предпочтительно,при температуре, лежащей в интервале от комнатной температуры, до, приблизительно, 5о9с. Ниже приведены результаты испытания на острую токсичность и проти
воопухолевую активность ,E oi токоферилкарбонил-5-фторурацила (соединение А). В качестве стандартных медикаментов выбраны ЕТ-207 и 5-фторурацил (5 FU).
Результаты испытания на острую
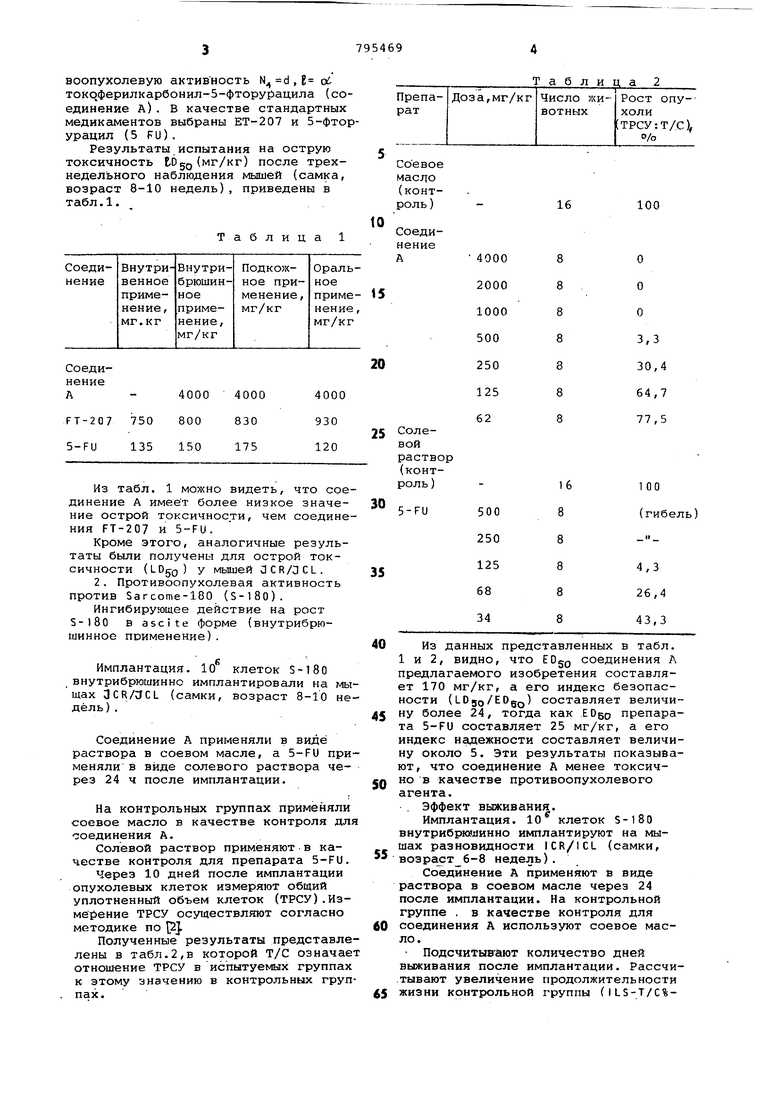




Имплантация, 10 клеток S-180 внутрибргошинно имплантировали на мьтщах 3CR/;JCL (самки, возраст 8-10 недель ) .
Соединение А применяли в виде раствора в соевом масле, а 5-FU применяли в виде солевого раствора через 24 ч после имплантации,
На контрольных группах применяли соевое масло в качестве контроля для соединения А,
Солевой раствор применяют в качестве контроля для препарата 5-FU.
Через 10 дней после имплантации опухолевых клеток измеряют общий уплотненный объем клеток (ТРСУ).Измерение ТРСУ осуществляют согласно методике по р}
Полученные результаты представлелены в табл.2,в которой Т/С означает отношение ТРСУ в испытуемых группах к этому значению в контрольных группах.
1 и 2, видно, что EDgQ соединения Л предлагаемого изобретения составляет 170 мг/кг, а его индекс безопасности (Юдо/ЕОдд) составляет величину более 24, тогда как ЮБО препарата 5-FU составляет 25 мг/кг, а его индекс надежности составляет величину около 5. Эти результаты показывают, что соединение А менее токсично в качестве противоопухолевого агента.
Эффект выживания. Имплантация. 10 клеток S-180 внутрибрюшинно имплантируют на мышах разновидности ICR/1CL (самки,
возраст 6-8 недель).
Соединение А применяют в виде раствора в соевом масле через 24 после имплантации. На контрольной группе . в качестве контроля для
соединения А используют соевое масло.
Подсчитывают количество дней выживания после имплантации. Рассчи.тывают увеличение продолжительности
жизни контрольной группы (ILS-T/C%100). Полученные результаты представлены в табл,3.
Таблица 3
Данные, представленные в табл.3, подтверждают тот факт, что соединение А оказывает действие при единичном применении 1/8 LО до.
Влияние на рост твердой опухоли в результате орального применения.
Имплантация. 1,8x10 клеток S-180 имплантируют подкожно на мышах разновидности ICR/ICL (самки, возраст 6-8 недель).
Каждое из лекарств применяют орально в виде раствора в сафлоровом масле через 3 ч после имплантации.
На контрольной группе для каждого из лекарств в качестве контроля Применяют сафпоровое масло.
Через 20 дней измеряют вес опухоли и рассчитывают отношение веса опухоли к весу опухоли у контрольной группы (Т/С,%).
Полученные результаты представле,ныв табл.4.
Таблица 4
100
106
87
33
Продолжение табл,
5008
47
10008
38
20008
36
148
258
FT-207
0
508
269
100
58
8 8 8 8 8 8 8
5
43
200
400
34
156
10
5-FU
0
20
55
Ч 63
40
80
5
Как следует из данных табл.4, минимальная эффективная доза соединения А составляет величину порядка 250 мг/кг, тогда как это значение
0 для FT-207 составляет 100/мг/кг,а для соединения 5-FU-около 20 мг/кг, соответственно. Что касается отношений минимальной эффективной дозы C к токсичной дозе (LOgo) для каждого из лекарств , то для соединения А это значение составляет величину менее 1/16; для FT-207-1/10; а для соединения 5-FU - 1/6, соответственно.Поэтому, пригодность соединения Д вы- «
0 ше, чем у других лекарств..
Противоопухолевая активность на L-1210 лейкемию.
Эффект выживания.
Имплантация. 10 клеток. L-121 О
5 лейкемии внутрибрюшинно имплантируют на мышах разновидности COF. Ссамки, возраст 8-10 недель).
Соединение А внутрибрюшинно применяют в виде раствора триглицерида со средней длиной цепи (МСТ)через
0 24 ч после имплантации.
Каждое из лекарств 5-FU и FT-207 применяют также внутрибрюшинно в виде солевого раствора через |24 ч после имплантации. На контрольной груп5пе в качестве контроля для соединения А применяют МСТ. Солевой раствор применяют в качестве контрольного вещества для препаратов-5-FU и
FT-207.
О
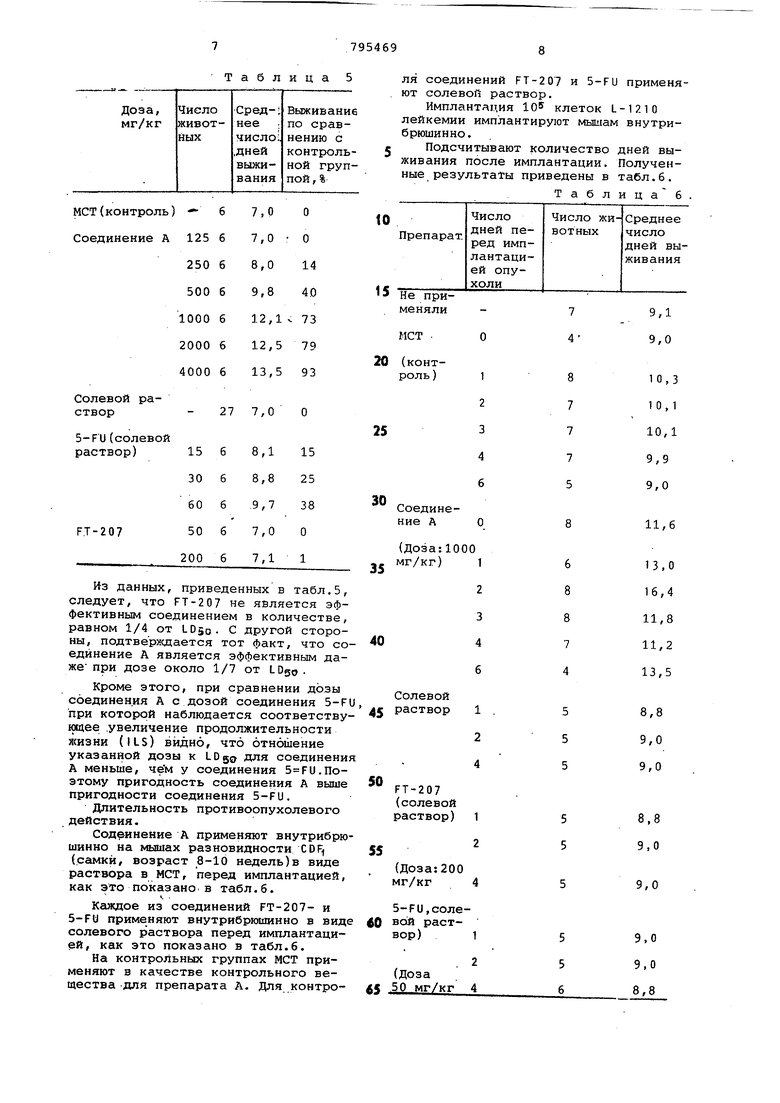
Определяют среднее время выживания после имплантации и рассчитывают увеличение продолжительности жизни :(ILS) по сравнению с контрольной группой. Полученные результаты представлены в табл. 5.
Из данных, приведенных в табл.6 видно, что соединение А дает эффект выживания как при применении в день имплантации клеток опухоли, так и за 1-6 дней перед имплантацией, а также, что соединение А проявляет противоопухолевое действие в течение 6 дней.
Как было отмечено выше, производные предлагаемого изобретения обладают значительно более низкой токсичностью и значительно более широким интервалом значений между токсичной дозой и эффективной дозой, чем это имеет место у соединений 5-FU и FT-207. Продолжительность действия производных предлагаемого изобретения более высока чем у -соединений 5-FU и FT-207.
Доза производных предлагаемого изобретения, когда они используются в качестве противоопухолевого агента, составляет 1-200 мг/кг в день, предпочтительно, 5-10 мг/кг для взрослых особей.
Производные предлагаемого изобретения могут применяться как орально так и парентерально. В качестве форм для применения могут использоваться порошки, гранулы, таблетки, капсулы, жидкости для инъекции,свечи и мази.
Такие рецептуры могут быть получены при использовании общепринятых эксипиентов обычными способами.
Пример. Синтез N iid , 1 oi токоферилкарбонил-5-фторурацила.
Получают суспензию добавлением 10,3 г (0,13 моль) 551-ного масляного раствора гидрида натрия к 100мл диметилформамида. Суспензию охлаждают до температуры ниже . К полученной суспензии медленно, по каплям при перемешивании, в течение 30 мин добавляют 150 мл раствора диметилформамида, содержащего 16,9 г (0,13 моль) 5-фторурацила-и палученный смешанный раствор вьщерживают в течение 1 ч при этих условиях.К этому раствору, медленно, по каплям при перемешивании,в течение 30 мин добавляют раствор 100 мл диметилформамида, содержащий 64,1 г (0,13 мол d,1-о -токоферилхлорформиата. Этотг раствор нагревают до и перемешивают еше в течение 1 ч. После пермешивания реакционному раствору дают охлаждаться до комнатной температуры, затем фильтруют. Фильтрат концентрируют при пониженном давлении.
Полученный в результате остаток в количестве 76 г дважды экстрагируют порциями бензола, по 300 мл каждая. Бензольный экстракт концентрируют при пониженном давлении. Полученный в / результате остаток в количестве 71 г перекристаллизовывают из этанола с получением целевого вещества в виде белого кристаллического порошка, имеющего температуру плавления 119120С. Выход64,7 г85%). Элементар0ный анализ соединения, имеющего предположительную формулу C Hj- FNjOs дал следующие результаты:
Вычислено,%: С 69,59; Н 8,76; N 4,77.
5
Найдено.%: С 69,44, Н 8,70; N 4,79.
ИК-спектр: (КВч).Три абсорбционные полосы поглощения соответствующие карбонильной группе, наблюдались в интервале 1700-1770 см .
0
Спектр ЯМР: (CDClj) : сГ 8,22 (,3a.b 8,0; Hj Н J; 2,60 (t 2; ); 2,09-2,0) (S 9 фенилметильная группа); 1,80-(, J 7Н2) ; 1 ,601,l8(); О ,9-0 , 8 (d 1 5) . Масс5спектр: М -586.
П р и м е р 2. Синтез Н, -(2,2,5, 7,8-пентаметилхроманил-6-карбонил)-5-фторурацила.
0
2,47 г (0,019 моль)-5-фторурацила и 5,13 г (0,019 моль) 2,2,5,7,8пентаметилхроманил-6-хлорформиатаподвергают реакции и последующей обработке согласно методике, описан5ной в примере 1. В результате полу-, чают целевое вещество в виде белого кристаллического порошка, имеющего температуру плавления 208-210С.
0
Выход 4,9 г (68,5%).
Элементарный анализ соединения предполагаемой формулы С Н FN О ;
Вычислено,%: С 60,63; Н 5,60; N 7,40..
Найдено,: С 60,75 Н 5,58;
5 N 7,41.
ИК-спектр :(КВч): три полосы аб;сорбц.ии, соответствующие карбонильной группе, наблюдали в интервале частот 1700-1770 см . Спектр ЯМР:
0 (дейтеропирндин) cr8,24(d 1 ,35ч,8,0; Hj, Hj,); 2,62 (1 2,); 2,08-2,04 ( фенилметильная группа),1,82 (,) 1,32(,метильная группа).
5
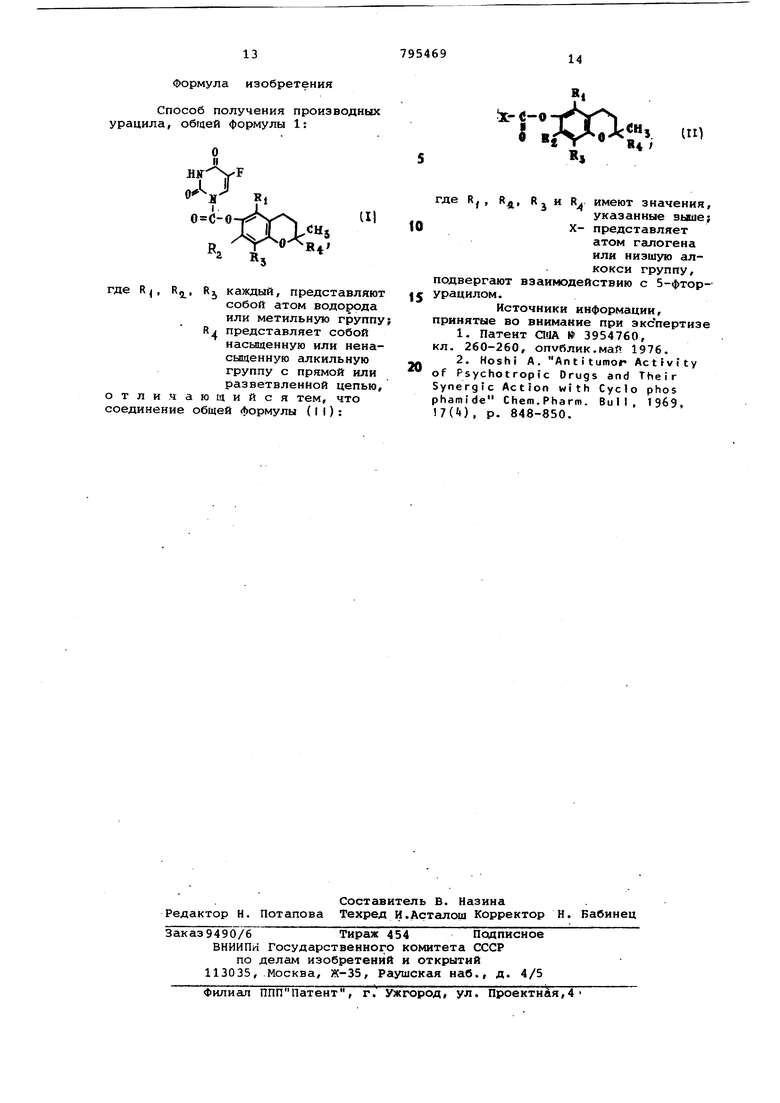
В табл, 7 даны соединения примеров 3-8. Формула изобретения Способ получения производных урацила, общей формулы 1: tj каждый, представляют , к, собой атом водорода или метильную группу RJ представляет собой насыщенную или ненасыщенную алкильную группу с прямой или разветвленной цепью, отличающийся тем, что соединение общей формулы (II): . i-€-o где Ri , R, R, и имеют значения, указанные выше; представляет атом галогена или низшую алкокси группу, подвергают взаимодействию с 5-фторурацилом. Источники информации, принятые во внимание при экспертизе 1,Патент QUA 3954760, кл. 260-260, опублик.май 1976. 2.Hoshi А. Antitumor Actfvity of Psychotropic Drugs and Their Synergic Action with Cyclo phos phamide Chem.Pharm. Bull, 1969, 17(), p. 848-850.
Авторы
Даты
1981-01-07—Публикация
1979-06-18—Подача