Данное изобретение относится к иммунологическому контролю злокачественных опухолей.
Данное изобретение относится к фармацевтическим композициям, увеличивающим или улучшающим эффективность известных антинеопластических средств или способов лучевой терапии посредством стимуляции иммунной системы онкологических пациентов.
Более точно данное изобретение относится к фармацевтическим композициям, включающим сочетание иммуностимулирующего средства и известного или экспериментального антинеопластического средства в качестве активных ингредиентов в смеси или сочетании с одним или несколькими разбавителями или эксципиентами.
В частности, данное изобретение также относится к сочетанию иммуностимулирующего средства и общепризнанных способов лучевой терапии для борьбы со злокачественными опухолями в смеси или сочетании с носителем или наполнителем, предназначенным для перорального или инъекционного пути введения.
Более конкретно объектом настоящего изобретения являются фармацевтические композиции, содержащие в качестве активных ингредиентов по меньшей мере одно иммуностимулирующее средство с заряженными или нейтральными группами общей формулы (I):
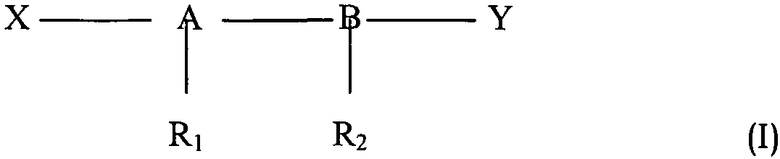
где
А-В представляют собой дисахариды,
X и Y представляют собой заряженные или нейтральные функциональные группы,
R1 и R2 представляют собой гидроксиацильные группы, которые могут быть ацилированы алифатической карбоновой кислотой,
применимые для борьбы со злокачественной опухолью вместе со способом лучевой терапии или вместе с известным антинеопластическим химиотерапевтическим средством, выбранным из группы, состоящей из алкилирующих средств, антиметаболитов, средств, действующих на микротрубочки, ингибиторов тирозинкиназы, в соединении или смеси с инертным нетоксичным фармацевтически приемлемым разбавителем или носителем.
Изобретение также относится к солям соединения общей формулы (I) с минеральным или органическим основанием, а именно фармацевтически приемлемым основанием.
Данное изобретение также относится к фармацевтической композиции, где иммунологически активное соединение представляет собой диацилированное соединение с заряженными или нейтральными группами общей формулы I:

где
А и В представляют собой β-(1,6)-связанный диглюкозаминовый дисахаридный скелет липида А формулы (II):
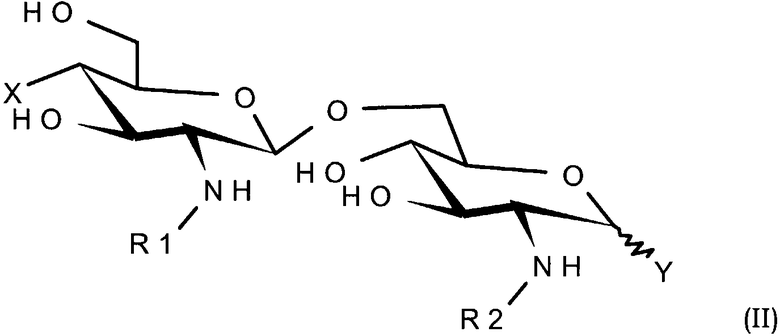
где
R1 и R2 каждый обозначает ацильную группу, являющуюся производной насыщенной или ненасыщенной, линейной или с разветвленной цепью карбоновой кислоты, имеющей от 2 до 24 атомов углерода, которая является незамещенной или содержащей один или более заместителей, выбранных из гидроксила, алкила, алкокси-, ацилокси-, амино-, ациламино-, ацилтио- и алкилтиогрупп.
Х обозначает нейтральную или заряженную группу, выбранную из следующих групп: дигидроксифосфорилокси, гидроксисульфонилокси, гидроксил, карбоксиалкокси, карбоксиалкилтио, карбоксиацилокси, карбоксиаминоацилокси или диаминоацилокси и аминоацилокси, и волнистая линия показывает α- или β-конфигурацию;
Y обозначает нейтральную или заряженную группу, выбранную из следующих групп: дигидроксифосфорилокси, гидроксисульфонилокси, гидроксил, карбоксиалкокси, карбоксиалкилтио, карбоксиаминоалкокси и аминоалкокси,
в сочетании с химиотерапией или биологической терапией, то есть стандартной или экспериментальной химиотерапией или иммунотерапией, или ионизирующим излучением, в смеси или в сочетании с одним или более нетоксичными, инертными, фармацевтически приемлемыми разбавителями или носителями.
Настоящее изобретение также относится к фармацевтическим композициям, в которых иммунологически активный ингредиент представляет собой триацилированные дифосфорилированные производные липида А структурной формулы (III):
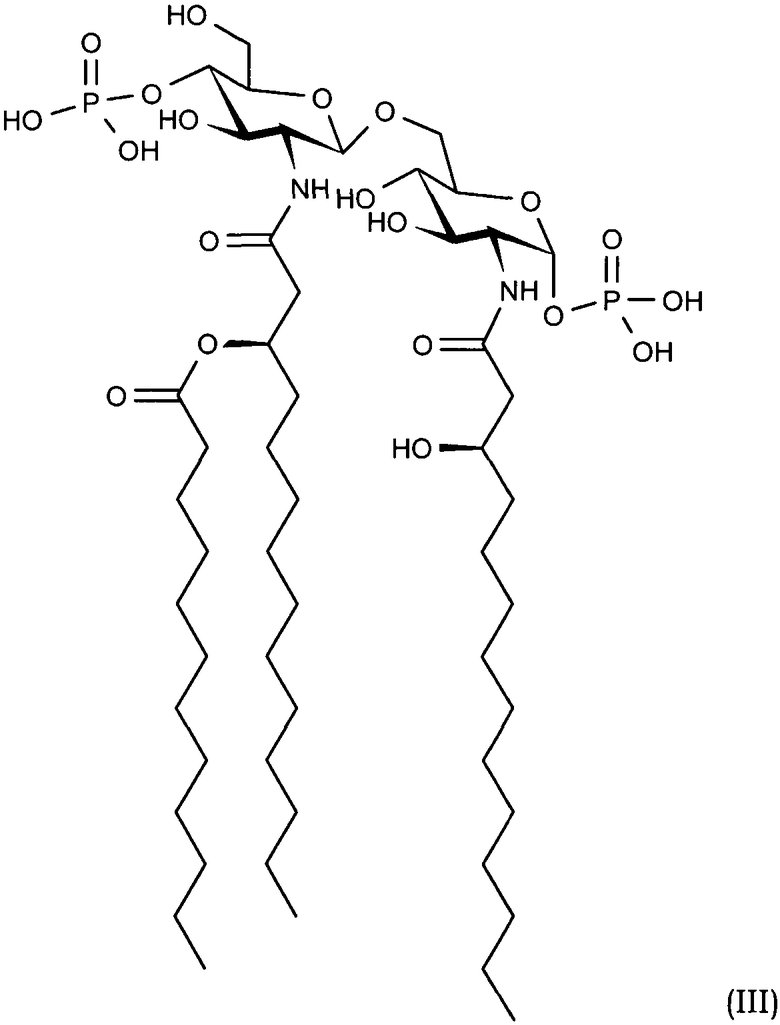
в сочетании или смеси с инертным, нетоксичным, фармацевтически приемлемым носителем или наполнителем.
Настоящее изобретение также относится к способам лечения злокачественной опухоли у теплокровных животных, включая людей, страдающих злокачественной опухолью, которые включают введение сочетания терапевтически эффективного количества смеси соединений общей формулы (I):

где
X, Y, A, B, R1 и R2 имеют вышеприведенные определения,
в сочетании с известным антинеопластическим средством, выбранным из группы, включающей любые из:
1) общепринятых или экспериментальных техник лучевой терапии или источника излучения, или химиосенсибилизатора,
2) одного или более средств, выбранных из группы, состоящей в качестве химиотерапевтического средства из алкилирующего средства, антиметаболического средства, средства, действующего на микротрубочки, ингибиторов тирозинкиназы,
в фармацевтически приемлемом носителе, эксципиенте или наполнителе, пригодном для перорального, парентерального, ректального, местного, подкожного или подслизистого пути введения.
Активные ингредиенты могут вводиться совместно в единичной стандартной дозировке или отдельно, или последовательно в отдельных стандартных дозировках, преимущественно в качестве набора, содержащего в отдельных контейнерах различные активные ингредиенты.
Данные фармацевтические композиции и способ их использования также основываются на широко признанных средствах, как и на заново развитых способах лечения неопластических заболеваний.
УРОВЕНЬ ТЕХНИКИ
Контроль злокачественных опухолей посредством иммунной системы
Здоровые клетки, нормально делящиеся, растут и, наконец, умирают, когда это необходимо, спланированным и хорошо контролируемым способом. Часто во время жизненного цикла случайно происходит, что индивидуальная клетка начинает развиваться бесконтрольно. Так как природа хорошо подготовилась, обычно на поверхности порожденных неконтролируемых клеток попутно возникают модифицированные антигены (антигены, ассоциированные с опухолью), которые обычно не присутствуют в нормальных неопухолевых клетках, таким образом позволяя в подавляющем большинстве случаев иммунной системе предотвратить появление многих злокачественных опухолей.
Опухолевые клетки могут остаться неопознанными иммунной системой
Однако некоторые опухолевые антигены представляют собой тканеспецифичные молекулы, общие для опухолевых клеток и здоровых клеток. Таким образом, данные слабые антигены не производят типичного вызова иммунитета. Дополнительно опухоли имеют различные признаки, которые делают сложными их распознавание и разрушение иммунной системой. Действительно, известные опухолевые клетки высвобождают иммуносупрессивные вещества (такие как, например, цитокин TGF-бета или простагландин PGE2), избегая иммунного распознавания.
Если иммунная система, вследствие какой-либо причины, не распознает опасность и не уничтожает пролиферирующие клетки, появляются злокачественные опухоли и метастазы.
Комбинирование иммунотерапии со стандартными химиотерапевтическими лекарствами
Когда диагностируется злокачественная опухоль, часто она является, к несчастью, не полностью излечимой посредством весьма агрессивных химиотерапевтических лекарств или способов, которые могут способствовать повреждению ослабленной иммунной системы человека.
Обычной практикой сегодня является применение иммуностимуляции (например, филграстим или NEUPOGEN®, лечение, которое стимулирует пролиферацию клеток крови, борясь с потенциальными осложнениями нейтропении), главным образом восстанавливая иммунную систему, часто сильно поврежденную посредством примененного химиотерапевтического средства или после лучевой терапии. Обычным рациональным стандартом является применение иммуностимулирующих средств в порядке восстановления “нормальной” клеточной формулы крови, избегая, насколько это возможно, оппортунистических инфекций у онкологических пациентов, подвергающихся противоопухолевой терапии.
Противоположно, в данной заявке предлагается, чтобы клиническое лечение иммуностимулирующим средством, представляющим собой производное триацилированного липида А проводилось до, одновременно или после применения широко признанных стандартов или экспериментальных противоопухолевых цитотоксических лекарств, или лечения посредством лучевой терапии в порядке улучшения эффективности противоопухолевого лечения, как показано ниже в примерах.
Тяжесть злокачественных опухолей
Злокачественные опухоли в настоящее время относятся к семейству пролиферативных заболеваний, которые убивают миллионы людей каждый год. Несмотря на современные достижения, такие как применение Gleevec®, остается необходимость в эффективных терапевтических средствах для борьбы со злокачественной опухолью и доля злокачественной опухоли может вырасти в дальнейшем на 50% - до 15 миллионов новых случаев к 2020 году (World Cancer Report, www.who.int/mediacentre/releases/2003/pr27/en/-40k).
В 2000 году злокачественные опухоли были ответственными за 12 процентов из около 56 миллионов смертей во всем мире от всех случаев. В 2000 году у 5,3 миллиона мужчин и 4,7 миллиона женщин развились злокачественные опухоли и в общей сложности 6,2 миллиона умерли от заболевания. Злокачественные опухоли остаются на третьем месте по летальности, после инфекционных и паразитарных заболеваний, с одной стороны, и коронарных заболеваний и заболеваний сердца, с другой стороны.
Рак легкого представляет собой наиболее распространенный рак в мире, представляя 1,2 миллиона новых случаев ежегодно: следующим является рак молочной железы - свыше 1 миллиона случаев; рак толстой и прямой кишок - 940000; желудка - 870000; печени - 560000; шейки матки - 470000; пищевода - 410000; головы и шеи - 390000; мочевого пузыря - 330000; злокачественная неходжкинская лимфома - 290000; лейкемия - 250000; простаты и тестикул - 250000; поджелудочной железы - 216000; яичников - 190000; почки - 190000; эндометрия - 188000; нервной системы - 175000; меланома - 133000; щитовидной железы - 123000; глотки - 65000; и заболевание Ходжкина - 62000 случаев.
Три ведущих вида рака различают три наиболее распространенные формы: рак легкого, ответственный за 17,8 процента всех летальных случаев, желудка - 10,4 процента и печени - 8,8 процента.
Основная терапия для борьбы со злокачественными опухолями
Большинство злокачественных опухолей классически лечатся:
- хирургическим путем,
- лучевой терапией,
- химиотерапией,
- и/или биологической терапией.
Хирургия
Во время данного вмешательства солидные опухолевые массы извлекаются из тела. Однако если уже имеются распространенные метастазы, данное лечебное вмешательство обычно становится неприменимым.
Лучевая терапия
Данный способ относится к применению излучения высокой энергии рентгеновских лучей, гамма-лучей, нейтронов и других источников уничтожения опухолевых клеток и уменьшения опухолей.
Данный способ может назначаться перед хирургическим вмешательством (новая вспомогательная терапия) для уменьшения опухоли, чтобы облегчить ее удаление. В другом случае лучевая терапия назначается после хирургического вмешательства (вспомогательная терапия) для разрушения каких-либо опухолевых клеток, которые могут оставаться в данной области.
Интересно, что недавно было продемонстрировано (De Ridder et al., Int J Radiat Oncol Biol Phys. 2003 Nov 1;57(3):779-86), что гипоксические клетки опухоли молочной железы (клетки ЕМТ-6) показывают уменьшенную чувствительность к излучению (от 0 до 20 Гр) 16 часов после активации NF-kB (и, следовательно, оксидом азота). Так как триацилированные производные липида А показали стимуляцию даже более высоких уровней оксида азота из макрофагов, чем LPS, установлено, что триацилированные производные липида А будут сильными противоопухолевыми средствами при применении в сочетании с лучевой терапией. Макрофаги изменяют радиосенситивную активность липида А (de Ridder et al., Int J Radiat Oncol Biol Phys. 2004 Oct 1;60(2):598-606), таким образом предполагая новую роль для иммунных клеток в реакции опухолевых клеток на лучевую терапию. Эффект одного триацилированного производного липида А соответственно общей формуле I показан ниже в данной системе.
Химиотерапия
Химиотерапия обычно назначается циклами: период лечения, один или более дней, последующий восстановительный период, несколько дней или недель, затем следующий период лечения и так далее. Здесь предлагается, что между или совместно с данными химиотерапевтическими циклами (предназначенными для уменьшения опухоли и выявления опухолевых антигенов) может выполняться стимуляция иммунной системы посредством триацилированных соединений по изобретению.
Рациональная поддерживающая химиотерапия
Любое эффективное и безопасное химиотерапевтическое средство уничтожит опухолевые клетки и не нанесет ущерба расположенным рядом здоровым клеткам. Данное может достигаться в теории посредством определения у опухолевых клеток уникальных свойств, которые не обнаружены в нормальных тканях.
Стратегия снижения клинического применения химиотерапевтических лекарств основывается на простом фактическом наблюдении, что большинство опухолевых клеток растет быстрее, чем нормальные клетки. Поэтому представляется рациональным нацеливание на некоторые специфические ферменты или клеточные элементы, связанные с циклом клеточного роста. Данная цитотоксическая стратегия предполагает, что быстрорастущие клетки были бы более поражены, а клетки, растущие медленно, подверглись бы меньшему поражению. Данный рациональный подход действительно применяется для развития многих химиотерапевтических средств, которые в настоящее время используются в клинике.
Химиотерапевтические средства являются активными преимущественно в течение фаз S и М клеточного цикла.
Ограничения химиотерапии
Помимо недостаточной клинической эффективности, данная стратегия имеет собственные токсикологические ограничения, так как некоторые нормальные клетки (такие как, например, пролиферирующие Т- и В-клетки) также нуждаются в отделении, когда это необходимо. Действительно, когда пациент страдает от поражения почек или печени и не может поэтому нормально элиминировать химиотерапевтическое средство, введение рекомендованного количества лекарства может также проявлять токсичность для пациента, неспособного метаболизировать и/или выделить его. Поэтому являются абсолютно необходимыми регулировки дозы, избегая неприемлемой токсичности или субтерапевтического дозирования.
Фармакокинетика для онкологических пациентов часто является очень сложной и, иногда, ограничивает методики химиотерапии пациентов.
Как изменить эффективность химиотерапии и уменьшить побочные эффекты
Здесь рассматривается, что адекватная и своевременно контролируемая комбинированная клиническая терапия широко признанными или экспериментальными химиотерапевтическими лекарствами, используемая в первую очередь для уменьшения количества и уничтожения опухолевых клеток (и, таким образом, потенциально обнаруживая связанные с опухолью антигены), последующая неспецифическая иммуностимуляция триацилированным соединением по настоящему изобретению изменяет эффективность онкостатического лекарства и дает возможность приобретения иммунологической (специфичной) памяти для достижения освобождения от клеток, производящих ассоциированный с опухолью антиген, и также ограничивает уровень наблюдаемых побочных эффектов, обеспечивая, например, снижение количества введений и/или доз химиотерапевтического лекарства.
Основные химиотерапевтические лекарственные средства
Текст адаптирован из
A Chemotherapy Primer: Why? What? and How?, Julia Draznin Maltzman, M.D, November 5, 2003, OncoLink, Abramson Cancer Center of the University of Pennsylvania
Химиотерапевтические средства могут разделяться на следующие классы:
- Алкилирующие средства
Например, Алретамин, BCNU, Бусульфан, Кармустин, CCNU, Хлорамбуцил, Хлорметин, Карбоплатин, Цисплатин, Циклофосфамид, Дакарбазин, Эстрамустин, Фотемустин, Ифосфамид, Ломустин, Мафосфамид, Мелфалан, Митомицин, Нимустин, Оксалиплатин, Прокарбазин, Стрептозоцин, Тиотепа, Лобаплатин, Мибоплатин и т.д.
- Интеркаланты/ингибиторы топоизомеразы II
Азакрин, Дактиномицин, Даунорубицин, Доксорубицин, Ацетат Эллиптиния, Эпирубицин, Идарубицин, Митоксантрон, Пирарубицин.
Пликамицин
Вабрубицин
Зорубицин
и т.д.
Они являются известными как обладающие высокой и необратимой кардиотоксичностью.
- Ингибиторы топоизомеразы I
Иринотекан и Топотекан
- Антиметаболиты
Они подклассифицированы на три класса:
- антагонисты фолиевой кислоты,
- аналоги пурина, и
- аналоги пиримидина.
Их примерами являются Капецитабин, Кладрибин, Цитарабин, Флударабин, Фторурацил (5-FU), Гемцитабин, Меркаптопурин, Метотрексат, Тиогуанин и т.п.
- Средства, действующие на микротрубочки (например, алкалоиды и токсоиды)
Паклитаксел, Доцетаксел, Таксол, Винбластин, Винкристин, Виндезин, Винорелбин и т.п.
- Ингибиторы тирозинкиназы
Ингибиторы протеинкиназы используются в качестве противоопухолевых терапевтических средств и биологических инструментов в сигнализации клеток. Двумя характерными членами данного семейства соединений являются Мезилат Иматиниба (Gleevec®) и Гефитиниб (Iressa®).
- Другие химиотерапевтические средства: они представляют собой ферменты или антибиотики, такие как:
- Аспарагиназа,
- Блеомицин,
Алкилирующие средства
Алкилирующие средства участвуют в общем механизме действия ядовитых горчичных соединений азота, первоначально разработанных для военного применения. Поэтому неудивительно, что такие средства показывают полный набор неблагоприятных результатов.
Они действуют на отрицательно заряженные участки ДНК. Посредством связывания ДНК изменяются репликация и транскрипция, прекращается клеточная активность и клетки начинают погибать. Данный класс противоопухолевых лекарств является очень мощным и применяется при многих типах опухолей (солидные опухоли и лейкемия). К несчастью, описанные побочные эффекты являются значительными (преимущественно снижение выработки спермы, прекращение менструаций и могут служить причиной стойкого бесплодия). Алкилирующие средства могут служить причиной вторичных опухолей. Наиболее распространенной вторичной опухолью является лейкемия (острая миелоидная лейкемия), которая может возникать спустя годы после окончания терапии.
Производные природных металлов, такие как производные платины, например цисплатин, демонстрируют некоторую активность против опухолей, главным образом против рака легкого и тестикул. Наиболее значительна токсичность цисплатина в повреждении почек. Второе поколение производных платины, называемое карбоплатин, имеет мало почечных побочных эффектов и может быть подходящим заменителем режимов, содержащих цисплатин. Оксалиплатин представляет собой третье поколение производных платины, которые активны при раке толстой кишки и не обладают ренальной токсичностью. Однако его главными побочными эффектами являются нейропатии.
Как предоставляется ниже, примеры на различных моделях, в которых используется аналог триацилированного липида А после лечения алкилирующими средствами, такими как циклофосфамид или цисплатин, показывают очень хорошую синергическую противоопухолевую активность. В предоставленных примерах “in vivo” (см. соответствующие разделы) в использованных условиях каждое средство индивидуально не дает удовлетворительных противоопухолевых результатов, и, довольно неожиданно, неспецифическая стимуляция иммунной системы посредством триацилированных производных липида А после первого неспецифического химиотерапевтического лечения предоставляет обнадеживающие противоопухолевые результаты, заслуживающие тестирования в клинических противоопухолевых испытаниях.
Интеркаланты/ингибиторы топоизомеразы II
Данные соединения формируют комплекс с ферментом и ДНК и таким образом ингибируют повторное лигирование ДНК. Они применяются преимущественно в лечении злокачественных заболеваний крови, раке молочной железы, раках пищеварительного тракта, раках половых органов, бронхиальных или конъюнктивальных саркомах. Их главными неблагоприятными эффектами являются миелосупрессия, рвота, кардиотоксичность и облысение.
Ингибиторы топоизомеразы I
Они специфично ингибируют топоизомеразу-I и, таким образом, транскрипцию и репликацию во время фазы S клеточного цикла.
Они преимущественно применяются для борьбы с раком толстой и прямой кишок. Их основными неблагоприятными эффектами являются миелосупрессия, нейтропения, рвота, облысение и холинергический синдром.
Антиметаболиты
Они применяются преимущественно против трофобластической карциномы, рака молочной железы, рака яичника, острой лейкемии, остеосаркомы, лимфомы.
Их основные неблагоприятные эффекты касаются преимущественно миелосупрессии, токсичности в отношении кожи и слизистых оболочек, диареи, рвоты.
В 1948 году Farber продемонстрировал, что аналог фолиевой кислоты вызывает ремиссию детской лейкемии. Затем были синтезированы другие аналоги, ингибирующие ключевые ферментативные реакции. Антиметаболиты вмешиваются в нормальные пути метаболизма, включая необходимые для производства новой ДНК (фаза S клеточного цикла). Антифолатом, наиболее широко применяющимся в противоопухолевой терапии с активностью против лейкемии, лимфомы, рака молочной железы, рака головы и шеи, сарком, рака толстой кишки, рака мочевого пузыря и хориокарцином, является метотрексат, который ингибирует ключевой фермент (дигидрофолатредуктаза), необходимый для синтеза ДНК.
Другим широко применяющимся антиметаболитом, нарушающим синтез ДНК, является аналог пиримидина 5-фторурацил, который преобразуется в монофосфат фтордезоксиуридина (5-FdUMP), который блокирует фермент тримидилатсинтазу, необходимый для эндогенного синтеза пиримидиновых оснований (С и Т). Пример сочетания триацилированного соединения структурной формулы I с 5-фторурацилом будет предоставлен ниже. Соединение имеет широкий диапазон активности, включающий рак толстой кишки, рак молочной железы, рак головы и шеи, рак поджелудочной железы, рак желудка, рак заднего прохода, рак пищевода и гепатомы. Однако 5-фторурацил метаболизируется посредством фермента дигидропиримидиндегидрогеназы (DPD), который не выражен у небольшой популяции пациентов. Когда данные пациенты получают инъекцию данного химиотерапевтического средства, они получают острую и тяжелую интоксикацию (супрессия костного мозга, тяжелая гастроинтестинальная токсичность и нейротоксичность, которая может включать судороги и даже кому). Капецитабин представляет собой пероральное соединение про-5-фторурацила, которое имеет сходные потенциальные побочные эффекты. Преметрексед представляет собой антифолатное антинеопластическое средство, препятствующее репликации клетки, предназначенное для инъекций (Alimta®), производимое Eli Lilly and Company.
Другие антиметаболиты, ингибирующие синтез ДНК и восстановление ДНК, включают: Цитарабин, Гемцитабин (Gemzar®), 6-меркаптопурин, 6-тиогуанин, Флударабин и Кладрибин.
Средства, действующие на микротрубочки (например, алкалоиды и анатоксины)
Алкалоиды, такие как Винбластин, Винкристин, Виндезин или Винорелбин, связывают тубулин, цитоплазматический белок и таким образом препятствуют формированию митотических веретен и блокируют митоз в метафазе.
Винкристин, винбластин и винорелбин были экстрагированы из листьев растения барвинок, Vinca rosea. Они преимущественно применяются для лечения злокачественных болезней крови (включая болезнь Ходжкина), аэродигестивных раков, нефробластом, раков молочной железы.
Их главными неблагоприятными эффектами являются миелосупрессия, тошнота, рвота, облысение, жгучесть, нейропатия и нейротоксичность.
Таксаны, впервые выделенные из коры Тихоокеанского тиса Taxus brevifolia в 1963 году, являются специфичными для фазы М клеточного цикла. Семейство включает паклитаксел и доцетаксел. Таксаны с высоким сродством связываются с микротрубочками и ингибируют их нормальное функционирование. Они являются эффективными против рака молочной железы, рака легкого, рака головы и шеи, рака яичника, рака мочевого пузыря, рака пищевода, желудка и рака предстательной железы. Данные средства, однако, снижают количество клеток крови.
Их главными неблагоприятными эффектами являются преимущественно миелосупрессия (нейтропения) и лимфатический отек.
Ингибиторы тирозинкиназы
Ингибитор тирозинкиназы Гефитиниб (Iressa®, AstraZeneca) применяется для лечения прогрессивного немелкоклеточного рака легкого (NSCLC), наиболее распространенной формы рака легкого в Соединенных Штатах.
Гефитиниб блокирует действие рецепторов EGF на клетках определенных раков легкого и имеет некоторые видимые эффекты против данных раков.
Некоторые распространенные побочные эффекты Iressar® включают в числе других: диарею, сыпь, прыщи, сухость кожи, тошноту, рвоту, зуд, снижение аппетита, слабость и потерю веса.
Ингибитор тирозинкиназы Мезилат Иматиниба (Gleevec®, Novartis) одобрен для лечения пациентов с несомненно неоперабельными и/или метастазирующими злокачественными стромальными гастроинтестинальными опухолями (GIST) и для лечения хронической миелоидной лейкемии (CML).
Мезилат Иматиниба представляет собой ингибитор сигнальной трансдукции, который действует посредством поражения активности тирозинкиназ. Активность одной из данных тирозинкиназ, известной как c-kit, считается управляющей ростом и делением большинства GIST. Иматиниб представляет собой ингибитор рецептора тирозинкиназ для тромбоцитарного фактора роста (PDGF) и фактора стволовой клетки (SCF), c-kit и ингибирует PDGF- и SCF-опосредованные клеточные события. In vitro иматиниб ингибирует пролиферацию и вызывает апоптоз в клетках GIST, который экспрессирует активация c-kit мутации.
Большинство пациентов, принимавших Gleevec® в клинических исследованиях испытывали побочные эффекты, такие как тошнота, задержка жидкости (отечность вокруг глаз, на стопах и т.п.), мышечные спазмы, диарея, рвота, кровоточивость, боли в мышцах и костях, сухость кожи, головная боль, утомление, суставные боли, нарушение пищеварения и одышка.
Другие химиотерапевтические средства
Блеомицин представляет собой малый белок, выделенный из грибка Streptomyces verticillus. Механизм его действия сходен с антрациклинами. Свободные радикалы кислорода формируются в результате разрыва ДНК и вызывают гибель опухолевых клеток. Данное лекарство редко применяется в качестве монотерапии, предпочтительнее в сочетании с другой химиотерапией. Блеомицин является активным средством в режимах для рака тестикул, а также лимфомы Ходжкина. Наиболее частым побочным эффектом данного лекарства является токсическое воздействие на легкие по причине образования свободных радикалов кислорода.
Аспарагиназа катализирует гидролиз аспарагина в аспарагиновой кислоте и аммонии и таким образом убивает опухолевые клетки, чувствительные к недостатку аспарагинсинтетазы (лимфоциты и клетки лимфоидного происхождения). Она используется для лечения заболеваний крови (острые лейкемии, лимфомы Ходжкина). Ее основными неблагоприятными эффектами являются гепатотоксичность, тошнота и, иногда, анафилактические шоки.
Биологическая терапия
Данный раздел содержит 3 части: моноклональные антитела, цитокины и иммуностимуляция посредством бактериальных средств. Соединения по настоящему изобретению принадлежат к данному классу средств.
Моноклональные антитела
Мышиные, химерные, ослабленные и моноклональные антитела человека (huMoAb) применяются для лечения рака у человека [Untch m, Ditsch N, Hermelink K., Immunotherapy: new options in breast cancer treatment., Expert Rev Anticancer Ther. 2003 Jun; 3(3):403-8].
Предполагается, что к 2010 году будут клинически применяться около 20 антител.
Применение моноклональных антител вызывает выработку специфических антител, направленных против антигенов, расположенных на поверхности опухолевых клеток. Образец опухолевых клеток пациента забирается и обрабатывается для производства специфических антител к опухолеспецифическим антигенам. Таким образом, при данном подходе к работе должно предоставляться достаточное количество уникальных антигенов к опухолевым клеткам. Кроме того, опухолевые антигены должны быть достаточно отличными от антигенов, произведенных нормальными клетками, провоцирующими ответную выработку антител.
Данные антитела (распознающие опухолевые клетки) могут применяться для уничтожения опухолевых клеток как самостоятельно, так и в качестве носителей других веществ, используемых для терапевтических или диагностических целей. Например, химиотерапевтические средства могут прикрепляться к моноклональным антителам, доставляющим высокие концентрации данных токсических веществ прямо к опухолевым клеткам. Теоретически данный подход является менее токсичным и более эффективным, чем общепринятая химиотерапия, поскольку уменьшает доставку вредных средств к нормальным тканям.
Эрбитукс (цетуксимаб) представляет собой моноклональное антитело, которое нацелено на рецептор эпидермального фактора роста (EGFR) и, таким образом, регулирует рост клеток. Предполагается, что эрбитукс влияет на рост опухолевых клеток посредством связывания EGFR так, что эндогенный эпидермальный фактор роста не может связаться и стимулировать рост клеток. Эрбитукс применяется для лечения метастазов раков толстой и прямой кишок. Инфузия эрбитукса может вызывать серьезные побочные эффекты, которые могут включать затруднение дыхания и снижение артериального давления, которые обычно регистрируются во время первого лечения. Также, иногда, было зарегистрировано интерстициальное заболевание легких (ILD). Другими, более общими побочными эффектами эрбитукса являются: сыпь (угри, сыпь, сухость кожи), утомляемость/слабость, лихорадка, запор и боль в животе.
Ритуксимаб (анти-CD20) был первым зарегистрированным МАВ для терапии фолликулярной лимфомы. Впечатляющие результаты были отмечены в сочетании с CHOP химиотерапией (циклофосфамид, доксорубицин, винкристин и преднизон) при фолликулярной и выраженной лимфомах.
Другими представленными на рынке моноклональными антителами являются: Алемтузамаб (Campath®, нацеленный на CDw52, выраженный на лимфоидных опухолях); Гемтузумаб-озогамицин (Mylotarg®, нацеленный на CD33, выраженный на бластах миелоидной лейкемии) и Тоситумаб (Bexxar®).
Цитокины
Большинство проверенных цитокинов для лечения злокачественных опухолей являются интерлейкином-2 и интерферонами.
Интерлейкин-2
Интерлейкин-2 (IL-2) представляет собой вещество, производимое лимфоцитами. В дополнение к существующему первичному фактору роста Т-клеток IL-2 усиливает различные функции натуральных клеток-киллеров (NK-клеток) и Т-клеток. IL-2 также активирует лимфокинактивированные клетки-киллеры (LAK-клетки). LAK-клетки разрушают опухолевые клетки и улучшают восстановление иммунных функций при определенных иммунодефицитных состояниях. Пациенты с почечноклеточным раком, меланомой и неходжкинской лимфомой демонстрировали некоторые реакции на терапию IL-2.
Наиболее сильным токсическим эффектом IL-2 является способность повышения проницаемости капилляров. Это может вызывать гипотензию, асцит, генерализованный отек тела (анасарка) и отек легких. Также часто встречаются озноб и жар в пределах нескольких часов после введения IL-2. Головная боль, недомогание и другие гриппоподобные симптомы также являются обычными. Гастроинтестинальные эффекты включают тошноту, рвоту, снижение аппетита, диарею и мукозит (воспаление слизистых оболочек).
Интерфероны
Интерфероны (IFN) представляют собой малые белки, которые ингибируют репликацию вируса и стимулируют клеточный (Т-клеточный) иммунный ответ. В настоящее время различают три больших типа IFN: альфа, бета и гамма. Каждый тип имеет сходные, но характерные способности для изменения биологических ответов. Альфа-IFN главным образом показан при применении в лечении гепатита С, но в настоящее время также назначается при лечении волосато-клеточного лейкоза и ассоциированной со СПИДом саркомы Капоши. Он также показывает некоторую терапевтическую эффективность против гематологических заболеваний, таких как слабо выраженная лимфома Ходжкина, кожная Т-клеточная лимфома, хронический миелоидный лейкоз и множественная миелома. Он также является отчасти эффективным при некоторых солидных опухолях, таких как почечноклеточный рак.
Бета-интерферон в настоящее время применяется для лечения рассеянного склероза.
Одним из наиболее распространенных побочных эффектов терапии IFN является гриппоподобный синдром. Симптомы включают лихорадку, озноб, тахикардию, мышечную боль, недомогание, утомление и головную боль.
Другие основные побочные эффекты IFN включают снижение количества белых кровяных клеток, анемию (при продленной терапии) и снижение количества тромбоцитов. Также могут быть представлены гастроинтестинальные симптомы, такие как снижение аппетита, тошнота, рвота и диарея. Диапазон токсического воздействия на центральную нервную систему от легкой спутанности и сонливости до судорожных припадков. Острая почечная недостаточность редка, но может случаться. Также может быть проблемой выпадение волос.
Иммуностимуляция посредством бактериальных средств
После многообещающих результатов испытаний на животных в шестидесятые годы специалисты начали крупномасштабные клинические испытания стимуляции иммунной системы онкологических пациентов с применением бактериальных средств, таких как Corinebacterium parvum (C. parvum) и Bacillus Calmette-Guerin (BCG). К несчастью, результаты данных ранних иммунотерапевтических испытаний были обескураживающими и лечение опухолей с применением иммуностимулирующих лекарств в чистом виде утратили актуальность.
Токсичность поступающих извне иммуностимуляторов сильно ограничивало их применение у онкологических пациентов. В 1976 году Morales et al. ввел интравезикально Bacillus Calmette-Guerin (BCG) для лечения поверхностного рака мочевого пузыря (Morales et al. 1976, повторно обсуждено в J Urol. 2002 Feb; 167(2 Pt 2):891-3; обсуждение 893-5). BCG, неспецифическая иммунотерапия для поверхностного рака мочевого пузыря, может рассматриваться в качестве наиболее успешной из всех способов иммунотерапии у человека (последний обзор см. Boyd, Urol Nurs. 2003 Jun; 23(3):189-91, 199; вопросы 192).
Противоопухолевый эффект липополисахаридов (LPS) хорошо доказан. В XIX веке Coley разработал противоопухолевую терапию, основанную на бактериальных токсинах (см. Coley WB, the Practitioner, November 1909). В 1940 годах было показано, что бактериальные липополисахариды (LPS) были по крайней мере частично ответственными за наблюдаемую противоопухолевую активность токсинов Coley. Более новые публикации показывают противоопухолевые эффекты LPS в экспериментальных моделях на животных и очень ограниченном количестве исследований, проведенных у человека. Поскольку LPS является очень токсичным и может вызвать эндотоксический шок, терапевтическое окно оказалось очень маленьким и пациенты могут лечиться только очень маленькими количествами LPS, которые часто также являются низкими для достижения желаемых благотворных эффектов.
Биологическая и токсическая активности LPS связаны с их липидным компонентом, называемым "липид А". Различные виды бактерий синтезируют различные структуры липида А, и они имеют варьирующиеся степени токсичности. Это позволяет предположить, что посредством модификации природного бактериального липида А может быть возможным приготовление производных, которые имеют ослабленную токсичность, но сохраняют благоприятную биологическую активность. Ряд различных производных липида А протестирован в экспериментальных животных моделях опухолей с некоторыми успехами.
В настоящее время доказано, что иммуностимуляция ОМ-174 триацилированных дифосфорилированных производных липида А структурной формулы (III) могли бы помочь иммунной системе организма достичь координированного сочетания неспецифического и специфического ответа на опухолеспецифический антиген, если они обнаруживаются первыми или сопутствующими классическим химиотерапевтическим средствам, как описано ниже.
Как только первое химиотерапевтическое лечение было выполнено, может быть необходимо стимулировать воспалительный ответ, повышающий первую неспецифическую иммунную защиту. Кроме того, специфические иммунные ответы могут активироваться вследствие наличия обнаруженного опухолеспецифического антигена. Данные специфические ответы, связанные с иммунологической памятью, обычно разделяются на гуморальный (иммунитет, предоставленный посредством антител, продуцируемых В-лимфоцитами) и клеточноопосредованный иммунитет (иммунитет, предоставленный посредством Т-лимфоцитов). Другими важными клетками являются клетки, осуществляющие презентацию антигена (КПА), такие как макрофаги и натуральные клетки-киллеры (NK-клетки). Макрофаги связывают антиген и “презентируют” антиген не подвергнутым какому-либо воздействию Т-клеткам. Данные клетки в свою очередь делаются активными и производят зрелые лимфоциты. NK-клетки являются цитотоксичными по отношению к опухолевым клеткам и клеткам, пораженным вирусом.
Предполагаемое комбинированное лечение триацилированными производными липида А
Задачей представляемой терапевтической стратегии борьбы с опухолями является первая атака опухолевых клеток при помощи стандартных или экспериментальных химиотерапевтических лекарств и, таким образом, обнаружение “in situ” опухолевых антигенов, и впоследствии помощь иммунной системе в подготовке соответствующего иммунного ответа. Альтернативно, лучевая терапия, предпочтительнее чем химиотерапия, может также быть использована. Кроме того, совместное применение иммуностимулирующего цитокина (такого как альфа-IFN) и триацилированного производного липида А может рассматриваться для поддержки ex vivo или in vivo созревания и активации человеческих моноцитпроизводных дендритных клеток, как описано B. Veran J., M. Mohty B. Gaugler, C. Chiavaroli и D. Olive. 2004, Immunobiology 209:67.
Задача изобретения, в сравнении с “современным уровнем техники” состоит, фактически, в том, что, соответственно сведениям заявителей, в экспериментальных исследованиях без использования животных не были раскрыты эффекты сочетания некоторых триацилированных дифосфорилированных производных липида А структурной формулы (II) с какими-либо стандартными химиотерапевтическими лекарствами, заявленными здесь, и применения двух неспецифических средств в качестве стандартного или экспериментального химиотерапевтического лекарства и иммуностимулирующего средства, указывающие на эффективность специфической (антигены, обнаруженные посредством химиотерапии) противоопухолевой терапии.
Настоящее изобретение основано на том факте, что триацилированные производные липида А могут быть использованы терапевтически для лечения многих форм опухолей в сочетании с соединениями и лекарствами, описанными ниже, или в сочетании с лучевой терапией.
Триацилированное производное липида А ОМ-174 в организме человека
Продукт хорошо переносился онкологическими пациентами. Дозы выше 1 мг ОМ-174/м2 посредством внутривенной инфузии достигались без неприемлемой токсичности соответственно негематологической шкале III и гематологической шкале IV NCI критериев общей токсичности.
Проанализированные цитокины (TNF-α, IL-1b, IL-1 ra, IL-6, IL-8, sTNF-RI, sTNF-RII, IL-10, IL-2, IL-2sRa, IFN-γ) показали профиль секреции, согласованный с производными липида А. Секреция происходила на всех стадиях и проявляла более “пациент”-, чем “доза”-зависимость.
Результаты данного исследования с однократной дозой указывали на выбор трех доз (0,6, 0,8 и 1,0 мг ОМ-174/м2) для повторных внутривенных инъекций (от 5 до 15 инъекций), примененных в фазе Ib исследования.
Фармакокинетические данные в организме человека (клиренс, объем распределения и период полувыведения) для ОМ-174 суммируются в таблице 1.
Суммарные фармакокинетические данные по ОМ-174
в организме человека
Список лекарств, применимых в комбинации с соединениями по изобретению
Алемтузанаб; Алретамин; Азакрин; Аспарагиназа (Elspar®); Анастрозол (Arimidex®); Бевацизумаб (Avastin®); Бикалутамид (Casodex®); Блеомицин (Blenoxan®); Бортезомиб (Velcade®); Бусульфан (Милеран); Капецитабин (Xeloda®); Карбоплатин (Параплатин); Кармустин (BCNU, BiCNU); Цетуксимаб (Erbitux®); Хлорамбуцил (Лейкеран); Хлорметин; Цисплатин (Platinol®); Кладрибин; Циклофосфамид (Cytoxan®, Neosar®); Цитарабин (Cytosar-U®, Ara-C); Дакарбазин (DTIC-Dome); Дактиномицин (Cosmegen®); Даунорубицин (Cerubidin®); Дексразоксан (Zinecard®); Доцетаксел (Taxotere®); Доксорубицин (Адриамицин, Рубекс); Эрбитукс (цетуксимаб); Ацетат Эллиптиниума; Эпирубицин; Эстрамустин; Этопозид (VePesid®, VP-16®); Цитрат Фентанила (Actiq); Флоксуридин (FUDR®, Фтордезоксиуридин); Фотемустин; Флударабин (Fludara®); Фторурацил (Адруцил, 5-FU); Флутамид (Eulexin®); Фульвестрант (Faslodex®); Гефитиниб (Iressa®); Гемцитабин (Gemzar®); Гемтузумаб; Ацетат гозерелина имплантат (Zoladex®); Гидроксимочевина (Hydrea®); Идарубицин (Hydrea®); Ифосфамид (IFEX®); Мезилат Иматиниба (Gleevec, STI-571); Иринотекан (Camptosar®, CPT-11); Лейковорин; Ацетат Лейпролида для депо-суспензии (Lupron®); Ломустин (ССNU, CeeNU®); Мафосфамид; Мехлорэтамин (Mustargen®, Nitrogen Mustard); Мелфалан (Alkeran®, L-PAM); Меркаптопурин (Purinethol®, 6-MP); Метотрексат (МТХ); Митомицин (Митомицин С, Мутамицин); Митотан (Содрен); Митоксантрон (Новантрон); Нилутамид (Nilandron®); Оксалиплатин (Eloxin®); Паклитаксел (Таксол); Памидронат (Аредиа); Пентостатин (Нипент); Пирарубицин; Пликамицин (Митрацин, Митрамицин); Премексетред (Alimta®); Прокарбазин (Муталан); ПРОКРИТ (Эпоэтин альфа); Полифепрозан 20 с кармустином имплантат (GLIADEL®); Ритуксимаб (Rituxan®); Стрептозоцин (Заносар); Тамоксифен (Nolvadex®); Тенипозид (Вумон); Тепотекан; Тиогуанин (6-TG, Thioguanine Tabloid®); Тиотепа (Тиоплекс); Тоситумомаб (Bexxar®); Токсалиплатин (Elotaxin®); Винбластин (Велбан); Винкристин (Онковин); Виндесин; Винорелбин (Навелбин).
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения по изобретению получают соответственно способу, описанному в WO 95/14026.
Соединения по изобретению могут быть в форме любой из кислот или какой-либо приемлемой соли, подходящей для инъекции существующим теплокровным животным и человеку. Соединения могут вводиться парентерально (предпочтительно внутривенно) после (или совместно с каким-либо подходящим составом) предварительной терапии, включающей стандартную лучевую терапию или классические или экспериментальные химиотерапевтические лекарства.
В первую очередь у человека опухоли могут лечиться обычно хорошо определенными или экспериментальными химиотерапевтическими лекарствами или лучевой терапией, обнаруживая опухолевые антигены пациента. Затем (или совместно) будет выполняться иммуностимуляция соединениями по изобретению (предпочтительно от 1 до 7 инъекций в неделю и, по меньшей мере, 5 парентеральных инъекций). Цикл общепринятого лечения может затем выполняться необязательно сниженными дозами.
Известно из предшествующей работы (раскрыто в WO 95/14026), что когда проверенный по существу как иммунотерапевтическое средство ОМ-174 показывает равномерную сильную терапевтическую активность на модели рака толстой кишки BDIX/ProB, даже если лечение начинается с 14 дня после индукции опухоли. Такое лечение ведет к одному из двух: излечивает или дает сильное подавление развития опухоли. В случае полной ремиссии животные специфически иммунизируются против опухоли, и повторная имплантация приводит к отторжению. При лечении, включающем повторные инъекции ОМ-174, схема введения являлась более важной, чем доза для терапевтического эффекта лекарства.
Ниже будет показано, что потенциально имеется большое преимущество в сочетании эффектов иммунотерапии (вызванной, например, ОМ®-174) с эффектами химиотерапии или лучевой терапии. Так, начальное лечение опухоли посредством, например, химиотерапии (алкилирующих средств, таких как аналоги цисплатина или циклофосфамид, или средств-антиметаболитов, таких как 5-FU) уменьшит массу и жизнеспособность опухоли и, посредством повреждения опухолевых клеток, может также привести их в состояние большей иммуногенности. Данное начальное неспецифическое лечение затем может повторяться посредством неспецифической иммунотерапии соединениями по изобретению, которые могут быть более эффективными в результате начальной химиотерапии. Иммунотерапия будет приводить к специфическому отторжению остающихся опухолевых клеток иммунной системой, предупреждать повторный рост какой-либо опухоли и рост метастазов.
Данное сочетание способов лечения потенциально предлагает очень действенный способ борьбы с опухолями, как описано в примерах ниже.
Преимущества и усовершенствование, обусловленное специфицированной терапией, будет более понятно из приложенных примеров и прилагаемой формулы изобретения.
ПРИМЕРЫ
Пример 1: усиление лечебного эффекта циклофосфамида посредством ОМ-174 на модели меланомы В16
Введение
Как известно в настоящее время, никакие экспериментальные исследования не раскрывали эффекты сочетания ОМ-174, триацилированного дифосфорилированного производного липида А структурной формулы (II) со стандартными химиотерапевтическими лекарствами, как те, что заявлены в данном документе.
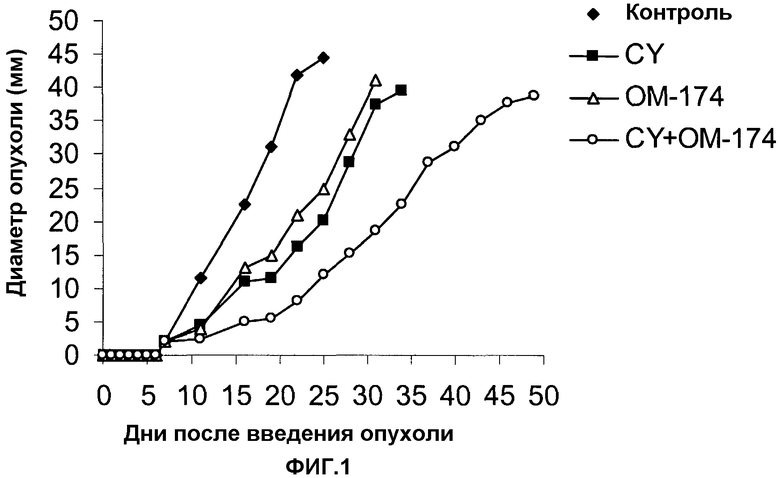
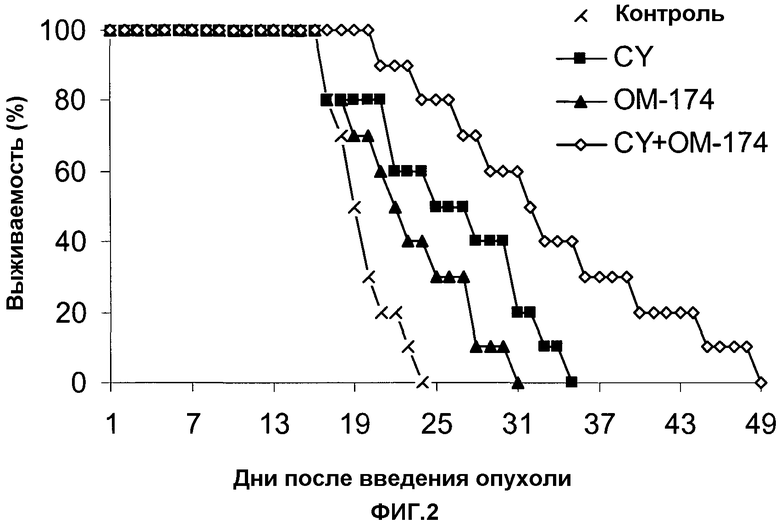
В данном примере показано, что ОМ-174 сам по себе частично ингибирует развитие опухоли (фиг.1) и незначительно удлиняет время выживания мышей с экспериментальной моделью меланомы В16 (фиг.2). В условиях, примененных в исследовании, противоопухолевая активность ОМ-174 является сопоставимой с активностью циклофосфамида (CY), сравнительного цитостатического лекарства.
Интересно, и данное является частью изобретения, что более выдающиеся эффекты достигаются посредством комбинирования двух средств в протоколе, состоящем из однократного введения CY (200 мг/кг, интраперитонеально) и последующих пяти инъекций ОМ-174 (1 мг/кг, интраперитонеально). См. фиг.1 и 2.
Иммунологические исследования подвергнутых лечению и контрольных мышей показывают, что противоопухолевая активность ОМ-174, одного или в комбинации с CY, опосредуется при помощи стимуляции ответов натуральных киллеров (NK) и цитотоксических Т-лимфоцитов (CTL), а также посредством значительного увеличения абсолютного количества NK1.1, CD4 и CD8 позитивных клеток. Поэтому ОМ-174 увеличивает противоопухолевый эффект хорошо известного химиотерапевтического лекарства циклофосфамида и, следовательно, является кандидатом для присоединения к химиотерапии в лечении опухолей у человека.
Животные и опухолевые клетки
Самцов мышей С57BL/6 в возрасте четырех-шести недель приобретают у Charles River (Calco, Corno, Italy). Клетки меланомы В16 периодически вносят подкожно (п.к.) сингенным мышам. В день 0 мышам вводят п.к. в правый бок 2×105 клеток меланомы В16. Рост опухоли измеряют ежедневно у каждой мыши, используя циркули, и рассчитывают средний диаметр опухоли в день. На 7 день после введения опухоли, всех мышей с п.к. опухолями диаметром 2-3 мм выделяют в различные экспериментальные группы, например, получающие введение фосфатно-буферного физиологического раствора (PBS)-контроля 3, CY, ОМ-174 или CY с ОМ-174.
Лекарства и способы лечения
Циклофосфамид (Sigma, St. Louis, MO) растворяют до 20 мг/мл в PBS непосредственно перед применением и вводят интраперитонеально 0,2 мл на мышь. Каждое животное, подвергаемое лечению, получает однократную дозу 200 мг/кг CY на 7 день. Данная доза выбирается на основании предыдущих экспериментов как наиболее активная доза, которая не приводит к заметной токсичности у данной линии мышей.
Иммуностимулирующее средство ОМ-174 представляет собой очищенный водорастворимый дифосфорилированный и триацилированный липид А, производный от E. сoli. Для исследования роста опухоли и выживаемости каждая мышь (20 в группе) получает ОМ-174 интраперитонеально (1 мг/кг) на 8, 13, 18, 23 и 28 дни после прививки опухоли. Анализы цитотоксической активности клеток селезенки и субпопуляций лимфоцитов различных экспериментальных групп (5 животных в группе) выполняют на 14 день после введения опухоли, например, после двух лечений ОМ-174 (на 8 и 13 дни).
Получение клеток селезенки
Мышей умерщвляют посредством сворачивания шеи на 14 день после прививки опухоли. Клетки селезенки получают посредством осторожного препарирования с помощью иглы индивидуальных селезенок в RPMI 1640 (Flow Laboratories, Irvine, Ayrshire, UK). Клетки фильтруют через Nytex с ячейкой 10 мкм, дважды отмывают и ресуспендируют в Complete Medium (CM): RPMI 1640, дополненной 10% эмбриональной телячьей сывороткой (FBS), 200 мМ L-глутамина, 25 мМ HEPES, пенициллином 5 Ед/мл и стрептомицином 50 мкл (все от Flow Laboratories).
Оценка цитотоксичности
Пассированные in vitro клетки YAC-1 (индуцированные вирусом саркомы Молони мышиные Т-клетки лимфомы происхождения A/SN) и пассированные in vivo клетки меланомы В16 используют в качестве клеток-мишеней в анализе высвобождения хрома. Клетки меланомы В16 получают из мышей-опухоленосителей, высевают в колбы с клеточной культурой (Falcon, Becton Dickinson and Co., Plymout, England) в течение первой недели выращивания в СМ. Клеточные линии В16 и YAC-1 получают из лабораторной коллекции и первоначально получают из Американской коллекции тканевых культур (ATCC).
Цитотоксическую активность клеток-эффекторов, собранных от каждой мыши, измеряют посредством стандартного анализа 4-часового 51Cr-высвобождения. Кратко, клетки-мишени собирают из культуры, дважды промывают, ресуспендируют по 5×106 клеток в 0,9 мл СМ и метят 100 мкCi (51Сr) хромата натрия (New England Nuclear, Boston, MA) в течение 1 часа при 37°С в инкубаторе с 5% СО2. После нанесения метки клетки трижды промывают в RPMI 1640 и высевают в U-образные 96-луночные микротитровальные планшеты (Flow Laboratories) по 1×104 клеток в лунке. Суспензию эффекторных клеток добавляют в учетверенные лунки, давая три соотношения E/T (например, 100:1, 50:1, 25:1) в окончательном объеме 200 мкл в лунке. Затем планшеты инкубируют в течение 4 часов при 37°С в инкубаторе с 5% СО2, 100 мкл супернатанта собирают из каждой лунки и измеряют радиоактивность с использованием счетчика гамма-квантов. Среднюю итоговую цитотоксичность ± S.E.M. подсчитывают из учетверенных чисел cpm от индивидуальных селезенок.
Иммунофлуоресцентное окрашивание и проточный цитометрический анализ субпопуляций клеток селезенки
Спленоциты от каждой мыши анализировали посредством проточной цитометрии. Для двойного флуоресцентного анализа субпопуляций клеток селезенки использовались следующие моноклональные антитела: флюоресцеин(FITC)-конъюгированный антимышиный NK1.1 PE (PharMingen, San Diego, CA), PE-конъюгированный антимышиный CD4 (PharMingen), FITC-конъюгированный антимышиный CD8 (PharMingen). Приблизительно 1×106 клеток селезенки ресуспендируют в 50 мл СМ и выполняют окрашивание при 4°С в течение 30 минут. Затем клетки промывают дважды в PBS, содержащем 0,02% азида натрия, и проводят проточный цитометрический анализ с применением FACscan проточного цитометра (Becton Dickinson).
Данные флуоресцентного анализа собирают с использованием волны возбуждения с длиной 488 нм от 15 мВт аргонового лазера с воздушным охлаждением. Эмиссию собирают через 585/42 нм пропускной ленточный фильтр. Собирают минимум 5000 результатов от каждого образца и преобразовывают в форму списка посредством компьютера Hewlett Packard 9000. Собранные данные проецированы на живые селезеночные лимфоциты посредством переднего и бокового угловых разбросов, исключая погибшие клетки, обломки, нелимфоидные клетки и клеточные агрегаты. Данные отображают в качестве процентного соотношения позитивных клеток к общему количеству подсчитанных клеток.
Статистический анализ
Для оценки сохранившихся функций применяют способ Каплана-Мейера и Log-rank тест выполняют для тестирования гомогенности сохранившихся функций параллельно в четырех группах (контрольная, CY, ОМ-174, CY + ОМ-174).
Опухолевый рост анализируют посредством Т-теста для непарных данных.
Т-тест Стьюдента используют для анализа контрольных средних значений в других экспериментах. Значения менее 0,05 считались значимыми.
Результаты
Опухолевый рост
Как показано на фиг.1, оба средства, CY и ОМ-174, будучи примененными индивидуально, незначительно, но отчетливо ингибировали рост опухоли В16, по сравнению с контрольной группой, не получавшей лечения. Важно, что сочетание ОМ-174 и CY приводит к лучшему торможению отношения опухолевого роста, которое было значительно лучшим, чем полученное посредством средств одиночных лечений.
Время выживания
CY и ОМ-174, применяющиеся по отдельности, незначительно, но отчетливо уменьшали среднее время выживания (СВВ) мышей по отношению к контрольной группе, не получавшей лечения. Комбинированное лечение CY и ОМ-174 вызывало лучшие результаты сроков выживания мышей, которые были значительно выше, чем не только у контрольных мышей, но также у мышей, получавших CY и ОМ-174 по отдельности. Фиг.2 показывает процентное соотношение выживания животных в каждой группе, получавшей лечение, в течение всего периода наблюдения.
Активность NK-клеток
Известно, что элиминация опухолевых клеток частично опосредуется через цитотоксическую активность NK-клеток. Поэтому была измерена цитотоксическая активность спленоцитов против NK-чувствительных (YAC-1) опухолевых клеток. Клетки селезенки получены от здоровых мышей или от мышей-опухоленосителей, получавших лечение PBS, CY, ОМ-174 или CY в комбинации с ОМ-174. Результаты представлены графически в таблице 2.
Действие лечения на активность NK и CTL
На 14 день после прививки опухоли пять мышей из каждой группы были умерщвлены и цитотоксичность NK и CTL измерялась, как описано в Материалах и Методах. Результаты отображались как среднее процентное отношение цитотоксичности ± S.E., производной от пяти индивидуально протестированных мышей из каждой группы. #р<0,001 в сравнении со здоровыми контрольными мышами. *р<001 в сравнении со всеми другими группами мышей, которым вводилась опухоль меланомы В16.
У здоровых мышей лечение ОМ-174 вызывало резкое и значительное возрастание активности NK-клеток по отношению к контрольным, не получавшим лечения. Такое же резкое и значительное возрастание активности NK-клеток наблюдалось также у мышей, получивших прививку меланомы В16. На 14 день контрольные и получавшие лечение CY мыши-опухоленосители показали сниженную NK-активность, когда сравнивали со здоровыми мышами, не получавшими лечения. ОМ-174 всегда был способен полностью восстанавливать NK-активность выше уровней, наблюдаемых у здоровых контрольных мышей, не получавших лечения. р<0,001 для О+CY+ОМ-174 в сравнении со всеми другими группами.
Цитотоксическая активность против аутологичных опухолевых клеток
Цитотоксичные Т-лимфоциты (CTL) также играют важную роль в элиминации опухолевых клеток. Данное было протестировано на специфическую цитотоксическую активность против аутологичных опухолевых клеток, применяя in vivo пассированные клетки меланомы В16 в качестве мишени, на клетках селезенки от здоровых мышей и мышей-опухоленосителей. Результаты данных экспериментов показаны выше, в таблице 2. Как ожидалось, было найдено, что клетки селезенки здоровых мышей не показывали обнаруживаемой цитотоксической активности против клеток В16. В противоположность этому, спленоциты мышей-опухоленосителей показывали заметную цитотоксическую активность против аутологичных опухолевых клеток, которая обнаруживалась и не возрастала посредством лечения CY. Введение ОМ-174 было способно индуцировать заметную стимуляцию активности CTL у мышей-опухоленосителей (двукратное возрастание). Интересно, что у мышей, получавших лечение с сочетанием ОМ-174 и CY, показанные высочайшие уровни цитотоксической активности против аутологичных опухолевых клеток увеличивались в 4 раза по сравнению с контрольными опухоленосителями и в 2 раза по сравнению с мышами-опухоленосителями, получавшими лечение только ОМ-174.
Анализ субпопуляции клеток селезенки
Определялись уровни воздействия различных способов лечения на субпопуляции лимфоцитов экспериментальных мышей и его корреляции с полученными результатами опухолевого роста, времени выживания и цитотоксической активности, процентные соотношения клеток селезенки, экспрессированных CD4, CD8 и NK1.1.
Как показано в таблице 3, мыши-опухоленосители показывали заметное снижение всех протестированных субпопуляций клеток селезенки в сравнении со здоровыми контрольными. Лечение ОМ-174 повышало процентное соотношение CD4+, CD8+ и NK1.1 позитивных клеток у здоровых мышей и мышей-опухоленосителей. Как уже упоминалось для других проанализированных параметров, наивысшее процентное соотношение CD4+, CD8+ и NK1.1 позитивных клеток было обнаружено у мышей, получавших лечение CY + ОМ-174, которые были выше величин, обнаруженных у здоровых мышей.
Воздействие лечения
на субпопуляции селезеночных лимфоцитов (%)
На 14 день после прививки опухоли мыши были умерщвлены и клетки, полученные из индивидуально обработанных селезенок, окрашивали с моноклональными антителами для FACS анализа. Результаты отображались как среднее процентное отношение позитивных клеток по отношению ко всем клеткам селезенки ± S.E.М., производной от пяти индивидуально протестированных мышей.
*р<005 по отношению ко всем другим группам мышей, которым вводили опухоль меланомы В16.
Вывод
В заключение, настоящий протокол комбинированного лечения представляется высокоэффективным на модели меланомы В16, подтверждающей эффективность иммунотерапевтического протокола с производными липида А. Действительно, результаты, полученные при стимуляции цитотоксической активности (неспецифических NK и опухолеспецифических CTL) клеток селезенки и повышение NK, CD4+ и CD8+ фенотипов последующим лечением ОМ-174 одним или в сочетании с CY, коррелируют с замедлением опухолевого роста и продлением времени выживания.
Основываясь на данных результатах, триацилированные дифосфорилированные производные липида А согласно структурной формуле (II) могут, таким образом, рассматриваться как кандидаты для объединения с химиотерапевтическими режимами лечения опухолей в клинике.
Пример 2: противоопухолевая активность интратуморального введения ОМ-174 с интраперитонеальным введением циклофосфамида при распространенных подкожных опухолях толстой кишки PROb у крыс BDIX.
Данный изучаемый здесь на колоректальной модели опухолей клеток эффект комбинированной последовательной терапии, использующей, во-первых, общепризнанное химиотерапевтическое лекарство циклофосфамид, и последующее уменьшение вызванной опухолью иммуносупрессии неспецифической интратуморальной иммуностимуляцией триацилированным производным липида А ОМ-174. В противоположность результатам, полученным с другими иммуностимулирующими лекарствами, такими как CpG или BCG, здесь демонстрируется, что противоопухолевая активность циклофосфамида сильно увеличивалась, когда следовало данное стандартное лечение посредством интратуморальных инъекций ОМ-174.
МАТЕРИАЛ, МЕТОДЫ И СТАТИСТИКА
Животные
Самки инбредной BDIX-линии крыс в возрасте 4-6 месяцев, массой 200-250 г, выращенные при постоянных условиях температуры, влажности и экспозиции искусственного освещения.
Химические вещества и лекарства
ОМ-174 от OM PHARMA, циклофосфамид (CY) от Sigma-Aldrich (L'Isle d'Abeau, Франция), внутрикожная BCG (вакцина BCG) от Paster Vaccins (Lyon, Франция). CpG (синтетические полинуклеотиды), синтезированные внутри лаборатории Prof Chauffert (Dijon, Франция).
Опухолевые клетки и модель опухоли
DHD/K12 клетки, происходящие от диметилгидразин-индуцированной опухоли толстой кишки у BD IX крыс. Для их стандартной канцерогенности выбирают клон PROb, вводимый сингенным крысам. Клетки PROb поддерживают в среде культивирования Ham's F10, дополненной 10% эмбриональной бычьей сывороткой. Клетки разделяют трипсином и ЭДТА и центрифугируют в присутствии полной среды культивирования с эмбриональной бычьей сывороткой до ингибирования трипсина. Клетки (2×106/крысу) суспендируют в 0,1 мл свободной от сыворотки среде Ham's F10, затем подкожно прививают анестезированным крысам в переднюю грудную область.
Лечение животных
Лечение самок BDIX крыс начинали на 36 день после подкожной прививки опухолевых клеток PROb, когда объем опухоли был примерно 1 см3. Эксперименты состояли из 8 групп крыс (6 животных в каждой группе). Контрольная группа не получала лечения. Другие группы получали, каждая, однократную инъекцию CY посредством интраперитонеального пути введения (25 мг/кг в 5 мл стерильного раствора NaCl) или иммуностимуляторы посредством интратуморального (и.т.) пути введения, начатого на 43 день, или интраперитонеального СРМ на 36 день, в комбинации с и.т. иммуностимулятором, начатым на 43 день. И.т. инъекции были сделаны на 43 день и 50 для BCG (100 мкл восстановленного раствора + 100 мкл NaCl для каждой интратуморальной инъекции). CpG (100 мкг на инъекцию в 200 мкл NaCl) и ОМ-174 (200 мкг на инъекцию в 200 мкл NaCl) вводили и.т. трижды в неделю в течение 4 недель (12 инъекций). Диаметр опухоли измеряли один раз в неделю кронциркулем.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
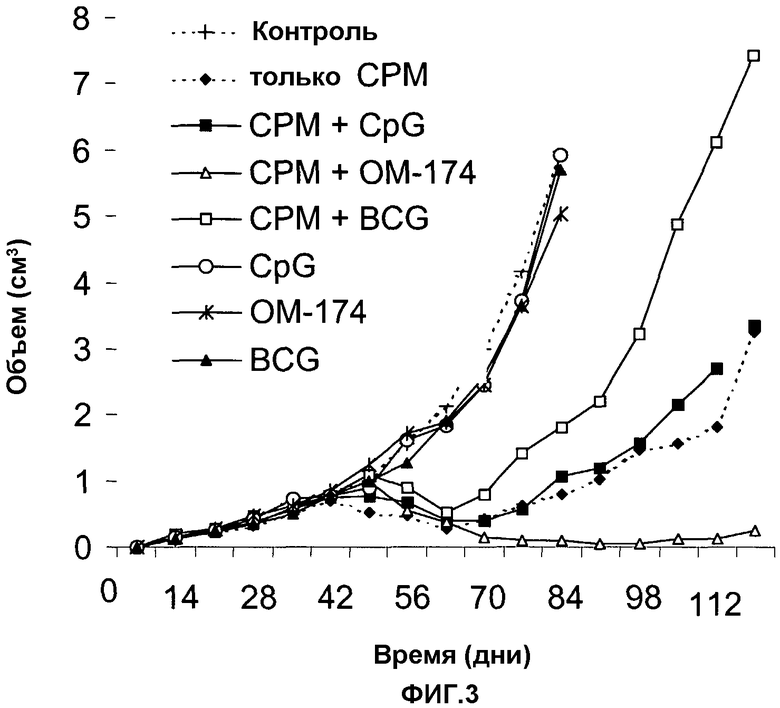
Только одни интратуморальные иммуностимуляторы (ОМ-174, BCG, CpG) не имели противоопухолевого эффекта относительно животных, не получавших лечения данных крупных, укоренившихся опухолей PROb (фиг.3). В противоположность этому, интраперитонеальный циклофосфамид вызывал временную регрессию подкожных опухолей, впоследствии возобновлявших рост у всех животных. Данное свойство находилось в соответствии с известной химиочувствительностью клеток PROb к алкилирующим средствам (Chauffert et al., 1992). Однако монотерапия СРМ была неспособна вылечить животных. BCG имел вредный эффект, непосредственно после его объединения с CY, активность CY была меньшей, чем при монотерапии CY. CpG не изменяли активность CY. Противоположно другим иммуностимуляторам, ОМ-174 сильно повышал противоопухолевый эффект CY. Все опухоли регрессировали в объеме больше, чем у животных, получавших лечение только CY, и полная и устойчивая регрессия была достигнута у 4 из 6 животных данной группы (см. таблицу 4).
Количество вылеченных животных
после различных способов лечения
В заключение, данные результаты демонстрируют, что ОМ-174 усиливал противоопухолевый эффект циклофосфамида при прогрессирующих подкожных опухолях у крыс. В настоящем эксперименте два других иммуностимулятора, BCG и CpG, ухудшали или совсем не улучшали эффект монотерапии циклофосфамидом соответственно.
Пример 3: повышение противоопухолевого эффекта химиотерапевтического средства цисплатина в комбинации с ОМ-174
Введение
В прошлом многократно продемонстрирован противоопухолевый эффект иммуностимулирующего средства ОМ-174 на BDIX/ProB модели карциноматоза брюшины у крыс (например, Onier et al., Clin Exp Metastasis. 1999 Jun; 17(4):299-306). Показано, что благотворный эффект является устойчиво максимальным (90% полных ремиссий), когда лечение начинается с 14 дня (D) после инъекции опухолевых клеток (сингенные клетки Prob). В противоположность этому, эффективность продукта уменьшается, когда лечение начинается с D21 или D28, и даже исчезает, когда лечение начинается с D35. В порядке поиска терапии, которая может быть адаптирована к человеку, здесь протестировано сочетание ОМ-174 с платиновым онкостатическим алкилирующим средством цисплатином посредством выбора экспериментальных условий, в которых ОМ-174 сам по себе не является оптимально активным. Как будет представлено ниже, результаты подсказывают, что сочетание цисплатин/ОМ-174 может иметь терапевтический эффект у людей, так как, когда цисплатин (3 мг/кг, в.в.) давался на D21, ОМ-174 все еще является высокоэффективным, даже когда вводился впервые на D21 или D28 и даже, иногда, на D35.
Следовали нижеприведенной методике:
Опухолевые клетки
Клетки PROb рака толстой кишки были исходно получены от опухоли BDIX крысы, индуцированной 1,2-диметилгидразином.
Линия крыс BDIX была создана в 1937 году H. Druckey. В настоящее время данные крысы поставляют Iffa-Credo (L'Asbresle, Франция).
Крысы BDIX, 4 месяца ± 1 месяц к началу эксперимента, 7 животных в группе, получивших интраперитонеально культивированные сингенные клетки PROb (и.п.) в день 0. Цисплатин (3 мг/кг) был введен в.в. на 21 день и лечение ОМ-174 (1 мг/кг, 5 инъекций в.в. в вену пениса каждый 5-й день) начато на 28 или 35 день. Здесь представлено выживание, последовавшее в примере до 72 дня.
Результаты
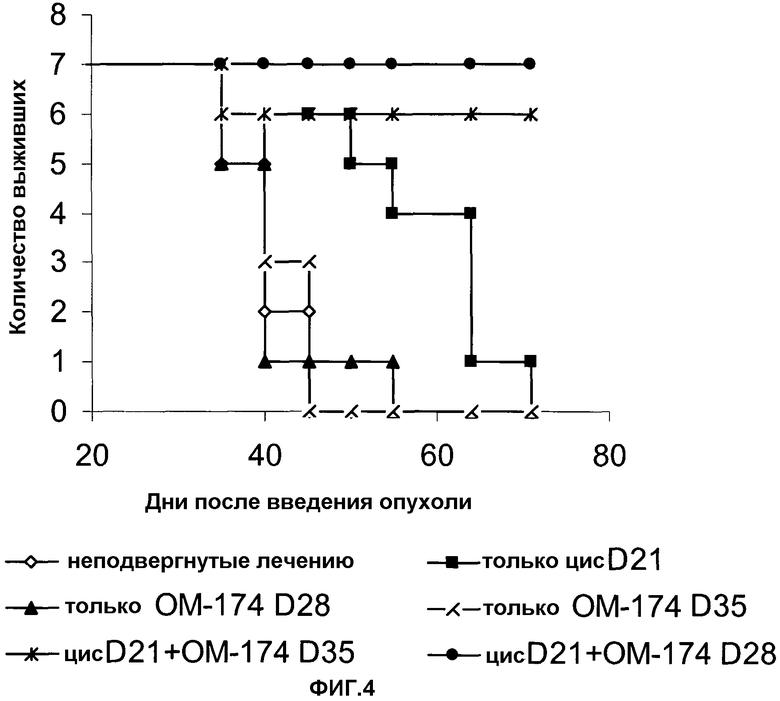
ОМ-174 сам по себе является вполне способным проявлять противоопухолевое действие, когда лечение (1 мг/кг, свыше 15 инъекций в.в., каждый 2-й день) начинается до 2 недель после прививки опухоли. Однако противоопухолевое действие является слабым, когда лечение начинается позже (28 день или 35 день, показано на фиг.4). Данное малоблагоприятное условие, безоговорочно, является преградой в реальной клинической ситуации, встречающейся у множества онкологических пациентов.
Например, цисплатин (3 мг/кг, в.в.) вводят на 21 день. Дополнительное иммуностимулирующее лечение ОМ-174 начинается только на 28 или 35 день (1 мг/кг, 5 инъекций в.в., каждый 5-й день). Кривые выживаемости показаны на фиг.4.
Вывод
Сочетание лечения ОМ-174 с цисплатином в данной, очень неблагоприятной среде дало гораздо более сильную противоопухолевую активность, чем любое из них в отдельности.
Как показано здесь, лечение цисплатином показывает только частичную эффективность, но, усиленное посредством иммуностимуляции ОМ-174, обнаруживает сильный противоопухолевый эффект.
Пример 4: усиление противоопухолевого эффекта химиотерапевтического средства 5-фторурацила (5-FU) в сочетании с ОМ-174
Введение
Антиметаболиты мешают прохождению нормальных метаболических путей, включая пути, необходимые для создания новых ДНК (фаза S клеточного цикла). Данный класс молекул часто применяют для лечения опухолей.
Клинически эффективным антиметаболитным лекарством, которое нарушает синтез ДНК, является 5-FU, применяемый в течение по меньшей мере четырех десятилетий (см. например, Rich et al., 2004). Он обладает широким диапазоном активности, включая рак толстой кишки, рак молочной железы, рак головы и шеи, рак поджелудочной железы, рак желудка, рак анального канала, рак пищевода и гепатомы.
Адекватная и контролируемая во времени клиническая комбинированная терапия, с помощью широко признанного химиотерапевтического лекарства, такого как 5-FU, первоначально используемая для уменьшения количества и умерщвления некоторых опухолевых клеток (и, таким образом, возможно, выявления опухольассоциированных антигенов) с последующей неспецифической иммуностимуляцией триацилированными производными липида А, вероятно, будет усиливать эффективность онкостатического лекарства и позволяет проводить настройку иммунологической (специфической) памяти, чтобы избавиться от клеток, несущих ассоциированный с опухолью антиген, и также, ограничить уровень наблюдаемых побочных эффектов, позволяя, например, снизить количество введений и/или доз химиотерапевтического лекарства.
Этот эксперимент был направлен на проверку эффективности сочетания 5-FU с ОМ-174 на крысиной модели опухолей толстой кишки.
Материалы и способы
Следовали следующей методике:
Продукты: ОМ-174-DP тестируют в сочетании с или без 5-FU, как описано ниже:
В день 0 (D0) 106 клеток PROb инъецируют и.п. каждой крысе. 5-FU вводят и.п. в дозе 30 мг/кг в дни 7 и 14. ОМ-174 инъецируют при дозе 1 мг/кг в.в. от дня 21 три раза в неделю в течение всего 10 инъекций.
Показатели
Все крысы (контроли и обработанные) умерщвляются СО2 на день 61. Эффективность лечения определяют по показателям, таким как выживаемость (фиг.5) и измерение классов данного рака в зависимости от количества и размера узлов, а также посредством измерений асцитов. Карциноматозы оценивают вслепую. Поскольку невозможно измерить объем карциноматоза, их классифицируют в соответствии с количеством и диаметром узлов:
- Класс 0: нет видимого узла
- Класс 1: некоторые подсчитываемые узлы с диаметром от 0,1 до 0,3 см;
- Класс 2: много неподсчитываемых узлов с диаметром от 0,1 до 0,3 см;
- Класс 3: некоторые узлы с диаметром 1 см заполняют брюшинную полость;
- Класс 4: полость полностью заполнена опухолевыми массами размером в несколько см.
Объем асцита измеряют двойным взвешиванием крыс.
Результаты
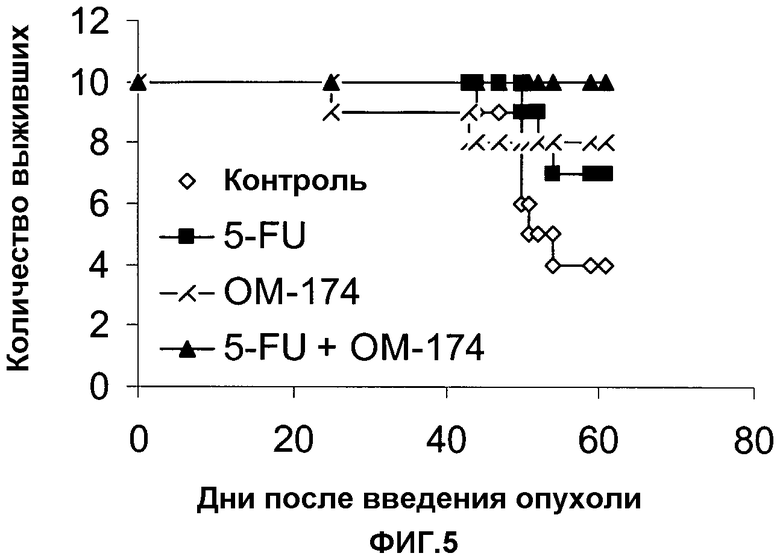
См. таблицу 5 и фиг.5.
Классы карциноматоза и объемы асцитов после лечения
Относительно классов:
Тест Mann-Whitney показывает значительное различие между группами контроля и ОМ-174, а также между группами контроля и 5-FU + ОМ-174. Не проявляется значительного различия между группами 5-FU и контроля. Существует значительное различие в средних баллах между группой контроля и обеими группами ОМ-174-DP и 5-FU + ОМ-174-DP (DP означает дифосфорилированное производное).
Соответствующая кривая выживания показана на фиг.5.
Вывод
Сочетание ОМ-174 + 5-FU является лучшим с позиции классов карциноматозов и времени выживания, чем для двух средств, взятых индивидуально в данной модели опухолей.
Пример 5: ОМ-174 в сочетании с лучевой терапией
Солидные опухоли снабжаются меньшими уровнями кислорода, чем нормальные ткани, вследствие слаборазвитой сосудистой сети и спорадической окклюзии кровеносных сосудов (van der Berge et al., 2001). Радиорезистентность, индуцированная гипоксией, признается основным препятствием для лечения рака (Dachs and Stratford, 1996). Возможность радиосенсибилизации гипоксических опухолевых клеток посредством иммуностимулирующего средства, способного индуцировать радикал оксида азота (NO, газ, фиксирующий повреждение ДНК, вызванное радиацией), представлено ниже. Будет показано, что NO, индуцированный ОМ-174, очевидно является мощным радиосенсибилизатором в модели опухолевых клеток мыши ЕМТ-6 как непосредственно в гипоксических условиях, так и опосредованно через активацию цитокинов, высвобождаемых макрофагами.
Непосредственный эффект ОМ-174 на клетки рака молочной железы ЕМТ-6
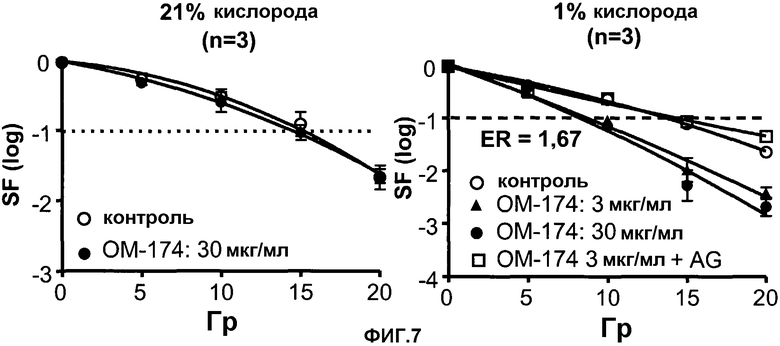
Непосредственный радиопротекторный эффект ОМ-174 на раковые клетки ЕМТ-6 тестируют первоначально in vitro как в нормальных (21%), так и в гипоксических (1%) кислородных состояниях. Условия гипоксии действительно отражают состояние клеток злокачественной опухоли, расположенных в нескольких микрометрах от капилляра. Для уничтожения этих клеток необходимы высокие дозы облучения, поэтому могут представлять интерес такие средства, как ОМ-174 при их внутриопухолевом или внутривенном введении.
Клетки ЕМТ-6 мышиной аденокарциномы молочной железы были культивированы в среде RPMI с 10% телячьей сывороткой в пластиковых флаконах. Монослойная культура ЕМТ-6, культивированная до раннего слияния, была подвергнута воздействию ОМ-174 в течение 16 часов в условиях с 21%-ным и с 1%-ным содержанием кислорода. После обработки ОМ-174 проводилось определение нитрита при помощи классического метода Griess. Значения были нормализованы для 200000 клеток на лунку.
Затем клетки были собраны при помощи трипсинизации, и оценивалась реакция на облучение, как описано выше (Van der Berge et al., 2001). Вкратце, микрогранулы (0,5×106 клеток) были получены в конических трубках посредством центрифугирования при 300 g в течение 5 минут. Метаболическое истощение кислорода в микрогранулах было вызвано инкубацией при 37°С до облучения. Микрогранулы были облучены с линейным ускорителем в дозе 2 Гр в минуту, и фракция выживших (SF) после облучения в дозах 5, 10, 15 и 20 Гр была определена при помощи 8-дневного анализа колониеобразования.
Результаты
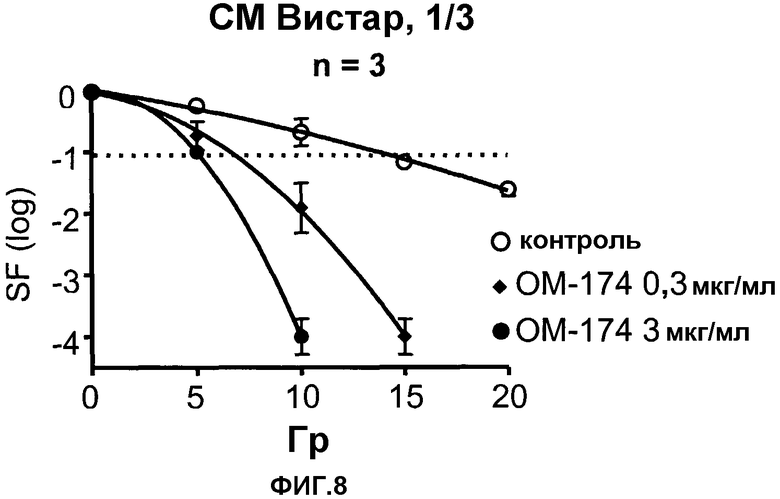
Как показано на фиг.6, клетки ЕМТ-6 продуцируют малые количества NO при стимуляции ОМ-174 и нормальных уровнях кислорода (21%-ное содержание кислорода). В противоположность этому, в условиях гипоксии (1%-ное содержание кислорода) определялась повышенная продукция NO. Интересен тот факт, что прямой клоногенный анализ (фиг.7) показывает, что ОМ-174 является прямым радиосенсибилизирующим средством для опухолевых клеток только в условиях гипоксии (доза облучения, необходимая для уничтожения 90% клеток, была в 1,67 раза ниже, чем доза, необходимая в отсутствие ОМ-174, как в количестве 3 мг/мл, так и в количестве 30 мг/мл). Непрямой радиосенсибилизирующий эффект на примере ОМ-174-индуцированной кондиционированной среды (СМ) от крыс Вистар, показан на фиг.8. В этих условиях высшая из протестированных доз (3 мкг/мл) обладала отчетливо более выраженным радиосенсибилизирующим действием, чем доза 0,3 мкг/мл.
Заключение
Данные результаты свидетельствуют о том, что ОМ-174 демонстрируют свойства как прямой, так и непрямой радиосенсибилизации, и таким образом, триацилированные дефосфорилированные производные липида А структурной формулы (II) являются хорошими кандидатами для использования в сочетании с лучевой терапией.
Общий вывод
В итоге данные результаты очевидно показывают и позволяют предположить, что неспецифическая иммуностимуляция триацилированными дифосфорилированными производными липида А структурной формулы (II) и, особенно, хорошо переносимым соединением ОМ-174 имеет мощный потенциал для усиления противоопухолевого действия, полученного при использовании хорошо отработанных или экспериментальных противоопухолевых способов, особенно классической химиотерапии и лучевой терапии.
Иммунотерапия триацилированным дифосфорилированным производным липида А структурной формулы (II) в любой соответствующей готовой форме, дозе, частоте введения будет применяться на человеке повторно парентерально, предпочтительно посредством внутривенного или внутриопухолевого пути введения. Предпочтительное лечение, выбранное из химиотерапии и/или лучевой терапии, будет применяться каждый раз в соответствии со стандартной практикой (состав, доза, частота и путь введения) до, одновременно или после иммунотерапии.
Необходимые дозировки соединения формулы II будут находиться в диапазоне от 0,05 до 100 мг/м2 для человека, предпочтительно, от 0,1 до 20 мг/м2.
Антинеопластическое средство применяют в дозах в очень широком диапазоне от 0,1 до 200 мг/кг.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЧЕТАННОЕ ПРИМЕНЕНИЕ EPA, DPA И DHA С ХИМИОПРЕПАРАТОМ | 2012 |
|
RU2637406C2 |
| КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2291710C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2011 |
|
RU2605335C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2018 |
|
RU2767664C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2011 |
|
RU2743643C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2018 |
|
RU2757373C2 |
| УЛУЧШЕННЫЕ СПОСОБЫ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2007 |
|
RU2481853C2 |
| ABX196 ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ РАКА МОЧЕВОГО ПУЗЫРЯ | 2018 |
|
RU2778812C2 |
| СПОСОБ ЛЕЧЕНИЯ РАКА (ВАРИАНТЫ) | 2006 |
|
RU2447889C2 |
| СПОСОБ ЛЕЧЕНИЯ СОЛИДНЫХ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ МЛЕКОПИТАЮЩИХ | 2024 |
|
RU2841088C2 |

Данное изобретение относится к области медицины и касается комбинации для лечения опухолевого заболевания, включающей в качестве активного ингредиента, по меньшей мере, одно иммуностимулирующее средство общей формулы (II) и одно или более химиотерапевтических средств, выбранных из группы, состоящей из алкилирующих средств, включающих карбоплатин, цисплатин и оксалиплатин, цитостатических средств, выбранных из циклофосфамида и его производных, и антиметаболитов, выбранных из фторурацила и его производных, и способу лечения опухолевых состояний. Изобретение обеспечивает повышенную эффективность лечения. 2 н. и 16 з.п. ф-лы, 8 ил., 5 табл.
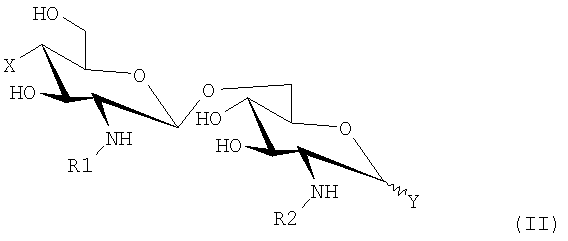
1. Комбинация, предназначенная для лечения теплокровных животных, включая людей, страдающих от опухолевого заболевания, включающая иммуномодулирующее средство общей формулы (II)
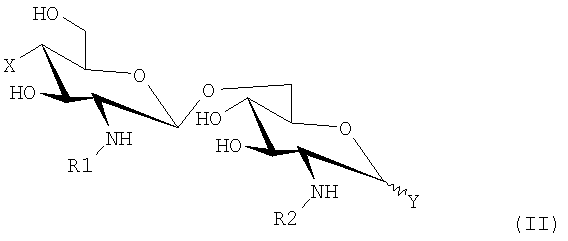
где
каждый из R1 и R2 обозначает ацильную группу, являющуюся производной карбоновой кислоты, имеющей от 2 до 24 атомов углерода, содержащую один или более заместителей, выбранных из гидроксила и ацилокси,
Х обозначает дигидроксифосфорилокси,
Y обозначает дигидроксифосфорилокси,
и волнистая линия показывает α- или β-ориентацию;
и одно или более химиотерапевтических средств, выбранных из группы, состоящей из алкилирующих средств, включающих карбоплатин, цисплатин и оксалиплатин, цитостатических средств, выбранных из циклофосфамида и его производных, и антиметаболитов, выбранных из фторурацила и его производных.
2. Комбинация по п.1, в которой средство общей формулы II находится в форме аддитивной соли с минеральным или органическим основанием.
3. Комбинация по п.1, в которой средство общей формулы II эстерифицировано гидроксидодеканоильным фрагментом.
4. Комбинация по п.1, в которой химиотерапевтическое средство находится в форме фармацевтически приемлемой аддитивной соли.
5. Комбинация по п.1, в которой средство общей формулы II представляет собой средство структурной формулы (III)
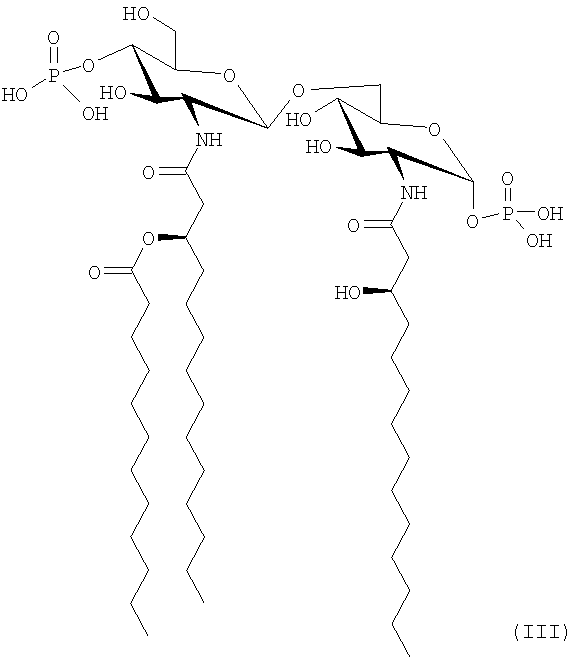
6. Комбинация по п.1, в которой иммуномодулирующее средство общей формулы (II) и химиотерапевтическое средство содержатся внутри единичного контейнера.
7. Комбинация по п.1, в которой иммуномодулирующее средство общей формулы (II) и химиотерапевтическое средство расположены внутри отдельных контейнеров.
8. Способ лечения опухолевого заболевания у теплокровных животных, включающих человека, который состоит во введении эффективного количества комбинации по п.1.
9. Способ по п.8, где комбинацию по п.1 вводят в фармацевтически приемлемом носителе, эксципиенте или составе посредством перорального, парентерального, ректального, местного, подкожного или подслизистого пути введения.
10. Способ по п.8, где иммуномодулирующее средство общей формулы (II) и одно или более химиотерапевтических средств назначают одновременно.
11. Способ по п.8, где иммуномодулирующее средство общей формулы (II) и одно или более химиотерапевтических средств назначают последовательно.
12. Способ по п.8, где иммуномодулирующее средство общей формулы (II) и одно или более химиотерапевтических средств применяют местно к опухолевой ткани.
13. Способ по п.8, где иммуномодулирующее средство общей формулы (II) и одно или более химиотерапевтических средств применяют в носителе с контролируемой или замедленной доставкой.
14. Способ по любому из пп.8-13, где опухолевое заболевание принадлежит к группам рака легкого, рака молочной железы, колоректального рака, рака желудка, рака печени, рака шейки матки, рака пищевода, рака головы и шеи, рака мочевого пузыря, злокачественных неходжкинских лимфом, лейкемии, рака простаты и рака яичка, рака поджелудочной железы, рака яичника, рака почки, рака эндометрия, рака нервной системы, меланомы, рака щитовидной железы, рака глотки и болезни Ходжкина, карциномы сквамозных клеток, глиомы, миеломы и других солидных или лимфомных опухолей.
15. Способ по п.8, где химиотерапевтическое средство выбирают из комплексов платины, таких как карбоплатин, цисплатин и оксалиплатин, а опухолевое заболевание представляет собой рак яичек, мочевого пузыря, легкого, пищевода, желудка, толстой и прямой кишок и яичника.
16. Способ по п.8, где химиотерапевтическое средство выбирают из циклофосфамида и его производных, а опухолевое заболевание представляет собой хроническую лимфоцитарную лейкемию, лимфомы, рак яичника и рак мочевого пузыря.
17. Способ по п.8, где химиотерапевтическое средство выбирают из фторурацила и его производных, а опухолевое заболевание представляет собой рак кишечника, молочной железы, желудка и пищевода.
18. Способ по п.8, в котором введение эффективного количества комбинации по п.1 производится в сочетании с лучевой терапией.
| ГЛЮКОЗАМИНОВЫЕ ДИСАХАРИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2154068C2 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Г-. . .' • ' . | 0 |
|
SU192296A1 |
| US 4912094 A, 27.03.1990 | |||
| ХАРКЕВИЧ Д.А | |||
| Фармакология | |||
| - М.: Медицина, 1993, с.45 | |||
| ДАРЬЯЛОВА С.Л., ЧИССОВ В.И | |||
| Диагностика и лечение злокачественных опухолей | |||
| - М.: Медицина, 1993, с.8. | |||
Авторы
Даты
2010-08-20—Публикация
2005-03-10—Подача