(5) УСТРОЙСТВО ДЛЯ ОПРЕДЕЛЕНИЯ СТЕПЕНИ НАДЕЖНОСТИ УКУПОРКИ ГЕРМЕТИЧЕСКИ ЗАКРЫТЫХ ЕМКОСТЕЙ



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ производства трихлорида лютеция-177 и технологическая линия для его реализации | 2017 |
|
RU2674260C1 |
| Способ производства трихлорида лютеция-177 и технологическая линия для его реализации | 2017 |
|
RU2676992C1 |
| Способ определения глюкозы в растворах | 1981 |
|
SU992570A1 |
| УНИВЕРСАЛЬНЫЙ АНАЛИЗАТОР ПАРОГАЗОВЫХ ПРОБ И ЖИДКОСТЕЙ И ВЕЩЕСТВ НА ПОВЕРХНОСТИ (ВАРИАНТЫ) | 2013 |
|
RU2526599C1 |
| Установка для получения дозированной смеси инертного радиоактивного газа с воздухом | 1961 |
|
SU259325A1 |
| СПОСОБ СУШКИ БИОПРЕПАРАТА В АМПУЛАХ | 1994 |
|
RU2108382C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ФОРТЕЛИЗИН, ОБЛАДАЮЩЕГО ФИБРИНОЛИТИЧЕСКИМИ СВОЙСТВАМИ, И ЕГО ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ИНФАРКТА МИОКАРДА | 2011 |
|
RU2448158C1 |
| Устройство для дозирования реакционноспособных и нестабильных жидких веществ и газовый хроматограф | 1987 |
|
SU1539656A1 |
| СПОСОБ ПРОМЫШЛЕННОГО ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 2010 |
|
RU2448727C2 |
| ДЕСОРБЕР | 1996 |
|
RU2099700C1 |
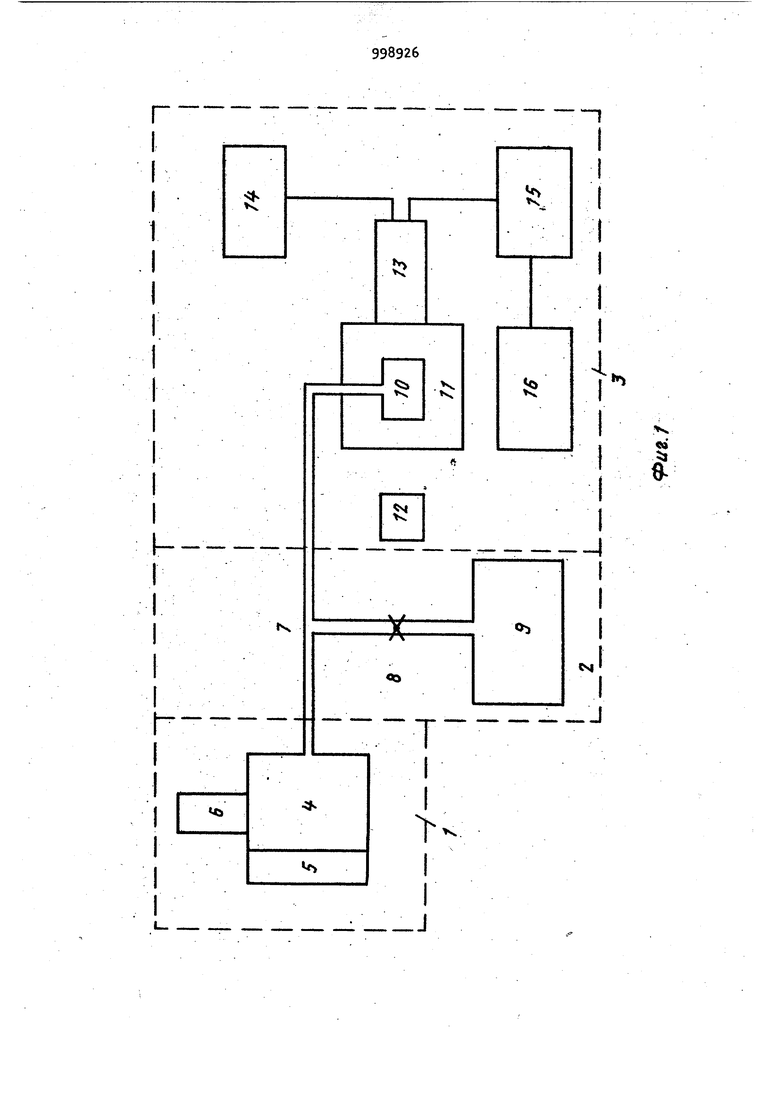
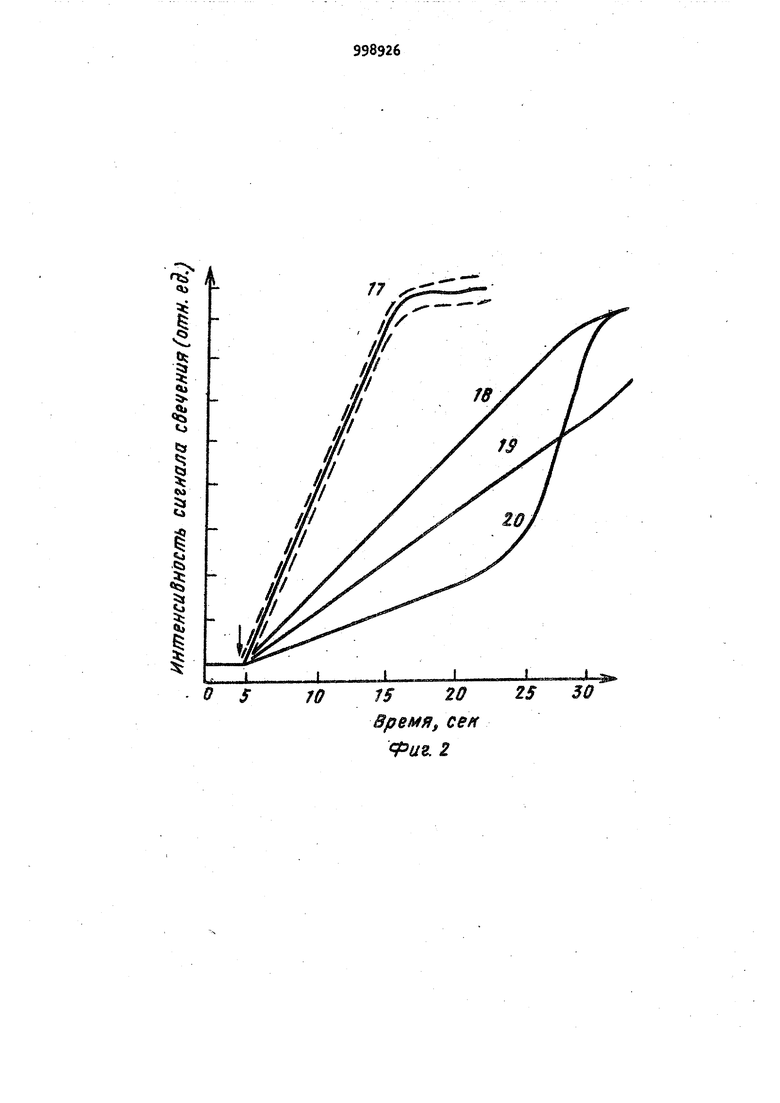
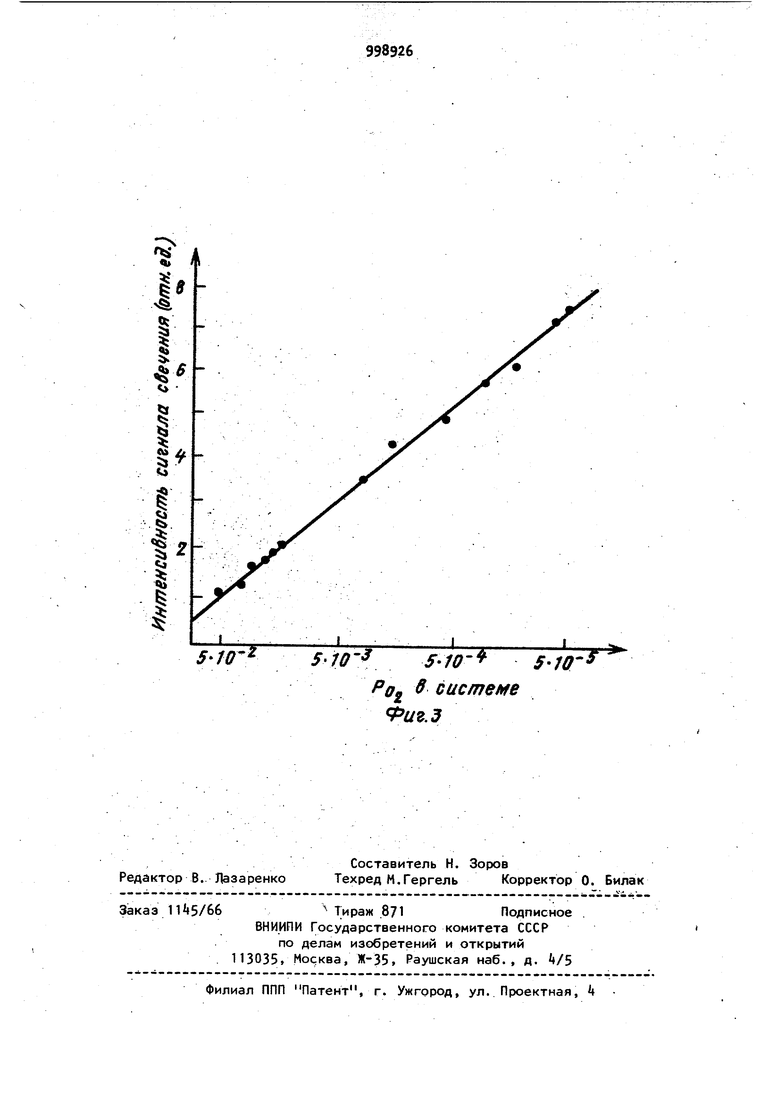

Изобретение относится в основном к промышленному получению медицинских и ветеринарных биологических препаратов и касается методов контроля содер жания кислорода в газовой фазе флако,нов и ампул биопрепаратов и качества их укупорки, оно также может быть Применено ив других случаях, когда необходимо определять герметичность укупорки и содержание кислорода в герметически закрытых емкостях. В настоящее время по рекомендации Всемирной организации здравоохранения (803) биологические препараты должны выборочно контролироваться на содержание остаточного кислорода и на качество их гepмetизaции в атмосфере инертных газов. Оба эти показателя определяют срок хранения и качество биопрепаратов, по скольку некачественная герметизация и повышенные концентрации кислорода в газовой фазе ампул и флаконов биопрепаратов приводят к быстрой инактивации активного начала препаратов. На сегодняшний день контроль этих показателей осуществляется порознь. Известно техническое решение, в котором для определения степени надежности укупорки герметически закрытых емкостей используют барокамеры, когда раствор метиленового синего под давлением в несколько атмосфер (З5 атм) просачивается через неплотности и трещины флаконов и ампул С J Однако такое оборудование является достаточно сложным и имеется лишь в нескольких зарубежных предприятикх по производству биопрепаратов. Наиболее близким техническим решением к изобретению является устройство для определения степени надежности укупорки герметически закрытых емкостей, содержащее блок для размещения этих емкостей, вакуумную линию и индикаторный блок L 2 . Определение степени герметичности осуществляют погружением ампул и флаконов в раствор метиленового синего и созданием вакуумной линией частич™ ного вакуума в течение 15-20 мин с последующим возвращением в условия нормального атмосферного давления. В ампулах и флаконах, имеющих трещины и мелкие отверстия, будет обнаруживаться какое-то количество красящего вещества. Индикация осуществляется визуально. Однако известным способом можно обнаруживать лишь большие дефекты, а мелкие трещины, которые образуются на сравнительно большом количестве ампул, обнаружить нельзя. Кроме того, недостатком известного способа также является невозможность определения кислорода в газовой фазе. Кислород вЬ флаконах с биопрепаратами определяют методом газовой хроматографии. Для этого пробу газа из флакона отбирают с помощью шприца и вводят в хроматограф. Анализ кислорода в хроматографе включает следующие операции: последовательную адсорбцию отдельных компонентов газовой смеси на адсорбенте и поочередное вымывание их током гелия с одновременным анализом теплопроводности протекающего газа. Концентрацию кислорода определяют по току в детекторе по теплопроводности. Время одного анализа около 2 мин Предел чувствительности по кислороду около 0,5 мл/л инертного газа. Имеются сведения о том, что применение газохроматографического метода для определения содержания кислорода в газовой фазе ампул с биопрепаратами не дало удовлетворительных результатов. Таким образом, из-за отсутствия подходящего метода определение кислорода в ампулах с биопрепаратами 8 СССР вообще не производится. Из сказанного очевидно, что выполнение рекомендаций ВОЗ связано с определенными ТРУДНОСТЯМИ, поскольку не обходимо иметь на каждом предприятии целый комплекс измерительной техники и проводить анализ на герметичность и содержание кислорода независимо в два этапа. Учитывая то, что СССР в достаточно широких масштабах поставляет продукцию (биопрепараты) за границу и эта продукция должна соответствовать требованиям 803, разработка оператив НОИ методики контроля этих показателей является важной практической задачей. Цель изобретения - сокращение времени анализа и проведение контроля на герметичность и остаточный кислород. Поставленная цель достигается тем, что в устройстве для определения сте- пени надежности укупорки герметически закрытых емкостей, содержащем блок для размещения этих емкостей, вакуумную линию и индикаторный блок, блок для размещения анализируемых емкостей содержит приспособление для их вскрытия и снабжен герметизирующей крышкой, индикаторный блок выполнен в виде оптически связанных кюветы с чувствительным к кислороду люминофором, ИСТОЧника света и системы регистрации, при этом блок для размещения анализируемых емкостей соединен посредством вакуумной линии с кюветой. На фиг. 1 изображено предлагаемое устройство; на фиг. 2 и 3 кривые, соответствующие обезгаживанию системы, Устройство содержит блок для размещения анализируемых емкостей 1, вакуумную линию 2 (с насосом), индикаторный блок 3- Блок для размещения анализируемых емкостей 1 включает в себя герметичную вакуумнуй камеру для ампул и флаконов 4, герметизирующую заглушку для ввода и вывода анализируемых емкостей с газом5, механизм для разгерметизации ампул и флаконов в условиях вакуума 6. Вакуумная линия содержит саму линию 7 вакуумный кран 8 и насос 9« Индикаторный блок содержит люминофор, расположённый в кварцевой кювете 10, которая связана вакуумной линией с блоком для размещения анализируемых емкостей, и находящийся, например, в фосфороскопе 11, источник света 12 и регистратор, состоящий, например из приемника излучения (ФЭУ) 13 высоковольтный источник питания ФЭУ Н, усилителя элект- : рических сигналов с ФЭУ 15, регистратора типа самописца 16. Анализ проводят следующим образом. В камеру k помещают исследуемый образец и камеру герметизируют крышкой 5- Включают вакуумный насос 9 источник света 12, фосфороскоп 11, высоковольтный источник питания 1, усилитель 15 и регистратор 1б. При этом кран 8 находится в положении, отделяющем вакуумный насос от осталь ной системы. На первом этапе произвр дят определение качества герметизации Для этого кран 8 открывают и ре гистрируют на ленте самописца 16 кинетику удаления воздуха из системы. На фиг. 2, 3 показаны кривые, соот ветствующие обезгаживанию системы. Для качественно герметизированных препаратов 17 (пунктиром обозначены допуски в кинетике удаления воздуха) .кривые имеют близкий вид, в то время как некачественно гермет,изированные препараты имеют самую различную кинетику 18, 19, 20. Однако во всех случаях кинетика удаления газа существенно более длительная. После проверки герметичности, в случае если биопрепарат герметизирован качественно, приступают к знализу на остаточный кислород в газовой фазе ампул и флаконов биопрепаратов. Для этого ампулу или флакон вскрывают с помощью устройства для вскрытия ампул и флаконов в вакууме 6 и регистрируют снижение сигнала свечения ин дикатора. По величине сигнала свечения индикатора с помощью,калибровочной кривой определяют концентрацию кислорода. Перед вскрытием ампулы ил флакона кран 8 вновь перекрывают. Как уже было сказано, для точного количественного определения содержания кислорода в газовой фазе образцов устройство предварительно калибруется по кислороду. На фиг. 3 преД ставлен график, показывающий зависимость между показаниями индикатора и концентрацией кислорода в системе. Калибровку осуществляют с помощью введения в систему порций газа с:известной концентрацией кислорода. Наприме р, можно калибровать устройство с помощью запаянных на воздухе стеклянных капилляров заданного . Калибровка проводится один раз перед целой серией анализов. П р и м е р. Выполнение анализа. Помещаем ампулу препарата осповакцйны в камеру 4, закрываем герметической крышкой 5 камеру, включаем в сет вакуумный насос Э, источник света 12 фосфороскоп 11 , высоковольтный блок Tt, усилитель 15 и самописец 16, Кра 8 перекрыт. На ленте самописца регис . рируем исходный сигнал от индикатора 10, соответствующий содержанию кисло рода в воздухе при атмосферном давле нии. На ленте самописца этот сигнал обозначен линией от О до стрелки (фиг. 2). После открытия крана 8 регистрируем кинетику обезгаживания системы и получаем кривую, соответствующую кривой 17 (фиг. 2), через 10 с после открытия крана его вновь закрывают , а ампулу вскрывают с помощью устройства длявскрытия ампул В вакууме 6. На ленте самописца регистрируем падение сигнала до уровня, соответствующего 6 условным единицам по калибровочному графику (фиг. 3). Из последнего находим, что в системе находится кислород, создающий давление Ю атм. . Учитывая, что в ампуле был газ под давлением 1 атм, а ее объем составляет 2,5 мл, находим, что концентрация кислорода в ампуле составляет 1 мл/л инертного газа. Эта величина получена расчётом по формуле К --у-, где ,Pj - парциальное давление кислорода в системе после вскрытия биопрепарата; PQ - парциальное давление кислорода в воздухе при атмосферном давлении; Vc - объем анализируемой порции газа из биопрепарата; Vp - объем системы. Символом К обозначена величина объемного отношения кислорода к объему анализируемой порции газа. В качестве люминофора в устройстве использован трипафлавин, сорбированный на силикагеле из водно-спиртовой смеси, которая дополнительно содержала сывороточный альбумин. Ломинофор готовили следующим образом. Трипафлавин растворяли в водноспиртовой смеси (соотношение компонентов 0,001:1:1 по весу), затем добавляли 0,05 белка (человеческий сывороточный альбумин в виде сухого порошка) и этой смесью заливали мелко размолотый силикагель с размером зерен около 0,1-0,2 мм, который предварительно был помещен в кварцевую ампулу. Ампула выполнена в виде небольшой емкостиобъемом 0,2 мл с площадью кварцевых стекол 2 см и зазором между ними 0,1 см. После наполнения )юветы водно-спиртовой смесью и пропитки силикагеля растворитель удаляли вакуумной возгонкой. Хорошие резул 1таты были также получены при использовании в качестве индикатора флавинадениндинуклеотида (ФАД), приготовленного тем же способом.Для нашей системы величина ее объема составляет 25 мл, откуда расчетом по формуле и получаем величину 10, т.е. в одном литре инертного газа содержится 1 мл кислорода. Время, затрачиваемое на проведение одного анализа, составляет не более 30 с. , Согласно требованиям ВОЗ концентрация кислорода в препаратах не должна превышать 1 мл/л. Из фиг. 3 видно, что предлагаемое устройство позволяет регистрировать остаточный кислород вплоть до 0,1 мл/л. В соответствии с требованиями ВОЗ контроль препаратов должен осуществляться выборочно, однако, учитывая массовый характер производства, время, затрачиваемое на проведение данного контроля, имеет немаловажное зна чение. Следует отметить, что предла гаемое устройство позволяет значитель но сократить- время на проведение анаЛИЗОВ. Другим важным преимуществом предла гаемого .устройства является его относительная Простота и дешевизна. Формула изобретения Устройство для определения степени надежности укупорки герметически закрытых емкостей, содержащее блок для размещения этих емкостей, вакуумную линию и индикаторный блок, о т л и чающееся тем, что, с целью одновременного сокращения времени анализа проведения контроля на герметичность и остаточный кислород, блок для размещения анализируемых емкостей содержит приспособление для их вскрытия и снабжен герметизирующей крышкой, индикаторный блок выполнен в виде оптически связанных кюветы с чувствительным к кис/юроду ломинофором, источника света и системы регистрации, при этом блок для размещения анализируемых емкостей соединен посредством вакуумной линии с кюветой. Источники информации. принятые во внимание при экспертизе Ь Brizell KG. and Shatwelj . Methods of detecting leaks inglass ampoules.-lhe Pharmacentical Journal t 1973, N 211, p. 73. 2. Melton H. et. al. Some problems jin sealing gas-filled glass-ampoules. International Symposium of freezedrying of biological products. Vashington, 1976, v. 36, p. kS (npoтотип).
Г
-1
Авторы
Даты
1983-02-23—Публикация
1981-07-08—Подача