Изобретение относится к медицине и ветеринарии, в частности к производству и использованию бактериальных препаратов, предназначенных для профилактических и лечебных целей.
Известен способ повышения неспецифической резистентности организма, предусматривающий введение в организм вакцины бактериального происхождения.
Недостатком этого способа является необходимость использования для приготовления вакцины патогенных микроорганизмов, что может привести к интоксикации, аллергизации, супрессии и т.п. Кроме того, область применения известного способа с достаточной достоверностью неизвестна, поскольку для определения эффективности вакцины использовались только экспериментальные животные - мыши.
Известен способ получения препарата для повышения резистентности организма, включающий культивирование микроорганизмов, отделение биомассы, последующее ее дезинтегрирование и очистку продукта путем дифференциального центрифугирования с последующей стерилизацией.
Технологическая схема способа выглядит следующим образом. Из грамотрицательных микроорганизмов Klebsiella pneumonie, Serratia marcescens, Escherichia coli при помощи механического разрушения и дифференциального центрифугирования выделяют фракцию мембран (при режиме 30000 g x 45 мин), которые гидролизуют лизоцимом. Фракцию неочищенных лиофилизированных протеогликанов гидролизуют при 56оС в течение 1 ч щелочью (0,1 М NaOH), после охлаждения суспензию нейтрализуют HCl, диализуют против дистиллированной воды, затем суспензию центрифугируют (30000 g x 45 мин). Лиофилизированная надосадочная жидкость представляет собой растворимые "неочищенные" мембранные протеогликаны. Отделение протеогликанов мол.м. 200000 и 400000 кД из суммарного продукта гидролиза осуществляют несколькими методами: щелочью, гипобромитом или хроматографической фильтрацией. Кроме того проводят дополнительный гидролиз "неочищенных" мембранных протеогликанов лизоцимом, с делипидированием несколькими растворителями.
Однако способ получения иммуномодулятора из 3-х представителей патогенных грамотрицательных микроорганизмов является сложным. Многоэтапная в 2-х вариантах схема выделения и очистки препарата преследует отделение из суммарной мембранной фракции протеогликанов нетоксичных иммуногенных компонентов мол. м. 200000 и 400000 кД. Упростить технологическую схему выделения протеогликанов невозможно, так как введение в макроорганизм природной смеси "неочищенных" антигенных иммуногенных компонентов мембран патогенных бактерий (K. pneumonie, E. coli, S. marcescens) приведет, как указывалось, к отрицательным явлениям интоксикации, аллергизации, супрессии и т.д.
Задачей изобретения является исключение вредных побочных явлений при вакцинации за счет использования для приготовления вакцины нетоксигенных штаммов микроорганизмов, расширение области применения способа, а также упрощение технологии, снижение трудоемкости, повышение производительности и степени безопасности за счет использования в качестве исходного материала нетоксигенного бактериального штамма.
Поставленная задача решается за счет использования в качестве вакцины препарата нетоксигенного штамма C. diphtheriae 5047, культивирование которого осуществляют на жидкой питательной полусинтетической среде с предварительным подращиванием маточного кульрурального раствора. Такая технология приводит к увеличению выхода биологически активной, но безвредной массы, уменьшению полиморфных форм клеток. Получаемый при этом состав однородных по размеру клеток в культуре увеличивает процент их разрушения, а следовательно и процент выхода конечного продукта - клеточных стенок. Важным преимуществом выращивания C. diphtheriae на жидкой полусинтетической питательной среде является возможность отказаться от использования в технологическом цикле каких-либо детергентов, поскольку за счет повышения однородности клеток упрощается фракционное разделение клеточных стенок от целых бактерий и других органелл клетки.
Исключение детергентов обеспечивает повышение чистоты продукта и улучшение экологических условий производства.
Оптимальные режимы центрифугирования - первая стадия центрифугирования не менее чем при 5000 g, в течение не менее чем 20 мин, и вторая стадия не менее чем при 14000 g, в течение не менее чем 20 мин - установлены на основании практических данных.
Экспериментально установлен оптимальный температурный режим тепловой стерилизации продукта - до 100оС, при превышении которого происходит инактивация биологической активности.
Использование тепловой стерилизации позволяет исключить какие-либо консерванты химического происхождения.
Для обеспечения возможности длительного хранения продукта его подвергают лиофильному высушиванию.
В качестве основы жидкой питательной полусинтетической среды используют гидролизат казеина, являющийся экономически более дешевым и технологически более стандартным.
Способ повышения неспецифической резистентности организма и способ получения препарата для него осуществляются следующим образом.
Начальным этапом получения препарата является выращивание микробной биомассы на основе нетоксигенного штамма Corinebacterium diphtheriae 5047, который хранится в коллекции ГИСК им. Л.А.Тарасевича под номером 2 и характеризуется следующими культурально-морфологическими и физиолого-биохимическими признаками.
Культурально-морфологические признаки. Сывороточный агар. После 18 ч роста полиморфные палочки длиной 1-5 мкм, толщиной 0,3-0,6 мкм. Кровяно-теллуритовая среда. Гладкие, черно-серые колонии. Мясопептонный бульон. Мелкие гранулы, выпадающие в осадок. Среда Пизу. Почернение среды, по ходу укола образуется "облачко" темно-коричневого цвета.
Физиолого-биохимические свойства. Аэроб. Оптимум роста при 37оС. Усваивает глюкозу, крахмал. Не расщепляет сахарозу. Проба на цистиназу положительная. Проба на уреазу отрицательная.
Серологические свойства. Не типируется агглютинирующими сыворотками I и II севовариантов. Типируется сывороткой к нетоксигенному gravis штамму 23607, выделенному от носителя. Штамм C. diphtheriae 5047 принадлежит к C. diphtheriae, var. gravis. Токсин не продуцирует. Отношение к фагам. По фаготипированию по схеме Крыловой относится к группе III, фаговарианта К.
Толщина основного массива клеточной стенки характеризуется двумя слоями.
Нетоксигенные Corinebacterium diphtheriae выращиваются в течение 16-18 ч на плотной питательной среде (рыбный гидролизат с добавлением сыворотки крупного рогатого скота) при температуре 37оС. Затем культуру смывают жидкой питательной средой на основе гидролизата казеина и после 5 ч культивирования вносят в рабочие емкости с той же жидкой питательной средой и проводят в течение 16-18 ч выращивание биомассы при постоянном перемешивании при температуре 37оС.
Микробные клетки осаждают центрифугированием не менее, чем при 5000 g в течение не менее 20 мин и трижды промывают физиологическим раствором при центрифугировании в режиме не менее 5000 g в течение не менее 20 мин.
Влажный осадок взвешивают, суспендируют в забуференном физиологическом растворе (рН 7,2) до концентрации клеток 5%. Затем целые клетки дезинтегрируют на ультразвуковой установке в течение 20 мин при частоте 20 кГц, амплитуде 14 мкм и охлаждении (льдом или водой) до 25-30оС.
Полученную после ультразвуковой обработки гомогенную суспензию дезинтеграта центрифугируют не менее, чем при 5000 g в течение не менее 20 мин с целью отделения неразрушенных клеток и их фрагментов от клеточных стенок. Осадок удаляют, надосадочную жидкость центрифугируют не менее, чем при 14000 g в течение не менее 20 мин. Осадок, представляющий собой препарат клеточных стенок, ресуспендируют в физиологическом растворе и снова центрифугируют не менее, чем при 14000 g в течение не менее 20 мин. Отмывание клеточных стенок от примеси цитоплазмы и питательной среды повторяют 3 раза. Отмытые клеточные стенки ресуспендируют в дистиллированной воде (маточный раствор). После определения содержания в маточном растворе N-ацетилглюкозамина по Элсону-Моргану его разводят до концентрации прививочных доз, разливают по амплитуде или флаконам, после чего его могут подвергнуть тепловой стерилизации при температуре до 100оС и лиофильному высушиванию. Сухой препарат - порошок беловатого цвета, после разведения в физиологическом растворе образует суспензию, разделяющуюся при стоянии на прозрачную жидкость и рыхлый осадок, разбивающийся при встряхивании.
Вакцинация препаратом обеспечивает повышение естественной резистентности, т. е. усиливает сопротивляемость организма к инфекционным болезням у людей и особенно у молодняка сельскохозяйственных животных (новорожденных телят и поросят), особи которых с первых дней подвержены инфекционным респираторным и кишечным заболеваниям.
П р и м е р 1. Иммунизация препаратом вызывает неспецифические сдвиги в иммунной системе макроорганизма, которые наиболее сильно выражены в группе носителей токсигенных C. diphtheriae. По сравнению с группой здоровых людей (контроль) у них наблюдается резкое увеличение всех популяций лимфоцитов: B-клеток, T-клеток, зрелых Т-клеток, незрелых Т-клеток.
П р и м е р 2. Препарат увеличивает содержание Т-хелперов (статистически значимое, P<0,05), T-супрессоров (выраженное, но статистически недостоверное, P>0,05).
Сдвиги в хелперно-супрессорном отношении у здоровых людей отсутствуют, а у бактерионосителей этот показатель имеет слабо выраженную тенденцию к увеличению.
Таким образом, иммунизация предлагаемым препаратом вызывает поликлональную стимуляцию иммунокомпетентных клеток.
П р и м е р 3. Функциональная хелперная активность лимфоцитов в группе носителей токсигенных C. diphtheriae до иммунизации и в первые 10 дн после иммунизации намного ниже, чем у здоровых людей. Существенные изменения хелперной активности лимфоцитов и у носителей, и у здоровых людей наблюдаются только к 21-у дню после иммунизации. Активность Т-хелперов у бактерионосителей резко возрастает. Активность Т-хелперов у здоровых людей - снижается. Таким образом, препарат вызывает без "бурного возмущения" неспецифически корригирующие сдвиги в численности и активности популяций иммунокомпетентных клеток и приводит их активность, как и численность, к динамическому равновесному состоянию: стабилизации Т-хелперов у здоровых лиц и к увеличению активности у носителей, доводя иммуную систему до физиологической нормы, тем самым оптимизируя резистентность макроорганизма.
П р и м е р 4. Кинетика изменений хелперно-супрессорного отношения у вакцинированных людей свидетельствует о том, что этот показатель варьирует в пределах нормы, т.е. доминирования иммуносупрессии, характерной для многих бактериальных вакцин, не наблюдается.
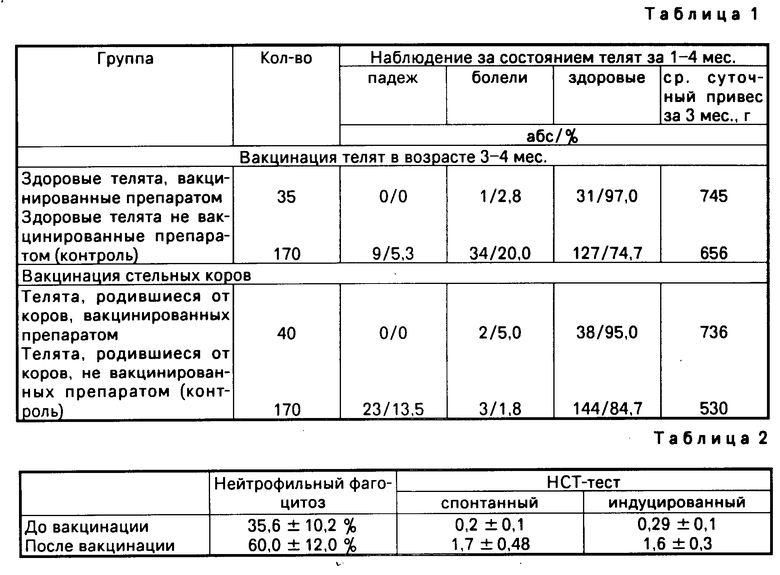
П р и м е р 5 (табл. 1). Клиническая характеристика состояния сельскохозяйственных животных после вакцинации предлагаемым препаратом.
При вакцинации препаратом стельных коров и телят он проявляет себя как абсолютно безвредный (атоксичен, ареактогенен, легко переносим, отсутствие местных реакций). Выживаемость иммунизированных телят составляет 100%, в то время как в контрольных неиммунных группах телят падеж молодняка достигал 5,3 и 13,5%. Аналогичная картина наблюдается в показателях заболеваемости. При этом средний привес у вакцинированных животных выше, чем у животных контрольной неимунной группы. Использование препарата для вакцинации приводит к снижению заболеваемости, падежа, способствует увеличению средне-суточного привеса.
П р и м е р 6 (табл. 2). Повышение неспецифической противоинфекционной резистентности после вакцинации животных препаратом отражается в увеличении активности поверхностных рецепторов иммунокомпетентных клеток (в тестах нейтрофильного дрожжевого фагоцитоза и НСТ-теста). Необходимо отметить, что помимо прямой функции - фагоцитарной активности, нейтрофилы выполняют в организме ряд других важных действий, непосредственно связанных с процессами гомеостаза. Таким образом, на фоне стимулирующего действия препарата функциональная значимость нейтрофилов увеличивается.
Из приведенных примеров видно, что использование изобретения в медицине и ветеринарии позволит снизить инфекционную заболеваемость у людей и особенно сельскохозяйственных животных, сократить применение других лечебных препаратов, в том числе реактогенных вакцин и антибиотиков, приводящих к сенсибилизации организма, нарушению микроэкологии кишечника и к увеличению плотности циркуляции высокопатогенных антибиотикоустойчивых штаммов микроорганизмов.
Вакцинация сельскохозяйственных животных иммунологически безвредным препаратом будет способствовать увеличению выхода натурального целевого продукта - мяса, молока, безопасного для потребления людьми и без аллергического компонента в его составе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИМБИОНТНЫЙ ШТАММ Corynebacteriae diphtheriae tox - № 108, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ИММУНОМОДУЛЯТОРА, СОЗДАЮЩЕГО НЕСПЕЦИФИЧЕСКУЮ РЕЗИСТЕНТНОСТЬ ПРОТИВ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ БАКТЕРИАЛЬНОЙ И ВИРУСНОЙ ПРИРОДЫ У СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 2011 |
|
RU2477751C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО БАКТЕРИАЛЬНОГО ПРЕПАРАТА, СОДЕРЖАЩЕГО СТРУКТУРНЫЕ КОМПОНЕНТЫ МИКРОБНОЙ КЛЕТКИ | 2002 |
|
RU2230113C1 |
| ПРОБИОТИЧЕСКИЙ БАКТЕРИАЛЬНЫЙ ПРЕПАРАТ КОРПУСКУЛЯРНЫХ АНТИГЕНОВ КОРИНЕБАКТЕРИЙ ЛИПОПЕПТИДОПОЛИСАХАРИДНОЙ ПРИРОДЫ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2468816C1 |
| Метабиотический препарат-иммуномодулятор, содержащий клеточные стенки симбионтных коринебактерий, для укрепления врожденного иммунитета и способ его получения | 2017 |
|
RU2648156C1 |
| СПОСОБ ПОВЫШЕНИЯ НЕСПЕЦИФИЧЕСКОЙ РЕЗИСТЕНТНОСТИ И ИММУНОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ СВИНЕЙ ПРИ ВАКЦИНАЦИИ | 2006 |
|
RU2321414C1 |
| СПОСОБ ПОВЫШЕНИЯ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА | 1999 |
|
RU2183462C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕКТИВНОЙ БЕЛОКСОДЕРЖАЩЕЙ ФРАКЦИИ БАКТЕРИЙ | 2006 |
|
RU2311197C1 |
| СПОСОБ ПОВЫШЕНИЯ ПРОТИВООПУХОЛЕВОЙ РЕЗИСТЕНТНОСТИ | 2009 |
|
RU2418599C1 |
| СПОСОБ ПОВЫШЕНИЯ КОЛОСТРАЛЬНОГО ИММУНИТЕТА И НЕСПЕЦИФИЧЕСКОЙ РЕЗИСТЕНТНОСТИ У ТЕЛЯТ | 2021 |
|
RU2765287C1 |
| СПОСОБ ПОВЫШЕНИЯ КОЛОСТРАЛЬНОГО ИММУНИТЕТА И НЕСПЕЦИФИЧЕСКОЙ РЕЗИСТЕНТНОСТИ У ТЕЛЯТ | 2023 |
|
RU2829968C1 |
Изобретение относится к медицине и ветеринарии, в частности к производству и использованию бактериальных препаратов, предназначенных для профилактических и лечебных целей, достигаемых путем повышения неспецифической резистентности у людей и сельскохозяйственных животных. Повышение неспецифической резистентности организма как у людей, так и у сельскохозяйственных животных достигается за счет использования в качестве вакцин препарата из нетоксигенного штамма Corinebacterium diphtheriae 5047. Препарат получают путем культивирования указанного штамма на жидкой питательной полусинтетической среде с предварительным подращиванием маточного культурального раствора. Выращенную биомассу дезинтегрируют, очищают путем дифференциального центрифугирования, стерилизуют и подвергают лиофильному высушиванию. Использование изобретения позволяет исключить вредные побочные явления (интоксикацию, аллергизацию, супрессию и т.п.) как при вакцинации людей и сельскохозяйственных животных, так и при производстве мясо-молочной продукции. 2 с. и 4 з.п. ф-лы, 2 табл.
| Патент США N 4501693, МКИ A 61K 37/102, 1985. |
Авторы
Даты
1994-09-15—Публикация
1992-05-25—Подача