Изобретение относится к биотехнологии, в частности к производству пробиотических бактериальных препаратов, и может быть использовано в ветеринарии и медицине для профилактики и лечения инфекционных заболеваний животных и человека, а также коррекции микробиоценозов.
С современных позиций микрофлору человека рассматривают как совокупность множества микробиоценозов, занимающих многочисленные экологические ниши на коже и слизистых всех открытых внешней среде полостей организма [1]. Симбиотические ассоциации микроорганизмов, составляющих микрофлору человека, чрезвычайно сложны по составу. Помимо достаточно хорошо известных групп бактерий - бифидобактерии, лактобациллы, клостридии, кампилобактеры, в состав нормальной микрофлоры входят многочисленные представители других видов микроорганизмов, в том числе коринебактерии [3]. Коринебактерии являются одним из основных представителей микрофлоры кожи, они входят также в состав микрофлоры дыхательных путей, полости рта, вагины, наружных гениталий. Вместе с тем роль коринебактерий, входящих в эти симбиотические ассоциации, недостаточно изучена и поэтому до настоящего времени неизвестно использование коринебактерий в качестве пробиотических микроорганизмов.
Бактериальные препараты - пробиотики используются в ветеринарии и медицине для лечения и профилактики многих инфекционных заболеваний. Широко известно применение бифидобактерий, лактобацилл, кишечных палочек, энтерококков, пропионибактерий и других представителей нормальной микрофлоры человека и животных для приготовления пробиотиков, биологически активных добавок, продуктов функционального питания. При этом во всех случаях используют живые микроорганизмы.
Вместе с тем из научной литературы известно, что теоретически пробиотики и БАДы могут быть приготовлены с использованием структурных компонентов микроорганизмов - представителей нормальной микрофлоры [2]. Однако до настоящего времени в доступной нам литературе сведения о таких разработках отсутствуют. Неизвестно также использование для приготовления пробиотиков симбионтных штаммов коринебактерии в виде живой культуры или структурных компонентов микробной клетки.
Задачей изобретения является создание пробиотического бактериального препарата, предназначенного для профилактики и лечения инфекционных заболеваний верхних дыхательных путей, кожи, вагины и других слизистых оболочек, а также коррекции микрофлоры открытых полостей человека и животных.
Указанная задача решается выявлением нетоксигенного симбионтного штамма коринебактерий дифтерии (Corynebacterium diphtheriae tox - № 5047 ГИСК им. Л.А. Тарасевича), клеточные стенки которого предназначены для приготовления пробиотического бактериального препарата с высокой терапевтической и профилактической активностью.
Для приготовления пробиотического препарата наращивают биомассу штамма (С. diphtheriae tox - № 5047 ГИСК им. Л.А. Тарасевича) на питательной среде, отделяют биомассу, дезинтегрируют ее, подвергают дифференциальному центрифугированию и стерилизации. Полученный пробиотик, представляющий собой клеточные стенки вышеуказанного штамма, используют для приготовления различных лекарственных форм: капсулы, капли, мази, таблетки, свечи, спрей (аэрозоль) и др.
Пример 1. Приготовление биомассы коринебактерий.
Штамм № 5047 выращивают в течение 16-18 часов на плотной питательной среде известного состава (рыбный гидролизат с добавлением сыворотки крупного рогатого скота в соотношении 3:1) при температуре 37°С. Затем культуру смывают жидкой питательной средой известного состава на основе гидролизата казеина и после 5 час культивирования при 37°С вносят в рабочие емкости с той же жидкой питательной средой и проводят в течение 16-18 час выращивание биомассы при постоянном перемешивании при температуре 37°С. Микробные клетки осаждают центрифугированием при 5000g в течение 20 мин и трижды промывают раствором хлорида натрия при центрифугировании в режиме не менее 5000g в течение 20 мин.
Пример 2. Получение препарата клеточных стенок коринебактерий.
Полученный влажный осадок целых клеток коринебактерий взвешивают, суспендируют в забуференном растворе хлорида натрия (pH 7,2) до концентрации клеток 5%. Затем эту суспезию (целые клетки) дезинтегрируют на ультразвуковой установке в течение 20 мин при частоте 20 кГц, амплитуде 14 мкм, при охлаждении (льдом или водой) до 25-30°С. Полученную после ультразвуковой обработки суспензию дезинтеграта центрифугируют при 5000g в течение 20 мин с целью отделения неразрушенных клеток и их фрагментов от клеточных стенок. Осадок удаляют, надосадочную жидкость центрифугируют при 14000g в течение 20 мин. Осадок, представляющий собой клеточные стенки, ресуспендируют в растворе хлорида натрия и снова центрифугируют при 14000g в течение 20 мин. Отмывание клеточных стенок от примеси цитоплазмы и питательной среды повторяют 3 раза. Отмытые клеточные стенки ресуспендируют в растворе глицина (15 мг в 1 мл). В полученном препарате определяют концентрацию биологически активного пептидополисахарида (расчет ведется по содержанию пентоз и гексоз по Биалю). Затем препарат разводят до необходимой концентрации и используют для получения той или иной лекарственной формы. При необходимости в зависимости от способа применения препарата его могут подвергнуть стерилизации при температуре 100°С и лиофильному высушиванию.
Пример 3. Приготовление капсул. Используются для коррекции микрофлоры кишечника.
Сухой лиофильно высушенный препарат рассыпают в капсулы в разной концентрации в зависимости от возраста больного.
Пример 4. Приготовление капель. Используются при локальных местных инфекционных поражениях кожи и слизистых оболочек.
Препарат в концентрации 3 мг в 1 мл используют при следующем соотношении компонентов, мас.%:
Препарат 0,15-0,2
Глицин 0,75-0,8
Янтарная кислота 0,05-0,5
Нипазол 0,0-0,1
Вода, мл 100
Янтарная кислота способствует заживлению ран и трещин, нормализует слизистую. Нипазол - консервант.
Пример 5. Приготовление суппозиторий (массой 2,4-2,7 г), соотношение компонентов в г, являются эффективным средством для лечения урогенитальных заболеваний, вызванных, в том числе, трихомонадами.
Препарат 0,003-0,005
Глицин 0,015-0,018
Твердый жир или Витасол 2,27-2,61
Аэросил 0,02-0,06
Эмульгатор - моностеарат
глицерина 0,01-0,03
Пример 6. Приготовление аэрозоля (в мас.%) для лечения слизистых оболочек верхних дыхательных путей.
Препарат 0,2-0,3
Глицин 1,0-1,3
Глицерин 1,05-1,1
Масло эвкалиптовое 0,05
Масло мяты перечной 0,05
Спирт этиловый 6,0
Азот 1,0-1,3
Вода очищенная До 100
Баллон содержит 150 аэрозольных доз.
Применение препарата с профилактической и лечебной целью при различных инфекционных заболеваниях, а также при лечении дисбактериозов открытых полостей животных и человека показало его клиническую эффективность.
Пример 7.
Так, препарат повышает резистентность мышей к инфекциям, вызываемым Klebs. Pneumoniae и St. Aureus. Это проявляется в выживаемости животных, а при стафилококковой инфекции и в уменьшении локальных очагов поражения кожи. Беспородным мышам за 1 сутки до заражения интраназально вводили раствор препарата в дозах 200 и 400 мкг. В таблице 1 представлены данные по влиянию препарата на устойчивость беспородных мышей на заражение их Klebs. Pneumoniae.

Пример 8.
В таблице 2 представлены результаты влияния препарата на заживление кожи мышей гибридов F1 (СВА × С 57 BI/6), пораженной стафилококковой инфекцией. Заражение кожи St. aureus в дозе 0,75×10-9 микробных клеток вызывало локальные очаги инфекции различной тяжести. Местное нанесение препарата в различной концентрации в виде суспензии в составе: клеточные стенки, глицин, глицерин избавляло животных от тяжелых стафилококковых поражений и оказывало эффективное терапевтическое действие, что проявлялось в ускорении сроков заживления очагов и избавляло животных от инфекции.

Пример 9.
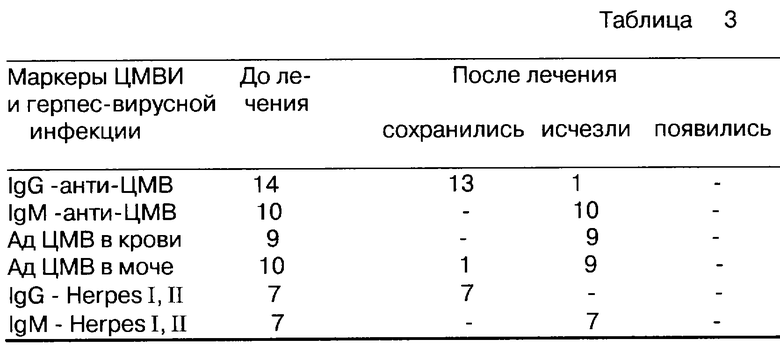
Использование препарата в виде капель и/или инъекций для лечения смешанной респираторно-вирусной инфекции с выраженной тенденцией формирования латентных форм: цитомегаловирусной (ЦМВИ) и герпес-вирусной инфекции приводило к значительному сокращению сроков освобождения организма от вирусов. В таблице 3 представлены результаты лечения препаратом 21 больных смешанной вирусной инфекцией, в крови которых определялись соответствующие циркулирующим вирусам маркеры.
Пример 10.
Введение препарата с питьевой водой с профилактической целью против кишечных инфекций телятам показало его абсолютную безвредность и эффективность. За три месяца наблюдения в опытной группе телят, принимавших препарат, не погиб ни один теленок. В контрольной группе телят, не принимавших препарат, наблюдалось их заболевание и падеж. При этом средний привес у телят, принимавших препарат, выше чем у животных контрольной группы.

Таким образом, впервые разработан эффективный пробиотический препарат на основе нетоксигенных коринебактерий дифтерии - представителей нормальной микрофлоры. Для его изготовления используется не вся микробная клетка, а только ее структурный компонент клеточная стенка, что обеспечивает его полную безвредность. Способ приготовления препарата высокотехнологичен и пригоден для использования в любых лекарственных формах - капсулах, порошках, мазях, аэрозолях, каплях, свечах и т.д. Изобретение обеспечивает повышение эффективности в профилактике и лечении инфекционных заболеваний животных и человека.
Источники информации
1. Шендеров Б.А. Медицинская микробная экология и функциональное питание. Том 1. Микрофлора человека и животных и ее функция. М.: Грантъ, 1998, с. 11.
2. Шендеров Б.А. Там же. Том 3. Пробиотики и функциональное питание. М.: Гранть, 2001, с. 32.
3. Bergey′s. Manual of Determinative Bacteriology - 9, 1994.
Изобретение относится к биотехнологии, в частности к производству пробиотических бактериальных препаратов, может быть использовано в ветеринарии и медицине для профилактики и лечения инфекционных заболеваний животных и человека, а также коррекции микробиоценозов. Для получения пробиотического бактериального препарата используют клеточные стенки симбионтного штамма нетоксигенных коринебактерий дифтерии Corynebacterium diphtheriae tox - № 5047 ГИСК им. Л.А. Тарасевича. Предлагаемый пробиотик безвреден, способ его приготовления высокотехнологичен и пригоден для использования в различных лекарственных формах – капсулах, порошках, мазях, аэрозолях, каплях, свечах и т. д., что обеспечивает повышение эффективности в профилактике и лечении инфекционных заболеваний животных и человека. 4 табл.
Способ получения пробиотического бактериального препарата, содержащего структурные компоненты клетки микроорганизмов, представителей нормальной микрофлоры, предусматривающий наращивание биомассы микроорганизмов, отделение ее с последующим выделением структурного компонента, отличающийся тем, что для приготовления пробиотического бактериального препарата в качестве структурного компонента микробной клетки используют клеточные стенки симбионтного штамма нетоксигенных коринебактерий дифтерии Corynebacterium diphtheriae tox - № 5047 ГИСК им. Л.А.Тарасевича.
| ШЕНДЕРОВ Б.А | |||
| Медицинская микробная экология и функциональное питание | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Микрофлора человека и животных и ее функция | |||
| - М.: Грантъ, 1998, с.11 | |||
| Там же, т.3 | |||
| Пробиотики и функциональное питание | |||
| - М.: Грантъ, 2001, с.32 | |||
| КОМПЛЕКСНЫЙ ПРОБИОТИЧЕСКИЙ ПРЕПАРАТ ВЕТЕРИНАРНОГО НАЗНАЧЕНИЯ | 1992 |
|
RU2084234C1 |
Авторы
Даты
2004-06-10—Публикация
2002-11-12—Подача