Изобретение относится к биотехнологии, в частности к производству пробиотических бактериальных препаратов, и может быть использовано для лечения и профилактики туберкулеза у людей и животных.
Туберкулез остается одним из самых распространенных и опасных инфекционных заболеваний, несмотря на то, что до 85% детей планеты вакцинированы против туберкулеза вакциной БЦЖ и постоянно совершенствуются терапевтические химиопрепараты (1, 2, 3).
Одной из причин недостаточной эффективности борьбы с туберкулезом является недостаточная эффективность вакцины БЦЖ на фоне постоянного роста числа лиц с пониженным иммунитетом. Другой причиной является рост числа штаммов М. tuberculosis, обладающих множественной лекарственной устойчивостью к применяемым химиопрепаратам, и отсутствие этиотропных иммунопрепаратов.
Туберкулез - хроническое инфекционное заболевание, наиболее часто поражающее легкие. Основным патогенетическим звеном туберкулеза является грануломатозное изменение структуры ткани вокруг очагов инфекции. Процесс формирования туберкулезной гранулемы начинается с проникновения М. tuberculosis в составе мелкодисперсных аэрозолей в альвеолы, где они поглощаются резидентными макрофагами. Взаимоотношение микобактерий с макрофагами определяет дальнейшее развитие туберкулезного процесса. Туберкулез считается классической внутримакрофагальной инфекцией (2, 5).
При высоком уровне неспецифической резистентности туберкулезные бактерии, попавшие в макрофагальные лизосомы, активно уничтожаются, высвободившиеся при этом антигены М. tuberculosis побуждают макрофаги к дальнейшей стимуляции воспалительных реакций, в основном неспецифического характера. Образуется доиммунная гранулема, инфекционный процесс обрывается (2).
При слабой потенции иммунитета ведущая роль в развитии инфекционного процесса принадлежит М. tuberculosis. Клеточные стенки М. tuberculosis содержат огромное количество разнообразных липидов, которые входят не только в состав поверхностной мембраны, но и пронизывают весь сложный регидный каркас пептидогликана и арабиногалактана (6, 7). Уникальный липопептидополисахаридный состав клеточных стенок М. tuberculosis позволяет им во время внутримакрофагального пребывания гибельно воздействовать на лизосомы, подавляя их образование или превращая в комфортную для себя зону. Замедленный процесс роста, длительное пребывание М. tuberculosis в лизосомах, беспрепятственный выход в цитоплазму, устойчивость к антимикробным факторам или их инактивация ослабляют чувствительность макрофагов к активирующим сигналам лимфоцитов, снижают их антигенпредставляющую функцию и уменьшают реакцию цитотоксических лимфоцитов. Инициирование М. tuberculosis такого поведения макрофагов дает им возможность ускользать от острого воспаления, усиливая эффекторные ресурсы гранулемы. Задержка воспалительного процесса способствует размножению М. tuberculosis и тем самым способствует развитию инфекционного процесса. Доиммунная гранулема у людей с низким уровнем иммунитета не останавливает туберкулезную инфекцию. Дальнейшие события тесно связаны со специфическим воспалением, в основе которого лежит образование иммунной гранулемы и аллергическая реакция макроорганизма на антигены М. tuberculosis (1, 2, 8).
Таким образом, противотуберкулезная защита определяется наличием высокого уровня неспецифического и/или специфического иммунитета.
В настоящее время для лечения туберкулеза используют различные химиопрепараты и антибиотики - тубазид, салюзид, метазид, изониазид, фтивазид, этамбутол, рифампицин, пиразинамид, стрептомицин и многие другие соединения. Стандартная схема лечения обычного туберкулеза, рекомендованная ВОЗ (схема DOTS), заключается в шестимесячном ежедневном применении стандартного набора лекарств (рифампицин, изониазид, паразинамид, этамбутол, стрептомицин). Однако туберкулез продолжает оставаться актуальнейшей социальной проблемой.
Известны попытки использовать в качестве дополнительных средств лечения туберкулеза различные биологически активные соединения, например, прополисное масло (9).
Бактериальные пробиотические препараты для лечения и профилактики туберкулеза не известны.
Известна композиция, включающая носитель и очищенный компонент липидов клеточной стенки микобактерий, предлагаемая для профилактики и лечения туберкулеза и для повышения неспецифической резистентности при различных аутоиммунных состояниях (11-19).
При этом в качестве очищенного компонента липидов клеточной стенки предлагают использовать миколовые кислоты, обладающие биологической активностью. В качестве носителя возможно использование фармакологически подходящего носителя или адъюванта, в частности масла Marcol 52 или парообразной жидкости. Известная композиция, содержащая очищенный компонент клеточной стенки микобактерий, рассматривается как наиболее близкий аналог заявленного пробиотического бактериального препарата симбионтных коринебактерий (15).
Для получения очищенного компонента липидов клеточной стенки используют микобактерии, продуцирующие миколовые кислоты. Возможно также использование Corynebacteriae, Nocardia и Rodococcus. Композиция включает отдельные компоненты липидов клеточной стенки микобактерий - миколовые кислоты или их смесь, выделенные химическим путем. Так как выделенная субстанция обладает токсичностью, ее подвергают дополнительной очистке. Результаты испытания миколовых кислот на животных подтверждают гипотезу авторов, что миколовые кислоты являются иммуногенами, способными индуцировать продукцию антител к миколовым кислотам. Результаты испытания композиции на людях, больных туберкулезом, свидетельствуют о том, что миколовые кислоты у больных способны вызывать выработку антимиколовых антител. Однако антитела были обнаружены всего у 2 из 58 больных туберкулезом. Антитела являются специфическими. Авторы заключают, что композиция очищенных миколовых кислот, выделенных из М. Tuberculesis H37Rv, обладает иммунорегуляторными и иммуногенными свойствами и может быть использована для профилактики и/или терапии болезней, особенно связанных с микобактериями.
Сведений о практическом использовании вышеуказанных составов для лечения и профилактики туберкулеза нет.
Заявляемое изобретение касается пробиотического бактериального препарата для профилактики и лечения туберкулеза, не обладающего токсичностью и способного индуцировать неспецифический и специфический противотуберкулезный иммунитет, и способа его получения.
Известно, что возбудитель туберкулеза М. tuberculosis относится к роду Mycobacterium семейства Mycobacteriaceae, которые входят в порядок Actinomycetales. К этому порядку принадлежит и род Corynebacterium. Их объединяют общие морфологические, физиологические, генотипические признаки, общая ультраструктура и химический состав клеточных клеток, которые отличаются от других прокариот.
Общность химической структуры основного компонента клеточных стенок Corynebacteriae и Mycobacteriae пептидогликана является наиболее надежным доказательством родственных связей между ними (6, 7).
Близкое родство коринебактерий и микобактерий, идентичность антигенов их клеточных стенок подтверждены иммунологическим ответом на их антигены. Серологическими методами (агглютинацией, преципитацией, электроиммунофорезом) выявлено наличие гомологичных антигенов в поверхностных структурах коринебактерий и микобактерий. Показано, что арабиноманнан и арабиногалактан клеточных стенок коринебактерий и микобактерий ответственны за перекрестные серологические реакции (6, 7).
Вместе с тем корпускулярные антигены клеточных стенок коринебактерий в отличие от корпускулярных антигенов микобактерий туберкулеза безвредны, не токсичны.
Наиболее близким аналогом заявленного способа является способ получения пробиотического бактериального препарата, содержащего структурные компоненты микробной клетки, для профилактики и лечения инфекционных заболеваний животных и человека, а также коррекции микробиоценозов. Для получения препарата используют клеточные стенки симбионтного штамма нетоксигенных коринебактерий Corynebacterium diphtheriae tox- №2 ГИСК им. Л.А. Тарасевича, из суспензии которых выделяют структурный компонент микробной клетки путем дезинтеграции и центрифугирования. Для этого полученный влажный осадок суспендируют в растворе хлорида натрия до концентрации клеток 5 масс.% и проводят дезинтеграцию на ультразвуковой установке в течение 20 мин при частоте 20 кГц и амплитуде 14 мкм при температуре 25-30°С. Суспензию дезинтеграта центрифугируют при 5000g, осадок удаляют, а надосадочную жидкость центрифугируют при 14000g в течение 20 мин. После чего отмывают клеточные стенки от примесей цитоплазмы и питательной среды и ресуспендируют в растворе стабилизатора - глицина (15 мг в 1 мл). В полученном препарате структурным компонентом клеточной стенки является пептидополисахарид, определенный по содержанию пентоз и гексоз по Биалю. Препарат разводят до необходимой концентрации и при необходимости подвергают его стерилизации при температуре 100°С и лиофильному высушиванию (20).
Однако вышеуказанным способом не представляется возможным получить пробиотический препарат для профилактики и лечения туберкулеза, направленный на повышение не только неспецифической резистентности, но и на формирование специфического иммунитета.
Технический результат заявляемых технических решений выражается в получении безопасного и эффективного пробиотического бактериального препарата для профилактики и лечения туберкулеза у человека и животных, представляющего собой корпускулярные антигены (липопептидополисахариды) клеточных стенок коринебактерий, идентичные по химическому составу и антигенным свойствам компонентам клеточных стенок микобактерий, что обеспечивает создание неспецифического и специфического противотуберкулезного иммунитета.
Указанный технический результат достигается тем, что способ получения пробиотического бактериального препарата, содержащего корпускулярные антигены симбионтных коринебактерий для профилактики и лечения туберкулеза, предусматривает наращивание биомассы симбионтного штамма Corynebacterium diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича в жидкой питательной среде, содержащей гидролизат казеина, осаждение микробных клеток центрифугированием, промывание при центрифугировании с получением осадка целых клеток, суспендирование их в растворе хлорида натрия, дезинтеграцию при температуре 25-30°С в течение 15 мин при частоте 20 кГц и амплитуде 14 мкм, последующее центрифугирование при 5000g и удаление оставшихся целых клеток, полученный надосадок центрифугируют при 14000g в течение 20 мин с получением осадка, представляющего собой корпускулярные антигены клеточных стенок коринебактерий, который ресуспендируют в растворе стабилизатора и подвергают дезинтеграции при температуре 25-30°С в течение 5 мин при частоте 20 кГц и амплитуде 14 мкм, полученный препарат разводят до концентрации 225-275 мкг/мл, стерилизуют и высушивают методом лиофилизации для использования в инъекционной форме или форме спрея.
В полученном предлагаемым способом препарате структурными компонентами клеточных стенок являются корпускулярные антигены клеточных стенок симбионтного штамма Corynebacterium diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича, который используют для профилактики и лечения туберкулеза. Препарат подвергают лиофильному высушиванию для получения лекарственных форм для парентерального введения или в форме спрея для местной аппликации ротоглотки.
Традиционно для получения пробиотических бактериальных препаратов используют базовые питательные среды общего назначения на основе гидролизата казеина, рыбного гидролизата с добавлением сыворотки крупного рогатого скота, МПА, мартеновский пептон, мартеновский агар с мясной водой двойной концентрации и т.п. среды.
В качестве стабилизатора из традиционно используемых, предпочтительно, выбран глицин из расчета 15 мг в 1 мл.
Ниже приведен пример получения пробиотического бактериального препарата корпускулярных антигенов симбионтных коринебактерий для профилактики и лечения туберкулеза и примеры, подтверждающие эффективность пробиотического препарата корпускулярных антигенов симбионтных коринебактерий для создания неспецифического и специфического противотуберкулезного иммунитета.
Пример 1.
Для приготовления препарата используют симбионтный пробиотический штамм Corynebacterium diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича. Биомассу наращивают в течение 16 ч при температуре 37°С на плотной питательной среде, содержащей рыбный гидролизат с добавлением сыворотки крупного рогатого скота. Затем культуру смывают жидкой питательной средой, содержащей, г/л: гидролизат казеина - 2,0, пептон - 10,0, глюкозу - 10,0, дрожжевой экстракт - 2,0, натрия хлорид - 6,0. Культивируют в течение 5 ч при температуре 37°С, вносят в ферментер с той же питательной средой и проводят наращивание биомассы при постоянном аэрировании при температуре 37°С в течение 16 ч. Микробные клетки осаждают центрифугированием при 5000g в течение 20 мин и трижды промывают раствором хлорида натрия при центрифугировании в режиме не менее 5000g в течение 20 мин.
Полученный влажный осадок целых клеток симбионтного штамма С.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича взвешивают, суспендируют в забуференном растворе хлорида натрия, рН 7,2, до концентрации клеток 5 масс.%. Затем суспензию целых клеток дезинтегрируют на ультразвуковой установке в течение 15 мин при частоте 20 гГц и амплитуде 14 мкм, при охлаждении льдом или водой до 25-30°С. Полученную суспензию дезинтеграта центрифугируют при 5000g в течение 15 мин с целью отделения неразрушенных клеток и их фрагментов от клеточных стенок. Осадок удаляют, надосадочную жидкость центрифугируют при 14000g в течение 20 мин. Полученный осадок ресуспендируют в растворе хлорида натрия и снова центрифугируют при 14000g в течение 20 мин. Отмывание корпускулярных антигенов клеточных стенок от примесей цитоплазмы и питательной среды повторяют 3 раза. Отмытые корпускулярные антигены ресуспендируют в растворе глицина из расчета 15 мг в 1 мл и повторно дезинтегрируют на ультразвуковой установке в течение 5 мин при частоте 20 кГц и амплитуде 14 мкм при температуре 25-30°С.
В полученном препарате определяют концентрацию биологически активного липопептидополисахарида по содержанию пентоз и гексоз. Затем препарат разводят до концентрации 250±25 мкг/мл, подвергают стерилизации при температуре 100°С и лиофильно высушивают для использования в инъекционной форме или форме спрея. Количество активного начала в 1 дозе конечного препарата зависит от лекарственной формы и возраста человека или животного.
Пример 2. Активность фагоцитирующих клеток перитониального экссудата мышей, иммунизированных препаратом корпускулярных антигенов клеточной стенки.
Мышей подкожно иммунизируют препаратом корпускулярных антигенов С.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича в дозе 200 мкг. Через две недели опытным животным в брюшную полость вводят живую культуру возбудителей дифтерии (C.diptheriae tox+). Эффективность фагоцитоза оценивают в перитониальной пробе по И.Ф.Здродовскому. Пробу берут через 3 часа после заражения. Основными показателями эффективности фагоцитоза были: количество свободных клеток С.diptheriae tox+, процент фагоцитирующих клеток в пробе перитониального экссудата (в 30 полях зрения), а также завершенность фагоцитоза. Результаты исследования приведены в таблице 1.
Из таблицы видно, что через 3 ч после заражения фагоцитирующие клетки контрольных животных концентрируются в очаге заражения, количество свободных бактерий С.diptheriae tox+ достигает 300, они продолжают размножаться, фагоцитирующие клетки составляют 57,9%. Разрушения бактериальных клеток внутри макрофагов не происходит.
У мышей, иммунизированных корпускулярными антигенами клеточных стенок симбионтного штамма С.diptheriae tox- №2 ГИСК им. Л.А.Тарасевича, выявлена повышенная активность фагоцитирующих клеток, процент макрофагов, завершающих фагоцитоз, составляет всего 11,8%, что подтверждается полным отсутствием свободных клеток C.diptheriae tox+ в пробе экссудата. Макрофаги представляют собой гигантские клетки с хорошо дифференцированным ядром, цитоплазмой, большим количеством свободных лизосом.
Таким образом, после иммунизации животных корпускулярными антигенами симбионтного штамма С.diptheriae tox- №2 ГИСК им. Л.А.Тарасевича в зоне контакта «иммунных» макрофагов с С.diptheriae tox+ они быстро активизируются, адсорбируют, поглощают и утилизируют токсичные C.diptheriae tox+.
Пример 3. Повышение активности нейтрофилов под влиянием корпускулярных антигенов симбионтного штамма С.diptheriae tox- №2 ГИСК им. Л.А.Тарасевича.
Роль нейтрофилов совместно с макрофагами заключается в разрушении целых клеток микроорганизмов и переработке бактериальных антигенов в форму, пригодную для восприятия их иммунокомпетентными клетками. Неспецифические реакции нейтрофилов и макрофагов являются предфазой создания специфического иммунитета.
В тесте НСТ показана активация кислородзависимого метаболизма нейтрофилов под влиянием корпускулярных антигенов клеточных стенок симбионтного штамма С.diptheriae tox- №2 ГИСК им. Л.А.Тарасевича. Антигены активно взаимодействуют с нейтрофилами человека, подвергаясь опсонизации нормальными антителами человека IgG-изотипа (антитела выделены из сыворотки здоровых людей).
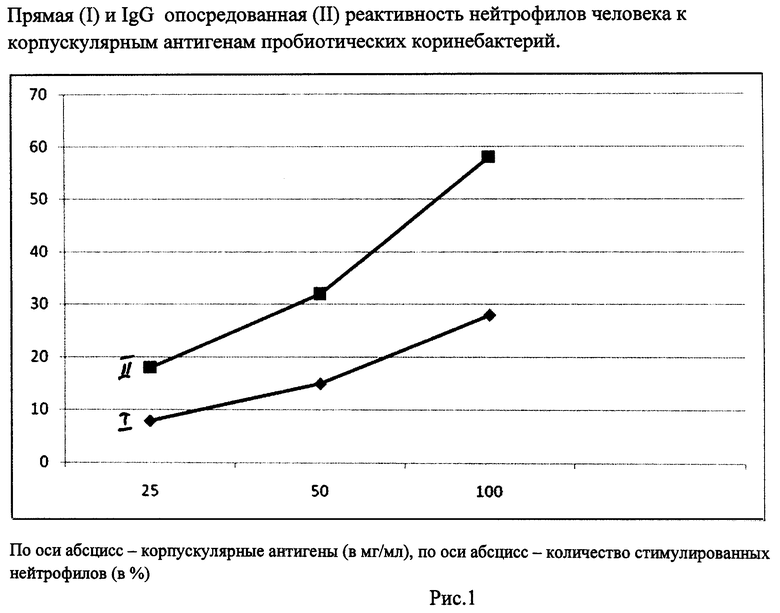
Активация нейтрофилов в прямой (без опсонизации IgG) реакции взаимодействия с антигенами клеточных стенок симбионтного штамма С.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича свидетельствует о функциональных возможностях антигенов клеточных стенок С.diptheriae tox_ в активации фагоцитирующих клеток (рис.1,2).
Таким образом, активация нейтрофилов корпускулярными антигенами симбионтного штамма C.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича приводит к повышению неспецифической резистентности макроорганизма.
Рис.1. Прямая (I) и IgG опосредованная (II) реактивность нейтрофилов человека к антигенам клеточных стенок штамма С.diphtheriae tox - №2 ГИСК им. Л.А.Тарасевича.
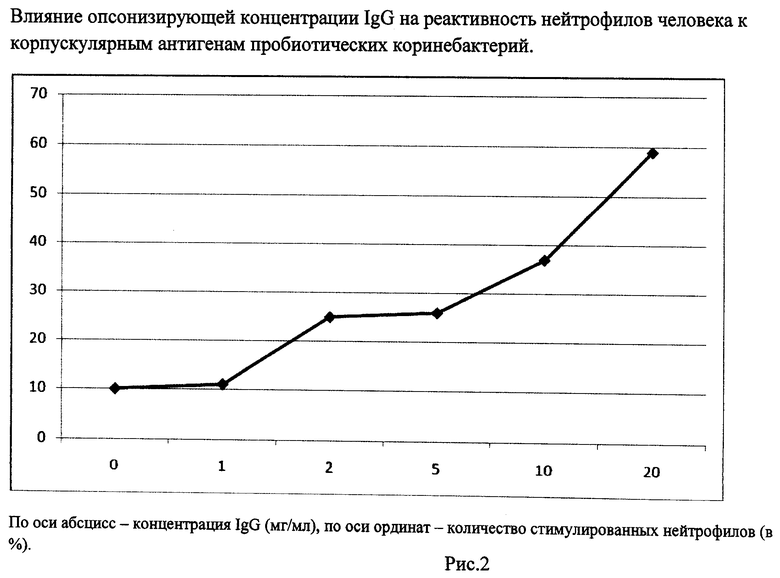
Рис.2. Влияние опсонизирующей концентрации IgG на реактивность нейтрофилов человека к корпускулярным антигенам симбионтного штамма C.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича.
По оси абсцисс - концентрация IgG (мг/мл), по оси ординат - количество стимулированных нейтрофилов (в %).
Пример 3.
Протективные свойства корпускулярных антигенов симбионтного штамма С.diphtheriae tox - №2 ГИСК им. Л.А.Тарасевича.
Две группы беспородных белых мышей иммунизируют корпускулярными антигенами симбионтных коринебактерий в дозах 200 мкг и 400 мкг. В контрольную группу входят животные, иммунизированные вакциной БЦЖ. Через 48 суток мышам обеих опытных групп и мышам контрольной группы вводят вирулентный штамм возбудителя туберкулеза в дозах 10-3, 10-5, 10-6 микробных клеток. В таблице 2 представлены данные по влиянию препарата на устойчивость беспородных белых мышей на заражение их вирулентным штаммом возбудителя туберкулеза.
Как видно, пробиотический бактериальный препарат корпускулярных антигенов клеточных стенок (липопептидополисахаридов) симбионтного штамма С.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича повышает резистентность мышей к туберкулезной инфекции. Это проявляется в выживаемости животных при заражении их вирулентным штаммом M.tuberculosis.
Таким образом, впервые предложен пробиотический бактериальный препарат для профилактики и лечения туберкулеза, направленный на повышение неспецифической резистентности, конкретно на активацию макрофагального звена клеточного иммунитета, а также на формирование специфического иммунитета.
Препарат представляет собой корпускулярные антигены (липопептидополисахариды) клеточных стенок симбионтного штамма С.diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича, идентичные по химическому составу и антигенным свойствам компонентам клеточных стенок микобактерий, что обеспечивает его нетоксичность, безопасность и эффективность. Противотуберкулезная защита осуществляется за счет создания напряженного неспецифического и специфического иммунитета. Способ получения препарата технологичен, безвреден. Препарат пригоден для использования в различных лекарственных формах для профилактики и лечения туберкулеза у людей и животных.


| название | год | авторы | номер документа |
|---|---|---|---|
| СИМБИОНТНЫЙ ШТАММ Corynebacteriae diphtheriae tox - № 108, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ИММУНОМОДУЛЯТОРА, СОЗДАЮЩЕГО НЕСПЕЦИФИЧЕСКУЮ РЕЗИСТЕНТНОСТЬ ПРОТИВ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ БАКТЕРИАЛЬНОЙ И ВИРУСНОЙ ПРИРОДЫ У СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 2011 |
|
RU2477751C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО БАКТЕРИАЛЬНОГО ПРЕПАРАТА, СОДЕРЖАЩЕГО СТРУКТУРНЫЕ КОМПОНЕНТЫ МИКРОБНОЙ КЛЕТКИ | 2002 |
|
RU2230113C1 |
| Метабиотический препарат-иммуномодулятор, содержащий клеточные стенки симбионтных коринебактерий, для укрепления врожденного иммунитета и способ его получения | 2017 |
|
RU2648156C1 |
| СПОСОБ ПОВЫШЕНИЯ НЕСПЕЦИФИЧЕСКОЙ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА И СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ ПОВЫШЕНИЯ НЕСПЕЦИФИЧЕСКОЙ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА | 1992 |
|
RU2019181C1 |
| Средство для стимуляции регенерации ткани печени при парентеральном введении и способ стимуляции регенерации ткани печени на его основе | 2017 |
|
RU2643591C1 |
| ПОЛИАНТИГЕННАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ И ВСПОМОГАТЕЛЬНОГО ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2019 |
|
RU2724896C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕННОГО ПРЕПАРАТА ИЗ MYCOBACTERIUM TUBERCULOSIS С РАСШИРЕННЫМ СПЕКТРОМ СЕРОПОЗИТИВНЫХ ФРАКЦИЙ В РЕАКЦИИ ИММУНОБЛОТИНГА | 2010 |
|
RU2431675C1 |
| ВАКЦИНА ПРОТИВ ТУБЕРКУЛЕЗА | 1999 |
|
RU2153354C1 |
| СПОСОБ СКРИНИНГА ПРОБИОТИЧЕСКИХ ПРЕПАРАТОВ ПРОТИВ НОКАРДИОФОРМНЫХ АКТИНОМИЦЕТОВ | 2009 |
|
RU2448162C2 |
| Рекомбинантный штамм Mycobacterium bovis rBCG-1 на основе вакцинного штамма Mycobacterium bovis BCG strain Russia 368 | 2022 |
|
RU2807732C1 |
Для получения пробиотического препарата наращивают биомассу симбионтного штамма Corynebacterium diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича в жидкой питательной среде, осаждают микробные клетки центрифугированием, промывают при центрифугировании с получением осадков целых клеток, суспендируют их в растворе хлорида натрия. Затем клетки дезинтегрируют при температуре 25-30°С в течение 15 мин при частоте 20 кГц и амплитуде 14 мкм, дезинтеграт центрифугируют при 5000g и удаляют оставшиеся целые клетки. Полученный надосадок центрифугируют при 14000g в течение 20 мин с получением осадка корпускулярных антигенов клеточных стенок коринебактерий липопептидополисахаридной природы, который ресуспендируют в растворе стабилизатора и подвергают дезинтеграции при температуре 25-30°С в течение 5 мин при частоте 20 кГц и амплитуде 14 мкм. Затем препарат разводят до концентрации 225-275 мкг/мл, стерилизуют и высушивают методом лиофилизации. Использование изобретения позволяет получить безопасный и эффективный препарат корпускулярных антигенов, обеспечивающий создание специфического и неспецифического иммунитета против туберкулеза. 2 н.п. ф-лы, 2 ил., 2 табл., 3 пр.
1. Способ получения пробиотического препарата корпускулярных антигенов коринебактерий липопептидополисахаридной природы для профилактики и лечения туберкулеза, характеризующийся тем, что наращивают биомассу симбионтного штамма Corynebacterium diphtheriae tox- №2 ГИСК им. Л.А.Тарасевича в жидкой питательной среде, содержащей гидролизат казеина, осаждают полученные микробные клетки центрифугированием, промывают осадок целых клеток при центрифугировании, далее клетки суспендируют в растворе хлорида натрия, дезинтегрируют при температуре 25-30°С в течение 15 мин при частоте 20 кГц и амплитуде 14 мкм, повторно центрифугируют при 5000g и удаляют оставшиеся целые клетки, полученный надосадок центрифугируют при 14000g в течение 20 мин и получают осадок, содержащий корпускулярные антигены клеточных стенок коринебактерий, осадок ресуспендируют в растворе стабилизатора и подвергают дезинтеграции при температуре 25-30°С в течение 5 мин при частоте 20 кГц и амплитуде 14 мкм, полученный дезинтеграт клеточных стенок разводят до концентрации 225-275 мкг/мл, стерилизуют и высушивают целевой продукт методом лиофилизации.
2. Пробиотический бактериальный препарат для профилактики и лечения туберкулеза, содержащий корпускулярные антигены коринебактерий липопептидополисахаридной природы, полученный способом по п.1.
| СПОСОБ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО БАКТЕРИАЛЬНОГО ПРЕПАРАТА, СОДЕРЖАЩЕГО СТРУКТУРНЫЕ КОМПОНЕНТЫ МИКРОБНОЙ КЛЕТКИ | 2002 |
|
RU2230113C1 |
| Устройство для упаковывания в рукав предметов | 1987 |
|
SU1465354A1 |
| RU 2008142140 A, 27.04.2010 | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| US 6433013 B1, 13.08.2002. | |||
Авторы
Даты
2012-12-10—Публикация
2011-06-23—Подача