Изобретение относится к способу получения новых физиологически активных соединений, а именно к способу получения конъюгированных вакцин против холеры. Изобретение наиболее эффективно может быть использовано в медицине для профилактической иммунизации против холеры.
Известны способы получения живых, убитых, химических вакцин [1-4]. Недостатком живых и убитых вакцин является их высокая реактогенность, кроме того, для живых нельзя исключить возможность реверсии холерогенности. Генно-инженерные вакцины характеризуются непродолжительностью и недостаточной напряженностью иммунитета [5].
Современные представления об особенностях иммунного ответа организма на отдельные протективные антигены холерного вибриона служат основой для конструирования вакцинных препаратов. Вакцины должны способствовать формированию антибактериального и антитоксического иммунитета, направленного как против колонизации возбудителей в кишечнике, так и против действия его токсического фактора, играющего основную роль в патогенезе холеры [6].
Выпускаемые в СССР убитая корпускулярная холерная вакцина и холерная вакцина (холероген-анатоксин+О-антиген) способны стимулировать: первая - антимикробный, вторая - антимикробный и антитоксический иммунитет при парентеральном введении [7,8]. Для поддержания напряженного иммунитета необходима ревакцинация через шесть месяцев. При этом отмечено развитие сенсибилизации, вторичных иммунодефицитов у привитых вследствие многократной вакцинации.
Использование в качестве отдельных иммунизирующих агентов анатоксина, B-субъединицы холерного энтеротоксина оказалось малоэффективным вследствие стимуляции только антитоксического иммунитета [1,2].
Наиболее близкой по технической сущности к заявляемому объекту является оральная комбинированная цельноклеточная вакцина с очищенной B-субъединицей холерного токсина.
Недостатками указанной вакцины являются невысокий защитный эффект наряду с высокой реактогенностью [9]. Применение оральных вакцин требует многократных ревакцинаций.
Целью изобретения является разработка способа получения вакцины против холеры, обладающей высокой эффективностью и безвредностью.
Это достигается конъюгацией антигена холерного вибриона - B-субъединицы холерного токсина на полимере-носителе - сополимере N-окиси этиленпиперазина и N-ацилгидразида этиленпиперазиний бромида (полиоксидония) азидным методом при соотношении носитель:антиген 3-5:1.
Принципиально новым в предлагаемом изобретении является создание на основе B-субъединицы холерного токсина и полимерного иммуноадъювантного носителя - полиоксидония высокоэффективной вакцины. При этом B-субъединица холерного токсина ответственна за связывание с клеточными рецепторами слизистой оболочки кишечника, то есть способствует формированию антитоксического иммунитета. Конъюгат стимулирует антительный ответ против антигенов, снижает аллергические и другие побочные реакции.
Процесс конъюгации проводят при весовом соотношении полиоксидония к B-субъединице 3-5:1. Увеличение соотношения приводит к снижению активности B-субъединицы, уменьшение - к снижению стабильности продукта. Предложенный способ конъюгации позволяет полностью избежать межмолекулярных и внутримолекулярных сшивок и получить конъюгаты с высоким выходом.
Выделение конъюгатов осуществляют хроматографическим методом, анализ проводят методами электрофореза в ПААГ, флуоресцентной спектроскопии и малоуглового лазерного светорассеяния.
Предложенный способ позволяет получать высокоиммуногенные конъюгаты, обладающие выраженными протективными свойствами, безвредные для организма.
Предложенная вакцина может быть использована как самостоятельно, так и в комплексе с конъюгатами деацилированных липополисахаридов (д-ЛПС) сероваров Инаба и Огава с полиоксидонием. Вакцинирующая смесь вышеуказанных конъюгатов, содержащая в своем составе антигены, принимающие участие в формировании антибактериального и антитоксического иммунитета, при однократном введении дает потенциирующий эффект, что ведет к увеличению протективности и иммунологической эффективности.
Испытания вакцинирующих соединений, полученных указанным способом, проведены на мышах и кроликах.
Проверка заявленного технического решения на соответствие его критерию "существенные отличия" показала, что ни в патентной, ни в научно-технической литературе не выявлено совокупности признаков, указанных в формуле изобретения.
Ниже приводятся конкретные примеры осуществления способа получения и анализа физиологических свойств целевого продукта.
П р и м е р 1. Получение конъюгата полиоксидония с B-субъединицей холерного энтероксина (конъюгат 1, соотношение полимер:белок - 3:1).
100 мг сополимера N-окиси этиленпиперазина и N-ацилгидразида этиленпиперазиний бромида [10] (мол.м. 40 КДа, 1-10 моль аминогрупп) растворяют в 4 мл 1 н. HCl. Раствор охлаждают до 2оС на ледяной бане. При охлаждении и перемешивании добавляют 1,15 мл 3%-ного раствора нитрита натрия. Через 15 мин доводят pH раствора до 8,5 добавлением 2 н. NaOH. Раствор 33 мг белка (B-субъединица холерного токсина), выделяемого согласно [11] в 10 мл 0,05 М фосфатного буфера pH 8,5, добавляют к раствору активированного сополимера. Поддерживают pH реакционной смеси добавлением 2 н. NaOH. Реакция продолжается в течение 12 ч при охлаждении (2оС) и перемешивании. Для выделения и очистки конъюгата реакционную смесь наносят на колонку (2,6 ˙ 90), заполненную ультрагелем АсА-34. В качестве элюента используют 0,05 М фосфатный буфер pH 7,5, содержащий 0,05 М NaCl. Выход конъюгата контролируют с помощью проточного спектрофотометра при 226 нм. Выделяют фракцию, выходящую в объеме колонки, содержащую белок и полимер (контроль фракций осуществляют методом флуоресцентной спектроскопии). Для контроля в идентичных условиях хроматографируют смесь нативной В-субъединицы и полиоксидония. Определение содержания белка и анализ конъюгата проводят методами флуоресцентной спектроскопии, электрофореза в ПААГ, малоуглового светорассеяния. В 1 мг препарата содержится 0,3 мг B-субъединицы холерного токсина.
Выход: 120 мг (90,2%).
П р и м е р 2. Получение конъюгата полиоксидония с B-субъединицей холерного энтеротоксина (конъюгат 2) проводят аналогично описанному в примере 1, соотношение полимер:белок в реакционной смеси составляет 5:1. В 1 мг конъюгата 2 содержится 0,15 мг белка. Выход: 90%.
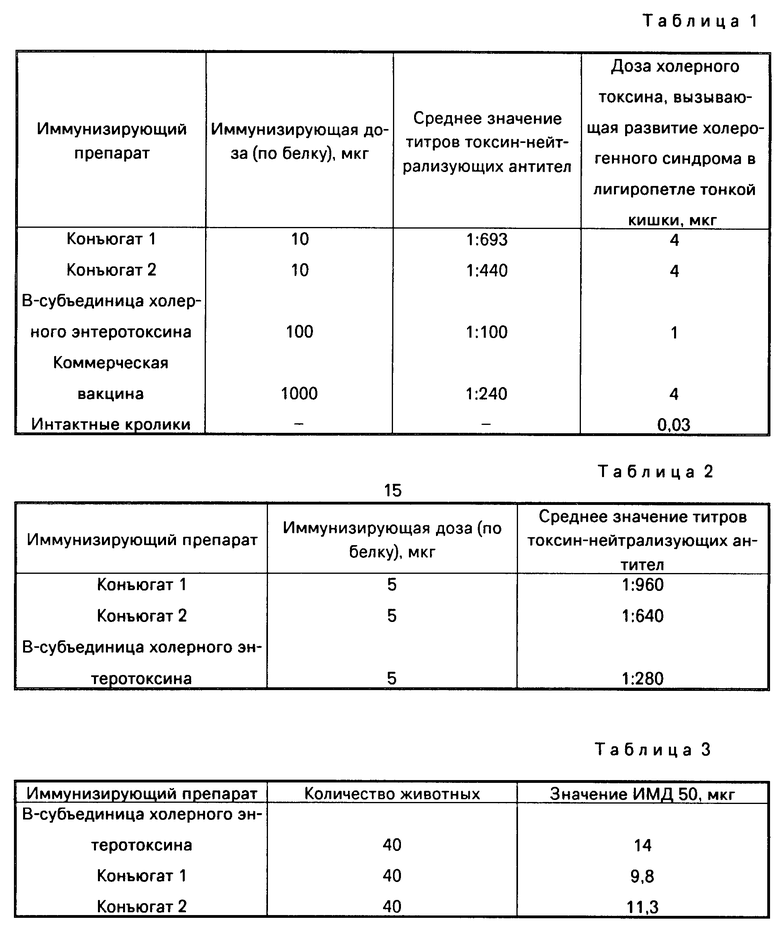
П р и м е р 3. Иммунологическую эффективность проверяют на кроликах (табл.1) и нелинейных белых мышах (табл.2) в условиях однократной подкожной иммунизации. В качестве показателя эффективности изучаемого препарата использовали средние значения титров токсиннейтрализующих антител, выявленных в системе реакций РПГА и РТПГА с холерным эритроцитарным диагностикумом и во внутрикожной пробе Крейга.
Через 21 день после иммунизации определяют токсиннейтрализующие антитела в сыворотке крови и напряженность местного антитоксического иммунитета по степени подавления холерогенного синдрома в лигированных петлях тонкой кишки иммунизированных кроликов при внутрикишечном введении возрастающих доз холерного энтеротоксина.
Проведено сравнительное изучение иммунологической эффективности коммерческой вакцины (холероген-анатоксин+O-антиген), B-субъединицы холерного токсина и конъюгированной вакцины. Данные приведены в табл.1, 2.
Из табл. 1 и 2 видно, что конъюгаты 1 и 2 обладают выраженным иммунным эффектом, стимулируют формирование антитоксического иммунитета, о чем свидетельствует накопление токсиннейтрализующих антител в сыворотке крови животных. Однократное введение этих препаратов способствует формированию напряженного местного антитоксического иммунитета в слизистой тонкого кишечника. Следует подчеркнуть, что конъюгаты проявляют высокую специфическую активность в дозах, в 100 раз меньших, чем коммерческая вакцина (холероген-анатоксин+O-антиген).
П р и м е р 4. Испытания иммуногенных свойств в тесте активной защиты мышей проводили у конъюгатов 1 и 2 и исходной B-субъединицы холерного энтеротоксина (табл. 3). Препараты вводят внутрибрюшинно однократно в дозах 0,25 мкг; 1,3 мкг; 6,5 мкг; 32,5 мкг по белку в объеме 0,5 мл по 10 мышей на дозу. Через 13+1 дней иммунизированных животных заражают внутрибрюшинно взвесью 4+1-часовой агаровой культурой вибрионов эльтор серовара Огава в дозе 500 ЛД 50, суспендированной в 5% муцине. Степень протекции оценивают по величине половинной иммунизирующей дозы (ИМД 50), которую определяли по методу Кербера в модификации Ашмарина. Определение ИМД 50 позволяет сопоставить активность препарата с содержанием в нем белка.
Результаты представлены в табл.3.
П р и м е р 5. Изучение безопасности вакцины проводилось в соответствии с требованиями Комитета вакцин и сывороток и включало оценку острой токсичности (при различных путях введения) и хронической токсичности с оценкой состояния периферической крови, функции печени и почек, состояния сердечно-сосудистой и центральной нервной систем, аллергической активности.
Установлено, что заявляемая вакцина не обладает местным раздражающим действием, не вызывает гибели мышей при введении им 1 человеко-дозы. В исследуемых органах и показателях крови закономерных изменений не обнаружено. На модели индукции аллергии замедленного типа (анафилактического шока у морских свинок) не выявлено аллергизирующего действия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ ХОЛЕРЫ | 1991 |
|
RU2021817C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОРАЛЬНОЙ ХИМИЧЕСКОЙ ВАКЦИНЫ | 1993 |
|
RU2076734C1 |
| СПОСОБ ЗАЩИТЫ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ ОТ КОЛИБАКТЕРИОЗА И САЛЬМОНЕЛЛЕЗА | 1988 |
|
RU2020958C1 |
| ОРАЛЬНАЯ ХИМИЧЕСКАЯ ВАКЦИНА ПРОТИВ ХОЛЕРЫ | 2000 |
|
RU2159128C1 |
| ШТАММ БАКТЕРИЙ VIBRIO CHOLERAE KM 200 - ПРОДУЦЕНТ ХОЛЕРНОГО ТОКСИНА И ТОКСИН - КОРЕГУЛИРУЕМЫХ ПИЛЕЙ АДГЕЗИИ | 2001 |
|
RU2193598C1 |
| АВИРУЛЕНТНЫЙ ШТАММ VIBRIO CHOLERAE НЕ-01 СЕРОГРУППЫ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ ШТАММА (ВАРИАНТЫ), ВАКЦИНА | 1994 |
|
RU2140981C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХОЛЕРНОГО ТОКСИНА ДЛЯ КОНТРОЛЯ ПРОИЗВОДСТВА ХОЛЕРНОЙ ХИМИЧЕСКОЙ ВАКЦИНЫ | 2022 |
|
RU2799574C1 |
| ШТАММ БАКТЕРИЙ VIBRIO CHOLERAE КМ206 КЛАССИЧЕСКОГО БИОВАРА СЕРОВАРА ОГАВА - ПРОДУЦЕНТ ПРОТЕКТИВНЫХ АНТИГЕНОВ | 2002 |
|
RU2222594C1 |
| Способ повышения эффективности противохолерной вакцинации для профилактики на экспериментальных животных | 2018 |
|
RU2691411C1 |
| ШТАММ БАКТЕРИЙ VIBRIO CHOLERAE КМ207 КЛАССИЧЕСКОГО БИОВАРА СЕРОВАРА ИНАБА - ПРОДУЦЕНТ ПРОТЕКТИВНЫХ АНТИГЕНОВ | 2002 |
|
RU2222595C1 |
Использование: в медицине для профилактической иммунизации против холеры. Сущность изобретения: проводят конъюгацию В-субъединицы холерного токсина с сополимером N-окиси этиленпиперазина и N-ацилгидразида этиленпиперазиний бромида с мол.м. 40 кДа азидным методом при весовом соотношении носитель - антиген 3 - 5 : 1. Предложенный способ позволяет получить безвредную, высокоиммуногенную вакцину, не вызывающую аллергического действия на организм. 3 табл.
СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ ХОЛЕРЫ, предусматривающий приготовление В-субъединицы холерного токсина, отличающийся тем, что В-субъединицу конъюгируют с носителем-сополимером N-оксида этиленпиперазина и N-ацилгидразида этиленпиперазиний бромида с ММ 40КД, причем конъюгирование проводят азидным методом при массовом соотношении носитель : антиген 3 - 5 : 1.
| J.Ciznar, N.Hussain, C.R.Ahsam, B.A.Kay et al Vaccine, v.7 | |||
| Говорящий кинематограф | 1920 |
|
SU111A1 |
Авторы
Даты
1994-10-30—Публикация
1991-06-05—Подача