Изобретение относится к новым физиологически активным соединениям, а именно к способу получения конъюгированных вакцин против холеры. Изобретение наиболее эффективно может быть иcпользовано в медицине для профилактичеcкой иммунизации против холеры.
Известны способы получения живых, убитых, химических вакцин [1-4].
Недостатком живых и убитых вакцин является их высокая реактогенность, кроме того, для живых нельзя исключить возможность реверсии холерогенности. Генно-инженерные вакцины характеризуются непродолжительностью и недостаточной напряженностью иммунитета [5].
Современные представления об особенностях иммунного ответа организма на отдельные протективные антигены холерного вибриона служат основой для конструирования вакцинных препаратов. Вакцины должны способствовать формированию антибактериального и антитоксического иммунитета, направленного как против колонизации возбудителей в кишечнике, так и против действия его токсического фактора, играющего основную роль в патогенезе холеры [6].
Выпускаемые в СССР корпускулярная холерная вакцина и холерная вакцина (холероген-анатоксин + O-антиген) способны стимулировать: первая - антимикробный, вторая - антимикробный и антитоксический иммунитет при парентеральном введении [7,8]. Для поддержания напряженного иммунитета необходима ревакцинация через шесть месяцев. При этом отмечено развитие сенсибилизации, вторичных иммунодефицитов у привитых вследствие многократной вакцинации.
Использование в качестве отдельных иммунизирующих агентов анатоксина, B-субъединицы холерного энтеротоксина оказалось малоэффективным вследствие стимуляции только антитоксического иммунитета.
Наиболее близкой по технической сущности к заявляемому объекту является конъюгированная бивалентная вакцина для парентерального введения на основе деацилированных липополисахаридов и белка наружной мембраны холерного вибриона.
Недостатком указанной вакцины и способа ее получения является низкая иммуногенность, а использование в качестве высокомолекулярного носителя белка вызывает при введении в организм нежелательные побочные эффекты, в частности аллергические реакции [9].
Целью изобретения является разработка способа получения вакцины против холеры, обладающей высокой эффективностью и безвредностью.
Это достигается конъюгацией антигенов холерного вибриона - деацилированных липополисахаридов (д-ЛПС) сероваров - Инаба или Огава на полимере-носителе - сополимере N-окиси этиленпиперазина и N-ацилгидразида этиленпиперазиний бромида (полиоксидония) с 2,4,6-трихлор-S-триазином в качестве связующего агента при весовом соотношении носитель - антиген 4-7:1.
Принципиально новым в предлагаемом изобретении является создание на основе д-ЛПС сероваров Инаба и Огава и полимерного иммуноадъювантного носителя - полиоксидония высокоэффективной вакцины. При этом д-ЛПС, являясь основным соматическим антигеном, отвечает за создание антимикробного иммунитета при вакцинации. Конъюгат стимулирует антительный ответ против антигенов, снижает аллергические и другие побочные реакции.
Процесс конъюгации проводят при весовом соотношении полиоксидония к д-ЛПС 4-7:1. Увеличение соотношения приводит к снижению активности д-липополисахарида, а уменьшение - к понижению стабильности продукта. Предложенный способ конъюгации позволяет полностью избежать межмолекулярных и внутримолекулярных сшивок и получить конъюгаты с высоким выходом.
Выделение конъюгатов осуществляют хроматографическим методом, анализ продуктов проводят методом ИК-спектроскопии, содержание углеводов в образце определяют по методу Дюбуа с фенол-серной кислотой.
Предложенный способ позволяет получать высокоиммуногенные конъюгаты, обладающие выраженными протективными свойствами, безвредные для организма.
Предложенные вакцины могут быть использованы как самостоятельно, так и в комплексе с конъюгатами B-субъединицы холерного токсина с полиоксидонием. Вакцинирующая смесь вышеуказанных конъюгатов, содержащая в своем составе антигены, принимающие участие в формировании антибактериального и антитоксического иммунитета, при однократном введении дает потенциирующий эффект, что ведет к увеличению протективности и иммунологической эффективности.
Испытания вакцинирующих соединений, полученных указанным способом, проведены на мышах.
Проверка заявленного технического решения на соответствие его критерию "существенные отличия" показала, что ни в патентной, ни в научно-технической литературе не выявлено совокупности признаков, указанных в формуле изобретения.
Ниже приводятся конкретные примеры осуществления способа получения и анализа физиологических свойств целевого продукта.
П р и м е р 1. Получение конъюгата полиоксидония с д-ЛПС серовара Инаба (конъюгат 1).
Деацилированные липополисахариды сероваров Инаба и Огава выделяют по методике [11]. Д-ЛПС имели следующие характеристики: мол. м. 1000 кДа содержание примесей белков и нуклеиновых кислот - 1,5-3% и 0,7-1,5% для сероваров Огава и Инаба соответственно.
100 мг д-ЛПС серовара Инаба растворяют в 5 мл 0,05 М натрий-фосфатного буфера pH 8,4 и добавляют 12 мг 2,4,6-трихлор-s-триазина в 2,5 мл диметилформамида. Активацию проводят при температуре 4оС при перемешивании в течение 0,5 ч при pH 8,4-8,6. К раствору активированного д-ЛПС добавляют 400 мг полиоксидония (мол. м. 40 кДа, 1,10 моль аминогрупп) [10] в 30 мл воды. Реакционную смесь перемешивают 24 ч при температуре 20оС, поддерживая pH 9,4-9,6 (0,1 н. NaOH). После этого pH смеси доводят до 10,6-11,0 и перемешивают еще 2 ч. По окончании реакции pH доводят до нейтрального. Для выделения и очистки конъюгата реакционную смесь наносят на хроматографическую колонку (6 ×120). В качестве носителя используют ультрагель АсА 34. Элюцию проводят 0,05 М фосфатным буфером pH 0,7 с ионной силой 1,0 М NaCl. Выход конъюгатсодержащей фракции контролируют с помощью проточного спектрофотометра при длине волны 226 нм. Выделяют фракцию, выходящую в объеме колонки и содержащую как полимер, так и углеводы (наличие углеводов определяют титрованием отдельных выходящих с колонки фракций фенолсерной кислотой). Раствор диализуют через полупроницаемую мембрану против 0,15 М NaCl в течение 24 ч. Содержание углеводов определяют методом Дюбуа с фенолсерной кислотой. Анализ конъюгата осуществляют методом ИК-спектроскопии. Выход 85%. Содержание углеводов 0,2 мг в 1 мг препарата (конъюгат 1).
П р и м е р 2. Получение конъюгата полиоксидония с д-ЛПС серовара Огава (конъюгат 2) проводят аналогично описанному в примере 1. Выход конъюгата 2 65%, содержание углеводов 0,12 мг в 1 мг препарата.
П р и м е р 3. Получение конъюгата полиоксидония с д-ЛПС серовара Инаба (конъюгат 3) проводят аналогично описанному в примере 1, соотношение полимер-углевод в реакционной смеси составляет 7:1. В 1 мг препарата конъюгата 3 содержится 0,1 мг углеводов. Выход 79%, содержание углеводов 0,15 мг в 1 мг препарата.
П р и м е р 4. Получение конъюгата полиоксидония с д-ЛПС серовара Огава (конъюгат 4) проводят аналогично описанному в примере 3. Выход конъюгата 4 56%, содержание углеводов 0,06 мг в 1 мг препарата.
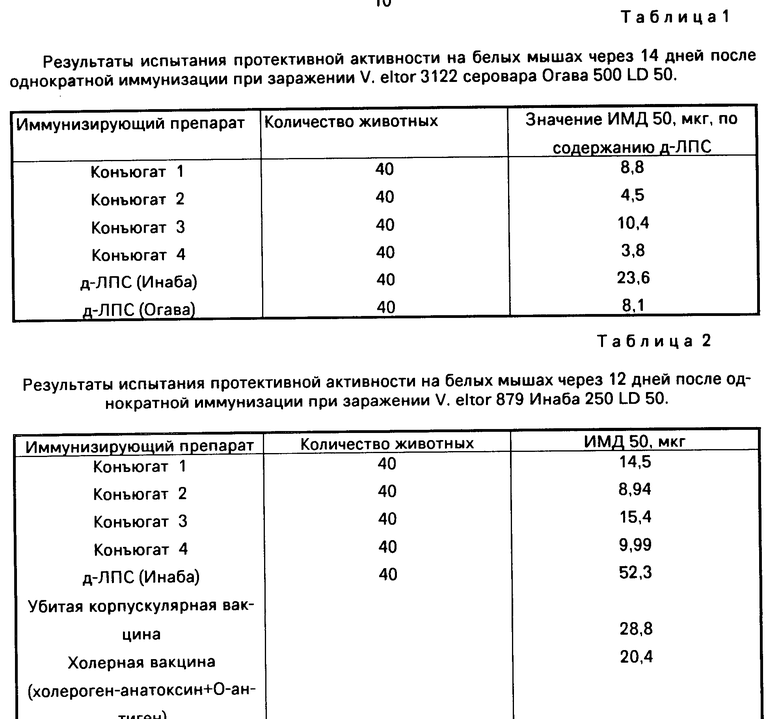
П р и м е р 5. Иммуногенную активность испытуемых препаратов определяют в тесте активной защиты. Нелинейных белых мышей весом 10-12 г вакцинировали однократно внутрибрюшинно в дозе 0,4 мкг; 2 мкг; 10 мкг; 50 мкг по д-ЛПС в объеме 0,5 мл по 10 мышей на дозу. Через 10-14 дней их подвергают внутрибрюшинному заражению вирулентными штаммами холерного эльтор вибриона обоих сероваров в дозах 78-500 LD 50. Через 3 сут. проводили учет защитного действия препаратов со статистической обработкой материала и определением половинной иммунизирующей дозы (ИМД 50). Определение ИМД 50 позволяет сопоставить активность препарата с содержанием в нем углеводов. В каждом опыте кроме обычного контроля группы чистых животных, зараженных вместе с опытными культурами вирулентных штаммов, применяли контроль - группы животных, вакцинированных убитой корпускулярной холерной вакциной и холероген-анатоксин + О-антиген. Результаты приведены в табл.1-2.
В табл.3 приведены результаты испытаний протективной активности смесей конъюгатов на основе сероваров Инаба и Огава. Соотношение компонентов 1:1 (по углеводам). Препараты вводились в виде смеси конъюгатов д-ЛПС различных сероваров.
Как видно из табл.1-3, конъюгаты 1-4 и их смеси обладают выраженными иммунными свойствами, определяемыми в тесте активной защиты мышей. Протективная активность конъюгированной вакцины в 1,5-2 раза, а смесей конъюгатов - почти в 10 раз выше протективности применяемых в СССP коммерческих вакцин (убитая корпускулярная вакцина и холероген-анатоксин + О-антиген).
П р и м е р 6. Безвредность вакцины определяли на нелинейных белых мышах, а также на гибридах (CBA C57B16)F1, мышах линии CBA весом 17-18 г. Каждый испытуемый образец аводили подкожно 5 животным в дозе 25+10 мкг деацилированного липополисахарида, конъюгированного с полиоксидонием в объеме 0,5 мл. Наблюдение проводили в течение 7 дней. Все животные по истечении 7 дней были живы. Проявления интоксикации, потеря веса отсутствовали. Через 2 сут. с момента введения вакцины регистрировалось увеличение веса животных на 8-10 г в группе.
На модели индукции аллергии замедленного типа (анафилактического шока у морских свинок) не выявлено аллергизирующего действия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ ХОЛЕРЫ | 1991 |
|
RU2021816C1 |
| Способ повышения эффективности противохолерной вакцинации для профилактики на экспериментальных животных | 2018 |
|
RU2691411C1 |
| ОРАЛЬНАЯ ХИМИЧЕСКАЯ ВАКЦИНА ПРОТИВ ХОЛЕРЫ | 2000 |
|
RU2159128C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОРАЛЬНОЙ ХИМИЧЕСКОЙ ВАКЦИНЫ | 1993 |
|
RU2076734C1 |
| АВИРУЛЕНТНЫЙ ШТАММ БАКТЕРИЙ Vibrio cholerae КМ 262 БИОВАРА ЭЛЬТОР СЕРОВАРА ОГАВА - ПРОДУЦЕНТ ПРОТЕКТИВНОГО О1 АНТИГЕНА | 2010 |
|
RU2425868C1 |
| СПОСОБ ПОЛУЧЕНИЯ O-АНТИГЕНА ХОЛЕРНОГО ОЧИЩЕННОГО | 1999 |
|
RU2143280C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТАБЛЕТИРОВАННОЙ ФОРМЫ ХОЛЕРНОЙ БИВАЛЕНТНОЙ ХИМИЧЕСКОЙ ВАКЦИНЫ | 2014 |
|
RU2563620C2 |
| СПОСОБ ПРОИЗВОДСТВА ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ХОЛЕРЫ | 1988 |
|
RU2080121C1 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ НАТИВНЫХ ХОЛЕРОГЕНА-АНАТОКСИНА И О-АНТИГЕНА VIBRIO CHOLERAE О1 КЛАССИЧЕСКОГО БИОВАРА ШТАММА 569 В СЕРОВАРА ИНАБА | 2011 |
|
RU2451522C1 |
| ШТАММ БАКТЕРИЙ VIBRIO CHOLERAE KM 200 - ПРОДУЦЕНТ ХОЛЕРНОГО ТОКСИНА И ТОКСИН - КОРЕГУЛИРУЕМЫХ ПИЛЕЙ АДГЕЗИИ | 2001 |
|
RU2193598C1 |

Использование: биотехнология, профилактика, конъюгированные вакцины против холеры. Сущность изобретения: проводят конъюгацию азидным методом диацилированных липополисахаридов сероваров Инаба или Огава с сополимером N-окиси этиленпиперазина и N-ацилгидразида этиленпиперазиний бромидом с мол. м. 40 кДа при весовом соотношении носитель: антиген 4 - 7 : 1. Способ позволяет получить безвредную, высокоиммуногенную вакцину, не вызывающую аллергического действия на организм. 3 табл.
СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ ХОЛЕРЫ путем конъюгации антигена из деацилированных липополисахаридов сероваров Инаба или Огава с носителем, отличающийся тем, что в качестве носителя используют сополимер N-окси этиленпиперазина и N-ацилгидразида этиленпиперазиний бромида с мол.м. 40 КДа, а конъюгацию проводят азидным методом при массовом соотношении носитель : антиген 4 - 7 : 1.
| ПОВЫШАЮЩИЙ ТЕПЛОПРОВОДНОСТЬ МАТЕРИАЛ | 2013 |
|
RU2598621C2 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1994-10-30—Публикация
1991-06-05—Подача