Изобретение относится к производным глицина или их физиологически приемлемым солям - новым биологически активным соединениям, обладающим способностью тормозить связывание фибриногена у фибриногенного рецептора тромбоцитов.
Близкими структурными аналогами являются глицинсодержащие производные 4-амидинофенилаланинов.
Однако известные соединения являются ингибиторами сериновых протеаз и не обладают свойством ингибировать связывание белков, таких как фибриноген, на соответствующие рецепторы на поверхности клеток.
Цель изобретения - поиск новых соединений в ряду производных глицина, обладающих способностью тормозить связывание фибриногена у фибриногенного рецептора кровяных телец.
Цель достигается описываемыми производными глицина общей формулы I:
R-CONH-CH2-CONH-CH(R')-CH2COOH где R - группа формулы
-CH(NH-Ra)-(CH2)1-6-NH-Rb (R - 1)
-(T)m-C6H4-CH2NH2 (R - 2)
-(T)m-C6H4-(NH)n-C(NH)-L (R - 3),
-(T) NC(NH)NH2 (R - 4) где m , n = 0, 1 Ra водород, -COO-C1-4-алкил, Z, -COC6H4N3 -SO2-нафтил или -COCH2N(Y)CH2CH2NHY Y = водород, Вос или Z Rc - группа формулы - C(NH) (CH2)0-3CH3 или
NC(NH)NH2 (R - 4) где m , n = 0, 1 Ra водород, -COO-C1-4-алкил, Z, -COC6H4N3 -SO2-нафтил или -COCH2N(Y)CH2CH2NHY Y = водород, Вос или Z Rc - группа формулы - C(NH) (CH2)0-3CH3 или
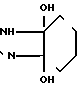 или, если Ra - группа формулы: -COC6H4N3, -SO2-нафтил, -COCH2N(Y)CH2CH2NHY, то Rb - амидиногруппа n = число 1 или 0 L = аминогруппа или, если n = 1, то L -(CH2)0-3CH3 Т = группа формулы -(СН2) (О)n, n = 1 или 0 -СН(Rd)CH2- или -СН2СО-, причем одна из содержащихся в Т-группе карбонильных групп может существовать в виде кеталя
или, если Ra - группа формулы: -COC6H4N3, -SO2-нафтил, -COCH2N(Y)CH2CH2NHY, то Rb - амидиногруппа n = число 1 или 0 L = аминогруппа или, если n = 1, то L -(CH2)0-3CH3 Т = группа формулы -(СН2) (О)n, n = 1 или 0 -СН(Rd)CH2- или -СН2СО-, причем одна из содержащихся в Т-группе карбонильных групп может существовать в виде кеталя
Rd - водород или NHRa
R1 - водород или CORo
Ro - -NH C1-4-алкил,
-NH(CH2)1-4 C2H4Hal, -NH C6H4COOH или радикал связанной через аминогруппу
α -аминокарбоновой кислоты, или их физиологически приемлемые соли, обладающие способностью тормозить связывание фибриногена у фибриногенного рецептора тромбоцитов.
В следующих примерах описано получение соединений формулы I.
П р и м е р 1. А) Раствор 55 мг (3-(п-аминофенил)-ДL-аланил)-Gly Asp (OtBu)Ser (tBu)OtBu - гидроиодида выдерживают в течение 2 ч при комнатной температуре под аргоном, в смеси 10 мл метиленхлорида и 5 мл трифторуксусной кислоты. После выпаривания растворителя получают 43 мг (86%) (3-)п-амидинофенил)-ДL-аланил)-GlyAspSerOH трифторацетата (2 : 3). Температура плавления 223-224оС из уксусного эфира (изопропилового эфира).
В) Исходный эфир приготавливают следующим образом:
а) охлажденный до 0оС раствор 1,95 г HSer(tBu) - OtBu - тозилата в ДМФ доводят до рН 8 посредством добавления N-метилморфолина. К нему добавляют раствор 2,1 г Z-Asp(OtBu)OSU в 160 мл ДМФ. После этого смесь в течение 1 ч при 0оС перемешивают под аргоном и в течение ночи выдерживают в холодильнике. Оставшийся после испарения растворителя остаток помещают в этилацетат и промывают насыщенным раствором бикарбоната натрия, водой, 1,0%-ным раствором бисульфата калия и снова водой, затем высушивается, фильтруется и упаривается. Получают 2,09 г (80%) Z-Asp(OtBu)-Ser(tBu)OtBu температура плавления 79-80оС из этилацетата /н-гексана;
б) 1,9 г - Asp(OtBu)Ser(tBu)OtBu гидрируют в 100 мл метанола в присутствии 0,1 г катализатора, 10% Pd/C. После поглощения теоретического количества водорода фильтруют и выпаривают досуха. Хроматография на силикагеле с метиленхлоридом (MeOH (98 : 2) дает 1,28 г (91%).
H Asp (OtBu)Ser(tBu)OtBu, MS : 389 (M + H)+
c) аналогично тому, как это описано в пункте а, из Z-Gly OSU и HAsp(OtBu) Ser(tBu)OtBu получают Z-Gly-Asp(OtBu) Ser(tBu)OtBu, выход - 86%
[ α]D - 6,9о (с 0,9 МеОН);
д) аналогично тому, как это описано в пункте б, посредством гидрогенолиза ZGly-Asp(OtBu)Ser(tBu)(OtBu) получают HGLy Asp(OtBu)Ser(tBu)(OtBu) выход 75%, MS : 446 (М + Н)+;
е) к раствору 200 мг N-Z-3-(п-цианофенил)аланина и 294 мг
HGly - Asp (OtBu)-Ser(tBu)OtBu в 10 мл ДМФ добавляют под аргоном 67 мг N-метилморфолина и 250 мг HВТУ и выдерживают смесь в течение ночи. Полученное затем после упаривания растворителя масло растворяют в этилацетате, раствор промывают 5%-ным раствором бикарбоната натрия и водой, сушат и упаривают. Остаток хроматографируют на силикагеле уксусным эфиром. Получают 160 мг соединения
(N-Z-3-(п-цианофенил)-ДL-аланил)-Gly-Asp(OtBu)-Ser(tBu) -OtBu (1 : 1 смесь эпимеров). Температура плавления 117-119оС из эфира/н-гексана.
f) раствор 362 мг соединения, полученного по пункту е, в 40 мл пиридина и 3 мл триэтиламина после насыщения его H2S, выдерживают в течение 2 дней, после чего он вымешивается в воде и экстрагируется этилацетатом. Продукт хроматографируют на силикагеле метиленхлоридом/метанолом. Получают 270 мг соединения (N-Z-3-(п-тиокарбоксамидофенил)-ДL-аланил)-Gly- Asp(OtBu)-Ser(tBu)OtBu (смесь эпимеров (1 : 1) MS : 786 (M +H+);
д) тиоамид, полученный в предыдущей стадии, растворяют в 30 мл ацетона, смешивают с 0,6 мл метилиодида и в течение 3 ч, нагревают под флегмой. После фильтрации и сгущения продукт осаждают добавлением эфира. Получают 181 мг (57% ) (N-Z-3-(п-метилтиокарбоксимидофенил)-ДL-аланил)- Gly-Asp(OtBu)-Ser(tBu)-OtBu-гидроиодида (смесь эпимеров 1 : 1), температура плавления 136-138оС;
h) раствор 180 мг иодила (полученного на предыдущей стадии) в 30мл МеОН смешивают с 37 мг ацетата аммония и нагревают при 60оС в течение 5 ч. После охлаждения и фильтрации продукт осаждают эфиром. Получают 89 мг (51%) (N-Z-3-(п-амидонофенил)-ДL-аланил)-Gly-Asp(OtBu) -Ser (tBu)-OtBu-гидроиодида (смесь эпимеров 1 : 1), температура плавления 150оС (разл.), из уксусного эфира /г-гексана.
i) аналогично тому, как это описано в пункте б, при гидрогенолизе продукта, полученного согласно пункта h, получают (3-)п-амидинофенил)-ДL-аланил) -Gly-Asp- (OtBu)-Ser(tBu)-OtBu-гидроиодида (смесь эпимеров 1 : 1), температура плавления 163-164оС уксусного эфира/н-гексана, выход 70%.
П р и м е р 2. А) аналогично тому, как это описано в примере 1А, при использовании (N-Вос-3)п-амидинофенил)-ДL-аланил) Gly-Asp(OtBu)-Val-OtBu-гидроиодидацетата (1 : 1) получают (3-(п-амидинофенил)ДL-аланил)-Gly-Asp-Val-OH -трифторацетат (1 : 1), температура плавления 174оС (разл.) из метанола/уксусного эфира, выход: 75%.
В) исходный материал может быть получен следующим образом:
а) при конденсации Z-Asp(OtBu)-OH и HValOtBu получают Z-Asp(OtBu)-ValOtBu, температура плавления 75оС (н-гексан), выход 93%;
б) посредством гидрогенолиза продукта, полученного на ступени а, получают H-Asp(OtBu)-ValOtBu, температура плавления 71оС, выход 93%;
в) посредством сочетания Z-GlyOSU и H-Asp(OtBu)-ValOtBu получают Z-Gly Asp(OtBu)-Val-OtBu, температура плавления 132оС (уксусный эфир), выход 87%;
д) посредством гидрогенолиза продукта, полученного на стадии с, получают H-Gly-Asp(OtBu)-ValOtBu выход 87%, [ α]D - 33,2оС (С 0,6 МеОН);
е) посредством сочетания рац. N-Вос-3-(п-цианофенил) аланина и H-Gly-Asp(OtBu)-Val-OtBu получают соединение (N-Вос-3-)п-цианофенил)-ДL-аланил)-Gly- Asp(OtBu)-Val(OtBu), температура плавления 140-145оС, из уксусного эфира/изопропилового эфира, выход 66%;
f) аналогично тому, как описано в примере 1В, f, д, h, из предыдущего соединения, через (N-Вос-3-(п-тиокарбокса- мидофенил)ДL-аланил)-Gly-Asp(OtBu)-Val- OtBu (смесь эпимеров 1 : 1), выход 96%, MS : 708 (M+H)+ и через (N-Вос-3-(п-метилтиокарбоксамидофенил)-ДL-аланил)-Gly -Asp(OtBu)-Val-OtBu-гидроиодид (смесь эпимеров (1 : 1), температура плавления 100оС (разл. ), выход 82% , получают (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp(OtBu)- -Val-OtBu-гидроиодид-ацетат (смесь эпимеров 1 : 1), температура плавления 154-156оС (разл.) (уксусный эфир), выход 89%.
П р и м е р 3. А) 95 мг (N-Вос-3-(п-гуанидинофенил)-L-аланил) Gly-Asp-(OtBu)-Val-OtBu растворяют в 10 мл этилацетата и смешивают с 5 мл 2,5 Н HСl. После 4 ч перемешивания при комнатной температуре фильтруют и осадок промывают уксусным эфиром. Получают 44 мг (53%) 3-(п-гуанидинофенил)-L-аланил)-Gly-Asp-Val-OH -пента-гидрохлорида, температура плавления 215оС (разл.) из диоксана.
В) Исходный материал может быть получен следующим образом:
а) посредством конденсации N-Вос-3-(п-нитрофенил)-1-аланина и HGly-Asp(OtVu)-ValOtBu получают (N-Вос-3-(п-нитро- фенил)-L-аланил)-Gly-Asp(OtBu)-ValOtBu температура плавления 106оС (н-гексан), выход 72%;
б) раствор 890 мг продукта, полученного на ступени а, в течение 3 ч гидрируют в 15 мл метанола в присутствии катализатора Pd/C. После фильтрования и упаривания растворителя оставшуюся пену хроматографируют на силикагеле смесью: этилацетат-метанолом (95 : 5) и кристаллизуют из изопропилового эфира. Получают 670 мг (79% ) соединения (N-Вос-3-(п-аминофенил)-L-аланил)-Gly-Asp(OtBu)-ValOtBu, температура плавления 110-112оС;
с) раствор 200 мг продукта, полученного на ступени б, и 60 мг 3,5-диметил-N-нитро-IH-пиразол-I-карбоксамидина в 3 мл этанола нагревают в течение 24 ч с образованием флегмы. Растворитель выпаривают и остаток хроматографируют на силикагеле метиленхлоридом/метанолом (98 : 2). После перекристаллизации из этилацетата /н-гексана получают 148 мг (66%) (N-Вос-3-(п-нитрогуанидино)фенил)-L-аланил)-Gly -Asp(OtBu)-ValOtBu, температура плавления 141-143оС;
д) раствор 118 мг соединения, полученного на предыдущей стадии в 3 мл уксусной кислоты, гидрируют в присутствии катализатора Pd/C (30 мг) в течение 3 дней. После удаления растворителя фильтрат хроматографируют на силикагеле смесью этилацетата и метанола (99 : 1). Получают 59 мг (54%) (N-Вос-3-(п-гуанидинофенил)-L-аланил)-Gly -Asp(OtBu)-ValOtBu MS : 706 (M+H)+.
П р и м е р 4. А) Аналогично тому, как это описано в примере 3А, посредством гидролиза (N-Вос-3-)N-аминонофенил)-ДL-аланил) Gly-Asp-(OtBu)-изобутиламид-гидроиодида получают (3-(п-амидино- фенил)-ДL-аланил)-Gly-Asp изобутиламид-гидрохлорид (смесь эпимеров 1 : 1), температура плавления 195-198оС (разл.) из диоксана: выход количественный.
В) исходный материал может быть получен следующим образом:
а) к приготовленной при -10оС смеси 5,12 г Z-Asp(OtBu)-OH-гидрата, 1,65 мл N-метилморфолина и 2 мл изобутилового эфира хлормуравьиной кислоты в 15 мл ТГФ по каплям добавляют 5,5 г изобутиламина, растворенного в 5 мл ТГФ. Через 3 ч освобожденный от растворителя остаток помещают в этилацетат (бикарбонат натрия 5%) и органическую фазу промывают водой. После высушивания, упаривания растворителя и хроматографии полученного масла на силикагеле этилацетатом получают 4,53 г (80%) Z-Asp(OtBu)-изобутиламида, температура плавления 69-70оС из н-гексана;
б) посредством гидрогенолиза продукта, полученного на стадии а, получают Н-Asp(OtBu)-изобутиламид, выход 97%, MS : 189, 171;
с) посредством связывания Z-Gly-OH c продуктом, полученным на стадии б, получают Z-Gly-Asp(OtBu)-изобутиламид, выход 87%, MS : 436 (M+H)+;
д) посредством гидрогенолиза продукта, полученного на предварительной ступени, получают H-Gly-Asp(OtBu) изобутиламид, выход 42%, MS : 302 (М+Н)+;
е) посредством связывания рац. N-Вос-3-(п-цианофенил) аланина и H-Gly-Asp(OtBu)-изобутиламида получают (N-Вос-3-(п- цианофенил)-ДL-аланил)-Gly-Asp(OtBu)-изо- бутиламид (смесь эпимеров 1 : 1), температура плавления 117-119оС (уксусный эфир/н-гексан), выход 27%;
f) аналогично тому, что описано в примере 1В, f, д, через (N-Вос-3-(п-тиокарбоксамидофенил)-ДL-аланил)-Gly -Asp(OtBu)-изобу-тиламид (смесь эпимеров 1 : 1) и через (N-Вос-3-(п-метилтиокарбоксимидофенил)-ДL-аланил)-Gly -Asp(OtBu)-изобутиламид-гид-роиодид (смесь эпимеров 1 : 1), температура плавления 145-147оС (разл.), выход 72%, получают соединение (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp(OtBu) -изобутил- амид-гидроиодид (смесь эпимеров 1 : 1), температура плавления 175-178оС, выход 60%.
П р и м е р 5. А) Аналогично тому, как это описано в примере 1А, получают, используя (N-Z-3-(п-амидинофенил)-ДL-аланил) Gly-Asp-(OtBu)-изобутиламид, соединение (N-Z-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp -изобутиламидтрифтора- цетат (смесь эпимеров 1 : 1), температура плавления 141-143оС (эфир), выход 91%.
В) Исходный материал может быть получен следующим образом:
а) посредством сочетания рац. N-Z-3- (п-цианофенил)аланина и H-Gly-Asp(OtBu)-изобутиламида получают (N-Z-3-(п-цианофенил)-ДL-аланил)-Gly-Asp(OtBu)-изобутила -мид (смесь эпимеров 1 : 1), температура плавления 121-123оС (этилацетат /н-гексан), выход 91%;
б) аналогично тому, как это описано в примере 1В f, д, h, через (N-Z-3-(п-тиокарбоксамидофенил)-ДL-аланил)-Gly -Asp(OtBu)- изобюутиламид (смесь эпимеров 1 : 1) и через (N-Z-3-(п-метилтиокарбоксимидофенил)-ДL-аланил)-Gly -Asp(OtBu) изобутиламид-гидроиодид (смесь эпимеров 1 : 1) получают (N-Z-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp(OBut) -изобутиламид-гидро- иодид (смесь эпимеров 1 : 1), температура плавления 160-163оС, выход 37%.
П р и м е р 6. Раствор 400 мг HArg-Gly-Asp-ValOH и 143 мг пиридин. HBr и 15 мл ДМФ прибавляют к 435 мг Z-(Aeg)Z-OSU. При помощи N-метилморфолина реакционную смесь доводят до рН 8,5 в течение ночи перемешивают и упаривают. Остаток растворяют в 0,3 н. уксусной кислоте и затем хроматографируют 0,2 н. уксусной кислотой на полисахаридной смоле (Сефадекс G-10). Одинаковые фракции объединяют и лиофилизуют. Водный раствор лиофилизата хроматографируют на полистирольной смоле в ацетатной форме (Довекс 44). Элюат лиофилизируют. Получают 143 мг Z-Aeg(Z)-Arg-Gly-Asp-ValOH MS 814 (M+H)+.
П р и м е р 7. Аналогично тому, как это описано в примере 1В, б, раствор 120 мг Z-Aeg(Z)-ArgGly-Asp-ValOH (пример 6) в 20 мл 0,1 н. уксусной кислоты гидрируют в присутствии катализатора Pd/C. Катализатор отфильтровывают, а фильтрат лиофилизируют. Получают 72 мг соединения Aeg-Arg-Gly-Asp-ValOH ацетат (1 : 1), MS : 546 (М+Н)+.
П р и м е р 8. К раствору 216 мг HArg-Gly-Asp-Ser-OH в 5 мл ДМФ и 5 мл Н2О прибавляют 242 мг Z-Aeg-(Z)-OSU и 0,11 мл N-метилморфолина. Реакционную смесь в течение 18 ч перемешивают и затем при помощи уксусной кислоты доводят до рН 5,3. Затем реакционную смесь экстрагируют этилацетатом. Водную фазу смешивают с катализатором Pd/C и гидрируют в течение 2 ч. Катализатор отфильтровывают, фильтрат лиофилизируют. Лиофилизат растворяют в 0,2 н. уксусной кислоте и хроматографируют на колонке из полисахаридной смолы (сефадекс G 25 S) 0,2 Н уксусной кислотой. Объединенные однородные фракции лиофилизируют. Получают 150 мг Aeg-Arg-Gly-Asp-SerOH ацетата (1 : 2), MS : 534 (M+H)+.
П р и м е р 9. Раствор 237,5 мг H-Arg-Gly-Asp-ValOH в 5 мл ацетона и 5 мл воды последовательно обрабатывают с 226 мг нафталин-2-сульфонхлорида и 168 мг бикарбоната натрия NaHCO3. После 2 ч перемешивания подкисляют уксусной кислотой и отгоняют ацетон. Водный остаток хроматографируют 0,2 н. уксусной кислотой на колонке Сефадекс G-25 S. Объединенные однородные фракции лиофилизируют. Получают 172 мг (2-нафтилсульфонил)-Arg-Gly-Asp-ValOH MS : 636 (M+H)+.
П р и м е р 10. Суспензия 3 г основы (носителя), состоящей из содержащей остаток п-бензилоксибензилового спирта стирол - 1% дивинилбензолсмолы, в 30 мл ДМФ последовательно смешивают с 0,6 г Fmoc-Nal(I)OH, 523 мг НВТУ, 16,8 мг 4-диметиламинопиридина и 0,24 мл ДIРЕА. Реакционную смесь в течение 24 ч встряхивают, в заключение смолу отфильтровывают и промывают ДМФ. Свободные гидроксильные группы в течение 30 мин ацетилируются в 30 мл ДМФ в присутствии 1,13 мл ангидрида уксусной кислоты и 2,02 мл N-этилди-изопропиламина. Далее описан весь цикл синтеза.
Протокол синтеза: Ступень Реагенты Время 1 ДМФ 2 х 1 мин 2 20% пипери-
дин/ДМФ 1 х 7 мин 3 ДМФ 5 х 1 мин 4 2,5
Fmoc-аминокис-
лота/ДМФ
+ 2,5 Аео. НВТУ
+ 2,5 Аео.-N этил-
диизопропиламин 1 х 90 мин 5 ДМФ 3 х 1 мин 6 Изопропиловый
спирт 2 х 1 мин
На каждой ступени синтеза используется 30 мл растворителя. Fmoc-Asp(OtBu)OH. FmocGlyOH. FmocArg(HCl)OH связывается согласно приведенному выше протоколу. Boc-Arg (Boc)OSU вводят в пептидную цепь. После окончания синтеза пептидную смолу высушивают. Ее суспендируют в 10 мл TFA/5 мл СН2Cl2 и 1 мл Н2О и встряхивают в течение 90 мин. Смолу затем отфильтровывают, фильтрат упаривают. Осадок лиофилизируют из воды. Лиофилизат хроматографируют 0,2 н. уксусной кислотой на колонке с сефадексом C-25S. Объединенные однородные фракции лиофилизируют. Лиофилизат, в свою очередь, хроматографируют на Довекс 44. Элюат лиофилизируют. Получают 49 мл NAeg-Arg-Gly-Asp-Nal(I)OH ацетата (1 : 1), M S : 644, (М+Н)+.
П р и м е р 11. Аналогично тому, как это описано в примере 10, исходя из 1,05 г Fmoc-NeOH получают 73,5 мг соединения Aeg-Arg-Gly-Asp-DIe-OH. TFA (1 : 1), M S : 560 (M+H)+.
П р и м е р 12. А) раствор 230 мг Вос-Lys (Z) Gly-Asp(OBzl)ValOBzl в 10 мл метанола гидрируют в присутствии катализатора Pd/C. Катализатор отфильтровывают, фильтрат упаривают. Остаток растворяют в 2 мл воды, при помощи 2 н. NaOH доводят до рН 9,5 и смешивают с 109 мг метилацетимидат НСl. Значение рН снова доводят до 9,5. После перемешивания в течение 90 мин реакционную смесь при помощи 1 н. HCl подкисляют до рН 4 и хроматографируют 0,2 н. уксусной кислотой на колонке Сефадекс G-25S. Однородные фракции объединяют и лиофилизируют. Получают 72 мг (N2-Boc-N6-(1-иминоэтил)-L-лизил)-Gly-Asp -ValOH MS : 559 (M+H)+.
В) Исходный материал может быть получен следующим образом: раствор 583 мг HGly-Asp(OBzl)-Val-OBzl (пример 15В, б) и 477,5 мг Вос-Lys(Z)-OSU в 10 мл ДМФ при помощи N-метилморфолина доводят до рН 8,5. После 18 ч перемешивания он сгущается, остаток помещают в уксусный эфир и воду. Органическую фазу промывают насыщенным раствором бикарбоната натрия, 5%-ным KHSO4.10%-ным K2SO4-раствором и насыщенным NaCl-раствором, затем сушат и фильтруют. Фильтрат сгущают, остаток кристаллизуют из эфира. Получают 385 мг BocLys(Z)-Gly-Asp(OBzl)-Val-OBzl, темп. плавления 95-101оС.
П р и м е р 13. А) 370 мг о-(Z-Arg-(Z2)-Gly-Asp(OtBu)-NH)-бензойной кислоты растворяют в 50 мл метанола и гидрируют в присутствии катализатора Pd/C. Фильтрат от катализатора сгущают в вакууме, остаток растворяют в 50 мл ДМФ и смешивают с 46 мг пиридин. HCl и 0,07 мл ДIРЕА. 203 мг НОВТУ готовят в 100 мл ДМФ, вышеназванный раствор прибавляют по каплям в среде аргона. После перемешивания в течение 20 ч добавляют еще 101,5 мг НОВТУ и 0,035 мл ДIРЕА. Реакционную смесь перемешивают еще в течение 18 ч и упаривают. Остаток растворяют в смеси метанол-вода и хроматографируют на колонке Довекс 44. Элюат упаривают ("сгущаются"), остаток растворяют в 20 мл TFA и после 30 мин сгущают. После хроматографии раствором 0,1% TFA-этанол на химически модифицированном силикагле (Лихросорб RP 18) получают 103 мг трифторацетата N-(о-азидобензоил-Arg-Gly-Asp)-антраниловая кислота (1) МS : 611 (M+H)+.
В) исходная кислота может быть приготовлена следующим образом:
а) раствор 1,6 г Z-Asp(OtBu)-OH в 2 мг толилата бензилового эфира антраниловой кислоты в 10 мл ДМФ смешивают с 1,92 г ТОВТУ и 1,78 мл ДIРЕА. После перемешивания в течение 20 ч реакционную смесь разделяют по фазам этилацетат и воду. Органическую фазу промывают раствором 5% KHSO4/ 10% K2SO4, водой, насыщенным раствором бикарбоната натрия, опять водой и насыщенным NaCl-раствором, после чего сушат посредством Na2SO4. Осушитель отфильтровывают и фильтрат сгущают. После кристаллизации из этанола получают 0,75 г N-(Z-Asp(OtBu) антраниловой кислоты, темп.плавления 123-124оС.
б) аналогично тому, как описано в примере 7, посредством гидрирования продукта, полученного на стадии а, получают 401 мг N(H-Asp(OtBu)-антраниловой кислоты.
с) к суспензии 401 мг продукта, полученного на стадии б, в 10 мл ДМФ добавляют 612 мг Z-Gly-OSU. При помощи N-метилморфолина реакционную смесь доводят до рН 8,5 и в течение 4 ч перемешивают. Затем реакционный раствор обрабатывают с 0,52 мл диэтиламиноэтиламина, перемешивают в течение 10 мин и потом помещают в уксусный эфир и 5% KHSO4 / 10% K2SO4-раствор. Органическую фазу промывают насыщенным раствором поваренной соли и высушивают. После фильтрации фильтрат сгущают. Остаток растворяют в метаноле и гидрируют в присутствии Pd/C. Катализатор отфильтровывают, фильтрат упаривают. Остаток растворяют в 10 мл ДМФ, смешивают с 673 мг Z-Arg(Z2)OSU и при помощи N-метилморфолина доводят до рН 8,5. После перемешивания в течение 18 ч продукт осаждают посредством вливания в раствор 5% KHSO4 / 10% K2SO4. При помощи хроматографии смесью метиленхлорид/метанол на силикагеле, после перекристаллизации из этанола получают 410 мг O-(Z-Arg-(Z2)-Gly-Asp(OtBu)-NH)-бензойной кислоты, температура плавления 102-103оС.
П р и м е р 14. А) К раствору 109 мг Вос Arg-Gly-Asp-ValOH в 3 мл 0,2 М бората натрия - буфера (рН 9) добавляют 55,5 мг 1,2-циклогександиона, после чего смесь перемешивают под аргоном в течение 24 ч. Реакционный раствор подкисляют уксусной кислотой до рН 4 и хроматографируют 0,2 н. уксусной кислотой на колонке Сефадекс G-25S. Однородные фракции объединяют и лиофилизируют. Получают 46 мг (N2-Boc-N5) (3а, 4,5,6,7,7а-гексагидро -3а,7а-дигидрокси-IH-бензимидазол-2-ил)L-орнитил),Gly -Asp-ValOH, MS : 658 (M+H)+.
В) Для приготовления исходной кислоты к раствору 1 г H-Arg-Gly-Asp-Val-OH и 340 мг пиридин. HBr в 15 мл диоксана и 15 мл воды последовательно прибавляют 480 мг ди-трет-бутилдикарбоната и 0,59 г NaHCO3. После перемешивания в течение 18 ч реакционную смесь упаривают (в вакууме). Остаток очищают смесью вода/этанол на пористой стиролдивинилбензолсополимерной смоле (MCl-Gel СНР20Р). Объединенные однородные фракции упаривают и лиофилизируют из воды. Получают 260 мг Boc-Arg-Gly-Asp-ValOH MS : 546 (M+H)+.
П р и м е р 15. А) к раствору 275,5 мг N-Boc-3-(п-аминофенил)-L-аланил-Gly-Asp-ValOH в 3 мл воды последовательно прибавляют 138 мг K2CO3 и 124 мг аминоиминометансульфоновой кислоты. После 18 ч перемешивания реакционную смесь подкисляют ледяной уксусной кислотой и хроматографируют 0,2 н. уксусной кислотой на колонке Сефадекс G-25S. Объединенные однородные фракции лиофилизируют. Получают 205 мг (N-Boc-3-(п-гуанидинофенил)-ДL-аланил)-Gly-Asp-ValOH-соль калия (1 : 1), MS : 632 (M+H)+.
В) Исходный материал может быть приготовлен следующим образом:
а) К охлажденному до -20оС раствору 32,3 мг Вос-Asp(OBzl)-OH в 150 мл ДМФ прибавляют 11 мл N-метилморфолина и 13,07 изобутилового эфира хлормуравьиной кислоты. Полученную суспензию перемешивают при -15оС и смешивают с охлажденной до -20оС суспензией 37,95 г H-Val-OBzl тозилата и 11 мл N-метилморфолина в 150 мл ДМФ. Реакционную смесь в течение 10 мин перемешивают при температуре ниже -10оС и в течение 2 ч - при комнатной температуре, затем фильтруют, фильтрат упаривают. Остаток растворяют в этилацетате, промывают 5% -м KHSO4 / 10%-ным K2SO4 - раствором, водой, насыщенным раствором бикарбоната натрия, водой и насыщенным раствором бикарбоната натрия, водой и насыщенным раствором поваренной соли и высушивают. Органическую фазу упаривают. Получают 52,9 мг Вос-Asp(OBzl)-Val-OBzl. Из него 10,24 г растворяют в 30 мл TFA и затем упаривают. Остаток кристаллизуют из смеси эталацетатгексан. Получают 8,3 г H-Asp-(OBzl)-Val-OBzl. TFA (1 : 1), темп. плавления 147-148оС;
б) к раствору 4,2 г H-Asp(OBzl)-Val-OBzl TFA в 50 мл этилацетата последовательно добавляют 2,72 г Вос-Gly-OSU и 0,88 мл N-метилморфолина, после чего смесь в течение 72 ч перемешивают при 20оС. Реакционную смесь затем обрабатывают этилацетатом и водой и органическую фазу отделяют и промывают 5%-ным KHSO4 / 10%-м K2SO4, водой, насыщенным раствором бикарбоната натрия, водой и насыщенным NaCl-раствором. После сушки упаривают. Остаток растворяют в 30 мл трифторуксусной кислоты, выдерживают в течение 20 мин при 20оС и затем упаривают. После кристаллизации из смеси этилацетат/ гексан получают 3,5 г HGly-Asp(OBzl)-Val-OBzl. TFA (1 : 1), темп. плавления 150-151оС.
с) к раствору 1,08 г N-Boc-3-(4-нитрофенил)-аланина и 2,04 г HGly-Asp-(OBzl)-Val-OBzl TFA в 15 мл ДМФ последовательно добавляют 1,4 г НВТ и 1,23 мл N-этилдиизопропиламина. После перемешивания в течение 3 ч реакционную смесь помещают в этилацетат и воду. Состав обрабатывают так, как это описано в пункте б, и после перекристаллизации из смеси этилацетат/гексан получают 1,8 г N-Boc-3-(4-нитрофенил)-ДL-аланил-Gly-Asp(OBzl), темпе- ратура плавления 155-157оС.
д) раствор 1,5 г N-Boc-3-(4-нитрофенил)-ДL-аланил-Gly-Asp-(OBzl) -Val-OBzl в 50 мл 90%-ной ледяной уксусной кислоты гидрируют в присутствии 10% Pd/C. Фильтрат от катализатора лиофилизируют из воды. Получают 910 мг N-Boc-3-(4-аминофенил)-ДL-аланил-Gly-Asp-ValOH MS : 552 (M+H)+.
П р и м е р 16. А) аналогично тому, как это описано в примере 1А, посредством ацидолиза (N-Вос-3-(п-амидинофенил)-ДL-аланил) - Gly-Asp(OZB)-Nal(I)-OH получают соединение 3-(п-амидинофенил)-ДL-аланил)-Gly-Asp-Nal(I)OH) TFA (1 : 2) (смесь эпимеров 1 : 1), температура плавления 170оС (разл.) (этанол/уксусный эфир).
В) исходный материал может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, а, посредством связывания Z-GlyOH и HAsp(OtBu)OMe получают Z-Gly-Asp(OtBu)OMe температура плавления 92-95оС (гексан), выход 89% от теоретич.
б) к раствору 27,0 г продукта, полученного на предыдущей стадии в 200 мл ацетона при охлаждении прикапывают 70 мл 1 н. NaOH, в течение 2 ч смесь перемешивают. Посредством добавления 10% -ного водного раствора лимонной кислоты рН смеси устанавливается на 4, растворитель выпаривают, при этом выпадает искомый сырой продукт. После перекристаллизации из смеси эфир/гексан получают 19,04 г Z-Gly-Asp(OtBu)-OH, температура плавления 101-104оС, выход 70%;
с) аналогично тому, как это описано в примере 1В, а, посредством сочетания продукта предыдущей ступени с H Nal(I)OMe получают Z-Gly-Asp(OtBu) Nal(I)OMe, температура плавления 59оС (гексан), выход 34%;
д) аналогично тому, как это описано в примере 1В, б, посредством гидрогенолиза продукта, полученного на предыдущей ступени, получают H-Gly-Asp(OtBu)-Nal(I)OMe, температура плавления 67-68оС (гексан), выход 72%;
е) аналогично тому, как это описано в примере 1В, е, посредством конденсации N-Вос-3-(п-цианофенил)-ДL-аланина с продуктом, полученным на предыдущей ступени, получают (N-Вос-3-(п-цинофенил)-ДL-аланил)-Nal(I)OMe (эпимеры), выход количественный, MS : 730 (M+H)+;
f) аналогично тому, как это описано в примере 1В, f, посредством тионирования продукта, полученного на предыдущей ступени, получают (N-Вос-3-(п-тиокарбамо- ил)фенил)-ДL-аланил) Gly-Asp(OtBu)-Nal(I)OMe (эпимеры), температура плавления 110-112оС, выход 75%;
д) аналогично тому, как это описано в примере 1В, д, посредством метилирования продукта, полученного на предыдущей ступени, получают (N-Вос-3-(п-метилтио)формимидоилфенил)-ДL-аланил)-Gly -Asp(OtBu)-Nal(I)OMe-гидроиодид (эпимеры), температура плавления 128-130оС (эфир), выход 64%;
h) аналогично тому, как это описано в примере 1В, h, посредством реакции продукта, полученного на предыдущей ступени, с NH4OAc получают (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp(OtBu) -Nal(I)-OMe-гидроиодид (эпимеры), температура плавления 139-141оС (эфир), выход 70%;
i) аналогично тому, как это описано в пункте б, из продукта, полученного на предыдущей ступени получают (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly -Asp(OtBu)Nal(I)OH (эпимеры), температура плавления 206оС (уксусный эфир), выход 97%.
П р и м е р 17. К раствору 70 мг [3-(п-амидинофенил-ДL-аланил]-Gly-Asp-Val-OH -трифторацетата (1 : 2) (смесь эпимеров 1 : 1) (пример 2) в 0,6 мл ДМФ при комнатной температуре, при газации аргоном добавляют 30 мг триэтиламина и 24 мг ди-трет-бутилкарбоната, смесь перемешивают в течение 75 мин. После добавления уксусной кислоты до установления рН смесь упаривают и остаток вносят в уксусный эфир для кристаллизации. После перекристаллизации из смеси метанол/уксусный эфир получают соединение [N-Вос-3-(п-амидинофенил)-ДL-аланил]-Gly-Asp-ValOH (смесь эпимеров 1 : 1), выход 63%.
П р и м е р 18.
А) аналогично тому, как это описано в примере 1А, при использовании (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp(OtBu) - п-фторфенэтиламид-гидроиодида (1 : 1 эпимеры) получают 3-(п-амидинофенил)-ДL-аланил-Gly-Asp-n -фторфенэтиламидтрифторацетат (5 : 8 эпимеры), температура плавления 192-195оС, выходж 61%.
В) исходный эфир может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, е, посредством связывания Z-Gly-Asp(OtBu)OH (пример 16В, б) и 4-фторфенэтиламина с НВТ получают Z-Gly-Asp(OtBu)п-фторфенэтиламид, MS : 502 (M+H)+,
б) аналогично тому, как это описано в примере 1В, б, посредством каталитического гидрогенолиза продукта, полученного на предыдущей ступени, получают H-Gly-Asp(OtBu)п-фторфенэтиламид, MS : 368 (M+H)+;
с) аналогично тому, как это описано в примере 1В, е, посредством связывания рац. N-Вос-3-(п-цианофенил)аланина с продуктом предыдущей ступени получают (N-Вос-3-(п-цианофенил)-ДL-аланил)-Gly-Asp (OtBu)п-фторфенэтиламид (1 : 1 эпимеры), MS : 662 (M+IIa)+;
д) аналогично тому, как это описано в примере 1В, f, посредством реакции продукта, полученного на предыдущей ступени, с Н2S получают (N-Вос-3-(тиокарбамоил)фенил)-ДL-аланил)-Gly-Asp(OtBu)-п -фторфенэтиламид (1 : 1 эпимеры), MS : 674 (M+H)+.
е) аналогично тому, как это описано в примере 1В, д, посредством реакции продукта, полученного на предыдущей ступени, с MeI получают (N-Вос-3-(п-метилтиоформимидоил)-фенил)-ДL-аланил)-Gly -Asp(OtBu)-п-фторфенэтиламид-гидроиодид (1 : 1) (эпимеры), температура плавления 134-136оС (разл.) (эфир);
f) аналогично тому, как это описано в примере 1В, h, посредством реакции продукта, полученного на предыдущей ступени, с ацетатом аммония получают (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp(OtBu)-п -фторфенэтиламид-гидроиодид (1 : 1 эпимеры), температура плавления 90-92оС (разл.) из эфира.
П р и м е р 19. А) аналогично тому, как это описано в примере 1А, при использовании (п-амидиногидроциннамил)-Gly-Asp(OtBu)-Nal(I)-OH получают (п-амидиногидроциннамил)-Gly-Asp-Nal(I)-OH-трифторацетат (1 : 1), температура плавления 196-199оС (этанол) (эфир), выход 48%.
В) исходный материал может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, е, посредством связывания 3-(п-цианофенил)пропионовой кислоты и H-Gly-Asp(OtBu)-Nal(I)-OMe (пример 16В, д)) получают (п-цианогидроциннамоил)-Gly-Asp(OtBu)-Nal(I)OMe, температура плавления 112-113оС (СН2Cl2/гексан);
б) аналогично тому, как это описано в примере 1В, f, д, h, посредством реакции продукта, полученного на предыдущей ступени с) последовательно, Н2 MeI и ацетатом аммония получают (п-амидиногидроциннамоил) -Gly-Asp(OtBu)-Nal(I)-OMe гидроиодид, температура плавления 140-142оС (эфир);
с) аналогично тому, как это описано в примере 16В, б, посредством щелочного омыления продукта, полученного на предыдущей ступени, получают (п-амидиногидроциннамоил) -Gly-Asp-(OtBu)-Nal(I)-OН, температура плавления 236-237оС (вода).
П р и м е р 20. Аналогично тому, как это описано в примере 1А, при использовании (N-Вос-3-(п-амидинофенил)-Д-аланил)-Gly-Asp(OtBu)-Val -OtBu гидроиодида получают (3-(п-амидинофенил)-Д-аланил)-Gly-Asp-Val-OH трифторацетат (1 : 2), температура плавления 128оС (разл.) (эфир) - выход - количественный.
П р и м е р 21. А) аналогично тому, как это описано в примере 16В, б, посредством омыления (N-(N-Вос-3-(п-амидинофенил)-ДL-аланил) Gly-Asp(OtBu)-п-амино)бензойная кислота-метиловый эфир - гидроиодида (эпимеры 1 : 1) получают (N-(N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly-Asp-п-амино) бензойную кислоту (1 : 1 эпимеры), температура плавления 205-206оС, (метанол), выход 48%.
В) Исходный материал может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, а, посредством связывания Z-Gly-Asp(OtBu)OH и бензилового эфира п-аминобензойной кислоты получают бензиловый эфир (N-(Z-Gly-Asp(OtBu)-п-амино)бензойной кислоты, выход 32%, MS : 590 (M+H)+;
б) аналогично тому, как это описано в примере 1В, б, посредством гидрогенолиза продукта, полученного на предыдущей ступени, получают (N-Gly-Asp(otBu)-п-амино) бензойную кислоту, температура плавления 160оС (разл.) из смеси метанол/AcOEt;
с) исходя из продукта, полученного на предыдущей ступени, посредством метилирования диазометаном получают метиловый эфир N-(Gly-Asp(OtBu)-п-амино) бензойной кислоты, температура плавления 78-82оС (гексан), выход 77%;
д) аналогично тому, как это описано в примере 1В, е, посредством связывания рац. N-Вос-3-(4-цианофенил)аланина и продукта, полученного на предыдущей ступени, получают метиловый эфир (N-((N-Вос-3-(п-цианофенил)-ДL-аланил)-Gly-Asp(OtBu)-п -амино)бензойной кислоты (смесь эпимеров 1 : 1), температура плавления 108оС (уксусный эфир/ гексан), выход 51%;
е) аналогично тому, как это описано в примере 1В, f, д, посредством тионирования и метилирования продукта, полученного на предыдущей ступени, получают метиловый эфир (N-((N-Вос-3-(п-метилтиоформимидоил)фенил)-ДL-аланил) Gly-Asp(OtBu)-п-амино)бензойной кислоты - гидроиодид (эпимеры 1 : 1), температура плавления 150-151оС (эфир), выход 77%;
f) аналогично тому, как это описано в примере 1В, h, исходя из продукта, полученного на предыдущей ступени, посредством аммонолиза его получают метиловый эфир (N-((N-3-(п-амидинофенил)-ДL-аланил)- Gly-Asp(OtBu)-п-амино)бензойной кислоты гидроиодид (эпимеры 1 : 1), температура плавления 179-181оС (разл.) (эфир), выход 79%.
П р и м е р 22. Аналогично тому, как это описано в примере 1А, посредством гидролиза продукта, полученного согласно примеру 21, получают (N-((3-(п-амидинофенил)-ДL-аланил)-Gly-Asp-п-амино) бензойную кислоту (эпимеры 1 : 1), температура плавления 214-216оС (метанол), выход 78%.
П р и м е р 23. А) раствор 180 мг (п-цианогидроциннамоил)-Gly-Asp-Val-OH в смеси 10 мл метанола/концентрированного водного раствора аммиака (2 : 1) гидрируют в присутствии 180 мг никеля Ренея. По истечении 20 ч раствор отфильтровывают от катализатора и досуха упаривают. Остаток очищают на ионообменной смоле в Н+-форме и затем помещают в гексан для кристаллизации. Получают (п-аминометилгидроциннамоил)-Gly-Asp(OtBu)-Val-OH, темп. плавления 175оС (разл.), выход 25%.
В) исходный нитрил готовят аналогично тому, как это описано в примере 1А, посредством ацидолиза (п-цианогидроциннамоил)-Gly-Asp(OtBu)-Val-OtBu (пример 24В, а), температура плавления 132-134оС (уксусный эфир / гексан), выход 69%.
П р и м е р 24. А) аналогично тому, как это описано в примере 19А, исходя из (п-амидиногидроциннамоил)-Gly-Asp(OtBu)- Val-OtBu-гидроиодида получают (п-амидиногидроциннамоил) Gly-Asp-ValOH трифторацетат (1 : 1,1), температура плавления 141-143оС (эфир), выход количественный.
В) исходный эфир может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, е, посредством связывания п-цианогидрокоричной кислоты с H-Gly-Asp(OtBu)-Val-OtBu (пример 2В, д) (получают (п-цианогидроциннамоил) Gly-Asp(OtBu)-Val OtBu, температура плавления 132-134оС (AcOEt/гексан), выход 87%;
б) аналогично тому, как это описано в примере 1В, f, посредством тионирования продукта, полученного на предыдущей ступени, получают N-(тиокарбамоил)гидроциннамоил-Gly-Asp(OtBu)-Val-OtBu - температура плавления 70-73оС (гексан), выход 72%;
с) аналогично тому, как это описано в примере 1В, д, посредством метилирования продукта, полученного на предыдущей ступени, получают п(метилтио)формимидоил)гидроциннамоил-Gly-Asp(OtBu)-Val-OtBu-гид- роиодид, температура плавления 55-60оС, (эфир-гексан), выход 94%;
д) аналогично тому, как это описано в примере 1В, h, посредством аммонолиза продукта, полученного на предыдущей ступени, получают (п-амидиногидроциннамоил)-Gly-Asp(OtBu)-Val-OtBu -гидроиодид, температура плавления 116-120оС (гексан), выход 90%.
П р и м е р 25. Аналогично тому, как это описано в примере 1А, исходя из (N-Вос-3-(п-амидинофенил)-ДL-аланил)-Gly -Asp(OtBu)- Val-OtBu-гидроиодида получают (3-(п-амидинофенил)-L-аланил)-Gly-Asp-Val-OH-три- фторацетат (2 : 3), температура плавления 164-166оС (EtOH/AeOEt), выход 75%.
П р и м е р 26. А) аналогично тому, как это описано в примере 1А, посредством ацидолиза ((п-амидинофенокси)ацетил-Gly-Asp(OtBu)-Val-OtBu -гидроиодида при помощи TFA получают (п-амидинофенокси)-ацетил-Gly-Asp-ValOH трифторацетат, температура плавления 140оС (уксусный эфир) гексан), выход 67%.
В) исходный эфир может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, е посредством связывания п-цианофеноксиуксусной кислоты и H-Gly- Asp(OtBu)-Val-OtBu получают (п-(цианофенокси)ацетил)-Gly-Asp(OtBu)-Val-OtBu, температура плавления 55оС (уксусный эфир/гексан), выход 81%;
б) аналогично тому, как это описано в примере 1В, f, д, посредством реакции продукта, полученного на предыдущей стадии, с H2S получают (п-(тиокарбамоил)феноксиацетил) - Gly, выход 80%, MS : 595 (M+H)+;
с) аналогично тому, как это описано в примере 1В, посредством реакции продукта, полученного на предыдущей стадии с метилиодидом получают (п-(метилтио)формимидоил)-фенокси-ацетил-Gly-Asp(OtBu) -Val-OtBu-гидроиодид, выход 83%, MS : 609 (М+Н)+;
д) аналогично тому, как это описано в примере 1В h, посредством реакции продукта, полученного на предыдущей ступени, с ацетатом аммония получают п-(Амидинофенокси)ацетил-Gly-Asp(OtBu)-Val -гидроиодид, температура плавления 102-106оС (уксусный эфир/гексан), выход 84%.
П р и м е р 27. А) аналогично тому, как это описано в примере 1А, используя (п-амидинофенил)ацетил-Gly-Asp(OtBu)-Val-OtBu- гидроиодид, получают (п-амидинофенил)ацетил-Gly-Asp-ValOH-трифторацетат 5 : 4, температура плавления 175-178оС (ацетонитрил/метанол), выход 53%.
В) исходный эфир может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, е, посредством сочетания п+цианофенилуксусной кислоты с HGly-Asp(OtBu)-Val-OtBu (пример 2В, д) получают (п-цианофенил)ацетил-Gly-Asp(OtBu)-ValOtBu, температура плавления 111оС (уксусный эфир/гексан);
б) аналогично тому, как это описано в примере 1В, f, д, h, посредством реакции продукта, полученного на предыдущей ступени, с H2S метилтиодидом и ацетатом аммония получают (п-амидинофенил) ацетил-Gly-Asp(OtBu)-Val OtBu MS : 562 (M+H)+.
П р и м е р 28. А) 216 мг N-(N-(N-(бензилоксикарбонил)-3-(п-(N-(бензилоксикарбо- нил)амидино)фенил)-ДL-аланил)глицил) β-аланинбензилового эфира и 72 мг 5% Pd/C в течение 28 ч перемешивают в 4,3 мл смеси этанол/уксусная кислота (19 : 1) под водородом. Продукт хроматографируют на силикагеле смесью метанол/уксусная кислота (9 : 1). Очищенные фракции упаривают, остаток растворяют в разбавленной соляной кислоте, фильтруют, нейтрализуют разбавленным аммиаком, опять фильтруют и фильтрат снова упаривают. Остаток вносят в метанол, фильтруют, фильтрат примешивают к эфиру. Выпавший осадок центрифугируют, промывают эфиром и высушивают. Получают 28 мг N-(N-(3-(п-амидинофенил)-ДL-аланилглицил)- β -аланиндигидрохлорид, MS : 336 (27, M+H)
В) для приготовления исходного эфира N-(бензилоксикарбонил)-3-(п-цианофенил)-ДL-аланин и N-глицин- β -аланин-бензиловый эфир - трифторацетат связывают с образованием N-(N-(N-(бензилоксикарбонил)-3-(п-цианофенил)-ДL -аланил)глицил)- β -аланин-бензилового эфира, температура плавления 134-135оС. Исходя из него, используя сероводород и триэтиламин в пиридине, получают N-(N-(-N-(-бензилоксикарбонил)-3-(п-(тиокарбамоил)фенил) -ДL- аланил)глицил- β -аланин-бензиловый эфир, температура плавления 150-151оС. Реакция с метилиодидом в ацетоне, затем с ацетатом аммония в метаноле и выдерживание с бензиловым эфиром хлормуравьиной кислоты и триэтиламином в THF дают N-(N-(N-(бензилоксикарбонил)-3-(п-(N-(бензилоксикарбо- нил)амидино)фенил)-ДL-аланил)глицил- β -аланил-бензиловый эфир, MS : 694 (100, М+Н).
П р и м е р 29. Аналогично тому, как описано в примере 1, исходя из 178 мг N-(N-(N-(п-Амидинофенокси)ацетил)глицил)-3- трет-бутокси-L-аланил)-3-фенил-L-аланин-трет-бутилового эфира гидроиодида, посредством выдерживания его с трифторуксусной кислотой в метиленхлориде, получают 91 мг трифторацетата N-(N-(N-(п-амидинофенокси)ацетил)-глицил)-L- β -аспартил)-3-фенил-L-аланина, температура плавления 175-179оС.
Исходный материал может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, а, посредством связывания 7,0 г Z-Asp(OtBu)-OSU с 4,72 г Phe-OtBu ˙HCl, после обработки, хроматографии на силикагеле (уксусный эфир) и перекристаллизации получают 7,1 г трет-бутилового эфира N-(N)бензилокси)карбонил)-3-(трет-бутокси- карбонил)-L-аланил)-3-фенил-L-аланина, температура плавления 94-95оС;
б) после каталитического гидрирования продукта, полученного на предыдущей ступени (10,3 г), в этаноле в присутствии 10% Pd/C при комнатной температуре и нормальном давлении, после хроматографии на силикагеле уксусным эфиром получают 5,94 г H-Asp(OtBu)-Phe-OtBu [ α] D = +9,16o (c = 0,6, CH3OH);
с) аналогично тому, как это описано в примере 1В, а, посредством реакции 4 г H-Asp(OtBu)-Phe-OtBu 3,43 г Z-Gly-OSU, после хроматографии на силикагеле уксусным эфиром получают 3,9 г N-(N-((бензилокси)карбонил)глицил)-3-(трет -бутоксикарбо- нил)-L- α -аспартил)-3-фенил-L-аланин-трет-бутиловый эфир;
д) аналогично тому, как это описано в примере 1, посредством гидрогенолиза продукта, полученного на предыдущей стадии (2,19 г), после хроматографии (CH2Cl2/CH2OH 9 : 1) и перекристаллизации получают 909 мг трет-бутилового эфира N-(N-глицил-3-(трет-бутоксикарбонил)-L- α] -аспартил-3-фенил-L-аланина, температура плавления 99-100оС;
е) аналогично тому, как это описано в примере 1В, е, посредством связывания 675 мг продукта, полученного на предыдущей ступени, с 266 мг п-цианофеноксиуксусной кислоты, после хроматографии на силикагеле (уксусный эфир) и перекристаллизации получают 687 мг трет-бутилового эфира N-(3-(трет-бутоксикарбонил)-N-(N-(п -цианофенокси)ацетил)глицил)-L-аланил)-3-фенил-L-аланина, температура плавления 83-85оС (уксусный эфир/гексан);
г) аналогично тому, как это описано в примере 1В, f, посредством реакции продукта, полученного на предыдущей ступени (650 мг), с сероводородом, после хроматографии (уксусный эфир) и кристаллизации получают 405 мг трет-бутилового эфира N-3-(трет-бутоксикарбонил)-N-(N-((п-тиокарба- моил)фенокси)ацетил)глицил)-L-аланил)-3-фенил-L-аланина, температура плавления 83-86оС (гексан);
о) аналогично тому, как это описано в примере 1В, д, посредством метилирования продукта, полученного на предыдущей ступени (390 мг), получают 375 мг соединения -N(3-(трет-бутоксикарбонил)-N-(N-((n-(1-ме- тилтио)формимидоил)фенокси)ацетил)гли- цил)-L-аланил)-3-фенил-L-аланин-трет-бути- ловый эфир - гидроиодид, температура плавления 162оС (уксусный эфир/метанол);
п) аналогично тому, как это описано в примере 1В, h, посредством реакции 358 мг продукта, полученного на предыдущей ступени, с ацетатом аммония получают 267 мг соединения N-(N-(N-((п-Амидинофенокси)ацетил)глицил)-3-трет-бутокси -L-аланил)-3-фенил-L-аланин-трет-бутиловый эфир - гидроиодид, температура разложения 76оС (уксусный эфир/гексан).
П р и м е р 30. Обработка 140 мг N-(N-(N-((2-(п-амидинофенил)-1,3-диоксолан-2-ил) ацетил)глицил)-3-(трет-бутоксикарбонил)- L-аланил)-3-фенил-L-аланин-трет-бутилово- го эфира-гидроиодида трифторуксусной кислотой в метиленхлориде дает 158 мг соединения N-(N-(N-((2-п-амидинофенил)-1,3-диоксалан-3 -ил)ацетил)глицил)-L- α -аспартил)-3-фенил-L-аланин-трифторацетат (1 : 1). Часть полученного продукта очищают посредством хроматографии (RP-18, элюирование водой, затем смесью вода/ацетонитрил 2 : 1) и перекристаллизации, причем получают продукт с температурой плавления 242-245оС.
Исходный материал может быть приготовлен следующим образом:
а) смесь 8 г 4-цианобензоилуксусной кислоты - этилового эфира, 80 мл этиленгликоля, 0,3 п-толуолсульфоновой кислоты и 250 мл толуола кипятят с водоотделителем. После окончания реакции растворитель удаляют, остаток помещают в метиленхлорид и 0,1 н. раствор едкого натра. Органический экстракт высушивают, фильтруют и упаривают. После хроматографии (силикагель, гексан/уксусный эфир 1 : 1) получают 4,4 г бесцветного масла, которое растворяют в 30 мл этанола. При охлаждении на ледяной бане прикапывают 15 мл раствора 1 н. едкого натра и, в заключение, оставляют полученную смесь на 6 ч при комнатной температуре. После удаления этанола водную фазу экстрагируют уксусным эфиром и нейтрализуют 1 н. соляной кислотой. Выпавшие кристаллы отфильтровывают, промывают водой и высушивают. Получают 2,3 г этиленкеталя 4-цианобензоилуксусной кислоты, температура плавления 151-152оС;
б) аналогично тому, как это описано в примере 1В, е, посредством связывания 256 мг этиленкеталя 4-цианобензоилуксусной кислоты и 449 мг H-Gly-Asp(OtBu)-Phe-OtBu (пример 29, д), после хроматографии и перекристаллизации получают 390 мг соединения N-(3-трет-бутоксикарбонил)-N-(N-((2-(п-цианофенил)-1,3 -диоксолан-2-ил)аце-тил)глицил)-L-аланил)-3-фенил-L -аланил- трет-бутиловый эфир, температура плавления 81-82оС (гексан);
с) аналогично тому, как это описано в примере 1В, f, посредством реакции продукта, полученного на предыдущей ступени (360 мг), с сероводородом получают 323 мг трет-бутилового эфира N-(3-трет-бутоксикарбонил)-N-(N-((1-(п -тиокарбамоил)фенил)-1,3-диоксолан-2-ил)ацетил)глицил)-L -ала-нил)-3-фенил-L-аланина, температура плавления 96-98оС (гексан);
д) аналогично тому, как это описано в примере 1В, д, посредством метилирования 280 мг продукта, полученного на предыдущей ступени, получают 324 мг соединения N-(3-(трет-бутоксикарбонил)-N-(N-((2-(п-)1 -метилтио)формимидоил)фенил)-1,3-диоксо- лан-2-ил)ацетил)глицил)-L-аланин)-3-фенил - L-аланин-трет-бутиловый эфир - гидроиодид (1 : 1), температура плавления 110-112оС (ацетон/диэтиловый эфир);
е) аналогично тому, как это описано в примере 1В, h, посредством аммонолиза 250 мг продукта, полученного на предыдущей ступени, получают 200 мг соединения N-(N-(N-((2-(п-амидинофенил)-1,3-диоксолан- 2-ил)ацетил)-глицил)-3-трет-бутоксикарбо-нил)-L -аланил)-3-фенил-L-аланин-трет-бути- ловый эфир - гидроиодид (1 : 1), температура плавления 129-130оС.
П р и м е р 31. Раствор 100 мг соединение N-(N-(N-((2-(п-амидинофенил)1,3-диоксолан-2 -ил)ацетил)глицил)-L- α -аспартил)- 3-фенил-L-аланин-трифторацетат в 10 мл смеси трифторуксусная кислота/вода (9 : 1) оставляют на ночь при комнатной температуре. После удаления растворителя, хроматографии остатка (RP-18, элюирование водой, смесью вода / ацетонитрил 1 : 1) и перекристаллизации получают 33 мг соединения N-(N-(N-(п-амидинобензоил)ацетил)глицил)-L-аспартил)-3 -фенил-L-аланин-трифторацетат (1 : 1), температура плавления 225-230оС (разложение).
П р и м е р 32. Аналогично тому, как это описано в примере 1А, исходя из 50 мг N-(N-(N-(3-1-амидино-4-пиперидинил)пропионил) глицил)-3-трет-бутоксикарбонил-L-аланил)-3-фенил-L -аланин-трет-бутилового эфира, после перекристаллизации получают 32 мг соединения N-(N-(N-(3-(1-амидино-4-пиперидинил)пропионил)глицил)-L- α -аспартил)-3-фенил-L-аланин-трифторацетат 1 : 1), температура плавления 146-148оС (эфир, разложение). Исходный материал может быть приготовлен следующим образом:
а) к раствору 553 мг S-метил-изотиокарбамидсульфата в 3,2 мл 2н. раствора едкого натра при 2оС добавляют 500 мг 4-пиперидинпропионовой кислоты. После выдерживания реакционной смеси в течение ночи при комнатной температуре, выпавшие кристаллы отфильтровывают, промывают водой, ацетатом и эфиром и высушивают. Получают 600 мг 1-амидино-4-пиперидинипропионовой кислоты, температура плавления выше 275оС;
б) аналогично тому, как это описано в примере 1В, е, посредством связывания 1,6 г 1-амидино-4-пиперидинпропионовой кислоты с 1,8 г H-Gly-Asp(OtBu)-Phe-OtBu в присутствии 928 мг гидрохлорида пиридиния получают 2,1 г трет-бутилового эфира N-(N-(N-(3-(1-амидино-4-пиперидинил)про-пионил)глицил)-3 -трет-бутоксикарбонил-L-аланил)-3-фенил-L-аланина, температура плавления 104-106оС (диизопропиловый эфир, разложение).
П р и м е р 33. Аналогично тому, как это описано в примере 1А, исходя из 17 мг 1-((N-(N-(п-амидиногидроциннамоил)глицил)-3 -(трет-бутоксикарбонил)-L-аланил)амино)- циклопентанкарбоновой кислоты, после кристаллизации получают 15 мг соединения 1-((N-(N-(п-амидиногидроциннамоил)гли- цил)-1- α -аспартил)-амино)-циклопентанкарбоновая кислота - трифторацетат (1 : 1), температура плавления 136-138оС (эфир, разложение). Исходный материал может быть приготовлен следующим образом:
а) аналогично тому, как это описано в примере 1В, е, исходя из 761 мг Z-Gly-Asp(OtBu)-OH (пример 16) и 359 мг соединения 1-аминоциклопентанкарбоновая кислота - метиловый эфир - гидрохлорид в тетрагидрофуране, после хроматографии на силикагеле уксусным эфиром, получают 920 мл третбутилового эфира N-(N-бензилоксикарбонилглицил)-3-((1-метоксикарбо- нил)-циклопентил)карбамоил)- α -аланина, MS (FAB), 506 (M+I)+;
б) аналогично тому, как это описано в примере 1В, б, посредством гидрогенолиза 880 мг продукта, полученного на предыдущей ступени, получают 620 метилового эфира 1-((3-(трет-бутоксикарбонил)-N-глицил-L- аланил)амино)циклопентанкарбоновой кислоты, MS (FOB) : 372 (M+I)+;
с) аналогично тому, как это описано в примере 1В, е, посредством связывания 310 мг 3-(п-цианофенил)пропионовой кислоты и 600 мг продукта, полученного на предыдущей ступени, после хроматографической очистки (силикагель, уксусный эфир - уксусный эфир/метанол 9 : 1) получают 635 мг метилового эфира 1-((3-(трет-бутоксикарбонил)-N-(N-(п -цианогидроциннамил)глицил)-L -аланил)амино)циклопентанкарбоновой кислоты, MS : 546 (M+NH4)+;
д) аналогично тому, как это описано в примере 1В f, д, h, посредством последовательной реакции 600 мг продукта, полученного на предыдущей ступени, с сероводородом, метилиодидом и ацетатом аммония получают 279 мг соединения метиловый эфир 1-((N-(N-(п-амидиногидроциннамил)глицил)-3-(трет -бутоксикарбонил)-L -аланил)амино)циклопентанкарбоновой кислоты - гидроиодид, температура плавления 98оС (разложение), MS (FAB) : 546 (M+I)+;
е) аналогично тому, как это описано в примере 16В, б, посредством щелочного гидролиза 157 мг продукта, полученного на предыдущей ступени, получают 24 мг 1-((N-(N-(п-амидиногидроциннамил)глицил)-3- (трет-бутоксикарбонил)-L-аланил)амино)ци- клопентанкарбоновой кислоты, температура плавления 163-164оС.
П р и м е р 34. Раствор 275,5 мг N-Вос-3-(4-аминофенил)-ДL-аланил-Gly-Asp-ValOH (пример 15В, д)) в 3 мл воды при помощи 1 н. NaOH доводят до рН 9,5. Этот раствор смешивают с 219 мг метилацетамидат ˙HCl, значение рН снова устанавливают на 9,5 при помощи 1 н. HCl. После перемешивания в течение 2 ч реакционную смесь подкисляют 1 н. HCl до рН 4 и хроматографируют 0,2 н. уксусной кислотой на колонке Сефадекс G-25. Главную фракцию лиофилизируют и очищают на колонке Лихросорб RP 18 смесью 0,05 М ацетат аммония - этанол. Однородные фракции лиофилизируют из воды. Получают 25 мг (3-(п-(ацетимидоиламино)фенил)-N-(трет-бутоксикарбонил) -ДL-аланил)-Gly-Asp-ValOH, MS : 593 (M+H)+.
Производные глицина формулы I и их соли тормозят связывание фибриногенов, фибронектина и Виллебрандфактора у фибриногенного рецептора кровяных телец (гликопротеин IIo/IIIa), а также связывание их и других адгезивных протеинов, таких как витронектин, коллаген и ламинин, с соответствующими рецепторами на поверхности различных типов клеток. Упомянутые соединения оказывают, тем самым, влияние на клетка - клетка и клетка - матрица - взаимодействие. Они препятствуют особенно возникновению тромбов кровяных частиц и могут применяться для борьбы или преодоления таких болезней как тромбозы, сотрясение мозга, сердечный инфаркт, воспаление и артериосклероз. Далее эти соединения обладают эффектом по отношению к опухолевым клеткам, так как они тормозят образование метастазов. Благодаря этому они могут также применяться в качестве противоопухолевого средства.
Торможение при связывании фибриногенов у фибриногенных рецепторов, гликопротеина IIb/IIIa может быть продемонстрировано следующим образом.
Гликопротеин IIb/IIIa получают из тритона Х-100 из экстракта кровяных телец крови человека и очищаются посредством лектина-афинной хроматографии и хроматографии на Arg-Gly-Asp-Ser афинной колонке.
Полученный таким образом рецепторный протеин связывается с микротитровой пластиной. Специфическое связывание фибриногена у иммобилизованного рецептора определяется с помощью EI IS A-системы.
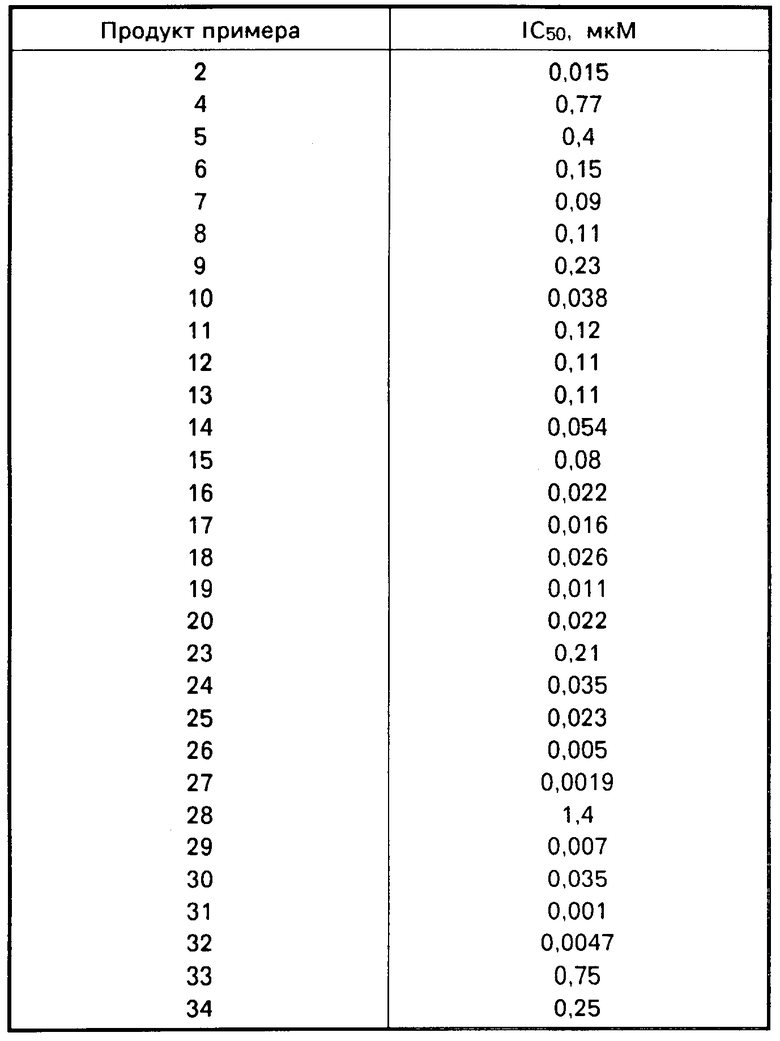
Нижеследующие IC50-значения соответствуют той концентрации тест-вещества, которое используется для того, чтобы затормозить на 50% связывание фибриногена у иммобилизованного рецептора (см. таблицу).
Описываемые соединения обладают очень низкой токсичностью. Так продукт примера 2 имеет ЛД5 = 600 мг/кг при внутривенном введении мышам.
Проведенные испытания показали, что описываемые соединения малотоксичны и обладают способностью тормозить связывание фибриногена у фибриногенного рецептора кровяных телец.
Назначение: в биохимии и медицинской химии благодаря способности тормозить связывание фибриногенного рецептора. Сущность изобретения: производные глицина общей формулы 1: R-CONH-CH2CONHCH(R′)CH2COOH , где R-группа формулы -CH(NHRa)-(CH2)1-6NH-Rb (R - 1) (T)m-C6H4·CH2NH2 (R - 2) (T)m-C6H4(NH)nC(NH)-L (R - 3) или n = 0 или 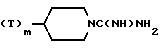 , Ra -водород, -COOC1-C4 -алкил, Z, -COC5H4N3 , -SO2 -нафтил или -COCH2H(Y)CH2CH2NH-Y y-водород, Вос или Z, Rb -группа формулы -C(NH)(CH2)0-3CH3 или
, Ra -водород, -COOC1-C4 -алкил, Z, -COC5H4N3 , -SO2 -нафтил или -COCH2H(Y)CH2CH2NH-Y y-водород, Вос или Z, Rb -группа формулы -C(NH)(CH2)0-3CH3 или 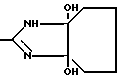 или же, если Ra -группа формулы -COC6H4N3, -SO2 -нафтил или -COCH2N(Y)CH2CH2NHY , то Rb -аминогруппа, где n - число 1 или 0, L-аминогруппа или же, если n - 1, то L - также -(CH2)0-3-CH3 Т - группа формулы -CH2-(O)n, n = 1 или, -CH(Rd)-CH2 или -CH2CO- , причем одна из содержащихся в Т-группе карбонильных групп может существовать в виде кеталя Rd -водород или NHRa или R′=H или COR0, R0- -NH0C1-4 алкил -NH(CH2)1-4-C0H4Hal, -NHC0H4COOH или радикал, связанный через аминогруппу α -аминокарбоновой кислоты или их физиологически приемлемые соли. Реагент 1: соединения вышеназванной общей формулы с защищенными аминогруппами: Phe, Ala - t-бутилоксикарбонильной, Asp, Val - ot-бутильной, Arg-бензилоксикарбонильной, Ala-бензильной. Реагент 2: деблокирующий. Полученные соединения малотоксичны и обладают высокой способностью ингибировать связывание фибриногена. 1 табл.
или же, если Ra -группа формулы -COC6H4N3, -SO2 -нафтил или -COCH2N(Y)CH2CH2NHY , то Rb -аминогруппа, где n - число 1 или 0, L-аминогруппа или же, если n - 1, то L - также -(CH2)0-3-CH3 Т - группа формулы -CH2-(O)n, n = 1 или, -CH(Rd)-CH2 или -CH2CO- , причем одна из содержащихся в Т-группе карбонильных групп может существовать в виде кеталя Rd -водород или NHRa или R′=H или COR0, R0- -NH0C1-4 алкил -NH(CH2)1-4-C0H4Hal, -NHC0H4COOH или радикал, связанный через аминогруппу α -аминокарбоновой кислоты или их физиологически приемлемые соли. Реагент 1: соединения вышеназванной общей формулы с защищенными аминогруппами: Phe, Ala - t-бутилоксикарбонильной, Asp, Val - ot-бутильной, Arg-бензилоксикарбонильной, Ala-бензильной. Реагент 2: деблокирующий. Полученные соединения малотоксичны и обладают высокой способностью ингибировать связывание фибриногена. 1 табл.
Производные глицина общей формулы
R - CONH - CH2 - CONH - CH (R1) - CH2COOH,
где R - группа формулы
-(CH) - (NH - Ra) - (CH2)1-6 - NH - Rb ( R - 1)
- (T)m - C6H4 - CH2NH2 (R - 2)
- (T)m - C6H4 - (NH)n - C ( NH) - L (R - 3)
-(T)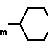 NC(NH)NH2 (R-4)
NC(NH)NH2 (R-4)
где m, n = 0,1,
Ra - водород, COO-C1 - C4-алкил, Z, -COC6H4N3, - SO2-нафтил или -COCH2N(Y)=CH2CH2NH-Y,
Y - водород, Вос или Z;
Rc - группа формулы -C(NH)(CH2)o-3-CH3 или
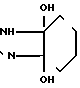
или, если Ra - группа формулы COC6H4N3, -SO2-нафтил или -COCH2N(Y)= CH2CH2NH-Y, то Rb - амидиногруппа;
n = 1 или 0;
L - аминогруппа или, если n = 1, то L - -(CH2)0-3-CH3;
T - группа формулы -CH2-(O)n, n = 0 или 1; -CH(Rd)-CH2- или -CH2CO-, причем одна из содержащихся в T-группе карбонильных групп может существовать в виде кеталя;
Rd - водород или -NH-Ra;
R1 - водород или -CO-R0;
R0 - -NH-C1 - C4-алкил, -NH(CH2)1-4-C6H4-Hal, -NH-C6H4 - COOH или радикал, связанный через аминогруппу α -аминокарбоновой кислоты,
или их физиологически приемлемые соли, обладающие способностью тормозить связывание фибриногена у фибриногенного рецептора тромбоцитов.
Приоритет по признакам:
23.02.89 при R - (R - 1), (R - 2) и (R - 3), причем в (R - 3) L = NH2;
29.11.89 при R - (R - 3), причем L = -(CH2)0-3-CH3, (R - 4) при T = -CH2CO-, причем содержащаяся в T-группе карбонильная группа может существовать как кеталь.
| H | |||
| Vieweg, G.Wagner "Synthesis of N alfa -tosyl-4 amidinophenylalanine derivatives withtwo C-terminally, inserted amino acids as poten fial ihibitors of serine proteinases" Pharmazie 1984, 39(2), 92-6. |
Авторы
Даты
1994-12-15—Публикация
1990-02-22—Подача