Изобретение относится к органической химии и касается усовершенствованного способа получения сложных эфиров N-метиленкарбокси-9-акридона различного строения, которые проявляют интенсивные биологические свойства, например являются низкомолекулярными индукторами интерферонов. Данные соединения проявляют противовирусную активность и могут быть использованы в качестве лекарственных средств.
Известен способ получения этилового эфира N-метиленкарбокси-9-акридона, заключающийся в алкилировании акридона этиловым эфиром монобромуксусной кислоты в безводном диметилформамиде. В качестве основания авторы предлагают использовать гидрид натрия. Реакцию проводят в атмосфере инертного газа [1]
Также известен способ получения этилового эфира N-метиленкарбокси-9-акридона путем взаимодействия акридона с этиловым эфиром монохлоруксусной кислоты в диметилформамиде. В качестве основания предлагается использовать гидроксид калия. Акридон и гидроксид калия кипятят в диметилформамиде, затем отгоняют азеотроп воды с диметилформамидом, добавляют этилхлорацетат. Смесь кипятят с обратным холодильником. Продукт реакции дважды экстрагируют хлороформом, который упаривают в вакууме. Полученный целевой продукт перекристаллизовывают из этанола. Выход конечного продукта на стадии сырца 72-75% после перекристаллизации 61-67% [2]
Этот способ получения этилового эфира N-метиленкарбокси-9-акридона выбран в качестве прототипа.
К недостаткам этого способа следует отнести:
получаемый в результате реакции этиловый эфир N-метиленкарбокси-9-акридона содержит значительное количество исходного продукта акридона (до 23-28%); в способе требуется значительное количество растворителя-диметилформамида;
диметилформамид при кипении частично разлагается с образованием реакционноспособного диметиламида, также вступающего в реакцию алкилирования, что загрязняет полученный целевой продукт;
способ трудоемкий, энергоемкий из-за стадии дополнительной очистки сырца, которая предусматривает двукратную экстракцию хлороформом и его последующее испарение в вакууме;
процесс образования калиевой соли акридона при использовании в реакции в качестве основания гидроксида калия, а в качестве растворителя диметилформамида сопровождается образованием поверхностно-активных веществ, что приводит к "вскипанию" реакционной массы и опасности ее выброса из реакционной емкости;
способ не является универсальным и не пригоден для получения различных сложных эфиров N-метиленкарбокси-9-акридона;
низкий выход целевого продукта.
Задачей изобретения является упрощение проведения технологического процесса получения сложных эфиров N-метиленкарбокси-9-акридона, сокращение времени, необходимого для получения целевых продуктов, увеличение безопасности в работе и главное повышение выхода и качества конечных продуктов.
Сущность нового способа заключается в том, что сложные эфиры N-метиленкарбокси-9-акридона получают путем взаимодействия акридона со сложными эфирами монохлоруксусной кислоты в диметилацетамиде с катализатором и в присутствии основания, причем в качестве оснований используют карбонаты щелочных металлов, а в качестве катализатора четвертичные аммониевые соли.
Способ осуществляют следующим образом.
Смесь акридона, карбоната щелочного металла (0,5-4 экв.) и четвертичной аммониевой соли (0,01-0,1 экв.) в диметилацетамиде выдерживают при температуре кипения диметилацетамида в течение 15-30 мин. Образующуюся в результате реакции воду отгоняют в виде азеотропа с диметилацетамидом, при этом удаляется около 15-20% диметилацетамида. Алкилирование осуществляется эфирами монохлоруксусной кислоты (метилхлорацетат, этилхлорацетат, пропилхлорацетат и т. п.) в количестве 1-4 эквивалентов при температуре кипения диметилацетамида в течение 20-45 мин. После окончания реакции реакционную массу охлаждают до 30-70оС и выливают в воду. Выпавший целевой продукт отделяют, промывают небольшим количеством этилового спирта, затем гексаном и высушивают при температуре не выше 150оС.
Анализ полученных соединений, проведенный методом количественной хроматографии в системах: а) хлороформ этанол (25:1), б) этанол этилацетат (1: 7) на пластинках Silufol VV-254, показал, что примесь акридона в синтезированных продуктах составляет менее 2%
Дополнительные анализы, проведенные методами масс-спектрометрии Н1 и С13 ЯМР-, УФ- и ИK-спектроскопии подтвердили полученные результаты и показали отсутствие в образцах других примесей.
Выход сложных эфиров N-метиленкарбокси-9-акридона составлял 82-88%
Способ проводился также в укрупненном масштабе (5-8 моль акридона) без снижения качества и выхода целевых продуктов и увеличения продолжительности процесса.
П р и м е р 1. 45 г акридона, 20 г безводного карбоната натрия, 0,5 г тетрабутиламмония йодистого смешивают с 100 мл диметилацетамида. Смесь кипятят с обратным холодильником 15 мин. Затем обратный холодильник заменяют на нисходящий и отгоняют смесь воды с диметилацетамидом ( ≈ 25 мл). После чего смесь охлаждают до 110-115оС и вносят 36,5 мл (42,25 г) этилхлорацетата и кипятят с обратным холодильником в течение 30 мин. Реакционную массу охлаждают до 70-60оС и выливают в 0,5 л воды, содержащей 200 г льда. Выпавший осадок отфильтровывают, промывают на фильтре 70 мл 96% этанола и 100 мл гексана. Высушивают при температуре не выше 120оС.
Получают 53 г этилового эфира N-метиленкарбокси-9-акридона, что составляет 84,7% Содержание акридона менее 0,5%
П р и м е р 2. 40 г акридона, 25 г безводного карбоната калия, 0,2 г тетраэтиламмония хлористого смешивают со 100 мл диметилацетамида. Смесь кипятят с обратным холодильником 30 мин. Затем обратный холодильник заменяют на нисходящий и отгоняют смесь воды с диметилацетамидом ( ≈ 25 мл). Смесь охлаждают до 140оС и вносят 50 г бутилхлорацетата и кипятят с обратным холодильником в течение 45 мин. Реакционную массу охлаждают до 30-40оС и выливают в 0,4 л воды, содержащей 150 г льда. Выпавший осадок отфильтровывают, промывают на фильтре 100 мл 96% этанола и 50 мл гексана. Высушивают при температуре 105оС.
Получают 57 г бутилового эфира N-метиленкарбокси-9-акридона, что составляет 85,5% Содержание акридона менее 1%
В качестве основания могут быть использованы карбонаты любых щелочных металлов (лития, натрия, калия и другие).
В качестве катализатора любые органические четвертичные аммониевые соли с различными анионами, содержащие предельные алифатические алкилы.
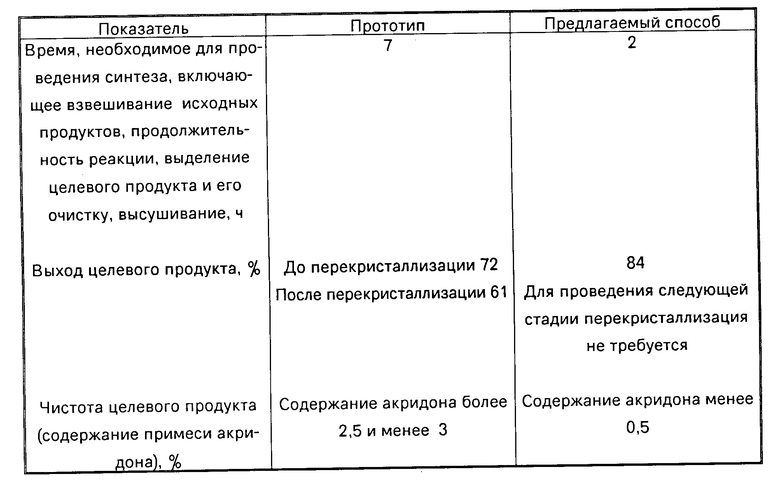
Сравнение данных таблицы показывают, что при использовании данного способа с прототипом в три раза сокращается время, необходимое для получения целевых продуктов, значительно (на 22-25%) увеличивается выход и возрастает чистота получаемых сложных эфиров N-метиленкарбокси-9-акридона.
Предлагаемый способ синтеза сложных эфиров N-метиленкарбокси-9-акридона опробован для получения соединений различного строения. Синтез метилового, этилового, пропилового, изопропилового, бутилового и амилового эфиров N-метиленкарбокси-9-акридона проходит практически в близких условиях и позволяет без изменения оборудования и параметров процесса получать данные соединения с выходом более 80%
Таким образом, совокупность признаков предлагаемого способа позволяет:
без изменения технологических параметров реакции получить широкий набор сложных эфиров N-метиленкарбокси-9-акридона;
упростить технологию получения сложных эфиров N-метиленкарбокси-9-акридона за счет исключения трудоемкой и длительной стадии очистки целевых продуктов; уменьшения объема используемого растворителя диметилацетамида; избежания образования поверхностно-активных примесей; использования значительно более безопасных в работе карбонатов щелочных металлов;
увеличить чистоту их конечных продуктов за счет сокращения времени реакции; использования катализатора четвертичных аммониевых солей;
повысить выход целевых продуктов до 82-88%
Использование: в качестве веществ, обладающих противовирусной активностью. Сущность изобретения: продукт - сложные эфиры N-метиленкарбокси-9-акридона. Реагент 1: сложные эфиры монохлоруксусной кислоты. Реагент 2: акридон. Условия реакции: в среде диметилацетамида в присутствии карбонатов щелочных металлов и четвертичных аммониевых солей в качестве катализатора. 1 табл.
СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ N-МЕТИЛЕНКАРБОКСИ-9-АКРИДОНА взаимодействием акридона с эфирами монохлоруксусной кислоты в среде органического растворителя в присутствии основания, отличающийся тем, что в качестве органического растворителя используют диметилацетамид, а в качестве основания карбонаты щелочных металлов и процесс ведут в присутствии четвертичных аммониевых солей в качестве катализатора.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Inglot A.D | |||
| и др | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
1995-04-20—Публикация
1993-01-28—Подача