Изобретение относится к способам стерилизации питьевой воды и может быть использовано для обеззараживания питьевой воды в процессе водоподготовки в различных областях народного хозяйства.
Известно применение активированного угля в процессе подготовки питьевой воды, при этом наблюдается значительное снижение концентрации органических примесей (1). Однако бактериологические исследования показали, что общее количество бактерий в фильтрате после активированного угля значительно.
Известно применение полигексаметиленгуанидина (ПГМГ) в дозах 0,2-0,9 мг/л в процессе биоцидной обработки воды оборотных систем (2). Но этот метод не пригоден для стерилизации питьевой воды, поскольку требует введения в воду в значительных количествах полигексаметиленгуанидина, что может отрицательно сказываться на количестве питьевой воды из-за наличия в ней полимера.
Наиболее близким по технической сущности и достигаемому результату к предлагаемому является способ очистки воды с применением бактерицидного активированного угля, получающегося привитой полимеризацией анионогенного мономера с катионным противоионом, обладающим бактерицидными свойствами в присутствии инициаторов полимеризации и инициаторов прививочной полимеризации.
В качестве подобных мономеров предпочтительно винильные и акриловые мономеры, имеющие сульфокислотную (-SO3H) или карбоксильную (-СООН) группы. В качестве катионных противоионов, обладающих бактерицидными свойствами, предла- гали четвертичное аммониевое соединение 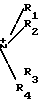 в котором один из заместителей четвертичного азота имеет длину приблизительно 8-10 углеродных атомов, либо замещенные гуанидины или бигуанидины. В качестве инициаторов прививки использовали ионы серебра, ионы железа (3). Однако этот способ имеет ряд существенных недостатков:
в котором один из заместителей четвертичного азота имеет длину приблизительно 8-10 углеродных атомов, либо замещенные гуанидины или бигуанидины. В качестве инициаторов прививки использовали ионы серебра, ионы железа (3). Однако этот способ имеет ряд существенных недостатков:
сложность метода получения этого адсорбента (прививка мономеров к поверхности угля, полимеризация мономеров;
использование такого угля предотвращает рост бактерий на поверхности и вокруг активированного угля;
введение в воду токсичных веществ;
процесс экономически нецелесообразен.
Технический результат заключается в увеличении эффективности процесса стерилизации воды.
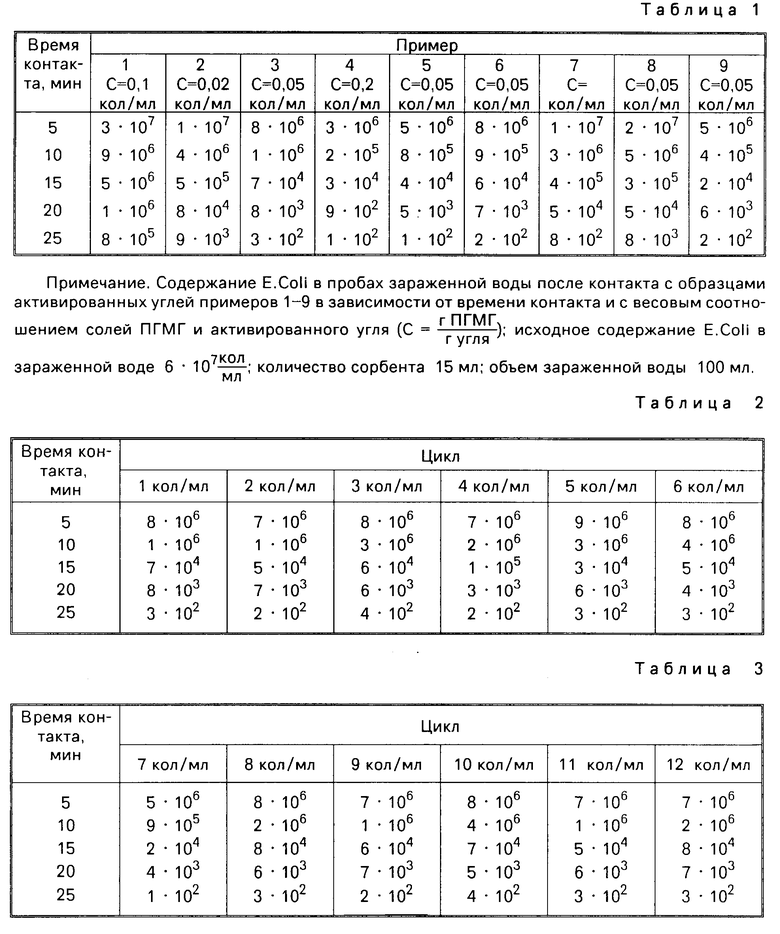
Это достигается тем, что в способе стерилизации питьевой воды воду пропускают через активированный уголь, предварительно обработанный солями полигексаметиленгуанидина с молекулярной массой 1-50 тыс.у.е. при этом соли полигексаметиленгуанидина (ПГМГ) и активированный уголь берут в массовом соотношении 0,02-0,2. Из солей ПГМГ предпочтительно применяют хлориды, фосфаты, карбонаты, глюконаты, обладающие бактерицидными свойствами. Например, элементарное звено хлорида ПГМГ [-(CH2)6-NH0 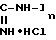 , молекулярная масса ПГМГ 10-50 тыс. Предпочтительное количество хлорида ПГМГ, адсорбированного на активированном угле 17,110-3 24,610-3
, молекулярная масса ПГМГ 10-50 тыс. Предпочтительное количество хлорида ПГМГ, адсорбированного на активированном угле 17,110-3 24,610-3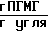 .
.
Известно, что поверхность активированного угля содержит значительное количество кислотных групп: карбоксильных, гидроксильных, поэтому возможна ионообменная адсорбция катиогенных бактерицидных соединений. Макромолекулы соли ПГМГ имеют высокую плотность положительного заряда и их адсорбция за счет кулоновского взаимодействия на поверхности активированного угля будет усиливаться за счет кооперативного взаимодействия многих положительно заряженных групп цепи макромолекул солей ПГМГ при рН больших рН диссоциации поверхностных кислотных групп активированного угля. Соотношение масс солей ПГМГ и активированного угля, равное 0,02-0,2 является наиболее оптимальным, так как применять соотношение менее 0,02 нецелесообразно, так как приводит к снижение эффективности процесса стерилизации воды, а более 0,2 приводит к большим потерям солей ПГМГ без увеличения их адсорбции, и, как следствие не приводит к увеличению эффективности самого процесса стерилизации.
П р и м е р 1. К 15 г активированного угля добавляют 30 мл водного раствора хлорида полигексаметиленгуанидинхлорида, концентрация 0,5 г/л. Смесь перемешивают на магнитной мешалке в течение 1 ч при температуре 22о С. Затем отделяют уголь от раствора полимера фильтрованием и определяют концентрацию хлорида ПГМГ в фильтрате спректрофотометрически. Метод основан на реакции образования окрашенного соединения с эозином максимум поглощения λ= 535 нм. Концентрация хлорида ПГМГ в фильтрате 0,325 г/о. Определяют количество хлорида ПГМГ, поглощенного активированным углем.
Для удаления излишков хлорида ПГМГ промывают активированный уголь дистиллированной водой порциями по 750 мл в течение 1 ч при перемешивании. В третьей порции промывной воды хлоридов ПГМГ не обнаружено. Суммарное количество хлорида ПГМГ, десорбировавшегося с активированного угля в промывные воды 0,45 ˙ 10-3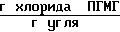 . Количество хлорида ПГМГ, оставшегося на активированном угле 3,1 ˙ 10-3
. Количество хлорида ПГМГ, оставшегося на активированном угле 3,1 ˙ 10-3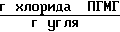
Уголь с адсорбированным хлоридом ПГМГ подсушивают при температуре 50о С и определяют его бактерицидность. Соотношение хлорида ПГМГ к активированному углю равно 0,01.
П р и м е р 2. Способ аналогичен методике, описанной в примере 1, за исключением концентрации исходного раствора хлорида ПГМГ, взято 300 мл раствора концентраций 1 г/л.
Отмывают уголь дистиллированной водой до тех пор, пока в промывных водах не обнаруживают хлорида ПГМГ.
Количество хлорида ПГМГ поглощенного активированным углем 13,0 ˙ 10-3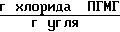 .
.
Количество хлорида ПГМГ, выделившегося в промывные воды 1,1 ˙ 10-3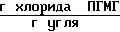 .
.
Количество хлорида ПГМГ, оставшегося на активированном угле после промывки его дистиллированной водой 11,9 ˙ 10-3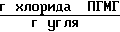 .
.
Соотношение хлорида ПГМГ к активированному углю равно 0,02.
П р и м е р 3. Способ аналогичен методике, описанной в примере 1, за исключением концентрации исходного раствора хлорида ПГМГ. В примере берут 300 мл водного раствора хлорида ПГМГ с концентрацией 2,5 г/л.
Количество хлорида ПГМГ, поглощенного активированным углем 30,6 ˙ 10-3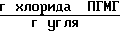 .
.
Количество хлорида ПГМГ, выделившегося в промывные воды 9,4 ˙ 10-3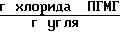 .
.
Количество хлорида ПГМГ, оставшегося на активированном угле после промывки его дистиллированной водой 21,2 ˙ 10-3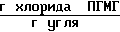 .
.
Соотношение хлорида ПГМГ к активированному углю равно 0,05.
П р и м е р 4. Способ аналогичен методике, описанной в примере 1, за исключением концентрации исходного раствора ПГМГ. В примере берут 300 мл водного раствора хлорида ПГМГ с концентрацией 10 г/л.
Отмывают уголь дистиллированной водой до тех пор, пока в промывных водах не обнаруживают хлорида ПГМГ.
Количество хлорида ПГМГ, поглощенного активированным углем 37,0 ˙ 10-3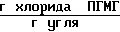 .
.
Количество хлорида ПГМГ, выделившегося в промывные воды 15,8 ˙ 10-3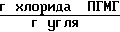 .
.
Количество хлорида ПГМГ, оставшегося на активированном угле после промывки его дистиллированной водой 21,2 ˙ 10-3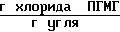 .
.
Соотношение хлорида ПГМГ к активированному углю равно 0,2.
П р и м е р 5. Способ аналогичен методике, описанной в примере 3. Но в этом примере используют фосфат ПГМГ. В примере берут 300 мл водного раствора фосфата ПГМГ с концентрацией 2,5 г/л.
Количество фосфата ПГМГ, поглощенного активированным углем 34,7 ˙ 10-3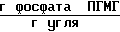
Количество фосфата ПГМГ, выделившегося в промывные воды 10,1 ˙ 10-3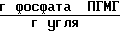 .
.
Количество фосфата ПГМГ, оставшегося на активированном угле после промывки его водой 24,6 ˙ 10-3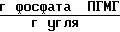 .
.
Соотношение фосфата ПГМГ к активированному углю равно 0,05.
П р и м е р 6. Способ аналогичен методике,описанной в примере 3, но в этом примере используют карбонат ПГМГ. В примере берут 300 мл водного раствора карбоната ПГМГ с концентрацией 2,5 г/л.
Количество карбоната ПГМГ, поглощенного активированным углем 29,0 ˙ 10-3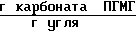 .
.
Количество карбоната ПГМГ, выделившегося в промывные воды 8,3 ˙ 10-3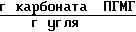
Количество карбоната ПГМГ, оставшегося на активированном угле после промывки его водой 20,7 ˙ 10-3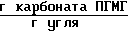 .
.
Соотношение карбоната ПГМГ к активированному углю равно 0,05.
П р и м е р 7. Способ аналогичен методике, описанной в примере 3. Но в этом примере используют глюконат ПГМГ. В примере берут 300 мл водного раствора глюконата ПГМГ с концентрацией 2,5 г/л.
Количество глюконата ПГМГ, поглощенного активированным углем 27,2 ˙ 10-3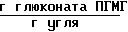 .
.
Количество глюконата ПГМГ, выделившегося в промывные воды 10,1 ˙ 10-3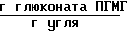
Количество глюконата ПГМГ, оставшегося на активированном угле после промывки его дистиллированной водой 17,1 ˙ 10-3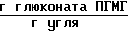 .
.
Соотношение глюконата ПГМГ к активированному углю равно 0,05.
П р и м е р 8. Способ аналогичен методике, описанной в примере 3, за исключением молекулярной массы хлорида ПГМГ. В примере использован хлорид ПГМГ молекулярной массы 1000 у.е.
Количество хлорида ПГМГ, поглощенного активированным углем 11,7 ˙ 10-3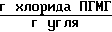 .
.
Количество хлорида ПГМГ, выделившегося в промывные воды 2,4 ˙ 10-3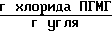 .
.
Количество хлорида ПГМГ, оставшегося на активированном угле после промывки его дистиллированной водой 9,3 ˙ 10-3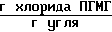 .
.
Соотношение хлорида ПГМГ к активированному углю равно 0,05.
П р и м е р 9. Способ аналогичен методике, описанной в примере 3, за исключением молекулярной массы хлорида ПГМГ. В примере использован хлорид ПГМГ молекулярной массы 50000 у.е.
Количество хлорида ПГМГ, поглощенного активированным углем 34,4 ˙ 10-3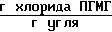 .
.
Количество хлорида ПГМГ, выделившегося в промывные воды 12,1 ˙ 10-3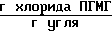 .
.
Количество хлорида ПГМГ, оставшегося на активированном угле после промывки его дистиллированной водой 22,3 ˙ 10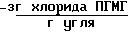 .
.
Соотношение хлорида ПГМГ к активированному углю равно 0,05.
Определение бактерицидности активированного угля. Для проведения испытания активированного угля на бактерицидную способность в водной среде используют культуру Е.Coli. Для этого культуру высевают на мясо-пептонный агар и инкубируют в течение суток при температуре 37о С, затем готовят суспензию этой культуры в фунологическом растворе и вносят ее в стерильную воду. Зараженную таким способом воду используют в дальнейшей работе.
Затем навеску исследуемого сорбента помещают в стерильную посуду, заливают зараженной водой и перемешивают на магнитной мешалке. Через определенные промежутки времени отбирают пробы для определения содержания в воде микроорганизмов. По истечении контрольного времени пробу отстаивают, декантируют. Активированный уголь промывают стерильной водой и повторяют испытания со следующей порцией зараженной воды.
Определение содержания Е. Coli в воде. Для определение содержания микроорганизмов типа Е.Coli в воде применяют метод посева на мембранный фильтр на среду Эндо, являющуюся избирательной средой для микроорганизмов данной группы.
Отобранную пробу подвергают разведению стерильной водой. После этого на вакуумном фильтровальном диске через мембранный фильтр фильтруют определенный объем пробы (обычно 1 мл) и помещают фильтр на среду Эндо. Чашки Петри с фильтрами инкубируют при температуре 37о С в течение 24 ч. После этого производят визуальный подсчет выросших колоний с учетом разведения каждой пробы.
В табл.1 приведены данные по исследованию бактерицидной активности предлагаемых образцов.
Из данных табл. 1 видно, что при соотношении компонентов, равном 0,01, эффективность не достаточна (пример 1), а при соотношении компонентов, равном 0,2, процесс обладает достаточной эффективностью (пример 4).
В табл. 2 и табл.3 представлены результаты исследования активированного угля с адсорбированными солями ПГМГ в процессе очистки зараженной воды в течение нескольких периодических циклов.
В таблице приведены данные для активированного угля, полученного способом, описанным в примере 3. Содержание Е.Coli в пробах зараженной воды после контакта с активированным углем примера 3. Исходное содержание Е.Сoli в зараженной воде 6 ˙ 107 кол/мл. Количество сорбента 15 мл; объем зараженной воды 100 мл.
Из данных табл. 2 видно, что в течение времени эксперимента 12 циклов снижения обеззараживающего действия не обнаружено.
Следовательно, предлагаемый способ обладает новыми свойствами, обеспечивающими положительный эффект, заключающийся в увеличении эффективности процесса стерилизации.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗИНФИЦИРУЮЩЕГО СРЕДСТВА | 1993 |
|
RU2039735C1 |
| БИОЦИДНАЯ ПРИСАДКА | 1995 |
|
RU2074234C1 |
| ГЕЛЬ ДЕЗИНФИЦИРУЮЩИЙ | 2005 |
|
RU2301057C1 |
| СРЕДСТВО ДЛЯ ДЕЗИНФЕКЦИИ КОЖНОГО ПОКРОВА | 2005 |
|
RU2292919C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЦИДНОГО СОРБЕНТА ДЛЯ ОБЕЗЗАРАЖИВАНИЯ ПИТЬЕВОЙ ВОДЫ | 2000 |
|
RU2167707C1 |
| БИОЦИДНЫЙ ПРЕПАРАТ | 1998 |
|
RU2142293C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗИНФИЦИРУЮЩЕГО СРЕДСТВА | 1998 |
|
RU2122866C1 |
| Привитые сополимеры полиоксиалкилена на полиалкиленгуанидине в качестве поверхностно-активных веществ и катионного полиэлектролита | 1990 |
|
SU1816769A1 |
| ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2006 |
|
RU2317950C1 |
| Дезинфицирующее средство | 1989 |
|
SU1687261A1 |
Область применения: стерилизация питьевой воды и обеззараживание питьевой воды в процессе водоподготовки в различных областях народного хозяйства. Сущность изобретения: для осуществления способа стерилизации питьевой воды ее пропускают через активированный уголь, предварительно обработанный солями полигексаметиленгуанидина с мол.м. 1 - 50 тыс. у. е., при этом соли полигексаметиленгуанидина и активированный уголь берут в массовом соотношении 0,02 - 0,2. Предлагаемый способ позволяет увеличить эффективность процесса стерилизации воды. 3 табл.
СПОСОБ СТЕРИЛИЗАЦИИ ПИТЬЕВОЙ ВОДЫ, включающий пропускание ее через активированный уголь, отличающийся тем, что активированный уголь предварительно обрабатывают солями полигексаметиленгуанидина с мол.м. 1 50 тыс. у.е. при этом соли полигексаметиленгуанидина и активированный уголь берут в массовом соотношении 0,02 0,2.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Патент США N 4898676, кл | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
Авторы
Даты
1995-05-10—Публикация
1993-07-20—Подача