Изобретение касается нового применения антипрогестомиметических соединений в скотоводстве.
Целью изобретения является применение антипрогестомиметических соединений для приготовления составов, предназначенных для синхронизации рождения у свиноматок.
В частности, предметом изобретения является применение соединений, обладающих антипрогестомиметической активностью, общей формулы (I)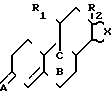 (I) где R1 углеводородный радикал, содержащий от 1 до 18 атомов углерода и могущий содержать один или несколько одинаковых или различных гетероатомов, соединенный со стероидным ядром атомом углерода;
(I) где R1 углеводородный радикал, содержащий от 1 до 18 атомов углерода и могущий содержать один или несколько одинаковых или различных гетероатомов, соединенный со стероидным ядром атомом углерода;
R2 углеводородный радикал с 1-8 атомами углерода;
Х остаток пятиугольного или гексагонального цикла, могущего быть замещенным и могущего содержать ненасыщенность; группировка С=А в положении 3-группировка оксо, свободная или блокированная в виде кеталя, группировка
C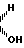 C
C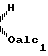 , C
, C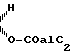 группировка C=NOH, группировка С=NOalc3 или группировка СН2, причем alc1, alc2 и alc3 радикал алкил с 1-8 атомами углерода или группировка аралкил с 7-15 атомами углерода и В и С образуют вместе двойную связь или эпоксидный мостик, также как и их аддитивные соли с кислотами.
группировка C=NOH, группировка С=NOalc3 или группировка СН2, причем alc1, alc2 и alc3 радикал алкил с 1-8 атомами углерода или группировка аралкил с 7-15 атомами углерода и В и С образуют вместе двойную связь или эпоксидный мостик, также как и их аддитивные соли с кислотами.
В частности, предметом изобретения является применение соединений, обладающих антипрогестомиметической активностью, которые отвечают формуле (I), где R1 углеводородный радикал с 1-18 атомами углерода, содержащий по меньшей мере один атом азота, фосфора или кремния, соединенный со стероидным ядром атомом углерода.
R2 предпочтительно насыщенный, прямолинейный или разветвленный радикал алкил с 1-4 атомами углерода, например радикал метил, этил, н-пропил или бутил.
Когда alc1, alc2 или alc3 радикал алкил, то предпочтительно касается радикала метил, этил, н-пропил или изобутил.
Когда alc1, alc2 или alc3 радикал аралкил, то предпочтительно касается радикала бензил.
Х предпочтительно остаток пятиугольного цикла, могущего быть замещенным.
Соединения формулы (I) являются известными соединениями и формулированы в европейском патенте N 0057115 и во французских патентах NN 2566779 [1] и 2625505 [2] где они представлены как обладающие различными свойствами, фармакологическими свойствами и, в частности, антипрогестомиметической активностью.
Некоторые продукты формулы (I), описанные и формулированные в заявке на французский патент N 8910648, поданной 8.08.89, еще не опубликованы; их получение дано ниже в опытной части.
Теперь открыто, что соединение формулы (I) обеспечивают замечательную синхронизацию рождения животных скотоводства, как это видно из результатов, данных ниже в опытной части.
После впрыскивания продукта подходящей дозы продукты формулы (I) приводят к рождению через меньше чем 36 ч и даже меньше чем 24 ч.
Предпочтительными соединениями являются продукты формулы (I), где В и С образуют вместе двойную связь, продукт формулы (I), где R2 радикал метил, продукт формулы (I), где группировка С=А группировка продукт формулы (I), где R1 радикал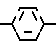 N
N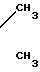 продукт формулы (I), где Х остаток цикла
продукт формулы (I), где Х остаток цикла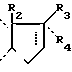 в котором R2 сохраняет предыдущее значение, R3 и R4 одинаковые или различные, либо атом водорода, либо радикал ОН, Оalc4, О-СОalc5, причем alc4 и alc5 радикалы алкил с 1-8 атомами углерода или аралкил с 7-15 атомами углерода, либо радикал алкинил или алкенил с 2-8 атомами углерода, либо радикал -
в котором R2 сохраняет предыдущее значение, R3 и R4 одинаковые или различные, либо атом водорода, либо радикал ОН, Оalc4, О-СОalc5, причем alc4 и alc5 радикалы алкил с 1-8 атомами углерода или аралкил с 7-15 атомами углерода, либо радикал алкинил или алкенил с 2-8 атомами углерода, либо радикал -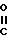 -CH2OH, либо радикал -COCH2OCOalc6, где alc6 радикал алкил с 1-8 атомами углерода, могущий быть замещенным, или радикал аралкил с 7-15 атомами углерода, либо радикал CO-CO2H, или CO-CO2alc7, где alc7 радикал алкил с 1-8 атомами углерода, либо радикал -
-CH2OH, либо радикал -COCH2OCOalc6, где alc6 радикал алкил с 1-8 атомами углерода, могущий быть замещенным, или радикал аралкил с 7-15 атомами углерода, либо радикал CO-CO2H, или CO-CO2alc7, где alc7 радикал алкил с 1-8 атомами углерода, либо радикал -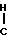 =O либо радикал -
=O либо радикал -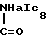 где alc8 радикал алкил с 1-8 атомами углерода или радикал аралкил с 7-15 атомами углерода, либо радикал -C=N, либо R3 и R4 образуют вместе радикал
где alc8 радикал алкил с 1-8 атомами углерода или радикал аралкил с 7-15 атомами углерода, либо радикал -C=N, либо R3 и R4 образуют вместе радикал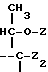
 где Z1 атом водорода, радикал алкил или радикал ацил с 1-8 атомами углерода и Z2 радикал алкил с 1-8 атомами углерода и, в частности, где Х остаток цикла
где Z1 атом водорода, радикал алкил или радикал ацил с 1-8 атомами углерода и Z2 радикал алкил с 1-8 атомами углерода и, в частности, где Х остаток цикла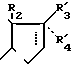 где R2 сохраняет данное выше значение и R31 радикал ОН, и R41 радикал алкинил или алкенил, содержащий до 4 атомов углерода.
где R2 сохраняет данное выше значение и R31 радикал ОН, и R41 радикал алкинил или алкенил, содержащий до 4 атомов углерода.
Среди предпочтительных аспектов изобретения можно назвать использование таких антипрогестомиметических соединений, как 17 бета-гидрокси-11 бета-(4-диметиламинофенил)-17 альфа-(1-пропинил)-эстра-4,9-диен-3-он (названный ниже продуктом А) или (Z) 11 бета-(4-диметиламинофенил)-17 бета-гидрокси 17 альфа-(1-пропинил)-эстра-4,9-диен-3-он, или 11 бета-(4-метилтиофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-иловый эфир янтарной кислоты, или одна из его щелочных солей, в частности соль натрия, или 11 бета-(4-диметиламинофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-иловый эфир янтарной кислоты, или одна из его щелочных солей, в частности соль натрия.
Получение упомянутых двух последних продуктов указано ниже в опытной части.
Особенно предметом изобретения является применение, согласно которому введение продукта осуществляют свиньям или коровам, или еще овцам, козам, кобылам.
Составы предпочтительно вводятся путем инъекций.
По предпочтительному методу 17 бета-гидрокси-11 бета-(4-диметиламинофенил)-17 альфа-(1-пропинил) эстра-4,9-диен-3-он вводится впрыскиванием свинье между 109 и 114 днем беременности дозы, находящейся между 1 мг и 3 мг на 1 кг веса животного, например 2 мг/кг от веса животного.
Примеры, приведенные ниже, поясняют изобретение, но не ограничивают его.
П р и м е р 1. Приготовление 1.
Соль натрия 11 бета-(4-диметиламинофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-илового эфира янтарной кислоты.
Стадия А.
Кислый сукцинат 11 бета-(4-диметиламинофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-ила.
Реакционная среда приготовляется прибавлением 2,15 кг янтарного ангидрида, 2,2 см3 триэтиламина и 215 мг 4-(диметиламино)-пиридина к раствору 2,15 г 11 бета-4-(диметиламинофенил)-17 бета-гидрокси 17 альфа-(1-пропинил)-эстра-4,9-диен-3-она в 22 см3 хлороформа, а затем нагревается с рефлюксом 42 ч, и прибавляют 430 мг 4-(диметиламино)-пиридина и 4,4 см3 триэтиламина. Рефлюкс продолжается 26 ч, и раствор тогда выливается на смесь вода лед. После декантации органического слоя этот последний промывается и сушится и хлороформ отгоняется, чтобы дать сухой экстракт коричневого цвета. Водный слой подкисляется 0,5 н. соляной кислотой, а затем нейтрализуется прибавкой ацетата натрия. Заново экстрагируют этиловым эфиром уксусной кислоты, и новая органическая фаза промывается водой, сушится и после отгонки растворителя приводит к остатку, который присоединяют к предыдущему. Продукт очищается на колонке двуокиси кремния, элюируя смесью эфир этиловый эфир уксусной кислоты (9-1) с 3% уксусной кислоты, и перекристаллизуется два раза в смеси эфир хлористый метилен. Получают 1,435 г целевого продукта. Т. пл. 165оС. (альфа) D +97o (к 0,8% в CHCl3).
Rf ≈0,40 (хроматография на тонком слое, основа: SiO2, элюент:эфир 9 этиловый эфир уксусной кислоты 1 уксусная кислота 3%).
Стадия Б.
Соль натрия 11 бета-(4-диметиламинофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-илового эфира янтарной кислоты.
В колбу, снабженную магнитной мешалкой, вводят 3 г полученного на стадии А продукта и 94 см3 этанола и наливают затем раствор 433 мг бикарбоната натрия в 94 см3 воды. После 30 мин перемешивания при комнатной температуре этанол пропускается через азеотропность, и оставшийся раствор отфильтровывается на миллипорной Rмембране (0,45 мкм) и лиофилизуется. Получают 2,88 г целевого продукта. (альфа)D + 48,5±1,5о (к 1% в воде).
Rf ≈0,54 (хроматография на тонком слое, основа: КС 18 ВатманR, элюент: метанол водный раствор ацетата аммония, 0,05 моль (80-20).
П р и м е р 2. Приготовление 2.
Соль натрия 11 бета-(4-метилтиофенил)-3-оксо-17 альфа-(1-пропинил)-экстра-4,9-диен-17 бета-илового эфира янтарной кислоты.
Стадия А.
Кислый 11 бета-(4-метилтиофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-иловый эфир янтарной кислоты.
В колбе, снабженной магнитной мешалкой и холодильником, смешивают 1,5 г 17 бета-гидрокси-11 бета-(4-метилтиофенил)-17 альфа-(1-пропинил)-эстра-4,9-диен-3-она и 15,3 см3 хлороформа, а затем вводят 1,86 г янтарного ангидрида, 6 см3 триэтиламина и 794 мг 4-(диметиламино)-пиридина и все это нагревают с рефлюксом 94 ч, выливают в 1 н. соляную кислоту и экстрагируют хлороформом. Хлороформовый слой промывается водой, сушится на сульфате натрия и растворитель удаляется под уменьшенным давлением при 40оС. Получают 2,26 г сырого продукта, который хроматографируют на колонке двуокиси кремния Кизельгура 60HR(элюент: хлористый метилен 97,5-метанол 2,5 уксусная кислота 1% ). После перекристаллизации в смеси хлористого метилена изопропилового эфира, образуется 826 мг кристаллов целевого продукта. Т. пл. 158оС.
Rf 0,61 (хроматография на тонком слое, основа: КС 18 ВатманR, элюент: метанол водный раствор ацетата аммония 0,05 моль (70-30).
Стадия Б.
Соль натрия 11 бета-(4-метилтиофенил)-3-оксо-17 альфа-(1-пропинил)-эстра-4,9-диен-17 бета-илового эфира янтарной кислоты.
Действуя как и в приготовлении 1, стадия Б, но исходя из раствора 108 мг бикарбоната натрия в 21,5 см3 воды и из 719 мг полученного на стадии А продукта в 21,5 см3 этанола, получают 720 мг лиофилизата, соответствующего целевому продукту. (альфа)D +74,5 ±1,5о (к 1% в воде). Rf 0,61 (хроматография на тонком слое, основа: КС 18 ВатманR, элюент: метанол водный раствор ацетата аммония, 0,05 моль (70-30).
Примеры фармакологических составов.
а) Были приготовлены растворы для впрыскивания, содержащие 150 мг 17 бета-гидрокси 11 бета-(4-диметиламинофенил)-17 альфа-(1-пропинил)-эстра-4,9-диен-3-она (продукт А).
б) Были приготовлены растворы для инъекции, содержащие 300 мг продукта А.
в) Были приготовлены растворы для инъекции, содержащие 600 мг продукта А.
г) Были приготовлены растворы для инъекции, содержащие 800 мг продукта А.
Опыт был произведен на самке свиньи. Свиньи были отобраны в зависимости от следующих критериев:
свиньи одного и того же происхождения (одна и та же схема селекции),
свиньи одного и того же опороса (3-го),
спаривание с одним и тем же боровом или искусственное оплодотворение с семенем одного и того же происхождения,
одинаковое число спариваний или оплодотворений,
спаривание или оплодотворение при первой поре спаривания после отнятия от груди (промежуток между отнятием от груди и порой спаривания одинаковый или очень близок),
одинаковая продолжительность кормления грудью.
Свиньи-самки разделяются на 3 следующие партии по "н" животных:
контрольная партия не получает никакого продукта,
одна партия получает внутримышечную инъекцию 2 мг/кг продукта А или 17 бета-гидрокси-1 бета-(4-диметиламинофенил)-17 альфа-(1-пропинил)-эстра-4,9-диен-3-она на 113 день периода беременности,
одна партия получает внутримышечную инъекцию 175 мкг клопростенола в виде ПЛАНАТАE на свинью на 113 день беременности.
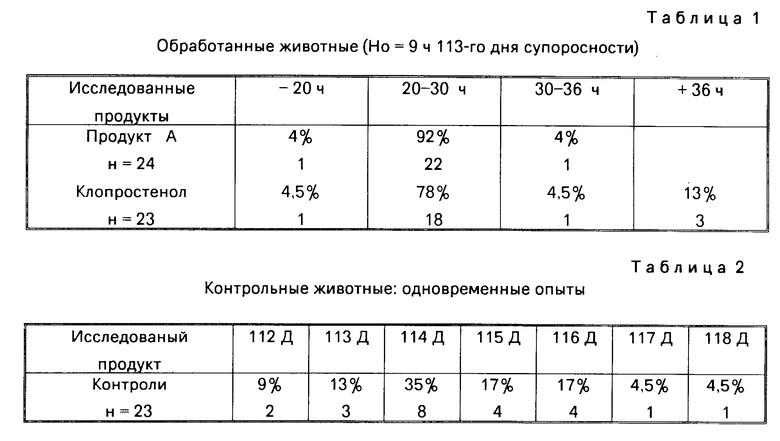
Было произведено измерение промежутка времени между впрыскиванием активного начала и рождением, табл. 1 и 2 дают в кратце полученные результаты.
Как следует из табл. 1 и 2 впрыскивание продукта А приводит к интересной синхронизации рождения, 92% обработанных животных рожают через 20-30 ч после введения продукта.
Использование: свиноводство. Сущность изобретения: соединения общей формулы (см. чертеж), где R1 - углеводородный радикал с 1 - 18 атомами углерода и могущий содержать один или несколько одинаковых или различных гетероатомов, соединенный со стероидным ядром атомом углерода; R2 - углеводородный радикал с 1 - 8 атомами углерода; X - остаток пятиугольного или гексагонального цикла, могущего быть замещенным и могущего содержать ненасыщенность; группировка C = A в положении 3-группировка оксо, свободная или блокированная в виде кеталя, группировка 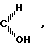
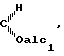
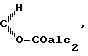 группировка C = NOH, группировка C = NOalC3 или группировка CH2, причем alC1, alc2 и alc3 -радикал алкил с 1 - 8 атомами углерода или группировка аралкил с 7 - 15 атомами углерода и B и C образует вместе двойную связь или эпоксидный мостик, также как и их аддитивные соли с кислотами, применяют в качестве средства для синхронизации рождаемости у свиноматок. Средство вводят свиноматкам в дозе 1 - 3 мг на 1 кг массы на 109 - 114 день супоросности. 92 % обработанных животных рожают через 20 - 30 ч после введения продукта. 2 с.п. ф-лы, 1 ил., 2 табл.
группировка C = NOH, группировка C = NOalC3 или группировка CH2, причем alC1, alc2 и alc3 -радикал алкил с 1 - 8 атомами углерода или группировка аралкил с 7 - 15 атомами углерода и B и C образует вместе двойную связь или эпоксидный мостик, также как и их аддитивные соли с кислотами, применяют в качестве средства для синхронизации рождаемости у свиноматок. Средство вводят свиноматкам в дозе 1 - 3 мг на 1 кг массы на 109 - 114 день супоросности. 92 % обработанных животных рожают через 20 - 30 ч после введения продукта. 2 с.п. ф-лы, 1 ил., 2 табл.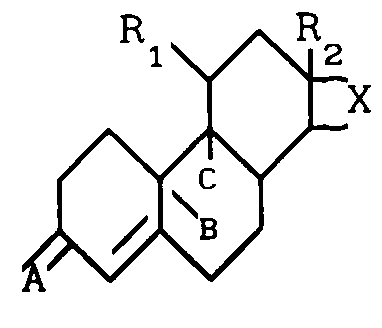
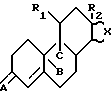
где R1 углеводородный радикал с 1 18 атомами углерода и могущий содержать один или несколько одинаковых или различных гетероатомов, соединенный со стероидным ядром атомом углерода;
R2 углеводородный радикал с 1 8 атомами углерода;
X остаток пятиугольного или гексагонального цикла, могущего быть замещенным и могущего содержать ненасыщенность;
группировка С А в положении 3 группировка оксо, свободная или блокированая в виде кеталя, группировка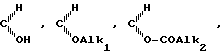
группировка C NOH, группировка C NOAlk3 или группировка CH2, причем Alk1, Alk2 и Alk3 C1 - C8-алкил или C7 C15-аралкил;
В и С образуют вместе двойную связь или эпоксидный мостик,
а также как и их адитивные соли с кислотами, в качестве средства для синхронизации рождаемости у свиноматок.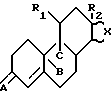
где R1 углеводородный радикал с 1 18 атомами углерода и могущий содержать один или несколько одинаковых или различных гетероатомов, соединенный со стероидным ядром атомом углерода;
R2 углеводородный радикал с 1 8 атомами углерода;
X остаток пятиугольного или гексагонального цикла, могущего быть замещенным и могущего содержать ненасыщенность, группировка С А в положении 3 группировка оксо, свободная или блокированная в виде кеталя, группировка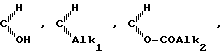
группировка C NOH, группировка C NOAlk3 или группировка CH2, причем Alk, Alk2 и Alk3 алкил с 1 8 атомамим углерода или группировка аралкил с 7 15 атомами углерода;
В и С образуют вместе двойную связь или эпоксидный мостик,
также, как и их аддитивные соли с кислотами, в дозе 1 3 мг на 1 кг массы животного на 109 114 день супоросности.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| The Huck Yndex an encyclopedio of chemicals, drugs, and biologicals, Ranway U.S.A., 1983, p.341. | |||
Авторы
Даты
1995-06-19—Публикация
1991-03-05—Подача