Настоящее изобретение относится к новым 19-норстероидам, имеющим в положении 11β- феноксиалкилсульфонамидную или феноксиалксилсульфонилкарбамидную цепь, к методу и к промежуточным продуктам их получения, и к содержащей их фармацевтической композиции.
Предметом настоящего изобретения являются соединения формулы (I):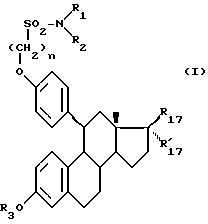
в которой R17 и R'17 таковы, что:
либо R17 и R'17 образуют вместе кетон;
либо R17 представляет собой гидроксильный радикал или ацилоксильный радикал, включающий не более 12 атомов углерода, а R'17 представляет собой атом водорода, алкильный, алкиленный или алкинильный радикал, включающий не более 8 атомов углерода, причем каждый из указанных радикалов может быть замещен;
R3 представляет собой атом водорода, линейный, разветвленный или циклический алкильный радикал, включающий не более 8 атомов углерода, или ацильный радикал, включающий не более 12 атомов углерода;
и в которой R1 и R2, одинаковые или различные, представляет собой атом водорода, линейный, разветвленный или циклический алкильный радикал, включающий от 1 до 8 атомов углерода, с возможностью замещения, ацильный радикал, включающий не более 12 атомов углерода, арильный или аралкильный радикал, причем каждый из указанных радикалов может быть замещен, в которых алкильный радикал включает не более 6 атомов углерода, а арильный радикал представляет собой моно или полициклический радикал, который может включать один или несколько гетероатомов, выбранных в группе, состоящей из атомов кислорода, азота и серы;
или R1 представляет собой карбамоильный радикал, монозамещенный линейным, разветвленным или циклическим алкильным радикалом, включающим не более 8 атомов углерода, с возможностью замещения, или же арильным или аралкильным радикалом, причем каждый из указанных радикалов может быть замещен, в которых алкильный радикал включает не более 6 атомов углерода, а арильный радикал представляет собой моно или полициклический радикал, который может включать один или несколько гетероатомов, выбранных в группе, состоящей из атомов кислорода, азота и серы, а R2 представляет собой атом водорода;
или R1 и R2 образуют с атомом азота, с которым они связаны, насыщенный азотированный 5-ти или 6-ти членный гетероцикл, содержащий второй гетероатом, выбранный в группе, состоящей из атомов азота, кислорода и серы, с возможностью замещения алкильным радикалом, включающим от 1 до 4 атомов углерода, или оксо-группой;
или R1 и R2 образуют диалкиламинометиленный радикал, причем каждый алкильный радикал включает от 1 до 4 атомов углерода, а n имеет целочисленное значение 18 или больше,
а также их аддитивные соли.
Под ацилоксильным радикалом понимают, в частности, радикал, соответствующий насыщенной или ненасыщенной алифатической или циклоалифатической кислоте и, в частности:
алкановой кислоте, такой как, например, уксусная, пропионовая, бутановая или изобутановая, валериановая или ундециленовая кислота;
гидроксиалкановой кислоте, такой как, например, оксиуксусная кислота;
циклоалкилкарбоновой или циклоалкилалкановой кислоте, такой как, например, циклопропиловая, циклопентил- или циклогексилкарбоновая, циклопентил- или цеклогексил- уксусная или пропионовая кислота; бензойной кислоте; салициловой или фенилалкановой кислоте, такой как фенилуксусная или фенилпропионовая кислота; аминокислоте, такой как диэтиламиноуксусная или диэтиламиноаспарагиновая; муравьиной кислоте или двухосновной кислоте с возможностью превращения в соль, такой как, например, бутандионовая кислота или ее мононатриевая соль. Речь идет, в первую очередь, о производном уксусной, пропионовой или бутановой кислоты.
Под ацильным радикалом понимают радикалы, соответствующие вышеуказанным радикалом.
Под алкильным радикалом понимают метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, трет-бутильный, n-пентильный, n-гексильный, 2-метилпентильный, 2,3-диметилбутильный, n-гептильный, 2-метилгексильный, 2,2-диметилпентильный, 3,3-диметилпентильный, 3-этилпентильный, n-октильный, 2,2-диметилгексильный, 3,3-диметилгексильный, 3-метил-3-этилпентильный. В первую очередь речь идет о метильном, этильном, пропильном, бутильном радикале.
Под циклоалкильным радикалом понимают такой радикал, как циклопропильный, циклобутильный, циклопентильный или циклогексильный. В первую очередь речь идет о циклопентильном радикале.
Когда R'17 представляет собой алкиленный радикал, речь может идти о таком радикале, как винильный, пропенильный, изопропенильный, аллильный, 2-метилаллильный, бутенильный или изобутенильный. В первую очередь речь идет о винильном или пропенильном радикале.
Когда R'17 представляет собой алкильный радикал, речь может идти о таком радикале, как этинильный, пропинильный, пропаргильный, бутинильный или изобутинильный. В первую очередь речь идет об этинильном или пропинильном радикале.
Под моноциклическим или полициклическим арильным радикалом, который может быть включен в аралкильный радикал, понимают:
моноциклический карбоциклический радикал, например фенильный радикал,
моноциклический гетероциклический радикал, например, такие радикалы как тиенильный, фурильный, пиранильный, пирролильный, имидазолильный, пиразолильный, пиридильный, пиразинильный, пиримидинильный, пиридазинильный, тиазолильный, оксазолильный, фуразанильный, пирролинильный, имидазолинильный, пиразолинильный, тиазолинильный, триазолильный, тетразолильный, а также изомеры положения гетероатома (гетероатомов), которые могут включать перечисленные радикалы,
радикал, состоящий из конденсированных карбоциклических циклов, например, нафтильный или фенантренильный радикал,
радикал, состоящий из конденсированных гетероциклических циклов, например, бензофуранил, бензотиенил, бензимидазолил, бензотиазолил, нафто [2,3-b] тиенил, тиантренил, изобензофуранил, хроменил, ксантенил, феноксатинил, индолизинил, изоиндолил, 3H-индолил, индолил, индазолил, пуринил, хинолизинил, изохинолил, хинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, птеридинил, карбазолил β- карболинил, акридинил, феназинил, фенотиазинил, феноксазинил, индолинил, изоиндолинил, имидазопиридил, имидазопиримидинил или же конденсированные полициклические системы, состоящие из гетероциклических моноциклов, таких, например, как указанные выше, например, фуро [2,3-b] пиррол или тиено [2,3-b] фуран, и в первую очередь фенильные радикалы, фурил, такой как 2-фурил, имидазолил, такой как 2-имидазолил, пиридил, такой как 2-пиридил, 3-пиридил, 4-пиридил, пиримидинил, такой как пиримид-2-ил, тиазолинил, такой как тиазол-2-ил, тиазолинил, такой как тиазолин-2-ил, триазолил, такой как триазол-2-ил, тетразолил, такой как тетразол-2-ил, бензимидазолил, такой как бензимидазол-2-ил, бензотиазолил, такой как бензатиазо-2-ил, пуринил, такой как пурин-7-ил, или хинолил, такой как 4-хинолил; а в качестве аралкильных радикалов можно, в частности, назвать метил или этил, замещенные одним из вышеперечисленных арильных радикалов.
Под насыщенным азотсодержащим гетероциклом с 5 или 6 атомами, который может включать второй гетероатом, выбранный среди атомов азота, кислорода и серы, с возможным замещением алкильным радикалом или карбонильной группой, понимают, в первую очередь, пирролидин, пиперидин, пиперазин, морфолин, тиаморфолин или имидазолидинон.
Заместители различных радикалов, перечисленных выше, выбирают, в первую очередь, в группе, состоящей из:
галогенного радикала, такого как фтор, хлор, бром, иод;
аминного, алкиламинного радикала, такого как метиламинный или этиламинный, диалкиламинного радикала, такого как диметиламинный, диэтиламинный, метилэтиламинный, причем каждый из указанных диалкиламинных радикалов может быть в окисленной форме;
аминоалкильного радикала, такого как аминометильный или аминоэтильный;
диалкиламиноалкильного радикала, такого как диметиламинометильный или диметиламиноэтильный;
диалкиламиноалкилоксильного радикала, такого как диметиламиноэтилоксильный;
гидроксильного радикала;
карбоксильного радикала, свободного, превращенного в сложный эфир, такого как алкоксикарбонильный, например, метоксикарбонильный или этоксикарбонильный, или превращенного в соль, например с помощью атома натрия или калия;
алкильного радикала, включающего от 1 до 8 атомов углерода, такого как метильный, этилпропильный, изопропильный, бутильный, изобутильный, трет-бутильный, с возможностью замещения одним или несколькими галогенными атомами, такими как, например, фтор, такой как трифторметил;
оксильного, цианильного, нитрильного, формильного радикала;
ацильного радикала, такого как ацетильный, пропионильный, бутирильный, бензоильный;
ацилоксильного радикала, такого как ацетоксильный или радикал формулы -O-CO-(CH2)nCO2H, в котором n имеет значение от 1 до 5;
алкоксильного, такого как метоксильный, этоксильный, пропилоксильный, изопропилоксильный, бутилоксильный;
алкилтионильного радикала, такого как метилтионильный, этилтионильный, пропилтионильный, изопропилтионильный, бутилтионильный;
карбамоильного радикала;
алкиленного радикала, такого как винильный, пропенильный;
алкинильного радикала, такого как этинильный, пропинильный, и
арильного радикала, такого как фенильный, фурильный, тиенильный.
В качестве примера подобных замещенных радикалов можно назвать, например, алкильный радикал, замещенный одним или несколькими галогенными атомами, например, такими как радикал фтор, такой как трифторметильный, трифторбутильный, пентафторпропильный, пентафторбутильный, пентафторпентильный, пентафторбутильный или нонафторбутильный, или, например, радикал хлор, такой как 2-хлорэтильный.
Можно также назвать, например, арильный радикал, замещенный одним или несколькими галогенными атомами, например, такими как радикал хлор, такой как 4-хлорфенильный.
Настоящее изобретение распространяется, естественно, на соли соединений формулы (I), например, на соли, образованные, когда соединения формулы (I) включают аминную функциональную группу, с помощью кислот, таких как хлористоводородная, азотная, серная, фосфорная, уксусная, муравьиная, пропионовая, бензойная, малеиновая, фумаровая, янтарная, винная, лимонная, щавелевая, глиоксиловая, аспарагиновая, бромистый водород, алкансульфоновые, такие как метансульфокислота или этансульфокислота, арилсульфоновые, такие как бензолсульфокислота или паратолуосульфокислота и арилкарбоновые, или, когда соединения формулы (I) включают аминную кислотную группу, с помощью солей щелочных или щелочноземельных металлов или аммония, с возможностью замещения.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как указано выше, отвечающие общей формуле (I'):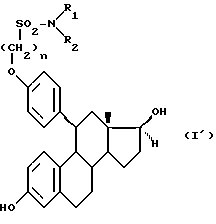
в которой R1 и R2, одинаковые или различные, представляют собой атом водорода, линейный, разветвленный или циклический алкильный радикал, включающий от 1 до 8 атомов углерода, с возможностью замещения, ацильный радикал, включающий не более 12 атомов углерода, или фенильный радикал, с возможностью замещения;
или R1 представляет собой карбамоильный радикал, монозамещенный линейным, разветвленным или циклическим алкильным радикалом, включающим не более 8 атомов углерода, с возможностью замещения, или же фенильным радикалом, с возможностью замещения, а R2 представляет собой атом водорода;
или R1 и R2 образуют с атомом азота, с которым они связаны, циклический карбамид типа
в котором n имеет значение 2 или 3,
или R1 и R2 образуют диметиламинометиленный радикал, n имеет значение, не превышающее 7, а также их добавляемые соли.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как определено выше, в которой R17 является гидроксильным радикалом, а R'17 является атомом водорода.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как определено выше, в которой n имеет значение 5 или 6.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как определено выше, в которой R1 и R2 представляют собой атом водорода.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как определено выше, в которой R1 и R2 представляют собой линейный, разветвленный или циклический алкильный радикал, включающий не более 8 атомов углерода, с возможностью замещения одним или несколькими галогенными атомами.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как определено выше, в которой R1 представляет собой атом водорода, а R2 является линейным, разветвленным или циклическим алкильным радикалом, включающим не более 8 атомов углерода.
Предметом настоящего изобретения являются, в частности, продукты общей формулы (I), как определено выше, в которой R1 представляет собой карбамоильный радикал, монозамещенный линейным, разветвленным или циклическим алкильным радикалом, включающим от 1 до 8 атомов углерода, или фенильным радикалом, причем каждый из указанных радикалов может быть замещен галогенными атомами, а R2 представляет собой атом водорода.
Предметом настоящего изобретения являются, в первую очередь, продукты формулы (I), как определено выше, имеющие нижеследующие наименования:
- N-бутил-5-[4-(3, 17β- дигидрокси-эстра-1,3,5 (10)-триен -11β- ил) фенокси]-пентансульфонамид,
- N-бутил-5-[4-(3, 17β- дигидрокси-эстра-1,3,5 (10)-триен -11β- ил) фенокси]-N-метилпентасульфонамид,
- 5-[4-(3, 17β- дигидрокси-эстра-1,3,5 (10)-триен -11β- ил) фенокси]-(2,2,3,3,4,4,4-гептафтурбутил)-N-метилпентасульфонамид.
Предметом настоящего изобретения является также метод получения соединений формулы (I), отличающийся тем, что соединение формулы (II):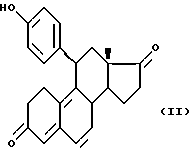
в которой фенольная функциональная группа может быть при необходимости защищена, подвергают:
а) либо воздействию галогенсодержащего производного формулы (III):
X-(CH2)n-SO2-NRAR'A
в которой X является галогенным атомом, n имеет вышеуказанное значение, RA и R'A, одинаковые или различные, представляют собой атом водорода, алкильный радикал, с возможностью замещения, ацильный радикал, арильный или аралкильный радикал, с возможностью замещения, причем следует иметь в виду, что хотя бы один из заместителей RA и R'A не является атомом водорода или что они образуют с атомом азота, с которым они связаны, насыщенный азотсодержащий гетероцикл с 5 или 6 атомами, который может включать второй гетероатом, выбранный среди атомов азота, кислородная и среды, с возможностью замещения алкильной группой, для получения продукта формулы (IV):
в которой n, RA и RA' имеют то же значение, что и раньше, который подвергают воздействию агента ароматизации цикла A, а затем, при необходимости, воздействию агента ацилирования гидроксильного радикала в положении 3 для получения продукта формулы (IA, соответствующего продукту формулы (I), в которой R1=RA и R2 = R'A: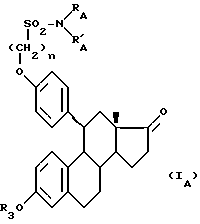
в которой n, RA и R'A имеют то же значение, что и раньше, а R3 представляет собой атом водорода или ацильную группу, продукт формулы (IA), при желании и в случае необходимости подвергают одной или нескольким из нижеследующих реакций, в соответствующем порядке:
восстановлению кетоновой функциональной группы в положении 17;
добавлению к кетоновой функциональной группе в положении 17 металлического комплексного соединения формулы (X):
M - R'17a (Х)
в которой M представляет собой атом металла, а R'17a имеет то же значение, что и R'17, за исключением атома водорода;
селективному ацилированию в положении 17, когда R17 является гидроксилом;
алкилированию или ацилированию гидроксильного радикала в положении 3;
омылению, когда R3 представляет собой ацильную функциональную группу;
возможному солеобразованию с помощью кислоты или основания.
б) либо воздействию агента ароматизации цикла A, и реакции защиты гидроксильного радикала в положении 3, а затем селективной реакции выделения защитной группы фенола в положении 11 для получения продукта формулы (V):
в которой Rр представляет собой защитную группу, который подвергают воздействию соединения формулы (III'):
X-(CH2)n-SO2-N=CH-N(Alk1)(Alk2), (III')
в которых X является галогенным атомом, Alk1 и Alk2 являются алкильными группами, включающими от 1 до 4 атомов углерода, а n имеет значение, не превышающее 18, а затем реакции гидролиза образовавшегося имина, для получения соединения формулы (VI):
в которой n и Rp имеют то же значение, что и раньше, и могут, в зависимости от характера группы Rp, соответствовать продукту формулы (I), продукт формулы (VI), который при желании и в случае необходимости подвергают одной или нескольким из нижеследующих реакций, в соответствующем порядке:
реакции выделения защитной группы Rp;
восстановлению кетоновой функциональной группы в положении 17;
добавлению к кетоновой функциональной группе в положении 17 металлического комплексного соединения формулы (X):
M-R'17a,
как указано выше;
селективному ацилированию в положении 17, когда R17 является гидроксилом;
алкилированию или ацилированию гидроксильного радикала в положении 3;
воздействию галогенида формулы (VII):
RB-X,
в которой RB является алкильным радикалом с возможностью замещения или ацильным радикалом, а X представляет собой галогенный атом, для получения соединения формулы (IB), соответствующего продукту формулы (I), в которой R1 = H и R2 = RB:
и в которой n, R17, R'17 и R3 имеют вышеуказанные значения;
воздействию изоцианата формулы (VIII):
Rc - NCO, (VIII)
в которой Rc является алкильным, арильным или аралкильным радикалом, причем каждый из радикалов может быть замещен для получения соединения формулы (Ic), соответствующего продукту формулы (I), в которой R1 представляет собой монозамещенный карбамоильный радикал, а R2 представляет собой атом водорода,
в которой n, R17, R'17 и R3 имеют вышеуказанные значения;
воздействию соединения формулы (IX):
(Alk3O)(Alk4O) CH-N(Alk1)(Alk2), (IX)
в которой Alk1, Alk2, Alk3 и Alk4 являются алкильными радикалами, включающими от 1 до 4 атомов углерода, для получения соединения формулы (ID), соответствующего продукту формулы (I), в которой R1 и R2 образуют диалкиламинометиленную группу: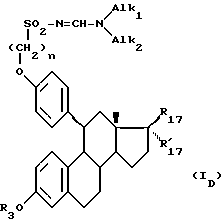
и в которой n, R17, R'17 и R3 имеют вышеуказанные значения;
алкилированию или ацилированию продукта формулы (IB) путем воздействия галогенидом (VII) для получения соответствующего диалкилированного, диацилированного или алкилацилированного сульфонамида;
реакции циклизации продукта формулы (Ic), когда Rc представляет собой радикал -(CH2)n-Hal, в котором n' равен 2 или 3, а Hal представляет собой галогенный атом, для получения продукта формулы (I'c), соответствующего продукту формулы (I), в которой R1 и R2 образуют вместе с азотом, с которым они связаны, циклический карбамид типа
возможному солеобразованию с помощью кислоты или основания.
Соединения формулы (IA), соответствующие соединения (I), в которой R1=RA и R2 = R'A, получают путем последовательного ввода соединения формулы (II) в реакцию c:
а) соединением формулы (III) в присутствии сильного основания, такого как гидрид натрия, в двухполюсном апротонном растворителе, таком как диметилформамид, действуя, например, при комнатной температуре, для получения промежуточного соединения формулы (IV);
б) ароматизирующим веществом, таким как смесь ацетилбромида и уксусного ангидрида, с последующей реакцией легкого омыления в присутствии, например, едкого кали в метаноле или едкого натра в метаноле.
Соединения формулы (VI) получают путем последовательного ввода в реакцию соединения формулы (II), в которой фенол в положении 11 может быть защищен, c:
а) ароматизирующим веществом, таким как гидроокись палладия на окиси магния в метаноле, с последующей реакцией защиты гидроксильной функциональной группы в положении 3 путем воздействия, например, хлорбензилом в присутствии карбоната калия в ацетоне, действуя при температуре кипения в течение 7 часов, после чего выполняется реакция селективной депротекции фенольной функциональной группы в положении 11, например путем легкого омыления в присутствии, например, едкого кали в метаноле или едкого натра в метаноле для получения промежуточного соединения формулы (V);
б) соединением формулы (III') в присутствии сильного основания, такого как гидрид натрия, в двухполюсном апротонном растворителе, таком как диметилформамид;
в) веществом для кислого гидролиза имина, образовавшегося на предыдущем этапе, таким как, например, хлористоводородная кислота в смеси метанола и тетрагидрофурана.
Соединения формулы (IB), соответствующие соединениям формулы (I), в которой R1 = H и R2 = RB, получают путем ввода соединения формулы (VI), в которой ORp является гидроксилом, защищенным, например, аралкильным радикалом, в реакцию с соединением формулы (VII), причем реакция выполняется, например, в присутствии едкого натра в ацетоне при температуре кипения или же в присутствии гидрида натрия в диметилформамиде при комнатной температуре.
Второе алкилирование или ацилирование может производиться в тех же условиях.
Соединения формулы (Ic), соответствующие соединениям формулы (I), в которой R1=H и R2=CONH-Rc, получают путем ввода соединения формулы (VI), в которой защитная группа гидроксильной функциональной группы в положении 3 выделяется, а кетоновая функциональная группа в положении 17 восстанавливается, в реакции с соединением формулы (VIII), причем реакция выполняется в присутствии сильного основания, такого как гидрид натрия, в двухполюсном апротонном растворителе, таком как диметилформамид, действуя, например, при комнатной температуре.
Когда Rc представляет собой радикал типа -(CH2)n'-Hal, в котором n' равен 2 или 3, на месте происходит реакция циклизации, что объясняется высокой основностью среды, для получения соединений формулы (I'c).
Соединения формулы (ID), соответствующие продуктам формулы (I), в которой R1 и R2 образуют диалкиламинометиленную группу, получают путем ввода соединения формулы (VI), в которой защитная группа гидроксильной функциональной группы в положении 3 выделяется, а кетоновая функциональная группа в положении 17 восстанавливается, в реакцию с соединением формулы (IX), причем реакция выполняется, например, в диметилформамиде при комнатной температуре.
Когда соединение формулы (I) содержит в положении 17 кетоновую функциональную группу, получают:
соответствующее гидроксилированное соединение 17-17-β, , например, путем воздействия восстановителем, таким как боргидрид натрия в нейтральном растворителе, таком как метанол;
соответствующее соединение, содержащее радикал R'17, представляющий собой алкильный, алкиленный или алкильный радикал, с возможностью замещения, путем добавления соединения формулы (X), такого, например, как комплексное соединение лития, в соответствии с методом, описанном в патенте ЕЭС EP 57115.
Разумеется, что если R'17, представляет собой алкильный, алкиленный или алкинильный радикал, с возможностью замещения функциональной группой, то последняя может быть временно защищена обычными методами.
Когда соединение формулы (I) содержит в положении 3 гидроксилированную группу, то получают соответствующий алкилированный стероид, используя для этого алкилирующий реактив, такой как соответствующий алкилиодид или алкилсульфат, например, метилсульфат или соответствующий ацилированный стероид, используя для этого обычный ацилирующий реактив, такой как ацилгалогенид, например, ацетилхлорид.
Когда соединение формулы (I) содержит в положении 17-β функциональную гидрокси-группу, то получают соответствующий 17-β ацилоксилированный стероид, используя для этого реактив для селективного ацилирования, например, уксусный ангидрид в пиридине, возможно в присутствии 4-диметиламинопиридина, или любой другой метод, хорошо известный специалистам.
Защитные группы, которые можно использовать для защиты функциональных групп, таких, например, как функциональная гидрокси-группа, выбирают среди обычных групп, хорошо известных в органической химии и, в частности, в химии пептидов. Неисчерпывающий перечень указанных функциональных групп, а также описание соответствующих методов выделения приводится во французском патенте FR 2499995, содержание которого приводится для справки в настоящей патентной заявке, а также в статье "Защитные группы в органическом синтезе" (GREENE и WUTS (1991 г.), изд. WILEY).
В качестве примера, для защиты фенола в положении 11 соединения формулы (II) можно назвать такие радикалы, как ацетильный, бензоильный или трет-бутилдиметилсилильный.
В качестве примера, для защиты гидроксила в положении 3 соединений формул (V) и (VI) можно назвать такие радикалы, как ацетильный, бензоильный или бензильный.
Например, реакция защиты гидроксила в положении 3 бензильной группой может осуществляться путем воздействия хлорбензила в присутствии сильного основания, такого как гидрид натрия, в двухполюсном апротонном растворителе, таком как диметилформамид, действуя при комнатной температуре, или же путем воздействия бензилбромида в присутствии менее сильного основания, такого как карбонат калия в ацетоне при температуре кипения. Интерес подобной защиты заключается в том, что она устойчива к реакции гидролиза или омыления.
Когда промежуточные соединения включают защищенные функциональные группы, соответствующее соединения со снятой защитой получают путем воздействия обычными агентами депротекции. Неисчерпывающий перечень указанных функциональных групп, а также описание соответствующих методов выделения приводится во французском патенте FR 2499995, содержание которого приводится для справки в настоящей патентной заявке, а также в статье "Защитные группы в органическом синтезе" (GREENE и WUTS (1991 г.), изд. WILEY).
Чисто для справки можно сказать, что когда фенол защищен ацетильной функциональной группой, реакция выделения указанной защитной группы может производиться с помощью омылителя, такого как едкое кали в спиртовой среде.
Когда фенол защищены трет-бутилдиметилсилильной группой, реакция выделения указанной защитной группы может производиться с помощью гидролизирующего вещества, такого как хлористоводородная кислота.
Когда функциональная гидрокси-группа в положении 3 защищена бензильной группой, реакция выделения указанной защитной группы может производиться методом гидрогенолиза путем воздействия, например, водородом в присутствии палладий-катализатора на активированном угле в смеси этилацетата, этанола и уксусной кислоты.
В предпочтительном способе исполнения настоящего изобретения:
используются соединения формулы (III), в которой X является, в первую очередь, атомом иода;
используются соединения формулы (III'), в которой X является, в первую очередь, атомом иода;
используются соединения формулы (VII), в которой X является, в первую очередь, атомом иода, в случае если RB является алкильным радикалом, и атомом хлора, в случае если RB является ацильным радикалом.
Настоящее изобретение распространяется также на метод, описанный выше, отличающийся тем, что на начальном этапе используют соединение, соответствующее соединению формулы (II), содержащему в положении 17 заменителя R17 и R'17, как определено выше.
Само собой разумеется, что при внедрении подобного метода, и как описано выше для радикала R'17, может появиться необходимость в промежуточных защитных группах радикалов R17 и R'17. Указанные защитные группы описаны выше. Вышеуказанные исходные продукты известны, например, из опубликованного патента ЕЭС N 0384482, или могут быть приготовлены методами, описанными в настоящей патентной заявке, на основе продуктов 17-оксо.
Соединения формулы (I) обладают интересными фармакологическими свойствами.
Исследование продуктов на гормональных рецепторах позволило выявить, что:
- соединения формулы (I) обладают глюкокортикоидной или антиглюкокортикоидной, прогестомиметической или антипрогестомиметической, андрогенной или ангиандрогенной, антиминералокортикоидной, эстрогенной или антиэстрогенной активностью.
Соединения формулы (I) обладают, в частности, исключительной антиэстрогенной активностью и антипролиферирующими свойствами, как явствует из приведенных далее результатов проведенных тестов.
Указанные свойства позволяют использовать соединения формулы (I) для борьбы с побочными эффектами глюкокортикоидов; они позволяют также бороться с нарушениями, вызванными повышенной секрецией глюкокортикоидов и, в частности, со старением вообще и, более конкретно, с гипертонией, замедленным зарубцовыванием, атеросклерозом, остеопорозом, диабетом, ожирением, а также ослаблением иммунитета и с бессоницей.
Указанные продукты могут также представлять интерес при лечении некоторых видов опухолей, экспримирующих гормональные рецепторы, в отношении которых продукты формулы (I) представляют сродство.
Соединения формулы (I), обладающие антипрогестомиметическими свойствами, могут использоваться при приготовлении оригинальных противозачаточных средств, в качестве средств для прерывания беременности или в качестве средства рабочей индукции.
Указанные продукты могут также использоваться в качестве средства для вызова менструации у женщин и вообще у самок теплокровных животных.
В этом случае указанные продукты вводятся в периоды, во время которых прогестерон играет важнейшую физиологическую роль, то есть, в частности, во время лютеальной фазы цикла, во время нидации (или импрегнации оплодотворенной яйцеклетки) и в период беременности. Противозачаточный метод согласно настоящему изобретению заключается во введении женщине как минимум одного из продуктов формулы (I) в течение 1 - 5 дней преимущественно в конце цикла. В этом случае указанный продукт вводится предпочтительно внутрь или во влагалище, однако он может также приниматься парентеральным путем. Вводить продукты возможно также внутриносовым путем.
Продукты формулы (I), обладающие антипрогестимиметическими свойствами, могут также использоваться при лечении гормональных нарушений и, к тому же, они могут представлять интерес при лечении гормонозависимых опухолей.
Их действие на гипофизарную секрецию позволяют использовать указанные продукты во время менопаузы.
Указанные продукты могут также использоваться для синхронизации менструального цикла и синхронизации родов у домашнего скота, в частности у крупного и мелкого рогатого скота.
Указанные продукты могут также использоваться для контроля фертильности домашних животных, таких как собаки и кошки.
Соединения формулы (I) могут быть также обладать прогестомиметическими свойствами и поэтому могут использоваться при лечении аменореи, дисменореи и лютеальной недостаточности.
Соединения формулы (I), обладающие антиандрогенными свойствами, могут использоваться при лечении гипертрофии и рака простаты, гиперандрогении, анемии, гирсутизма и акне. Они могут также использоваться в качестве противозачаточных средств для человека.
Соединение формулы (I), обладающие экстрогенными свойствами, могут также использоваться при лечении нарушений, связанных с гипофолликулинемией, например аменореи, дисменореи, повторяющихся абортов, предменструальных расстройств, а также для лечения менопаузы и остеопороза.
Антиэкстрогенные и антипролиферирующие свойства соединений формулы (I) позволяют их использовать при лечении гормонозависимых карцином, таких как, например, карцинома молочной железы и ее метастазы, а также при лечении доброкачественных опухолей молочной железы.
Таким образом, предметом настоящего изобретения являются соединения формулы (I), а также, в качестве медикаментов, их добавляемые соли, допустимые с фармакологической точки зрения.
Среди медикаментов, являющихся предметом настоящего изобретения, можно назвать, в частности, соединения, описание которых приводится в экспериментальной части, и, в первую очередь, продукты Примеров 2, 7 и 8.
Полезная дозировка медикаментов зависит от заболевания, которое предстоит лечить, а также от способа их приема; она может колебаться, например, от 1 до 100 мг в день для взрослых при приеме внутрь.
Изобретение распространяется на фармацевтические соединения, которые включают, в качестве действующего начала, как минимум один из определенных выше медикаментов.
Соединения формулы (I) вводятся через пищеварительный канал, парентеральным путем или локально, например, подкожным путем. Они могут предписываться в виде простых или дражевидных таблеток, капсул, гранул, суппозиториев, шариков, препаратов для инъекций, мазей, кремов, гелей, микросфер, имплантатов, патчей, приготовленных традиционными методами.
Действующее начало (действующие начала) может вводиться в основы, обычно используемые при изготовлении фармацевтических составов, такие как тальк, аравийская камедь, лактоза, амидон, стеарат магния, какао-масло, водные или безводные связующие, жиры животного или растительного происхождения, производные парафина, гликоли, различные увлажняющие, диспергирующие или эмульсионные агенты, консерванты.
Соединения формул (IV), (V) и (VI) представляют собой новые промежуточные продукты и поэтому предметом настоящего изобретения, в качестве новых промышленных продуктов и, в частности в качестве промежуточных продуктов для внедрения метода изобретения, являются соединения формул (IV), (V) и (VI).
Среди новых промежуточных продуктов, являющихся предметом настоящего изобретения, можно назвать продукты, получение которых описывается ниже, в экспериментальной части:
- N-бутил-5-[4-(3,17-диоксо-эстра-4,9-диен -11β- ил)фенокси]-N- метилпентансульфонамид,
- 5-[4-(3,17-диоксо-эстра-4,9-диен -11β- ил)фенокси]-N- (2,2,3,3,4,4,4-гептафторбутил)-N-метилпентансульфонамид,
- 11β- (4-гидроксифенил)-3-[(фенилметил)окси]-эстра-1,3,5(10)- триен-17-он,
- 5-[4-(17-оксо-3-[(фенилметил)окси] -эстра-1,3,5(10)-триен-11β- ил]фенокси]-пентансульфонамид.
Соединение формулы (I), необходимое для внедрения метода, описывается, в частности, в патентной заявке ЕЭС EP 0 384 842 (Приготовление Примера 43).
Далее, в экспериментальной части, приводятся примеры приготовления продуктов формул (III) и (III'). Указанные соединения, как правило, уже известны и их приготовление осуществляется с использованием методов, аналогичных методам, описанным в экспериментальной части.
Приводимые далее примеры иллюстрируют изобретение, вместе с тем не ограничивая его.
Приготовление 1: N-[(диметиламино)метилен]-5- иодпентансульфонамид
Этапа: 5-хлорпентансульфонамид
В среде инертного газа в раствор 2,5 г 5-хлорпентансульфонилхлорида (получение описано в статье: Bull. Soc. Chim. Belg. (1965) 74 21) в 30 тетрагидрофурана при температуре 0/+5oC добавляют по капле 2,5 мл 28-процентного водного раствора аммония. Затем температуре дают подняться от +3oC до +16oC и взбалтывают при комнатной температуре в течение 2 ч. После этого тетрагидрофуран выпаривают при пониженном давлении, забирают в воде, экстрагируют с использованием метиленхлорида, промывают водой, а затем водным раствором хлорида натрия, высушивают и выпаривают при пониженном давлении. Таким образом получают 2,01 г искомого продукта (tпл 62oC).
Инфракрасный спектр: Трихлорметан (CHCl3)
-NH2 - 3448 см-1 - 3352 см-1
-SO2- - 1344 см-1 - 1150 см-1
-NH2 - 1545 см-1
Этап Б: 5-хлор-N-[(диметиламино)метилен]-пентансульфонамид
В среде инертного газа в раствор 1,5 г продукта, полученного на предыдущем этапе, в 8 мл диметилформамида при комнатной температуре добавляют по капле 1,29 мл N,N-диметилформамиддиметилацеталя. Затем раствор взбалтывают при комнатной температуре в течение 3 ч, после чего вливают в 1-процентный водный раствор гидрогеносульфата натрия, экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 1,809 г искомого продукта.
Инфракрасный спектр: (CHCl3)
-N=CH-N< - 1629 см-1
-SO2- - 1349 см-1 - 1119 см-1
Этап В: N-[(диметиламино)метилен]5-иодпентансульфонамид
В раствор 2,09 г продукта, полученного на предыдущем этапе, в 31,5 мл метилэтилкетона (МЭК) добавляют 2,98 г иодида натрия, после чего доводят за 4 ч до температуры кипения. После охлаждения добавляют воды, экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 2.69 г целевого продукта.
Инфракрасный спектр: (CHCl3)
-N=CH-N< - 1629 см-1
Приготовление 2: N-бутил-5-иод-N-метилпентансульфонамид
Этап А: N-бутил-5-хлор-N-метилпентансульфонамид
В среде инертного газа в раствор 410 мг 5-хлорпентансульфонилхлорида в 10 мл метиленхлорида добавляют 0,47 мл N-бутилметиламина. Затем температуре дают подняться от +13oC до +26oC и, полсле охлаждения до 0/+5oC, добавляют 0,55 мл триэтиламина и взбалтывают в течение 2 ч при комнатной температуре. После этого раствор вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием метиленхлорида, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 486 мг целевого продукта.
Инфракрасный спектр: (CHCl3)
-SO2-N< - 1334 см-1 - 1142 см-1
Этап Б: N-бутил-5-иод-N-метилпентансульфонамид
В раствор 449 мг продукта, полученного на предыдущем этапе, в 4,5 мл метилэтилкетона добавляют 526 мг иодида натрия и взбалтывают в течение 4 ч при температуре кипения. После охлаждения и выпаривания метилэтилкетона при пониженном давлении добавляют воды, экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 572 мг целевого продукта.
Инфракрасный спектр: (CHCl3)
-SO2-N< - 1334 см-1 - 1141 см-1
Приготовление 3: N-(2,2,3,3,4,4,4-гептафторбутил)-5-иод-N- метилпентансульфонамид
Этап А: 5-хлор-N-(2,2,3,3,4,4,4-гептафторбутил)-N- метилпентансульфонамид
В раствор 200 мг 5-хлорпентансульфонилхлорида в 5 мл метиленхлорида добавляют 500 мг N-(2,2,3,3,4,4,4-гептафторбутил)-N-метиламинхлоргидрата, полученного согласно патенту ЕЭС 384842 - Пример 75, а затем, при температуре 0/+5oC, 0,55 мл триэтиламина, после чего взбалтывают в течение 2 ч при комнатной температуре. Затем добавляют воды, экстрагируют с использованием метиленхлорида, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 378 мг искомого продукта.
Инфракрасный спектр: (CHCl3)
-SO2-N< - 1354 см-1 - 1341 см-1 - 1148 см-1
Примесь C = O - 1730 см-1
Этап Б: N-(2,2,3,3,4,4,4-гептафторбутил)-N-иод-N- метилпентансульфонамид
В раствор 355 мг продукта, полученного на предыдущем этапе, в 3 мл метилэтилкетона добавляют 300 мг иодида натрия, после чего доводят за 4 ч до температуры кипения. После выпаривания растворителя остаток забирают в воде и экстрагируют с использованием этилацетата. Затем промывают водным раствором тиосульфата натрия, а затем хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 425 мг целевого продукта в виде бесцветной вязкой жидкости, которая медленно кристаллизуется.
Инфракрасный спектр: (CHCl3)
N-SO2- - 1354 см-1 - 1341 см-1 - 1148 см-1
Приготовление примера 1: 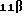 -[4-гидроксифенил)-3-[(фенилметил) окси]-эстра-1,3,5(10)-триен-17-он
-[4-гидроксифенил)-3-[(фенилметил) окси]-эстра-1,3,5(10)-триен-17-он
Этап А: 11β -[4-бензоилокси)фенил]-эстра-4,9-диен-3,17-дион
В среде инертного газа в раствор 8,758 г 11β- -(4-гидроксифенил)-эстра-4,9-диен-3,17-дион, полученного согласно патенту ЕЭС 384842 - Пример 43, в 92 мл ацетона и 27 мл водного раствора едкого натра (молярная концентрация = 1 моль/л) добавляют по капле, при температуре 0/+5oC, 3 мл бензоилхлорида. В конце введения бензоилхлорида наблюдается осаждение бензоата; взвесь следует взбалтывать в течение 10 мин в ледяной ванне, а затем 30 мин при комнатной температуре. После этого смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 0,1 моль/л), экстрагируют с использованием этилацетата, промывают насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 12,98 г сырого продукта, который кристаллизуют из смеси метиленхлорида и простого изопропилового эфира. В результате получают 9,93 г искомого продукта (tпл 196oC).
Инфракрасный спектр: (CHCl3)
> C = O в положении 17 + кетон Ar-O-CO-Ph - 1736 см-1 (F)
Сопряженный кетон - 1659 см-1 - 1602 см-1
C = C ароматич. - 1505 см-1 - 1490 см-1
Этап Б: 11β- [4-(бензоилокси)фенил]-3-гидрокси-эстра-1,3,5 (10)-триен-17-он
В раствор 10,07 мг продукта, полученного как указано на предыдущем этапе, в 104 мл метанола добавляют 10,1 г 20-процентной гидроокиси палладия на магнии. Затем нагревают при температуре кипения в течение 1 ч 30 мин. После охлаждения взвесь фильтруют, промывают нерастворимый катализатор смесью метиленхлорида и метанола (50 : 50) и выпаривают досуха фильтрат при пониженном давлении. остаток (10,72 г) подвергают хроматографии на двуокиси кремния (элюант : этилацетат-циклогексан (40 : 60)). В результате получают 7,72 г искомого продукта (tпл 265oC).
Инфракрасный спектр: (CHCl3)
-OH - 3599 см-1
> C = O - 1733 см-1 (F) - 1611 см-1 - 1602 см-1
C = C ароматич. - 1585 см-1 - 1508 см-1
Этап В: 11β- [4-(бензоилокси)фенил] -3-[(фенилметил)окси] - эстра-1,3,5(10)-триен-17-он
В раствор 6,462 мг продукта, полученного на предыдущем этапе, в 110 мл ацетона добавляют 3,82 г карбоната калия и 4,9 мл бромбензила (Fluka A007832). Затем нагревают за 7 ч до температуры кипения, а затем, после охлаждения, выпаривают досуха при пониженном давлении. Остаток забирают в этилацетате и вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 0,5 моль/л), повторно экстрагируют с использованием этилацетата и промывают насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Остаток (12,2 г) подвергают хроматографии на двуокиси кремния (элюант : этилацетат-циклогексан (25 : 75)). В результате получают 6,68 г искомого продукта.
Инфракрасный спектр: (CHCl3)
> C = O - 1734 см-1 комплекс. - 1604-1608 см-1 - 1586 см-1
C = C ароматич. - 1576 см-1 - 1508 см-1 - 1501 см-1
Этап Г: 11β- (4-гидроксифенил)-3-[(фенилметил)окси]- эстра-1,3,5(10)-триен-17-он
В раствор 6,64 мг продукта, полученного на предыдущем этапе, в 87,5 мл метанола и 87,5 мл тетрагидрофурана добавляют 12 мг водного раствора едкого натра (молярная концентрация = 2 моль/л). Затем раствор взбалтывают в течение 1 ч при комнатной температуре и вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 0,5 моль/л). После этого экстрагируют с использованием этилацетата, промывают водой, после этого насыщенным водным раствором бикарбоната натрия, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 6,52 г искомого сырого продукта, который подвергают кристаллизации из метиленхлорида. В результате получают 4,62 г целевого продукта (tпл 240oC).
Инфракрасный спектр: (CHCl3)
-OH - 3600 см-1
> C = O - 1733 см-1 - 1613 см-1 - 1594 см-1
C = C ароматич. - 1574 см-1 - 1513 см-1 - 1500 см-1
Пример 1: 5-[4-(3, 17β- дигидрокси-эстра-1,3,5(10)-триен- 11β -ил)фенокси]-пентансульфонамид
Этап А: N-(диметиламино)метилен]-5-[4-[17-оксо-3- [(фенилметил)окси]-эстра-1,3,5(10)-триен- -11β- ил]фенокси]-пентансульфонамид
В среде инертного газа во взвесь 2,92 г продукта, полученного на Этапе Г Приготовления Примера 1, в 69 мл диметилформамида и 403 мг гидрида натрия в 50% масла, после взбалтывания в течение 25 мин добавляют раствор 2,67 г продукта, полученного в Приготовлении 1 (Этап В), в 25 мл диметилформамида. Затем взвесь нагревают до +50oC и по истечении 10 мин получают раствор, который выдерживают при взбалтывании при указанной температуре в течение 1 ч 15 мин. Затем раствор охлаждают до комнатной температуры и вливают в 1-процентный водный раствор гидрогеносульфата натрия, экстрагируют с использованием этилацетата, промывают водой, после этого насыщенным раствором тиосульфата натрия, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Остаток (6,75 г) подвергают хроматографии на двуокиси кремния (элюант : этилацетат). В результате получают 3,82 г искомого продукта.
Инфракрасный спектр: (CHCl3)
> C = O в положении 17 - 1733 см-1 комплекс.
-N=CH- - 1629 см-1 - 1612 см-1 (площадка) - 1575 см-1
C = C ароматич. - 1512 см-1 - 1500 см-1
-SO2- - 1349 см-1
Этап Б: 5-[4-[17-оксо-3-[(фенилметил)окси]-эстра- 1,3,5(10)-триен- -11β- ил]фенокси]-пентансульфонамид
В среде инертного газа во взвесь 3,818 г продукта, полученного на предыдущем этапе, в 59 мл метанола и 28 мл тетрагидрофурана добавляют 17,7 мл чистой концентрированной хлористоводородной кислоты при 22oБ. Смесь нагревают при температуре +80oC в течение 1 ч 30 мин, а затем, после охлаждения, вливают в насыщенный водный раствор бикарбоната натрия, экстрагируют с использованием этилацетата и промывают насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Остаток (4,15 г) подвергают хроматографии на двуокиси кремния (элюант : этилацетат/циклогексан (60 : 40)). В результате получают 2,89 г искомого продукта.
Инфракрасный спектр: (CHCl3)
-NH2 - 3444 см-1 - 3350 cv-1
> C = O в положении 17 - 1733 см-1 - 1610 см-1
C = C ароматич. - 1580 см-1
+
-NH2 - 1545 см-1
Этап В: 5-[4-[ 17β- гидрокси-3-[(фенилметил)окси]-эстра- 1,3,5(10)-триен- -11β- ил]фенокси]-пентансульфонамид
В среде инертного газа в раствор 1,36 г продукта, полученного на предыдущем этапе, в 6 мл метанола и 6 мл тетрагидрофурана при температуре 0o/+5oC добавляют 169 мг гидрида бора и натрия. После взбалтывания в течение 1 ч при температуре 0o/+5oC смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным раствором хлористого натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 1,299 г искомого сырого продукта, который подвергают кристаллизации из смеси метиленхлорида и простого изопропилового эфира. В результате получают 1,295 г целевого продукта (tпл 146oC).
Инфракрасный спектр: (CHCl3)
-OH - 3609 см-1
-NH2- - 3444 см-1 - 3353 см-1 - 1609 см-1
C = C ароматич. - 1580 см-1 - 1512 см-1 - 1500 см-1
-NH2 - 1544 см-1
Этап Г: 5-[4-[3, 17β- дигидрокси-эстра- 1,3,5(10)-триен- 11β- ил]фенокси]-пентансульфонамид
В раствор 1,295 г продукта, полученного на предыдущем этапе, в 50 мл этанола и 5 мл уксусной кислоты добавляют 161 мг 10-процентного палладия на активированном угле (тип E 10N, Degussa), после чего взбалтывают в течение 2 ч при давлении 1640 мбаров водорода. Затем фильтруют, промывают смесью метанола и метиленхлорида (1 : 1), выпаривают досуха при пониженном давлении и отгоняют уксусную кислоту толуолом. Таким образом получают 1,04 г сырого искомого продукта, который подвергают кристаллизации из этанола. В результате получают 736 мг целевого продукта (tпл 175oC).
Инфракрасный спектр: (Вазелиновое масло)
Комплексное поглощение в области OH/NH: - 1616 см-1
C = C ароматич. - 1580 см-1
+
-NH2 - 1511 см-1
-SO2 - 1333 см-1 - 1153 см-1
Пример 2: N-бутил-5-[4-[3, 17β- дигидрокси-эстра- 1,3,5(10)-триен- 11β- ил]фенокси]-пентансульфонамид
Этап А: N-бутил-5-[4-[17-оксо-3-[(фенилметил)окси] - эстра-1,3,5(10)-триен- β ил]фенокси]-пентансульфонамид
В среде инертного газа в раствор 500 мг продукта, полученного на Этапе Б Примера 1, в 6,5 мл ацетона и 0,96 мл водного раствора едкого натра (молярная концентрация = 1 моль/л) добавляют 0,188 мл 1-иодбутана. Затем взбалтывают при температуре кипения в течение 52 ч и охлаждают перед выпариванием ацетона при пониженном давлении. После этого забирают в этилацетате и вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 0,5 моль/л), экстрагируют с использованием этилацетата, промывают водой, а затем последовательно насыщенным раствором тиосульфата натрия и насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 612 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : этилацетат/циклогексан (50 : 50)). В результате получают 68 мг искомого продукта (Rf = 0,40 этилацетат/циклогексан (50 : 50)).
Инфракрасный спектр: (CHCl3)
-NH- - ≈ 3400 см-1
> C = O - 1733 см-1 - 1610 см-1
C = C ароматич. - 1579 см-1 - 1511 см-1 - 1510 см-1
-SO2- - 1327 см-1 + 1141 см-1
Этап Б: N-бутил-5-[4-[ 17β- гидрокси-3-[(фенилметил)окси] - эстра-1,3,5(10)-триен- -11β- ил]фенокси]-пентансульфонамид
В среде инертного газа в охлажденный до 0/+5oC раствор, включающий 294 мг продукта, полученного на предыдущем этапе, в 1,3 мл тетрагидрофурана и 1,3 мл метанола добавляют 33 мг гидрида бора и натрия. Затем взбалтывают в течение 1 ч при температуре 0/+5oC, вливают в водный раствор хлристоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 300 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : этилацетат/циклогексан (50 : 50)). В результате получают 194 мг искомого продукта (Rf = 0,25 этилацетат/циклогексан (50 : 50)).
Этап В: N-бутил-5-[4-[ 3,17β- дигидрокси-эстра-1,3,5(10)-триен- -11β- ил]фенокси]-пентансульфонамид
В раствор 194 мг продукта, полученного на предыдущем этапе, в 5 мл этилацетата, 5 мл этанола и 5 мл уксусной кислоты добавляют 44 мг 10-процентного палладий-катализатора на активированном угле, после чего взбалтывают в течение 15 мин при давлении 1700 мбаров водорода. После этого взвесь фильтруют, промывают смесью метанола и метиленхлорида (1 : 1), фильтрат выпаривают досуха при пониженном давлении, отгоняют уксусную кислоту толуолом и высушивают при пониженном давлении. Таким образом получают 172 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : метиленхлорид/изопропанол (96 : 4)). В результате получают 142 мг целевого продукта.
Инфракрасный спектр: (CHCl3)
-OH - 3601 см-1
-NH- - 3400 см-1 - 1610 см-1
C = C ароматич. - 1581 см-1 - 1512 см-1
-SO2- - 1327 см-1 - 1140 см-1
Пример 3: 5-[4-( 3,17β- дигидрокси-эстра-1,3,5(10)-триен- 11β -ил)фенокси]-N-[(диметиламино)метилен)-пентансульфонамид
В раствор 200 мг продукта, полученного на Этапе Г Примера 1, в 1,5 мл диметилформамида добавляют 0,062 мл N, N-диметилформамиддиметилацеталя и взбалтывают в течение 1 ч 30 мин при комнатной температуре. Затем вливают в 1-процентный водный раствор гидрогеносульфата натрия, экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 227 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : метиленхлорид/изопропанол (95 : 5)). В результате получают 168 мг целевого продукта.
Инфракрасный спектр: (CHCl3)
-OH - 3602 см-1
-N=CH- - 1629 см-1 - 1611 см-1
C = C ароматич. - 1580 см-1 - 1512 см-1
Пример 4: N-бутил-N'-5-[4-(3, 17β-дигидрокси-эстра-1,3,5(10)- триен -11β- ил)фенокси]пентилсульфонил]-карбамид
В среде инертного газа в раствор 200 мг продукта, полученного на Этапе Г Примера 1, в 2 мл диметилформамида добавляют 20 мг гидрида натрия и, после 10-минутного взбалтывания при комнатной температуре, 0,046 мл бутилизоцианата. После взбалтывания в течение 1 ч при комнатной температуре, смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 317 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : метиленхлорид/изопропанол (95 : 5)). В результате получают 146 мг целевого продукта.
Инфракрасный спектр: (Вазелиновое масло)
OH-NH - ≈ 3360 см-1 - + полное поглощение
> C = O - 1675 см-1 - 1610 см-1
C = C ароматич. - 1577 см-1
+ амид ---> - 1540 см-1 - 1510 см-1
-SO2 - 1340 см-1 - 1146 см-1
Пример 5: N-(4-хлорфенил)-N'-5-[4-( 3,17β- дигидрокси-эстра-1,3,5(10)- триен -11β- ил)фенокси]пентилсульфонил]-карбамид
В среде инертного газа в раствор 183 мг продукта, полученного на Этапе Г Примера 1, в 2 мл диметилформамида добавляют 22 мг 50-процентного гидрида натрия и, после 10-минутного взбалтывания при комнатной температуре, 73 мг 4-хлорфенилизоцианата. После взбалтывыания в течение 5 ч при комнатной температуре, смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 289 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : метиленхлорид/изопропанол (92,5 : 7,5)). В результате получают 86 мг целевого продукта.
Инфракрасный спектр: (Вазелиновое масло)
Комплексное поглощение в области OH/NH:
> C = O - ≈ 1698 см-1 - 1607 см-1
C = C ароматич. - 1540 см-1
+ амид - 1511 см-1 - 1494 см-1
Пример 6: 1-[5-[4-( 3,17β- дигидрокси-эстра-1,3,5(10)- триен -11β- ил)фенокси]пентилсульфонил]-2-имидазолидинон
В среде инертного газа в раствор 200 мг продукта, полученного на Этапе Г Примера 1, в 2 мл диметилформамида добавляют 20 мг 50-процентного гидрида натрия и, после 10-минутного взбалтывания при комнатной температуре, 0,035 мл 2-хлорэтилизоцианата. После взбалтывания в течение 1 ч 30 мин при комнатной температуре, смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Таким образом получают 278 мг продукта, который подвергают хроматографии на двуокиси кремния (элюант : этилацетат и затем метиленхлорид/изопропанол (92,5 : 7,5)). В результате получают 102 мг целевого продукта.
Инфракрасный спектр: (Вазелиновое масло)
Комплексное поглощение в области OH/NH:
> C = O - 1726 см-1 - 1612 см-1
C = C ароматич. - 1580 см-1 - 1510 см-1 - 1505 см-1 (площадка)
-SO2- - 1155 см-1
Пример 7: N-бутил-5-[4-( 3,17β- дигидрокси-эстра-1,3,5(10)- триен -11β- ил)фенокси]N-метилпентансульфонамид]
Этап А: N-бутил-5-[4-(3,17-диоксо-эстра-4,9-диен- 11β -ил] фенокси]-N-метилпентансульфонамид
В среде инертного газа во взвесь 58 мг 50-процентного раствора гидрида натрия в масле в 6 мл диметилформамида добавляют 362,5 мг 11β -(4-гидроксифенил)-эстра-4,9-диен-3,17-диона, полученного согласно патенту ЕЭС 384842 - Пример 43, и, после 30-минутного взбалтывания при комнатой температуре, добавляют раствор 417 мг продукта, полученного в Приготовлении 2 (Этап Б), в 1,5 мл диметилформамида. Во время введения температуре дают подняться с +23oC до +27oC, а затем взбалтывают в течение 45 мин. Затем смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают водой, а затем последовательно насыщенным раствором тиосульфата натрия и насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Остаток (883 мг) подвергают хроматографии на двуокиси кремния (элюант : этилацетат-циклогексан (60 : 40)). В результате получают 433 мг искомого продукта.
Инфракрасный спектр: (CHCl3)
> C = O в положении 17 - 1735 см-1
Диенон - 1658 см-1 - 1609 см-1
C = C + - 1600 см-1 (площадка)
C = C ароматич. - 1580 см-1 - 1509 см-1 (сильн.) - 1333 см-1
-SO2N< - 1140 см-1
Этап Б: N-бутил-5-[4-( 3,17β- гидрокси-эстра-1,3,5(10)-триен -11β- ил] фенокси]-N-метилпентансульфонамид
1. Ароматизация
В среде инертного газа в раствор 404,5 мг продукта, полученного на предыдущем этапе, в 4 мл метиленхлорида при температуре 0o/+5oC добавляют 0,32 мл уксусного ангидрида и 0,16 мл ацетилбромида. Затем взбалтывают в течение 15 мин при указанной температуре в течение 1 ч 15 мин при комнатной температуре.
2. Омыление ацетата
В реакционную смесь, охлажденную до температуры 0o/+5oC добавляют 0,3 мл метанола и, после 10-минутного взбалтывания, выпаривают досуха при пониженном давлении при комнатной температуре. Затем забирают в 2,4 мл метанола и 2,4 мл тетрагидрофурана и добавляют 0,47 мл натрового щелока. После этого взбалтывают в течение 45 мин при комнатной температуре.
3. Восстановление кетона в положение 17
В реакционную смесь, охлажденную до температуры 0o/+5oC добавляют 131 мг гидрида бора и натрия. После взбалтывания в течение 45 мин при комнатной температуре смесь вливают в водный раствор хлористоводородной кислоты (молярная концентрация = 1 моль/л), экстрагируют с использованием этилацетата, промывают водой, а затем насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Остаток (393 мг) подвергают хроматографии на двуокиси кремния (элюант : этилацетат-циклогексан (50 : 50)). В результате получают 193 мг искомого продукта.
Инфракрасный спектр: (CHCl3)
-OH - 3600 см-1 - 1610 см-1
C = C ароматич. - 1581 см-1 - 1512 см-1
-SO2N< - 1332 см-1 - 1138 см-1
Пример 8: 5-[4-( 3,17β- дигидрокси-эстра-1,3,5(10)-триен -11β- ил)фенокси]-N-(2,2,3,3,4,4,4-гептафторбутил)-N-метилпентансульфонамид
Этап А: 5-[4-(3,17-диоксо-эстра-4,9-диен -β- ил)фенокси]-N-(2,2,3,3,4,4,4-гептафторбутил)-N-метилпентансульфонамид
В раствор 255 мг 11β-(4-гидроксифенил)-эстра-4,9-диен-3,17-диона, полученного согласно патенту ЕЭС 384842 - Пример 43, в 4,5 мл диметилформамиде добавляют 40 мл 50-процентного раствора гидрида натрия в масле. После 30-минутного взбалтывания при комнатной температуре добавляют 400 мг продукта, полученного в Приготовлении 3 (Этап Б) и взбалтывают при комнатной температуре в течение 45 мин. Затем смесь вливают в водный раствор хлористоводородной кислоты (молярная кислота = 1 моль/л), экстрагируют с использованием этилацетата, промывают последовательно насыщенным раствором тиосульфата натрия и насыщенным водным раствором хлорида натрия, высушивают и выпаривают досуха при пониженном давлении. Остаток (600 мг) подвергают хроматографии на двуокиси кремния (элюант : этилацетат-бензин G (55 : 45)). В результате получают 335 мг искомого продукта.
Инфракрасный спектр: (CHCl3)
>C = O в положении 17 - 1735 см-1
Диенон - 1658 см-1 - 1609 см-1
C = C + - 1580 см-1
C = C ароматич. - 1509 см-1 - 1342 см-1
-SO2N< - 1448 см-1
Этап Б: 5-[4-( 3,17β- дигидрокси-эстра-1,3,5(10)-триен -11β- ил)фенокси] -N-(2,2,3,3,4,4,4-гептафторбутил)-N-метилпентансульфонамид
1. Ароматизация
В раствор 430 мг продукта, полученного на предыдущем этапе, в 3,5 мл метиленхлорида при температуре 0o/+5oC добавляют 0,35 мл уксусного ангидрида и 0,20 мл ацетилбромида и взбалтывают в течение 40 мин при комнатной температуре.
2. Омыление ацетата
В реакционную смесь, охлажденную до температуры 0o/+5oC добавляют 0,5 мл метанола и выпаривают досуха при пониженном давлении. Затем забирают в 3,5 мл метанола и добавляют 0,6 мл натрового щелока.
3. Восстановление кетона в положение 17
В реакционную смесь добавляют 228 мг гидрида бора и натрия. После взбалтывания в течение 20 мин при комнатной температуре подкисляют до pH = 2 с использованием 2 н. хлористоводородной кислоты, после чего экстрагируют с использованием метиленхлорида, высушивают и выпаривают досуха при пониженном давлении. Остаток (429 мг) подвергают хроматографии на двуокиси кремния (элюант : этилацетат-бензин G (40 : 60)). В результате получают 266 мг целевого продукта (tпл 136oC-138oC).
Инфракрасный спектр: (CHCl3)
-OH - 3615 см-1 - 1610 см-1
C = C ароматич. - 1581 см-1 - 1512 см-1 - 1491 см-1
-SO2N< - 1342 см-1 - 1148 см-1
Фармацевтические соединения
Были приготовлены таблетки, имеющие следующую формулу:
Продукт примера 7 - 50 мг
Основа для готовой таблетки - 120 мг
(Деталировка основы: тальк, крахмал, стеарат магния).
Были приготовлены взвеси для инъекций, имеющие следующую формулу:
Продукт примера 7 - 25 мг
Основа (водный дисперсивный раствор): бензиловый спирт, полисорбат 80, карбоксиметилцеллюлоза (натриевая соль), хлорид натрия, вода для приготовления препарата для инъекций для флакона емкостью - 1 мл
Фармакологическое исследование продуктов изобретения
1) Исследование воздействия продуктов изобретения на гормональные рецепторы
В данном исследовании используют либо естественный гормональный рецептор крысы (AR), либо рекомбинантный рецептор человека (PR, GR и ER).
Андрогенный рецептор простаты крысы
Самцы крыс Sprague Dawley EOPS весом от 180 до 200 г подвергаются кастрации. Через 24 ч после кастрации животные умерщвляются. После этого у них вырезают простаты, взвешивают и гомогенизируют при температуре 0oC с помощью трубчатого измельчителя тефлон-стекло в забуференном растворе TS (Tris 10 ммоль, сахароза 0,25 моль, ДТТ 2 ммоль, MoNa 20 ммоль, ФМСФ (фенилметансульфонилфторид) 0,1 ммоль, pH 7,4) (из расчета 1 г ткана на 8 мл буферного раствора). Затем гомогенат подвергают центрифугированию (209 000 г • 30 мин) при температуре 0oC. Полученные таким образом аликвоты надсадочной жидкости подвергаются инкубации при температуре 0oC в течение инкубационного периода в 24 ч при постоянной концентрации (T) тритированного тестостерона, и в присутствии возрастающих концентраций (от 0 до 1000 • 10-9 моль), либо тестируемого продукта (от 1 до 25000 • 10-9 моль). Концентрация связанного тритированного тестостерона (B) измеряется затем в каждом инкубате методом адсорбции углем-декстраном.
Прогестеронный рецептор человека
Рекомбинантный рецептор человека получают путем суперэкспрессии в системе клеток насекомых Baculovirus в соответствии с общим методом, описанным Н. Р. УЭББОМ с соавторами (Journal of Methods in Cell and Molecular Biology, 1990 г., том 2, N 4, стр. 173-188), а применение которых описано в экспрессии гормональных рецепторов человека, например, глюкокортикоидного рецептора человека (Ж. СРИНИВАЗАН с соавторами. Molecular Endocrinology, 1990 г., том 4, N 2, стр. 209-216).
Для ввода фрагмента ДНКс, описанного П. КАСТНЕРОМ с соавторами (The EMBO Journal, 1990 г., том 9, N 5, стр. 1603-1614), включающего кодирующую область для прогестеронного рецептора человека и для приготовления соответствующего рекомбинантного вируса используют комплект "BaculoGolg Transfection Kit" (PharMingen, обозн. 21000K).
Полученный таким образом рекомбинантный вирус используется для экспрессии прогестеронного рецептора в клетках насекомых SF9 (ATCC CRL1711) в соответствии с вышеописанным общеизвестным методом. От 2 • 107 до 2,5 • 107 клеток SF9 культивируются в склянке "Фалкон" на 175 см2 в среде TNM-FH "СИГМА" с добавлением 10% плодной телячьей сыворотки (SVF) и 50 мкг/мл гентамицина. После заражения и инкубации при температуре +27oC в течение 40-42 ч клетки подвергают лизису в 1 мл лизисного буфера (1) путем выполнения цикла замораживания-размораживания, который повторяют еще два раза. Надсадочную жидкость, содержащую рекомбинантный прогестеронный рецептор человека, хранят дозами по 1 мл в жидком азоте.
Надсадочную жидкость разбавляют в момент использования в соответствии с диапазоном разбавления от 1/10 до 1/100 буферным раствором (Tris 10 ммоль, сахароза 0,25 моль, HCl при pH 7,4 с содержанием 0,1% желатина), после чего инкубируют в течение 24 ч при температуре 0oC при постоянной концентрации (T) тритированного 17 α , 21-диметил 19-нор-прегна 4,9-диен-3,20-диона, в присутствии возрастающих концентраций либо холодного прогестерона (от 0 до 2500 • 10-9 моль), либо холодного тестируемого продукта (от 1 до 2500 • 10-9 моль). Затем концентрация связанного тритированного 17,21-диметил 19-нор-4,9-прегнан-3,20-диона (В) измеряется в каждом инкубате методом адсорбции углем-декстраном.
Глюкокортикоидный рецептор человека
Надсадочную жидкость клеток SF9, содержащую рекомбинатный глюкокортикоидный рецептор человека, получают по методу, описанному выше для прогестеронного рецептора с использованием фрагмента ДНКс, описанного С.М. ХОЛЛЕНБЕРГОМ с соавторами (Nature, 1985 г, том 318, N 19/26, стр. 635), включающего кодирующую область для глюкокортикоидного рецептора человека. Полученные клетки подвергают лизису в лизисном буфере (2).
Надсадочную жидкость инкубируют в течение 24 ч при температуре 0oC при постоянной концентрации (Е) тритированного 11β,17β -дигидрокси-6,21-диметил прегна 1,4,6-тиен-20-ин-3-она, в присутствии возрастающих концентраций либо холодного дексаметазона (от 0 до 1000 • 10-9 моль), либо холодного тестируемого продукта (от 1 до 25000 • 10-9 моль). Затем концентрация связанного тритированного 11β,17β-дигидрокси-6,21-диметил прегна 1,4,6-триен-20-ин-3-она (В) измеряется в каждом инкубате методом адсорбции углем-декстраном.
Эстрогенный рецептор человека
Надсадочную жидкость клеток SF9, содержащую рекомбинантный эстрогенный рецептор человека, получают по методу, описанному выше для прогестеронного рецептора с использованием фрагмента ДНКс, описанного в векторе экспрессии HEGO Л. ТОРА с соавторами (The EMBO Journal, 1989 г., том 8, N 7, стр. 1981-1986), включающего кодирующую область для эстрогенного рецептора человека "дикого типа" с глицином в положении 400. Полученные клетки подвергают лизису в лизисном буфере (1).
Надсадочную жидкость инкубируют в течение 24 ч при температуре 0oC при постоянной концентрации (T) тритированного эстрадиола в присутствии возрастающих концентраций либо холодного эстрадиола (от 0 до 100 • 10-9 моль), либо холодного тестируемого продукта (от 1 до 25000 • 10-9 моль). Затем концентрация связанного тритированного эстрадиола (В) измеряется в каждом инкубате методом адсорбции углем-декстраном.
Выражение результатов и методы расчета
Расчет относительного связующего воздействия (ARL)
Для начала прочерчивают две кривые: процент связанного тритированного гормона B/BO в зависимости от логарифма концентрации холодного контрольного гормона или в зависимости от логарифма концентрации холодного тестируемого продукта.
Затем определяют следующую прямую уравнения:
I50 = 100 (BO / BO + Bмин / BO) / 2; I50 = 100 (1 + Bмин / BO) / 2 = 50 (1 + Bмин / BO),
в котором:
- BO: Концентрация связанного тритированного гормона в отсутствие любого холодного продукта;
- B: Концентрация связанного тритированного гормона в присутствии концентрации X холодного продукта;
- Bмин: Концентрация связанного тритированного гормона в присутствии значительного избытка холодного контрольного гормона (500 нмоль).
Пересечения прямой I50 и кривых позволяют вычислить концентрации холодного контрольного гормона (CH) и холодного тестируемого продукта (CX), которые ослабляют на 50% связь тритированного гормона с рецептором.
Относительное связующее воздействие (ARL) тестируемого продукта определяется с помощью уравнения ARL = 100 (CH) / (CX).
ARL контрольных продуктов: эстрадиола, прогестерона, дексаметазона и тестостерона произвольно принимается равными 100.
При этом получают следующие результаты ARL (см. в конце описания)
Заключение
Изученные продукты, в частности продукты Примеров 2 и 8, имеют выраженное связующее воздействие на эстрогенный рецептор.
Продукты Примеров 2, 7 и 8 имеют выраженное связующее воздействие на глюкокортикоидный и прогестеронный рецепторы.
Лизисный буфер:
(1) Tris - HCl pH 8 : 20 ммоль, ЭДТА : 0,5 ммоль, ДТТ : 2 ммоль, глицерин : 20%, KCl : 400 ммоль, ПИК 1%.
(2) Фосфат калия pH 7,0 : 50 ммоль, ДТТ : 5 ммоль, глицерин : 20%, молибдат натрия : 20 ммоль, ПИК 1%.
ПИК: лейпептин, пепсатин A, апротинин, антипаин, химостатин. Конечная концентрация каждого из них: 2,5 мкг/мл.
2) Антипролиферирующее воздействие продуктов изобретения на рост опухолевой клетки грудных желез у человека (MCF-7)
Описание теста
а) Культура клеток
Линии MCF-7 выдерживаются в культуре в основной среде (см. 1), содержащей 5% плодной телячьей сыворотки, при температуре +37oC во влажной среде, содержащей 5% CO2. Клетки с подслиянием собирают путем трипсинации (трипсин : 0,1% ЭДТА : 0,02%), а затем промывают легким центрифугированием. Образец взвешенных клеток вычисляется на клетке Малассеза.
б) Исследование роста
Клетки повторно взвешиваются в основной среде без фенолового красного в присутствии 5% дестероидированного SVF и стимулируются с помощью либо 0,1 нмоль эстрадиола, либо 10 нг/мл ЭГФ + 1 нг/мл ПДГФ. Затем клетки засеивают из расчета 50 тыс. клеток на каждую ячейку многоячеистых пластинок (24 ячейки на 2,5 см2). По истечении 24 ч после засеивания (день 0) тестируемый продукт добавляют к среде в виде этанолового раствора (конечная концентрация этанола: 0,1%) с концентрацией от 10-11 до 10-6 моль, причем контролируемые ячейки получают ту же концентрацию этанола. Среды, содержащие продукт, обновляются через каждые 48 ч. В конце эксперимента (дни с 7 по 9) среда отсасывается, а клетки немедленно фиксируются с помощью 250 мкл метанола для дозировки ДНК.
Антипролиферирующая активность продуктов оценивается за счет способности ингибировать увеличение ДНК относительно контроля.
в) Дозировка ДНК
ДНК дозируют флюорометрическим методом с использованием ДАБК (3,5 диаминобензойной кислоты) (см. 2): в каждую ячейку добавляют 200 мкл ДАБК; затем пластинки инкубируют в течение 45 мин при температуре +56oC, а затем добавляют 2 мл 1 н. хлористоводородной кислоты. Флюоресценция измеряется с помощью флюорометра (длина возбуждающей волны: 408 нм, длина излучающей волны: 510 нм).
Количество ДНК на каждую ячейку оценивается относительно контрольного диапазона, полученного обработкой в тех же условиях стандарта ДНК телячьего тимуса.
Результаты
Концентрация в нМ, ингибирующая на 50% рост клеток MCF-7, стимулируемый с помощью ЭГФ + ПДГФ (CI50), определяется вышеуказанным способом.
Продукт Примера 2 : CI50 = 0,016 нмоль.
Продукт Примера 7 : CI50 = 0,015 нмоль.
Продукт Примера 8 : CI50 = 0,026 нмоль.
(1) Основную среду получают следующим образом:
К среде МОС (Минимальная основная среда) добавляют:
- неосновные аминокислоты (GIBCO): 1%,
- пенистрепто (пенициллин: 100 ед/мл, стрептомицин: 0,1 мг/мл),
- фунгизон: 0,1%,
- глутамин: 2 ммоль,
- бикарбонат натрия: 2,25 мг/мл.
(2) Пузас и Гудмен, Analytical Biochemistry, том 86, стр. 50, 1978 г.

Описываются новые 11β-замещенные 19-норстероиды общей формулы (I), в которой n = 5 или 6; R1 и R2, одинаковые или различные -атом водорода, линейный или разветвленный алкильный радикал С1-С8, возможно замещенным галогеном, или R1 -карбамоильный радикал, монозамещенный линейным или разветвленным алкильным радикалом С1-С8 или фенильным радикалом, возможно замещенным атомом галогена, а R2 - атом водорода, или R1 и R2 вместе с атомом азота, с которым они связаны, образуют циклический карбамид формулы (II), в которой n = 2 или 3, или R1 и R2 образуют диалкил-С1-С4-аминометиленовый радикал. Соединения формулы (I) обладают глюкокортикоидной или антиглюкокортикоидной, прогестомиметической или антипрогестомиметической, андрогенной или антиандрогенной, эстрогенной или антиэстрогенной активностью и могут входить в состав фармацевтических композиций. 4 с. и 6 з.п. ф-лы, 1 табл.
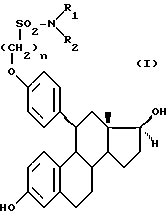

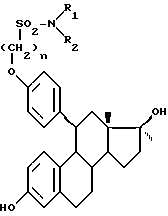
в которой n = 5 или 6;
R1 и R2, одинаковые или различные, - атом водорода, линейный или разветвленный алкильный радикал C1 - C8, возможно замещенный галогеном, или R1 - карбамоильный радикал, монозамещенный линейным или разветвленным алкильным радикалом C1 - C8 или фенильным радикалом, возможно замещенным атомом галогена, а R2 - атом водорода, или R1 и R2 вместе с атомом азота, с которым они связаны, образуют циклический карбамид формулы
в которой n = 2 или 3, или R1 и R2 образуют диалкил-C1 - C4-аминометиленовый радикал.
N-бутил-5-[4-(3,17β-дигидрокси-эстра-1,3,5(10)-триен11β-ил)фенокси]-пентансульфонамид,
N-бутил-5-[4-(3, 17β-дигидрокси-эстра-1,3,5(10)-триен11β-ил)фенокси]-N-метилпентансульфонамид,
5-[4-(3,17β-дигидрокси-эстра-1,3,5(10)-триен-11-ил)фенокси/-N-(2,2,3,3,4,4-гептафторбутил)-N-метилпентансульфонамид.
в которой фенольная гидроксигруппа может быть при необходимости защищена,
подвергают действию галогенпроизводного общей формулы III
X-(CH2)n-SO2-NRAR'A,
где Х - атом галогена;
n имеет значение, указанное в п.1;
RA и R'A одинаковые или различные, - атом водорода, линейный или разветвленный алкильный радикал C1 - C8, возможно замещенный галогеном, причем хотя бы один из RA и R'A не является атомом водорода,
для получения соединения общей формулы IV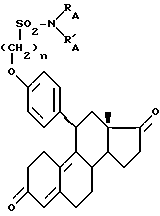
которое затем подвергают действию агента, ароматизирующего цикл A, с получением соединения формулы IA
где n и Rp имеют вышеуказанные значения,
которое далее при необходимости подвергают одной или нескольким из следующих реакций в соответствующем порядке: восстановление кетогруппы в положении 17, селективное ацилирование в положении 3, омыление полученной ацильной группы с последующим возможным солеобразованием с помощью кислоты, или соединение формулы II
подвергают действию агента ароматизирующего цикл A с одновременной защитой гидроксигруппы в положении 3, а затем реакции выделения защитной группы фенола в положении II для получения соединения общей формулы V
в которой Rp - защитная группа,
которое подвергают воздействию соединения формулы III'
X-(CH2)p-SO2-N=CH-N(Alk1)(Alk2),
где X - атом галогена;
Alk1 и Alk2 - алкильный радикал C1 - C4;
n = 2,
с последующим гидролизом образовавшегося имина для получения соединения общей формулы VI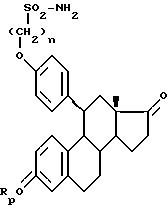
где n и Rp имеют вышеуказанные значения,
которое при необходимости подвергают реакции снятия защитной группы Rp, восстановлению кетогруппы в 17-м положении, ацилирования гидроксильного радикала в положении 3, воздействию галогена формулы VII:
RB-X,
где RB - алкильный радикал C1 - C8, возможно замещенный галогеном;
X - атом галогена,
для получения соединения общей формулы IB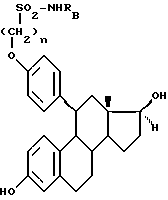
где n имеет вышеуказанное значение,
или воздействию изоцианата общей формулы VIII
Rc-NCO,
в которой Rc - алкильный радикал C1 - C8, возможно замещенный галогеном,
для получения соединения общей формулы Ic, соответствующего соединению формулы I, где R1 - монозамещенный карбамоильный радикал, а R2 - атом водорода,
где n имеет вышеуказанное значение
воздействию соединения общей формулы IX
(Alk3O)(Alk4O)CH-N(Alk1)(Alk2),
в которой Alk1 - Alk4 являются алкильными радикалами, включающими от 1 до 4 атомов углерода,
для получения соединения общей формулы ID, соответствующего продукту формулы I, в которой R1 и R2 образуют ди-C1 - C4-алкиламинометиленовую группу
в которой n, R17, R'17 и R3 имеют значения, указанные в п.1 формулы,
реакции циклизации продукта формулы Ic, когда Rc представляет собой радикал -(CH2)n'-Hal, где n' = 2 или 3, а Hal - атом галогена,
для получения соединения формулы Ic, соответствующего соединению формулы I, где R1 и R2 образуют вместе с атомом азота, с которым они связаны, циклический карбамид формулы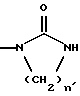
где n' = 2 или 3,
возможно солеобразования с помощью кислоты.
| СПОСОБ УСТРАНЕНИЯ КОРРОЗИОННЫХ СВОЙСТВ СВЯЗУЮЩЕГО | 0 |
|
SU347370A1 |
| Пресс-форма для изготовления винтовых режущих пластинок твердого сплава | 1951 |
|
SU116974A1 |
| УСТРОЙСТВО для УЧЕТА МОЛОКА НА ДОИЛЬНЫХ | 0 |
|
SU369881A1 |
| ГИДРОМОЛОТ | 0 |
|
SU375347A1 |
| J.Steroid | |||
| Biochem | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
| Тринус Ф.П | |||
| Фармако-терапевтический справочник | |||
| - Киев: Здоровья, 1989, с.265. | |||
Авторы
Даты
1999-10-27—Публикация
1994-06-16—Подача