Изобретение относится к гербицидным производным карбоксамида, способу их получения, гербицидным композициям, включающим эти производные, а также их применению для борьбы с нежелательными растениями.
Хорошо известна гербицидная активность соединений 2-фенокси-3-пиридинкабоксамида. Известны 2-феноксиникотинамидные гербициды. Также известно, что 2-феноксиникотиновые кислоты гербицидно неактивны, а производные N-алкиламида обнаружили слабую гербицидную активность, в то время как N-фенил и N-бензиламиды являются самыми активными соединениями данного типа. В действительности, Diflufenican [N-(2,4-дифторфенил)-2- (3-трифторметилфенокси)-3-пиридинкарбоксамид] был впоследствии разработан различными исследовательскими группами в качестве промышленного гербицида для применения против широколиственных сорняков в озимых хлебных злаках, таких как озимая пшеница и ячмень.
Известны N-алкиламиды Гутмана, а также родственные N-алкенил и N-алкиниламиды. Наиболее активным из полученных и испытанных алифатических амидов является N-(1,2-диметилпроп-2-енил)-2-(3- трифторметилфенокси)-3-пиридинкарбоксамид, который дает 85% борьбы перед прорастанием и только 57% борьбы после прорастания на определенных узко- и широколиственных видах.
В изобретении обнаружено, что соединения 2-фенокси-6-пиридинкарбоксамида с алифатическим (как прямолинейным, так и алициклическим) или иным замещением атома азота в амиде имеют чрезвычайно высокую гербицидную активность против характерных узко- и широколиственных испытываемых видов при применении перед и/или после прорастания, причем некоторые соединения проявляют 80-100% эффективность против испытываемых видов как перед, так и после прорастания.
Таким образом, изобретение касается соединения, имеющего общую формулу I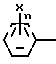 O
O - N
- N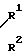
(I) где n целое число от 1 до 5, а единственный или каждый из Х, независимо друг от друга, представляет собой атом водорода или галогена, алкил- или алкокси-группу, произвольно замещенную одним или более одинаковыми или различными заместителями, выбранными из группы, состоящей из атомов галогена, циано-, гидрокси- и алкоксигрупп, или циано-, нитро-, акленилокси-, алкинилокси-, алкилтио-, галогеналкилтио-, алкенилтио- или алкинилтиогруппу;
m 0 или целое число от 1 до 3, а единственный или каждый из Y, независимых друг от друга, представляет собой атом галогена или алкильную или галогеналкильную группу;
Z атом кислорода или серы; и R1 и R2 каждый, независимо друг от друга, представляют собой атом водорода, алкильную группу, произвольно замещенную одним или более одинаковыми или различными заместителями, выбранными из группы, состоящей из атомов галогена или гидрокси-, циано-, алкокси-, алкилтио-, алкоксикарбонил- или моно-, или диалкиламиногрупп, алкенил-, алкинил-, циклоалкил- или произвольно замещенную циклоалкилалкильную гpуппу, или гидрокси-, алкокси-, алкенилокси-, алкинилокси-, алкоксикарбонил-, амино-, моно- или диалкиламино-, алкоксикарбониламиногруппу, ариламино-группу, произвольно замещенную атомом галогена, или диалкилкарбамоильную группу; или R1 и R2, взятые вместе, представляют собой алкиленовую цепь, произвольно прерываемую атомом кислорода или серы, или группой -NR-, в которой R представляет собой атом водорода или алкильную группу.
Если любой из заместителей X, Y, R1 и R2 представляет собой или содержит алкильную, алкенильную или алкинильную группу в качестве заместителя, она может быть линейной или разветвленной и обычно содержит до 12, преимущественно до 8 и, в особенности, до 5, атомов углерода. Таким образом, к примеру, алкильная группа R2 может представлять собой бутил, например, н-бутил, изо-бутил, втор-бутил или трет-бутил. Если присутствует циклоалкильная замещающая группа, она обычно содержит от 3 до 8, преимущественно от 3 до 6 атомов углерода в кольце. Арильная группа обычно представляет собой фенил. Алкиленовая цепь содержит от 3 до 6, преимущественно 4 или 5 звеньев, Атом галогена обычно обозначает фтор, хлор, бром или йод, преимущественными галогеналкильными группами являются трифторметил, трифторэтил и фторэтил.
Заместитель(ли) Хn может находиться в любом свободном положении или сочетании положений в фенольном кольце.
Желательно, чтобы один феноксизаместитель Х находился в 3-(или мета-) положении и преимущественно представлял собой атом водорода, фтора, хлора или брома или нитро-, этил-, метокси или, в особенности, трифторметильную группу. Если присутствуют дополнительные заместители Х, они обычно находятся в положении 4- и/или 5- и могут быть такими же или, преимущественно, другими по отношению к мета-заместителю Этот дополнительный заместитель(ли) Х преимущественно представляет собой атом хлора и, в особенности, фтора.
Заместитель(ли) Хn может находиться и в других положениях и может представлять собой, к примеру, 2,3- или 2,5-диметил.
Преимущественно присутствует только один или два заместителя Х, наиболее предпочтительно один, или же Х представляет собой 3-трифторметил.
Предпочтительно m равно 0.
Предпочтительно Z представляет собой атом кислорода.
Радикалы R1 и R2, когда они присутствуют по отдельности, могут б ыть одинаковыми или различными. Предпочтительно R1 представляет собой атом водорода или С1-4 алкил или С2-4 алкенил, подходящую аллильную группу, более предпочтительно водород или С1-4 алкил, а R2 представляет собой незамещенную С1-8 алкильную группу, в особенности С1-6 алкил, С1-4алкильную группу, замещенную фтором, гидрокси-, циано-, С1-2 алкокси-, (С1-2-алкокси)карбонил-, или моно- или ди-(С1-2 алкил)амино-, например, фторэтил, трифторэтил, цианопропил, гидроксиэтил, метоксиэтил, этоксикарбонилметил или диметиламиноэтил, С3-8 циклоалкильную группу, в особенности циклопропил, циклобутил, циклопентил или ци клогексил, С2-4алкенильную группу, например аллил или метилаллил, С2-4 алкинильную группу, например пропинил, С1-4 алкоксигруппу, например этокси, (С1-4алкил)аминогруппу, например метиламино, С2-4 алкенилоксигруппу, например пропенилокси, (С1-2 алкокси)карбонильную группу, например этоксикарбонил, (С1-2 алкокси)карбониламиногруппу, например этоксикарбониламино, ди(С1-2 алкил)карбамоильную группу, например, диметилкарбамоил, ариламиногруппу, например фениламино или п-хлорфениламино, или галогензамещенную (С3-6 циклоалкил)С1-4 алкильную группу, например хлорзамещенный циклопропилметил.
Особо предпочтительно, чтобы либо R1 представлял собой атом водорода в то время, как R2 представлял бы собой незамещенную С1-5алкильную группу, С1-2 алкильную группу, замещенную фтором или метокси, С3-6 циклоалкильную группу, С3 алкенильную группу, С3 алкинильную группу, С1-2 алкоксигруппу, С3 алкенилоксигруппу или хлорзамещенную циклопропилметильную группу, либо R1 представлял собой С1-3 алкильную группу в то время, как R2 представлял бы собой ту же самую С1-3алкильную группу или хлорзамещенную циклопропилметильную группу.
Особое предпочтение отдается соединениям, в которых R1 представляет собой атом водорода, а R2 представляет собой этил, пропил, циклопропил или циклобутильную группу.
Если R1 и R2 вместе представляют собой алкиленовую цепь, она обычно состоит из 4 или 5 звеньев и представляет собой, например, группу -(СН2)4-, -(СН2)2О(СН2)2- или -(СH2)2NR(СН2)2-, где R С1-2 алкильная группа, обычно
метил. Предпочтительно R1 и R2 представляют собой -(СН2)4-группу.
Cоединения, имеющие общую формулу I, можно получить либо путем взаимодействия соответствующего производного феноксипиколиновой кислоты с соответствующим амином (способ А), либо путем взаимодействия соответствующего производного 2-галоген-6-пиридинкарбоксамида с соответствующим фенолятом щелочного металла (способ Б). Эти способы являются развитием заявленного изобретения.
В соответствии со способом А соединение, имеющее общую формулу I, в котором Z представляет собой кислород, получают путем взаимодействия соединения, имеющего общую формулу II O
O (II) где Хn и Ym такие, как определено выше, а L представляет собой отщепляющуюся группу, с амином, имеющим общую формулу NHR1R2, где R1 и R2 такие, как определено выше.
(II) где Хn и Ym такие, как определено выше, а L представляет собой отщепляющуюся группу, с амином, имеющим общую формулу NHR1R2, где R1 и R2 такие, как определено выше.
Отщепляющаяся группа это любая группа, которая под воздействием условий реакции отщепляется от исходного соединения, активируя таким образом реакцию в активном центре.
Отщепляющаяся группа L обычно представляет собой атом галогена, например атом брома или, в особенности, хлора, или алкоксигруппу, обычно C1-4 алкокси, в особенности метокси.
Способ по варианту А обычно выполняют в присутствии инертного органического растворителя, например диметилформамида, или ароматического углеводорода, например бензола или толуола, или галогенированного углеводорода, например дихлорметана, или эфира, например диэтилового эфира, или сложного эфира, например этилацетата, температура обычно находится в пределах от 0 до 100оС.
Обычно реакцию проводят, используя по существу эквимолярные количества реагентов. Однако может быть целесообразно использовать один из реагентов, обычно амин, в избытке, например, таким образом, чтобы молярное соотношение производного феноксипиколиновой кислоты и амина находилось в пределах 1: (1-1,1).
Если L представляет собой атом галогена, реакцию обычно проводят при температуре от 0 до 50оС, преимущественно при температуре окружающей среды, и обычно в присутствии основания, например, карбоната калия или, предпочтительно, основного амина, такого как триэтиламина, или избытка исходного соединения амина.
Если L представляет собой алкоксигруппу, реакцию обычно проводят при температуре от 0 до 100оС, предпочтительно при комнатной температуре (или 20оС) и в отсутствии добавки основания.
В соответствии со способом Б соединение, имеющее общую формулу I, в которой Z представляет собой кислород, получают путем взаимодействия соединения, имеющего общую формулу III
Hal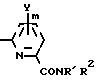 (III) в которой Ym, R1 и R2 такие, как определено выше, а HaI представляет собой атом галогена, с соединением, имеющим общую формулу IY
(III) в которой Ym, R1 и R2 такие, как определено выше, а HaI представляет собой атом галогена, с соединением, имеющим общую формулу IY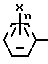 OM (IY) где Xn такое, как определено выше, а М представляет собой атом щелочного металла.
OM (IY) где Xn такое, как определено выше, а М представляет собой атом щелочного металла.
Обычно HaI представляет собой атом брома или, в особенности, хлора. Обычно R представляет собой атом калия или, в особенности, натрия.
Реакцию по способу Б можно провести путем приготовления фенолята щелочного металла из фенола, используя алкоксид щелочного металла, такого как метоксид натрия, и затем обработки полученного фенолята по существу эквимолярным количеством реагента III, обычно при повышенной температуре, например при температуре кипения, с медным катализатором, таким как хлорид меди, в пиридине в присутствии ароматического углеводорода, такого как ксилол.
Другой способ по варианту Б можно осуществить в присутствии гидрида щелочного металла, например гидрида натрия, в сухом растворителе, таком как диметилформамид, обычно при повышенной температуре, например при температуре от 50 до 125оС, или в присутствии карбоната щелочного металла, например, карбоната натрия или калия, и затем обработки оксидом меди и/или порошком меди в органическом растворителе, таком как диметилформамид или хинолин, обычно при температуре от 20 до 150оС, предпочтительно при температуре кипения реакционной смеси.
Соединения, имеющие общую формулу I, в которой Z представляет собой атом серы, обычно получают путем взаимодействия соединения, имеющего общую формулу I, в которой Z представляет собой атом кислорода, с пентасульфидом фосфора при нормальных условиях, например, путем нагревания, обычно при кипении, в присутствии инертного ароматического растворителя, например бензола, толуола, пиридина или хинолина.
Предлагаемые соединения можно выделить и очистить обычными способами, например путем экстракции растворителем, выпариванием сопровождающимся перекристаллизацией или путем хроматографии на двуокиси кремния.
Соединения, имеющею формулу II, можно получить, используя соответствующие феноксизамещенные пиколиновые кислоты обычными способами или, например, эфиром с использованием, например, спиртов и кислотных катализаторов или тионилхлорида, или используя хлориды и бромиды кислот, например, тионилхлорид или тионилбромид. Кислотные же соединения можно получить обычными способами из хлорпиколиновой кислоты или ее сложного эфира. Хлорпиколиновую кислоту или ее сложный эфир можно получить известными способами.
Соединения, имеющие формулу III, можно получить способами, аналогичными способу А, путем взаимодействия замещенного амина, имеющего формулу NHR1R2, с производными 2-гелоген-6-пиридинкарбоновой кислоты, имеющим общую формулу V
Hal (V) где Ym HaI и L такие, как определено выше.
(V) где Ym HaI и L такие, как определено выше.
Соединения, имеющие формулу V, можно получить обычными способами из пиколиновой кислоты.
Замещенные амины NHR1R2 и феноляты, имеющие формулу IV, либо известны, либо их можно получить обычными способами.
Было обнаружено, что предлагаемые соединения обладают чрезвычайно высокой гербицидной активностью, проявляющейся в широком интервале в отношении трав и, в особенности, широколиственных сорняков, включая Alopecurus myosuroides (лисохвост мышехвостниковидный), Avena fatua (овсюг), Steria fabetii (гигантский лисохвост), Seteria viridis (щетинник зеленый), Ipomoea purpurea (ипомея), Galium aparine (подмаренник цепкий), Solanum nigrum (паслен черный), Veronika persica (вероника персидская) и Stellaria media (звездчатка средняя), в случае их применения до и после прорастания. Было обнаружено, что некоторые из предлагаемых соединений проявляют селективность по отношению к малым зерновым злакам, например маису, пшенице, ячменю и рису, а также к широколиственным культурам, например сое, подсолнечнику и хлопку, что свидетельствует о их возможном применении для борьбы с сорняками, растущими в этих культурах.
Другой целью изобретения является разработка гербицидной композиции, включающей связанное с носителем соединение по формуле I, определенное выше, а также способ получения такой композиции, включающей связывание соединения по формуле I с носителем.
Следующей целью изобретения является применение предлагаемого соединения или композиции в качестве гербицида. Далее, в соответствии с изобретением, предлагается способ борьбы с нежелательными растениями путем обработки очага их произрастания предлагаемым соединением или композицией. Обработку очага произрастания можно проводить как до, так и после прорастания. Доза используемого активного ингредиента может, например находиться в пределах от 0,01 до 10 кг/га, обычно от 0,05 до 4 кг/га. Очаг произрастания может представлять собой, например, почву или растения на засеянном участке, а типичными культурами являются хлебные злаки, такие, как пшеница и ячмень, а также широколиственные культуры, такие, как соя, подсолнечник и хлопок.
В качестве носителя в предлагаемых композициях можно использовать любой материал, с которым активный ингредиент образует композицию, облегчающую применение в отношении очага произрастания, подвергаемого обработке, причем это может быть, например, растение, посевной материал или почва, или облегчающую хранение, тpанспоpтиpовку или обращение. Носитель может быть твердым или жидким, включая материал, находящийся обычно в газообразном состоянии, но сжатый до образования жидкости, можно применять любой из носителей, обычно использующихся для образования гербицидных композиций. Предпочтительно композиции в соответствии с изобретением содержат от 0,5 до 95 мас. активного ингредиента.
Подходящие твердые носители включают природные и синтетические глины и силикаты, например природные кремнеземы, такие как диатомит; силикаты магния, например тальк; магниевоалюминиевые силикаты, например attapulgites и вермикулит; силикаты алюминия, например каолинит, montmorillonites и слюду; карбонат кальция; сульфат кальция; сульфат аммония; синтетические гидрированные оксиды кремния и синтетические силикаты кальция или алюминия; элементы, например углерод и серу; природные и синтетические смолы, например кумароновую смолу, поливинилхлорид, а также полимеры и сополимеры стирола; твердые полихлорфенолы; битум; парафины; а также твердые удобрения, например суперфосфаты.
Подходящие жидкие носители включают воду; спирты. например изопропанол, и гликоли; кетоны, например ацетон, метилэтилкетон, метилизобутилкетон и циклогексанон; эфиры; ароматические или аралифатические углеводороды, например бензол, толуол и ксилол; фракции нефти, например керосин и светлые минеральные масла; хлорированные углеводороды, например четыреххлористый углерод, перхлорэтилен и трихлорэтан. Часто используют смеси различных жидкостей.
Применяемые в сельском хозяйстве композиции обычно составляют и транспортируют в концентрированном виде, впоследствии их разбавляет потребитель перед применением. Присутствие небольших количеств носителя, являющегося поверхностно-активным веществом, облегчает процесс разбавления. Таким образом, предпочтительно, чтобы, по крайней мере одним из составляющих предлагаемой композиции носителей является поверхностно-ак- тивное вещество. Например, композиция может содержать, по крайней мере, два носителя, по крайней мере, один из которых является поверхностно-активным веществом.
Поверхностно-активное вещество может представлять собой эмульгатор, диспергатор или смачиватель; оно может быть неионным или ионным. Примером подходящих поверхностно-активных веществ являются натриевые или кальциевые соли полиакриловых кислот и лигнинсульфоновые кислоты; продукты конденсации жирных кислот или алифатических аминов или амидов, содержащих, по крайней мере, 12 углеродных атомов в молекуле, с этиленоксидом и/или пропиленоксидом; сложные эфиры жирных кислот и глицерина, сорбита, сахарозы или пентаэритрита; их конденсаты с этиленоксидом и/или пропиленоксидом; продукты конденсации жирных спиртов или алкилфенолов, например, п-октилфенола или п-октилкрезола, с этиленоксидом и/или пропиленоксидом; сульфаты или сульфонаты этих продуктов конденсации; соли щелочных или щелочноземельных металлов, предпочтительно натриевые соли, сложных эфиров серной или сульфоновой кислот, содержащих, по меньшей мере, 10 атомов углерода в молекуле, например, лаурилсульфат натрия, втор-алкилсульфаты натрия, натриевые соли сульфонированного касторового масла, также алкиларилсульфонаты натрия такие, как додецилбензолсульфонат. а также полимеры этиленоксида и сополимеры этиленоксида с пропиленоксидом.
Предлагаемые композиции можно составить, например, в виде смачиваемых порошков, гранул, растворов, эмульгируемых концентраторов, эмульсий, концентратов суспензий и аэрозолей. Смачиваемые порошки обычно содержат 25, 50 или 75 мас. активного ингредиента, а также, в дополнение к твердому инертному носителю, обычно 3-10 мас. диспергатора и, при необходимости, 0-10 мас. стабилизатора(ов) и/или других добавок, таких как смачиватели или связующие вещества. Порошки обычно готовят в виде концентрата, имеющего тот же состав, что и смачиваемые порошки, но без диспергатора, и их разбавляют в поле другим твердым носителем с образованием композиции, содержащей обычно 1/2 10 мас. активного ингредиента. Гранулы обычно имеют размер между 10 и 100 BS mesh (1,675-0,152 мм), и их можно приготовить путем агломерации или пропитки. В большинстве случае гранулы содержат 1/2 75 мас. активного ингредиента и 0-10 мас. добавок, таких, как стабилизаторы, поверхностно-активные вещества, медленно выделяющиеся модификаторы и связующие вещества. Так называемые "сухие свободнотекучие порошки" состоят из сравнительно мелких гранул, имеющих сравнительно высокую концентрацию активного ингредиента. Эмульгируемые концентраты обычно содержат, кроме растворителя, и, при необходимости, со-растворителя, 10-50 мас./объем активного ингредиента, 2 20 мас. /объем эмульгаторов и 0 -20 мас./объем других добавок, таких, как стабилизаторы, смачиватели и ингибиторы коррозии. Концентраты суспензий обычно составляют таким образом, чтобы получить стабильный, неоседающий текучий продукт, и они обычно содержат 10-75 мас. активного ингредиента, 0,5-15 мас. диспергаторов, 0,1-10 мас. суспендирующих агентов, таких как защитные коллоиды и загустители, 0-10 мас. других добавок, таких как пеногасители, ингибиторы коррозии. Стабилизаторы, смачиватели и связующие вещества, а также воду или органическую жидкость, в которой активный ингредиент практически нерастворим, также могут присутствовать некоторые органические твердые вещества или неорганические соли, растворенные в композиции, которые помогают предотвратить осаждение или используются в качестве антифризов для воды.
Еще одной целью изобретения являются водные дисперсии и эмульсии, например композиции, полученные путем разведения предлагаемого смачиваемого порошка или концентрата водой. Указанные эмульсии могут быть типа вода-в-масле или масло-в-воде, и могут иметь консистенцию густой сметаны.
Предлагаемые композиции могут также содержать и другие ингредиенты, например соединения, обладающие инсектицидными или фунгицидными свойствами или другие гербициды.
Изобретение более подробно иллюстрируется примерами. В примере 1 показано приготовление сложного эфира, имеющего общую формулу II, а примеры с 2 по 63 относятся к получению соединений, имеющих формулу I; примеры с 2 по 61 выполнены по способу А, пример 62 по способу Б, а пример 63 путем превращения соединения, имеющего общую формулу I, в котором Z кислород в соединение, или Z сера. Все структуры были подтверждены масс-спектроскопией и/или 300'Н ЯМР.
П р и м е р 1. Получение метил-6-(3- α α α -трифторметилфенокси) пиколината.
Раствор метоксида натрия (из 1,3 г натрия в 20 мл метанола) добавляли к раствору 3- α α α -трифторметилфенола (8,9 г) в ксилоле (50 мл). Растворители выпаривали под вакуумом для получения сухого фенолята натрия. Затем добавляли пиридин (250 мл) и ксилол (50 мл), далее хлорид меди (1,5 г) и смесь нагревали до кипения. Затем по каплям добавляли раствор метил-6-хлорпиколинота (8,5 г) в ксилоле (50 мл). Смесь кипятили с обратным холодильником в течение 14 ч. После охлаждения смесь выливали в воду (500 мл) и подкисляли разбавленной серной кислотой. Ксилольный слой отделяли, а водный слой экстрагировали диэтиловым эфиром. Соединенные экстракты промывали рассолом, сушили над безводным сульфатом магния и выпаривали. Остаток очищали на колонке, заполненной силикагелем, используя 5% (объем/объем) диэтиловый эфир/дихлорметан в качестве элюента, с образованием озаглавленного соединения (7,4 г) в виде твердого вещества желтого цвета, имеющего температуру плавления 43-44оС.
Анализ, С14H10O3NF3: Рассчитано: C 56,6; H 3,4; N 4,7.
Получено: С 55,6; H 3,4; N 4,9.
m/e: Теоретически: 297
Получено: 297
П р и м е р 2. N-н-пропил-2-(3- α α α -трифторметилфенокси)-6- пиридинкарбоксамид.
(а). Приготовление 6-(3- α α α -трифторметилфенокси)пиколиновой кислоты.
Раствор метил 6-(3- α α α -трифторметилфенокси)пиколината (8 г) в 50%-ном водном метаноле (45 мл), содержащий гидроксид натрия (2,5 г), кипятили с обратным холодильником в течение 3 ч. Метанол выпаривали, а к остатку добавляли еще воды, и водный раствор экстрагировали диэтиловым эфиром. Затем водную фазу подкисляли разбавленной соляной кислотой для осаждения 6-(3-α α α -трифторметилфенокси)пиколиновой кислоты (7,1 г) в виде твердого вещества белого цвета, имеющего температуру плавления 92-93оС.
Анализ
C13H8NO3F3: Рассчитано: C 55,1; H 2,8; N 4,9.
Получено: C 53,3; H 3,0; N 5,0.
m/e: Теоретически: 283
Получено: 283
(б). Приготовление N-н-пропил-2-(3- α α α -трифторметилфенокси)- 6-пиридинкарбоксамида
6-(3-α α α -трифторметилфенокси)пиколиновую кислоту (1,5 г) в тионилхлориде (20 мл) кипятили с обратным холодильником в течение 1 ч. Избыток тионилхлорида выпаривали под вакуумом, а к остаточному пиколинилхлориду добавляли дихлорметан (20 мл). Раствор н-пропиламина (0,6 г) и триэтиламина (1,0 г) в дихлорметане (20 мл) добавляли по каплям при температуре окружающей среды. После перемешивания в течение 1/2 ч реакционную смесь промывали водой, сушили над безводным сульфатом магния, а затем дихлорметан выпаривали. Остаток очищали на колонках, заполненных силикагелем, используя 5% (объем/объем) диэтиловый эфир/дихлорметан в качестве элюента, при этом получали N-н-пропил-2-(3-α α α -трифторметилфенокси)-6-пиридинкарбоксамид (1,5 г) в виде масла.
Анализ,
C16H15O2N2F3: Рассчитано: C 59,3; Н 4,6; N 8,6.
Получено: C 60,0; H 5,0; N 8,7.
m/e: Теоретически: 324
Получено: 325
П р и м е р 2А. Приготовление N-н-пропил-2-(3- α α α -трифторметилфенокси)-6-пиридинкарбоксамида.
Смесь метил-6-(3- α α α -трифторметилфенокси)пиколината, (8 г) и н-пропиламина (1,4 г, избыток) оставляли при комнатной температуре на один час. Избыток н-пропиламина выпаривали, получали целевое соединение (0,7 г) в виде бесцветного масла.
Анализ
C16H15O2N2F3: Рассчитано: C 59,2; H 4,6; N 8,6.
Получено: C 58,6; H 4,9; N 8,8.
m/e: Теоретически: 324
Получено: 324
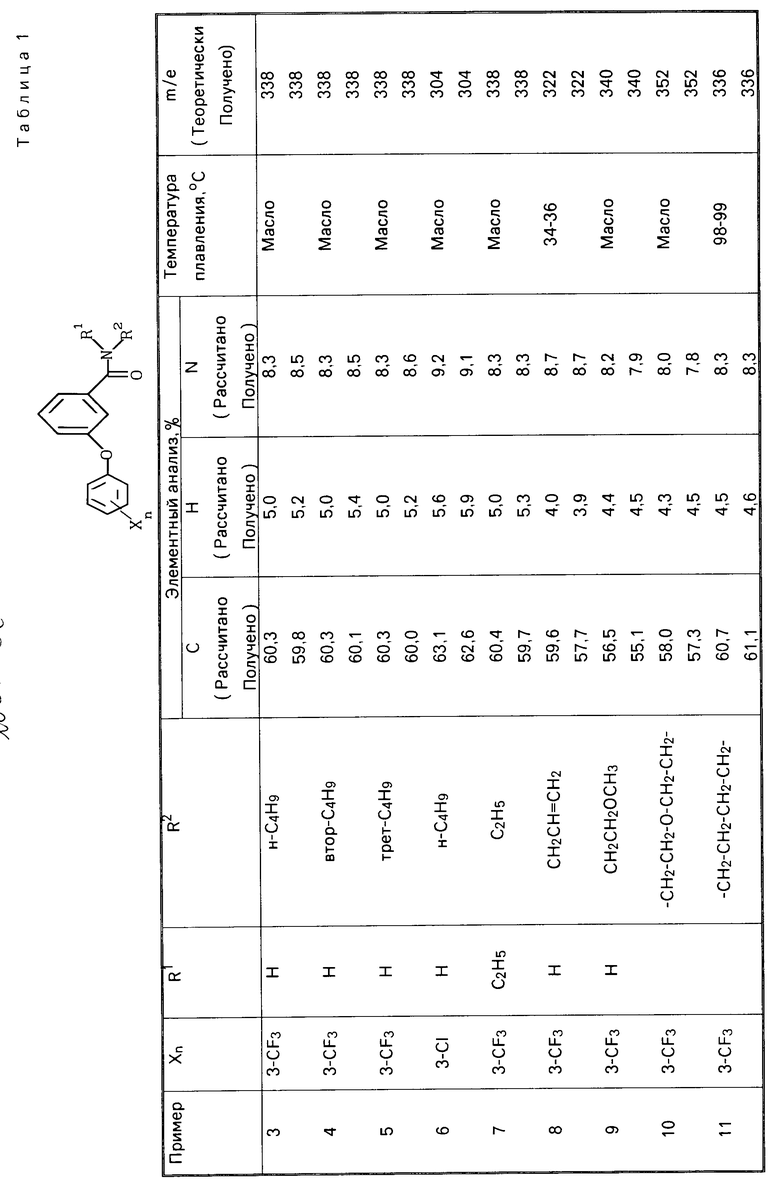
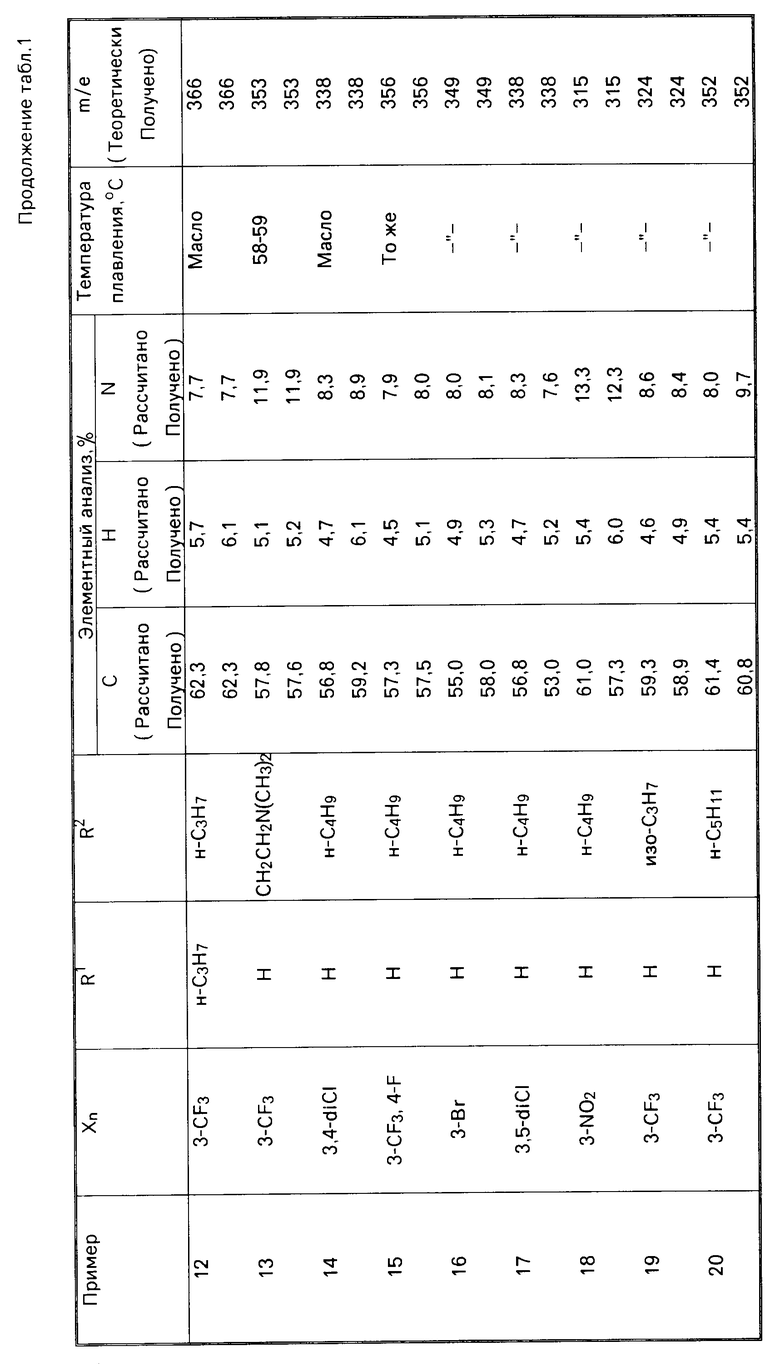
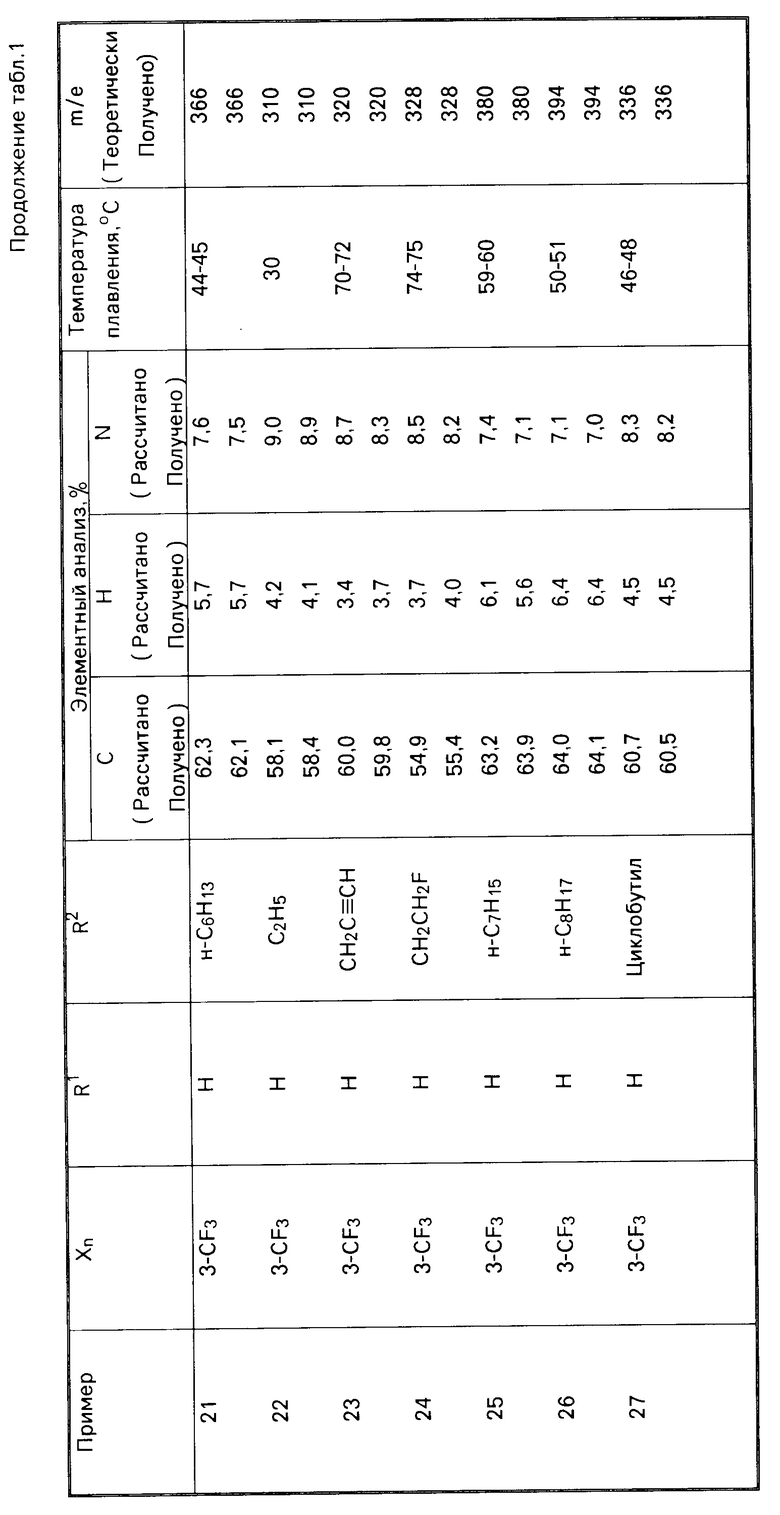
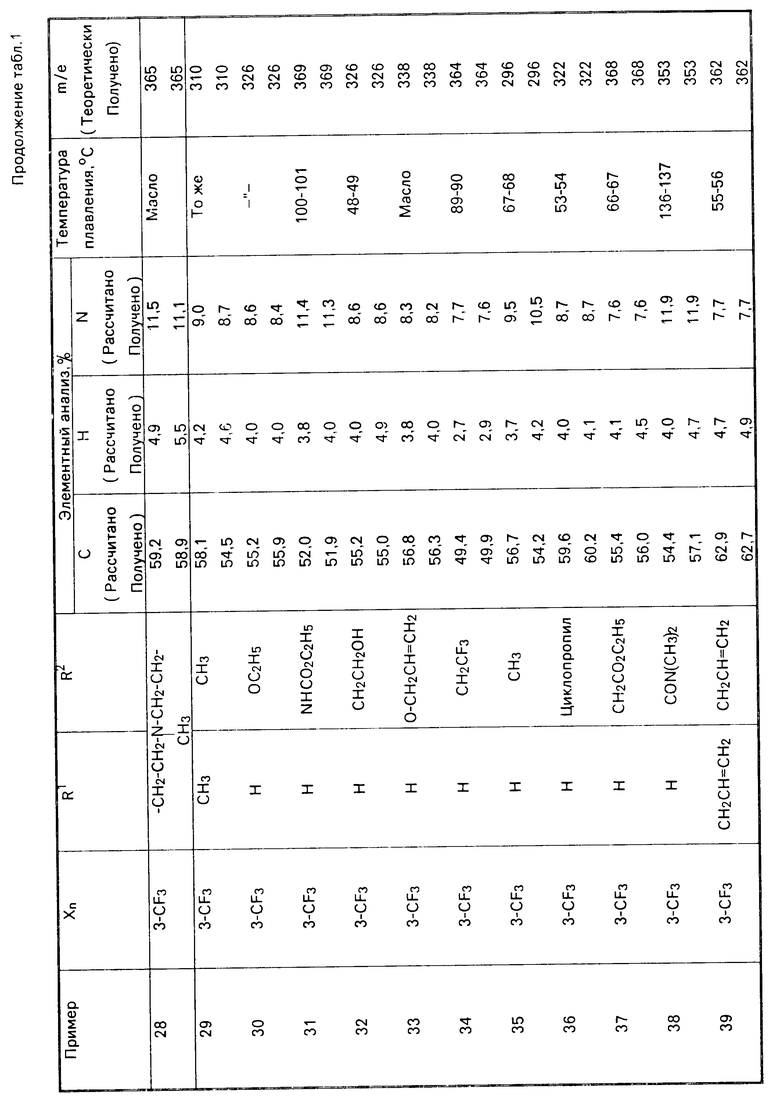
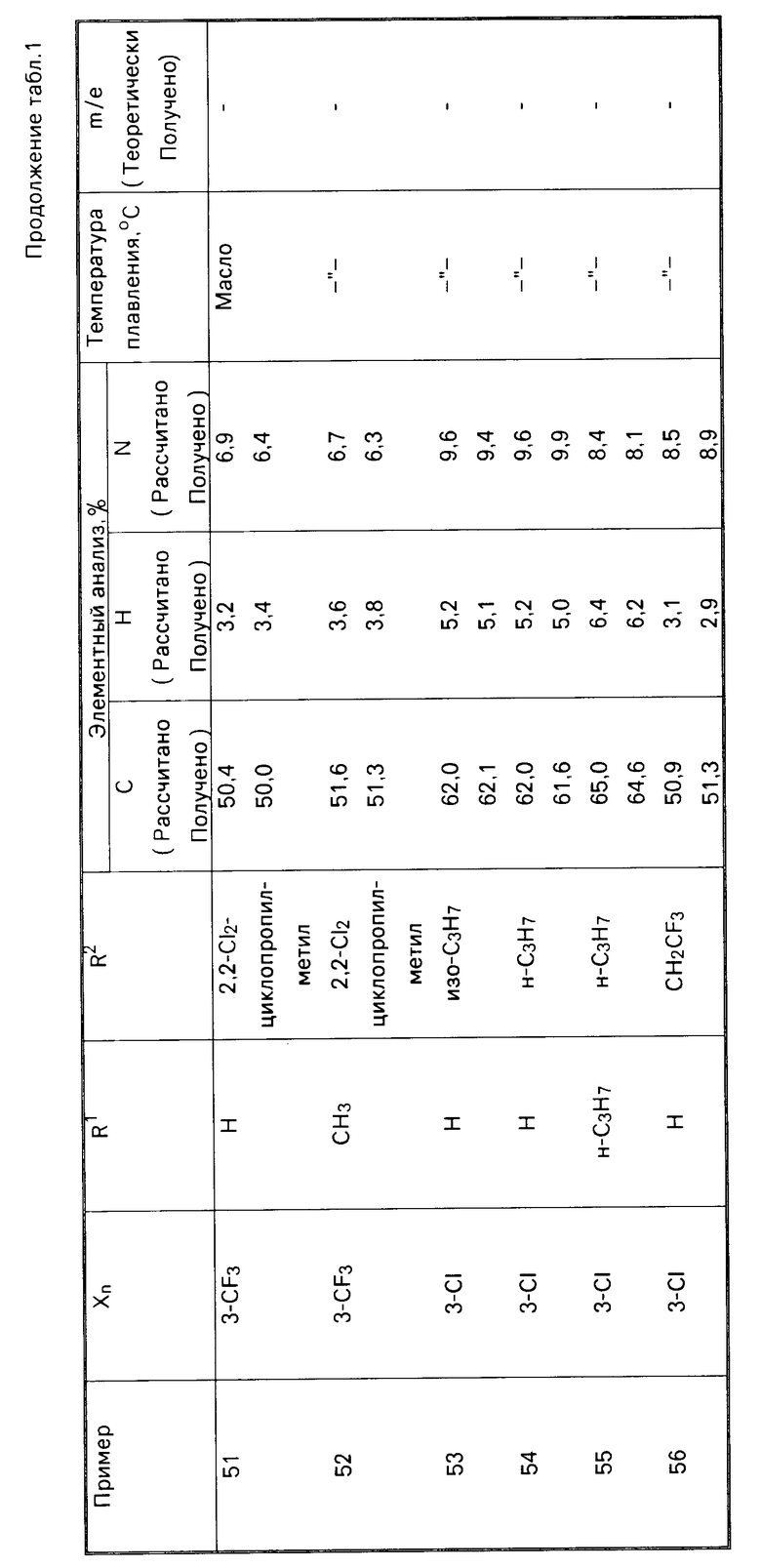
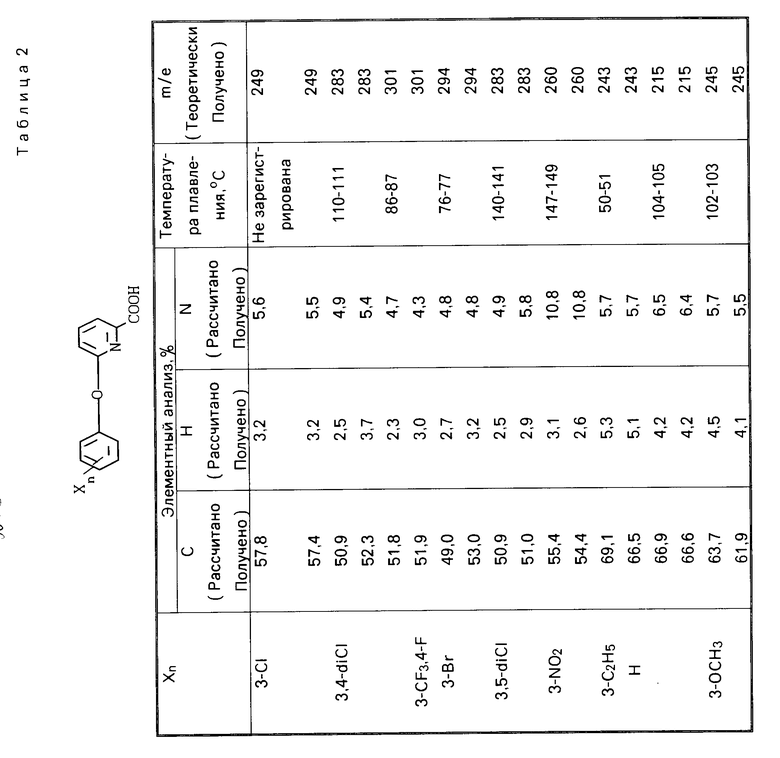
П р и м е р ы 3-61. Другие соединения, имеющие общую формулу I, были приготовлены способом, описанным в примере 2, с соответствующим выбором исходных материалов. Показатели полученных соединений, имеющих формулу I, приводятся в табл.1, а в табл.2 приводятся данные исходных кислот.
П р и м е р 62. Приготовление N-н-пропил-2-(3- α α α -трифторметилфенокси)-6-пиридинкарбоксамида.
(а). 6-хлорпиколиновую кислоту (3 г) и тионилхлорид (50 мл) кипятили с обратным холодильником в течение часа. Избыток тионилхлорида выпаривали под вакуумом, а к остаточному пиколинилхлориду добавляли дихлорметан. Раствор выливали в избыток н-пропиламина в дихлорметане. Затем раствор промывали водой, сушили над безводным сульфатом магния и выпаривали дихлорметан, при этом получали 6-хлоp-2-N-н-пропилпиридинкарбаксамид (3 г) в виде желтого масла.
Анализ
C9H11N2OCl: Рассчитано: C 54,5; H 5,5; N 14,1.
Получено: C 54,2; H 5,9; N 14,0
m/e: Теоретически: 198
Получено: 198
(б). Раствор метоксида натрия (0,4 г натрия в 20 мл метанола) добавляли к раствору 3- α α α -трифторметилфенола (2,6 г) в ксилоле (20 мл). Растворители выпаривали под вакуумом, при этом получали сухой фенолят натрия. Добавляли пиридин (14 мл) и ксилол (30 мл), а затем хлорид меди (0,4 г) и смесь нагревали до кипения. Раствор 6-хлор-2-N-н-пропилпиридинкарбоксамида (3 г) в ксилоле (20 мл) добавляли по каплям, и полученную смесь кипятили с обратным холодильником в течение 18 ч. После охлаждения смесь выливали в воду и подкисляли разбавленной соляной кислотой. Затем проводили экстрагирование диэтиловым эфиром. Соединение экстракты сушили над безводным сульфатом магния и выпаривали. Остаток очищали на колонке, заполненной силикагелем, используя 5% (объем/объем) ди этиловый эфир/дихлорметан в качестве элюента, при этом получали восстановленное исходное вещество (6-хлор-2-N-н-пропилпиридинкарбоксамид, 60%) и названное соединение (40%) в виде бесцветного масла.
П р и м е р 63, Приготовление N-н-бутил-2-(3- α α α -трифторметилфенокси)-6-пиридинтиокарбоксамида.
Смесь N-н-бутил-2-(3-α α α, -трифторметилфенокси)-6-пиридинкарбоксамида (0,6 г) и пентасульфида фосфора (1,0 г) в пиридине (50 мл) кипятили с обратным холодильником в течение 2 ч. Пиридин выпаривали, а к остатку добавляли воду. Затем водный раствор экстрагировали метиленхлоридом. Экстракты промывали разбавленной соляной кислотой, затем водой и сушили над безводным сульфатом магния. Дихлорметан выпаривали, а остаток очищали на колонке, заполненной силикагелем, используя дихлорметан в качестве элюента, при этом получали озаглавленное соединение (0,5 г) в виде твердого вещества желтого цвета, имеющего температуру плавления 61-62оС.
Анализ,
C17H17N2OF3: Рассчитано: C 57,6; H 4,8; N 7,9.
Получено: C 61,0; H 4,7; N 8,1.
m/e: Теоретически: 354
Получено: 354
П р и м е р 64. Гербицидная активность.
Для того, чтобы оценить гербицидную активность предлагаемых соединений, их испытывали, используя в качестве образца ряд растений: маис, Zea mays (MZ); рис, Orysa satiba (R); куриное просо, Echinockloa crusgalli (BG); овес, Avena sativa (O); лен, Linum usitatissimum (L); горчица, Sinapsis alba (M); сахарная свекла, Beta vulgaris (SB) и соя, Glycine max (S).
Испытания делились на две категории до прорастания и после прорастания. Испытания до прорастания включали опрыскивание почвы, засеянной семенами упомянутых видов растений, жидкой композицией, включающей предлагаемое соединение. Испытания после прорастания были двух видов, а именно орошение почвы и опрыскивание листьев. Орошение почвы проводили следующим образом: в котором росли сеянцы упомянутых видов, орошали жидкой композицией, включающей предлагаемое соединение. Пpи опрыскивании листьев сеянцы опрыскивали такой композицией.
В качестве используемой в испытаниях почвы брали приготовленную садовую плодородную землю.
Используемые в испытаниях композиции готовили из растворов испытываемых соединений в ацетоне, содержащих 0,4 мас. алкилфенолэтиленоксид конденсата, имеющего товарный знак ТР1ТО11 Х-155. Эти ацетоновые растворы разбавляли водой и полученные композиции променяли при дозировке, включающей до 5 кг или 1 кг активного вещества на гектар, что равноценно объему до 900 л на гектар при опрыскивании почвы и листьев, и при дозировке, включающей до 10 кг активного вещества на гектар, что равноценно приблизительно 3000 л на гектар при орошении почвы.
В качестве контрольной в испытаниях до прорастания использовали необработанную засеянную почву, а в испытаниях после прорастания необработанную почву, на которой растут сеянцы.
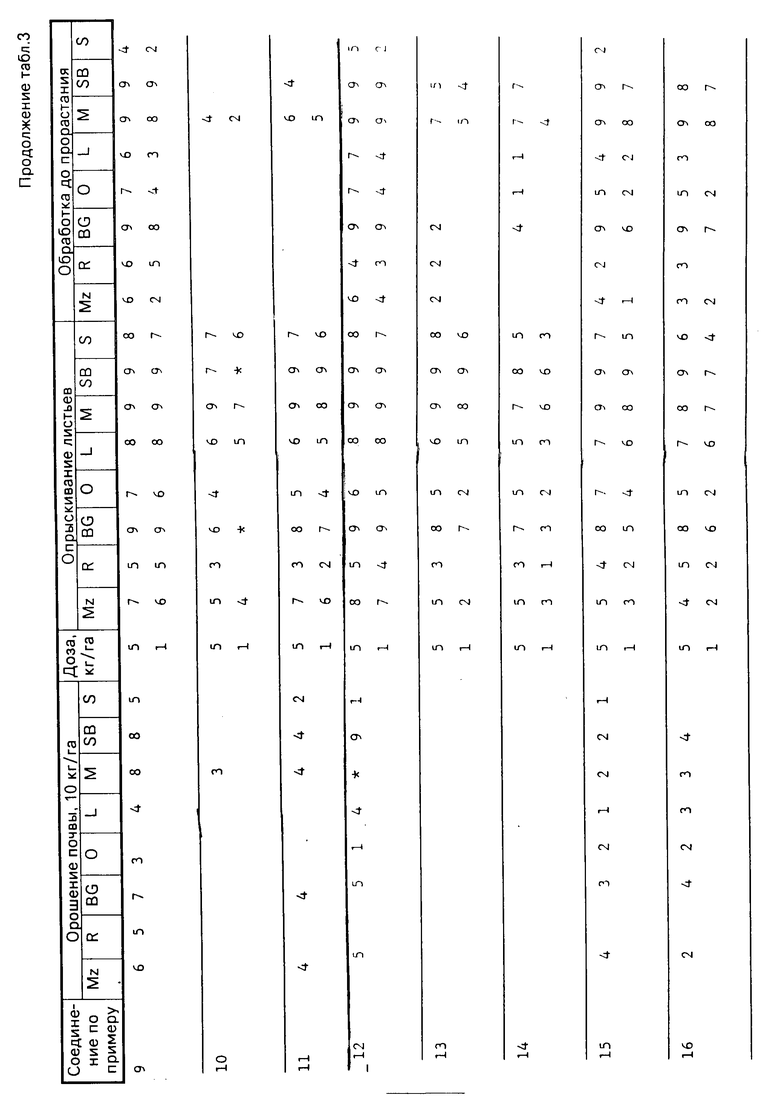
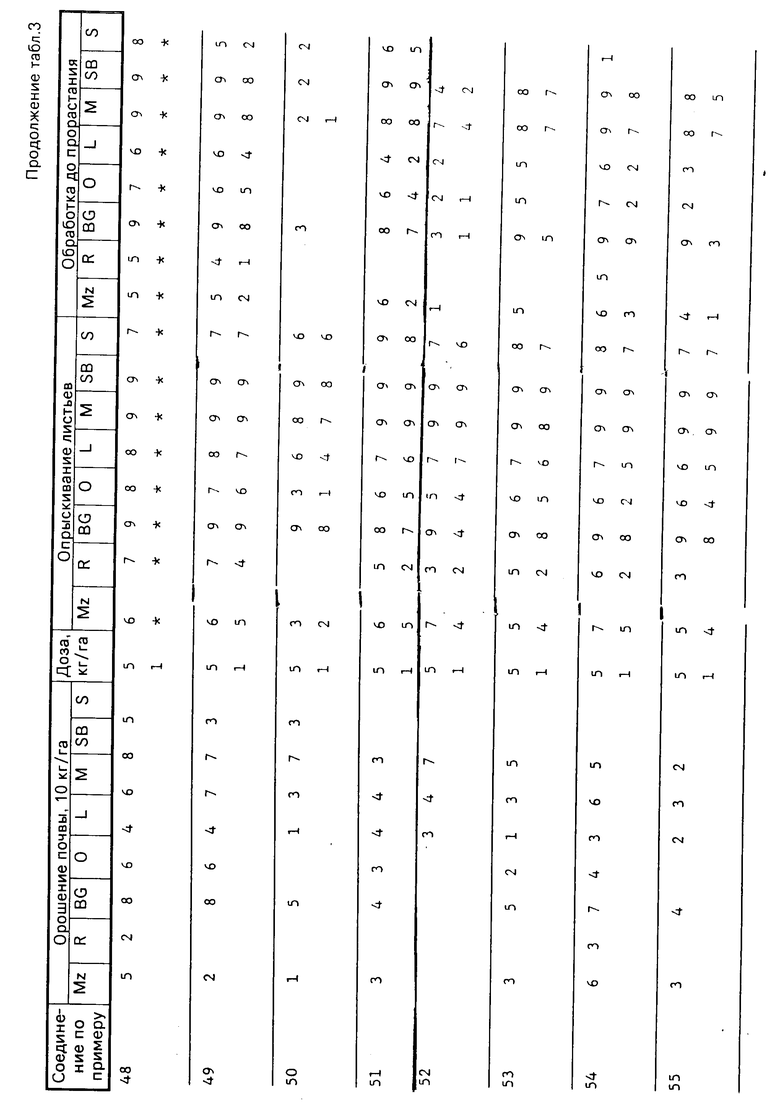
Действие гербицида на испытываемые соединения оценивали визуально через двенадцать дней после опрыскивания листьев и почвы и через тринадцать дней после орошения почвы и регистрировали по шкале 0-9. Оценка 0 обозначает рост на необработанной контрольной почве, а оценка 9 обозначает уничтожение (т.е. 100% эффективность). Увеличение на 1 единицу по линейной шкале равняется приблизительно 10%-ному увеличению эффективности.
Результаты испытаний приведены в табл.3, в которой соединения отождествляются со ссылкой на предшествующие примеры. В таблице пустое пространство обозначает оценку 0, а звездочка обозначает, что результат не был получен.
П р и м е р 65. (А) Композиция в виде смачивающегося порошка, г: 95 активного ингредиента, 3 полиметакрилат Na (диспергирующий агент), 2 октилсульфосукцинат натрия (смачивающий агент).
(В) Смачивающаяся композиция, г: 50 активного ингредиента, 3 полиметакрилат Na (диспергирующий агент), 2 октилсульфосукцинат Na (смачивающий агент) 45 чистая глина.
(С) Эмульсионные концентраты, г: 25 активного ингредиента, 45 ксилол, 20 циклогексанон, 10 эмульгатор (смесь додецилбензолсульфоната Са и нонилфенолэтоксилата).
(D) 1 г активного ингредиента, 10 г ацетона, 0,04 г Тритон Х-155 (торговая марка алкилфенол/этиленоксида конденсата) и 600 г воды.
Концентрация активного ингредиента соответственно: (A) 95% (В) 50% (С) 25% (D) 0,164%








Использование: сельское хозяйство, химические средства защиты растений. Сущность изобретения: продукт ф-лы I, где N-1 или 2, X - независимо друг от друга водород, галоген, низший алкил, возможно замещенный галогеном, низший алкоксил, нитрогруппа, Z - кислород или сера, R′ - водород, низший алкил, низший алкенил, R″ - водород, C1-C8 -алкил, возможно замещенный 1 или 3 атомами галогена, OH, CN низший алкокси, низшим алкоксикарбонилом, низшей диалкиламиногруппой, низший алкенил, низший алкинил, C3-C6 -циклоалкил, C3-C6 -циклоалкилнизший алкил, замещенный двумя атомами галогена в циклоалкильной части, низший алкоксил, низший алкенилоксил, низший алкоксикарбонил, низший алкиламин, фениламин, возможно замещенный галогеном, низший алкоксикарбониламино, низший диалкилкарбамоил, R′ и R″ вместе с атомом азота образуют морфонил, пирролидинил, 4-метилпиперазинил. Гербицидная композиция содержит эффективное количество продукта и целевые добавки. Структурная формула (см. чертеж). 3 с.п. ф-лы, 1 ил.
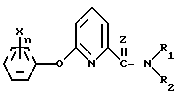
где n целое число 1 или 2;
X независимо друг от друга водород, галоген, низший алкил, возможно замещенный галогеном, низший алкоксил, нитрогруппа;
Z кислород или сера;
R1 водород, низший алкил, низший алкенил;
R2 водород, C1 C8-алкильная группа, возможно замещенная одним или тремя атомами галогена, гидрокси, циано, низшим алкокси, низшим алкоксикарбонилом, низшей диалкиламиногруппой, низший алкенил, низший алкинил, C3 C6-циклоалкил, C3 C6-циклоалкилнизший алкил, замещенный двумя атомами галогена в циклоалкильной части, низший алкоксил, низший алкенилоксил, низший алкоксикарбонил, низший алкиламин, фениламин, возможно замещенный галогеном, низший алкоксикарбониламино, низший диалкилкарбамоил;
R1 и R2 вместе с атомом азота образуют морфолил, пирролидинил, 4-метилпиперазинил,
обладающие гербицидной активностью.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Патент США N 4327218, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-06-19—Публикация
1991-11-26—Подача