Изобретение относится к производным сульфонамида, к процессам их получения и к их использованию в качестве гербицидов.
Сульфонамидные соединения хорошо известны по их биологической активности. Некоторые классы производных сульфонамида являются полезными в качестве гербицидов, в то время как другие классы являются полезными в качестве антибактериальных агентов.
Обнаружен отличный в структурном отношении класс пpоизводных сульфонамида, которые обладают полезными гербицидными свойствами.
Настоящее изобретение представляет соединение общей формулы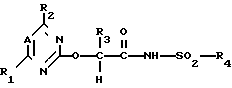 I в которой А представляет собой атом азота или группу CR5;
I в которой А представляет собой атом азота или группу CR5;
R1, R2 и R5 каждый независимо представляет собой атом водорода или галоген, формил, циано, карбокси или азидогруппу, или необязательно замещенный алкил, алкенил, алкинил, циклоалкил, алкокси, алкенилокси, алкинилокси, арилокси, алкилтио, алкенилтио, алкенилтио, арилтио, алкилкарбонил, алкоксикарбонил, амино, аминокси или диалкилиминокси группу;
R3 представляет собой атом водорода или необязательно замещенную алкильную, алкенильную, алкинильную, циклоалкильную, гетероциклическую, аралкильную или арильную группу; и
R4 представляет собой необязательно замещенную алкильную, аралкильную, арильную или гетероциклическую группу; или их соли.
Алкильный, алкенильный или алкинильный радикал или фрагмент может быть группой с прямой или разветвленной цепью. Обычно алкильный радикал или фрагмент имеет 1-12 атомов углерода, предпочтительно 1-6, особенно 1-4 атомов углерода.
Алкенильный и алкинильный радикал или фрагменты подходящим образом содержат 2-12 атомов углерода, предпочтительно 2-6, особенно 2-4 атомов углерода. Циклоалкильные группы подходящим образом имеют 3-8 кольцевых членов в виде атомов углерода.
Арильный радикал или арильный фрагмент в аралкильном, арилокси или арилтио радикале может быть одинарной или сконденсированной карбоциклической кольцевой системой, имеющей 6-10 кольцевых членов. Подходящим образом арильный радикал или фрагмент включает одинарную кольцевую систему и предпочтительно представляет собой фенильное кольцо.
Гетероциклический радикал подходящим образом представляет собой одинарную или сконденсированную, насыщенную или ненасыщенную кольцевую систему, имеющую 5-10, предпочтительно 5 или 6 кольцевых членов, из которых 1-3 кольцевых членов могут быть гетероатомами, выбранными из атомов кислорода, азота и серы.
Радикалы, представленные символами R1, R2, R3, R4 и R5, могут быть незамещенными или замещенными. Когда заместители присутствуют, замещающими группами могут быть любые из групп, обычно применяемых при модификации и/или разработке пестицидных соединений, и особенно заместители, которые сохраняют или усиливают гербицидную активность, связанную с соединениями настоящего изобретения, или влияют на устойчивость действия, проникновение в почву или растение, или способствует любому другому желательному свойству гербицидных соединений. В каждом радикале может присутствовать один или более одинаковых или различных заместителей.
Необязательные заместители для алкильной, алкенильной, алкинильной, алкокси, алкенилокси, алкинилокси, алкилтио, алкенилтио, алкинилтио, алкилкарбонильной, алкоксикарбонильной групп или алкильных фрагментов в арильных группах могут быть независимо выбраны из одного или более атомов галогена, и алкокси, алкенилокси, арилокси, гидрокси, алкилтио, арилтио, арильных, алкилсульфонильных, алкилсульфинальных, алкилендиокси, алкилендитио, галоидалкильных и алкоксикарбонильных групп, гетероциклических групп, и диалкилиминокси, необязательно замещенных амино, триалкилсилильных, алкилкарбонильных, арилкарбонильных, алкоксикарбонильных, карбокси, циано, тиоцианато и необязательно замещенных аминокарбонильных групп.
Необязательные заместители для арильной, циклоалкильной, арилокси или арилтио групп, гетероциклических колец или арильных фрагментов в аралкильных группах могут быть независимо выбраны из одного или более атомов галогена и нитро, циано, алкильных, галоидалкильных, алкокси, галоидолкокси, алкилтио, алкилсульфонильных, моно- или диалкилсульфонамидо, арилокси, карбокси, алкоксикарбонильных и аралькоксикарбонильных групп.
Необязательные заместители для аминогрупп или для аминофрагмента в аминокси или аминокарбонильной группе могут быть подходящим образом независимо выбраны из алкильной, алкенильной, арильной, алкокси, амино, моно- или диалкиламино, ариламино, алкоксиалкильной, галоидалкильной, гидрокси, гидроксиалкильной, циано, карбоксиалкильной или алкилкарбониламино, или амино группа может образовывать часть гетероциклического кольца.
Подходящими солями изобретения являются сельскохозяйственно приемлемые соли соединений общей формулы 1. Соли могут образовываться с неорганическими или органическими катионами с помощью обычных способов. Такие соли подходящим образом включают соли с неорганическими катионами, происходящими из щелочных металлов и щелочно-земельных металлов, таких как, например, натрий, калий, кальций и магний, и из переходных металлов, например, меди, и соли с органическими катионами, такими как алкиламмониевый и алкилсульфониевый катионы.
Алкильный радикал или фрагмент, когда он присутствует в качестве заместителя или в виде части замещающей группы, предпочтительно имеет 1-4 атомов углерода, особенно 1 или 2 атома углерода. Галоидалкильный или галоидалкокси радикал подходящим образом имеет 1-3 атомов галогена; предпочтительным галоидалкильным радикалом является трифторметильная группа, а предпочтительным галоидалкокси радикалом является трифторметокси группа. Как заместитель алкенильный фрагмент подходящим образом имеет 2-4 атомов углерода. Арильный радикал, когда он присутствует в виде заместителя, предпочтительно является фенильной группой.
Атом галогена в качестве заместителя подходящим образом представляет собой атом фтора, хлора или брома.
А предпочтительно представляет собой атом азота или группу СН.
Подходящие примеры радикалов R1 и R2 включают С1-С4-алкильные группы и С1-С4-алкокcи группы. Предпочтительно R1 и R2 независимо выбраны из метильных групп и метокси групп.
Подходящие примеры радикала R3 включают водород, необязательно замещенный С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С3-С6-циклоалкил, фен С1-С4-алкил, бензильные и фенильные группы, и 5- или 6-членные гетероциклические группы. Предпочтительно радикал R3 выбран из атомов водорода, С1-С4-алкильных групп и фенильных групп.
Подходящим образом радикал R4 представляет собой С1-С6-алкильную группу или необязательно замещенную фенильную или бензильную группу или тиенильную группу. Предпочтительно, R4 представляет собой С1-С4-алкильную группу, особенно метильную группу, незамещенную фенильную группу или фенильную группу, замещенную одним или более, предпочтительно 1 или 2, одинаковых или различных заместителей, выбранных из атомов галогена, нитро групп и С1-С4 алкильной, С1-С4галоидалкильной, С1-С4-галоидалкокси, карбокси и С1-С4-карбонильной групп. Особенно предпочтительными заместителями являются фтор, хлор, бром, нитро, метил, трихлорметил, трифторметокси и метоксикарбонил.
Должно быть понятно, что соединения настоящего изобретения, в которых R3 является отличным от атома водорода, имеют асимметричный атом углерода и, следовательно, существуют в различных стереоизомерных формах. Настоящее изобретение соответственно включает все индивидуальные изомерные формы соединений общей формулы 1 и смеси их в любых пропорциях. Так, в объеме настоящего изобретения включены R и S-энантиомеры соединения общей формулы 1А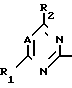 O
O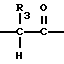 NH
NH SO
SO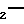 R4 IА в которой А, R1, R2 и R4 имеют значения, определенные выше, и R3является отличным от атома водорода, и их смеси.
R4 IА в которой А, R1, R2 и R4 имеют значения, определенные выше, и R3является отличным от атома водорода, и их смеси.
Настоящее изобретение далее представляет способ получения соединения настоящего изобретения, который включает
a) взаимодействие соединения общей формулы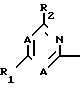 O
O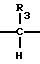 CO2H II
CO2H II
в которой А, R1, R2 и R3 имеют значения, определенные выше, или соответствующего сложного эфира, хлорангидрида кислоты или ангидрида кислоты с соединением общей формулы
NH2SO2R4 /III/ в которой R4 имеет значения, определенные ранее, или его солью, если необходимо, в присутствии агента, активирующего карбоксил, или
b) взаимодействие соединения общей формулы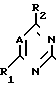
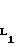 IV в которой А, R1 и R2 имеют значения, определенные ранее, а L1представляет собой удаляемую группу, с ди-солью соединения общей формулы
IV в которой А, R1 и R2 имеют значения, определенные ранее, а L1представляет собой удаляемую группу, с ди-солью соединения общей формулы
L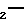
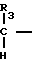
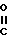 NHSO2R4 V в которой R3 и R4 имеют значения, определенные ранее, и L2 представляет гидрокси группу, и, если необходимо или желательно, превращение получающегося в результате соединения в любое другое соединение изобретения.
NHSO2R4 V в которой R3 и R4 имеют значения, определенные ранее, и L2 представляет гидрокси группу, и, если необходимо или желательно, превращение получающегося в результате соединения в любое другое соединение изобретения.
Удаляемой группой является любая группа, которая будет в условиях реакции отщепляться от исходного материала, промотируя таким образом реакцию в определенном участке.
Удаляемой группой в соединении общей формулы IV удобным образом является атом галогена, например, атом брома, хлора или иода, или, особенно для пиримидиновых исходных материалов, алкансульфонильная группа, например, метансульфонил.
Ди-солью соединения V подходящим образом является ди(щелочно-металлическая) соль, предпочтительно ди-натриевая соль.
Процесс (a) подходящим образом осуществляется при комнатной или повышенной температуре, т. е. при температуре выше 20оС. Предпочтительным температурным интервалом для осуществления реакции является интервал от 20 до 80оС; особенно подходящая температура реакции находится в интервале от 20 до 50оС. Молярное отношение реагента II к реагенту III может быть, например, в интервале 1,0-5,0, предпочтительно 1,0-2,5.
Реакция (a) подходящим образом осуществляется в интервале органическом растворителе, таким как углеводородный растворитель, например, бензол или толуол, хлорированный углеводород, например, дихлорметан или хлороформ, спирт, например, метанол или этанол, простой эфир, например диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, кетон, например, ацетон или метилэтилкетон, сложный эфир, например, этилацетат, апротонный полярный растворитель, например, диметилформамид, диметилацетамид или диметилсульфоксид или натрил, например, ацетонитрил.
Предпочтительно реакция (a) осуществляется в присутствии третичного амина, например, триэтиламина. Другие подходящие третичные амины включают пиридин и 1,8-диазабицикло (5.4.0)ундец-7-ен.
Когда реагент II находится в форме свободной карбоновой кислоты, карбоксигруппу нужно активировать для протекания реакции. Подходящие карбоксил-активирующие агенты включают 2-хлор-N-метилпиридинийиодид, дициклогексилкарбодиимид и карбонилдиимидазол. Подходящим образом кислотный реагент II активируется карбоксилактивирующим агентом в присутствии инертного органического растворителя при комнатной или повышенной температуре, например, при температуре в интервале от 20оС до температуры кипения с обратным холодильником смеси, перед добавлением реагента III и, если необходимо, третичного амина.
Процесс (b) подходящим образом осуществляется при температуре в интервале от комнатной до температуры дефлегмации реакционной среды, предпочтительно в интервале от 100 до 150оС, например при 120оС. Молярное отношение реагентов IV:V составляет подходящим образом в интервале 1,0-2,5.
При реакции (b) ди-соль может подходящим образом получаться из соединения V, в котором L2 представляет собой гидроксигруппу с помощью действия щелочного металла, такого как металлический натрий или калий, или, удобным образом, сильного основания, например, гидрида щелочного металла, такого как гидрид натрия или калия, гидрида щелочно-земельного металла, такого как гидрид кальция, алкоголята щелочного металла, такого как трет-бутилат калия, или гидроокиси щелочного металла, такой как гидроокись натрия или калия. Подходящим образом превращения соединения V в ди-соль происходит на месте.
Подходящим образом реакция (b) осуществляется в присутствии растворителя; типичными растворителями являются, например, растворители те же самые, что указаны выше для процесса (a).
Соединение общей формулы (I), полученное по любому из способов (a) или (b), может превращаться в другое соединение общей формулы I по способам, известным специалистам в данной области, при условии, что проявляется забота для обеспечения того, чтобы сульфонамидная группа не испытывала отрицательного воздействия.
Так, например, соединений общей формулы I, где R1 и/или R2представляет собой атом галогена, подходящим образом хлор, может преобразовываться в другие производные с помощью нуклеофильного замещения, например, с помощью реакции с двумя эквивалентами амина, такого как диметиламин, давая соответствующее соединение общей формулы I, в которой R1 и/или R2 представляет собой замещенную аминогруппу. Аналогичным образом, соединение общей формулы I, в которой R1 и/или R2представляет собой атом галогена, может подвергаться взаимодействию с двумя эквивалентами алкилтиометаллорганического соединения, например, метантиолата натрия, давая соответствующее соединение общей формулы I, в которой R1 и/или R2 представляет собой алкилтиогруппу, такую как метилтио, или может гидрироваться, давая соответствующее соединение, в котором R1 и/или R2 представляют атом водорода.
Реакции превращения кислоты и соли могут осуществляться с использованием общепринятых приемов соответствующим образом.
Индивидуальные энантиомеры могут получаться с использованием стереоспецифических реагентов или с помощью общепринятых приемов разделения или расщепления.
Полученные соединения изобретения могут, если необходимо, выделяться и очищаться с использованием обычных технологических приемов.
Подходящие исходные карбоновые кислоты общей формулы II и их сложные эфиры, а также их получение описаны и заявлены в Европейской патентной заявке N 90201334.1. Так, исходные карбоновые кислоты общей формулы II и их сложные эфиры могут получаться или с помощью реакции соединения общей формулы.
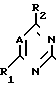
 VI в которой R1, R2 и А имеют значения, определенные выше, и представляет удаляемую группу, например, атом галогена или алкансульфонильную группу, с соединением общей формулы:
VI в которой R1, R2 и А имеют значения, определенные выше, и представляет удаляемую группу, например, атом галогена или алкансульфонильную группу, с соединением общей формулы:
H 
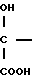 R3 VII в которой R3 имеет значения, определенные выше, или его сложным эфиром, или для соединений, в которых А представляет CR5, с помощью реакции соединения общей формулы:
R3 VII в которой R3 имеет значения, определенные выше, или его сложным эфиром, или для соединений, в которых А представляет CR5, с помощью реакции соединения общей формулы: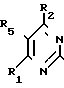
 VIII в которых R1, R2 и R5 имеют значения, определенные выше, предпочтительно со сложным эфиром соединения общей формулы:
VIII в которых R1, R2 и R5 имеют значения, определенные выше, предпочтительно со сложным эфиром соединения общей формулы:
H 
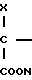 R3 IX в которой R3 имеет значения, определенные выше, и Х представляет удаляемую группу, например, атом галогена или сульфонилокси группу, и, если необходимо или желательно, осуществляют превращение получающегося в результате сложного эфира в другой сложный эфир или в соответствующую кислоту, или превращение кислоты в другую кислоту или сложный эфир. Производные хлорангидрид кислоты или ангидрид кислоты получаются из соединений формулы II с помощью стандартных приемов.
R3 IX в которой R3 имеет значения, определенные выше, и Х представляет удаляемую группу, например, атом галогена или сульфонилокси группу, и, если необходимо или желательно, осуществляют превращение получающегося в результате сложного эфира в другой сложный эфир или в соответствующую кислоту, или превращение кислоты в другую кислоту или сложный эфир. Производные хлорангидрид кислоты или ангидрид кислоты получаются из соединений формулы II с помощью стандартных приемов.
Реагенты общей формулы III являются или известными или могут получаться с использованием приемов, описанных в литературе.
Исходные триазиновые соединения общей формулы IV и VI (т.е. в которых А атом азота) являются или известными, или могут быть получены с использованием приемов, описанных в литературе. Например, такие соединения могут получаться из 2,4,6-трихлортриазина с помощью таких способов, как описание авторами Dudley et al, J.Am.Chem.Soc. 73, 2986, (1951), Koopman et al, Rec. Trav.Chim. 79, 83, (1960), Hirtetal, Helv.Chim. Acta, 33, 1365, (1950), Kobe et al, Monatshe fte fur Chemie, 101, 724, (1970) и Ross et al, описание к патенту США N 3316263.
Исходные пиримидины общей формулы IV и VIII могут получаться с помощью общепринятых приемов, например, с помощью методов, описанных в Heterocyclic compounds, 16 "The Pyrimidines", изд. Д. Brown, Interscience, 1962.
Соединения общей формулы V могут быть получены из соответствующих бензилокси производных: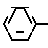 CH
CH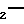 O
O 
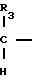
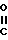 NHSO2R4 с помощью гидрирования, подходящим образом с использованием газообразного водорода в сочетании с палладиевым или платиновым катализатором на угле. Бензилокси производные могут быть получены по способу, аналогичному реакции (a), описанной выше, с помощью взаимодействия соответствующей 2-бензилоксикарбоновой кислоты:
NHSO2R4 с помощью гидрирования, подходящим образом с использованием газообразного водорода в сочетании с палладиевым или платиновым катализатором на угле. Бензилокси производные могут быть получены по способу, аналогичному реакции (a), описанной выше, с помощью взаимодействия соответствующей 2-бензилоксикарбоновой кислоты: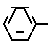 CH
CH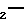 O
O 
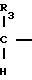
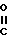 -OH или ее реакционноспособного производного с соединением общей формулы III, описанным выше, или ее солью.
-OH или ее реакционноспособного производного с соединением общей формулы III, описанным выше, или ее солью.
Соединения общей формулы VII являются или известными, или могут быть получены с помощью общепринятых процедур. Соединения, в которых R3представляет арильную группу, могут, например, получаться с помощью обработки соответствующего альдегида, R3CHO, с подходящим цианидным соединением, например, цианидом калия или триметилсилилцианидом, соответственно с иодистым цинком или бисульфитом натрия, с последующим превращением циано заместителя в кислотную группу, см. например. Schnur and Morville, J. Med. Chem. 29, 770 (1986) и патентное описание США N 4537623. Соединения, в которых R3 представляет алкильную группу, могут, например, получаться по способу Коlasа и Miller, J. Org. Chem. 52, 4978 (1987), исходя из подходящей аминокислоты с помощью превращения в 2 стадии.
Соединения общей формулы IX могут получаться с помощью общепринятых приемов, например, с помощью галоидирования соответствующего соединения, например, с помощью процедуры, описанной Еpstein et al. J. Med. Chem. 24, 481 (1981).
Соединения общей формулы I, как было найдено, обладают активностью в качестве гербицидов, проявляя широкий спектр активности до и после появления всходов против нежелательных видов растений.
Настоящее изобретение, следовательно, представляет гербицидную композицию, которая включает соединение настоящего изобретения в сочетании с носителем.
Предпочтительно в композиции настоящего изобретения имеются, по крайней мере, два носителя, по крайней мере, один из которых является поверхностно-активным агентом.
Настоящее изобретение далее предлагает использование соединения согласно изобретению в качестве гербицида.
Далее в соответствии с изобретением предлагается способ уничтожения нежелательного роста растений на участке их распространения с помощью обработки указанного участка соединением или композицией согласно изобретению. Участком может быть, например, почва или растения на площадях посадки сельскохозяйственных культур. Применение по отношению к участку может быть довсходовым или после появления всходов. Доза используемого активного ингредиента может составлять, например, от 0,01 до 10 кг/га, предпочтительно 0,05-5 кг/га.
Носителем в композиции согласно изобретению может быть любой материал, с которым активный ингредиент формулируется для облегчения применения по отношению к подлежащему обработке участку, которым может быть, например, растение, семена или почва, или для облегчения хранения, транспортировки или обращения с ними. Носитель может быть твердым или жидким, включая материал, который обычно является газообразным, но который сжат для образования жидкости, и может использоваться любой из носителей, обычно используемых при приготовлении препаративных форм гербицидных композиций. Предпочтительно композиции согласно изобретению содержат 0,5-95% по весу активного ингредиента.
Подходящие твердые носители включают природные и синтетические глины и силикаты, например, природные кремнеземы, такие как диатомовые земли; силикаты магния, например, тальки; алюмосиликаты магния, например, аттапульгиты и вермикулиты; силикаты алюминия, например, каолиниты, монтмориллониты и слюды; карбонат кальция; сульфат кальция; сульфат аммония; синтетические гидратированные окиси кремния и синтетические силикаты кальция или алюминия; элементы, например, углерод и серу; природные и синтетические смолы, например, кусароновые соли, поливинилхлорид и полимеры и сополимеры стирола; твердые полихлорфенолы; битумы; воски; и твердые удобрения, например, суперфосфаты.
Подходящие жидкие носители включают воду; спирты, например, изопропанол и гликоли; кетоны; например, ацетон, метилэтилкетон, метилизобутилкетон и циклогексанон; простой эфир; ароматические или аралифатические углеводороды, например, бензол, толуол и ксилол; нефтяные фракции, например, керосин и легкие минеральные масла; хлорированные углеводороды, например, четыреххлористый углерод, перхлорэтилен и трихлорэтан. Часто подходящими являются смеси различных жидкостей.
Сельскохозяйственные композиции часто формулируются и транспортируются в концентрированном виде, который впоследствии разбавляется пользователем перед применением. Присутствие небольших количеств носителя, которым является поверхностно-активный агент, облегчает данный процесс разбавления. Так, предпочтительно, чтобы, по крайней мере, один носитель в композиции согласно изобретению был поверхностно-активным агентом. Например, композиция может содержать, по крайней мере, два носителя, по крайней мере, один из которых является поверхностно-активный агент.
Поверхностно-активным агентом может быть эмульгирующий агент диспергирующий агент или смачивающий агент; он может быть неионным или ионным.
Примеры подходящих поверхностно-активных агентов включают натриевые или кальциевые соли полиакриловых кислот и лигнинсульфокислот; продукты конденсации жирных кислот или алифатических аминов или амидов, содержащих, по крайней мере, 12 атомов углерода в молекуле, с окисью этилена и/или окисью пропилена; сложные эфиры жирных кислот и глицерина, сорбита, сахарозы или пентаэритрита; конденсаты этих соединений с окисью этилена и/или окисью пропилена; продукты конденсации жирного спирта или алкилфенилов, например, п-октил-фенола или п-октил-крезола, с окисью этилена и/или окисью пропилена; сульфаты или сульфонаты этих продуктов конденсации; соли щелочных или щелочно-земельных металлов, предпочтительно натриевые соли сложных эфиров серной или сульфоновой кислот, содержащих, по крайней мере, 10 атомов углерода в молекуле, например, лаурилсульфат натрия, вторичные алкилсульфаты натрия, натриевые соли сульфированного касторового масла, и алкиларилсульфонаты натрия, такие, как додецилбензолсульфонаты; и полимеры окиси этилена и окиси пропилена.
Композиции изобретения могут также содержать другие активные ингредиенты, например, соединения, обладающие инсектицидными или фунгицидными свойствами или другие гербициды.
П р и м е р 1. 2-(4,6-Диметилпиримидин-2-ил)окси-N-фенилсульфонилпропионамид.
a) Метил 2-(4,6-диметилпиримидин-2-ил)оксипропионат.
2-Гидрокси-4,6-диметилпиримидин (37,1 г, 0,299 моля) в 500 мл ацетона доводился почти до температуры дефлегмации. Затем быстpо с помощью капельной воронки добавлялось 50 г (0,299 моля) метил 2-бромпропионата, и порциями добавлялся карбонат калия (41,3 г 0,288 моля). Смесь нагревалась с обратным холодильником в течение ночи. После отфильтровывания белого осадка ацетон удалялся из фильтрата с помощью выпаривания, и неочищенный жидкий продукт очищался с помощью мгновенной хроматографии на колонке. Получалось 19,6 г (0,093 моля) требуемого соединения в виде бледно-желтого масла.
Выход: 31 по массе.
ЯМР δ (CDCl3): 6,57 (1H, c), 5,17 (1H, кв), 3,60 (3Н, с), 2,25 (6Н, с), 1,51 (3Н, с), млн. дол. b) 2-(4,6-Диметилпиримидин-2-ил)оксипропионовая кислота.
Продукт стадии (a) (16,76 г, 0,0798 моля) растворялся приблизительно с 150 мл метанола, при перемешивании добавлялось около 150 мл 10% по массе гидроокиси натрия. После нахождения в течение 30 мин при комнатной температуре метанол удалялся с помощью выпаривания, и оставшаяся смесь обрабатывалась 10% по массе соляной кислотой (pH 2). Белое твердое вещество, желаемый продукт, осаждался из раствора и выделялся с помощью фильтрования. Твердое вещество далее очищалось с помощью растирания с диэтиловым эфиром. После сушки общий выход требуемого продукта, полученного с помощью данной процедуры, был приблизительно 100% по весу (16,06 г, 0,082 моля целевого соединения).
Точка плавления: 117оС.
с) 2-(4,6-Диметилпиримидин-2-ил)окси-N-фенилсульфонилпропионамид
Триэтиламин (2,84 г, 0,028 моля) добавлялся к 2,00 г (0,0102 моля) продукта стадии (b) в сухом ацетонитриле (100 мл), а затем при 50оС добавлялось также 3,00 г, 0,0118 моля, 2-хлор-N-метилпиридинийиодида. Смесь перемешивалась при 50оС в течение 30 мин, а затем добавлялось 3,32 г (0,0212 моля) бензолсульфонамида и 1,42 г (0,014 моля) триэтиламина, и перемешивание продолжалось при 50оС в течение еще 30 мин. Смеси давали возможность охладиться до температуры окружающей среды (примерно 20оС) и оставляли ее на ночь, причем в течение всего периода поддерживалось перемешивание. Затем с помощью выпаривания удалялся ацетонитрил, добавлялось 50 мл воды, смесь подкислялась до pH 2, добавлялось 50 мл диэтилового эфира, и раствор энергично перемешивался в течение 1 часа. Желаемый продукт, бежевое твердое вещество, образовывалось и отфильтровывалось в сушилке.
Получалось 2,13 г целевого соединения, выход 62% по весу.
Точка плавления: 188,0oC.
Элементный анализ, Вычислено: С 53,7; Н 5,1; N 12,5 Найдено: С 53,8; Н 5,1; N 12,4
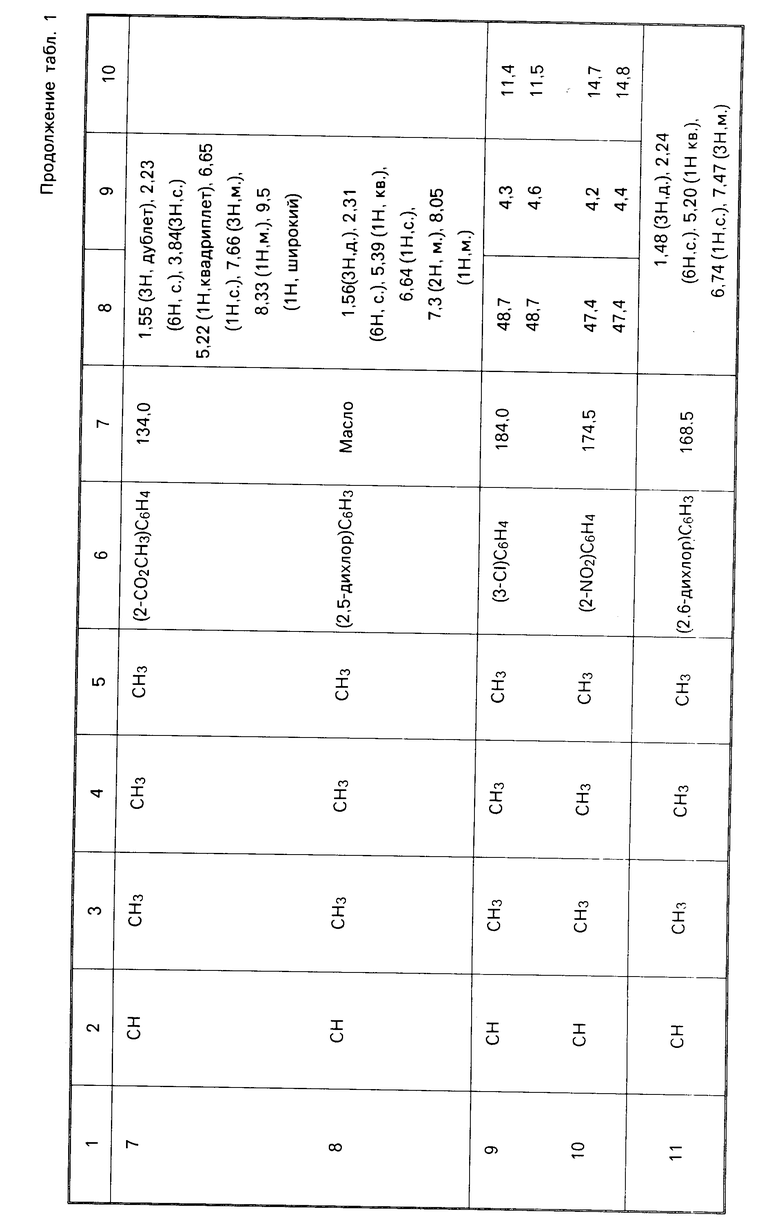
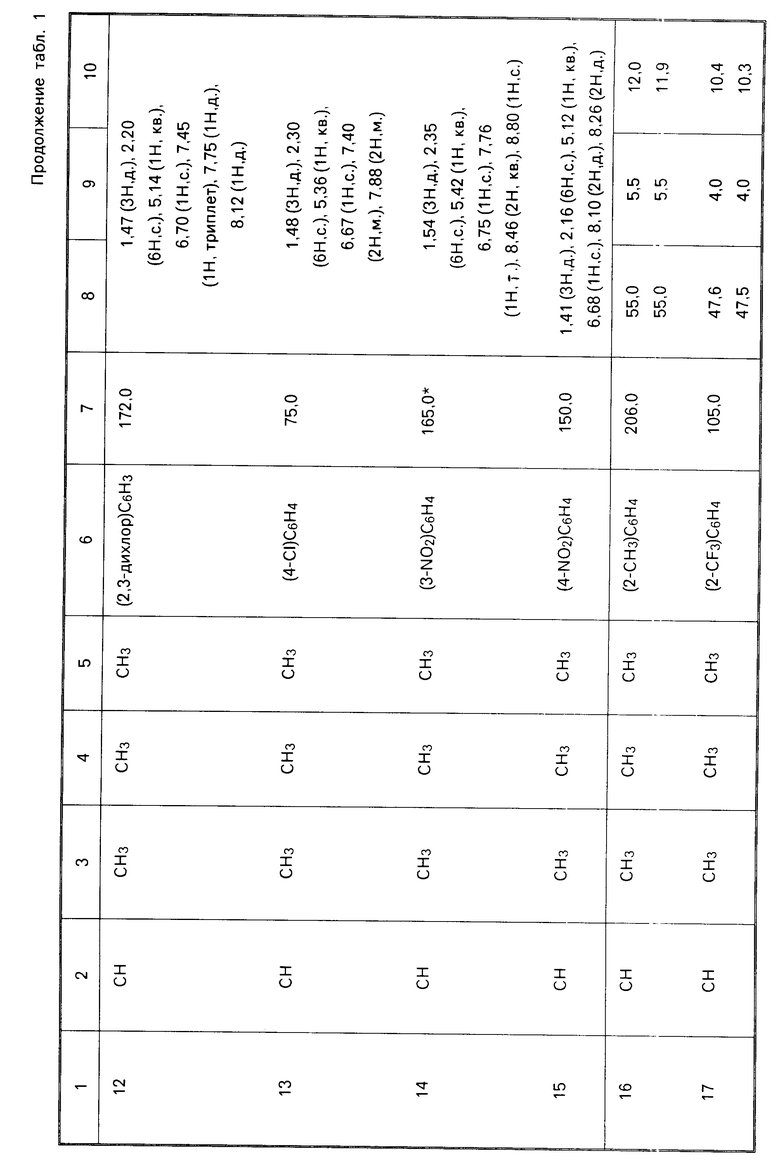
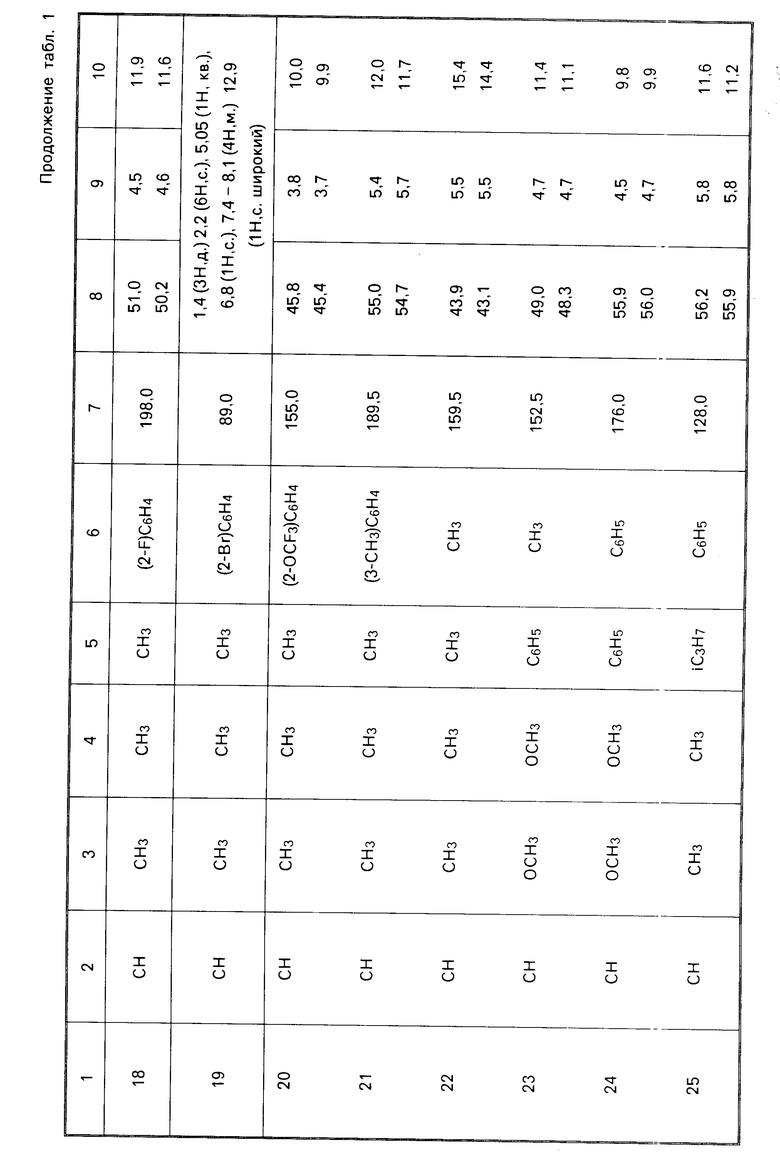
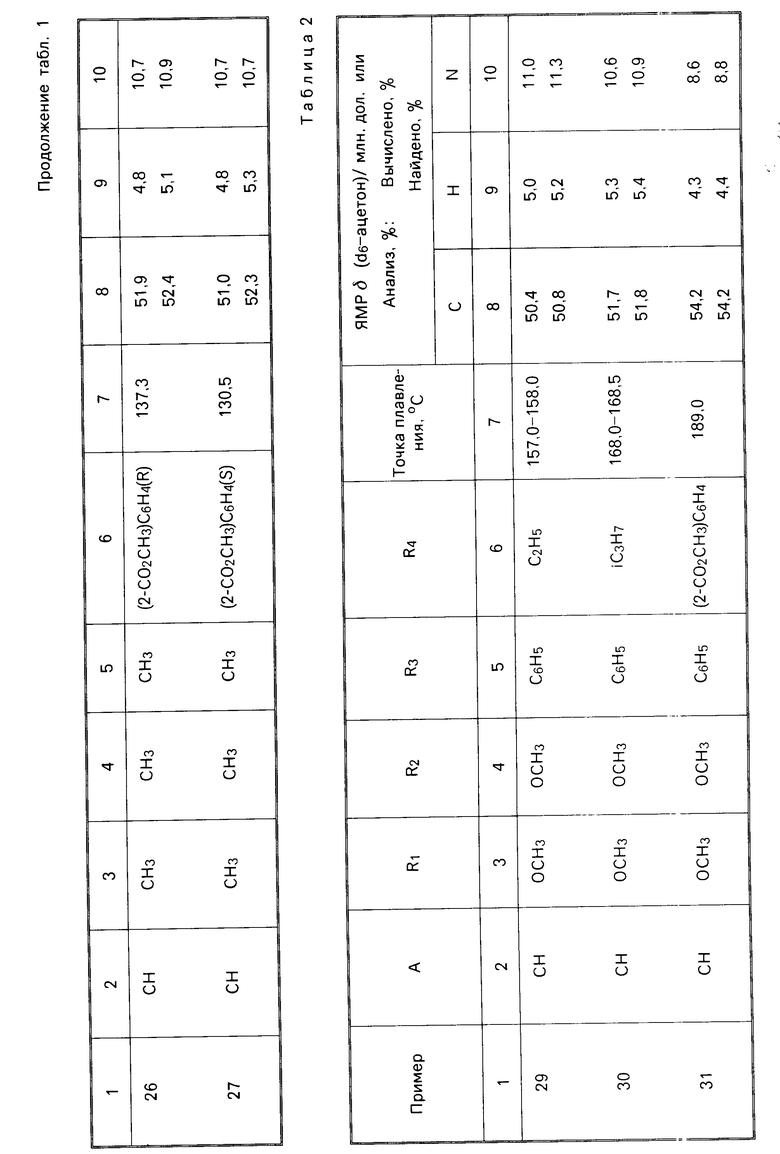
П р и м е р ы 2-25. Следующие соединения общей формулы I были получены по способу, аналогичному способу, описанному в примере 1 выше. Аналитические и физические данные даны в табл.1. Звездочка у точки плавления в табл. 1 обозначает "с разложением". Определения ЯМР, данные для примеров 11, 12 и 15, осуществлялись в d6-ацетоне, а не в дейтерохлороформе (CDCl3).
П р и м е р 28. 2-(4,6-Диметоксипиримидин-2-ил)окси-N-(метилсульфонил)пропион- амид.
К раствору 1,1-карбонилдиимидазола (1,70 г, 0,0105 моля) в сухом тетрагидрофуране (130 мл) добавлялась по каплям при комнатной температуре 2-(4,6-диметоксипиримидин-2-ил)оксипропионовая кислота (2,28 г, 0,01 моля), полученная, как описано в 1 (b) выше, в тетрагидрофуране (30 мл). Раствор нагревался с обратным холодильником в течение получаса и оставлялся охлаждаться. В виде одной порции твердого вещества добавлялся метансульфонамид (0,95 г, 0,01 моля), и смесь перемешивалась в течение 15 минут перед тем, как добавлялся 1,8-диазабицикло(5.6.0)ундец-7-ен (1,52 г, 0,01 моля) в тетрагидрофуране (30 мл) по каплям при комнатной температуре (примерно 20оС). После непродолжительного периода тетрагидрофуран удалялся, и остаток подкислялся раствором 1М соляной кислоты. Продукт экстрагировался хлороформом; подвергался обратной промывке водой и сушился. Растворитель удалялся, и продукт очищался на силикагеле при элюировании 3% по объему смесью метанол/хлороформ, давая целевое соединение в виде твердого вещества (1,79 г).
Выход: 50% по весу.
Точка плавления: 178,0оС.
Элементный анализ, Вычислено: C 39,4; H 4,9; N 13,8 Найдено: С 38,5; H 4,9; N 13,0
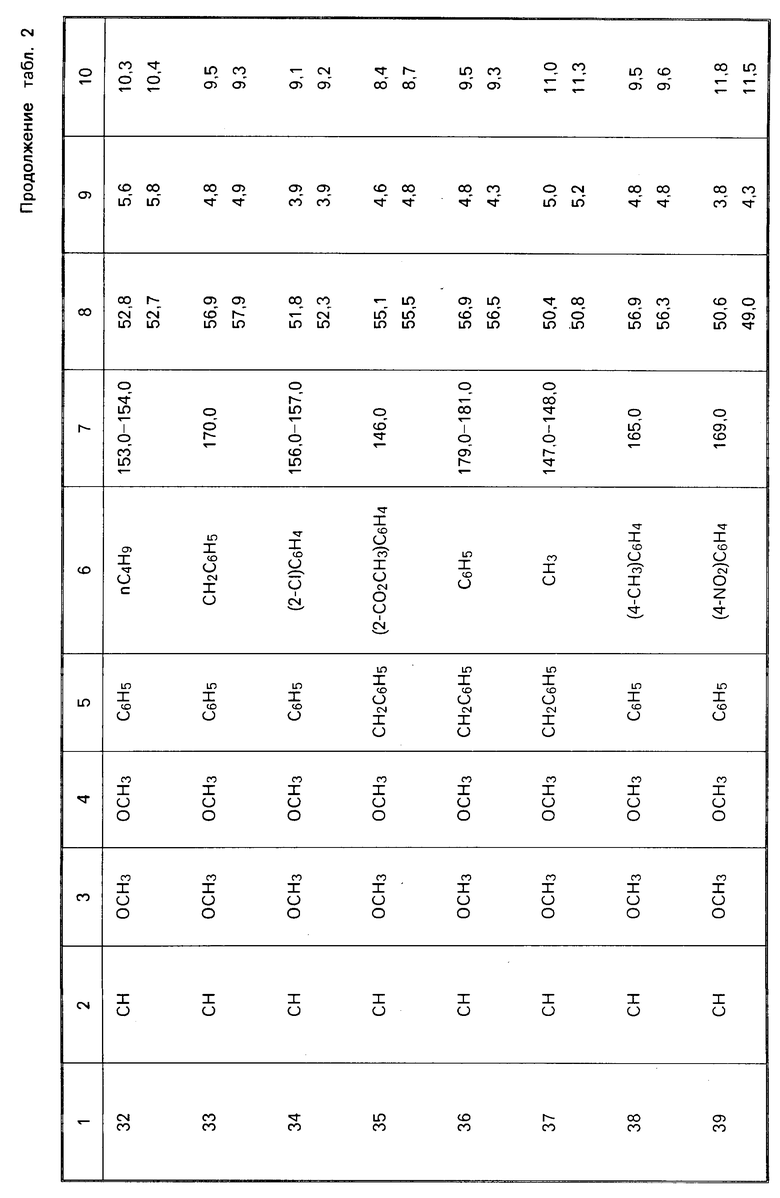
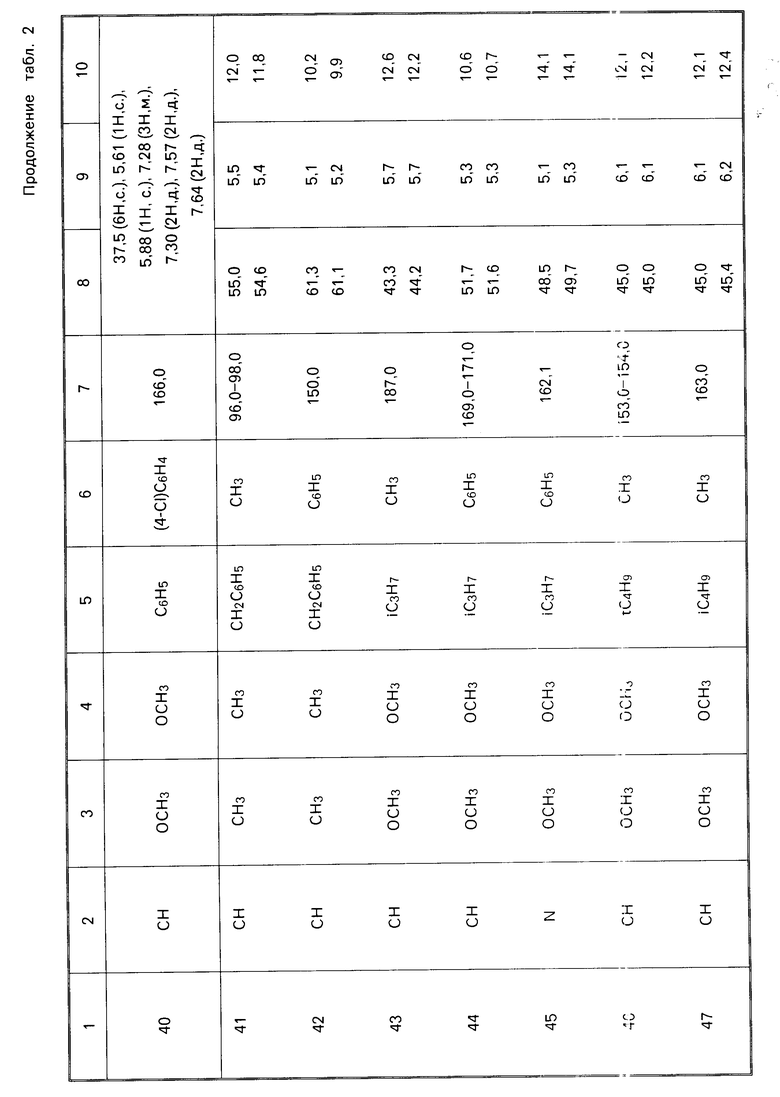
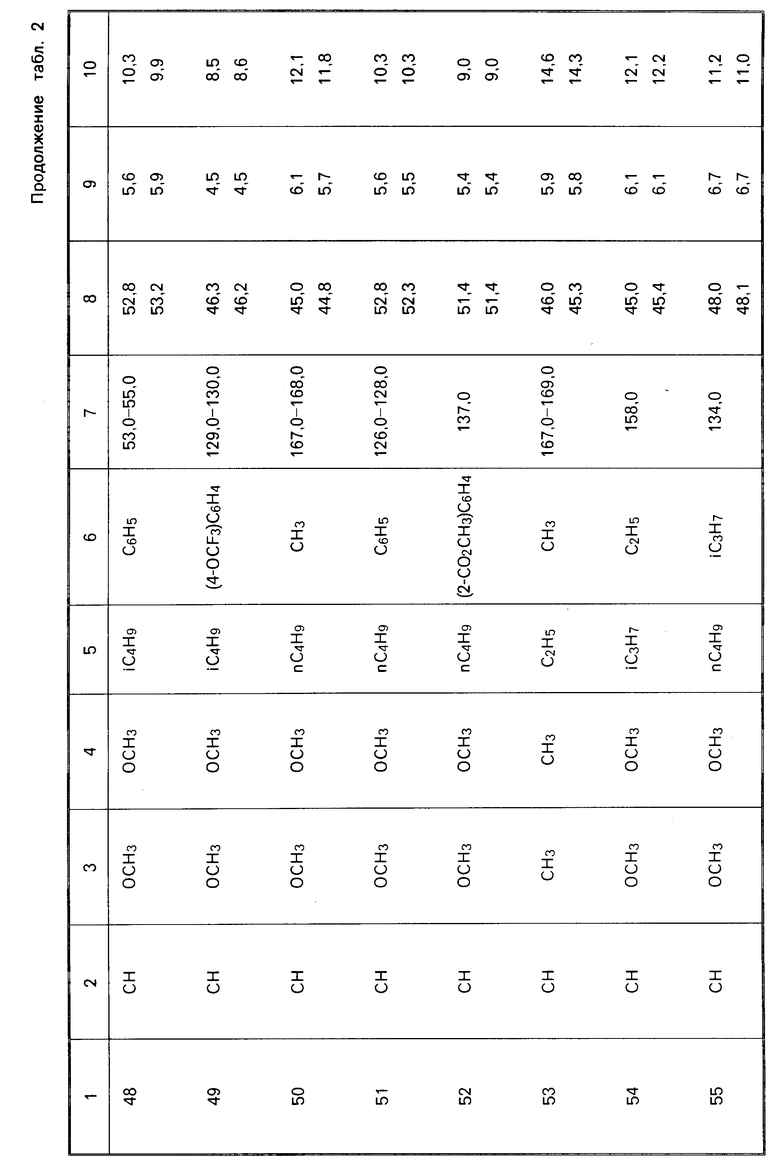
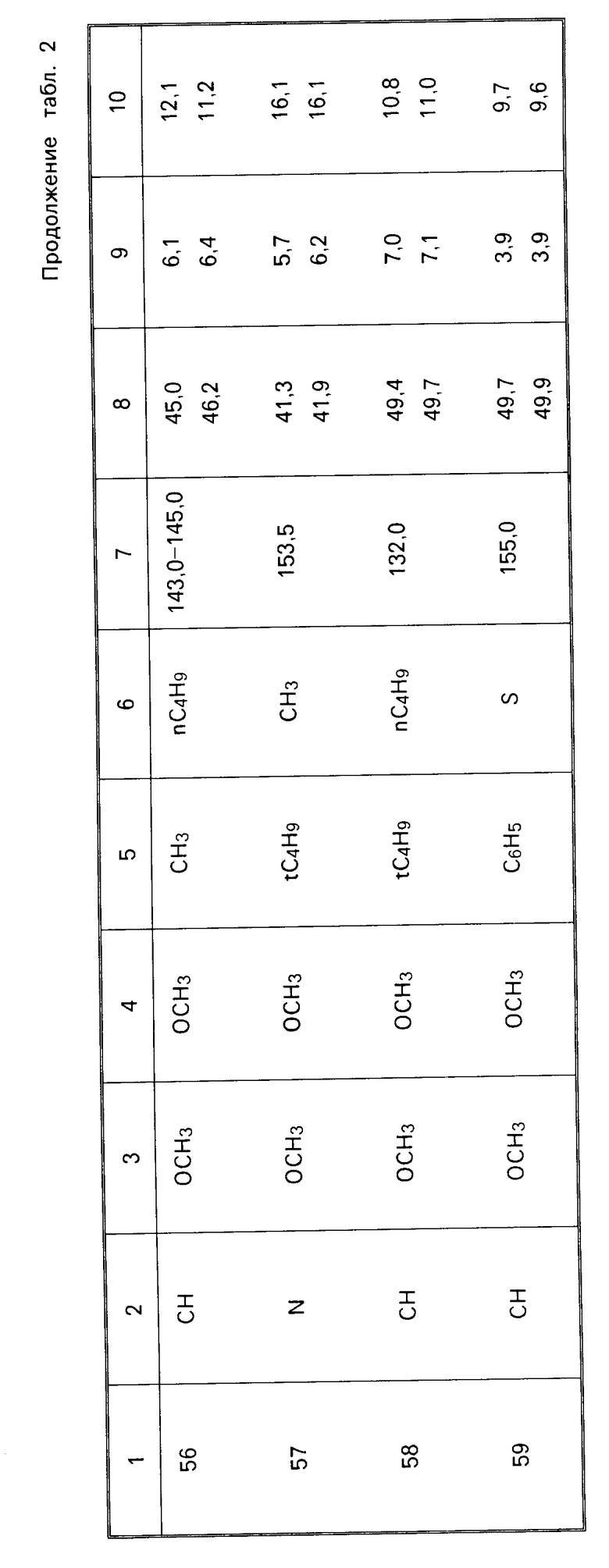
П р и м е р ы 29-59. Дополнительные соединения общей формулы I получались по способу, аналогичному процедуре, описанной в примере 28. Подробности о полученных соединениях даны в табл.2.
П р и м е р 60. 2-(4,6-Диметоксипиримидин-2-ил)окси-N-фенилсульфонил пропионамид.
0,12 г (0,0048 моля) гидрида натрия добавлялось к ацилсульфонамиду HOСН(CH3)CONHSO2C6H5 (0,50 г, 0,0022 моля) в 50 мл диметилформамида при комнатной температуре (примерно 20оС) и смесь перемешивалась в сухой атмосфере в течение 40 мин. Затем добавлялось 0,5 г (0,0022 моля) 4,6-диметокси-2-менсульфонил-пиримиди- на, что вызывало некоторое выделение пузырьков газа. Реакционная смесь нагревалась до 120оС и поддерживалась при данной температуре в течение 1 ч. После данного периода времени диметилформамид выпаривался, остальная жидкость разбавлялась водой и подкислялась до pH 2; продукт затем экстрагировался в диэтиловый эфир. После сушки и концентрирования и очистки с помощью мгновенной хроматографии с использованием 5% по объему смеси метанол/хлороформ получилось целевое соединение в виде коричневого масла (0,23 г, 0,0006 моля).
Выход: 28% по массе.
Элементный анализ, Вычислено: C 49,0; H 4,6; N 11,4 Найдено: C 48,1; H 5,0; N 11,0
П р и м е р 61. 2-(4,6-Диметокситриазин-2-ил)окси-N-фенилсульфонилпропионамид.
2-Гидрокси-N-фенилсульфонилпропионамид (1,50 г, 0,066 моля) растворился в сухом диоксане. При температуре окружающей среды добавлялся гидрид натрия, и смесь перемешивалась в течение 1 часа. Раствор подогревался до 50оС в течение 20 минут. 2-Хлор-4,6-диметокси-триазин (1,15 г, 0,0066 моля) добавлялся к раствору динатриевой соли: и смесь нагревалась с обратным холодильником в течение 2 ч.
Диоксан выпаривался, а остаток растворялся в воде и экстрагировался этилацетатом. Водный слой затем подкислялся до pH 2 и экстрагировался этилацетатом. Экстракты сушились над сульфатом магния, и растворитель упаривался, давая целевое соединение в виде желтого масла (0,83 г, 0,0023 моля).
Выход: 34% по весу.
ЯМР δ (CDCl3): 1,55 (3H, д), 3,95 (6Н, с), 5,38 (1Н, кв.), 7,54 (2Н, т. ), 7,66 (1Н, т.), 8,04 (2Н, д.), 9,14 (1Н, с), млн. дол.
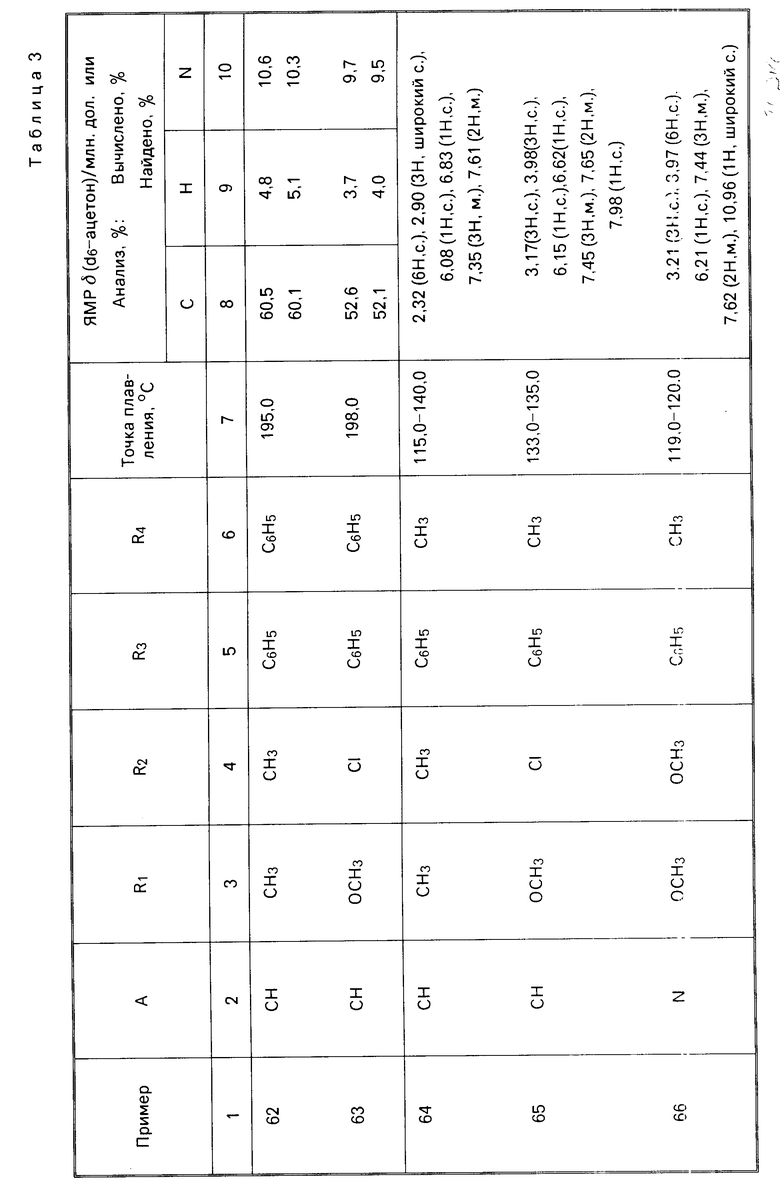
П р и м е р ы 62-66. Следующие соединения общей формулы I получались по способу, аналогичному процедуре, описанной в примере 61. Подробности о полученных соединениях даны в табл.3.
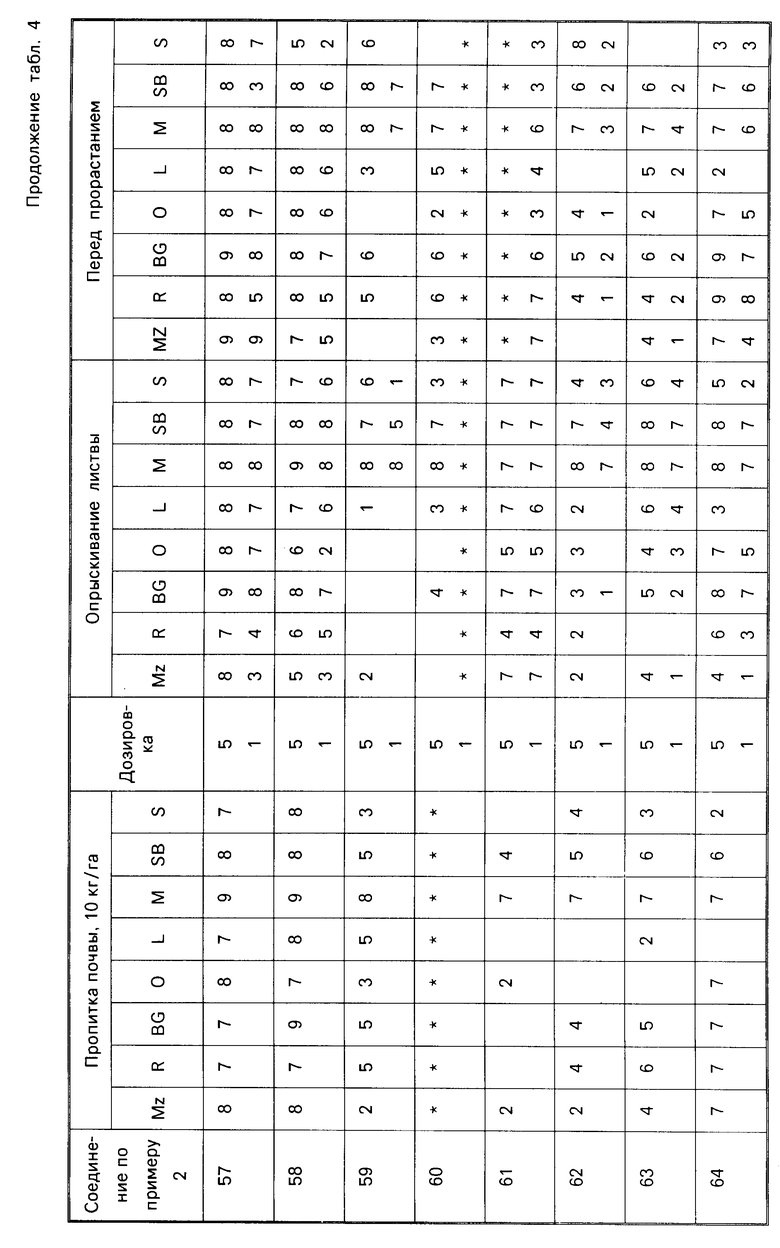
П р и м е р 67. Гербицидная активность.
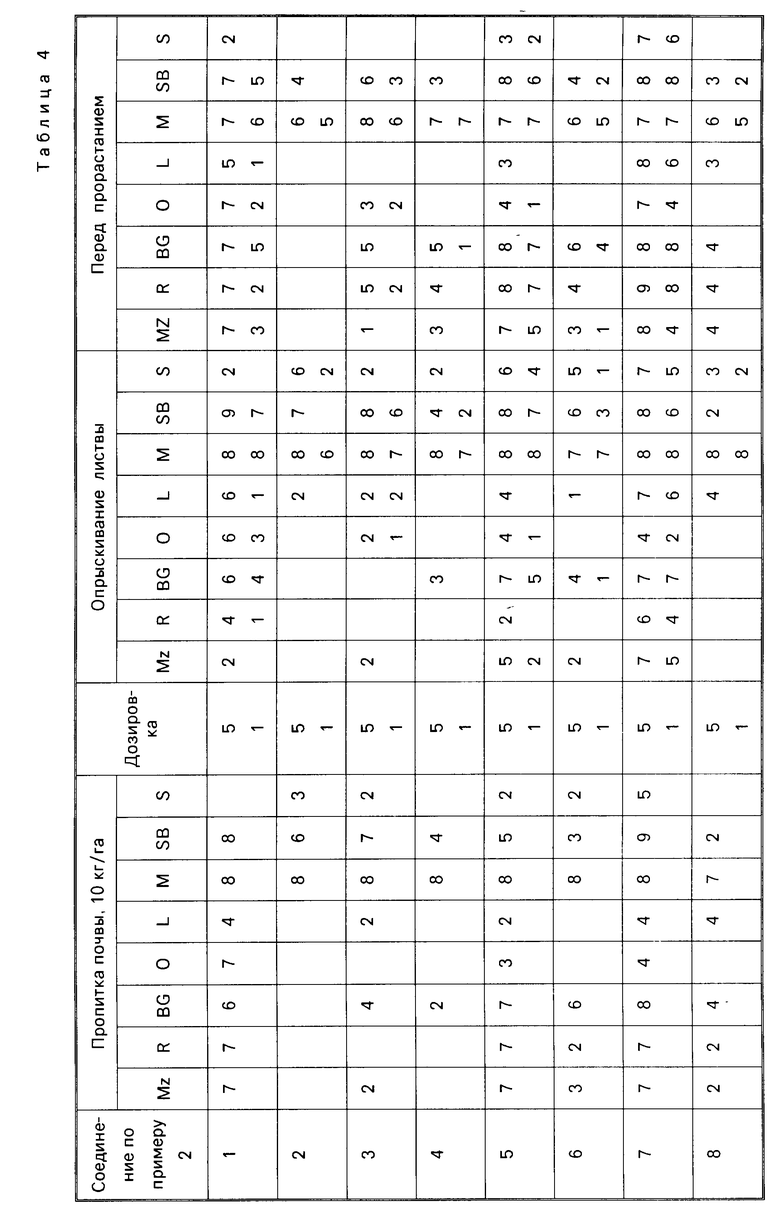
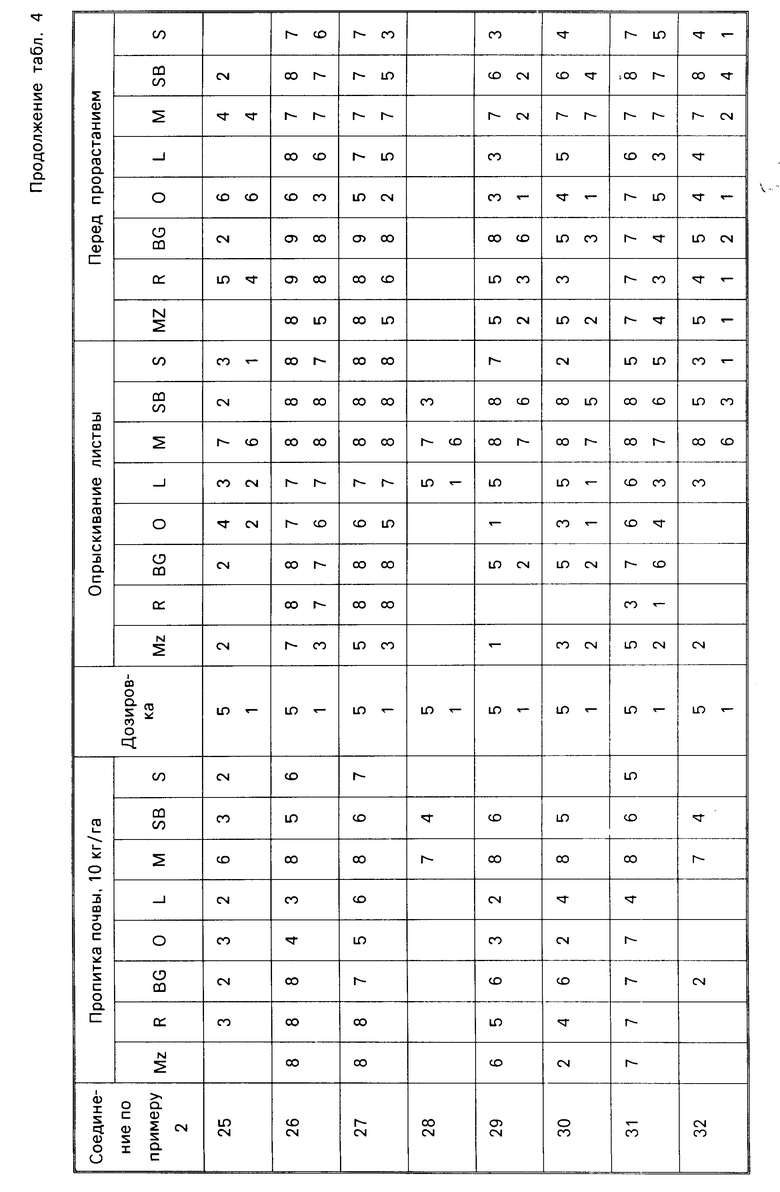
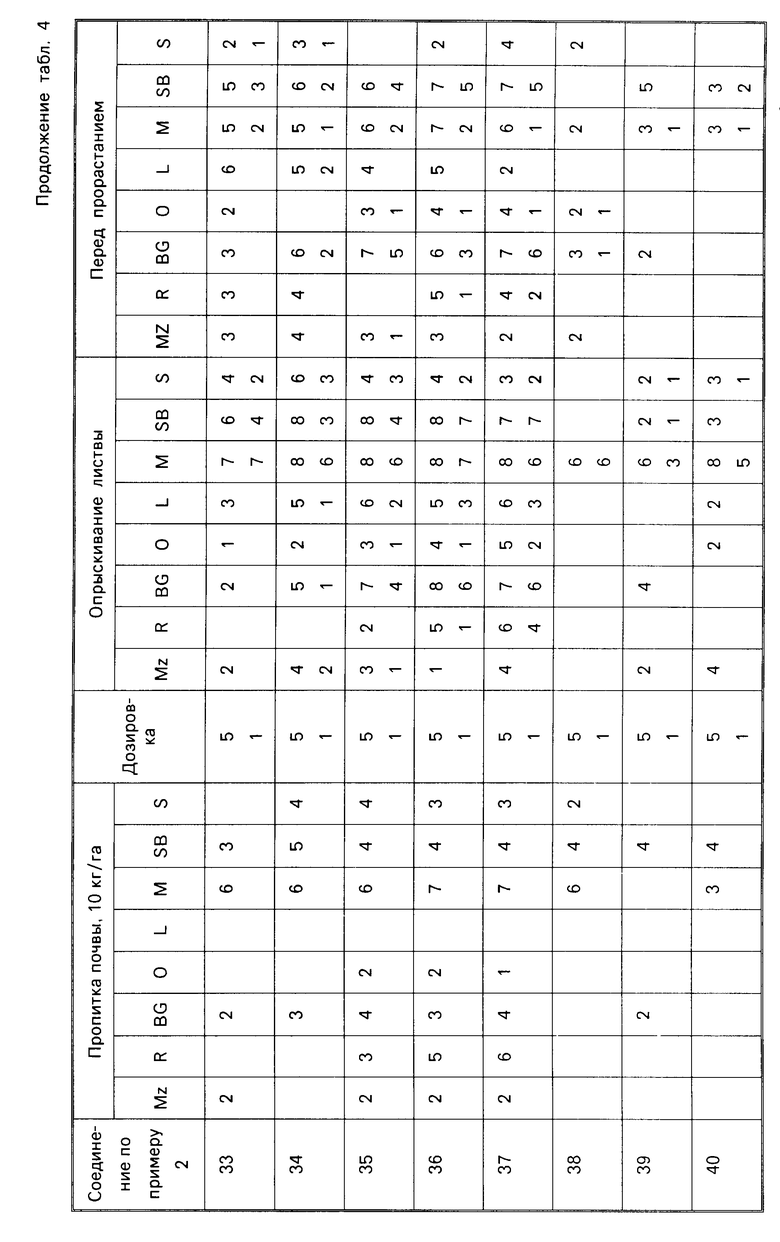
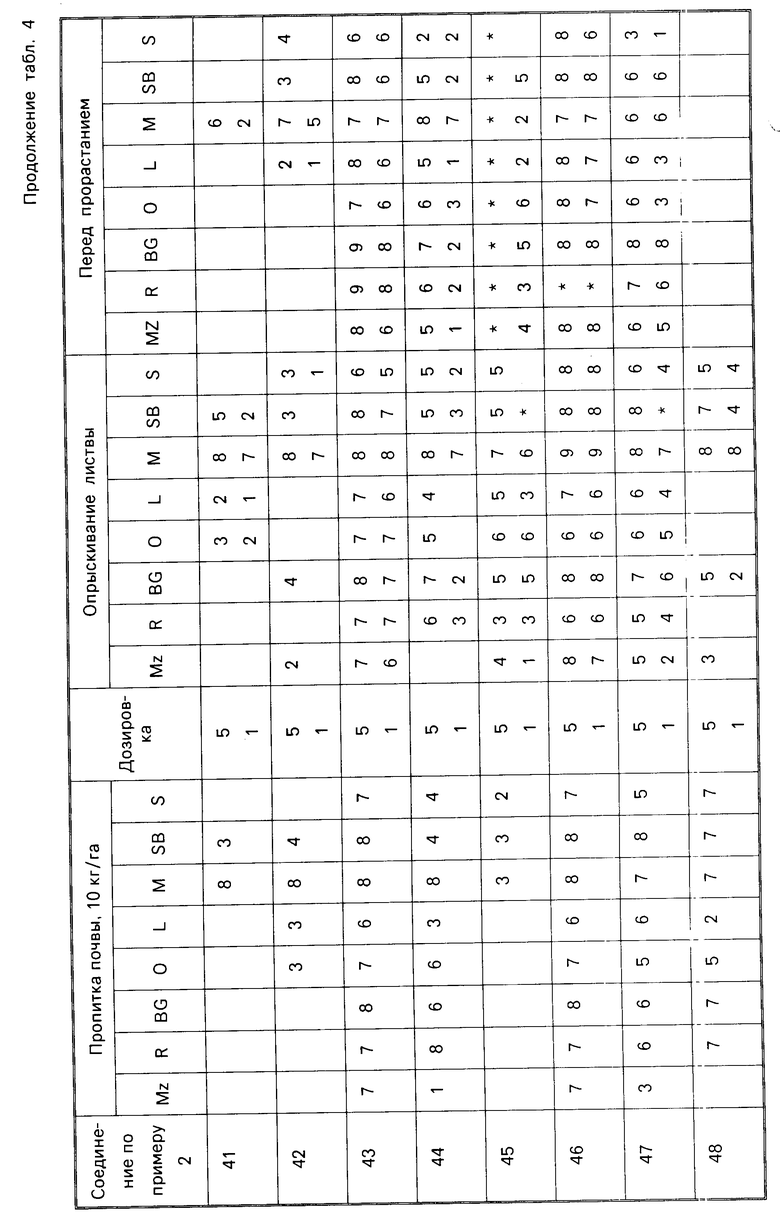
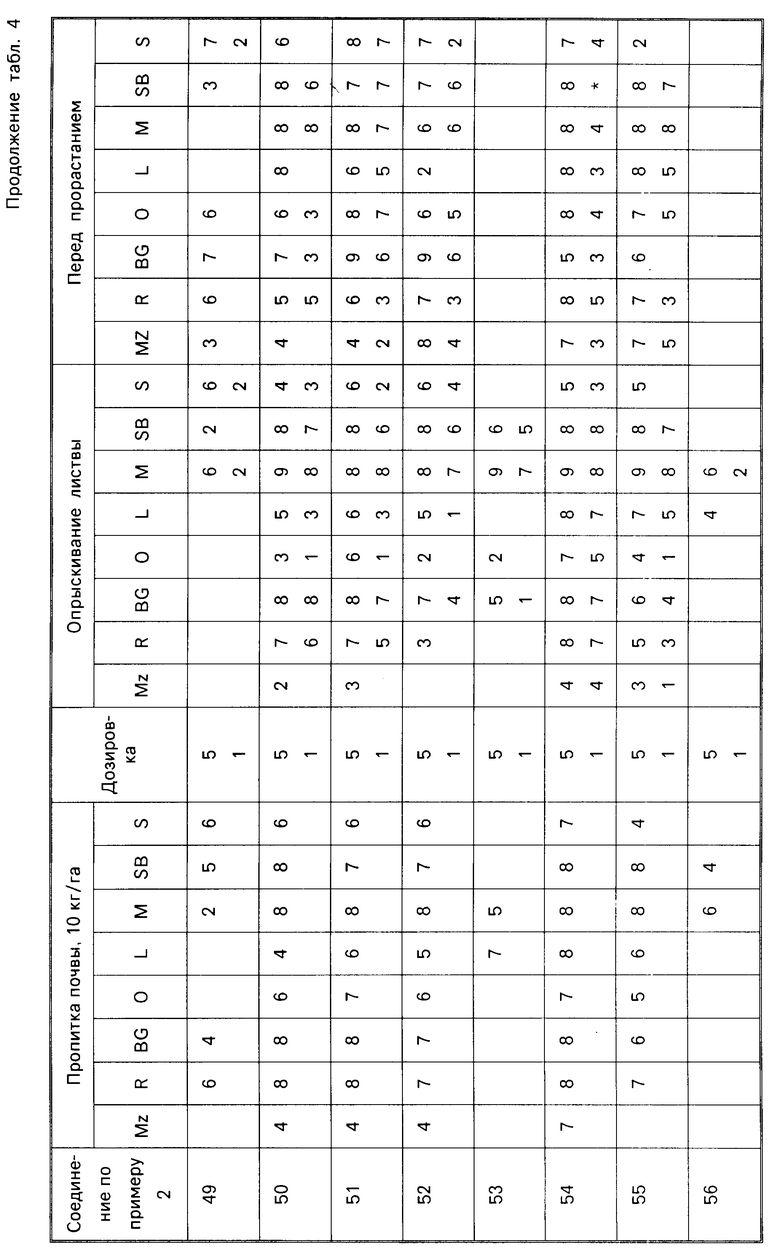
Для оценки их гербицидной активности соединения согласно изобретению испытывались с использованием в качестве характерного ряда растений: кукурузы, Zea mays (Mz); риса Oryza zativa (R); ежовника, Есhinochloa crusgalli (BG); овса, Avena sativa (O); льна обыкновенного, Linum usitatissimum (L); горчицы, Sinapsis alba (M); сахарной свеклы, Веta vulgaris (SB) и сои, Glycine max (S).
Испытания делятся на две категории, до появления всходов и после появления всходов. Предвсходовые испытания включали распыление жидкой препаративной формы соединения на почву, в которую незадолго высеивались семена видов растений, упомянутых выше. Послевсходовые испытания включали два типа опытов, а именно испытания с орошением почвы и испытания с опрыскиванием листвы. При испытаниях с орошением почвы, в которой росли саженцы растений указанных выше видов, орошались или пропитывались жидкой препаративной формой, содержащей соединение изобретения, а при испытаниях с опрыскиванием листвы саженцы растений опрыскивались такой препаративной формой.
Почвой, используемой в испытаниях, был приготовленный садовый суглинок.
Препаративные формы, используемые в испытаниях, получались из растворов испытываемых соединений в ацетоне, содержащих 0,4% по весу конденсата алкилфенола и окиси этилена, доступного под торговой маркой ТРИТОН Х-155. Эти ацетоновые растворы разбавлялись водой, и получающиеся готовые препаративные формы применялись при уровнях доз, соответствующих 5 или 1 кг активного материала на гектар в объеме, эквивалентном 600 л на гектар, при испытании с опрыскиванием почвы и опрыскиванием листвы, и при уровне дозы, эквивалентной 10 кг активного материала на гектар в объеме, эквивалентном приблизительно 3000 л на гектар, при испытаниях по орошению почвы.
В качестве контроля при предвсходовых испытаниях использовалась необработанная засеянная почва, а при испытаниях после появления всходов необработанная почва, содержащая саженцы растений.
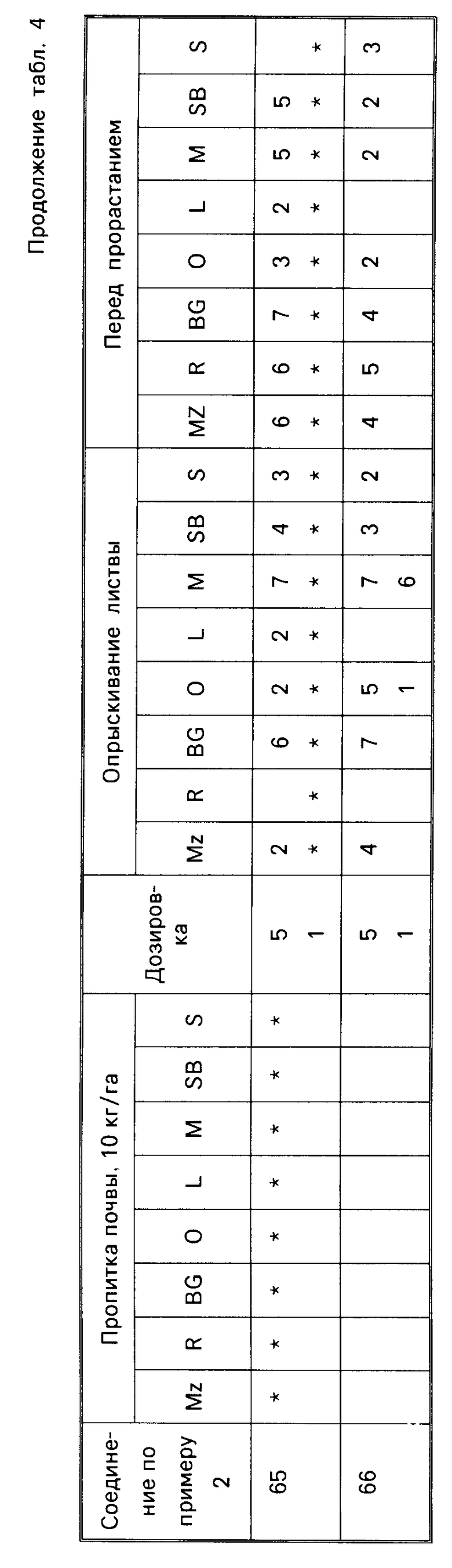
Гербицидный эффект испытываемых соединений оценивался визуально через 12 дней после опрыскивания листвы и почвы, и через 13 дней после (орошения) дренирования почвы и регистрировался по шкале 0-9.
Оценка 0 указывает на рост, как в необработанном контроле, а оценка 9 обозначает гибель. Увеличение на 1 единицу по линейной шкале соответствует приблизительно 10% увеличению уровня эффекта.
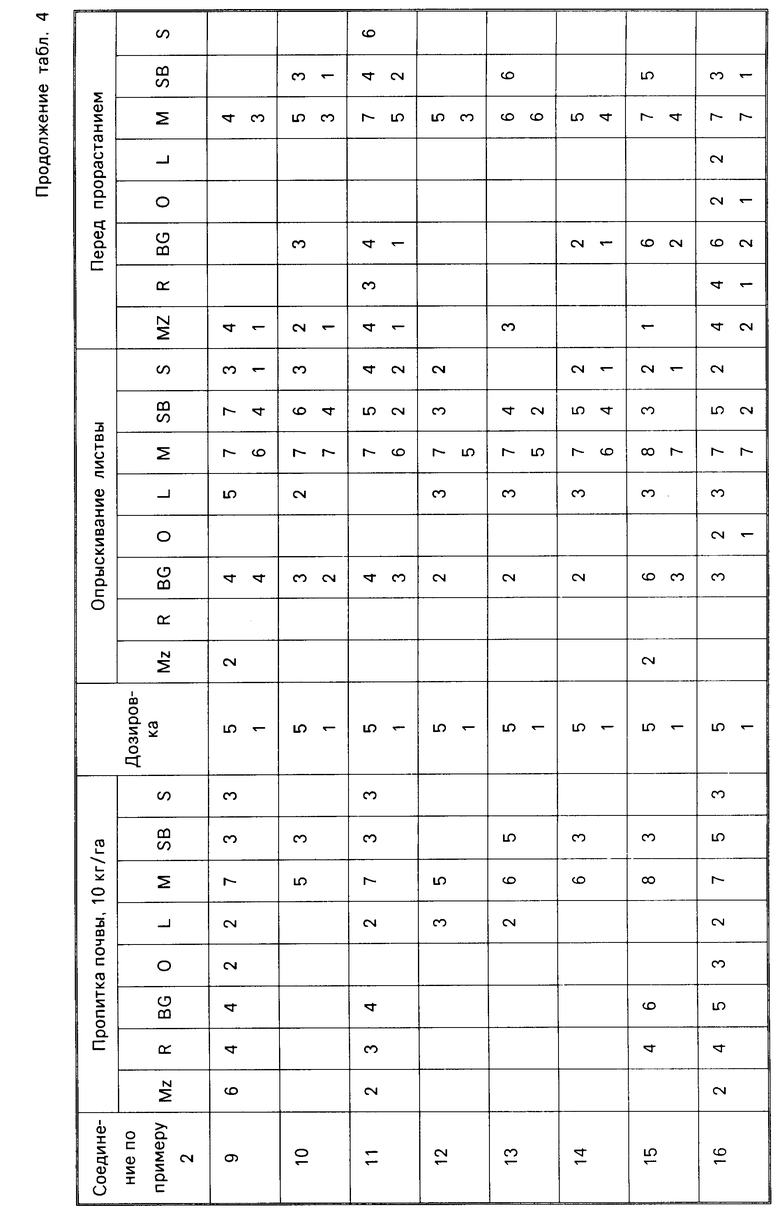
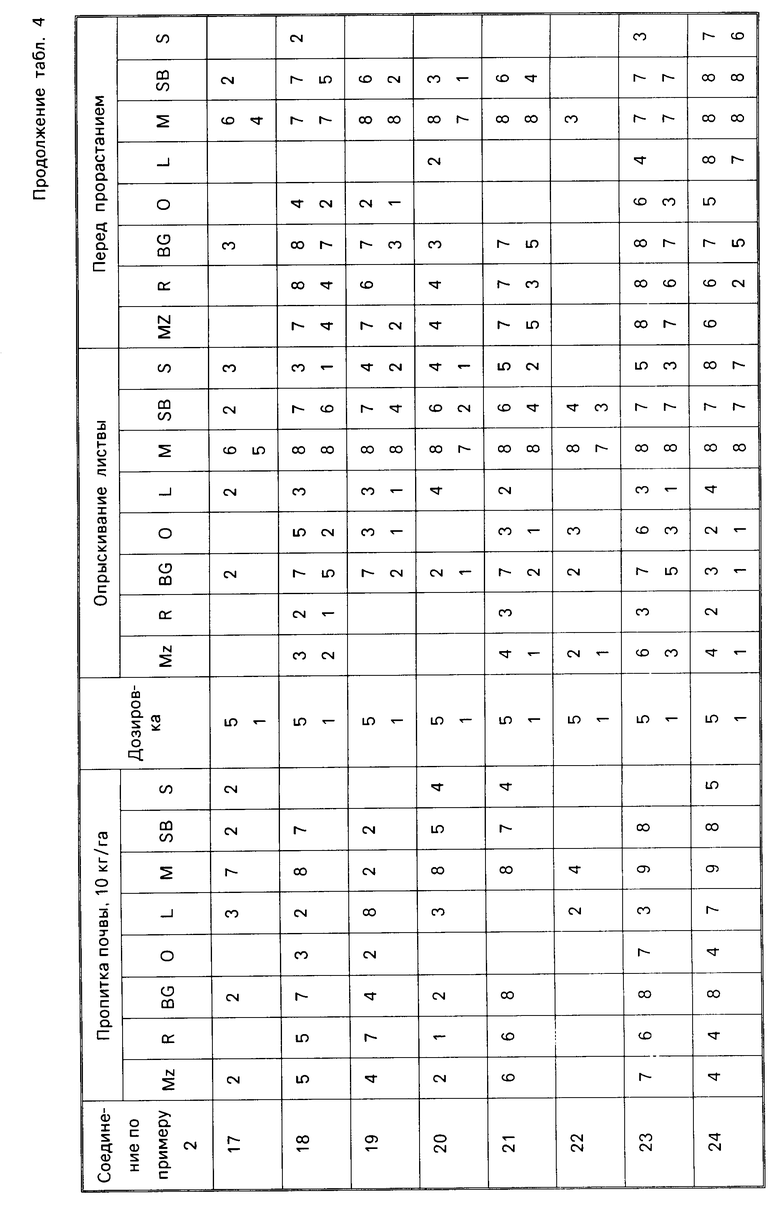
Результаты испытаний представлены ниже в табл.4, в которой соединения идентифицируются ссылкой на предшествующие примеры. Звездочка в следующей ниже таблице обозначает, что не было получено никакого результата; отсутствие числовой величины указывает на нулевую оценку.
Ниже приводятся данные гербицидных испытаний, сравнивающие пример 16 (соединение А) с соединением 96 ЕР-А-0212969 (соединение В). Данные относятся к опрыскиванию листьев и предвсходовым испытаниям при дозе нанесения 1 кг/га, а методика испытаний приведена в примере 67 настоящего описания.
Соединение А является намного более селективным относительно горчицы (M), нежели соединение В.
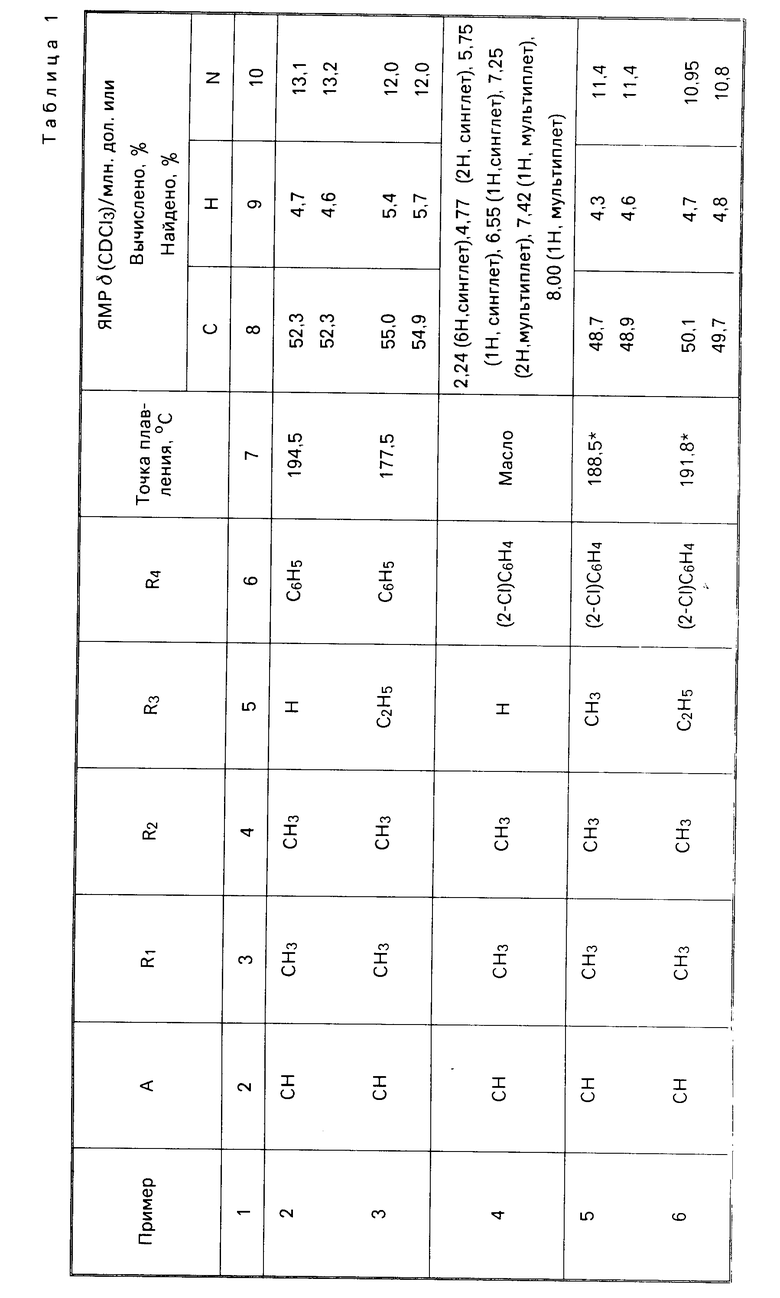
Использование: в сельском хозяйстве, в частности в способе борьбы с нежелательной растительностью. Сущность изобретения: в способе используют производные сульфонамидов ф лы I 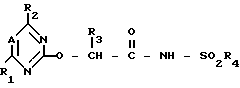 , где А - СН или N, R1-C1-C4 -алкил или C1-C4 -алкокси, R2-C1-C4 -алкил, C1-C4 -алкокси, галоген, R3 -водород, C1-C6 -алкил, фенил, бензил, R4-C1-C6 -алкил, бензил, тиенил, фенил, возможно замещенный галогеном, C1-C4 -алкилом, C1-C4 -галоидалкилом, C1-C4 -галоидалкоксилом, нитро, C1-C4 -алкоксикарбонилом, причем соединение берут в количестве 1 10 кг/га. 2 с. п. 5 з. п. ф лы.
, где А - СН или N, R1-C1-C4 -алкил или C1-C4 -алкокси, R2-C1-C4 -алкил, C1-C4 -алкокси, галоген, R3 -водород, C1-C6 -алкил, фенил, бензил, R4-C1-C6 -алкил, бензил, тиенил, фенил, возможно замещенный галогеном, C1-C4 -алкилом, C1-C4 -галоидалкилом, C1-C4 -галоидалкоксилом, нитро, C1-C4 -алкоксикарбонилом, причем соединение берут в количестве 1 10 кг/га. 2 с. п. 5 з. п. ф лы.
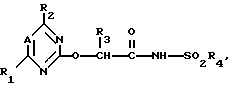
где А СН или азот;
R1 С1 С-алкил или С1 С4-алкокси;
R2 С1 С4-алкил, C1 C4-алкокси или галоген;
R3 водород, С1 С6-алкил, фенил или бензил;
R4 С1 С6-алкил, бензил, тиенил, фенил, не обязательно замещенный одним или более галогеном, С1 С4-алкилом, С1 С4-галоидалкилом, С1 С4-галоидалкоксилом, нитро или С1 С4-алкоксикарбонилом.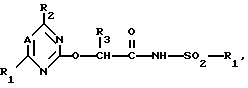
где А СН или азот;
R1 С1 С4-алкил или С1 С4-алкокси;
R2 С1 С4-алкил, С1 С4-алкокси или галоген;
R3 водород, С1 С6-алкил, фенил или бензил;
R4 C1 C6-алкил, бензил, тиенил или фенил, не обязательно замещенный одним или более галогеном, С4 С4-алкилом, С1 С4-галоидалкилом, С1 С4-галоидалкоксилом, нитро или С1 С4-алкоксикарбонилом,
в дозе 1 10 кг/га.
| ШТАМП ДЛЯ ПРОБИВКИ ОТВЕРСТИЙ | 0 |
|
SU212969A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1995-11-10—Публикация
1990-07-30—Подача