Изобретение относится к новым аминовым производным, процессам их получения и инсектицидам, содержащим в качестве селективных соединений указанные производные.
На протяжении многих лет в области исследования инсектицидов было разработано и внедрено в практическое использование огромное количество химических продуктов, например фосфорорганические инсектициды, такие как паратион и малатион, и карбаматные инсектициды, такие как карбарил и метомил. Эти инсектициды сыграли очень большую роль в улучшении сельскохозяйственного производства. Однако в последние годы некоторые из этих инсектицидов находятся под контролем из-за загрязнения окружающей среды вследствие остатка или накопления в природе, кроме того, в результате использования на протяжении длительного периода времени имеет место заражение устойчивыми насекомыми-вредителями. Следовательно, необходима разработка новых химических средств, которые обладают превосходными инсектицидными характеристиками в отношении разнообразных типов насекомых-вредителей, включая указанные устойчивые насекомые-вредители, и которые могут использоваться безопасно.
Известно соединение, которое не обладает никакой инсектицидной активностью CH2-NH
CH2-NH Cl
Cl
(Boll. Chim. Farm, 1979 118/11/661-666).
Следующее ниже соединение описывается в патенте США N 4918088, и имеет инсектицидную активность CH2-NH
CH2-NH CH3
CH3
Однако данное соединение не проявляет инсектицидной активности против чешуекрылых насекомых и зеленой рисовой цикадки, которые являются более серьезными вредителями для сельскохозяйственных культур, хотя оно обнаруживает активность против хлопковой тли.
Цель изобретения предоставить сельскохозяйственные химикаты, которые могут успешно синтезироваться в промышленном масштабе, оказывают определенное действие и являются безопасно применимыми.
Предлагаемое соединение обладает высокой инсектицидной активностью как против чешуекрылых, так и против полукрылых насекомых.
Настоящее изобретение относится к соединениям, имеющим формулу
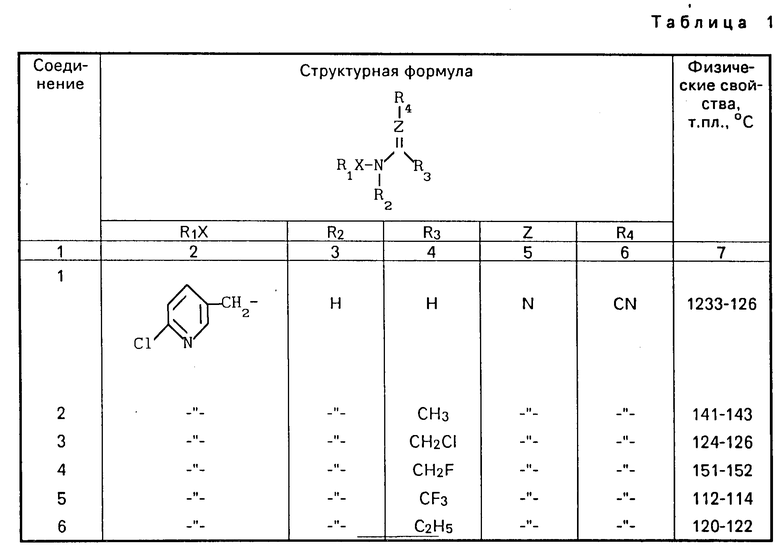
R1-X- R3 (I) где R1 необязательно замещенное 5-6-членное ароматическое гетерокольцо, содержащее атом азота, за исключением незамещенного 2-пиридила;
R3 (I) где R1 необязательно замещенное 5-6-членное ароматическое гетерокольцо, содержащее атом азота, за исключением незамещенного 2-пиридила;
Х необязательно замещенный С1-С3-алкилен или алкилиден;
R2 водород, карбамоил, моно- или ди-С1-С5-алкилкарбамоил, тиокарбамоил, моно- или ди-С1-С5-алкилтиокарбамоил, сульфамоил, моно- или ди-С1-С5-алкилсульфамоил, необязательно замещенный С1-С5-алкил, необязательно замещенный С2-С5- алкенил, необязательно замещенный С2-С5-алкинил, необязательно замещенный С3-С8-циклоалкил, необязательно замещенный С3-С8-циклоалкенил, необязательно замещенный арил или -Y-R5;
Y O, S(O)n, CO, CS или СО2;
n 0, 1 или 2;
R5 водород, необязательно замещенный С1-С5-алкил, необязательно замещенный С2-С5-алкенил, необязательно замещенный С2-С5-алкинил, необязательно замещенный С3-С8-циклоалкил, необязательно замещенный С3-С8-циклоалкенил или необязательно замещенный арил;
R3 водород, необязательно замещенный С1-С5-алкил, необязательно замещенный С2-С5-алкенил, необязательно замещенный С2-С5-алкинил, необязательно замещенный С3-С8-циклоалкил, или необязательно замещенный С3-С8-циклоалкенил;
R4 циано или нитро;
Z СН или N; или его соли.
Соединения данного изобретения могут приостанавливаться в соответствии со следующими схемами реакцией.
1. Способ получения 1: -
- + R
+ R R4 или R
R4 или R _____→
_____→ 
где r1 и r2 С1-С5-алкил;
R1-R4 и Х имеют указанные значения.
Реакция осуществляется в неактивном органическом растворителе, предпочтительно в ароматическом углеводородном растворителе таком как ксилол, толуол или бензол, в присутствии кислотного катализатора, такого как n-толуолсульфокислота, если необходимо при нагревании с обратным холодильником (в условиях дефлегмации) (2). Способ получения 2:
R


где r3 С1-С5-алкил;
R1-R3 и Х имеют указанные значения.
Данная реакция осуществляется в инертном органическом растворителе, предпочтительно в спирте, таком как метанол, этанол, при температуре между комнатной и точкой кипения используемого растворителя.
3) Способ получения 3: NH
NH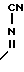 R3
R3

 R1-X-
R1-X- R3
R3
где Наl галоген;
R1-R3 и Х имеют указанные значения.
Данная реакция осуществляется в инертном органическом растворителе, предпочтительно в ДМФ, ТГФ, бензоле, ацетонитриле, ацетоне, метилэтилкетоне, в присутствии акцептора кислоты, такого как карбонат калия, гидрид натрия, триэтиламин, между комнатной температурой и точкой кипения используемого растворителя
4) Способ получения 4: + R
+ R al _____→
al _____→ 
где R1-R3, Х и Hal имеют указанные значения. Данная реакция осуществляется таким же образом, как реакция способа получения 3.
(5) Способ получения 5:
R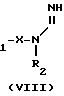 R3
R3 R1-X-
R1-X-

где R1-R3 и Х имеют указанные значения.
Данная реакция осуществляется в инертном органическом растворителе, предпочтительно ацетонитриле, четыреххлористом углеводороде, дихлорэтане, в присутствии реагента нитрования, такого как тетрафторборат нитрония, между -20оС и точкой кипения используемого растворителя.
После того как реакция завершается, обычная последующая обработка дает целевое соединение. Структура соединений данного изобретения определялась с помощью таких средств, как ИК, ЯМР, масс-спектры и др.
Если R2 водород в соединении данного изобретения, могут существовать таутомеры, представленные как
R1-X-NH R3 R1-X-N
R3 R1-X-N R3
R3
Могут также существовать синантиизмеры, если Z N, и цистрансизомеры, если Z СН, представленные
R1-X- R3 R1-Z-
R3 R1-Z- R3
R3
Соотношение варьирует в зависимости от, например, условий инструментов для проведения анализа.
Следующие примеры поясняют предлагаемое изобретение.
П р и м е р 1. 2-(2-Хлор-5-пиридилметиламино)-1-нитро-1-бутен CH2NH2+C2H5COCH2NO2 ____→
CH2NH2+C2H5COCH2NO2 ____→  CH2NH
CH2NH
В 50 мл толуола смешивали 4,2 г 2-хлор-5-пиридилметиламина, 3,5 г 1-нитро-2-бутанона и 0,1г n-толуолсульфоновой кислоты, смесь нагревали с обратным холодильником в течение 2 ч. Растворитель затем отгоняли и остаток очищался с помощью хроматографии на колонке на силикагеле, давая 4,1 г соединения N 368, (табл. 1) т.пл. 95-98оС.
П р и м е р 2. 2-(2-Хлор-5-пиридилметиламино)-1-циано-1-пропен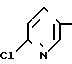 CH2NH2+CH3COCH2CN ____→
CH2NH2+CH3COCH2CN ____→  CH2NH
CH2NH
1,4 г 2-хлор-5-пиридилметиламина и 0,8 г 1-циано-2-пропанола смешивали и смесь перемешивали при комнатной температуре на протяжении ночи. Растворитель затем отгонялся и остаток очищался с помощью хроматографии на колонке из силикагеля, давая 1,7 г соединения N 528. (табл. 1). Т.пл. 95-98оС.
П р и м е р 3. N-Циано-N-(2-хлор-5-пиридилметил)-N-метилацетамидин CH2NHCH3+C2H5O
CH2NHCH3+C2H5O H3 ______→
H3 ______→  CH
CH H3
H3
В 20 мл метанола смешивали 1,6 г N-метил-2-хлор-5-пиридилметиламина и 1,2 г этил-N-цианоацетамидина, смесь перемешивали при комнатной температуре в течение ночи. Растворитель затем отгонялся и остаток очищался с помощью хроматографии на колонке на силикагеле, давая 1,8 г соединения N 22 (табл. 1) Т.пл. 101-103оС.
П р и м е р 4. N-Циано-N'-(2-хлор-5-пиридилметил)-N'-этилацетамидин CH2NH
CH2NH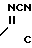 H3 + C2H5I ______→
H3 + C2H5I ______→  CH
CH H3
H3
0,7 г Гидрид натрия (чистота 60% 0,7 г) добавляли к раствору 3 г N-циано-N-(2-хлор-5-пиридилметил)ацетамидина в 20 мл N,N-диметилформамида при температуре ледяной бани. После перемешивания смеси при той же температуре в течение 1 ч к смеси добавляли 2,7 г иодистого этила с последующим перемешиванием в течение 5 ч при комнатной температуре. Реакционную смесь затем выливали в смесь льда с водой, экстрагировали этилацетатом, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный остаток очищался с помощью хроматографии на колонке на силикагеле, давая 1,6 г соединения N 51 (табл. 1). Т.пл. 100-101оС.
П р и м е р 5. N-Циано-N-(2-хлор-5-пиридилметил)-N'-метилацетамидин
CH3NH H3 +
H3 +  ______→
______→ 
Нитрид натрия (чистота 60% 0,6 г) добавляли к раствору 1,3 г N-циано-N'-метилацетамидина в 20 мл N,N-диметил- формамида при температуре ледяной бани. После перемешивания смеси при той же температуре в течение 1 ч к смеси добавляли 2,2 г 2-хлор-5-пиридилметилхлорида с последующим перемешиванием в течение 5 ч при комнатной температуре. Реакционную смесь затем выливали в смесь лед-вода, экстрагировали этилацетатом, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный остаток очищался с помощью колонной хроматографии на силикагеле, давая 1,5 г соединения N 22 (табл. 1). Т.пл. 101-103оС.
Ссылочный пример. N-(2-хлор-5-пиридил)-N-метилацетамидинхлоргидрат +
+

К 40 мл этанола добавляли 5,1 г N-(2-хлор-5-пиридилметил)-N-метиламина, а затем 4 г хлоргидрата этилацетамидата при 0оС. После перемешивания в течение часа реакционная смесь оставлялась подогреваться до комнатной температуры и перемешивалась на протяжении ночи. Растворитель затем отгонялся. Полученный белый остаток промывался диэтиловым эфиром, давая 7,3 г целевого соединения. Т.пл. 192-197оС.
П р и м е р 6. N-(2-Хлор-5-пиридилметил)-N-метил-N-нитроацетамидин

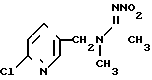
К суспензии 1 г N-(2-хлор-5-пиридилметил)-N-метиламинхлоргидрата в 10 мл сухого ацетонитрила добавляли по каплям 0,7 г ДВV в атмосфере азота при комнатной температуре. После перемешивания в течение 30 мин раствор добавляли по каплям к суспензии 0,6 г тетрафторбората нитрония в 5 мл сухого ацетонитрила в атмосфере азота при охлаждении с помощью cмеси льда с водой и оставляли перемешиваться в течение 4 ч. После этого смесь выливалась в смесь лед-вода, затем экстрагировалась несколько раз хлороформом. Объединенный хлороформный слой сушился над сульфатом магния, фильтровался и отгонялся. Неочищенное масло очищалось с помощью колоночной хроматографии на силикагеле, давая0,3 г соединения N 236 (табл. 1).ND25 1,5808.
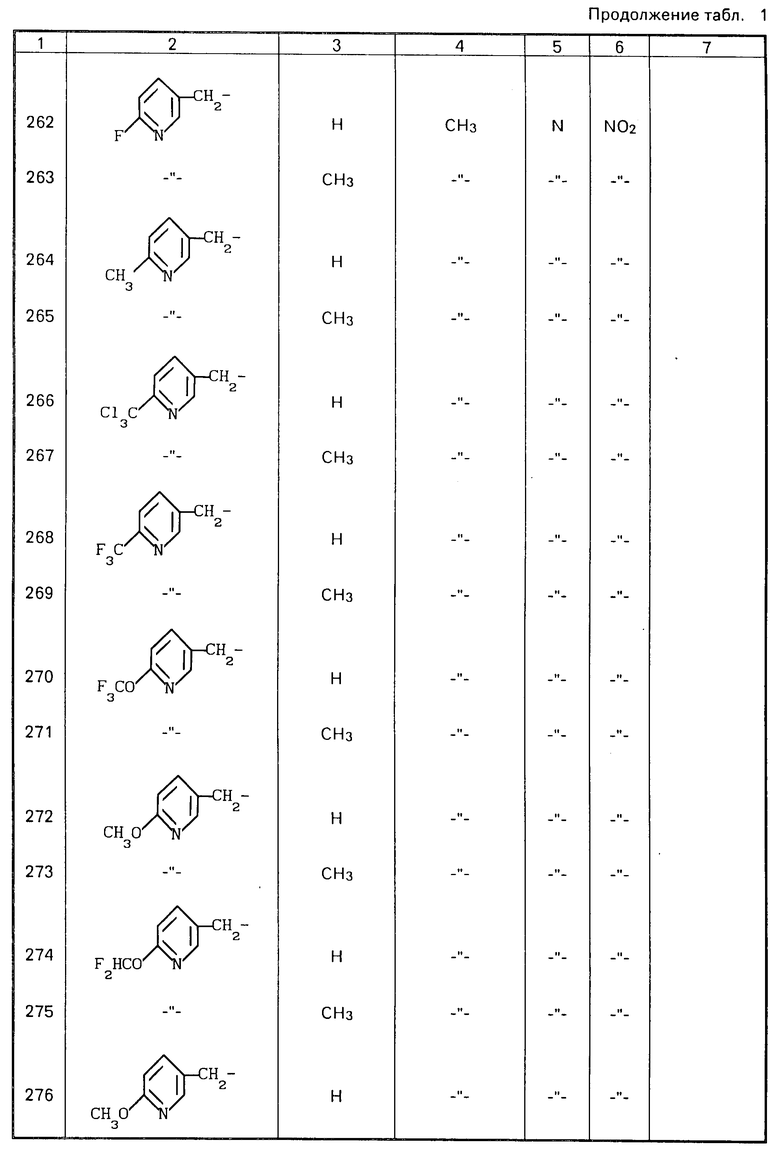
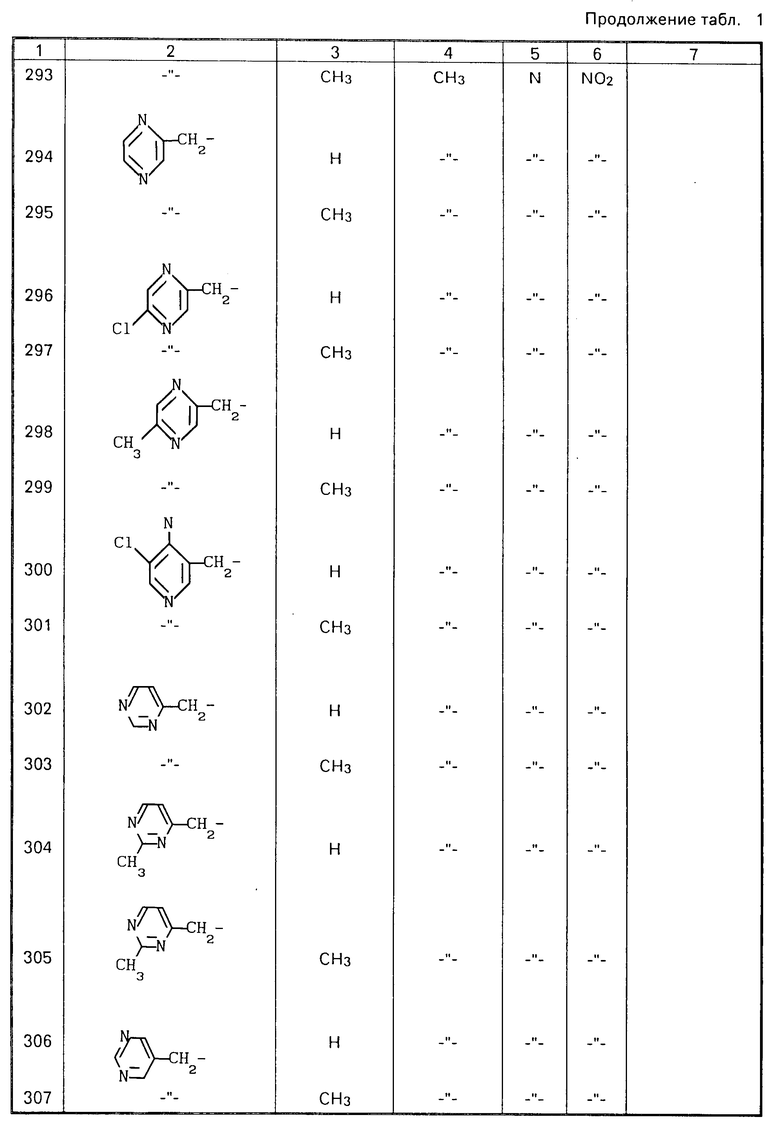
Типичные примеры соединений данного изобретения, включая соединения, описанные выше, перечислены в табл. 1.
Соединения данного изобретения проявляют высокую инсектицидную активность против разнообразных видов насекомых вредителей, таких как совки, моль капустная, тля, цикадки и дельфациды. В последние годы снижение регулирующего эффекта фосфорорганических и карбаматных инсектицидов, которое вызвано выработкой устойчивости к этим инсектицидам, стало серьезной проблемой. В такой ситуации разработка новых инсектицидов, являющихся эффективными по отношению к устойчивым вредителям, весьма необходима. Соединения данного изобретения обладают превосходящей инсектицидной активностью не только против чувствительных штаммов, но также и против устойчивых организмов.
Инсектициды, по данному изобретению содержат в качестве активных ингредиентов один или более типов соединений, выраженных общей формулой (1). Эти активные ингредиенты могут использоваться такими, как они получены, но обычно применяются в виде любой из форм, свойственных обычным сельскохозяйственным ядохимикатам, а именно: в виде смачиваемого порошка, дуста, эмульгируемого концентрата, суспензионных концентратов, химикатов для окуривания, фумигантов, гранул или других готовых препаративных форм. В качестве добавок и носителей используется соевая мука, пшеничная мука или другие виды растительной муки, диатомовая земля, апатит, гипс, тальк, пирофиллит глина или другие тонкодисперсные минеральные порошки, когда необходимы твердые препаративные формы.
Когда требуются жидкие препаративные формы, тогда в качестве растворителей используют керосин, минеральное мало, нефть, растворитель нафту, ксилол, циклогексан, циклогексанон, диметилформамид, диметилсульфоксид, спирт, ацетон, воду и пр. Если необходимо, можно добавить поверхностно-активные агенты для того, чтобы получить гомогенную и подходящую препаративную форму. Смачиваемые порошки, эмульгируемые концентраты, суспензионные концентраты и др. полученные таким образом, разбавляются водой для получения суспензий или эмульсий заданной концентрации, перед тем как они фактически распыляются на растения в поле. Дусты или гранулы применяются непосредственно без дополнительной обработки.
Соединение данного изобретения является эффективным, но они могут использоваться при смешении с различными типами инсектицидов, акарицидов и фунгицидов.
Типичными примерами акарицидов и инсектицидов, которые могут использоваться при смешении с соединениями данного изобретения, являются следующие.
Акарициды (фунгициды): хлоробензилат, хлоропропилат, проклонол, бромпропилат, дикофол, динобутон, бинапакрил, хлордимеформ, амитраз, пропаргит, PPPS, бензоксимат, гекситиазокс, фенбутатиноксид, полинактин, хинометионат, тиохинокс, хлорфензон, тетрадимефон, фенпроксид, авермектины, клофентезин, флубензимид, феназахин, пиридабен, фенпроксимат, хлорфенетол, тиофанатметил, беномил, тирам, ипробенфос, эдифенфос, фталид, пробеназол, изопропиолан, хлороталонил, каптан, полиоксин-В, бластицидин-S, касугамицин, валидамицин, трициклазол, пирохилон, феназиноксид, мепронил, флуталонил, пенцикурон, ипродион, гимексазол, металаксил, трифлумизол, дикломезин, теклофталам, винклозолин, процимидон, битертанол, триадимефон, прохлораз, пирифенокс, фенаримал, фенпропиморф, трифорин, металаксил, оксикарбоксин, перфразоат, дикломедин, флуазинам, оксадиксил, этохинолак, ТРТН, пропамокарб, фосетил, дигидрострептомицин, анилазин, дитианон, диэтофенкарб.
Инсектициды (акарициды): фосфорорганического и карбаматного типа; например фентион, фенитротион, диазинон, хлорипирифос, оксидепрофос, вамидотион, фентоат, диметоат, формотион, малатион, трихлорфон, тиометон, фосмет, меназон, дихлорвос, ацефат, ЕРВР, диалифос, паратионметил, оксидеметонметил, этион, альдикарб, пропоксур, метомил, фенобукарб, ВРМС, пираклофос, монокротофос, салитион, картап, карбосульфан, карбофуран, бенфуракарб, метолкарб, карбарил, пиримикарб, этиофенкарб, феноксикарб.
Инсектициды (акарициды) пиретроидного типа: перметрин, циперметрин, дельтаметрин, фенвалерат, фенпропатрин, пиретрины, аллетрин, тетраметрин, ресметрин, партрин, диметрин, пропратрин, бифентрин, протрин, флувалинат, цифлутрин, цигалотрин, флуцитринат, этофенпрокс, циклопротрин, тралометрин, силанеофан.
Инсектициды бензоилфенилмочевинового типа и других типов: дифлубензурон, хлорфлуазурон, трифлумурон, тефлубензурон, бупрофезин, пирипроксифен, флуфеноксурон, машинное масло.
Ниже даны некоторые примеры препаративных форм. Носители поверхностно-активные агенты и др. которые добавляются, не ограничиваются указанными примерами.
П р и м е р 7. Эмульгируемый концентрат, ч.
Соединение данного изобретения 10 Алкилфенолполиоксиэтилен 5 Диметилформамид 50 Ксилол 35
Компоненты смешиваются и растворяются. Для использования при распылении или опрыскивании жидкая смесь разбавляется водой с получением эмульсии.
П р и м е р 8. Смачиваемый порошок, ч.
Соединение данного изобретения 20
Сложный эфир серной кислоты и высшего спирта 5 Диатомовая земля 70 Двуокись кремния 5
Эти компоненты смешиваются и измельчаются для получения тонкодисперсного порошка, который для использования путем распыления разбавляется водой с получением суспензии.
П р и м е р 9: Дуст, ч:
Соединение данного изобретения 5 Тальк 94,7 Двуокись кремния 0,3
Эти ингредиенты смешиваются и измельчаются, используются в измельченном виде при распылении.
П р и м е р 10. Гранулы, ч.
Соединение данного изобретения 5 Глина 73 Бентонит 20
Диоктилсульфосукцинат натрия 1 Фосфат натрия 1
Указанные соединения гранулируются и применяются при использовании такими, как они есть.
Промышленная применимость.
Приведенные ниже испытания показывают инсектицидную активность соединений данного изобретения.
И с п ы т а н и е 1. Эффективность в отношении хлопковой тли.
Инокулировались 30-50 насекомых хлопковой тли на делянку (лоток) с использованием небольшой щеточки на листьях огурцов, которые высевались в лотки, 10 см диаметром, возрасте 10 дн. после прорастания. Через день пораженные насекомые-вредители (пораненные) удалялись, распылялся химический раствор, который приготавливали так, чтобы эмульгируемый концентрат, описанный в примере 7, разбавлялся водой до концентрации соединения 125 част./млн. согласно предписанию. Лотки помещались в термостатическую камеру при 25оС и влажности 65% Спустя 7 дней подсчитывалось число живых вредителей, эффективность контроля или уничтожения вычислялась по сравнению со случаем необработанного лотка. Результаты показаны в табл. 2.
И с п ы т а н и е 2. Эффективность в отношении зеленой рисовой цикадки.
Сеянцы риса в возрасте после прорастания 7 дн. погружались в химический раствор, который приготовляли так, что эмульгируемый концентрат инсектицида, описанный в примере 7, разбавляли водой до концентрации соединения 125 част. /млн. на 30 с. После сушки на воздухе обработанные сеянцы помещали в опытные трубки и инокулировали 10 насекомых личинок 3-е возрастной стадии зеленой рисовой цикадки, устойчивой к фосфорорганическим и карбаматным инсектицидам. Трубки покрывали газовой тканью и помещали в термостат с температурой 25оС и влажностью 65% Спустя 5 дн. проверялась смертность.
Результаты показаны в табл. 3.
И с п ы т а н и е 3. Эффективность в отношении рисовой совки.
Испытуемые соединения преобразовывались в препаративную форму смачиваемого порошка таким же образом, как в примере 8. Соединения разбавляли водой до концентрации 125 част./млн. Листья кукурузы погружались в химический раствор на 30 с. После сушки на воздухе обработанный лист помещали в чашку Петри и инокулировали пять личинок рисовой совки 3-ей возрастной стадии. Чашки Петри закрывались стеклянными крышечками и помещались в термостат с температурой 25оС и относительной влажностью 65% Смертность проверялась через 5 дн. Каждый опыт повторялся два раза. Результаты показаны в табл. 4.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕНЗАМИДОКСИМА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО ДЛЯ ЗАЩИТЫ СЕЛЬСКОХОЗЯЙСТВЕННЫХ РАСТЕНИЙ | 1995 |
|
RU2140908C1 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА И ИНСЕКТИЦИДЫ, ВКЛЮЧАЮЩИЕ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2005 |
|
RU2424232C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2083562C1 |
| СОЕДИНЕНИЕ ДИГАЛОГЕНПРОПЕНА, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ИНСЕКТИЦИДНО-АКАРИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С ВРЕДНЫМИ НАСЕКОМЫМИ | 1994 |
|
RU2130008C1 |
| ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1988 |
|
RU2009642C1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИНСЕКТОАКАРИЦИДНАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2114107C1 |
| ПРОИЗВОДНЫЕ 3(2Н)-ПИРИДАЗИНОНА И СПОСОБ БОРЬБЫ С ВРЕДНЫМИ НАСЕКОМЫМИ | 1988 |
|
RU2033992C1 |
| ПРОИЗВОДНЫЕ АМИДА N-СУЛЬФОНИЛКАРБОНОВОЙ КИСЛОТЫ, ВКЛЮЧАЮЩИЕ N-СОДЕРЖАЩЕЕ 6-ЧЛЕННОЕ АРОМАТИЧЕСКОЕ КОЛЬЦО, ФУНГИЦИДНАЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИИ И СПОСОБЫ БОРЬБЫ С СОРНЯКАМИ И ФИТОПАТОГЕННЫМИ ГРИБКАМИ | 1993 |
|
RU2117662C1 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛИДИНА И ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2009133C1 |
| СОКРИСТАЛЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2625481C1 |





































Использование: в качестве инсектицидов. Сущность изобретения: продукт - производные амина ф-лы (R1X)(R2)N-CR3-Z-R4, где R1 -пиридил, который может быть замещен галогеном, C1-C4- -алкилом, галоидзамещенным C1-C4- алкилом, необязательно галоидзамещенным C1-C4- алкокси, C1-C4- алкилмеркапто, C1-C4- алкилсульфонилом, фенокси, циано, нитро, C1-C4- алкиламиногруппой, за исключением незамещенного 2-пиридила, пиразил, пиразолил, пиридазил или тиазолил, которые могут быть замещены C1-C4- алкилом или галогеном; Х-прямой или разветвленный C1-C3- алкилен; R2-H, C1-C5- алкилкарбамоил, необязательно замещенный C1-C5- алкил, C2-C5 -алкенил, C2-C5- алкинил, C3-C6- циклоаклил, фенил или радикал -Y-R5; Y-O, SO2, СО или CO2, R5 -Н, необязательно замещенный C1-C5- -алкил, C3-C6- циклоалкил или необязательно замещенный фенил; R3- Н, необязательно замещенные C1-C5- алкил, C2-C5- алкенил, C3-C8- алкинил, C3-C8- циклоалкил или C3-C8- циклоалкенил; R4 -циано или нитро; Z-CH или n или их соли. Реагент 1: R1X(R2)-NH, где R1 и R2 указаны выше. Реагент 2: R3COCH2R4, где R3 и R4 указано выше. Условия реакции: выделение в свободном виде или в виде соли. 2 с.п. ф-лы, 4 табл.
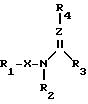
где R1 пиридил, который может быть замещен галогеном, C1 - C4-алкилом, галогензамещенным C1 C4-алкилом, C1 - C4-алкокси, C1 C4-алкилмеркапто, C1 - C4-алкилсульфонилом, фенокси, циано, ди-C1 - C4-алкиламиногруппой, за исключением незамещенного 2-пиридила, пиразил, пиразолил, пиридазил или тиазолил, которые могут быть замещены C1 - C4-алкилом или галогеном;
Х прямой или разветвленный C1 C3-алкилен;
R2 водород, ди-C1 C5-алкилкарбамоил, необязательно замещенный C1 C5-алкил, C2 C5-алкенил, C2 - C5-алкинил, C3 C6-циклоалкил, фенил или радикал Y - R5, где Y O, SO2, CO или CO2, а R5 водород, необязательно замещенный C1 C5-алкил, C3 - C6-циклоалкил или галогензамещенный фенил;
R3 водород, необязательно замещенный C1 C5-алкил или C3 C6-циклоалкил;
R4 циано или нитро;
Z CH или N,
или их соли.
где R1 пиридил, который может быть замещен галогеном, C1 - C4-алкилом, галогензамещенным C1 C4-алкилом, C1 - C4-алкокси, C1 C4-алкилмеркапто, C1 - C4-алкилсульфонилом, фенокси, циано, ди-C1 - C4-алкиламиногруппой, за исключением незамещенного 2-пиридила, пиразил, пиразолил, пиридазил или тиазолил, которые могут быть замещены C1 - C4-алкилом или галогеном;
Х прямой или разветвленный C1 C3-алкилен;
R2 водород, ди-C1 C5-алкилкарбамоил, необязательно замещенный C1 C5-алкил, C2 C5-алкенил, C2 - C5-алкинил, C3 C6-циклоалкил, фенил или радикал Y - R5, где Y O, SO2, CO или CO2, а R5 водород, необязательно замещенный C1 C5-алкил, C3 C6-циклоалкил или галогензамещенный фенил;
R3 водород, необязательно замещенный C1 C5-алкил или C3 C6-циклоалкил;
R4 циано или нитро;
Z CH или N,
или их соли в количестве 5 20 мас. целевые добавки остальное.
| Патент США N 4918088, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1995-06-27—Публикация
1991-06-05—Подача