Изобретение относится к новому антибиотику балимицину, получаемому из актиномицентной культуры Hoeshst India Limited У-8621022. Балимицин представляет собой антибактериальный антибиотик, относящийся к классу гликопептидов структурной формулы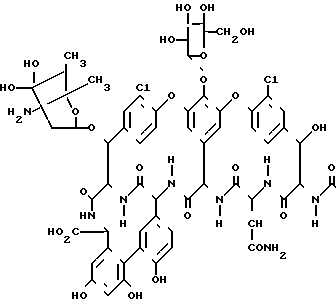
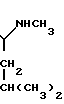
Гликопептидные антибиотики являются антибиотиками с узким спектром действия, которые обладают активностью главным образом по отношению к грамположительным бактериям. Их активность по отношению к стойким к метицилину штаммам S.aureus (MRSA) делает их ценным лекарственным препаратом при лечении инфекций, вызываемых MRSA. Они могут также использоваться в качестве стимуляторов роста в ветеринарии. Гликопептидные антибиотики известны и описаны в Topics in Antibiotic Chemistry. т.5, с. 119 (1980), Journal of Antibiotics, т. 38, с. 561 (1985), Journal of Antibiotics, т. 40, с. 924 (1987), Journal of Organic Chemistry, т. 54, с. 983 (1989).
Однако описанный балимицин отличается от всех известных гликопептидных антибиотиков своей молекулярной формулой, поэтому он составляет предмет настоящего изобретения. Ключевой поиск в Chemical Abstracts по молекулярному весу и молекулярной формуле также подтвердил новизну этого соединения.
Микроорганизм культуры N Hoechst India Limited У-86, 21022, называемый далее У-8621022, использующийся для получения балимицина, был выделен из почвы, собранной в лесу Thamu, Гималаи, Индия. Микроорганизм У-8621022 относится к отряду Аctinomycetales. Он внесен в Германскую коллекцию микроорганизмов с соблюдением условий Будапештского договора от 6 апреля 1990 года под номером DSM 5908.
Задачей настоящего изобретения является также создание способа получения нового антибиотика балимицина из культуры N Hoechst India Limited У-8621022, ее мутантов и вариантов. Предлагаемый способ включает выращивание культуры У-8621022, ее мутантов и вариантов в аэробных условиях в питательной среде, содержащей источники углерода и азота, питательные неорганические соли и микроэлементы, и очистку антибиотика от культурного бульона. Источниками углерода могут быть крахмал, глюкоза, сахароза, декстрин, фруктоза, меласса, глицерин, лактоза или галактоза. Предпочтительным источником углерода является глицерин. Источниками азота могут быть соевая мука, мука из арахисовых орехов, дрожжевой экстракт, экстракт из мяса, пептон, солодовый экстракт, настой кукурузы, желатин или касаминовые кислоты. Предпочтительным источником азота является мука их арахиса. В качестве питательных неорганических солей могут использоваться гидрофосфат натрия, гидрофосфат калия, хлорид натрия, хлорид кальция, карбонат кальция, нитрит натрия, хлорид кальция, карбонат кальция, интит натрия, сульфат аммония или сульфат магния. Микроэлементами могут быть соли железа, марганца, меди, цинка, кобальта или других тяжелых металлов.
Выращивание культуры N У-8621022 предпочтительно осуществляют при 28-32оС и рН 6,6-8,0. Наиболее предпочтительными условиями выращивания этой культуры являются температура 29±1оС и рН примерно 7,0.
Ферментацию проводят предпочтительно в течение 60-72 ч. При этом достигается оптимальный выход антибиотика в соответствии с настоящим изобретением. По конкретному варианту осуществления ферментацию проводят в течение 68-72 ч в погруженном состоянии во встряхиваемых колбах или лабораторном ферментере. При желании к содержимому ферментера может добавляться антивспениватель, например Desmophen (полиспирты, фирма Bager-AG, Леверкузен, ФРГ). Протекание ферментации и образование соединения в соответствии с настоящим изобретением может контролироваться с помощью высокопроизводительной жидкостной хроматографии (НР С) или путем определения биологической активности культурного бульона по отношению к Staphylococci с помощью известного метода анализа по диффузии бактерий в агаровых пластинах. Предпочтительной культурой является Staphylococcus aureus 3066, который, как известно из литературы, является стойким по отношению к бета-лактамовому антибиотику метицилину.
(полиспирты, фирма Bager-AG, Леверкузен, ФРГ). Протекание ферментации и образование соединения в соответствии с настоящим изобретением может контролироваться с помощью высокопроизводительной жидкостной хроматографии (НР С) или путем определения биологической активности культурного бульона по отношению к Staphylococci с помощью известного метода анализа по диффузии бактерий в агаровых пластинах. Предпочтительной культурой является Staphylococcus aureus 3066, который, как известно из литературы, является стойким по отношению к бета-лактамовому антибиотику метицилину.
Балимицин может быть выделен из культурального бульона, например, путем прямой адсорбции на подходящем адсорбенте, в частности, на активированном угле, Diaion HP-20 (высокопористая смола на основе полистиролдивинилбензольного сополимера, фирма Mitsubishi Chemical Industries Япония), или амберлите ХАD (пористая смола на основе полистирольного эфира акриловой кислоты, фирма Rohm S.Haas CO. США). Предпочтительным адсорбентом является Diaion НР-20. Элюирование балимицина из адсорбента может быть осуществлено с помощью подвижных фаз, таких как вода, метанол, ацетон, ацетонитрил или их подходящие комбинации. Предпочтительными элюентами являются водный раствор метанола или ацетон.
(высокопористая смола на основе полистиролдивинилбензольного сополимера, фирма Mitsubishi Chemical Industries Япония), или амберлите ХАD (пористая смола на основе полистирольного эфира акриловой кислоты, фирма Rohm S.Haas CO. США). Предпочтительным адсорбентом является Diaion НР-20. Элюирование балимицина из адсорбента может быть осуществлено с помощью подвижных фаз, таких как вода, метанол, ацетон, ацетонитрил или их подходящие комбинации. Предпочтительными элюентами являются водный раствор метанола или ацетон.
Вышеуказанные активные элюаты, содержащие балимицин, могут быть сконцентрированы и затем дополнительно очищены различными способами. К примеру, для этой цели могут быть использованы реадсорбция и элюирование с использованием в качестве адсорбента активированного древесного угля, амберлита ХАD-4 и 7 Diaion НР-20, гель-фильтрация с использованием сефадекса LH-20 или гелей ряда С (фирма Pharmacia Fine Chemicals АВ, Швеция) и воды-метанола, ацетона или их подходящих комбинаций в качестве элюента, ионообменная хроматография с использованием IRC (H+) при рН 6,5-89,5 и 0,1 и НСl в качестве элюента, или жидкостная хроматография под средним давлением (МРLC) на подходящем адсорбенте, например диоксиде кремния, модифицированном диоксиде кремния, таком как обратнофазный диоксид кремния, например октадецилдиметилсилилированный диоксид кремния (RP-18), нейтральный оксид алюминия.
Кроме того, для этой цели можно использовать противоточную хроматографию с определенной многокомпонентной системой. Предпочтительный способ очистки включает многократную МРL C на RP-18 с использованием в качестве элюента водного раствора метанола или ацетонитрила, содержащего подходящие добавки, такие, например, как кислота или соль.
Балимицин может быть переведен в его фармакологически приемлемую соль, например, путем взаимодействия с неорганической или органической кислотой, такой как HCl, H2SO4, лимонная, молочная, янтарная, уксусная, трифторуксусная кислоты, осуществляемого известным способом.
Физико-химические и спектральные характеристики балимицина (в виде трифторацетата).
Балимицин и его физиологически приемлемые соли могут вводиться в организм, например, орально, внутримышечно или внутривенно. Фармацевтические препараты, содержащие балимицин в качестве активного вещества, также являются предметом настоящего изобретения. Они могут быть получены путем смешения указанного соединения с одним или несколькими фармакологически приемлемыми вспомогательными веществами и/или наполнителями, такими, например, как носители, эмульгаторы, скользящие вещества, корригенты, красители или буферы, и перевода затем в фармакологическую форму, например, таблетки, таблетки с покрытием, капсулы или суспензии, или растворы, подходящие для парентерального введения.
Примерами подходящих вспомогательных веществ и/или наполнителей являются трагант, лактоза, тальк, агар-агар, полигликоли, этанол и вода. Подходящими и предпочтительными для парентерального введения являются водные суспензии или растворы. Можно также вводить активные вещества и как таковые, без инертных веществ или разбавителей. Для этого они используются в подходящей форме, например, в виде капсул.
Подходящие дозы соединений в соответствии с настоящим изобретением или их физиологически приемлемых кислых аддитивных солей для взрослых особей весом примерно 60 кг находятся в пределах примерно 0,1-20, предпочтительно 0,5-4 г/день.
Можно вводить указанную дозу в один или, что предпочтительно, в несколько приемов. Единичная доза может содержать примерно 50-4000, предпочтительно примерно 500-2000 мг активного вещества. Более подробно настоящее изобретение характеризуется нижеследующими примерами и формулой изобретения.
П р и м е р 1. Выделение культуры У-8621022 из почвы (а) Состав питательной среды, г: кукурузный крахмал 10,0 казеин 1,0 пептон 1,0 дрожжевой экстракт 1,0 К2НРО4 0,5 порошок агара 13,0
деминерализованная вода 1,0 л рН 7,5 (в) Посев почвы и выделение.
10 г почвы, собранной в лесу Thamu, Гималаи, Индия, добавляли к 90 мл стерилизованной деминерализованной воды в колбе Эрлеймейера на 250 мл, которую встряхивали в течение 2 ч на ротационной встряхивающей машине (220 об. /мин). Полученную суспензию почвы последовательно разбавляли в 10 раз до 10-5. 10 мл суспензии из последнего разбавления помещали в центре стерильной стеклянной чашки Петри диаметром 15 см, в которую затем заливали 50 мл вышеуказанной среды для выделения с добавкой 25 мкг/мл амфотерицина В в качестве антигрибкового агента, охлаждали до 45оС и тщательно перемешивали, совершая кругообразные движения. Смеси суспензии и среды давали затем осесть и выдерживали в течение 7 дней при 28±1оС. Периодически осматривали содержимое чашек Петри и отделяли культуру N У-8621022 от растущих микроорганизмов.
П р и м е р 2. Сохранение культуры У-8621022. Состав среды для сохранения.
Культуру N У-8621022 сохраняли в следующей среде, г: солодовый экстракт 10,0 дрожжевой экстракт 4,0 глюкоза 4,0 порошок агара 13,0
деминерализованная вода 1,0 л рН 7,0
После растворения компонентов при нагревании раствор разливали в пробирки и стерилизовали в течение 20 мин при 121оС. Пробирки затем ставили в наклонное положение и охлаждали. При этом происходило затвердевание раствора. Скошенный агар засевали культурой N У-8621022 с помощью проволочной петли и выдерживали при 28±1оС до начала интенсивного роста. Выращенную культуру хранили в холодильнике при 8оС.
П р и м е р 3. Ферментация культуры У-8621022 в встряхиваемых колбах
Состав среды 1 для засева, г: глюкоза 15,0 соевая мука 15,0 настой кукурузы 5,0 СаСО3 2,0
деминерализованная вода 1000 мл рН 7,0
Указанную среду для засева разливали в колбы Эрленмейера на 500 мл в количестве по 80 мл и выдерживали в автоклаве в течение 20 мин. Колбы затем охлаждали до комнатной температуры, содержимое каждой колбы засевали с помощью петли хорошо развитой культурой в соответствии с примером 2 и встряхивали на вращающейся встряхивающей машине в течение 72 ч (при скорости вращения 240 об./мин) при 29±1оС, получая в результате посевную культуру.
Состав продукционной среды, г: глицерин 15,0 соевая мука 10,0 СаСO3 1,0 NaCl 5,0 СоСl2 0,001
деминерализованная вода 1000 мл рН 7,0
По 60 мл продукционной среды заливали в колбы Эрленмейера на 500 мл и выдерживали в автоклаве в течение 20 мин при 121оС. Колбы затем охлаждали и засевали вышеуказанной посевной культурой (1 об.). Ферментацию проводили на вращающейся встряхивающей машине (скорость вращения 240 об./мин) при 29±1оС в течение 68 ч.
Количество образующегося антибиотика определяли с помощью высокопроизводительной жидкостной хроматографии и испытания на биологическую активность по отношению к S/aureus 3066, проводимого известным диффузионным методом. После сбора клеток культурный бульон подвергали центрифугированию и балимицин выделяли из фильтрата и очищали, как это описано в примере 4.
П р и м е р 4. Выращивание культуры У-8621022 в ферментаторах.
Получение посевной культуры в встряхиваемых колбах.
Посевную среду в соответствии с примером 3 помещали в количестве 160 мл в литровые колбы Эрленмейера и выдерживали в автоклаве в течение 20 мин. Выращивание посевной культуры в колбах осуществляли таким же образом, как это описано в примере 3.
Ферментация в промышленных масштабах.
Состав продукционной среды, г: глицерин 15,0 соевая мука 10,0 СаСО3 1,0 NaCl 5,0
деминерализованная вода 1000 мл рН 6,8
100 мл продукционной среды с добавкой 30 мл десиофена в качестве антивспенивателя стерилизовали в ферментаторе Marubishi in situ в течение 24 мин при 121оС, охлаждали до 29±1оС и засевали 3 л вышеуказанной посевной культуры.
Ферментацию проводили в следующих условиях: температура 29±5оС перемешивание 110-120 об./мин азерация 80-100 ер
продолжитель- ность выращивания 69-72 ч
Образование антибиотика контролировали с помощью анализа биологической активности по отношению к S.aureus 3066. В процессе ферментации рН культурного бульона находилось в пределах 6,0-7,0. После окончания выращивания культурный бульон подвергали центрифугированию, антибиотик балимицин выделяли из фильтрата культуры и подвергали очистке, как это описано ниже.
Выделение и очистка балимицина.
Примерно 100 мл полученного, как это описано в примере 4, в результате выращивания бульона отделяли от мицелия путем центрифугирования. Полученный фильтрат бульона (80 л, рН 6,5) пропускали через колонку, заполненную 5 л Diaion НР-20 с водой. Колонку затем промывали 40 мл деминерализованной воды до обесцвечивания промывной воды. После этого колонку промывали 8 л 1 М водного раствора NaCl и 10 л деминерализованной воды. Описанный процесс повторяли еще раз. Колонку затем промывали 9 л 30%-ного водного раствора МеОН, и, наконец, проводили элюирование 51 л 75%-ного водного раствора, фракциями по 1 л. Присутствие балимицина в элюатах контролировали с помощью определения биологической активности по отношению к Staphylococcus aureus 3066, являющемуся стойким организмом по отношению к метицилину. Объединенные активные элюаты концентрировали в вакууме при 40-45оС до объема примерно 1 л и лиофизировали, получая в результате 38 г сырого порошкообразного балимицина.
Этот сырой материал, разделенный на 3 порции по 10 г каждая, подвергали жидкостной хроматографии под средним давлением (МL PC) в стеклянной колонке размером 6,5х55 см, заполненной RP-18, объем которого составлял 1,2 л. Элюирование проводили водой, содержащей 0,1% трифторуксусную кислоту (TFA), затем 5%-ным ацетонитрилом (4 л) и 7,5%-ным водным раствором ацетонитрила (9 и 10% ацетонитрила, 24,5 л), содержащим 0,1% трифторуксусной кислоты. Балимицин элюировался 10%-ным ацетонитрилом, который собирали фр акциями по 500 мл. Антибиотиковую активность в них контролировали in vitro. Объединенные активные элюаты концентрировали в вакууме при 40оС и лиофилизировали, получая в результате 2,1 г балимицина в виде бледно-желтого порошка. В результате трех таких операций из 30 г сырого балимицина получали 6,3 г получистого продукта.
6,3 г полученного получистого балимицина разделяли на три порции по 2,1 г и подвергали окончательной очистке с помощью MPLC в стеклянной колонке размером 6,0х45 мм со слоем RP-18 500 мл. Колонку промывали 1 л воды, содержащей 0,1% TFA, и затем последовательно 2 и 1,5 л 5% и 7,5%-процентного водного раствора ацетонитрила соответственно, содержащего 0,1% TFA. Балимицин элюировали 10% -ным водным раствором ацетонитрила, содержащим 0,1% TFA, отбирая фракции по 250 мл, наличие балимицина в которых контролировали с помощью УФ-детектора при 220 нм и анализа на антибиотиковую активность, проводимого in vitro. Собранный элюат в количестве 8 л концентрировали в высоком вакууме при 40оС и лиофилизировали, получая 600 мг балимицина в форме трифторацетата в виде белого порошка. Из 6,3 г получистого продукта получали 1,8 г чистого балимицина.
Далее приводятся характеристики и свойства балимицина, полученного согласно изобретению.
1. Биологические свойства балимицина
Антибактериальная активность балимицина в единицах МIC, необходимой для торможения роста различных бактерий, приведена в табл. 2.
13С-ЯМР-спектр балимицина в (Д6)-DMCO, Т=320оК, с=28 мг/мл
Сигнал мультиплет- хим. сдвиг Сигнал мультиплет- хим. сдвиг
ность ность
1 с 211,47 34 д 116,13
Идентификация У-8621022
Идентификация У-86-21022 на уровне рода как Hocardia основана на анализе клеточной стенки, как предложено Н.Р. Lechevalier в Руководстве по систематической бактериологии Берже, т. 4, 1987. Морфологическая и биохимическая характеристика основана на процедурах, рекомендованных Е.В. Shirling and D. Gottlieb в Международном проекте по стрептомицетам в International Journal of Systematic Barteriology, т. 16, N 3, 1966, с. 313-340.
Анализ клеточной стенки Диагностические арабиноза, сахара галактоза ДАР мезо-ДАР миколовые кислоты присутствуют
Культуральные характеристики У-8621022 приведены в табл. 3.
Микроскопическое наблюдение
Рост на ISP средах показал спутанный до длинного разветвленный субстратный мицелий. Нет конидиоспор, спорангия или склероций.
Использование источников углерода У-8621022 Сахар Использование Отрицательный контроль Д-глюкоза + Сахароза + Д-ксилоза + Д-маннит + Инозитол + L-рамноза +
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАНКОРЕЗМИЦИН (ВАРИАНТЫ), ЕГО ИСПОЛЬЗОВАНИЕ, ШТАММ AMYCOLATOPSIS ВИДА HIL-006734 ДЛЯ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2228337C2 |
| ГЛИКОПЕПТИДЫ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ, ОБЛАДАЮЩИЙ АНТИБИОЦИДНЫМ ДЕЙСТВИЕМ | 1992 |
|
RU2099349C1 |
| Способ получения гликопептидных антибиотиков А82846А, А82846В и А82846С или их солей, штамм актиномицета NocaRDIa оRIеNтаLIS NRRL 18098-продуцент гликопептидных антибиотиков А82846А, А82846В и А82846С, Штамм актиномицета NocaRDIa оRIеNтаLIS NRRL 18099-продуцент гликопептидных антибиотиков А82846А, А82846В и А82846С и штамм актиномицета NocaRDIa оRIеNтоLIS NRRL 18100-продуцент гликопептидных антибиотиков А82846А, А82846В и А82846С. | 1987 |
|
SU1724015A3 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА ПРАДИМИЦИНА, ШТАММ ACTINOMADURA SPECIES - ПРОДУЦЕНТ ПРАДИМИЦИНА | 1992 |
|
RU2057181C1 |
| МУМБАЙСТАТИН, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКОГО ПРЕПАРАТА | 1999 |
|
RU2221870C2 |
| Способ получения антибиотика | 1978 |
|
SU738517A3 |
| СПОСОБ ФЕРМЕНТАТИВНОГО ПОЛУЧЕНИЯ ЦЕФАЛОСПОРИНА С | 1992 |
|
RU2094463C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА | 1990 |
|
RU2029783C1 |
| ТИОМАРИНОЛ, ОБЛАДАЮЩИЙ АНТИБАКТЕРИАЛЬНЫМИ СВОЙСТВАМИ, ШТАММ МИКРООРГАНИЗМА ALTEROMONAS RAVA SANK-73390 - ПРОДУЦЕНТ ТИОМАРИНОЛА И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА ТИОМАРИНОЛА | 1992 |
|
RU2077534C1 |
| АНТИБИОТИК ИНА 5812, ШТАММ-ПРОДУЦЕНТ Streptomyces roseoflavus ИНА-Ас-5812 И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА | 2013 |
|
RU2572341C2 |




Использование: медицина, микробиологическая промышленность, производство антибиотиков, ветеринария. Сущность изобретения: новый антибиотик балимицин, способ его получения и штамм Actinomycetes species DSM 5908 продуцент балимицина. Балимицин, представляющий собой соединение молекулярной формулы C66H73Cl2N9O24 является новым гликопептидным антибиотиком, который получают путем культивирования микроорганизма Actinomycetes species DSM 5908 в аэробных условиях в питательной среде, содержащей источники углерода, азота минеральных солей и микроэлементов при 38 - 32°С и при рН 6 8 в течение 68 72 ч погруженным методом, целевой продукт выделяют из культуральной жидкости и очищают хроматографией. 3 с. и 1 з.п. ф-лы, 2 ил. 3 табл.

2. Способ получения антибиотика балимицина структурной формулы
заключающийся в том, что культивируют штамм микроорганизма Actipomycetesspecies DS M5908 в аэробных условиях в питательной среде, содержащей источники углерода, азота, минеральных солей и микроэлементов при 28 32oС и pH 6 8 в течение 68 72 ч погруженным методом, целевой продукт выделяют из культурной жидкости и очищают хроматографией.
Приоритет по пунктам
27.07.90 по пп. 2 4.
Авторы
Даты
1995-09-10—Публикация
1991-07-25—Подача