Изобретение относится к новым соединениям антибиотика и способам их получения.
В описании патента Великобритании 2166436 описано получение антибиотиков 541, которые можно выделить из продукта ферментации вида Streptomyces. Антибиотики S541 представляют собой группу родственных соединений, имеющих неполную форму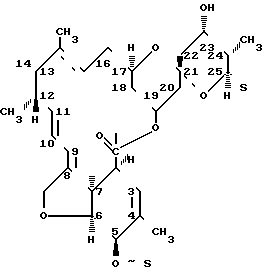 Выявлена дополнительная группа соединений, обладающих антибиотической активностью, которые можно получить посредством выделения их из культуры микроорганизмов рода Sterptomyces. Новые соединения предлагаемого изобретения обладают антибиотической активностью и/или применяются как промежуточные продукты при получении других активных соединений, и/или при выделении или очистке соединений антибиотиков S541.
Выявлена дополнительная группа соединений, обладающих антибиотической активностью, которые можно получить посредством выделения их из культуры микроорганизмов рода Sterptomyces. Новые соединения предлагаемого изобретения обладают антибиотической активностью и/или применяются как промежуточные продукты при получении других активных соединений, и/или при выделении или очистке соединений антибиотиков S541.
Предлагаемые соединения представляют собой 23-кетон, аналоги антибиотиков S541.
Таким образом, в одном варианте настоящего изобретения предлагаются, в частности, соединения формулы (II)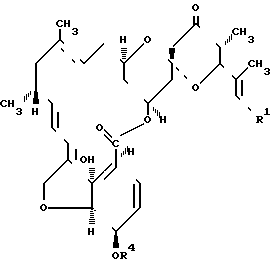 где R1 представляет метильную, этильную или изопропильную группу OR4, является гидроксильной группой или метоксигруппой.
где R1 представляет метильную, этильную или изопропильную группу OR4, является гидроксильной группой или метоксигруппой.
В указанных соединениях формулы (II) R1 является изопропильной группой.
Особенно важными активными соединениями предлагаемого изобретения являются соединения формулы (II), в которых R1 является изопропильной группой и OR4 представляет гидроксильную группу.
Соединения предлагаемого изобретения могут применяться в качестве антибиотиков и/или как промежуточные соединения для получения других активных соединений и/или при выделении и очистке соединений антибиотиков S541.
Предлагаемые соединения обладают антибиотической активностью, например антигельминтной активностью, против нематодов, в частности анти-эндопаразитарной и анти-эктопаразитарной активностью.
Эктопаразиты и эндопаразиты заражают людей и целый ряд животных, особенно имеют широкое распространение среди сельскохозяйственных животных, таких как свиней, овец, крупного рогатого скота, коз и домашней птицы, лошадей и домашних животных, например собак и кошек. Паразитатная инфекция домашнего скота, приводящая к анемии, недостаточности питания и потере веса, является основной причиной экономических потерь во всем мире.
К представителям эндопаразитов, заражающих указанных животных и/или людей, относятся Ancelostoma, Ascaridia, Ascaris, Aspicularis, Brugia, Bunostomum, Copillar Chabortia, Cooperia, Dictyocaulus, Pirofilaria, Dracunculus, Enterobius, Haemonehus, Acterakis, Loa hecator, Nematodirus, Nematospiroides, Heligomoroidis, Nippostrongylus, Oesophagostomun, Onchocerca, Ostertagia, Oxyuris, Parascaris, Strongylus, Strongyloides, Syphacia, Foxascacis, Toxocara, Trichonema, Trichostrongylus, Trichinella, Trichuris, Uncinaria и Wuchareria.
Примерами эктопаразитов, заражающих животных и/или людей, являющимся членистоногие энтопаразиты, например жалящие насекомые, падальная муха, блоки, вши, клещи, сосущие насекомые, искодовые клещи и другие двукрылые насекомые-вредители.
К примерам такого рода октопаразитов, заражающих животных и/или людей, относятся Ambylomma, Boophilus Chorioptes, Calliphore, Demodex, Demallenia, Dermatobia Gastrophilus, Haematobia, Haematopinus, Haemophysalis, Hyalomma, Hyperderma, Ixodes, Linognathus, Lucilia, Melophagus, Oestrus, Otobius, Otodectes, Psorergates, Rhipicephal Sarcoptes, Stomoxys и Tabanus.
Обнаружено, что предлагаемые соединения эффективно действуют как in vitro, так и in vivo, против широкого ряда эндопаразитов и эктопаразитов. В частности, обнаружено, что предлагаемые соединения активно действуют против нематодов, таких как Haemonchus contortus, Ostertagicircu mcincta, Irichostrongglus colubiformis, Dicty caulus Viviparis, Cooperia oncophera, ostertagia ostertagi, Hematospi roides dufius и Nippostrongylus brazililusis, и паразитарных клещей, например Sarcoptes sp. и Psoroptes sp. Таким образом предлагаемые соединения применяются при лечении животных и людей с эндопаразитарной и/или эктопаразитарной инфекциями.
Виды паразитов меняются в соответствии с хозяином (животным) и доминирующим местонахождением инфекции. Следовательно, например, возбудители Haemonchus contortus, Ostertagia circumcincta и Trichostrongylus colubifornus обычно поражают овец и преимущественно локализуются в желудке и тонкой кишке, в то время как Dictyocaulus, Viviparus, Cooperia oncophora и Ostertagia ostertagi обычно поражают крупный рогатый скот и локализованы в легких, кишечнике или желудке соответственно.
Антибиотическая активность предлагаемых соединений может быть продемонстрирована, например, своей активностью in vitro против свободно живущих нематодов, например Cacnorhabiditis elegans.
Кроме того заявленные соединения имеют применение в качестве противогрибковых веществ, например, против штаммов Candida, как например, Candida albicans и Candida glabrata, и против дрожжей, таких как Saccharomyces carlsbergensis.
Предлагаемые соединения имеют применение в борьбе с вредителями-насекомыми, клещами и нематодами в сельском хозяйстве, садоводстве, лесоводстве, здравоохранении и хранении продуктов. Ими можно успешно обрабатывать вредителей почвы и сельскохозяйственных культур, включая хлебные злаки (например, пшеницу, ячмень, маис, рис), овощи (например, сою), фрукты (например, яблоки, виноград и цитрусовые), корнеплоды (например, сахарную свеклу, картофель). Характерными примерами таких вредителей являются фруктовые клещи и тля, например Aphis fabae, Aulacorthum circumflexum, Myzus persical, Nephotettix cincticeps, Hilparvate lugens, Panonychus ulmi, Phorodon humuli, Phyllocoptruta oleivora, Tetranychus urtical и представители рода Trialeuroides, нематоды, например представители рода Aphelencondes, Olobodera, Heterodes Miloidogyne и Panagrellus, чешуйчатые, например Helioth Plutella и Spodeptera, долгоносик-каландрина, например Anthonomus grandis и Sitophlus granarius, хрущаки мучные, например Tribolium castaneu, мухи, например Musca domestica, муравьи Рихтера; моли-минеры узкокрылые; Pear psylla трипсы табачные; таракановые, например Blatella germanica и Pesiplaneta amerilna, москитные, например Aedes algypti.
Предложены соединение формулы (II), которые могут быть использованы в качестве антибиотиков. В частности, их можно использовать при лечении животных и людей, пораженных эндопаразитарной, эктопаразитарной и/или грибковой инфекциями и в качестве пестицидов для борьбы с вредителями-насекомыми, клещами и нематодами, в сельском хозяйстве, садоводстве или лесном хозяйстве, в качестве пестицидов для борьбы с вредителями-насекомыми, клещами и нематодами, в сельском хозяйстве, садоводстве или лесном хозяйстве, в качестве пестицидов и других обстоятельствах, например в хранилищах, зданиях или других общественных местах или местах локализации сельскохозяйственных вредителей. Предлагаемые соединения могут быть применены либо к хозяину (животному или человеку), либо к культурным растениям или другой растительности, либо к самим вредителям или месту их расположения.
Предлагаемые соединения могут быть сформулированы для приема в любой удобной форме при использовании в ветеринарии или практической медицине. Таким образом, предлагаемое изобретение содержит в пределах своего объема фармацевтические композиции, содержащие соединение, пригодное для применения в ветеринарии или терапии. Такие композиции могут быть представлены при использовании в традиционной форме с помощью одного или нескольких подходящих носителей или наполнителей.
Предлагаемые композиции содержат составы в форме, особенно пригодной для парентерального (в том числе, введение внутрь молочной железы), орального, ректального, местного применения в виде имплaнтанта, для применения при глазных, ушных или заболеваниях мочеполовой системы, подходящими способами и агентами для приготовления состава предлагаемых соединений пригодных для использования в ветеринарии или терапии, являются способы, которые описаны в патенте Южной Африки N 85/7049 для соединений антибиотиков S541.
Предлагаемые соединения можно применять в комбинации с другими фармацевтически активными ингредиентами.
Суммарная суточная доза предлагаемых соединений с применением как в ветеринарии, так и в терапии, будет соответственно в интервале 1-2000 мг/кг веса тела, предпочтительно 50-1000 мг/кг, причем указанные дозировки можно принимать в дробных дозах, например 1-4 раза в день.
Предлагаемые соединения можно составлять в любой удобной форме, пригодной для земледелия или садоводства. Таким образом предлагаемое изобретение включает в пределах своего объема составы, содержащие соединение, предназначенное для применения в земледелии или садоводстве. Такие рецептуры включают сухие или жидкие формы, например дусты, включая пылевидные субстраты или концентраты, порошки, в том числе растворимые или смачиваемые порошки, гранулы, включая микрогранулы и диспергируемые гранулы, таблетки, текучие вещества, эмульсии, например, разбавленные эмульсии или эмульгируемые концентраты, пропиточные составы, например, составы для пропитки корней и семян, протравливатели семян, семенные гранулы, масляные концентраты, масляные растворы, инъекции, например инъекции в ствол, растворы или опрыскивания, дымы и туманы.
Подходящие способы и агенты для составления рецептуры предлагаемых соединений для применения в садоводстве или земледелии включают те, которые раскрыты в патенте Южной Африки N 85/7049 для антибиотиков S541.
При составлении рецептуры концентрация активного вещества обычно составляет от 0,01 до 99 мас.% и более предпочтительно от 0,01-40 мас.%.
Промышленные (товарные) продукты обычно приготовлены в виде концентрированны композиций, которые при использовании разбавляют до требуемой концентрации, например от 0,001 до 0,0001 мас.%.
При использовании в ветеринарии или в садоводстве и земледелии и в случае, когда предлагаемые соединения являются продуктами, образуемыми посредством ферментации, желательно использовать весь бродильный бульон в качестве источника активных соединений. Кроме того, может быть пригодно использование обезвоженного бульона (содержащего мицелий) или мицелия, отделенного из бульона и пастеризованного или более предпочтительно высушенного. При желании указанный бульон или мицелий могут быть сформированы в композиции, как указывалось выше, включающие традиционные инертные носители, наполнители или разбавители.
Антибиотические соединения предлагаемого изобретения могут вводиться и применяться в комбинации с другими активными ингредиентами.
В частности, предлагаемые соединения антибиотика могут использоваться вместе с соединениями антибиотиков S541 или с другими антибиотическими соединениями, в случае, когда неочищенные продукты брожения взаимодействуют без предшествующего или последующего отделения; при использовании соединений в земледелии, где важно обеспечить (сохранить) низкую себестоимость продукции.
Предлагается способ получения соединений формулы (II), включающий стадию культивирования микроорганизма Steptomyces, способного образовывать хотя бы одно из предлагаемых соединений и при желании выделять из него указанное соединение.
Микроорганизмами, способными образовывать вышеуказанные вещества, являются штаммы нового вида рода Streptomyces, которые называются Streptomyces thermoarohaensis - образец указанного микроорганизма, который является почвенной культурой, помещен на хранение в постоянную коллекцию национального собрания промышленных и морских бактерий Torry Resear Station, Aberdeen, United Kingtom с присвоением ему регистрационного номера NCYB 121015, Мутанты штамма Streptomyces thermoarchaensis NCIB 12015 могут также быть преимущественно использованы, и в постоянную коллекцию культур Национального собрания промышленных и морских бактерий сданы в депозитарное хранение (26.06.1985 г) 4 штамма мутантов, которым были присвоены регистрационные номера NCIB 12111, NCIB 12112, NCIB 12113 и NCIB 12114.
Получение предлагаемых соединений посредством ферментации подходящего вида Streptomyces может быть достигнуто общепринятыми методами, например путем выращивания микроорганизма Streptomyces в присутствии способных к ассимиляции источников углерода, азота и минеральных солей, способные к ассимиляции источники углерода могут быть при наличии азота и минералов либо простых или комплексных питательных веществ. Источники углерода обычно включают глюкозу, мальтозу, крахмал, глицерин, кормовую патоку, декстрин, лактозу, сахарозу, фруктозу, карбоксильные кислоты, аминокислоты, глицериды, спирты, алканы и растительные масла. Источники углерода обычно содержат 0,5-10 мас.% сбраживаемой среды.
Источники азота включают бобово-соевую муку, настойку пшеницы, растворы, перегонки, дрожжевые экстракты, муку из семян хлопка, пептоны, муку из земляного ореха, содовый экстракт, черную патоку, казеин, смеси аминокислот, аммоний (газообразный или раствор), соли аммония и нитраты. Кроме того можно использовать мочевину и другие амиды. Источники азота обычно содержат 0,1-10 мас.% сбраживаемой среды.
Питательные минеральные соли, которые могут быть включены в культуральную среду, содержат применяемые соли, имеющие способность отдавать ионы натрия, калия, аммония, железа, магния, цинка, никеля, кобальта, марганца, ванадия, хрома, кальция, меди, молибдена, бора, фосфата, сульфата, хлорида и карбоната.
Культивирование Streptomyces стрептомицеты обычно проводится при температуре в интервале 20-50оС, предпочтительно 25-40оС, более предпочтительно около 34оС, причем желательно сопровождать ее аэрацией и взбалтыванием, например встряхиванием или интенсивным перемешиванием. Среда может быть первоначально инокулирована небольшим количеством спорулированных взвесей микроорганизмов, но для избежания задержки роста можно приготовить растительный посевной материал микроорганизма путем инокуляции небольшого количества культуральной среды спорообразной формой указанного организма, при этом растительный инокулянт, который получен, может быть перенесен в сбраживаемую среду или в одну или более стадий посева, где возникает дополнительный рост перед переносом в основную ферментационную среду. Процесс ферментации обычно проводят при рН в интервале 5,5-8,5, предпочтительнее 5,5-7,5.
Ферментацию можно проводить в течение 2-10 дней, например около 5 дней.
В том случае, когда желательно отделить материал, содержащий соединения предлагаемого изобретения из всего бродильного бульона или выделить любое из отдельных соединений, указанное можно осуществлять посредством общепринятой методики выделения и отделения веществ. Предлагаемые соединения содержатся в мицелиях клеток, но их также можно обнаружить в бродильном бульоне, таким образом техника выделения может также быть применена к бродильному бульону после очистки. Методика выделения веществ может иметь широкое разнообразие.
Предлагаемые соединения могут быть выделены и отделены посредством разнообразных методов фракционирования, например элюированием, осаждением, фракционной кристаллизацией, экстракцией растворителем, которые можно комбинировать различными способами.
Выявлено, что экстракция растворителем и хроматография наиболее подходящих для выделения и отделения предлагаемых соединений.
После ферментации мицелий может быть собран традиционными методами, например фильтрацией или нейтрифугированием. После этого, например, соединения могут быть экстрагированы из мицелия соответствующими органическими растворителями, такими как кетоны, например ацетоном, метилэтилкетоном или метилизобутилкетоном: углеводородом, например гексаном; галогензамещенным углеводородом, например хлороформом, карбонтетрахлоридом или метиленхлоридом; спиртами, например метанолом или этанолом; или сложными эфирами, например метилацетатом или этилацетатом. Если мицелий содержит значительное количество воды, нужно использовать водорастворимые растворители.
Для достижения оптимального извлечения соединений желательно проводить более одной экстракции. Первую экстракцию надо выполнять с использованием смешивающегося с водой растворителя, например метанола или ацетона. Антибиотики можно извлечь как неочищенный экстракт путем удаления растворителя. Экстракты растворителя могут далее быть экстрагированы после уменьшения объема растворителя, например, выпариванием. На этой стадии предпочтительно использовать несмешивающийся с водой растворитель, например гексан, хлороформ, метиленхлорид или этилацетат, или их смеси, при этом для достижения хорошего разделения соединений антибиотика вводится достаточное количество воды. При удалении водонерастворимой фазы получают продукт, содержащий одно или более предлагаемых соединений, возможно вместе с соединениями антибиотика S541.
Очистку и/или отделение предлагаемых соединений можно осуществлять традиционными методами, например хроматографией (включая высокоэффективную жидкостную хроматографию на соответствующей подложке, такой как двуокись кремния, нефункциональная макросетчатая адсорбционная смола, например, поперечно-сшитые полистирольные смолы, такие как смолы Amberlite XAL-2 XAD-4 или XAD-1180 (Rohm Haus Ltd), или смола S112 (Kusteel Ltd), или поперечно-сшитый декстран, смешивающийся с органическим растворителем, например Sephadex LH 20 (Pharmacia UK Lud), или в случае высокоэффективной жидкостной хроматографии на подложках с обратной фазой, таких как углеводород, нанесенный на двуокись кремния, например С18, сшитая двуокись кремния. Подложка может быть в виде слоя с насадкой.
В случае использования нефункциональных макросетчатых смол, например XAD - 1180 или S112, для элюирования можно использовать смеси органических растворителей, например ацетонитрила с водой.
Раствор указанных соединений в соответствующем растворителе загружают в хроматографическую колонку из двуокиси кремния или Sephadex после первого уменьшения объема растворителя. Колонку могут по выбору промыть, а затем вымыть растворителем подходящей полярности. При применении колонок из Sephad и двуокиси кремния в качестве растворителей можно использовать спирты, например метанол; углеводороды, например гексан, ацетонитрил; галогензамещенные углеводороды, например хлороформ или метиленхлорид; или сложные эфиры, например этилацетаты.
Элюирование и разделение (очистку соединений) можно регулировать тонкослойной хроматографией и высокоэффективной жидкостной хроматографией, используя свойства соединений.
Предлагаемые соединения могут первоначально быть очищены хроматографией на двуокиси кремния, используя элюат, такой как хлороформ, этилацетат с последующей высокоэффективной жидкостной хроматографией. Полученный таким образом очищенный продукт может быть затем подвергнут хроматографии на сефадексовых колонках с использованием элюата, например ацтонитрила, а затем предлагаемые соединения могут быть выделены жидкостной хроматографией с высокой характеристикой.
Используя подходящие комбинации, соединения формулы (II) выделены как твердые вещества в почти чистом виде. Последовательность, при которой осуществляют стадии очистки, выбор тех, которые используют, и степень достигаемой очистки могут очень отличаться. Указанные соединения могут применяться при степени чистоты, соответствующей их предназначению. При использовании их в медицине желательно иметь степень чистоты хотя бы 90%, предпочтительно более 95%. Для ветеринарии и другого применения достаточна более низкая степень чистоты, например 30% или ниже.
Все температуры приведены при 0оС.
Соединения обозначены со ссылкой на источник "Факторы", которые представляют собой перечисленные ниже соединения формулы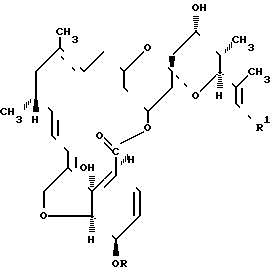 Фактор R R1 A -H -CH(CH3)2 B -CH3 -CH3 C -H -CH3 D -H -CH2CH3 E -CH3 -CH2CH3 F -CH3 -CH(CH3)2
Фактор R R1 A -H -CH(CH3)2 B -CH3 -CH3 C -H -CH3 D -H -CH2CH3 E -CH3 -CH2CH3 F -CH3 -CH(CH3)2
Факторы A,B,C, D, E,F можно получить способом, который описан в патенте Великобритании N 2166436.
П р и м е р 1. 23-кето Фактор А. 0,41 мл спорообразной суспензии Steptomyces thermard lusis NCIB 12015 в 10%-ном глицерине используют для инокуляции в 250 мл колбе Erlenmyez, содержащей 50 мл культуральной среды, состоящей из D-глюкозы 15,0 gl-1, глицерина 15,0 gl-1, соевого пептона 15,0 gl-1, NaCl 3,0 gl-1 и CaCO3 1,0 gl, добавлено до нормы дистиллированной воды. Перед помещением в автоклав рН доведена до 7,0 водным раствором АОН.
Колбу инкубируют при 28оС в течение 2 дней на круговой качалке, работающей при скорости 250 об/мин с 50 мм в диаметре движением по орбите, 4 мл порции используют затем для инокуляции каждого из четырех двухлитровых флаконов с широким горлышком, содержащих каждый по 200 мл одной и той же среды перед инкубированием в тех же самых условиях в течение 2 дней.
Содержимое указанных 4 флаконов далее используют для инокуляции 70-литрового ферментатора, содержащего 40 л той же культуральной среды с добавлением пропиленгликоля 2000 (0,06%). Полипропиленгликоль 2000 вводится в течение всего процесса ферментации для регулирования пенообразованием. Ферментацию проводят при 28оС с энергичным перемешиванием и аэрацией, достаточной для поддержания уровня растворенного кислорода больше 30% насыщения. Через 24 ч процесса брожения 800 мл и 9-литровые порции переносят в 70-литровый ферментатор, содержащий 40 л культуральной среды и 700-литровый ферментатор, содержащий 450 л культуральной среды соответственно. Оба ферментатора содержат культуральную среду, состоящую из D-глюкозы 2,5 gl-1 Malt, декстрина (М D30E) 25,0 gl-1, Arkasoy 50 12,5 gl-1, Beet Molasses 1,5 gl-1, K2HPO4 0,125 gl-1, CaCO3 (Ar) 1,25 gl-1 и силикона 1520 (Dow Corning) 0,6 gl-1, приведенную к норме дистиллированной водой. Перед стерилизацией рН доводят до 6,5 водным раствором H2SO4.
Указанные процессы ферментации выполняют при 34оС при энергичном размешивании и аэрации, достаточной для сохранения уровня растворенного кислорода больше, чем 30% насыщения. При необходимости добавляют антивспениватели из полипропиленгликоля 2000. Через 24 ч рН в каждом из ферментаторов доводят до 7,2 путем введения водного раствора H2SO4. Продукты ферментации собирают и объединяют через 4 дня.
Мицелий (10 кг) из собранной жидкой среды (423 л) выбирают в центрифуге Sparples PS 16AY. Мицелий интенсивно перемешивают в метаноле (5 л) в течение 40 мин и затем отфильтровывают. Остаток повторно суспендируют в метаноле (15л) и вновь фильтруют. Соединившиеся фильтраты (55 л) смешивают с водой (27 л) и 60-80 петролейным эфиром (предел кипения 60-80оС) (30 л) и перемешивают в течение 20 мин.
Полученные фазы отделяют в центрифуге Westfalia MEM12, а метанольную фазу (75 л) смешивают снова с водой (38 л) и 60-30 петролейным эфиром (30 л). Через 20 мин фазы вновь отделяют в центрифуге, причем в фазу петролейного эфира, чтобы разрушить полученную эмульсию, вводят ацетон (2,0 л). Метанольную фазу (110 л) смешивают с водой (38 л) и 60-80 петролейным эфиром (30 л) в третий раз, фазы отделяют как раньше. Ацетон (3 л) добавляют снова к петролейной эфирной фазе для разрушения полученной эмульсии.
Три фазы гексана объединяют (90 л) и концентрируют при низком давлении (температура выпарки 25оС). Концентрат (9,8 л) высушивают сульфатом натрия (3 кг) и выпаривают до масла.
Полученное масло растворяют в дихлорметане (0,5 л) и фильтруют через Дукалит 478. Раствор (0,9 л) загружают в хроматографическую колонну (150х10 см) на двуокиси кремния (Merck) при загрузке 6 л/ч, промывают дихлорметаном (4 л) и элюируют смесью хлороформа с этилацетатом (3:1). Фракции, элюирующие между 14,6 и 33,3 л, концентрируют до твердого вещества и растворяют в смеси хлороформа с ацетоном (3:1).
Полученный раствор повторно хроматографируют на колонке двуокиси кремния с тем же самым растворителем. Фракции, элюирующие между 14,5 и 31,5 л, высушивают до твердого вещества и растворяют в смеси хлороформа с этилацетатом (3: 1). Полученный раствор вновь хроматографируют на двуокиси кремния при тех же условиях, что и раньше, затем фракции элюирования между 14 л высушивают до твердого вещества.
Твердое вещество растворяют в 70%-ном ацетонитриле в воде (1,23 л) с достаточным количеством метанола, добавляемого для получения светлого раствора. Указанный раствор хроматографируют в 5 мл порциях на колонке Sperisorb ODS2. Содержимое колонны элюируют с помощью 70%-ного ацетонитрила при скорости течения, которая возрастает от 20 до 34 мл/мин через 24 мин. Фракции из каждой порции, которые элюированы между 12,4 и 16, были собраны вместе и разбавлены равным объемом воды. Полученный раствор затем загружают в колонку Mortedison на полистироле с сетчатой структурой (2 л). Колонку промывают 35%-ным раствором ацетонитрила и элюируют ацетоном. Фракции, элюирующие между 0,5 и 1,25 л, высушивают до твердого вещества.
Твердое вещество растворяют в ацетонитриле (20 мл) и хроматографируют на колонке из Sephades LH20 в том же растворителе. Фракции, элюирующие между 1,08 и 1,26, собирают и высушивают до твердого вещества.
Твердое вещество растворяют в 60%-ном ацетонитриле (10 мл) с достаточным количеством метанола, добавляемого для получения чистого раствора. Раствор хроматографируют в 2 мл порциях еще раз на колонке из Spherisorb OD92 и элюируют с помощью 60%-ного ацетонитрила при 25 мл/мин. Фракции, элюирующие между 0,95 и 1,08 л, собирают вместе и высушивают до твердого вещества. Полученное твердое вещество повторно растворяют в хлороформе (5 мл) и хроматографируют на колонке из силикагеля Merch 60. Раствор элюируют хлороформом при 10 мл/мин, и фракции, элюирующие между 400 и 790 мл, высушивают с получением названного соединения (33 мг) в виде твердого вещества, HNR-спектр соответствует содержащемуся 23-кето фактору А. Е.1-масс-спектроскопия дала ион молекулы при 610 и характеристические фрагменты при 592, 549, 498, 482, 370, 263 и 151.
Образец представлен, чтобы сравнить 23-кето фактор А, полученный при высокоэффективной жидкостной хроматографии с аналогичным кетоном, образуемым при химическом окислении фактора А.
| название | год | авторы | номер документа |
|---|---|---|---|
| МАКРОЦИКЛИЧЕСКИЙ ЛАКТОН, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИБИОТИЧЕСКОЙ АКТИВНОСТЬЮ, И ИНСЕКТОАКАРИЦИДНАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2100354C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ | 1988 |
|
RU2015981C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОЛИДНЫХ СОЕДИНЕНИЙ | 1990 |
|
RU2029770C1 |
| МАКРОЛИДНЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИБИОТИЧЕСКОЙ АКТИВНОСТЬЮ, ВЕТЕРИНАРНАЯ КОМПОЗИЦИЯ, ИНСЕКТОАКАРИЦИДОНЕМАТОЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ УНИЧТОЖЕНИЯ НАСЕКОМЫХ И/ИЛИ КЛЕЩЕЙ, НЕМАТОД | 1992 |
|
RU2099334C1 |
| Способ получения антибиотика в 508 | 1977 |
|
SU715034A3 |
| Способ получения антибиотика S @ , штаммы стрептомицетов - продуценты антибиотика S @ | 1985 |
|
SU1738090A3 |
| Способ получения антибактериального вещества | 1973 |
|
SU618053A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПИЛЮЛЬ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ | 1990 |
|
RU2014832C1 |
| Способ получения кормовой добавки на основе антибиотика @ 290 | 1974 |
|
SU1047377A3 |
| Способ получения антибиотика | 1970 |
|
SU469265A3 |
Использование: биотехнология, ветеринария. Сущность: культивируют не менее 2-х дней один из штаммов микроорганизма Streptomyces thermoarchaensis NCIB 12015, 12111, 12112, 12113 или 12114 в аэробных условиях при 20 - 50°С и рН 5,5 - 8,5. Из культуральной жидкости выделяют антибиотик формулы, приведенный в описании изобретения. При необходимости его очищают хроматографией. Целевой продукт обладает антигельминтозной активностью.
СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА формулы
заключающийся в том, что культивируют штамм микроорганизма Streptomyces thermoarchaensis N CIB 12015 или один из его мутантов Streptomyces thermoarchaensis N CIB 12111, Streptomyces thermoarchaensis N CIB 12112, Streptomyces thermoarchaensis N CIB 12113 или Streptomyces thermoarchaensis N CIB 12114 в аэробных условиях в присутствии усваиваемых источников углерода, азота и минеральных солей при 20 - 50oС и pH 5,5 - 8,5 в течение по меньшей мере двух дней, целевой продукт выделяют из культуральной жидкости и при необходимости получения его в чистом виде очищают хроматографией.
Авторы
Даты
1995-02-27—Публикация
1990-02-26—Подача