Изобретение относится к улучшению выделения драгоценных металлов, таких как золото и серебро, в частности к выделению золота из его водных цианидных растворов. Выделение достигается контактированием водного цианидного раствора, содержащего драгоценный металл, в частности золото с реактивом, содержащим гуанидиновую функциональную группу. Гуанидиновым реактивом экстрагируют золото из водного раствора, после чего золото отделяют из гуанидинового реактива и затем выделяют обычными методами.
Способ изобретения типа жидкость жидкость представляет собой жидкостной ионообменный процесс, в котором нерастворимое в воде производное гуанидина растворяют в несмешивающемся с водой жидком углеводородном растворителе, полученный раствор контактируют с металлсодержащей водной фазой с экстрагированием части содержащегося металла в органическую фазу. Затем фазы разделяют и содержащийся металл извлекают из органической фазы с помощью водной извлекающей среды.
Широкий спектр по существу несмешивающихся с водой жидких углеводородных растворителей может быть использован в способе извлечения металла, в том числе алифатические ароматические углеводороды, такие как керосин, бензол, толуол, ксилол и т.п. Выбор несмешивающегося с водой жидкого углеводородного растворителя или смесей растворителей для конкретного промышленного процесса будет зависеть от ряда факторов, включая конструкцию установки для экстракции растворителем (например, сочетание смесителя-отстойника, экстракторы Подбельняка и т. д. ), количеств извлекаемого металла и т.п. Предлагаемый способ находит особое применение в извлечении экстракцией драгоценных металлов, таких как золото и/или серебро. К рекомендуемым для применения в способе извлечения благородного металла относятся алифатические и ароматические углеводороды с температурой вспышки 150о F (66оС) и выше и растворимостью в воде менее 0,1 мас. Растворители химически инертны. К представительным промышленным растворителям относится ионообменный растворитель Шеврон (производства Стандарт Ойл, шт. Калифорния), температура вспышки 195o F (91оС). Эскед 100 и 110 (производства Эксон-Юэроп, температура вспышки 180 oF (82оС), Норпар 12 (производства Эксон-ЮСЭ1, температура вспышки 160 Fo (71оС), Коноко-С1214 (производства Коноко, температура вспышки 160oF (71оС), Ароматик 150 (ароматический керосин производства Эксон-ЮСЭЙ, температура вспышки 150oF (66оС) и различные другие сорта керосина и нефтяные фракции производства других нефтяных компаний. В способе настоящего изобретения растворы органического растворителя содержат 0,005-20 мас. производного гуанидина и 0,01-1 мас. производного. Кроме того объемные отношения органической к водной фазе меняются в широких пределах, поскольку контактирование любого количества раствора гуанидина с содержащей металл водной фазой будет приводить к экстрагированию каких-то количеств металла в органическую фазу. Однако в промышленных масштабах рекомендуются отношения в интервале 50:1 1: 50. В смесителе желательно установить эффективное O/B отношение около 1:1 путем рециркуляции одного из потоков. На практике экстракцию и извлечение обычно проводят при комнатной температуре и нормальном давлении, хотя также применимы и более высокие и/или более низкие температуры и/или давления. Наиболее предпочтительно весь процесс осуществлять непрерывно с рециркулированием подвергшегося извлечению органического растворителя на контактирование с дополнительными количествами, содержащими драгоценный металл растворами цианида.
В способе типа жидкость жидкость гуанидиновый реагент должен быть растворим в органическом несмешивающемся с водой органическом растворителе в пределах 0,005 мас. или быть способным растворяться в таких количествах с помощью модифицирующих растворимость веществ. Такие модификаторы растворимости включают длинноцепные алифатические С6-С20-спирты, такие как н-гексанол, и н-2-этилгексанол, изодеканол, додеканол, тридеканол, гексадеканол и октадеканол, длинноцепные алкилфенолы, такие как гептилфенол, октилфенол, нонилфенол и додецилфенол, фосфорорганические соединения, такие как три-(низкий)-С4-С8-алкилфосфаты, в особенности трибутилфосфат и три-(2-этил-гексил)фосфат.
Извлечение драгоценных металлов из их водных растворов зависит от многих факторов, в том числе концентрации иона металла конкретного присутствующего аниона и рН водного раствора, а также от концентрации используемого в органической фазе конкретного гуанидина. Для каждого водного раствора металла и раствора-реагента гуанидина будет какой-то предпочтительный или оптимальный набор условий извлечения, и специалист на основе приведенной здесь информации, в особенности нижеследующих примеров, способен с привлечением небольшого числа пробных опытов определить оптимальные условия для рассматриваемой конкретной системы. Это в равной степени справедливо и для операций по извлечению из органической фазы. При этом имеется в виду, что по меньшей мере часть содержащегося в органической фазе металла переносится в водную извлекающую среду. Содержащиеся в водной извлекающей среде металлы затем выделяются из среды желательно обычными методами, предпочтительно электролизом. Отношения органической содержащей металл фазы к водной извлекающей фазе могут также меняться в широких пределах. Однако общая цель процесса заключается в получении содержащего металл извлекающего раствора известных состава и концентрации, пригодного для выделения металла обычными методами, например электролизом. Обычно металл присутствует в более высоких концентрациях в водной извлекающей среде по сравнению в исходным содержащим металл раствором. В этой связи исходные водные содержащие металл растворы содержат 1-5 ч/млн золота, 1-2 ч/млн серебра и 5-10 ч/млн меди плюс следы других металлов. Полученный кучным выщелачиванием раствор в среднем содержит 0,5-2 ч/млн золота, 0,5-2 ч/млн серебра и 5-10 ч/млн меди плюс другие металлы. Концентрация золота в извлекающих водных растворах, из которых выделяют золото, будет 50-1000 ч/млн. Концентрация, в основном, будет зависеть от применяемых извлекающих растворов и их эффективности. На стадии извлечения из органической фазы отношения содержащей металл органической фазы к водной извлекающей среде будет в интервале 1:1 20:1. Водные извлекающие растворы являются основными извлекающими растворами с рН более 11. В качестве извлекающего реагента рекомендуется применять щелочной раствор гидроокиси натрия, который может содержать цианид-анионы, имеет рН выше 11, обычно 12 или выше, по меньшей мере 13. Могут также применяться растворы гидроокиси калия или кальция. После выделения обычными методами металла из водного извлекающего раствора водный щелочной раствор рециркулируют.
Рекомендуемые производные гуанидина, применимые в системе типа жидкость жидкость, отвечают формуле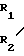 N
N 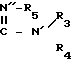 где R группы (R1-R5) по отдельности выбирают из группы, включающей водород и углеводородные группы с вплоть до 25 атомов углерода (1-25), при этом не более одной R-группы представлено водородом, общее число атомов углерода в R-группах равно по меньшей мере 16, по меньшей мере одна из углеводородных групп имеет 6 атомов углерода.
где R группы (R1-R5) по отдельности выбирают из группы, включающей водород и углеводородные группы с вплоть до 25 атомов углерода (1-25), при этом не более одной R-группы представлено водородом, общее число атомов углерода в R-группах равно по меньшей мере 16, по меньшей мере одна из углеводородных групп имеет 6 атомов углерода.
Применяемые в процессе экстракции типа жидкость жидкость нерастворимые в воде производные гуанидина растворимы в несмешивающихся с водой углеводородных растворителях, в которых также растворимы и соли драгоценных в пределах 0,005% Применяемые в процессе экстракции соединения также имеют значения рН в воде более 12, предпочтительно более 13.
В процессе экстракции типа жидкость твердое вещество в ионообменную смолу вводят гуанидиновую функциональность химической реакцией с производными гуанидина.
Вышеприведенное описание касалось систем экстракции типа жидкость жидкость. Могут применяться и системы типа жидкость твердое вещество, в которых гуанидиновый реагент вводится в ионообменную смолу путем химического связывания гуанидиновой функциональности со скелетом смолы. В этой связи термин экстракция означает в применяемом здесь значении как включающий как жидкие, так и твердые средства селективного удаления или иначе отделения соединений драгоценного металла. Если для обработки или контактирования содержащего золото водного раствора применяют ионообменную смолу, содержащую гуанидиновую функциональность, то такая смола должна быть нерастворима в воде. При контактировании водного раствора цианида, содержащего драгоценные металлы, драгоценные металлы селективно абсорбируются гуанидиновым реагентом на ионообменной смоле. Затем соединения металла элюируются с ионообменной смолы путем контактирования с раствором гидроокиси натрия, упомянутого ранее в качестве извлекающего раствора. Технология, применяемая в производстве нераствоpимых в воде ионообменных смол, используемых в предлагаемом способе, хорошо известна специалистам, особенно специалистам в области полимеризации мономеров с целью получения полимерных композиций, применимых в качестве ионообменных смол. В настоящем изобретении рекомендуются хлорметилированные полистирол-дивинилбензольные смолы, которые в химической реакции с соответствующим соединением образуют гуанидиновую функциональность, содержащуюся на ионообменной смоле. Такие смолы с различным содержанием дивинилбензола (ДВБ) хорошо известны специалистам. Могут использоваться смолы, содержащие до 25% ДВБ. Однако рекомендуются смолы с содержанием ДВБ не более 13-15% Также желательно, чтобы содержание ДВБ было по меньшей мере 3-4% наиболее предпочтительно 8-10%
Хотя рекомендованы полистирольные смолы, но могут быть также использованы ионообменные смолы с другой основой, матрицей или скелетом. Могут быть использованы любые приемлемые скелеты или матрицы, способные нести гуанидиновую функциональность в качестве активной группы. Рекомендуется, чтобы смолы несли только гуанидиновую функциональность, поскольку другие группы могут повлиять на улучшенную работу реагентов. К другим смолистым основам или матрицам, которые могут быть использованы, относятся мочевино-формальдегидные и меламин-формальдегидные смолы.
Размер частиц ионообменной смолы может меняться в широких пределах при условии, что частицы достаточно мелки, чтобы отвечать требованиям кинетики адсорбции и элюирования, в то же время достаточно крупны, чтобы раствор протекал через слой смолы без связывания и создания избыточного давления: можно было осуществлять удобный отсев смолы от раствора. Рекомендуется смола размером 6-12 меш. Количество связанного с ионообменной смолой гуанидина может меняться в широких пределах. Оно определяется объемными характеристиками слоя ионообменной нерастворимой в воде смолы. Обычно скорость потока через слой ионообменной смолы будет такой, при которой обеспечивается эффективная абсорбция на ионообменной нерастворимой в воде смоле.
После абсорбции ионообменной смолой, содержащей гуанидиновый реагент, соединений драгоценного металла водный раствор цианида отделяют от ионообменной смолы и абсорбированные соединения драгоценного металла элюируют с ионообменной смолы. Для элюирования приемлемы те же водные отделяющие растворы, что и в случае процесса экстракции типа жидкость жидкость. Наиболее эффективным элюентом является водный раствор гидроокиси натрия с рН выше 11, более желательно выше 12 и предпочтительно по меньшей мере 13.
П р и м е р 1. Получение ди-, три- и тетраалкилгуанидинов.
А. П, П-Бис (2-этилгексил)-N',N''-дициклогексилгуанидин.
Смесь 41,3 г (0,2 моля) дициклогексил карбодиимида, 72,4 г (0,3 моля) бис (2-этилгексил) амина и 200 мл трет-бутанола кипятят 7 ч, трет-бутанол отгоняют при атмосферном давлении, а остаток отдувают при 180оС и 0,08-0,09 мм Нg. Остаток весом 60,8 г по данным ЯМР имеет чистоту 90% содержит следы амина и около 5% дициклогексилкарбодиимида.
В. Аналогичным образом получены другие дициклогексилгуанидины путем замены бис (2-этилгексил)амина другими первичными и вторичными аминами. Использованием ди-н-бутиламина получен соответствующий ди-н-бутилдициклогексилгуанидин, использованием 2-этилгексиламина получают 2-этилгексилдицик- логексилгуанидин и изотридециламин дает изотридецилдициклогексилгуанидин.
C. N,N'-Бисизотридецилгуанидин.
В колбу на 2 л загружают 60,6 г (0,657 моля) бромистого циана и 750 мл гептана, после чего в течение 32 мин прибавляют 524,6 г (2,63 моля) тридециламина (смесь изомеров), поддерживаемая охлаждением температура в пределах 25-30оС. Затем реакционную смесь кипятят около суток. Охлажденную реакционную смесь разбавляют этиловым эфиром и трижды промывают 5%-ным NaOH. Содержащую продукт фазу сушат и отдувкой растворителя получают 568,7 г остатка. Полученный остаток отдувают в роторном испарителе при 0,05 мм Hg до 120оС и получают 270,4 г продукта, содержащего 81-89% гуанидина и 11% исходного амина.
П р и м е р 2. Получение N-метил- и N,N-диметилгуанидиновых смол, A-N-метил- и N,N-диметилгуанидиновой смолы.
(1) Получение смолы к H2NCH2-функциональностью дивинилбензола (60 г) в 1,2-дихлорэтане (180 мл) и безводного четыреххлористого олова (3 мм) медленно прибавляют N-хлорметилфальимид (40 г) в течение 5 ч. Смесь выдерживают при той же температуре 4 ч. После охлаждения до комнатной температуры шарики отфильтровывают, промывают 1,2-дихлорэтаном и затем метанолом. ИК-спектр показал введение в шарики имидной функциональности.
Затем шарики (58 г) гидролизуют в присутствии гидразина (21 мл) и гидроокиси натрия (4 г) в этаноле (180 мл). Смесь кипятят и реакцию контролируют до момента исчезновения в ИК-спектре полосы, характерной для имида. По данным ИК шарики имеют H2N-функциональность.
(2) Получение смолы с МеNH-(C-NH)-HCH2 функциональностью.
Полученные выше шарики (8 г) контактируют с раствором солянокислой кислоты с превращением H2N-групп в НCl H2N-группы. Отфильтрованные шарики обрабатывают метилцианамидом (100 ммолей получены из бромистого циана и метиламина в эфире при 0оС) в кипящем бутаноле в течение 12 ч. Затем шарики отфильтровывают и последовательно промывают раствором NaOH, водой, метанолом, эфиром и сушат в вакууме. ИК-спектр смолы показал наличие в ней гуанидиновой функциональности.
Вышеприведенная реакция повторена с заменой метилцианамида N,N-диметилцианамидом и получением N,N-диметилцианидиновой смолы.
В. N,N,N',N''-тетраметилгуанидиновая смола.
(1) Хлорметилирование макропористых шариков из полистирол-дивинилбензола.
К диметоксиэтану при 15-20оС медленно прибавляют сульфурилхлорид (54 г) и к полученной смеси добавляют полистиролдивинилбензольные шарики (40 г). После трехчасового перемешивания добавляют четереххлористое олово (4 г) и смесь кипятят (примерно 45оС) 7 ч. Шарики отделяют и промывают тетрагидрофураном. Элементарным анализом установлено присутствие 8% хлорида.
(2) Введение N,N,N',N'-тетраметилгуанидина в хлорметилированные шарики.
Хлорметилированные шарики (20 г) смешивают 100 ммолями N,N,N',N'-тетраметилгуанидина в толуоле (200 мл) и тетрагидрофуране (200 мл) и полученную смесь кипятят 2 дня. Затем шарики отфильтровывают, промывают водной щелочью, этанолом и эфиром, после чего сушат на воздухе.
Продукты примера 1 затем испытывают на экстрагирование золота построением изотерм экстракции МакКейба-Тиле с целью показать улучшенную селективность более высоко углеводородзамещенных гуанидинов (тетра- и пентазамещенные). В данных испытаниях использованы следующие экспериментальные методики.
П р и м е р 3. 1. Получение экстракционных растворов и водных исходных растворов.
В данных процессах экстракции в качестве растворителя применяют либо Ароматик 150-ароматический керосин, либо Эскед-110-алифатический керосин. В качестве экстрагента используют бис, трис- или тетраалкилгуанидины в концентрации 10 мМ в растворителе. Органический растворитель в качестве сорастворителя включает 50 г/л тридеканола.
Каждый исходный раствор содержит 17 л NaCN, рН 10,8 около 50 мг/л Fe и Au, Ag, Cu и Zn в концентрациях, указанных в таблицах.
2. Методика опытов с изотермами экстракции МакКейба-Тиле (таблицы 1-3).
Органический экстракционный раствор и водный исходный раствор в отношениях (об/об) органический водный растворы 2/1, 1/1 и 1/2 помещают в делительную воронку и контактируют 10 мин.
В каждом испытании фазы разделяют. Каждую фазу фильтруют и собирают. Водную фазу анализируют на концентрацию металла с помощью атомной абсорбционной спектроскопии (ААС), также как и исходный раствор. Значения концентраций металла в органических растворах после контактирования подсчитывают на основании данных ААС для водных растворов. В отдельных опытах содержащую металл органическую фазу анализируют с помощью ААС и полученные данные используют для контроля данных ААС для водных растворов.
3. Методика экстракции и опыты по выявлению селективности (таблица 4).
В делительную воронку помещают органический экстракционный раствор (30 мл) и водный исходный раствор (30мл) и контактируют 10 мин. Затем фазы разделяют, каждую фазу фильтруют и собирают. В одну фазу анализируют на концентрацию металла с помощью атомной абсорбционной спектроскопии (ААС) так же, как и исходный раствор. Значения концентрации металла в органических растворах после контактирования рассчитывают на основании данных ААС для водных образцов.
Т а б л и ц а 1
Изотерма экстракции МаККЕЙВА-ТИЛЕ
Бис-(изотридецил)гуанидин
Экстракционный раствор: 10 мМ гуанидина, 50 г/л тридеканона в керосине Эскед 110
Исходный раствор, мг/л: Au 14,7; Ag 52,1; Cu 53,9; Zn 56,7.
Концентрация металла в органической фазе после контактирования
O/B Au Ag Cu Zn
2/1 6,3 21,4 16,5 27,8
1/1 2,3 35,4 20,9 54,1
1/2 23,2 51,2 20,6 101
Т а б л и ц а 1А
Экстракция и селективное действие бис(изотридецил)гуанидина
(O/B 1/1)
Экстракционный раствор: 10 мМ гуанидина, 50 г/л тридеканола в керосине Эскед 110
Отношение Au в растворе/металл в растворе
Раствор, экстрагированного
Au Ag Cu Zn
Исходный
раствор 0,282 0,273 0,259
Раствор
после контак-
тирования 83,7 0,347 0,588 0,227
Т а б л и ц а 2
Изотерма экстракции МаККЕЙБА-ТИЛЕ
Бис(циклогексил)изотридецилгуанидин
Экстракционный раствор: 10 мМ гуанидина, 50 г/л тридеканола в керосине Эскед 110
Исходный раствор, мг/л: Au 14,8; Ag 52,7; Cu 52,7; Zn 55,7
Концентрация металла в органической фазе после контактирования, мг/л:
O/B Au Ag Cu Zn
2/1 7,8 17,5 13,8 27,4
1/1 13,8 29,7 14,7 54,4
1/2 26,2 43,6 18,2 106
Т а б л и ц а 2А
Экстракция и селективное действие бис(циклогексил)изотридецилгуанидина (O/B1/1)
Экстракционный раствор: 10 мМ гуанидина, 50 г/л тридеканола в керосине Эскед 110
Раствор, экстрагирования
Au Ag Cu Zn
Исходный
раствор 0,281 0,281 0,266
Раствор после
контакти-
рования 93,2 0,465 0,939 0,254
Т а б л и ц а 3
Изотерма экстракции МаККЕЙБА-ТИЛЕ
Бис(циклогексил)-бис(2-этилгексил)гу-анидин
Экстракционный раствор: 10 мМ гуанидина, 50 г/л тридеканола в керосине Ароматик 150
Исходный раствор, мг/л: Au 16,9; Ag 28,8; Cu 28,7; Zn 28,9.
Концентрация металла в органической фазе после контактирования, мг/л:
O/B Au Ag Cu Zn
2/1 7,8 7,0 0,01 12,8
1/1 14,9 11,2 0,02 9,3
1/2 27,2 16,2 0,04 10,0
Т а б л и ц а 3А
Изотерма экстракции МаККЕЙБА-ТИЛЕ
Бис(циклогексил)-бис(2-этилгексил)гу-анидин
Экстракционный раствор: 10 мМ гуанидина, 50 г/л тридеканола в керосине Ароматик 150
Раствор, экстрагирования
Au Ag Cu Zn
Исходный
раствор 0,587 0,589 0,885
Органичес-
кий раствор
после контак-
тирования
88,2 1,33 745 1,61
Т а б л и ц а 4
Экстракция и селективное действие различных трис- и тетраалкилгуанидинов
Экстракционные растворы: 10 мМ гуанидина, 50 г/л тридеканола в керосине Эскед 110
Исходный раствор, мг/л: Au 15,1; Ag 51,5; Cu 53,1; Zn 52,7
Отношение экстра. A/экстрагированный металл экстрагирования экстрагирования
Au Ag Cu Zn
Бис(циклогексил)-
Бис(Н-бутил)гуа-
нидин 82,8 1,15 1,25 0,424
Бис(циклогексил)-
н-октил-гуанидин 97,4 0,383 0,662 0,282
(Этилгексил)-гуа-
нидин 95,4 0,463 0,873 0,277
Отношение к дру-
гим металлам
в исходном
растворе 0,293 0,294 0,287
Продукт примера 2 метилзамещеные гуанидиновые смолы также испытаны на экстрагирование и извлечение золота. В таких смолах гуанидиновые реагенты одним из атомов азота уже связаны со смолой, вследствие чего триметил- и тетраметилзамещенные смолы являются высокозамещенными смолами.
П р и м е р 4. Экстракция и извлечение золота.
А. N-Метилгуанидиновая смола
Абсорбция. N-Метилгуанидиновую смолу контактируют в различных количествах с порциями по 10 мл водного раствора, содержащего 14,5 ч/млн золота и 500 ч/млн цианида (рН около 10). Получены водные рафинаты со следующими концентрациями золота.
Масса смолы, мг(Au) в рафинате, ч/млн: 10 1,19 24 0,1 66 0,1 79 0,1
Извлечение. 150 мг смолы нагружают контактированием с 50 мл водного раствора, содержащего 120 ч/млн золота и 500 ч/млн цианида (рН 9,8) с получением 166 мг нагруженной смолы и рафината, содержащего 1,27 ч/млн золота. Нагруженную смолу затем обрабатывают при 10 мл водного раствора, содержащего 1% NaOH и 0,5% NaCN при различных отношениях смола/водный раствор. Получены водные растворы со следующими концентрациями золота
Масса нагружен- (Au) в водном
ной смолы, мг: растворе, ч/млн: 6,2 6,7 12 13,7 19 25,5 25 27,6
В. N,N-Диметилгуанидиновая смола.
Абсорбция. Различные количества смолы контактируют с порциями по 10 мл водного раствора, содержащего 14,5 ч/млн золота и 500 ч/млн цианида (рН около 10). Получены рафинаты со следующими концентрациями золота.
Масса смолы, мг: (Au) в рафинате, ч/млн: 14 0,12 30 0,1 70 0,1 96 0,1
Извлечение. 150 мг смолы нагружают контактированием с 50 мл водного раствора, содержащего 120 ч/млн и 500 ч/млн цианида (рН 9,8), с получением 200 мг нагруженной смолы и рафината, содержащего 1,19 ч/млн золота. Нагруженную смолу обрабатывают водным раствором, содержащим 1% NaOH и 0,5 NaCN, при различных отношениях смола/водный раствор. Получены водные растворы со следующими концентрациями золота.
Масса нагруженной смолы, мг: (Au) в водном растворе, ч/млн:
7,5 7,25
15 13,2
29 24,2
63 38,8
С. Тетраметилгуанидиновая смола.
Абсорбция. Различные количества смолы контактируют с порциями по 10 мл водного раствора, содержащего 135,5 ч/млн золота и 500 ч/млн цианида (рН 10). Концентрация золота, оставшаяся в водных рафинатах, следующая:
Масса смолы, мг: (Au) в рафинате, ч/млн: 32 113 75 77 174 36 267 26,5
Извлечение. Смолу (1 г) нагружают контактированием с 50 мл водного раствора, содержащего 1000 ч/млн золота и 500 ч/млн цианида (рН 11,9), с получением 1,4 г нагруженной смолы и рафината, содержащего 828 ч/млн золота. Нагруженную смолу обрабатывают 10 мл водного раствора, содержащего 1% NaOH и 0,5% NaCN, при различных отношениях смола-водный раствор. Полученные водные растворы содержат золото в следующих концентрациях.
Масса нагружен- (Au) в водном
ной смолы, мг: растворе, ч/млн: 49 24,8 78 36,6 160 66,6
Вышеприведенные опыты показывают, что высокозамещенные гуанидиновые продукты (тетра- или пента(углеводород)замещенные несмолистые гуанидиновые производные реагенты) обеспечивают улучшенную селективность по отношению к золоту по сравнению с другими металлами, присутствующими в водном щелочном растворе цианида. В продуктах со смолистой основой или скелетом один из N-атомов замещен смолистой матрицей или скелетом, т.е. три- или тетра(углеводород)замещенный смолистый реагент соответствует тетра- или пента(углеводород)замещенному несмолистому продукту с обеспечением улучшенной селективности. Данные примера 4 показывают также, что метилзамещенные смолистые гуанидиновые реагенты также пригодны для экстракции золота из водных щелочных растворов цианида, и совсем необязательно, чтобы смолистый реагент, применяемый в системе типа твердое вещество жидкость, содержал углеводородные группы с по меньшей мере 2 атомами углеводорода в любом углеводородзамещенном продукте, хотя присутствие высших углеводородных замещающих групп может оказаться необходимым в системах типа жидкость-жидкость для обеспечения необходимой растворимости в подобных системах типа жидкость-жидкость.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ извлечения благородных металлов из щелочных цианистых растворов | 1987 |
|
SU1831508A3 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ТОКСИЧНЫХ ЦИАНИДОВ И ТЯЖЕЛЫХ МЕТАЛЛОВ ИЗ ЩЕЛОЧНЫХ РАСТВОРОВ | 1994 |
|
RU2131284C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ДРАГОЦЕННОГО МЕТАЛЛА ИЗ ВОДНЫХ ЩЕЛОЧНЫХ РАСТВОРОВ ЦИАНИДА | 1993 |
|
RU2114924C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЗОЛОТА ИЗ ЩЕЛОЧНЫХ ЦИАНИДНЫХ РАСТВОРОВ | 2009 |
|
RU2412261C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЗОЛОТА ИЗ ЩЕЛОЧНЫХ ЦИАНИДНЫХ РАСТВОРОВ | 2014 |
|
RU2557866C1 |
| ГРАНУЛЫ МОЛЕКУЛЯРНО ИМПРИНТИРОВАННЫХ ПОЛИМЕРОВ ДЛЯ ЭКСТРАКЦИИ МЕТАЛЛОВ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2719736C2 |
| СПОСОБ ПЕРЕРАБОТКИ ОТХОДОВ, СОДЕРЖАЩИХ МЕДЬ, ЦИНК, СЕРЕБРО И ЗОЛОТО | 1996 |
|
RU2109076C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ МЕТАЛЛА | 1989 |
|
RU2091311C1 |
| ВОДНЫЙ РАСТВОР ДЛЯ ВЫЩЕЛАЧИВАНИЯ БЛАГОРОДНЫХ МЕТАЛЛОВ (ВАРИАНТЫ) | 1990 |
|
RU2102507C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ДРАГОЦЕННОГО МЕТАЛЛА ИЗ УГЛЕРОДИСТЫХ РУД | 1993 |
|
RU2108402C1 |
Изобретение относится к способам выделения драгоценных металлов и ионообменным смолам для их выделения. Способ выделения драгоценных металлов, таких как золото и серебро, заключается в контактировании с определенными гуанидиновыми реагентами. Гуанидиновые реагенты не только экстрагируют драгоценный металл, но также обеспечивают преимущества, заключающиеся в селективности по отношению к золоту по сравнению с другими металлами. Реагенты являются тетра- и пента(углеводород) замещенными несмолистыми гуанидиновыми реагентами и три- и тетра(углеводород) замещенными смолистыми гуанидиновыми реагентами. 2 с. и 13 з. п. ф-лы, 4 табл.
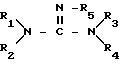
где R1 R5 выбирают из группы: H, ионообменный смолистый носитель или углеводородная группа с вплоть до 25 атомов углерода,
последующее отделение фазы производного гуанидина, содержащего драгоценный металл, и выделение драгоценного металла из указанной фазы щелочным раствором с рН выше 12, отличающийся тем, что в качестве гуанидинсодержащего реагента используют реагент, выбранный из группы: тетра- или пента(углеводород)замещенный несмолистый гуанидиновый реагент или три- или тетра(углеводород)замещенный смолистый гуанидиновый реагент, при этом если одна из R-групп от R1 до R5 является ионообменным смолистым носителем, то одна из оставшихся R-групп представляет алифатическую углеводородную группу с 1 25 атомами углерода и если она отлична от метилгруппы, то минимум три R-группы углеводородные, в случае, если одна из R-групп от R1 до R5 является несмолистым носителем, то не более одной R-группы представлено водородом, а остальные R-группы представлены алифатическими углеводородными группами с 1 25 атомами углерода при общем числе атомов углерода в группах R1 R5 не менее 16.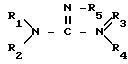
где одна из R-групп (R1 R5) представлена ионообменной смолой и по меньшей мере одна из оставшихся R-групп представлена алифатической углеводородной группой с 1 25 атомами углерода, и если она отлична от метила, тогда по меньшей мере три из R-групп представлены углеводородами и не более трех R-групп представлены метилами.
| Патент США N 4814007, кл | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
Авторы
Даты
1995-10-27—Публикация
1990-10-10—Подача