Изобретение относится к мономеру трет-бутил-L-тирозил-пептидогликана и его меченному 125I производному, к процессу их получения и применению новых соединений данного изобретения в фармацевтических препаратах; мономер трет-бути- локсикарбонил-L-тирозил-пептидогликана особенно показан для фармацевтических препаратов, обладающих иммуномодулирующей и противоопухолевой активностью, тогда как новое меченое изотопом 125I производное проявляет свойства связывания антител анти-PGM.
Известно, что мономер пептидогликана (PGM, G1cNAc-β -(1->>4)-MurNAc-L-Ala-D-i G1n-[(L)-мезо-A2-pm-(D)-амид-(L)-D-Ala-D-Ala] являющийся наименьшим повторяющимся пептидогликановым звеном стенок клеток Brevibacterium divaricatum, проявляет иммуномодулирующую, противоопухолевую и антиметастатическую активность [1]
Известно, что образование пептидной связи может быть достигнуто при условии, что аминокислота
сначала превращается в N-защищенную аминокислоту путем введения так называемых защитных групп;
активируется по карбоксигруппе;
проводится реакция с защищенной С-концевой аминокислотой, ди-, три- или полипептидами;
защитные группы полученных ди-, три- или полипептидов тщательно удаляются с помощью соответствующих реакций [2]
Далее в полуфункциональных молекулах весьма сложной структуры, такой как, например, мономер пептидогликана, состоящий из дисахарид пентапептидов (фрагменты сахара и пептида), гидроксильные группы на C1cNAC и Mur NAC (сахарный фрагмент молекулы) должны защищаться и по завершении реакции образования пептидной связи следует осуществить снятие защиты сахарного фрагмента.
Известно также, что традиционный метод включения тирозина в пептид или белок является "методом активного эфира", при котором Boc-L-Tyr-ONSu является ацилирующим компонентом (Assoian R.K. Anal. Biochem, 1980, 103, 70).
Все возрастающая потребность в новых веществах, потенциально обладающих иммуностимулирующим действием и возможной противоопухолевой активностью, привела к идее данного изобретения, относящегося к новому веществу мономеру трет-бутилоксикарбонил-L-тирозил-пепти-догликана (Boc-Tyr-PGM) и к его меченому 125I производному.
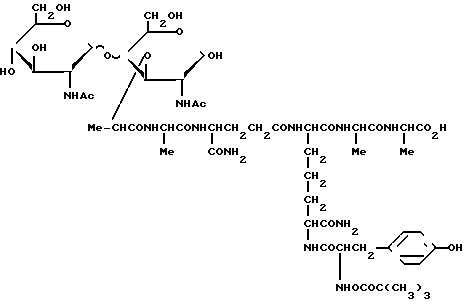 (I)
(I)
Новый мономер пептидогликана формулы (I) дает возможность предоставить соединение увеличенной липофильности, что сделает возможным более легкое проникновение вещества сквозь стенки клетки и продлевает время его нахождения в организме. Это достигается путем введения природной ароматической аминокислоты тирозина в молекулу PGM, посредством чего из дисахарид пентапептида получают дисахаридгексапептид (Boc-Tyr-PGM), который впоследствии подвергают мечению радиоактивным 125I, давая таким образом его производное
125I-Boc-Tyr-PGM (II)
В процессе получения нового производного мономера пептидогликана применяли известные методы химии пептидов и впервые синтез выполняли с помощью полностью незащищенной молекулы очень сложной структуры.
Процесс получения нового производного PGM по данному изобретению иллюстрируется следующей схемой реакции:
дисахар ид-пент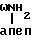 тид-СOOH+Boc-Tyr-ONSu
тид-СOOH+Boc-Tyr-ONSu 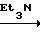 1
1
В соответствии с изобретением осуществляют региоселективную реакцию Boc-Tyr-ONSu с омега-аминогруппой мезо-диаминопимелиновой кислоты в молекуле PGM в присутствии триэтиламина, дающую новое производное дисахаридгексапептид, которое сначала выделяют с помощью гель-хроматографии на колонке "Сефадекс G-25" и хроматографии на колонке с силикагелем, после чего оно полностью очищается и адаптируется для биологических исследований с помощью гель-хроматографии на "Биогель Р-2".
Мечение Boc-Tyr-PGM радиоактивным иодом осуществляется с помощью стандартного Т-хлораминового метода [3]
После электрофильного замещения фенольного кольца в ортоположении по отношению к гидроксильной группе в тирозине получается меченая 125I молекула высокой специфической активности и достаточной радиохимической стабильности.
Процесс получения представлен следующей схемой: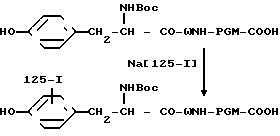

Согласно изобретению, синтез меченного радиоактивным иодом Boc-Tyr-PGM проводят с помощью стандартного Т-хлораминового метода с применение Na[125I] дающего иодированный продукт (II), который выделяют с помощью гель-хроматогорафии на колонке "Сефадекс G-25" и применяют при исследовании реакции связывания антиген-антитело.
Новое дисахарид-гексапептидное PGM-производное может использоваться в фармацевтических средствах, обладающих иммуномодулирующей и противоопухолевой активностью, тогда как новое меченое 125I производное может использоваться в фармацевтических препаратах, характеризуемых свойствами связывания антител анти-PGM.
П р и м е р 1. Мономер третбутилоксикарбонил-L-тирозил-пептидогликана (I).
Мономер пептидогликана (PGM, 100 мг, 0,1 ммоля) растворяли в сухом диметилформамиде (ДМФ, 2,6 мл) при добавлении триэтиламина (30 мкл). В охлажденный водой со льдом раствор добавляли небольшими порциями при перемешивании твердый Boc-Tyr-ONSu (56 г, 0,12 ммоля). Реакцию вели в течение 16 ч при комнатной температуре, после чего ДМФ выпаривали в вакууме, создаваемом механическим насосом. Густой сиропообразный остаток после выпаривания растворяли в воде, подкисляли твердой лимонной кислотой до рН 3, после чего его экстрагировали этилацетатом (3 х 10 мл). Водную часть концентрировали до 2 мл и загружали на колонку "Сефадекс G-25" (90 х 2,5 см) в воде. Фракции (3 мл) исследовали на поглощение при длине волны 230 нм, и те, что соответствовали соединению с большей молекулярной массой, объединяли и выпаривали. Полученный стекловидный остаток (110 мг) растворяли в смеси н-бутанола, этанола, NH3 (25% ) и воды в соотношении 5:3:2:2, после чего хроматографировали на колонке с силикагелем с тем же самым элюентом. Нейтрализация с помощью HOAc и выпаривание фракций давало продукт, который окончательно очищали с помощью гель-хроматографии на колонке "Биогель Р-2" (70 х 2,5 см) при элюировании водой. Наиболее мобильные фракции объединяли, концентрировали и лиофилизовали. Получалось 58 г (46%) чистого Boc-Tyr-PGM (I).
Результаты анализа аминокислот: G1oNH2 0,82; MurNH2 0,57; Ala 3; Glu 1; A2pm 0,98; Tyr 0,80.
1Н-ЯМР-спектр (D2O): 1,29 (c, Me C), 1,34-1,70 (м, частично перекрывается Me3C, 21 H, 3 x Me-Ala + лактоил-Me), 1,89 и 1,98 (2, sc 6H, 2 x NAc), 6,77 и 7,07 (2g, 2H каждый, 1Н,Н 8,55 Гц, С6Н4-).
Тонкослойная хроматография: н-бутанол-этанол-NH3 (25%) вода (5:3:2:2), детекция парами иода и пептидным реагентом, Rf=0,5.
П р и м е р 2. Мономер трет-бутилоксикарбонил-[125I]-L-тирозил-пептидогликана (II).
В раствор Boc-Tyr-PGM (5 мкг) в фосфатном буфере (25 мкл, 0,5-М, рН 7,5) добавляли Na[125I] (10 мкл, 3,7 х 10 Bq, 1 мCi) хлорамин Т (50 мкг) в фосфатном буфере (25 мкл, 0,25 М, рН 7,5) и через 45 с реакция останавливалась добавлением метабисульфита натрия (50 мкг) в 25 мкл воды. Реакционную смесь сразу же загружали в колонку "Сефадекс G-25" (30 х 1,5 см), которую предварительно промывали раствором человеческого альбумина и уравновешивали фосфатным буфером 0,025 М с рН 7,5, который использовали при элюировании. Фракции (2 мл) проверяли на радиоактивность, а те, что соответствовали Boc[125I] -L-Tyr-PGM, объединяли. Специфическая активность полученного производного (II): приблизительно 3,12 MBq/мкг (0,087 мCi/мкг).
П р и м е р 3. Иммуностимулирующая активность мономера трет-бутилоксикарбонил-L-тирозил-пептидогликана (Boc-Tyr-PGM).
Иммуностимулирующую активность Boc-Tyr-PGM испытывали на мышах, иммунизированных эритроцитами овец (красные кровяные тельца овец, SRBC).
Мышей (CBA или AKR), по пять в группе, иммунизировали внутрибрюшинно эритроцитами овец (1 х 108 SRBC) в растворе Хенкса. Днем позже (день иммунизации + 1) контрольной группе мышей назначали внутривенно только раствор Хенкса, тогда как подопытной группе мышей давали внутривенно 200 мкг Boc-Tyr-PGM в растворе Хенкса; в качестве положительного контроля использовали группу мышей, которой назначали внутривенно 200 мкл мономера пептидогликана (PGM) в растворе Хенкса. Через 4 дня (день иммунизации + 4) в селезенке методом Джерне определяли число антителаобразующих клеток (клетки, образующие бляшки PFC) (Jerne N.K. Nordin A.A. and Heury C. The agar plaque tecnique for recogniring antibody producing cells. in Cell Bound Antibodies, 1963, p. 109, Wistar Institute Press, Philadeephia).
Результаты испытаний перечислены в табл. 1.
Boc-Tyr-PGM продемонстрировал иммуностимулирующую (адъювантную) активность на обоих типах штаммов мышей, у которых было обнаружено увеличение числа PFC примерно на 50% по сравнению с контрольной группой. В обоих испытаниях эффективность Boc-Tyr-PGM была сравнима с эффектом положительного контроля, т.е. мономера пептидогликана.
П р и м е р 4. Противоопухолевая (антиметастатическая) активность мономера трет-бутилоксикарбонил-L-тирозил-пепти-догликана (Boc-Tyr-PGM).
Противоопухолевую активность Boc-Tyr-PGM исследовали на мышах, инокулированных меланомой В-16.
Мышам (С5 7 BL/6, самцы, возраст 4 мес), по 5 в группе, давали каждой внутривенно по 1 х 105 клеток меланомы В-16 в день 0.
Одну группу мышей выбрали в качестве контрольной и в дальнейшем не лечили никаким способом. Мышам экспериментальных групп вводили каждой внутривенно 1 мг Boc-Tyr-PGM в соответствии со следующим протоколом:
1-я группа день 3;
2-я группа день 7;
3-я группа дни 3 и 7 (всего 2 мг Boc-Tyr-PGM).
В качестве положительного контроля были выбраны три группы мышей, получавшие PGM внутривенно (PL1VA) в соответствии с тем же протоколом.
Макроскопически определяемые метастазы в легких подсчитывали после умерщвления на день 23. Результаты представлены в табл. 2.
Лечение Boc-Tyr-PGM давало антиметастатический эффект, выражающийся в уменьшении числа метастаз во всех группах мышей, которых лечили (степень ингибирования составляла 37,8-43,6%).
У мышей, которых лечили в разные периоды времени (в день 3 или 7) и с различной общей дозой лекарства (1 мг в день 3 или 7 или всего 2 мг в день 3 и 7), никакой существенной разницы в степени ингибирования не наблюдалось.
Эффект Boc-Tyr-PGM сравним с эффектом PGM (PL1VA), который использовали в качестве положительного контроля.

Использование: в медицине в качестве соединений, обладающих иммуностимулирующей и противоопухолевой активностью. Сущность изобретения: мономер трет-бутилоксикарбонил-L-тирозил-пептидогликан (Boc-Tyr-PGM) и его 125J меченое производное и способ их получения. Реагент 1: N-гидроксисукцинимидный эфир трет-бутилоксикарбонил-L-тирозина, реагент 2: мономер пептидогликана (PGI) конденсируют в присутствии триэтиламина, полученный Boc-Tyr-PGM отделяют с помощью гель-хроматографии на колонке "Сефадекс G-25" и последующей хроматографии на колонке с силикагелем и с "Биогель Р-2", полученный продукт обрабатывают Na 125J и хлорамином T, 125J Boc-Tyr-RGM отделяют на колонке "Сефадекс G-25", элюируя фосфатным буфером. Boc-Tyr-PGM - растворим в воде, непирогенен при применении на кроликах в дозе 0,3 мг/кг, нетоксичен ин витро для лимфоцитов и макрофагов (200 мкг/10 клеток). 2 с. и 1 з. п. ф-лы, 2 табл.
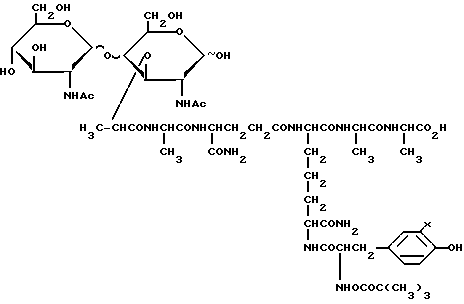
где X H,
и его 125J-меченое производное (X 125J).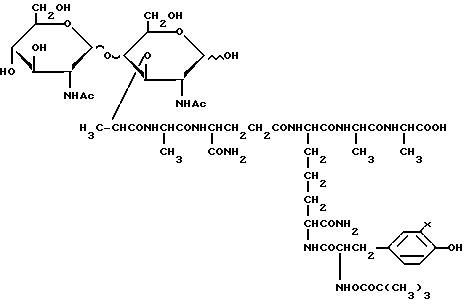
где X H или 125J,
отличающийся тем, что N-гидроксисукцинимидный эфир трет-бутилоксикарбонил-L-тирозина конденсируют в присутствии триэтиламина с незащищенным мономером пептидогликана формулы II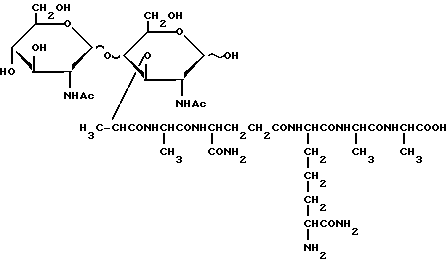
полученный мономер трет-бутилоксикарбонил-L-тирозил пептидогликана формулы I, где X H, отделяют с помощью гельхроматографии на колонке "Сефадекс G-25" и последующей хроматографии на колонке с силикагелем и на колонке с "Биогель P-2" и, в случае необходимости, полученный продукт обрабатывают Na125J и хлорамином T, процесс прерывают бисульфитом натрия, меченый продукт отделяют на колонке "Сефадекс G-25", элюируя фосфатным буфером.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Bolton a.e., B kh | |||
| Radioiodination Techniques, second Edition, p.109, Amserdam Int | |||
| plc | |||
| Endland. | |||
Авторы
Даты
1995-10-27—Публикация
1991-12-20—Подача