Изобретение относится к радиофармацевтическим продуктам. Более конкретно, изобретение относится к новому нитридному комплексу переходного металла, который может быть использован в качестве радиофармацевтического продукта, обладающего кардиотоническим тропизмом.
Из международной заявки WO-85/03063 известны нитридные комплексы технеция, получаемые в результате осуществления реакции замещения с соединением 99mТсNСl4, при этом указывается, что эти комплексы можно использовать в качестве радиофармацевтических продуктов.
Однако в этом документе не приводятся результаты, свидетельствующие о связывании этих комплексов в организме, и следовательно не говорится об их тропизме в отношении определенных органов и, в частности, сердца.
Среди радиофармацевтических продуктов, обладающих кардиотоническим тропизмом, известны комплексы технеция, которые содержат в качестве лиганда изонитрилы, замещенные простым эфиром, как это описано в заявке на Европейский патент ЕР-А-0233368 и диоксимные комплексы технеция, описанные в заявке на Европейский патент ЕР-A-0268801. Однако эти комплексы образуются из лигандов, которые трудно синтезируются.
Цель изобретения разработка радиофармацевтических продуктов, которые можно было бы использовать в качестве диагностических или лечебных продуктов, в частности, в качестве радиофармацевтических продуктов с кардиотоническим тропизмом, например, для сцинтиграфии миокарда.
Эта цель достигается с помощью нитридного комплекса переходного металла формулы:
/M ≡ N/L1L2,
в которой М означает Те99, Re186, Re188, а L1 и L2 остатки лигандов формулы: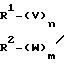 N C
N C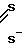
в которой V и W представляют собой О, S или Se, n и m равняются 0 или 1, а R1 и R2, которые могут иметь одинаковые или различные значения, представляют алкильный радикал с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, который может быть замещен низшей алкоксигруппой.
Радиофармацевтические продукты, включающие комплексы переходного металла в соответствии с вышеуказанной формулой, обладают кардиотоническим тропизмом, что делает их весьма полезными в качестве продуктов для диагностики или лечения сердечных заболеваний.
В комплексах по изобретению использование переходного металла, в частности, зависит от применения радиофармацевтического продукта.
Так, если предполагается использовать этот продукт для диагностических целей, применяется радиоактивный переходный металл с относительно коротким периодом полураспада, например, технеций 99m.
Если же этот радиофармацевтический продукт предполагается использовать для лечебных целей, применяется переходный металл, создающий эффективное излучение для лечения и имеющий более длительный период полураспада, такой как рений, например, Re-186 или Rе-188.
Нитридные комплексы технеция, используемые в настоящем изобретении, можно получить в соответствии со способом, предложенным Балдасом.
Однако предпочтение обычно отдается получению этого комплекса в соответствии с более простым способом, который легче осуществлять в больничной лаборатории и который позволяет получить высокий выход.
Этот способ включает следующие последовательные стадии:
1) взаимодействие окисленного соединения переходного металла с:
а) первым лигандом, выбираемым из группы, включающей замещенные или незамещенные, ароматические и низшие алифатические фосфины
б) вторым реагентом, выбираемым из нитридов аммония и щелочных металлов и азотистых лигандов, имеющих группу  N-N
N-N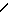 , в которой атомы азота присоединяются к атомам водорода и/или к одновалентным органическим группам через атом углерода, либо в которой один из атомов азота присоединяется к атому углерода, либо в которой один из атомов азота присоединяется к атому углерода двухвалентной органической группы через двойную связь, а другой атом азота присоединяется к атомам углерода и/или одновалентным органическим группам через атом углерода, и
, в которой атомы азота присоединяются к атомам водорода и/или к одновалентным органическим группам через атом углерода, либо в которой один из атомов азота присоединяется к атому углерода, либо в которой один из атомов азота присоединяется к атому углерода двухвалентной органической группы через двойную связь, а другой атом азота присоединяется к атомам углерода и/или одновалентным органическим группам через атом углерода, и
2) взаимодействие промежуточного соединения, полученного на первой стадии, с соединением формулы: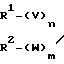 N C
N C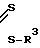 pH2O(X)
pH2O(X)
в которой R1, R2, V, W, n, m имеют указанные значения, R6представляет ион щелочного металла, Н+ или NH+4, а р равняется 0 или является целым числом от 1 до 5.
При выполнении этого способа с использованием технеция в качестве переходного металла окисленным соединением переходного металла может быть пертехнетат аммония или щелочного металла. В том случае, если переходным металлом является рений, можно использовать перренат аммония или щелочного металла.
Таким образом, на первой стадии этого способа получают нитридный комплекс технеция, который затем взаимодействует с соединением формулы (Х) с целью замены первого и второго лигандов этим соединением.
Для осуществления этой реакции можно в асептических условиях ввести первый лиганд, а именно нитрид аммония или щелочного металла, либо азотистый лиганд в сосуд, а затем добавить необходимое количество окисленного соединения переходного металла, например, пертехнетат технеция 99m, после доведения показателя рН до соответствующего значения путем добавления кислоты или основания.
Эту реакцию можно осуществлять при комнатной температуре или при повышенной температуре от 50 до 100оС. Температура и показатель рН, в частности, зависят от второго азотистого лиганда. Этот процесс обычно происходит при рН 2-7.
На первой стадии можно использовать первый и второй лиганды в виде спиртовых, гидроспиртовых или водных растворов и просто добавлять эти растворы к окисленному соединению переходного металла.
На второй стадии продукт, полученный в первой стадии, подвергают взаимодействию с соединением формулы (Х) в водном растворе обычно при показателе рН выше 7 и, например, в буфере из бикарбоната натрия-карбоната.
На второй стадии также можно использовать спиртовой или гидроспиртовой раствор соединения (Х).
Первый лиганд, который позволяет получить нитридный комплекс, представляет органический лиганд с атомом фосфора в качестве донора электронов, который выбирают из замещенных или незамещенных, алифатических и ароматических фосфинов.
Приемлемые фосфины могут иметь формулу
P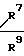 R8,
R8,
в которой R7, R8 и R9, которые могут иметь одинаковые или различные значения, представляют атом водорода, алкильный радикал, арильный радикал, алкоксильный радикал или алкильный или арильный радикал, замещенный группой, выбираемой из амино-, амидо-, циано- или сульфонатных радикалов.
Примерами фосфинов этого типа являются трифенилфосфин, трисульфированный трифенилфосфин, диэтилфенилфосфин, триэтилфосфин, триметилфосфин и трис(2-цианоэтил)-фосфин Р(CH2-CH2CN)3.
На первой стадии в качестве второго реагента можно использовать нитрид аммония или щелочного металла, например, нитрид натрия, или азотистый лиганд, имеющий группу  N-N
N-N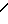 такой как гидразин и его производные.
такой как гидразин и его производные.
Можно применять различные азотистые лиганды этого типа. Обычно в качестве азотистого лиганда предпочтительно используется дитиокарбазиновая кислота или ее производное.
Таким образом, вторым азотистым лигандом может быть дитиокарбазиновая кислота или ее производное формулы:
H2N-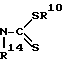
в которой R10 представляет атом водорода, алкильный радикал или арильный радикал, а R14 представляет атом водорода, алкильный радикал, арильный радикал, алкоксильный радикал, алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильного, карбоксильного, амино-, амидо- и меркапто-радикалов, и амино-радикалы, замещенные по крайней мере одним алкильным радикалом.
Им также может быть продукт конденсации, полученный в результате взаимодействия дитиокарбазиновой кислоты с кетоном или алифатическим альдегидом формулы R15-СО-R16. В этом случае он имеет формулу: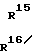 C= N-
C= N-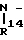 C
C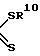
в которой R10 представляет атом водорода, алкильный радикал или арильный радикал; R14 представляет атом водорода, алкильный радикал, арильный радикал, алкоксильнрый радикал, алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильных, карбоксильных, амино-, амидо- и меркапто-радикалов, или арильный радикал, замещенный по крайней мере одной группой, выбираемой из атомов галогенов, алкоксильных, гидроксильных, амино- и меркапто-радикалов, или аминорадикал, замещенный по крайней мере одним алкильным радикалом; а R15 и R16, которые могут иметь одинаковые или различные значения, представляют атом водорода, алкильный радикал или алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильных карбоксильных, амино-, амидо- и меркапто-радикалов.
Производным дитиокарбазиновой кислоты, используемым в качестве второго лиганда, также может быть продукт конденсации дитиокарбазиновой кислоты с кетоном или ароматическим альдегидом. В этом случае это производное имеет формулу: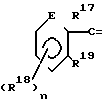 N
N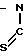
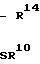
в которой R10 представляет атомы водорода, алкильный радикал или арильный радикал; R14 представляет атом водорода, алкильный радикал, арильный радикал, алкоксильный радикал, алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильных, карбоксильных, амино-, амидо- и меркапто-радикалов, или арильный радикал, замещенный по крайней мере одной группой, выбираемой из атомов галогенов, алкоксильных, гидроксильных, амино- и меркапто-радикалов, и аминорадикал, замещенный по крайней мере одним алкильным радикалом; R17представляет атом водорода, алкильный радикал, алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильных, карбоксильных, амино-, амидо- и меркапто-радикалов; R18 представляет атом водорода, атом галогена, алкоксильный радикал, аминорадикал или аминорадикал, замещенный по крайней мере одной алкильной группой, R19представляет атом водорода, гидроксильный радикал или меркапто-радикал, Е представляет атом углерода или атом азота, а n является целым числом от 1 до 4, либо в которой n равняется 2, а два элемента R18 расположены рядом друг с другом, образуя ароматический цикл.
В качестве второго лиганда также можно использовать продукт, полученный путем конденсации дитиокарбазиновой кислоты с кетоном, включающим гетероцикл с пятью звеньями. В этом случае второй лиганд имеет формулу: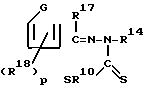
в которой R10 представляет атом водорода, алкильный радикал или арильный радикал; R14 представляет атом водорода, алкильный радикал, арильный радикал, алкоксильный радикал, алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильных карбоксильных, амино-, амидо- и меркапто-радикалов, или арильный радикал, замещенный по крайней мере одной группой, выбираемой из атомов галогенов и алкоксильных, гидроксильных, амино- и меркапто-радикалов, и аминорадикал, замещенный по крайней мере одним алкильным радикалом; R17представляет атом водорода, алкильный радикал, алкильный радикал, замещенный по крайней мере одной группой, выбираемой из гидроксильных, карбоксильных, амино-, амидо- и меркапто-радикалов, R18 представляет атом водорода, атом галогена, алкоксильный радикал, аминорадикал или аминорадикал, замещенный по крайней мере одной алкильной группой, G представляет S или 0, а р равняется 1, 2 или 3.
Примеры вторых азотистых лигандов, которые могут использоваться при осуществлении изобретения, включают S-метил-бета-N(2-гидроксифенил)метилендитиокарба- зат, S-метилдитиокарбазат, S-метил-N-метил-дитиокарбазат, альфа-N-метил-S-метил-бета-N-пиридилметилендитиокарбазат и альфа-N-метил-S-метил-бета-N(2-гидроксифенил)метилендитиокарбазат.
Если радиофармацевтический продукт в соответствии с изобретением предполагается использовать для диагностических целей, его необходимо получить в момент применения.
Радиофармацевтические продукты в соответствии с изобретением, в частности, можно использовать для сцинтиграфии миокарда.
В этом случае нитридный комплекс технеция, полученный при осуществлении способа по изобретению, инъецируют больному, подлежащему обследованию, после чего производят сцинтиграфию сердца.
При инъецировании этого продукта количества различных лигандов должны соответствовать стехиометрии получаемых комплексов. Конечное количество инъецируемого продукта, в частности, зависит от используемых лигандов и их токсичности.
Обычно удовлетворительные результаты достигаются в результате использования общих количеств лигандов от 0,05 до 0,40 мг/кг массы тела.
Общее количество переходного металла, например, доза технеция, обычно составляет от 185 до 740 Mbq (5-20 милликюри).
После введения нитридного комплекса переходного металла можно производить удовлетворительное обследование в течение 0,5-3 ч с достижением хорошего контраста, четких изображений и хорошего выявления патологических изменений.
Другие отличительные признаки и преимущества настоящего изобретения станут более понятными из следующих иллюстративных, не ограничивающих изобретения примеров.
П р и м е р 1. Получение бис(диэтилдитиокарбамат)нитридного комплекса 99mТс(V) (ТсNDEDC).
а) Получение промежуточного соединения
В склянку, аналогичную той, которая используется для получения пенициллина вводят 0,4 мл раствора, содержащего 2˙10-2 молей/л (2,5 мг/мл) S-метилдитиокарбазата в этиловом спирте, затем 0,2 мл 2 ˙10-2молей/л (5 мг/мл) раствора трифенилфосфина в этиловом спирте и 0,1 мл 1 н. раствора хлористоводородной кислоты.
После этого добавляют 0,5- 1 мл раствора пертехнетата натрия (Тс99m) и осуществляют реакцию при 80оС в течение 30 мин или при 100оС в течение 15 мин.
б) Получение конечного комплекса.
К содержимому склянки, полученному на стадии а), добавляют 0,1 мл 1 н. раствора NaOН и 0,5 мл раствора, содержащего 0,18 моль/л тригидратированного диэтилдитиокарбамита натрия (40 мг/мл) в 0,5 моля/л-1 буфера из бикарбоната натрия карбоната при показателе рН 9,0.
Эту реакцию осуществляют в течение 15 мин при 100оС, в течение 30 мин при 80оС или в течение 60 мин при комнатной температуре.
Радиохимическую чистоту полученного комплекса исследовали с помощью тонкопленочной хроматографии с использованием силикагеля и толуола в качестве растворителя.
Полученный комплекс характеризовался скоростью движения по хроматографической бумаге (Rf), равной 0,3-0,4. Радиохимическая чистота равнялась или превышала 93%
П р и м е р 2. Получение бис(диэтилдитиокарбамат)нитридного комплекса 99mТс(V) (ТсNDEDC)
а) Получение промежуточного соединения.
В склянку, аналогичную той, которая используется для получения пенициллина, вводят 0,2 мл раствора, содержащего 7,7˙ 10-2 молей/л (5,0 мг/мл) нитрида натрия в воде, затем 0,2 мл 2 ˙ 10-2 молей/л (5 мг/мл) раствора трифенилфосфина в этиловом спирте и 0,1 мл 1 н. раствора хлористоводородной кислоты.
После этого добавляют 0,5-1 мл раствора пертехнетата натрия (Тс-99m) и осуществляют реакцию при 80оС в течение 30 мин или при 100оС в течение 15 мин.
б) Получение конечного продукта.
К содержимому склянки, полученному на стадии а), добавляют так же, как в примере 1, 0,1 мл 1 н. раствора NaOН и 0,5 мл раствора, содержащего 0,18 моля/л (40 мг/мл) тригидратированного диэтилдитиокарбамата натрия в 0,5 моля/л буфере из бикарбоната натрия карбоната при рН 9. Эту реакцию выполняют так же, как в примере 1.
Исследуют радиохимическую чистоту полученного продукта с помощью тонкопленочной хроматографии, при этом результаты идентичны результатам, полученным в примере 1.
П р и м е р 3.
Получение бис(диэтилдитиокарабамат)нитридного комплекса 99mТс(V) (ТсNDEDC).
а) Получение промежуточного соединения.
В склянку, аналогичную той, которая используется для получения пенициллина, вводят 0,2 мл раствора, содержащего 7,7˙ 10-2 молей/л (5 мг/мл) нитрида натрия в воде, затем 0,4 мл раствора, содержащего 1 ˙ 10-2 молей/л (2 мг/мл) трис(2-цианоэтил)-фосфина в воде и 0,1 мл 1 н. раствора хлористоводородной кислоты.
После этого добавляют 0,5-5 мл раствора пертехнетата натрия (99mТс) и осуществляют реакцию при 80оС в течение 30 мин или при 100оС в течение 15 мин способ получения без спирта.
б) Получение конечного комплекса.
Для получения комплекса ТсNDEDC из ранее полученного промежуточного соединения используют рабочую процедуру, описанную в примере 1, стадия б).
П р и м е р 4. Получение бис(диэтилдитиокарбамат)нитридный комплекс 99mТс(V) (ТсNDEDC).
а) Получение промежуточного соединения.
В склянку, аналогичную той, которая используется для получения пенициллина, вводят 0,2 мл раствора, содержащего 7,7 ˙ 10-2 молей/л (5 мг/мл) нитрида натрия в воде, затем 0,4 мл раствора, содержащего 1˙ 10-2молей/л трис(2-цианоэтил)-фосфина.
После этого добавляют 0,5-5 мл раствора пертехнетата натрия /99mТс) и осуществляют реакцию при 80оС в течение 30 мин или при 100оС в течение 15 мин. Этот процесс выполняли при рН, близком к 7.
б) Получение конечного продукта.
К содержимому склянки, полученному на стадии а), добавляют 0,5 мл раствора, содержащего 0,18 моля/л (40 мг/г) тригидратированного диэтилдитиокарбамата натрия в 0,5 моля/л буфере из бикарбоната натрия карбоната при рН 9. Реакцию осуществляют так же, как в примере 1.
П р и м е р 5. Получение бис(диметилдитиокарбамат)нитридного комплекса 99mТс(V) (ТсNDMDC).
Выполняют рабочую процедуру, описанную в примере 1, за исключением того, что на конечной стадии диэтилдитиокарбамат заменяют 0,5 мл раствора, содержащего 0,18 моля/л дигидратированного диметилдитиокарбамата натрия (30 мг/мл) в таком же буфере. Получают комплекс технеция ТсNDMDC c радиохимической чистотой, эквивалентной такому же показателю, определенному в примере 1.
П р и м е р 6. Получение бис(ди-н-пропилдитиокарбамат)нитридного комплекса 99mТс(V) (ТсNDPDC).
Выполняют рабочую процедуру, описанную в примере 1, за исключением того, что диэтилдитиокарбамат заменяют 0,5 мл раствора, содержащего 0,18 моля/л (40,7 мг/мл) сесквигидратированного ди-н-пропилдитиокарбамата натрия в смеси с 0,5 моля/л буфера из бикарбоната натрия карбоната с рН 9 и этиловый спирт с объемным отношением 7:3.
Получают комплекс технеция ТсNDPDC с радиохимической чистотой, эквивалентной аналогичному показателю, определенному в примере 1.
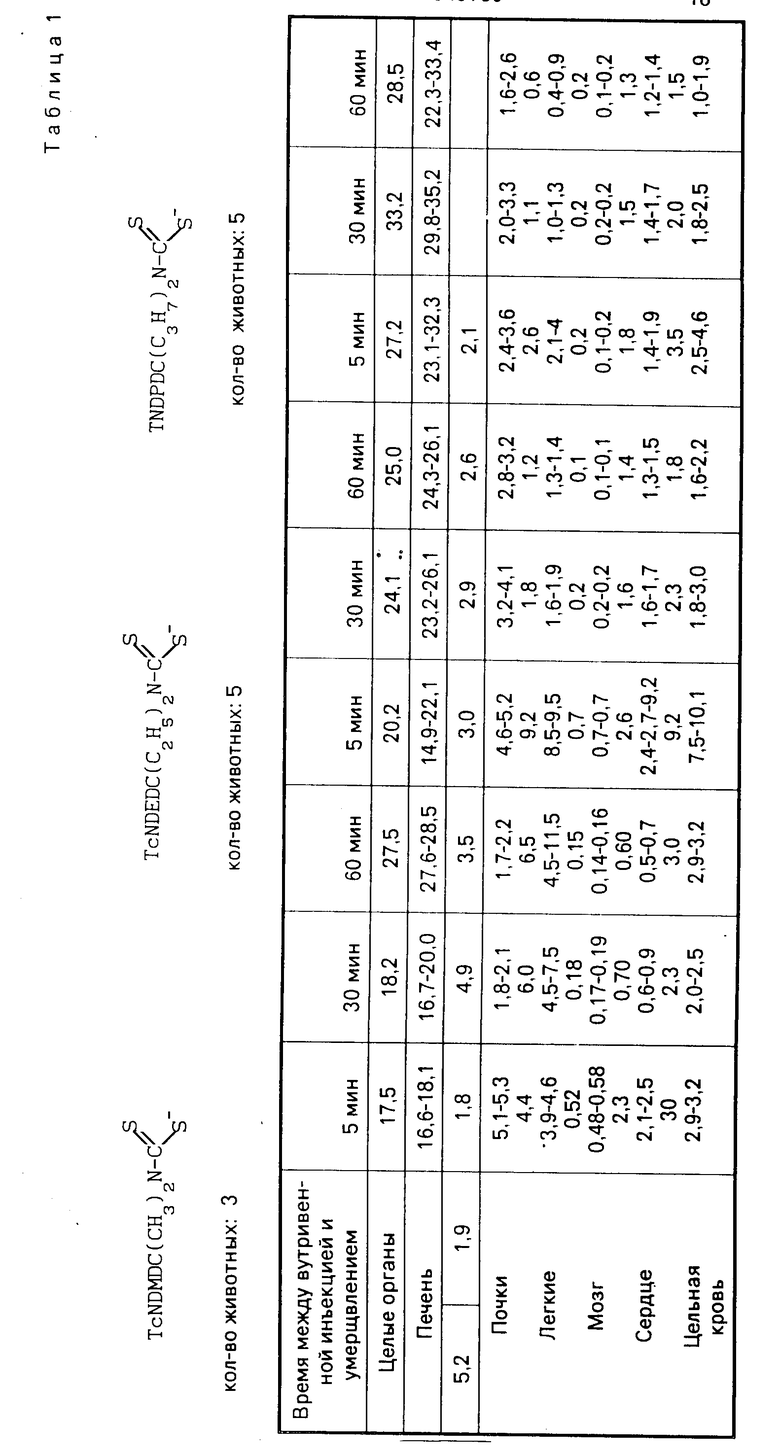
П р и м е р ы 7-9. В этих примерах исследовали свойства комплексов, полученных в примере 1, 5 и 6, посредством определения их биологического распределения у самцов крыс линии "Spraque Daw ley" массой 200± 20 г.
В этом случае крысам, анестезированным пентобарбиталом натрия, инъецировали дозу миотропного лиганда, равную 15 мкмолям/кг массы тела, которая соответствует дозе ионизирующего излучения в 1-2,5 мкСi. Через 5, 30 или 60 мин после инъекции этого продукта крыс умерщвляли и удаляли их органы. После этого определяли радиоактивность, характерную для каждого органа.
Полученные результаты приведены в табл.1 и показывают в процентном выражении инъецированную радиоактивность, обнаруженную в органах, вслед за отбором проб и счетом.
Величины, приведенные в табл.1 представляют среднее значение и два крайних значения.
Табл. 1 показывает, что эти комплексы обладают хорошим кардиотоническим тропизмом.
П р и м е р 10. Получение бис(N,N-диметоксидиэтилдитиокарбамат)нитридного комплекса 99mТс(V) (ТсNMeDC).
а) Получение промежуточного соединения.
В склянку, аналогичную той, которая используется для получения пенициллина, вводят 0,5 мл раствора, содержащего 0,8 ˙10-2 моля/л (1 мг/мл) S-метил-N-метилдитиокарбазата в воде, затем 0,5 мл раствора 2 ˙10-2 молей/л (10 мг/мл) трисульфированного трифенилфосфина в воде и 0,1 мл 1 н. раствора хлористоводородной кислоты. После этого добавляют 0,5-5 мл раствора пертехнетата натрия (Тс99m) и осуществляют реакцию при 80оС в течение 30 мин или при 100оС в течение 15 мин.
б) Получение конечного комплекса.
К содержимому склянки, полученному на стадии а), добавляют 0,1 мл 1 н. раствора NaOН и 0,5 мл раствора, содержащего 0,1 моля/л диметоксиэтилдитиокарбамата натрия (23 мг/мл) в 0,5 моля/л буфера из бикарбоната натрия карбоната при рН 9,5. Эту реакцию осуществляют в течение 30 мин при комнатной температуре.
Получают нитридный комплекс ТсNMEDC или комплекс формулы (Тс ≡ N/L1L2, в которой L1 и L2 представляли соединение формулы (Y1).
П р и м е р 11. Получение бис(N-этил-N-(2-метоксиэтил)дитиокарбамат)-нитридного комплекса 99mТс(V) (ТсNEMEC)
Выполняют рабочую процедуру, описанную в примере 10, для получения промежуточного соединения из S-метил-N-метилдитиокарбазата и трисульфированного трифенилфосфина. После этого получали конечный продукт в соответствии с рабочей процедурой, описанной в примере 10, но при этом используют 0,5 мл раствора 0,1 моля/л N-этил-N-(2-метоксиэтил)-дитиокарбамата натрия (20 мг/мл) вместо диметоксиэтилдитиокарбамата натрия по примеру 10.
Получают бис((N-этил-N-(2-метоксиэтил)-дитиокарбамат)нитридный комплекс 99mТс(V), то есть продукт формулы:
/Тс ≡ N/L1L2, в которой L1 и L2 представляют соединения формулы (VII).
П р и м е р 12. Получение бис(N-этил-N-(3-метоксипропил) -дитиокарбамат)-нитридного комплекса 99mТс(V) (ТсNEMPC).
Выполняли рабочую процедуру, описанную в примерах 10 и 11, для получения этого комплекса из промежуточного соединения, полученного на стадии а) примера 10, при этом в качестве реагента на стадии б) применяют 0,5 мл раствора 0,1 моля/л N-этил-N-(3-метоксипропил)-дитиокарбамата натрия (22 мг/мл).
Получают нитридный комплекс ТсТЕМPC или комплекс формулы (Тс≡N)L1L2, в которой L1 и L2 представляют соединение формулы (VIII).
П р и м е р 13. Получение бис(N-этил-N-(2-этоксиэтил)-дитиокарбамат)-нитридного комплекса 99mТс(V) (ТсNEEDC).
Выполняли рабочую процедуру, описанную в примере 10, для получения промежуточного соединения и конечного продукта за исключением того, что в качестве реагента для получения конечного продукта используют 0,5 мл раствора 0,1 моля/л N-этил-N-(2-этоксиэтил)-дитиокарбамата натрия (22 мг/мл).
Получают нитридный комплекс ТсNEEDC или комплекс формулы (Тс ≡ N/L1L2, в которой L1 и L2 представляют соединение формулы (1Х).
П р и м е р 14. Получение бис(N-метокси-N-метилдитиокарбамат) нитридного комплекса 99mТс(ТсNMEMC).
а) Получение промежуточного соединения.
Выполняют рабочую процедуру, описанную в примере 10, для получения промежуточного соединения при использовании тех же реагентов и создании таких же условий реакции.
б) Получение конечного комплекса.
К содержимому склянки, полученному на стадии а), добавляют 0,1 мл 1 н. раствора NaOН и 0,5 мл раствора, содержащего 0,13 моля/л N-метокси-N-метилдитиокарбамата натрия (20 мг/мл) в 0,5 моля/л буфера из бикарбоната натрия карбоната при рН 9,5. Эту реакцию выполняют в течение 30 мин при комнатной температуре.
Получают комплекс ТсNMEМС, имеющий формулу (Тс≡N/L1L2, в которой L1 и L2 представляют: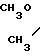 N-C
N-C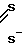
П р и м е р 15. Получение бис(N-метокси-N-этилдитиокарбамат/нитридного комплекса 99mТс/V/ /ТсNMEEC/.
Выполняют рабочую процедуру, описанную в примере 14, для получения этого комплекса технеция из того же промежуточного соединения с использованием для получения конечного продукта 0,5 мл раствора 0,12 моля/л N-метокси-N-этилдитиокарбамата натрия (20 мг/мл). Получают комплекс ТсNMEEC, в частности, комплекс формулы (Тс≡N/L1L2, в которой L1 и L2 имеют формулу: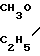 N-C
N-C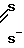
П р и м е р 16. Получение бис/N-этокси-N-метилдитиокарбамат/нитридного комплекса 99mТс/V/ /ТсNEТМС/.
В этом примере выполняют рабочую процедуру, описанную в примере 14, за исключением того, что в качестве реагента для получения конечного продукта используют 0,5 мл раствора 0,12 моля/л N-этокси-N-метилдитиокарбамата натрия (20 мг/мл).
Получают комплекс технеция формулы (Тс ≡ N/L1L2, в которой L1 и L2 имеют формулу: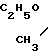 N-C
N-C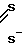
П р и м е р 17. Получение бис(N-этокси-N-этилдитиокарбамат) нитридного комплекса 99mТс(V)(ТсNEТЕС).
Выполняют рабочую процедуру, описанную в примере 14, для получения этого комплекса технеция с использованием в качестве реагента на второй стадии 0,5 мл раствора, содержащего 0,11 моля/л N-этокси-N-этилдитиокарбамата (20 мг/мл).
Получают комплекс формулы (Тс≡ N/L1,L2, в которой L1 и L2 имеют формулу: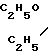 N-C
N-C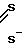
П р и м е р 18. Биологические свойства комплексов, полученных в соответствии с примерами 10-13 и 17, исследовали посредством определения величины удерживания радиоактивности миокардом у собак весом от 10 до 15 кг.
В этом случае собакам, анестезированным пентобарбиталом натрия и находящимся в условиях искусственной вентиляции легких, инъецировали дозу, равную 2 мкмолям/кг массы тела миотропного комплекса технеция, которая соответствует дозе облучения, равной 2-5 mCi.
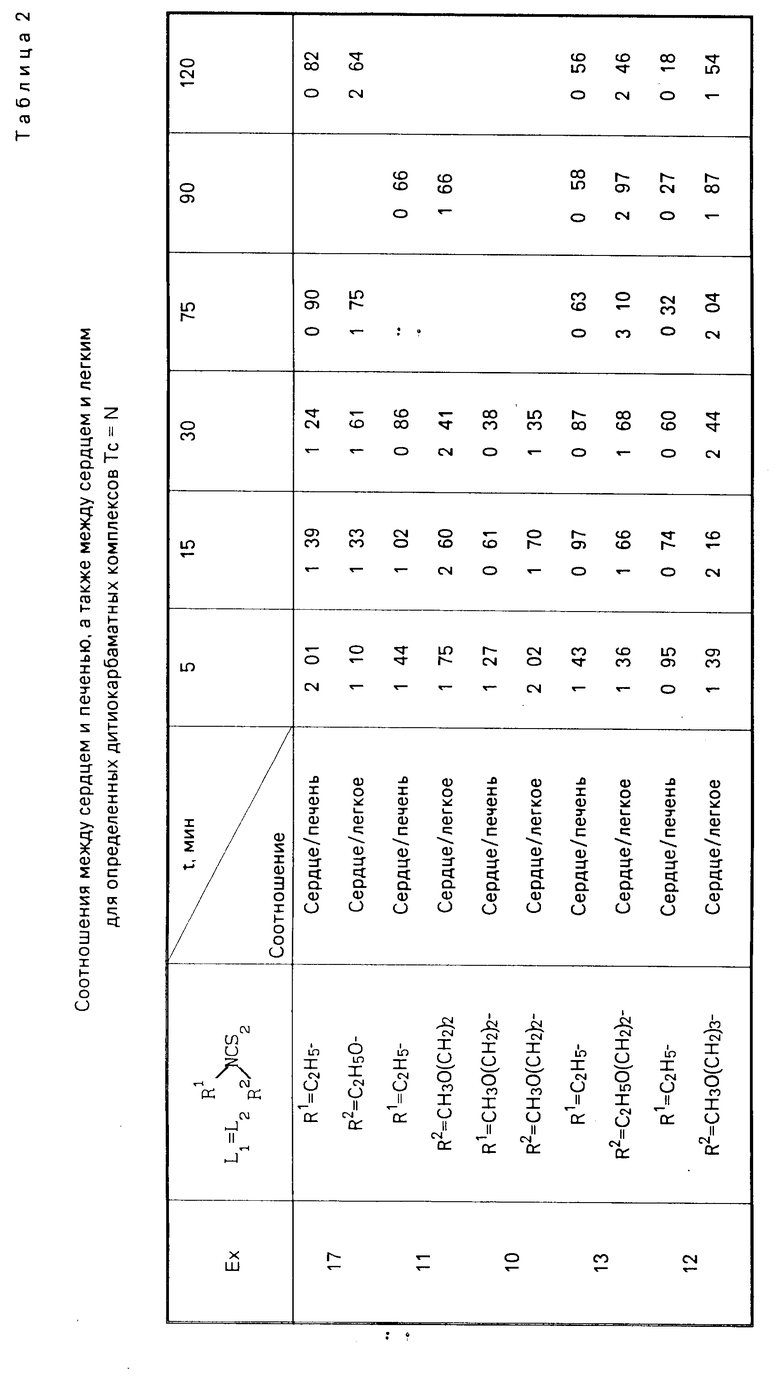
Величину удерживания радиоактивности миокардом и окружающими органами (легки и печень) определяли исходя из динамической восприимчивости между инъекцией и концом исследования с использованием гамма-камеры при установлении представляющих интерес участков для каждого органа. Все испытуемые комплексы обеспечили хорошее визуальное воспроизведение миокарда.
Величины контрастирования сердца и печени, а также сердца и легкого измеряли путем установления простого соотношения между числом биений на единицу поверхности (или точку) в органах. Величины соотношения между сердцем и печенью, а также между сердцем и легким приведены в табл.2.
Соотношения между шумами целевого органа и фоновыми шумами являются весьма благоприятными.
П р и м е р ы 19-21. В этих примерах исследуются свойства комплексов, полученных в примерах 15-18, путем определения их биологического распределения у самцов крыс линии "Spraque Dawley" весом 200± 20 г.
В этом случае крысам, анестезированным пентобарбиталом натрия, инъецировали дозу комплекса, соответствующую 15 мкмолям/кг массы тела миотропного лиганда, которая соответствует дозе облучения, равной 1-2,5 mkCi.
Через 5, 30 или 60 мин после инъекции этого продукта крыс умерщвляли и удаляли органы. Определяли радиоактивность, характерную для каждого из органов.
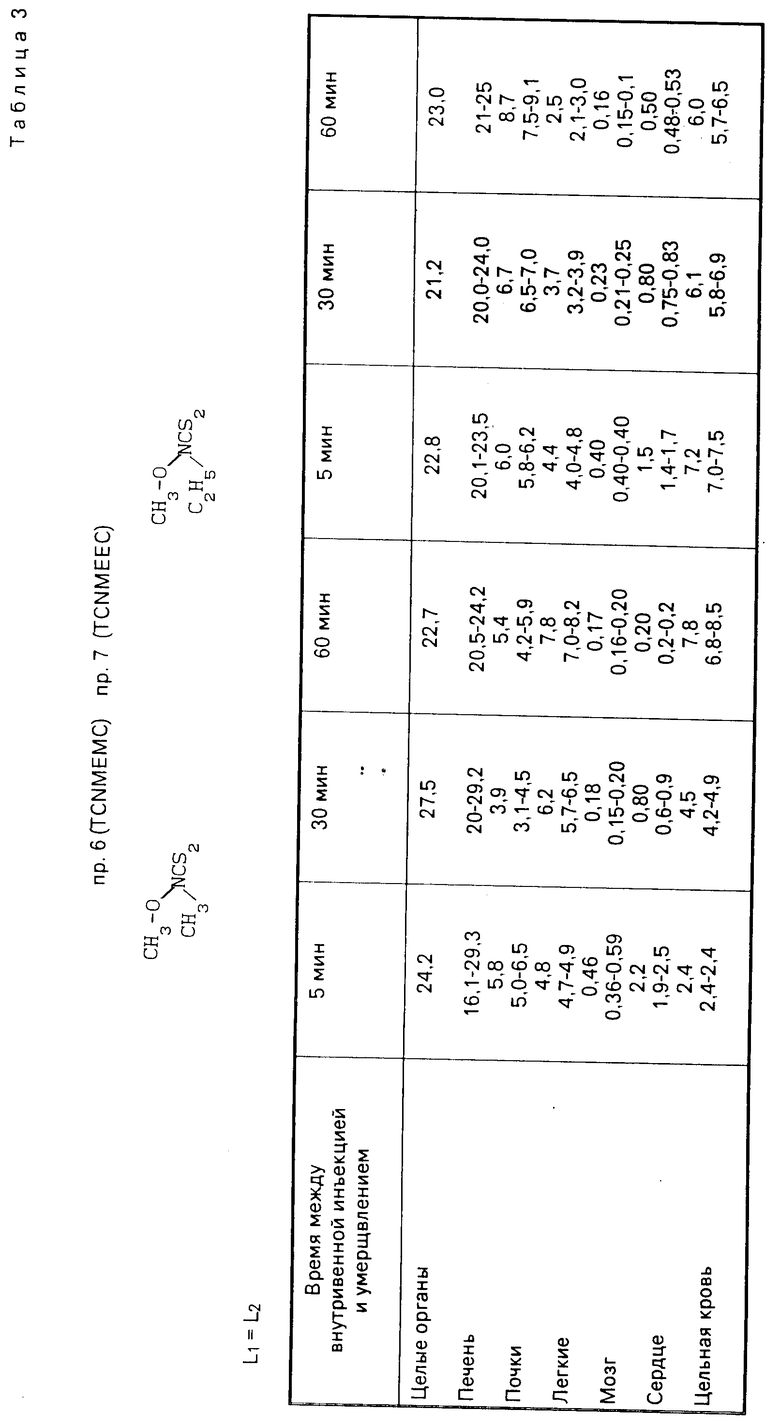
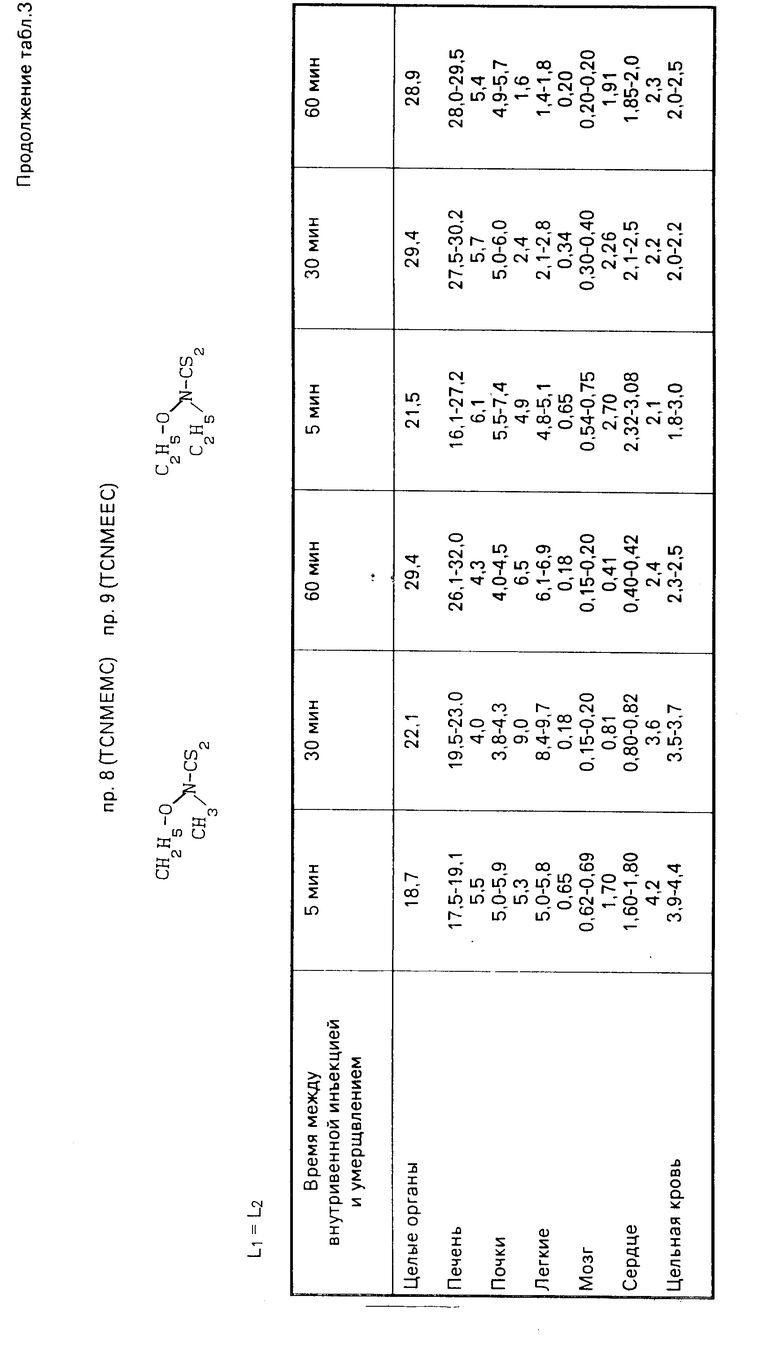
Полученные результаты приведены в табл.3 и представлены в виде процентного выражения инъецированной радиоактивности, обнаруженной в органе, после отбора проб и счета. Величины, приведенные в таблице 3, представляют среднее значение и два крайних значения.
Из табл. 3 видно, что эти комплексы обладают хорошим кардиотоническим тропизмом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ ПЕРЕХОДНЫХ МЕТАЛЛОВ | 1990 |
|
RU2026300C1 |
| КОНЪЮГАТЫ, ПОЛУЧЕННЫЕ ИЗ КОМПЛЕКСОВ МЕТАЛЛОВ И ОЛИГОНУКЛЕОТИДОВ, СРЕДСТВА, СОДЕРЖАЩИЕ КОНЪЮГАТЫ, ИХ ИСПОЛЬЗОВАНИЕ В РАДИОДИАГНОСТИКЕ, А ТАКЖЕ СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2165771C2 |
| КОМПОНЕНТ КАТАЛИЗАТОРА ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ И СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1998 |
|
RU2203908C2 |
| РАДИОФАРМАЦЕВТИЧЕСКИЕ ПРОДУКТЫ | 2007 |
|
RU2448733C2 |
| N-МЕТИЛГОМОЦИСТЕИНЫ, ИХ ПРИМЕНЕНИЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2305678C2 |
| НОВЫЕ КОМПОЗИЦИИ НА ОСНОВЕ ПОЛИСАХАРИДОВ, ПРИВИТЫХ С ПОМОЩЬЮ ПОЛИАМИННЫХ ИЛИ ПОЛИСУЛЬФИРОВАННЫХ СОЕДИНЕНИЙ | 2008 |
|
RU2481856C2 |
| РАДИОФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ (ТЕРАПИИ) КОСТНЫХ ПОРАЖЕНИЙ СКЕЛЕТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2407746C2 |
| СПОСОБ ПОЛУЧЕНИЯ β -ФЕНИЛИЗОСЕРИНА И ЕГО АНАЛОГОВ, ПРОИЗВОДНЫХ α -ФЕНИЛИЗОСЕРИНА, ПРОИЗВОДНЫЕ АЗЕТИДИНОНА | 1993 |
|
RU2103258C1 |
| СТАБИЛИЗИРОВАННЫЕ КОМПОЗИЦИИ ТЕХНЕЦИЯ-99m (Tc) | 2005 |
|
RU2403067C2 |
| ТАКСОИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1995 |
|
RU2144920C1 |
Использование: в качестве радиофармацевтического продукта, обладающего кардиотоническим тропизмом. Сущность изобретения: нитридный комплекс переходного металла ф-лы 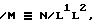 где M-Tc99, Re,186, Re,188:L′ L2 остатки лигандов ф-лы
где M-Tc99, Re,186, Re,188:L′ L2 остатки лигандов ф-лы 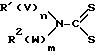 где R
где R
НИТРИДНЫЙ КОМПЛЕКС ПЕРЕХОДНОГО МЕТАЛЛА общей формулы
/M ≡ N/ L1 L2,
где M Tc99, Re186, Re188;
L1 и L2 остатки лигандов общей формулы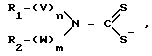
где R1 и R2, одинаковые или различные, C1 C6 алкил с прямой или разветвленной цепью, который может быть замещен низшей алкоксигруппой;
m и n 0, 1;
W и V 0, S, Se,
полученные взаимодействием пертехнетата или перрената аммония или щелочного металла с первым лигандом, выбранным из низшего алифатического или ароматического фосфина, вторым реагентом, выбираемым из группы нитрида аммония или нитрида щелочного металла, и азотистым вторым лигандом, выбранным из соответствующего S-низшего алкилтиокарбазата, гидразина в форме хлоргидрата, тиосемикарбазида, с последующим добавлением к полученному промежуточному соединению дитиокарбамата общей формулы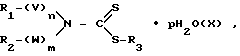
где R1, R2, V, W, n и m имеют указанные значения;
R3 ион щелочного металла, H+, NH
p 0 или 1 5.
| Устройство для выпрямления опрокинувшихся на бок и затонувших у берега судов | 1922 |
|
SU85A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-12-10—Публикация
1989-11-24—Подача