Изобретение относится к способу получения гидроокиси щелочного металла хлорощелочным электролизом, в котором раствор хлорида щелочного металла подвергают электролизу с образованием гидроокиси щелочного металла, хлора и водорода.
Во многих странах проблемой хлорощелочных производств является дисбаланс между спросом на гидроокись щелочного металла и на хлор, которые представляют собой главные продукты электролиза. Ожидается, что в будущем этот дисбаланс ухудшится вследствие давления экологических факторов, обусловленных использованием хлора и конечных продуктов его переработки. Результатом этого является необходимость нахождения альтернативных способов получения гидроокисей щелочных металлов, поскольку они не могут быть получены в адекватных количествах с помощью известного хлорощелочного электролиза.
Другие известные способы получения гидроокисей щелочных металлов включают в себя:
химическое декарбонирование соды известковым молоком или аммиаком;
электролитическое разложение сульфата щелочного металла с образованием гидроокиси щелочного металла и серной кислоты;
декарбонирование соды кислым раствором сульфата щелочного металла и электролиз полученного таким образом раствора сульфата с образованием гидроокиси щелочного металла;
каталитическое разложение сульфида щелочного металла с образованием гидроокиси щелочного металла и двуокиси серы и
электролитическое разложение хлората щелочного металла с образованием гидроокиси щелочного металла и двуокиси хлора.
Как правило, хлорат получают электрическим разложением хлоридов щелочных металлов.
Все эти известные способы являются невыгодными для нынешних производителей гидроокисей щелочных металлов. Наиболее общеизвестные альтернативные способы имеют следующие недостатки: образование в способе слишком больших количеств сернистых соединений, не имеющих крупномасштабного применения, в качестве побочных продуктов; слишком большие расходы на сырье и энергию по сравнению с рыночной ценой продукта; способ требует больших капиталовложений, и, таким образом, капитальные затраты на производство слишком велики по сравнению с рыночной ценой продукта.
Целью изобретения является создание способа получения гидроокиси щелочного металла, который позволяет избежать недостатков известных способов, может быть осуществлен на хлорощелочных производствах, позволяет, кроме того, контролировать на требуемом уровне соотношение образующихся при хлорощелочном электролизе гидроокиси щелочного металла и хлора и позволяет дополнительно получать водород и согласно одному из вариантов осуществления также и хлорат щелочного металла, которые могут быть далее утилизированы.
Главные отличительные признаки настоящего изобретения изложены в формуле изобретения.
Изобретение основано на том, что, по крайней мере, часть используемого в хлорощелочном гидролизе хлорида щелочного металла может быть получена нейтрализацией или декарбонированием карбоната щелочного металла хлором или газообразным хлористым водородом. При декарбонировании карбоната щелочного металла хлором в водном растворе одновременно образуется хлорат щелочного металла.
Под щелочным металлом в данном контексте имеются в виду в первую очередь натрий и калий, в особенности натрий.
При использовании для нейтрализации хлора продуктами реакции нейтрализации карбоната щелочного металла в водном растворе являются двуокись углерода, хлорид и хлорат щелочного металла.
При использовании для нейтрализации хлористого водорода продуктами реакции нейтрализации карбоната щелочного металла являются двуокись углерода, хлорид щелочного металла и вода.
Согласно первому предпочтительному варианту осуществления изобретения карбонат щелочного металла и хлор на стадии нейтрализации подаются в реактор, содержащий воду или раствор хлорида щелочного металла, или раствор хлората щелочного металла и хлорида щелочного металла. При нейтрализации карбоната щелочного металла хлором образуются хлорид и хлорат щелочного металла. Раствор становится пересыщенным в отношении хлорида, и, таким образом, хлорид щелочного металла может быть отделен от раствора в виде кристаллов. Затем этот хлорид щелочного металла используют обычным путем в электролизе, получая хлор, гидроокись щелочного металла и водород. Предпочтительно по крайней мере часть хлора рециркулируют в вышеуказанный реактор. Для того чтобы избежать перенасыщения раствора в реакторе в отношении хлората, побочный поток выводится из реактора для дальнейшей переработки хлората.
Полученный из реактора кристаллический хлорид щелочного металла предпочтительно растворяют в жидком рециркулянте хлорощелочного производства, т.е. в разбавленном растворе щелочного металла, выходящего со стадии хлорощелочного электролиза; концентрацию получаемого раствора предпочтительно поддерживают близкой к концентрации насыщенного раствора. После очистки этот раствор возвращают на стадию хлорощелочного электролиза.
Согласно второму предпочтительному варианту осуществления изобретения карбонат щелочного металла и хлор на стадии нейтрализации смешивают с разбавленным раствором хлорида щелочного металла, выходящим со стадии хлорощелочного электролиза. При нейтрализации карбоната щелочного металла хлором образуются хлорид и хлорат щелочного металла. Хлорат щелочного металла удаляют из полученного раствора или превращают в требуемый продукт известным способом и полученный таким образом концентрированный раствор хлорида щелочного металла после очисти возвращают на стадию хлорощелочного электролиза для получения гидроокиси щелочного металла, хлора и водорода. Предпочтительно по крайней мере часть полученного хлора направляют на вышеупомянутую стадию нейтрализации.
Согласно третьему предпочтительному варианту осуществления изобретения нейтрализацию проводят, добавляя карбонат щелочного металла к выходящему из электролитических ячеек раствору хлорида щелочного металла, в котором растворен газообразный хлористый водород, и полученный таким образом раствор хлорида щелочного металла подают после очистки в электролитические ячейки.
Согласно четвертому предпочтительному варианту осуществления изобретения нейтрализацию проводят, добавляя карбонат щелочного металла к выходящему из электролитических ячеек раствору хлорида щелочного металла и затем нейтрализуя карбонат газообразным хлористым водородом, и полученный таким образом раствор хлорида щелочного металла подают после очистки в электролитические ячейки.
Согласно пятому предпочтительному варианту осуществления изобретения, нейтрализацию проводят в закрытом контуре циркуляции, содержащем первоначально или воду, или раствор хлорида щелочного металла. Затем в контур циркуляции вводят карбонат щелочного металла и или газообразный хлористый водород, или хлористоводородную кислоту. После декарбонирования карбоната щелочного металла раствор становится пересыщенным в отношении хлорида щелочного металла, который затем может быть отделен от раствора в виде кристаллов. Затем эти кристаллы подают в рециркулируемый со стадии хлорощелочного электролиза раствор для получения хлора, гидроокиси щелочного металла и водорода.
Следовательно, при нейтрализации образуется раствор хлорида щелочного металла обычного хлорощелочного производства, этот раствор хлорида щелочного металла очищают известными способами в зависимости от конкретной электролитической ячейки.
Подаваемый на стадию хлорощелочного электролиза раствор хлорида щелочного металла предпочтительно является близким к насыщенному.
Величина pH раствора при нейтрализации предпочтительно больше 3, особенно предпочтительно от 3 до 11.
Нейтрализацию можно проводить непрерывно или периодически в широком интервале температур, предпочтительно от 20 до 100oC. При использовании для нейтрализации хлора концентрации хлората и хлорида щелочного металла в выводимом со стадии нейтрализации растворе зависят от температуры. Нейтрализацию можно проводить в одну или в несколько стадий.
Согласно способу настоящего изобретения, хлорид щелочного металла подвергают электролизу в электролитических ячейках известным способом для получения гидроокиси щелочного металла. Электролиз можно проводить в ячейках с ртутным катодом, диафрагмой или мембраной. Качество получаемого после электролиза раствора гидроокиси щелочного металла эквивалентно качеству, получаемому при известном хлоридном способе.
Используемый для нейтрализации карбоната щелочного металла газообразный хлор предпочтительно получают электролизом. Хлорид декарбонирует природный карбонат, снова образуя хлорид щелочного металла, хлорат щелочного металла и двуокись углерода. Двуокись углерода может быть далее очищена и сжижена известным способом для дальнейшего использования. Хлорат щелочного металла может быть использован для получения хлората щелочного металла, или в процессе, где расходуется хлорат щелочного металла, или может быть превращен в раствор хлорида действием хлористоводородной кислоты, или может быть разрушен, или может быть далее очищен каким-либо иным желаемым образом.
Используемый для нейтрализации карбоната щелочного металла хлористый водород предпочтительно получают из газообразных хлора и водорода в аппарате синтеза, куда подают также известный избыток газообразного водорода, требующийся для синтеза хлористого водорода. После синтеза полученный водородсодержащий газообразный хлористый водород можно поглотить известным способом или водой, или разбавленным раствором хлористоводородной кислоты. Нагревание концентрированного раствора хлористоводородной кислоты дает чистый газообразный хлористый водород, который поглощается разбавленным раствором хлорида щелочного металла, выходящим из электролитических ячеек. Полученным кислым раствором хлорида декарбонируют природный карбонат, снова получая хлорид щелочного металла и двуокись углерода. Двуокись углерода может быть далее очищена и сжижена известным способом для последующего использования.
Замечательным преимуществом настоящего изобретения является то, что для осуществления способа могут быть использованы существующие, но не полностью загруженные хлорощелочные производства. Согласно настоящему изобретению, контролируя количество карбоната щелочного металла, можно влиять на то, какая часть хлора, образующегося при электролизе, остается в виде товарного продукта процесса. Одним из существующих отличий изобретения является, в частности, то, что, меняя количество соли, полученной из карбоната щелочного металла и вводимой в процесс, можно плавно регулировать в пределах от около 0% до около 100% соотношение товарного хлора и получаемой гидроокиси щелочного металла. Остальная часть хлорида щелочного металла, требующегося для электролиза, обеспечивается подачей новых порций хлорида щелочного металла в рециркулируемый раствор.
Другим важным преимуществом изобретения является то, что при хлорировании карбоната предпочтительно образуется хлорат, который можно утилизировать легко и экономично. Регулируя температуру в реакторе, можно влиять на содержание хлората и хлорида в получаемом растворе и, следовательно, получать состав раствора, который наилучшим образом соответствует предстоящему использованию.
Третьим важным преимуществом изобретения является то, что образующийся при хлорощелочном электролизе водород может быть с выгодой использован или в других химических процессах, или в качестве экологически чистого топлива при производстве энергии.
Степень нейтрализации карбоната щелочного металла можно регулировать количеством водорода или хлористого водорода и, следовательно, обеспечивать надлежащие условия для очистки и электролиза раствора хлорида щелочного металла.
Среди наиболее замечательных преимуществ в отношении существующих хлорощелочных производств можно упомянуть следующие: в способе может быть использован дешевый, даже неочищенный карбонат щелочного металла, пригодный для электролитического использования. В рамках способа не происходит образования в качестве побочных продуктов вредных сернистых соединений. Существующая производительность электролитической ячейки может быть использована полностью. Капиталовложения, которых требует способ на существующих производствах, очень малы по сравнению с альтернативными способами при той же производительности по гидроокиси щелочного металла. Способ очень гибок при изменении потребностей в производстве хлора и щелочи. Себестоимость гидроокиси щелочного металла при реализации способа согласно настоящему изобретению очень мала по сравнению с альтернативными способами. При использовании для нейтрализации хлора в качестве побочных продуктов образуются хлорат и водород, которые могут быть экономично утилизированы, и, следовательно, способ более выгоден экономически.
На фиг.1 показана блок-схема, иллюстрирующая принципы получения гидроокиси щелочного металла согласно настоящему изобретению, приспособленная для получения щелока; на фиг.2 блок-схема, иллюстрирующая принципы второго варианта получения гидроокиси щелочного металла согласно настоящему изобретению, приспособленная для получения щелока; на фиг.3 блок-схема, иллюстрирующая принципы третьего варианта получения гидроокиси щелочного металла согласно настоящему изобретению, приспособленная для получения щелока; на фиг. 4 блок-схема, иллюстрирующая принципы четвертого варианта получения гидроокиси щелочного металла согласно настоящему изобретению, приспособленная для получения щелока.
На фиг.1 стадия электролиза обозначена номером 1. На стадию электролиза через стадию очистки 4 подают раствор хлорида натрия. На стадии электролиза 1 получают целевые продукты раствор гидроокиси натрия и водород, которые могут быть далее подвергнуты обработке известным способом. Полученный на стадии электролиза 1 газообразный хлор транспортируют в реактор 2, куда газообразный хлор может также быть подан через стадию сжижения 6 и стадию испарения 7. В реакторе 2 кристаллы хлористого натрия, являющиеся продуктом реакции хлора и соды, отделяют от реакторного раствора и на стадии насыщения 3 растворяют в разбавленном растворе соли, возвращаемом со стадии электролиза 1; при необходимости на стадии 3 добавляется дополнительный хлорид натрия. Насыщенный раствор соли подают со стадии насыщения 3 на стадию очистки 4, и далее на стадию электролиза 1. В реакторе 2 образуются также двуокись углерода CO2 и хлорат натрия, которые направляют на стадию дальнейшей переработки 5 и 8. Стадия дальнейшей переработки 5 может заключаться в отделении хлората натрия от раствора или в его использовании как такового в других процессах.
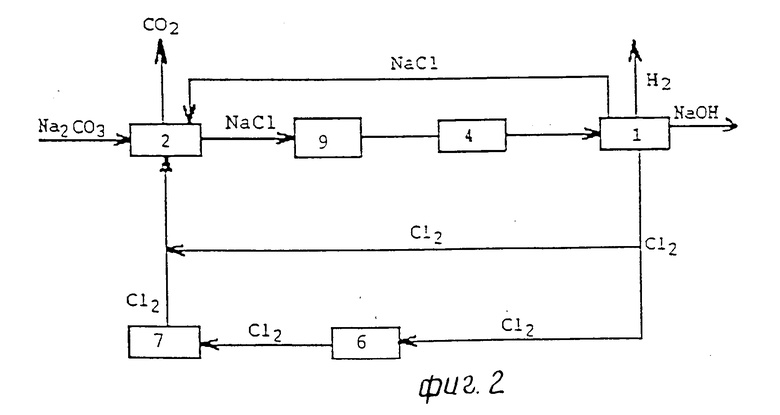
На фиг. 2 раствор хлорида натрия подают на стадию электролиза 1 через стадию очистки 4. На стадии электролиза 1 получают целевые продукты раствор гидроокиси натрия и водород, которые далее могут быть подвергнуты обработке известным способом. Карбонат натрия и полученный на стадии электролиза 1 хлор непосредственно добавляют в реакторе 2 к раствору, рециркулируемому со стадии хлорощелочного электролиза. Газообразный хлор может быть также подан в реактор 2 через стадии ожижения 6 и испарения 7. Образовавшийся в реакторе 2 в рециркулируемом растворе хлорат превращают в требуемое соединение известным способом на стадии 9, откуда концентрированный раствор соли направляют на стадию очистки 4 и далее на стадию электролиза 1. Если хлор является товарным продуктом, то к рециркулируемому раствору добавляют дополнительное количество хлористого натрия, например, в позиции 2.
На фиг.3 стадия электролиза обозначена номером 1. На стадию электролиза подают раствор хлористого натрия, полученный на стадии очистки хлористого натрия 4. На стадии электролиза 1 получают целевой продукт раствор гидроокиси натрия, который далее может быть подвергнут обработке известным способом. Полученные на стадии электролиза газообразные хлор и водород направляют на стадию синтеза хлористоводородной кислоты 10, откуда хлористоводородную кислоту направляют на стадию выделения газообразного хлористого водорода 11. Полученный чистый газообразный хлористый водород на стадии поглощения хлористого водорода 12 поглощается разбавленным раствором хлористого натрия, отводимым со стадии электролиза. Полученный кислый раствор хлористого натрия направляют на стадию нейтрализации 2, где добавляют соду. На стадии нейтрализации 2 происходит декарбонирование соды кислым раствором хлорида с образованием хлорида натрия, который направляют на стадию очистки хлористого натрия 4, и двуокиси углерода, которую направляют на стадию очистки двуокиси углерода 8.
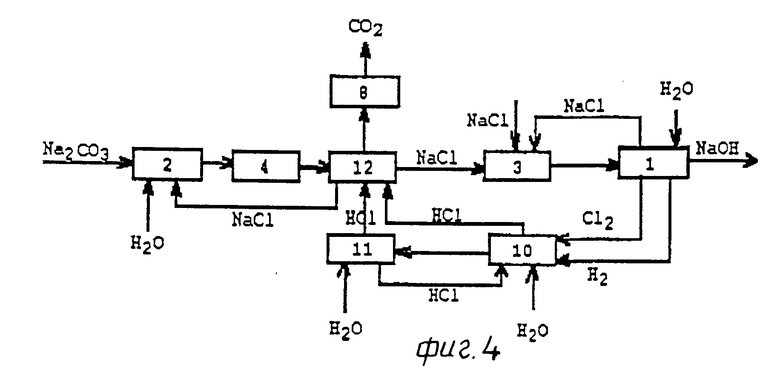
На фиг.4 стадия электролиза обозначена номером 1. На эту стадию со стадии насыщения 3 подают раствор хлористого натрия; если получаемый хлор является товарным продуктом, то на стадию 3 подают хлористый натрий извне. На стадии электролиза 1 получают целевой продукт раствор гидроокиси натрия, который может быть далее обработан известным способом. Полученные на стадии электролиза 1 газообразные хлор и водород подаются на стадию синтеза хлористоводородной кислоты 10. Оттуда хлористоводородная кислота может подаваться непосредственно или через стадию испарения 11 в реакторе 12. В реакторе 12 хлористоводородная кислота декарбонирует соду с образованием хлористого натрия, двуокиси углерода и воды. Раствор становится пересыщенным в отношении хлорида, и хлористый натрий может быть отделен от раствора в виде кристаллов. Затем эти кристаллы направляют на стадию насыщения 3. Из реактора 12 раствор соли возвращают на стадию растворения соды 2, с которой его через стадию очистки 4 направляют в реактор 12. Образовавшуюся двуокись углерода очищают в позиции 8 и направляют на дальнейшую обработку.
Работоспособность способа была испытана с помощью нескольких тестов лабораторного масштаба. Их целью было определить влияние температуры, pH и различных концентраций на протекание реакции. Согласно полученным результатам хлорид образуется в количествах, в пять раз или более чем в пять раз превосходящих количество хлората. Конечное значение pH составляет, в зависимости от степени хлорирования, больше трех. Согласно кривой растворимости хлората/хлорида имеется корреляция между температурой и концентрациями, которая определяет состав раствора, выводимого из реактора.
Далее изобретение поясняется с помощью примеров.
Пример 1. Берут 250 мл раствора, содержащего, г/л;
NaCl 170
NaClO3 400
Na2CO3 50
Температура, oC 30
Через этот раствор пропускают газообразный хлор до тех пор, пока весь карбонат натрия не прореагирует с хлором. Остаточный хлор удаляют из полученного раствора перемешиванием. Анализируют полученные хлорированный раствор и кристаллы. В результате получают раствор, содержащий, г/л:
NaCl 185,2
NaClO3 406,2
Получают 9,3 г кристаллической соли, содержащей 0,42 г и 8,92 г NaCl. Конечное значение pH равно 4,7.
Пример 2. В 1 л воды растворяют 100 г Na2CO3. pH полученного раствора 10,2. Этот раствор хлорируют до исчерпания Na2CO3. В результате получают раствор, содержащий 83,9 г NaCl, 25,5 NaClO3 и 5,5 г активного хлора. Конечное значение pH 6,2.
Пример 3. Берут тысячу миллилитров раствора хлористого натрия, имеющего температуру 65oC и концентрацию 253 г NaCl на литр. Этим раствором медленно поглощают 30 г газообразного хлористого водорода, полученного нагреванием 33%-ной хлористоводородной кислоты. К кислому раствору соли медленно добавляют 45 г технического карбоната натрия с содержанием Na2CO3 99,3% После прекращения выделения двуокиси углерода находят, что конечная концентрация соли равна 298 г/л. Конечная температура раствора равна 55oC, конечное значение pH 5. Согласно анализу, образуется 49 г хлористого натрия, что хорошо согласуется с теоретическими вычислениями. Качество полученного раствора таково, что он может использоваться как исходный раствор для электролиза.

Изобретение относится к способу получения гидроокиси щелочного металла хлорощелочным электролизом, в котором раствор хлорида щелочного металла подвергают электролизу для получения гидроокиси щелочного металла, хлора и водорода и в котором по меньшей мере часть используемого для электролиза хлорида щелочного металла получают нейтрализацией карбоната щелочного металла хлором или хлористым водородом. 16 з.п. ф-лы, 4 ил.
Приоритет по пунктам:
13.03.92 по пп.6, 7, 9, 10, 11, 12, 15, 16, 17;
19.02.93 по пп.2, 3, 4, 5, 13 и 16.
Приоритет по признакам:
13.03.92 в п.1 признаки: способ получения гидроокиси щелочного металла электролизом раствора хлорида щелочного металла с получением хлора и водорода, по крайней мере, часть раствора хлорида получают нейтрализацией раствора карбоната соответствующего щелочного металла с хлорсодержащим агентом, причем в качестве хлорсодержащего агента используют хлористый водород с получением в растворе хлорида щелочного металла, в п.8 признаки: нейтрализацию проводят в рециркулируемом растворе, в который подают карбонат щелочного металла и хлористо-водородную кислоту или газообразный хлористый водород.
| Якименко Л.М | |||
| Производство хлора, каустической соды и неорганических хлорпродуктов | |||
| - М.: Химия, 1974, с.193-194, рис.4-1. |
Авторы
Даты
1997-09-27—Публикация
1993-03-12—Подача