Данная заявка устанавливает приоритет предварительной заявки США № 60/973948, зарегистрированной 20 сентября 2007 г., предварительной заявки на патент США № 61/032802, зарегистрированной 29 февраля 2008 г., и предварительной заявки на патент США № 61/033298, зарегистрированной 3 марта 2008 г., все содержание которых полностью включено в данный документ в качестве ссылки.
УРОВЕНЬ ТЕХНИКИ
1. Область техники, к которой относится изобретение
Данное изобретение в целом относится к области удаления диоксида углерода и, одновременно с его удалением, других загрязняющих веществ из потоков отходов. Более конкретно, данное изобретение относится к удалению диоксида углерода и других загрязняющих веществ из потоков отходов посредством абсорбции диоксида углерода и других загрязняющих веществ из концентрированных потоков, например дымовых газов, и последующего совместного образования карбонатных и/или бикарбонатных материалов, которые захватывают и нейтрализуют любые абсорбированные попутные загрязняющие вещества.
2. Предшествующий уровень техники
Значительный внутригосударственный и международный интерес как в частном, так и в коммерческом секторе на протяжении последних четырех десятилетий фокусируется все в большей степени на промышленных выбросах в атмосферу. В частности, внимание сфокусировано на парниковых газах, которые обладают способностью влиять на удерживание солнечного тепла в атмосфере, вызывая "парниковый эффект". Парниковый эффект происходит, когда тепло, поступающее от солнца, задерживается в атмосфере и гидросфере земли, увеличивая среднюю температуру воздуха, температуру океана и другие средние температуры планеты Земля, вплоть до температуры изменения климата и включая ее; данный эффект в целом рассматривается как влияние антропогенной деятельности на тепловой баланс Земли, хотя размеры и степень воздействия на это сжиганием материалов человечеством, а также пределы, направление и величина этого влияния находятся в процессе обсуждения. Несмотря на степень обсуждения, все согласны в том, что удаление CO2 (и других химикатов) из локальных источников эмиссии полезно, если затраты на выполнение этого достаточно малы.
Газы, вызывающие парниковый эффект, преимущественно образованы диоксидом углерода и производятся муниципальными электростанциями и электростанциями крупных промышленных предприятий, хотя они могут также производиться при любом обычном сжигании углерода (например, автомобилями, при очистке участков земли от тропического леса, простым горением и т.д.), однако места их наиболее концентрированных выбросов на планете связаны с электростанциями, что делает уменьшение или устранение выбросов из этих фиксированных мест привлекательным для привлечения технологии удаления. Поскольку производство энергии является первопричиной выбросов парниковых газов, то на протяжении последних тридцати лет интенсивно исследуются и изучаются такие способы, как уменьшение углеродоемкости, улучшение эффективности и отделение углерода от дымовых газов электростанций различными средствами.
Уменьшение углеродоемкости включает альтернативное применение неуглеродных источников энергии, таких как ядерные, гидроэлектрические, фотогальванические, геотермальные и другие источники электрической энергии, чтобы уменьшить процентную долю энергии, произведенной исключительно сжиганием углерода. Несмотря на то что эти методы выработки электроэнергии продолжают возрастать по отношению к общему производству электроэнергии, предполагаемые показатели мирового потребления электроэнергии, как ожидается, будут возрастать быстрее, чем производство электроэнергии этими методами. Поэтому ожидается, что выбросы углеродных парниковых газов будут увеличиваться, несмотря на развитие неуглеродных источников электроэнергии.
Улучшение эффективности обычно фокусировалось на методах улучшения сжигания углерода предварительным сжиганием, обезуглероживанием, сжиганием в кислороде и т.д., посредством первоначального уменьшения количества образованного CO2 и последующего окисления всех потенциальных загрязняющих веществ как можно более полным образом. К тому же, данный метод увеличивает количество энергии, генерируемой в расчете на эмиссию диоксида углерода, обеспечивая улучшение эффективности. Несмотря на то что успехи в этой области улучшили эффективность сжигания, еще остается потребность в дополнительных улучшениях в этой области.
Попытки связывания углерода (в первоначальной форме газообразного CO2) проводились многими различными методами, которые могут быть в общем классифицированы как геологические, наземные или океанические системы. Эти методы в основном относились к транспортировке образованного диоксида углерода к физическим местоположениям и инжекции диоксида углерода в геологические, грунтовые или океанические хранилища. Каждый из этих методов связывания включает большие затраты на приготовление CO2 к транспортировке, выполнение транспортировки и выполнение инжекции в "углеродное хранилище". Как таковые, эти методы в целом экономически не оправданы и во многих случаях потребляют больше энергии, чем первоначальный произведенный углерод.
Связывание может также включать некоторые промышленные процессы, которые включают процессы с применением очистки в скруббере, мембран, дешевого O2 и гидратов. Однако каждый из этих методов страдает тем, что капитальные затраты на оборудование возрастают до экономически невыгодных пределов, и чрезмерно высоко влияние захвата CO2 на стоимость электроэнергии.
Вышеупомянутые недостатки не предполагают полного их охвата, а, скорее, представляют часть из тех недостатков, которые влияют на эффективность известных методов удаления диоксида углерода из потоков отходов; однако тех, что упомянуты здесь, достаточно, чтобы продемонстрировать то, что методологии, имеющиеся в данной области, не вполне удовлетворительны, и что имеется значительная потребность в способах, описанных и заявленных в этом изобретении.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Варианты осуществления данного изобретения относятся к способам удаления первоначального количества диоксида углерода из газового потока, содержащих: получение гидроксида в водной смеси; получение хлора; смешивание гидроксида с газовым потоком, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего удаляется часть первоначального количества диоксида углерода из газового потока; объединение хлора с водой с образованием хлорноватистой кислоты; разложение хлорноватистой кислоты с образованием хлористоводородной кислоты и кислорода; и объединение хлористоводородной кислоты с карбонатом кальция с образованием хлорида кальция и уменьшенного количества диоксида углерода. В других вариантах осуществления способ также содержит получение водорода; и сжигание водорода на электростанции. В некоторых вариантах осуществления уменьшенное количество диоксида углерода является половиной от первоначального количества диоксида углерода. В другом варианте осуществления гидроксид является гидроксидом натрия.
Другие варианты осуществления данного изобретения относятся к способу удаления первоначального количества диоксида углерода из газового потока, содержащему: получение гидроксида в водной смеси; получение хлористоводородной кислоты; смешивание гидроксида с газовым потоком, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего удаляется часть первоначального количества диоксида углерода из газового потока. В некоторых вариантах осуществления способ также содержит получение водорода; и сжигание водорода на электростанции. В другом варианте осуществления уменьшенное количество диоксида углерода является половиной от первоначального количества диоксида углерода. В другом варианте осуществления гидроксид является гидроксидом натрия.
Другие варианты осуществления данного изобретения относятся к устройству, включающему: электролизную камеру, содержащую по меньшей мере один катод и по меньшей мере один анод, электролизная камера приспособлена для получения гидроксида, водорода и хлора во время применения; первую группу смесительного оборудования, соединенную с возможностью функционирования с электролизной камерой и с трубопроводом, приспособленным для протекания газового потока во время применения, смесительное оборудование приспособлено для смешивания гидроксида из электролизной камеры с газовым потоком во время применения, чтобы создать смесь, в которой соединения углерода, серы и/или азота в газовом потоке могут реагировать с гидроксидом; вторую группу смесительного оборудования, соединенную с возможностью функционирования с электролизной камерой и приспособленную для смешивания хлора с водой во время применения с образованием хлорноватистой кислоты; технологическое оборудование, приспособленное для разложения хлорноватистой кислоты, с образованием хлористоводородной кислоты и кислорода; третью группу смесительного оборудования, приспособленную для объединения хлористоводородной кислоты и карбоната кальция, с образованием хлорида кальция и диоксида углерода во время применения; и разделительную камеру, соединенную с возможностью функционирования со смесительным оборудованием и приспособленную для разделения смеси на отдельные газообразную фазу и твердотельную и/или жидкую фазу.
Другие варианты осуществления данного изобретения относятся к устройству, включающему: электролизную камеру, содержащую по меньшей мере один катод и по меньшей мере один анод, электролизная камера приспособлена для получения гидроксида, водорода и кислорода во время применения; первую группу смесительного оборудования, соединенную с возможностью функционирования с электролизной камерой и с трубопроводом, приспособленным для протекания газового потока во время применения, смесительное оборудование приспособлено для смешивания гидроксида из электролизной камеры с газовым потоком во время применения, чтобы создать смесь, в которой соединения углерода, серы и/или азота в газовом потоке могут реагировать с гидроксидом; камеру, соединенную с возможностью функционирования со стороной анода ячейки и приспособленную для разделения смеси на отдельные газообразную фазу и жидкую фазу; и камеру, соединенную с возможностью функционирования со стороной катода ячейки и приспособленную для разделения смеси на отдельные газообразную фазу и жидкую фазу.
Другие варианты осуществления данного изобретения относятся к устройству, включающему: электролизную камеру, содержащую по меньшей мере один катод и по меньшей мере один анод, электролизная камера приспособлена для получения гидроксида, при одновременном подавлении образования водорода посредством потребления кислорода во время применения; первую группу смесительного оборудования, соединенную с возможностью функционирования с электролизной камерой и с трубопроводом, приспособленным для протекания газового потока во время применения, смесительное оборудование приспособлено для смешивания гидроксида из электролизной камеры с газовым потоком во время применения, чтобы создать смесь, в которой соединения углерода, серы и/или азота в газовом потоке могут реагировать с гидроксидом; камеру, соединенную с возможностью функционирования со стороной анода ячейки и приспособленную для разделения смеси на отдельные газообразную фазу и жидкую фазу; и камеру, соединенную с возможностью функционирования со стороной катода ячейки и приспособленную для разделения смеси на отдельные газообразную фазу и жидкую фазу.
Другие варианты осуществления данного изобретения относятся к способу отделения тяжелых металлов от воды в конденсате дымовых газов от процесса, в котором диоксид углерода удаляется из газового потока на электростанции, включающему: получение хлоридной соли; смешивание соли с водой и/или паром, чтобы получить раствор; электролиз раствора, чтобы получить гидроксид и газообразный хлор; смешивание части гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; добавление части гидроксида к конденсату дымовых газов, чтобы изменить величину его pH с кислой на щелочную, что приводит к осаждению тяжелых металлов; и пропускание конденсата через фильтрующую среду. В некоторых вариантах осуществления фильтрующая среда содержит активированный уголь. В других вариантах осуществления конденсат пропускается под действием силы тяжести через фильтрующую среду. В еще одних вариантах осуществления конденсат активно прокачивается через фильтрующую среду.
Другие варианты осуществления данного изобретения относятся к способу отделения тяжелых металлов от воды в конденсате дымовых газов от процесса, в котором диоксид углерода удаляется из газового потока на электростанции, включающему: получение хлоридной соли; смешивание соли с серной кислотой и нагревание, чтобы получить раствор; испарение результирующей хлористоводородной кислоты из смеси; электролиз раствора сульфата, чтобы получить гидроксид и газообразный кислород; смешивание части гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; добавление части гидроксида к конденсату дымовых газов, чтобы изменить величину его pH с кислой на щелочную, что приводит к осаждению тяжелых металлов; и пропускание конденсата через фильтрующую среду. В некоторых вариантах осуществления фильтрующая среда содержит активированный уголь. В других вариантах осуществления конденсат пропускается под действием силы тяжести через фильтрующую среду. В еще одних вариантах осуществления конденсат активно прокачивается через фильтрующую среду. В еще одних вариантах осуществления кислород расходуется в электролизной ячейке, чтобы подавить образование водорода.
Другие варианты осуществления данного изобретения относятся к способу повторного использования газообразного хлора от процесса, в котором диоксид углерода удаляется из газового потока на электростанции, включающему: получение хлоридной соли; смешивание соли с водой и/или паром, чтобы получить раствор; электролиз раствора, чтобы получить гидроксид и газообразный хлор; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; реакционное взаимодействие газообразного хлора с водой и светом, чтобы получить хлористоводородную кислоту и кислород; и возврат кислорода к впускному отверстию для воздуха электростанции. В некоторых вариантах осуществления хлористоводородная кислота нейтрализуется ее реакционным взаимодействием с бикарбонатными продуктами элементов I группы, отделенными от смеси, чтобы получить хлоридную соль элемента I группы, воду и газообразный диоксид углерода. В других вариантах осуществления хлористоводородная кислота нейтрализуется ее реакционным взаимодействием с карбонатными продуктами элементов II группы, отделенными от смеси, чтобы получить хлоридную соль элемента II группы и газообразный диоксид углерода. В еще одних вариантах осуществления хлористоводородная кислота нейтрализуется ее реакционным взаимодействием с карбонатными продуктами элементов I группы, отделенными от смеси, чтобы получить хлоридную соль элемента I группы и бикарбонат элемента I группы. В еще одних вариантах осуществления реакция выполняется простым смешиванием. В еще одних вариантах осуществления реакция выполняется при прохождении через мембрану, и из кислотно-щелочной батареи, образованной таким образом, извлекается мощность постоянного тока.
Другие варианты осуществления данного изобретения относятся к способу получения хлористоводородной кислоты от процесса, в котором диоксид углерода удаляется из газового потока на электростанции, содержащему: получение хлоридной соли; смешивание соли с серной кислотой, чтобы получить раствор; испарение результирующей хлористоводородной кислоты из смеси; электролиз раствора сульфата, чтобы получить гидроксид и газообразный кислород; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока. В некоторых вариантах осуществления хлористоводородная кислота нейтрализуется ее реакционным взаимодействием с бикарбонатными продуктами элементов I группы, отделенными от смеси, чтобы получить хлоридную соль элемента I группы, воду и газообразный диоксид углерода. В других вариантах осуществления хлористоводородная кислота нейтрализуется ее реакционным взаимодействием с карбонатными продуктами элементов II группы, отделенными от смеси, чтобы получить хлоридную соль элемента II группы и газообразный диоксид углерода. В еще одних вариантах осуществления хлористоводородная кислота нейтрализуется ее реакционным взаимодействием с карбонатными продуктами элементов I группы, отделенными от смеси, чтобы получить хлоридную соль элемента I группы и бикарбонат элемента I группы. В еще одних вариантах осуществления реакция выполняется простым смешиванием. В еще одних вариантах осуществления реакция выполняется при прохождении через мембрану, и из кислотно-щелочной батареи, образованной таким образом, извлекается мощность постоянного тока. В еще одних вариантах осуществления кислород расходуется в электролизной ячейке, чтобы подавить образование водорода.
Другие варианты осуществления данного изобретения относятся к способу удаления диоксида углерода из газового потока на электростанции, содержащему: получение хлоридной соли; смешивание соли с водой и/или паром, чтобы получить раствор; электролиз раствора, чтобы получить гидроксид и газообразный хлор; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; в котором смешивание осуществляется в паре барботажных колонн, которые включают карбонатор, в котором образуется карбонат из гидроксида и диоксида углерода, и бикарбонатор, в котором образуется бикарбонат из карбоната. В некоторых вариантах осуществления бикарбонатор смочен и насажен, однако имеет по существу нулевой уровень жидкости, и соединен с жидкостным карбонатором. В других вариантах осуществления бикарбонатор и карбонатор оба смочены и насажены, однако имеют по существу нулевой уровень жидкости.
Другие варианты осуществления данного изобретения относятся к способу удаления диоксида углерода из газового потока на электростанции, включающему: получение хлоридной соли; смешивание соли с серной кислотой, чтобы получить раствор; испарение результирующей хлористоводородной кислоты из смеси; электролиз сульфата, чтобы получить гидроксид и газообразный кислород; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; в котором смешивание осуществляется в паре барботажных колонн, которые включают карбонатор, в котором образуется карбонат из гидроксида и диоксида углерода, и бикарбонатор, в котором образуется бикарбонат из карбоната. В некоторых вариантах осуществления бикарбонатор смочен и насажен, однако имеет по существу нулевой уровень жидкости, и спарен с жидкостным карбонатором. В других вариантах осуществления бикарбонатор и карбонатор оба смочены и насажены, однако имеют по существу нулевой уровень жидкости.
Другие варианты осуществления данного изобретения относятся к способу удаления диоксида углерода из газового потока на электростанции, включающему: получение хлоридной соли; смешивание соли с серной кислотой, чтобы получить раствор; осаждение результирующего сульфата из смеси при оставлении хлористоводородной кислоты; добавление осадка к водному раствору; электролиз раствора, чтобы получить гидроксид и газообразный хлор; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; в котором смешивание осуществляется в единственной барботажной колонне, в которой гидроксид преобразуется в верхней секции колонны в карбонат, который затем преобразуется в бикарбонат в нижней секции колонны.
Другие варианты осуществления данного изобретения относятся к способу удаления диоксида углерода из газового потока на электростанции, включающему: получение хлоридной соли; смешивание соли с водой и/или паром, чтобы получить раствор; электролиз раствора, чтобы получить гидроксид и газообразный водород; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; в котором отходящая теплота от электростанции используется для повышения температуры, при которой происходит электролиз, до температуры, при которой энергия, требующаяся для электролиза, равна теоретической максимальной энергии, которая может быть возвращена от газообразного водорода, полученного электролизом.
Другие варианты осуществления данного изобретения относятся к способу удаления диоксида углерода из газового потока на электростанции, содержащему: получение хлоридной соли; смешивание соли с серной кислотой, чтобы получить раствор; испарение результирующей хлористоводородной кислоты из смеси; электролиз раствора сульфата, чтобы получить гидроксид и газообразный водород; смешивание гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока; в котором отходящая теплота от электростанции используется для повышения температуры, при которой происходит электролиз, до температуры, при которой энергия, требующаяся для электролиза, равна теоретической максимальной энергии, которая может быть возвращена от газообразного водорода, полученного электролизом.
Термины "содержать" (и любая форма от "содержать", такая как "содержит" и "содержащий"), "иметь" (и любая форма от "иметь", такая как "имеет" и "имеющий"), "содержать в себе" (и любая форма от "содержать в себе", такая как "содержит в себе" и "содержащий в себе"), и "включать" (и любая форма от "включать", такая как "включает" и "включающий") являются глаголами-связками, допускающими изменения. В результате способ или устройство, которые "содержат" "имеют" "содержат в себе" или "включают" одну или несколько стадий или один или несколько элементов, обладают этими одной или несколькими стадиями или элементами, однако не ограничиваются обладанием этими одной или несколькими стадиями или элементами. Подобным образом, элемент устройства или способ, который "содержит" "имеет" "содержит в себе" или "включает" одну или несколько особенностей, обладает этой одной или несколькими особенностями, однако не ограничивается обладанием этими одной или несколькими особенностями. Термин "применение" должен интерпретироваться таким же образом. Таким образом, в качестве примера, стадия способа, которая включает "применение" определенной информации, означает, что по меньшей мере применяется указанная информация, однако это не исключает возможность того, что может быть также применена неуказанная информация. Кроме того, структура, которая сконфигурирована определенным образом, должна быть сконфигурирована по меньшей мере указанным образом, однако также может быть сконфигурирована таким образом или образами, которые не указаны.
Термины в единственном числе означают один или несколько, если только в данном описании ясным образом не указано иное. Термин "другой" определяется как по меньшей мере второй или больше. Термины "в основном" и "примерно" определяется как по меньшей мере близкий к данной величине (и включающий ее) или состоянию (предпочтительно в пределах 10% от величины, более предпочтительно в пределах 1% от нее и наиболее предпочтительно в пределах 0,1% от нее).
Как использовано в данном документе, термины "карбонаты" или "карбонатные продукты" обычно определяются как минеральные компоненты, содержащие карбонатную группу, CO3. Соответственно, термины охватывают как смеси карбонат/бикарбонат, так и компоненты, содержащие лишь карбонатный ион. Термины "бикарбонаты" и "бикарбонатные продукты" обычно определяются как минеральные компоненты, содержащие бикарбонатную группу, HCO3. Соответственно, термины охватывают как смеси карбонат/бикарбонат, так и компоненты, содержащие лишь бикарбонатный ион.
При образовании бикарбонатов и карбонатов с применением некоторых вариантов осуществления данного изобретения термин "соотношение ионов" относится к числу ионов натрия в продукте, разделенному на число атомов углерода, присутствующих в этом продукте. Соответственно, в отношении потока продукта, образованного чистым бикарбонатом (NaHCO3), может быть сказано, что он имеет "соотношение ионов" 1,0 (Na/C), в то время как в отношении потока продукта, образованного чистым карбонатом (Na2CO3), может быть сказано, что он имеет "соотношение ионов" 2,0 (Na/C). Более конкретно, в отношении бесконечного числа непрерывных смесей карбоната и бикарбоната может быть сказано, что они имеют соотношения ионов, изменяющиеся между 1,0 и 2,0.
В некоторых предпочтительных вариантах осуществления данного изобретения хлористоводородная кислота добавляется к хлориду натрия исходного соляного раствора хлорощелочной электролизной ячейки, обеспечивая протекание следующей реакции:
H2O+NaCl+aHCl+энергия → NaOH+(l/2+a/2)H2+(l/2+a/2)Cl2
В этом уравнении термин "a" определяется как "коэффициент протонирования", который представляет собой отношение протонов (ионов H+) к ионам натрия (ионам Na+).
Как использовано в данном документе, термин "связывание" применяется, как правило, в отношении способов или технологий, результат которых частично или полностью заключается в удалении CO2 из локальных источников выбросов и в хранении этого CO2 в некоторой форме, с тем, чтобы предотвратить его возврат в атмосферу. Применение этого термина не исключает рассмотрение любой формы описанных вариантов осуществления как методов "связывания".
Как использовано в данном документе, термин "экологическая эффективность" применяется как синоним термина "термодинамическая эффективность" и определяется как количество CO2, связанного посредством определенных вариантов осуществления данного изобретения в расчете на количество потребленной энергии (как представлено уравнением "∂CO2/∂E"). Связывание CO2 выражается в процентах от общего количества CO2, выпускаемого электростанцией; потребление энергии сходным образом выражается, исходя из общего потребления энергии электростанцией.
Как использовано в данном документе, термины "низковольтный электролиз" и "LVE" применяются в отношении электролиза при напряжениях ниже примерно 5 В.
Описания хорошо известных способов обработки, соответствующих компонентов и оборудования опущены, чтобы не препятствовать излишними деталями пониманию способов и устройств по данному изобретению. Описания способов и устройств по данному изобретению, включая приложения, являются примерными и неограничивающими. Определенные замены, модификации, добавления и/или перегруппировки, входящие в объем формулы изобретения, однако не указанные в прямой форме в этом описании, могут стать очевидными для специалистов в данной области, в том числе для обычных специалистов, на основании этого описания.
Другие особенности и связанные с ними преимущества станут очевидными при ссылке на представленное ниже подробное описание конкретных вариантов осуществления в сочетании с сопроводительными чертежами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Представленные ниже чертежи приведены в качестве примера и являются неограничивающими. Чертежи образуют часть данного описания и включены для дополнительной демонстрации определенных особенностей данного изобретения. Данное изобретение может быть лучше понято посредством ссылки на один или несколько из этих чертежей в сочетании с описанием иллюстративных вариантов осуществления, представленных в данном документе.
Фиг. 1 представляет собой схему технологического процесса, показывающую некоторые варианты осуществления данного изобретения.
Фиг. 2A показывает устройство для исследования основных особенностей одного из вариантов осуществления обезуглероживающей части данного изобретения.
Фиг. 2B показывает экспериментальные результаты абсорбции/конверсии.
Фиг. 2C показывает экспериментальные результаты абсорбции/конверсии.
Фиг. 2D представляет собой график, показывающий расстояние соприкосновения газ/жидкость (м, глубина текучей среды), необходимое для удаления 90% CO2.
Фиг. 2E представляет собой график, показывающий соотношение ионов в продукте в зависимости от процентной доли CO2, абсорбированного в экспериментальном реакторе.
Фиг. 3 представляет собой график, показывающий температурную характеристику для текучей среды внутри реакционной камеры при протекании реакции в течение указанного времени.
Фиг. 4 представляет собой график, представляющий исследование заводнения 5-футовой (1,524 м) колонны.
Фиг. 5 представляет собой график, показывающий типичные рабочие линии вольтамперных характеристик для разных величин pH анолита и температурных условий.
Фиг. 6 представляет собой блок-схему устройства, включающего реактор, в котором водород не утилизируется, в соответствии с вариантами осуществления данного изобретения.
Фиг. 7 представляет собой блок-схему устройства, включающего реактор, в котором водород утилизируется посредством возврата к топливному элементу постоянного тока, в соответствии с вариантами осуществления данного изобретения.
Фиг. 8 представляет собой график, показывающий процентную долю CO2, абсорбированного в барботажной колонне, в зависимости от глубины текучей среды и в зависимости от скорости газа на границе раздела при низких скоростях на границе раздела.
Фиг. 9A представляет собой график, показывающий теоретически максимальную абсорбцию CO2 и экспериментальные результаты, в соответствии с вариантами осуществления данного изобретения.
Фиг. 9B показывает допущения и расчеты для модели дымовых газов для электростанции с применением некоторых варианты осуществления данного изобретения.
Фиг. 9C показывает рабочую нагрузку декарбонатора и необходимость во вспомогательном каустике для электростанции с применением некоторых вариантов осуществления данного изобретения.
Фиг. 9D показывает нагрузку секции электролиза и требования для электростанции с применением некоторых вариантов осуществления данного изобретения.
Фиг. 9E показывает расчеты отходящей теплоты для электростанции с применением некоторых вариантов осуществления данного изобретения.
Фиг. 9F показывает расчеты энергетического баланса и экологической эффективности для электростанции с применением некоторых вариантов осуществления данного изобретения.
Фиг. 10 показывает экологическую эффективность различных смоделированных электростанций с применением некоторых вариантов осуществления данного изобретения.
Фиг. 11 представляет собой график, показывающий процентную долю энергии, сэкономленной для м2 площади нормализованной конструкции LVE.
ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Данное изобретение относится к процессам связывания, в которых диоксид углерода удаляется из потоков отходов и преобразуется в карбонатные и/или бикарбонатные продукты. Варианты осуществления способов и устройств по данному изобретению содержат один или несколько из следующих главных компонентов: (1) процесс водного обезуглероживания, посредством которого газообразный CO2 абсорбируется водной щелочной смесью и затем реагирует с гидроксидом, с образованием карбонатных и/или бикарбонатных продуктов; (2) процесс разделения, посредством которого карбонатные и/или бикарбонатные продукты отделяются от жидкой смеси; (3) процесс электролиза рассола или сульфата для получения гидроксида натрия, который применяется в качестве абсорбирующей текучей среды в процессе обезуглероживания; и (4) образование и применение побочных продуктов от процессов обезуглероживания и электролиза, включающих газообразный хлор, карбонат и бикарбонат натрия и газообразный водород. Каждый из этих главных компонентов поясняется более подробно ниже.
Различные варианты осуществления данного изобретения предоставляют преимущества по сравнению с имеющимися в данное время технологиями абсорбирования диоксида углерода из потоков отходов. Некоторые потенциальные преимущества, которые могут быть реализованы посредством данного изобретения, включают следующее.
В отличие от процессов, которые физически удаляют углерод в удаленное место, совместного образования в промышленном масштабе карбонатов и/или бикарбонатов натрия из хлорида натрия и диоксида углерода посредством синтеза непосредственным образом преобразует нежелательный газообразный диоксид углерода в химикаты на месте производства электроэнергии, потенциально устраняя расходы на транспортировку к месту связывания.
В отличие от других попыток обезуглероживания потоков дымовых газов, которые не поддаются модифицированию, варианты осуществления данного изобретения могут быть модифицированы для применения на существующих электростанциях, существенно уменьшая капитальные затраты, требующиеся для реализации обработки с обезуглероживанием. Кроме того, обработка с обезуглероживанием является масштабируемой и может быть выполнена в масштабах от опытного применения до применения в промежуточных масштабах и вплоть до полномасштабного производства посредством добавления дополнительных реакторных узлов.
В отличие от других процессов в данной области процесс обезуглероживания в определенных вариантах осуществления связывает диоксид углерода в экономически выгодные химикаты и одновременно производит полезные побочные продукты, такие как газообразный хлор, карбонат натрия и газообразный водород. Поскольку побочные продукты от процесса обезуглероживания экономически выгодны, то они компенсируют затраты на связывание и в системах, сконструированных надлежащим образом, делают процесс связывания сам по себе прибыльным.
Благодаря попутному процессу активной очистки эмитированных дымовых газов в скруббере в данном процессе активно удаляются промывкой другие нежелательные кислые загрязняющие вещества, такие как SOx, NOx, HgOx, и другие. Кроме того, процесс очистки газа в скруббере может приводить к улавливанию и/или захвату карбонатом натрия других компонентов и/или загрязняющих веществ в газовом потоке (например, золы от угля и т.п.), посредством чего они удаляются из газового потока.
Частные варианты осуществления данного изобретения содержат способ удаления диоксида углерода из газового потока, содержащий: получение гидроксида в водной смеси; смешивание гидроксида с газовым потоком, чтобы получить карбонатные продукты (определенные как продукты, содержащие карбонатную группу, CO3), бикарбонатные продукты (определенные как продукты, содержащие бикарбонатную группу, HCO3) или смесь карбонатных и бикарбонатных продуктов в образованной смеси; и отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока. Гидроксид может быть гидроксидом любого вида, включая, однако, не ограничиваясь ими, гидроксид натрия, гидроксид калия, гидроксид кальция, гидроксид магния и гидроксид алюминия. Обычным специалистам в данной области будет понятно, что возможно достижение сходного химического поведения и обезуглероживания при любом числе гидроксидов или смесей гидроксидов. В некоторых предпочтительных вариантах осуществления гидроксид является гидроксидом натрия.
В некоторых вариантах осуществления способ также включает контроль технологического процесса, чтобы получать в основном лишь карбонатные продукты или в основном лишь бикарбонатные продукты. В других вариантах осуществления способ также включает контроль технологического процесса, чтобы получать смесь карбонатных и бикарбонатных продуктов, такая смесь может содержать примерно X% карбоната и примерно Y% бикарбоната, при любой из следующих комбинаций X-Y: 1-99, 2-98, 3-97, 4-96, 5-95, 6-94, 7-93, 8-92, 9-91, 10-90, 15-85, 20-80, 25-75, 30-70, 35-65, 40-60, 45-55, 50-50, 55-45, 60-40, 65-35, 70-30, 75-25, 80-20, 85-15, 90-10, 91-9, 92-8, 93-7, 94-6, 95-5, 96-4, 97-3, 98-2 или 99-1.
В некоторых вариантах осуществления смешивание осуществляется в двух отдельных камерах, с одной камерой, применяемой, чтобы получить карбонатные продукты, и с другой камерой, применяемой, чтобы получить бикарбонатные продукты. В других вариантах осуществления смешивание осуществляется в барботажной колонне или в последовательности барботажных колонн. В еще одних вариантах осуществления отделение карбонатных и/или бикарбонатных продуктов от смеси включает процесс разделения осаждением при нагревании. В некоторых вариантах осуществления теплота для процесса отделения извлекается из теплообмена с поступающими дымовыми газами. Отделенный карбонат может быть в виде водной суспензии или в виде раствора гидроксида, карбоната и воды при разных концентрациях во время отделения, и в таком случае он затем может быть высушен посредством любого из многочисленных методов. В некоторых вариантах осуществления не требуется высушивание карбоната. Например, суспензия карбоната натрия может быть применена при обработке жесткой воды. Несомненно, специалистам в данной области известен широкий выбор видов применения карбоната, полученного способами по данному изобретению, например суспензионные смеси бикарбоната натрия и карбоната натрия могут быть суспендированы в цистерне для применения в различных видах производства детергентов, в производстве стекла в качестве флюса, а также, как указано выше, для обработки воды.
В некоторых вариантах осуществления способ также содержит транспортировку карбонатных продуктов в удаленное место связывания; объединение карбонатных продуктов с кислотой в ходе реакции нейтрализации, с образованием чистого диоксида углерода; и инжекцию диоксида углерода в углеродное хранилище. В других вариантах осуществления другие компоненты газового потока нейтрализуются и/или вовлекаются/захватываются в процессе образования карбоната, включая SOx, NOx и материал, содержащий ртуть.
В некоторых вариантах осуществления получение гидроксида содержит: получение соли; смешивание соли с водой и/или паром, чтобы получить раствор; и электролиз раствора, чтобы получить гидроксид. В других вариантах осуществления получение гидроксида содержит: получение соли; смешивание соли с серной кислотой и нагревание, чтобы получить раствор сульфата; испарение хлористоводородной кислоты дополнительной теплотой при оставлении сульфата элемента I группы; и последующий электролиз этого раствора сульфата, чтобы получить гидроксид. В некоторых вариантах осуществления раствор подвергается электролизу с применением напряжения примерно 5 В или более, в то время как в других вариантах осуществления раствор подвергается электролизу с применением напряжения менее чем примерно 5 В. В некоторых вариантах осуществления раствор подвергается электролизу с применением напряжения между 1 В и 5 В, включая примерно 1,5 В, примерно 2,0 В, примерно 2,5 В, примерно 3,0 В, примерно 3,5 В, примерно 4,0 В или примерно 4,5 В или же в любом интервале между любыми этими значениями.
В некоторых вариантах осуществления кислота добавляется к раствору перед его электролизом. Кислота может быть кислотой любого вида, которая может предоставлять протоны в раствор, включая, однако, не ограничиваясь ею, хлористоводородную кислоту. Обычным специалистам в данной области будет понятно, что возможно достижение сходного химического поведения и электролиза при любом числе кислот или смесей кислот. В некоторых предпочтительных вариантах осуществления кислотой является хлористоводородная кислота. В других вариантах осуществления количество кислоты, добавляемой к раствору, основывается на определении оптимального коэффициента протонирования, который обеспечивает наименьшую энергию для получения реагентов и наибольшую энергию, извлекаемую из продуктов.
В еще одних вариантах осуществления стадия электролиза выполняется в электрохимической ячейке, имеющей сторону католита и сторону анолита, и карбонатные и/или бикарбонатные продукты рециркулируются к стороне католита электрохимической ячейки. В других вариантах осуществления энергия, требующаяся для выполнения способа, пополняется отходящей теплотой, извлекаемой из потока дымовых газов.
Другие варианты осуществления изобретения содержат способ удаления диоксида углерода из газового потока, содержащий: получение гидроксида натрия в водной смеси; смешивание гидроксида натрия с газовым потоком, чтобы получить карбонат натрия, бикарбонат натрия или смесь карбоната и бикарбоната натрия; и отделение указанного карбоната и/или бикарбоната натрия от смеси, посредством чего диоксид углерода удаляется из газового потока.
В некоторых вариантах осуществления способ также включает контроль технологического процесса, чтобы получать в основном лишь карбонат натрия или в основном лишь бикарбонат натрия. В других вариантах осуществления способ также содержит контроль технологического процесса, чтобы получать смесь карбоната и бикарбоната натрия, такая смесь может содержать примерно X% карбоната натрия и примерно Y% бикарбоната натрия, при любой из следующих комбинаций X-Y: 1-99, 2-98, 3-97, 4-96, 5-95, 6-94, 7-93, 8-92, 9-91, 10-90, 15-85, 20-80, 25-75, 30-70, 35-65, 40-60, 45-55, 50-50, 55-45, 60-40, 65-35, 70-30, 75-25, 80-20, 85-15, 90-10, 91-9, 92-8, 93-7, 94-6, 95-5, 96-4, 97-3, 98-2 или 99-1.
В некоторых вариантах осуществления смешивание осуществляется в двух отдельных камерах, с одной камерой, применяемой, чтобы получить карбонат натрия, и с другой камерой, применяемой, чтобы получить бикарбонат натрия. В других вариантах осуществления смешивание осуществляется в барботажной колонне или в последовательности барботажных колонн. В еще одних вариантах осуществления отделение карбоната и/или бикарбоната натрия от смеси включает процесс разделения осаждением при нагревании. В некоторых вариантах осуществления теплота для процесса отделения извлекается из теплообмена с поступающими дымовыми газами.
В некоторых вариантах осуществления способ также содержит: транспортировку карбоната натрия в удаленное место связывания; объединение карбонатных продуктов с кислотой в ходе реакции нейтрализации, с образованием чистого диоксида углерода; и инжекцию диоксида углерода в углеродное хранилище.
В некоторых вариантах осуществления получение гидроксида натрия содержит: получение хлорида натрия; смешивание хлорида натрия с водой и/или паром, чтобы получить рассол; и электролиз рассола, чтобы получить гидроксид натрия и газообразный хлор. В других вариантах осуществления получение гидроксида содержит: получение соли; смешивание соли с серной кислотой и нагревание, чтобы получить раствор сульфата и хлорид водорода в виде газа, оставляющего раствор сульфата элемента II группы; и электролиз этого раствора сульфата, чтобы получить гидроксид. В некоторых вариантах осуществления рассол подвергается электролизу с применением напряжения примерно 5 В или более, в то время как в других вариантах осуществления он подвергается электролизу с применением напряжения менее чем примерно 5 В. В некоторых вариантах осуществления раствор подвергается электролизу с применением напряжения между 1 В и 5 В, включая примерно 1,5 В, примерно 2,0 В, примерно 2,5 В, примерно 3,0 В, примерно 3,5 В, примерно 4,0 В или примерно 4,5 В или же в любом интервале между любыми этими значениями.
В некоторых вариантах осуществления стадия электролиза выполняется в электрохимической ячейке, имеющей сторону католита и сторону анолита, и карбонат и/или бикарбонат натрия рециркулируются к стороне католита электрохимической ячейки. В других вариантах осуществления энергия, требующаяся для выполнения способа, пополняется тепловой энергией, извлекаемой из потока отходящего газа. В еще одних вариантах осуществления способ также содержит сбор газообразного хлора, в то время как в других производится газообразный водород. В некоторых вариантах осуществления газообразный водород и газообразный хлор сжигаются с образованием хлористоводородной кислоты, которая добавляется к рассолу перед его электролизом. В других вариантах осуществления газообразный водород сжигается с атмосферным кислородом или кислородом от исходных химикатов с образованием воды, в то время как в еще одних вариантах осуществления способы включают применение газообразного водорода для производства энергии. В некоторых вариантах осуществления отделение карбоната и/или бикарбоната натрия от смеси включает процесс разделения осаждением при нагревании, в котором теплота для процесса разделения извлекается из энергии, произведенной газообразным водородом, в то время как в других вариантах осуществления теплота поступает от энергии потока отходящего газа. В других вариантах осуществления газообразный водород сжигается совместно с углем, чтобы улучшить выбросы от сжигания угля, или применяется в процессе сжигания для возврата топливным элементом электричества постоянного тока.
В некоторых вариантах осуществления поток отходящего газа является потоком отработанных газов от станции, в то время как в других вариантах осуществления станция является электростанцией, в которой применяется источник топлива на базе углерода.
В некоторых вариантах осуществления поток отработанных газов содержит CO2 и H2O.
Частные варианты осуществления данного изобретения также включают устройство, содержащее: электролизную камеру, содержащую по меньшей мере один катод и по меньшей мере один анод, камера приспособлена для получения гидроксида во время применения; смесительное оборудование, соединенное с возможностью функционирования с электролизной камерой и с трубопроводом, приспособленным для протекания газового потока во время применения, смесительное оборудование приспособлено для смешивания гидроксида из электролизной камеры с газовым потоком во время применения, чтобы создать смесь, в которой соединения углерода, серы и/или азота в газовом потоке могут реагировать с гидроксидом; и разделительную камеру, соединенную с возможностью функционирования со смесительным оборудованием и приспособленную для разделения смеси на отдельные газообразную фазу и твердотельную и/или жидкую фазу.
В некоторых вариантах осуществления электролизная камера содержит мембранную, диафрагменную и/или ртутную ячейку. В некоторых вариантах осуществления смесительное оборудование является реактором периодического действия или последовательностью реакторов периодического действия, в то время как в других вариантах осуществления смесительная камера является узлом для абсорбции/реакционного взаимодействия газ/жидкость или последовательностью узлов для абсорбции/реакционного взаимодействия газ/жидкость. В других вариантах осуществления смесительная камера является кристаллизационной колонной или последовательностью кристаллизационных колонн, в то время как в других вариантах осуществления она является барботажной колонной или последовательностью барботажных колонн.
В некоторых вариантах осуществления устройство также содержит сушильную камеру, соединенную с возможностью функционирования с разделительной камерой и приспособленную для удаления жидкости из твердотельной и/или жидкой фазы во время применения, в то время как в других вариантах осуществления сушильная камера приспособлена для нагревания твердотельной и/или жидкой фазы во время применения. В еще одних вариантах осуществления устройство определено как соединенное с возможностью функционирования с электростанцией.
В некоторых вариантах осуществления электролизная камера приспособлена для получения газообразного хлора и гидроксида натрия из хлорида натрия и воды во время применения. В других вариантах осуществления смесительное оборудование приспособлено для смешивания гидроксида из электролизной камеры с диоксидом углерода из газового потока во время применения, чтобы получить карбонатные и/или бикарбонатные продукты.
В еще одних вариантах осуществления данное изобретение включает способ определения оптимального рабочего напряжения и тока электрохимической ячейки для функционирования при низком напряжении по отношению к увеличенной области, для заданной Вамперной характеристики заданном протонировании. В других вариантах осуществления изобретение включает способ определения более низкого термодинамического предела при рабочем напряжении для данной электролитической ячейки, применяемой в процессе. В некоторых вариантах осуществления предоставлен способ определения экологической эффективности (∂CO2/∂E) в целом для устройств, которые выполняют работу по удалению CO2 из потоков отходов, наряду с тем, что другие варианты осуществления включают способ определения экологической эффективности (∂CO2/∂E) специально для устройств, применяются в данном изобретении в любом из вариантов его осуществления. Другие варианты осуществления включают способ получения экстремально чистого газообразного водорода при малом влиянии на затраты, его стоимость соответствует извлекаемому энергосодержанию.
I. Обзор преимуществ
Подобно любому другому способу или устройству, которые функционируют для выполнения технических требований, многие варианты осуществления данного изобретения потребляют некоторое количество энергии для выполнения абсорбции CO2 и других химикатов из потоков дымовых газов и для выполнения других целей вариантов осуществления данного изобретения, как описано в данном документе. Однако одним из преимуществ определенных вариантов осуществления данного изобретения является то, что они предоставляют уровни экологической эффективности, превосходящие известный уровень техники, как поясняется в деталях в Примерах 5 и 6. Как это очевидно из данных в Примерах 5 и 6, увеличенное извлечение отходящей теплоты или энергии, не образующей газы, создающие парниковый эффект, для энергоснабжения процесса, применение низковольтного электролиза и улучшение возврата электрической энергии из утилизации энергии водорода могут дополнительно улучшить экологическую эффективность процесса, вплоть до того уровня (или даже выше него), когда процесс полностью снабжается энергией посредством извлечения и повторного использования отходящей теплоты (и извлечения энергии водорода), и обеспечивает абсорбцию практически 100% CO2, эмитированного электростанцией.
Кроме того, одним из преимуществ применения экстремальной химии в определенных вариантах осуществления данного изобретения заключается в том, что в процессе абсорбции слабокислого CO2 практически полностью абсорбируются сильные кислоты, SOx и NOx, а также, в меньшей степени, ртуть. Испытания с применением SOx/Ar и NOx/Ar в загружаемых одностадийных декарбонаторах показали удаление более 99% этих компонентов дымовых газов ("более 99%" означает, что присутствие любого загрязняющего вещества в случае обработки 14 л/мин дымовых газов не обнаруживалось в образованном потоке воздуха газовой хроматографией, т.е. загрязняющие вещества были практически удалены. В определенных вариантах осуществления данного изобретения попутная очистка газа в скруббере от NOx, SOx и соединений ртути может предполагать увеличенное экономическое значение; т.е. посредством применения вариантов осуществления данного изобретения угли, которые содержат большие количества этих соединений, могут быть сожжены на электростанции, в некоторых вариантах осуществления, при меньшем результирующем загрязнении, чем в случае более высокосортных углей, используемых без преимуществ процесса абсорбции CO2 в соответствии с некоторыми вариантами осуществления данного изобретения.
Кроме того, способность определенных вариантов осуществления данного изобретения к масштабированию может достигать крайних пределов; т.е., поскольку в некоторых вариантах осуществления процесс контролируется в отношении электрической мощности, этот расход электрической мощности может быть фактически масштабирован до уровня отдельных молекул абсорбента, созданных в любое заданное время. Также возможность точного определения количества абсорбированного CO2 является практичной и простой: определяется масса образованных карбонатных/бикарбонатных продуктов, измеряется соотношение в них ионов посредством анализа, выполняется расчет для определения числа абсорбированных молей CO2, и количество абсорбированного CO2 легко подтверждается и измеряется (фактор, который может оказаться выгодным в случае некоторых интенсифицированных режимов для удаления CO2 и других химикатов в дымовых газах).
Другим дополнительным преимуществом определенных вариантов осуществления данного изобретения, которое отличает их от других процессов удаления CO2, является то, что, при некоторой рыночной конъюнктуре, продукты обладают значительно большей стоимостью по сравнению с требующимися реагентами или полезной мощностью или амортизационными расходами на электростанцию. Иными словами, определенные варианты осуществления являются промышленными способами производства хлор-гидрокарбонатных продуктов с выгодой, наряду с тем, что осуществляется значительное удаление CO2 и попутных загрязняющих веществ, являющихся нежелательными. Все другие конкурентные способы захвата CO2 являются простым увеличением расходов на эксплуатацию.
II. Схема технологического процесса
Фиг. 1 изображает упрощенную схему технологического процесса, иллюстрирующую основные типичные варианты осуществления устройств и способов в соответствии с данным изобретением. Эта схема представлена лишь в иллюстративных целях и, соответственно, она лишь изображает характерные варианты осуществления данного изобретения и не предназначена для ограничения объема формулы изобретения каким-либо образом. Как показано на Фиг. 1, дымовые газы (FG) вводятся в процесс в месте 901, опционально после первоначального обмена отходящей теплотой с системой генерации постоянного тока на базе отходящей теплоты. Дымовые газы FG, вводимые в этом примере в качестве смеси газов при 300°C, первоначально направляются по трубе 902 в теплообменник дымовые газы/бикарбонат 903, в котором температура дымовых газов уменьшается в этом примере до 120-140°C. Подобным образом дымовые газы продолжают перемещение через теплообменник анолит/дымовые газы 904 и католитный теплообменник 905, при уменьшении температуры газов до 95°C, и затем через теплообменник вода/дымовые газы 929 с дополнительным уменьшением их температуры до 30°C. Дымовые газы, оставляющие теплообменник вода/дымовые газы 929, затем вводятся в клапанный узел, узел 931 контроля смешивания дымовых газов, в котором дымовые газы с температурой 30°C могут быть смешаны с дымовыми газами с температурой 120-140°C, также доставляемых в узел 931 контроля смешивания дымовых газов посредством трубы 906 для обработки горячих дымовых газов. Смеси дымовых газов с температурой в интервале 30-140°C могут быть затем дифференцированным образом введены в нижнюю часть колонны 907 карбонизации/абсорбции, которая может быть барботажной колонной с насадкой или без насадки, в которой газ индектируется или барботируется с тем результатом, что газ образует пузырьки, которые поднимаются через текучую среду и направляются к верхнему выпускному отверстию 908. В этом варианте осуществления частично или полностью обезуглероженная текучая среда затем инжектируется и проходит через колонну бикарбонизации/конверсии 909, поднимаясь в виде пузырьков через текучую среду в этой колонне, вытягивается дополнительно воздуходувкой и выталкивается в выпускное отверстие 910.
Текучая среда, применяемая в теплообменнике дымовые газы/бикарбонат 903, является бикарбонатом/карбонатом натрия и различными сульфатами, нитратами, ртутью и твердотельными частицами и аэрозолями, абсорбированными из дымовых газов в колоннах абсорбции/конверсии (907 и 909). Посредством соприкосновения с дымовыми газами, поступающими при 300°C, эта жидкая текучая среда нагревается до температур, достаточных для создания значительного давления водяного пара, образуя пар, когда текучая среда инжектируется в резервуар 911, который затем конденсируется в конденсаторе 912, в результате чего образуется дистиллированная вода, рециркулируемая в резервуар 913 для утилизации H2O и используемая далее, после любого требуемого кондиционирования, с образованием рассола в смесителе 914 для рассола. Текучая среда, применяемая в теплообменнике анолит/дымовые газы 904, является рассолом, изготовленным добавлением солей элементов группы 1 и группы 2 (в этом примере NaCl) к воде, либо поступающей из основного узла 915 подачи воды, либо поступающей частично или полностью из резервуара 913 для утилизации H2O. Этот рассол подкисляется добавлением газообразного HCl, абсорбированного водой, или от исходного химиката HCl, при управлении посредством контроллера pH 916 с обратной связью. Эта текучая среда циркулирует через анолитную секцию 917 электролизной ячейки 933. Подобным образом текучая среда, применяемая в теплообменнике католит/дымовые газы 905, является водным раствором NaOH, который циркулирует через католитную секцию 918 электролизной ячейки 933. Когда pH католита выходит за пределы минимальной величины pH (которая соответствует концентрации) в контрольной точке 919, то концентрированный NaOH доставляется в резервуар 920 для хранения гидроксида.
Текучая среда, применяемая в теплообменнике вода/дымовые газы 929, поступает из достаточно большого водяного резервуара при достаточно низкой температуре, чтобы выполнять теплообмен. В некоторых вариантах осуществления эта система теплообмена может быть применена в качестве системы "предварительного нагревания" для растворов бикарбоната/карбоната перед дальнейшим теплообменом в теплообменнике дымовые газы/бикарбонат 905. Кроме того, в некоторых вариантах осуществления резервуары, включающие основной узел 915 подачи воды, резервуар 937 для хранения H2O для теплообмена и резервуар 913 для утилизации H2O, могут быть частично или полностью объединены.
Протонированный рассол, циркулирующий через анолитную секцию 917 электролизной ячейки 933, подвергается воздействию процесса электролиза с образованием газообразного хлора, который отбирается и перемещается, для этого примера, посредством линии 921 для газообразного хлора в реактор 924 для получения гипохлорита натрия. Ионы натрия и ионы водорода (протоны) перемещаются через мембрану электролизной ячейки 933 в католитную секцию 918. При этом ионы натрия замещают ионы водорода в воде, обеспечивая возможность образования газообразного водорода, который отбирается в трубопровод 922 для поступающего чистого газообразного водорода и направляется в топливный элемент H2/O2 923, в котором он объединяется с атмосферным O2, чтобы генерировать электроэнергию постоянного тока, которая утилизируется в электролизной ячейке 933 в этом примере, и получить чистую воду, которая рециркулируется через контур 935 для отбора чистой воды 935 в резервуар 913 для утилизации H2O. Газообразный хлор, доставляемый в реактор 924 для получения гипохлорита натрия, приводится в соприкосновение (барботируется) через гидроксид натрия, доставляемый в реактор из резервуара 920 для хранения гидроксида. Получаемый в результате гипохлорит натрия отводится в резервуар и направляется на рынок или для дальнейшего применения в качестве исходного химиката. Некоторое количество хлора и образованный газообразный HCl, образованный (при применении сверхстехиометрического количества будет осуществляться непрерывное рециркулирование HCl, за исключением возмещаемых потерь) сжиганием в топливном элементе HCl 925, затем рециркулируется через линию 926 для возврата кислого газа с HCl в смеситель 914 для рассола.
Гидроксид, произведенный и сохраненный или же полученный из исходных химикатов и хранящийся в резервуаре 920 для хранения гидроксида, является абсорбирующей текучей средой, вводимой в колонну 907 карбонизации/абсорбции. Она затем проходит через колонну бикарбонизации/конверсии 909 и после этого направляется (в виде смеси бикарбоната/карбоната в воде) в теплообменник дымовые газы/бикарбонат 903. После удаления воды испарением полученная суспензия из концентрированного бикарбоната/карбоната направляется в резервуар 927 для конечного бикарбоната, из которого она может отбираться для дополнительной обработки или очистки или же она может быть направлена в хранилище или на рынок.
Каждый из общих компонентов устройств и способов в соответствии с данным изобретением, описанных выше и показанных на Фиг. 1, описан более подробно ниже.
III. Водное обезуглероживание (абсорбция) CO2 из потоков отходов и его конверсия в карбонат и бикарбонат
Как указано выше, в некоторых вариантах осуществления устройства и способы по данному изобретению применяют процесс водного обезуглероживания, в соответствии с которым газообразный CO2 абсорбируется водной щелочной смесью, в которой он затем реагирует с гидроксидом, с образованием карбонатных и бикарбонатных продуктов. Во многих вариантах осуществления данного изобретения, в отличие от других схем захвата/связывания, гидроксид натрия применяется в качестве основной абсорбирующей текучей среды. Гидроксид натрия в различных концентрациях известен как готовый абсорбент CO2. Когда диоксид углерода приводится в соприкосновение с водным раствором гидроксида натрия, то может быть образована совокупность продуктов в диапазоне от чистого бикарбоната натрия (NaHCO3) до чистого карбоната натрия (Na2CO3) и могут создаваться разные условия, которые будут смещать равновесие в том или другом направлении, даже к крайнему положению (или вблизи него) и к значительному концентрированию (посредством либо химии процесса, либо удалением воды различными средствами) и осаждению бикарбоната, карбоната или смешанному осадку, содержащему оба соединения.
Когда диоксид углерода приводится в соприкосновение с водным раствором гидроксида натрия, поведение текучей среды внутри реакционной камеры может быть аппроксимировано так, как представлено на Фиг. 3, когда реакция протекает в течение указанного времени. Две фазы изменения температуры соответствуют двум отличным реакционным режимам и идентифицируют их.
(1) Первоначальная фаза абсорбции, в которой CO2 легко абсорбируется. Способность текучей среды к абсорбции уменьшается, когда концентрация OH уменьшается, и абсорбция заканчивается и в отдельных случаях реверсируется, когда концентрация ионов OH истощена. Реакция является экзотермической на протяжении этой части и образует почти исключительно карбонат.
(2) Вторая фаза абсорбции, во время которой CO2 трудно абсорбируется. Прохождение дымовых газов через смесь не вызывает сколь-либо результативной абсорбции CO2 текучей средой, однако текучая среда существенно охлаждается посредством потерь тепла от испарения вследствие любого испарения воды, вследствие любых потерь CO2 с переходом в испаренное состояние и вследствие протекающих эндотермических реакций. Во время этой фазы карбонат натрия, уже образовавшийся в растворе, конвертируется в бикарбонат натрия, в соответствии со следующей требуемой результирующей стехиометрией:
Na2CO3(водн. р-р)+H2O(жидкая фаза)+CO2(водн. р-р)→2NaHCO3(водн. р-р)
Эта последовательность из первоначальной карбонизации и последующей бикарбонизации воспроизводимым образом может быть продемонстрирована посредством повторяющегося приведения в действие устройства по Фиг. 2A (как поясняется подробно в Примере 3) до пределов абсорбции текучей среды и после них при разных концентрациях абсорбента.
Две фазы отличаются характеристиками, показанными в таблице 1 ниже.
мическая
мическая
Несмотря на то что в вариантах осуществления данного изобретения может применяться одна и та же камера для осуществления этих двух процессов in situ, разная природа реакций позволяет предположить, что разделение реакций на две камеры и их раздельная оптимизация является более подходящим путем для предпочтительных вариантов осуществления. Независимо от "внутренней компоновки" передаточных узлов (т.е. степени периодичности против непрерывности, числа камер, резервуаров, ступеней и т.п.), данные фундаментальные два процесса происходят в этой последовательности при уровнях концентрации, достаточных для предоставления хорошей абсорбции.
Поэтому, поскольку некоторые варианты осуществления данных способов и устройств по данному изобретению могут быть с контролем технологического процесса, чтобы получать чистый или почти чистый бикарбонат натрия, в некоторых вариантах осуществления данного изобретения в связи с этим захватывается один атом углерода на один атом натрия, полученный электролизом, вместо ½ (улучшение в достигаемой экологической эффективности номинально в два раза (2X) по сравнению с образованием карбоната). Соответственно, количество энергии для электролиза и затраты на обработку, чтобы получить моль гидроксида, удваивали "нормальную" способность к абсорбции при применении для образования бикарбоната, по сравнению с эффективностью абсорбции/использования энергии при образовании карбоната.
В различных вариантах осуществления данного изобретения могут быть получены разнообразные соотношения концентраций бикарбонат/карбонат во всем диапазоне. В предпочтительных вариантах осуществления концентрации, температуры, давления расходы и т.п. параметры текучих сред могут быть отрегулированы, чтобы оптимизировать долю "применимого" абсорбированного CO2, чтобы оптимизировать образование бикарбоната.
В некоторых вариантах осуществления данного изобретения может регулироваться pH в текучей среде для абсорбирования (концентрация ионов OH) в качестве средства регулирования степени абсорбции CO2 и других газов. В некоторых предпочтительных вариантах осуществления может быть применена увеличенная концентрация солей/карбонатов, чтобы дополнительно способствовать реакции с образованием бикарбоната. Рыночная стоимость продуктов и экономические факторы могут предоставлять возможность функционирования для получения продукта, обогащенного карбонатом, в течение некоторого периода времени, затем продукта, обогащенного бикарбонатом, в течение другого периода времени и т.д., при средней для электростанции величине Na/C, затем образующей меру эффективности использования ионных компонентов, создаваемых для абсорбции/конверсии.
Посредством разделения двух процессов на две отдельные камеры и перехода между камерами в месте выпуска OH температура находится в статическом равновесии или падает, и изменяется ослабление абсорбции и способ, посредством которого устройство для обезуглероживания может быть выполнено конструктивно и оптимизировано. Специалисту в данной области будет понятно, что могут быть сконструированы периодические, псевдонепрерывные, непрерывные и т.п. версии этого простого двухстадийного процесса обезуглероживания.
Кроме того, при намерении выполнения абсорбции при минимально возможном расходе энергии во многих предпочтительных вариантах осуществления данного изобретения могут быть применены реакторы в виде барботажной колонны (с насадкой или без насадки, с горизонтальным потоком текучей среды или без него), которые по своей природе создают большую площадь соприкосновения жидкость/газ, чтобы способствовать массопередаче, из которой конструкция в целом извлекает выгоду посредством возможности использования ступеней малой высоты (3 м или меньше), которые тем не менее обеспечивают достижение абсорбции 90%+ при малом сопротивлении или давлении, преодолеваемом насосом, при подаче текучих сред, и поэтому сконструированы с большой горизонтальной площадью, чтобы достигнуть промышленного масштабирования (широких мелких ванн или эквивалентных резервуаров), опционально с горизонтальным перемещением, чтобы соответствовать непрерывному функционированию. Некоторые варианты осуществления данного изобретения могут применять контакторы газ-жидкость с различными другими конфигурациями, при условии, что эти устройства обеспечивают требуемое соприкосновение газа с жидкостью.
Фиг. 4 представляет исследование заводнения 5-футовой (1,524 м) колонны, в которой сопротивление составляет примерно 0,01 фунта/кв. дюйм (изб. давл.) (6,9 Па), плюс 1,52 фунта/кв. дюйм (изб. давл.) (10,5 кПа) напора, чтобы преодолеть давление текучей среды с глубиной 5 футов (1,524 м). Эти потери и другие затраты на сжатие, как предполагается, составляют менее 1% от базовых затрат на электростанцию менее чем на 1% и в качестве таковых рассматриваются как незначительные и не рассчитываются в примерах. Фиг. 4 подтверждает, что чрезвычайно низкие величины сопротивления на пути протекания текучей среды будут приводить к чрезвычайно низким затратам энергии на сжатие, и экологическая эффективность устройства не ухудшается вследствие избыточных затрат энергии на сжатие или обработку газа.
Экологическая эффективность вариантов осуществления представляемых способов и устройств улучшается посредством выполнения наименьшей работы, потенциально возможной для абсорбции CO2, и одним из факторов, который уменьшает эту эффективность, является степень сжатия, нагнетание текучей среды и воздуха, которое требуется для выполнения данного процесса. С этой целью, сконструированы абсорберы с эффективностью, увеличенной в два раза (способные к удалению 99% CO2 из поступающего потока дымовых газов, который содержит 60% CO2 в N2), чтобы функционировать с "короткими ступенями", которые предоставляют высокие степени абсорбции CO2.
Предпочтительные варианты осуществления данного изобретения применяют поверхность переноса жидкость-газ большой площади (барботажную колонну, с насадкой или без нее, или ее эквивалент в виде резервуаров со статической или перемещающейся текучей средой), чтобы достичь высокой степени абсорбции при малой высоте абсорбирующей текучей среды, понижая тем самым сопротивление, требующееся для приведения текучих сред в соприкосновение, и эта "конструкция с короткими ступенями" соответственно требует, чтобы широкие, короткие "ванны" или их эквиваленты в трубопроводах, желобах, резервуарах и т.д. были применены для эффективной абсорбции больших количество CO2.
Реакции обезуглероживания по данному изобретению в основном считаются относящимися к основному направлению промышленности, и все ссылки на них в литературе ограничиваются массопередачей. На практике, при применении колонн с насадкой или без насадки при значительной площади соприкосновения газа с жидкостью в способах абсорбции с подъемом пузырьков через текучую среду, реакция проявляется как имеющая малые ограничения в отношении массопередачи, или, иначе говоря, применение данного способа с барботажной колонной для приведения в соприкосновение жидкости и газа обеспечивает преодоление простым образом ограничений в массопередаче: барботирование через барботер при отсутствии насадки при расстоянии соприкосновения газ/жидкость лишь 30 см продемонстрировало создание мгновенных степеней абсорбции CO2 98%+ (см. Фиг. 2B и 2C, рассмотренные в Примере 3), и на протяжении существенных для промышленного масштаба периодов времени в 15-25 минут текучая среда способна обеспечивать в среднем абсорбцию 80%+. При этом практически не ограничивается массопередача, и практическое экспериментирование, даже при прогонах с простой загрузкой до прекращения процесса, демонстрирует быструю массопередачу при такой хемосорбции.
Три примера конструкции абсорбционных реакторов с высокой степенью абсорбции CO2/NaOH поясняются подробно в Примерах 1-3. Выводы, сделанные из Примеров 1-3, заключаются в том, что высокие скорости абсорбции при коротких ступенях NaOH доказывают свою пригодность и демонстрируют возможность удаления в промышленных масштабах высокой процентных долей поступающего CO2 при низком сопротивлении в резервуарах производственных размеров.
Подводя итог вышесказанному, определенные варианты осуществления данного изобретения, в отношении обезуглероживающей части способов и устройств, содержат одну или несколько из следующих отличительных черт:
(1) применение коротких стадий, чтобы достигнуть высоких скоростей абсорбции CO2 в фазе карбонизации реакции;
(2) отделение и обработка карбонизованной текучей среды в процессе бикарбонизации посредством продолжающегося соприкосновения с технологическим газом, содержащим CO2 (или другим газом, содержащим CO2, при концентрациях CO2 больше, чем парциальное давление CO2 после реформирования абсорбирующей текучей средой);
(3) выполнение последовательности технологических операций, которые могут быть применены, посредством регулирования параметров процесса и концентрации, чтобы получить чистый бикарбонат, чистый карбонат и различных их смеси; и
(4) варианты осуществления данного изобретения могут иметь такую эффективность, что предоставляют соотношение натрий/абсорбированный углерод 1:1; это оптимизирует количество абсорбированного CO2 в расчете на энергиию в кВт·ч (вариант экологической эффективности, (∂CO2/∂E)), использованную при производстве реагента.
IV. Отделение продуктов
Как указано выше, в некоторых вариантах осуществления устройства и способы в соответствии с данным изобретением применяют процесс отделения, посредством которого карбонатные и бикарбонатные продукты отделяются от жидкого раствора. Отделение продуктов от жидкого раствора требует сложного процесса. Образование кислого карбоната натрия (NaHCO3 или бикарбоната натрия) и карбоната натрия (Na2CO3 или кальцинированной соды) при равновесном состоянии в жидкой фазе с гидроксидом натрия (NaOH или каустической содой) происходит в широком интервале температур и давлений и предоставляет разные конечные точки равновесия, заданные разными парциальными давлениями CO2. Посредством регулирования концентрации основания, температуры, давления, размера реактора, глубины текучей среды и степени карбонизации может быть вызвано протекание осаждение карбоната и бикарбоната. В качестве варианта, карбонатные/бикарбонатные продукты могут быть в некоторых предпочтительных вариантах осуществления отделены от содержащейся в них воды посредством обмена тепловой энергией с поступающими дымовыми газами. Кроме того, вследствие постоянной разности в растворимости между карбонатом натрия и бикарбонатом натрия могут быть достигнуты определенные неочевидные моменты при обработке; например, одна из специфических особенностей равновесия карбонатов натрия в определенных щелочных растворах заключается в том, что воздействие тепла способствует осаждению твердотельного вещества; соответственно, при определенных условиях карбонаты проявляют способность к самоосаждению из водных растворов при высокой чистоте (93%+).
В качестве альтернативы, в определенных вариантах осуществления теплота для процесса отделения может быть получена из водорода, произведенного при первоначальном электролизе, или посредством использования отходящей теплоты, содержащейся в потоке поступающих дымовых газов. Процесс кристаллизации по своей природе очищает кристаллизующийся минеральный материал посредством хорошо известного процесса кристаллизации.
Выходящие потоки жидкости, в зависимости от конструкции реактора, могут включать воду, NaOH, NaHCO3, Na2CO3 и другие растворенные газы в различном равновесном состоянии. Растворенные выпускаемые компоненты в следовых количествах, такие как H2SO4, HNO3 и Hg, также могут быть обнаружены. В одном из вариантов осуществления, чтобы разделить/удалить выходящие потоки жидкости, например, для удаления/отделения воды от карбонатов (в этом смысле слова "карбонаты" означают смеси карбоната и бикарбоната, возможно с присутствующими также гидроксидами; любой метод отделения, примененный к любой такой смеси, включает, вероятно, добавление тепловой энергии, чтобы испарить воду из смеси), вода может быть доведена до кипения с испарением воды при применении ребойлера 106, показанного на Фиг. 6. В качестве альтернативы, оставление частично основного раствора (например, NaOH при концентрации примерно 1М) и последующее нагревание раствора в отдельной камере может вызывать осаждение сравнительно чистого Na2CO3 в сборном резервуаре и рециркулирование остающегося NaOH назад в реактор 200. В других вариантах осуществления чистый карбонат, чистый бикарбонат и их смеси в равновесных концентрациях и/или в виде суспензии или в концентрированной форме могут периодически перемещаться в цистерну. В других вариантах осуществления потоки жидкости могут быть перемещены в испарительные резервуары/области, в которых жидкость, такая как вода, может быть удалена испарением.
При ссылке на Фиг. 6, показанная конструкция реактора может извлекать энергию, скрытую в водороде, полученном электролизом, в качестве топлива для сгорания, газа для бойлера или в топливных элементах H2/O2. Реактор 200 может быть использован для функционирования в стационарном режиме, при котором NaOH и NaHCO3 могут производиться в пропорции примерно 50:50. Газообразный водород, произведенный при первоначальном электролизе, может быть применен для производства тепла, и NaHCO3 может быть осажден в разделительной камере 108 при отводе остающегося NaOH в реактор 200. Суспензия из разделительной камеры 108 может быть подана в камеру 110 для обработки воды, которая может быть связана с разделительной камерой 108. В качестве альтернативы, суспензия может быть сохранена и затем, при необходимости, подаваться в камеру 110 для обработки воды.
Фиг. 7 иллюстрирует другую конструкцию реактора в соответствии с вариантом осуществления данного изобретения. В частности, Фиг. 7 показывает повторное захватывание некоторой избыточной энергии, применяемой для образования водород в качестве побочного продукта. Совместное применение высокоэффективного топливного элемента на месте эксплуатации может предоставить возможность рекуперации постоянного тока, который может быть использован для приложения и отчасти для подачи в качестве тока для электролиза. Смесительная камера 300 предоставляет смесь, включающую, однако, не ограничиваясь ими, NaOH, NaHCO3 и NOx, SOx и Hg в разделительную камеру 308. Разделительная камера 308 может разделять смесь на твердотельную и/или жидкую фазы посредством приложения тепла к смеси. Сушильная камера (не показана) разделительной камеры 308 может удалять жидкости из твердотельной и/или жидкой фазы во время процесса посредством обеспечения теплом. Результирующая разбавленная форма NaOH предоставляется в бойлер 306, который переводит кипением разбавленный NaOH в концентрированную форму и предоставляет концентрат в смесительную камеру 300 через контур возврата. Вода из бойлера 306 может быть предоставлена в электролизную камеру 302, в частности в смеситель 302A для рассола. Результирующий продукт Na2CO3/NaHCO3 (суспензия) из разделительной камеры 308 может быть направлен для коммерческого применения. В одном из вариантов осуществления суспензия карбоната может быть непосредственным или косвенным образом (например, посредством сохранения NaHCO3 для последующего использования в процессе, таком как обработка жесткой воды) предоставлена в установку 310 для обработки воды. В качестве альтернативы, NaHCO3 может быть затем очищен, высушен, отгружен и предоставлен для других видов промышленного применения.
Высвобождение газообразных продуктов включает принятие во внимание концепции безопасности выпуска NaOH или его компонентов, т.е. выпуска "щелочного дождя" электростанцией следует избегать, так же как и выпуска "кислотного дождя". Однако гидроксид натрия обычно используется как элемент очистки в скруббере для продуктов от электростанции и допущен к применению EPA. Обращение с гидроксидом натрия, так же как и процедуры устранения высвобождения щелочи хорошо, известны в данной области. Например, простой и недорогой конденсатор/узел возврата может предотвращать любую существенную эмиссию NaOH в газообразные выбросы.
В способе отделения карбоната осаждением в соответствии с некоторыми вариантами осуществления данного изобретения, карбонат в равновесном состоянии стерически связывает диоксид углерода и абсорбирует газ при соприкосновении с ним, при по существу мгновенной конверсии в карбонатный ион. Цепь реакций может лимитироваться массопередачей, так что, когда диоксид углерода абсорбирован основанием, последующие ионные реакции происходят быстрым образом.
Равновесное состояние карбоната натрия имеет характеристику, в соответствии с которой при повышении температуры Na2CO3 естественным образом осаждается и собирается, что делает возможным его отбор в качестве суспензии, при содержании некоторой доли NaOH в данной суспензии. В одном из вариантов осуществления обработка этой суспензии с просачиванием некоторого количества влажного хлора, произведенного в цикле с хлором, может быть применена для снижения содержания NaOH образованием незначительного количества NaCl в NaHCO3 при уровнях, которые соответствуют или меньше уровней для карбоната натрия, произведенного разработкой подземных месторождений минерала "трона" или отложений. Как таковое, равновесное состояние карбонат натрия/каустик обеспечивает полное перемещение углерода из газа в жидкость и в твердое вещество. В других вариантах осуществления может оказаться выгодным применение контура для карбоната в качестве среды для сбора суспензии золы, гидроксида натрия и других различных карбонатов и примесей и отгрузки суспензии в качестве материала для дорожного основания.
V. Электролиз для производства абсорбирующей текучей среды при низких энергиях
Как указано выше, в некоторых вариантах осуществления устройства и способы в соответствии с данным изобретением используют электролиз рассола для производства гидроксида натрия, который применяется в качестве абсорбирующей текучей среды в процесс обезуглероживания. Электролиз рассола является электрохимическим процессом, применяемым главным образом в производстве концентрированного гидроксида натрия (каустической соды) и газообразного хлора и обычно описываемым в литературе, относящейся к данному вопросу, следующим уравнением:
2 NaCl+2 H2O+e- → 2 NaOH+H2(газ)+Cl2 (газ)
Электролиз рассола может быть выполнен посредством трех основных видов стандартных электролизных ячеек: диафрагменными, ртутными и мембранными ячейками. Каждый из этих видов ячеек производит одни и те же выходные продукты из одним и тех же реагентов на входе. Они отличаются один от другого в основном тем, каким образом реагенты и продукты отделяются одни от других.
В одном из вариантов осуществления может быть применена мембранная ячейка по следующим нескольким причинам. Во-первых, озабоченность в отношении охраны окружающей среды, связанная с ртутью, уменьшила потребность в ртутных ячейках. Во-вторых, диафрагменные ячейки могут производить сравнительно слабощелочной продукт, который содержит значительные концентрации соли и хлоридных ионов и требует существенной последующей повторной обработки/отделения, чтобы удалить значительное содержание соли из каустика. В-третьих, прогресс в области технологии фторсодержащих полимеров увеличил срок службы и электрическую эффективность мембранных ячеек, при этом на рынке производителей обычно гарантируется срок службы, превышающий 5 лет. Кроме того, эффективности, выражаемые в мощности на тонну каустика, превышают их величины для диафрагменных и ртутных ячеек в предпочтительных видах реализации на практике.
Узлы для обработки с мембранной ячейкой характеризуются, однако без ограничений, следующими загрузками и продуктами в обобщенном виде:
Анод: NaCl+2275 кВт·ч/тонну Cl2 → Cl2 (газ)
↓
Катод: H2O ввод + e- → NaOH + H2(газ)
Ионы натрия проходят через мембрану или диафрагму и перемещаются из стороны анода к стороне катода. Вода потребляется на стороне катода, чтобы высвободить водород и образовать гидроксид.
Следует заметить, что требуемая мощность (например, 2275 кВт·ч/тонну хлора) может зависеть от конструкции индивидуальной электролизной ячейки. Соответственно, требуемые величины могут изменяться.
Многие предпочтительные варианты осуществления могут применять мембранные ячейки для выполнения этой функции. Мембранные ячейки обладают несколькими преимуществами по сравнению с другими процессами для электролиза рассола. Во-первых, мембранные ячейки не содержат и не производят каких-либо опасных для окружающей среды веществ (например, ртути) и являются электрически эффективными по сравнению с диафрагменными и ртутными ячейками. Они также используют контур с концентрированным/разбавленным/пополняемым NaCl, так что они могут хорошо подходить для применения в качестве узла непрерывной обработки "соляного контура". Далее, NaOH, произведенный в мембранных ячейках, без дополнительного испарения/концентрирования может иметь естественный подходящий уровень концентрации для применения в процессе обезуглероживания (например, 30-33% NaOH по массе). Кроме того, водород, произведенный мембранными ячейками, является "чистым", примерно уровня "для электронной промышленности", и относительно свободен от NaCl или других загрязнений. В качестве такового, водород может быть сжат и перемещен в резервуары в качестве газообразного H2 класса "для электронной промышленности", применяемого для производства электроэнергии на месте использования, например, в качестве горючей смеси с низкосортным углем или для получения технической выгоды от сжигания. В качестве варианта, водород может быть применен в качестве топлива для бойлера для процессов отделения, которые могут выполняться после обезуглероживания. Технология с применением мембранных ячеек также может быть легко масштабирована от лабораторного уровня до заводского производства посредством добавления небольших дополнительных узлов. Кроме того, газообразный хлор, произведенный посредством мембранного процесса, менее "влажный" по сравнению с тем, что произведен другими стандартными электролитическими процессами. По существу, цикла с одной ступенью сжатия может быть достаточно для производства хлора класса для обработки воды.
Рассмотренное выше представляет опубликованное в литературе и осуществленное на практике состояние в данной области, как это обычно выполняется с производством газообразного хлора и каустической соды в качестве конечных коммерческих продуктов. Однако цели определенных вариантов осуществления данного изобретения отличаются в некоторых отношениях, что приводит к отличающимся химическим методикам, применяемым для другого конечного результата определенных вариантов осуществления данного изобретения.
Дополнительные варианты осуществления базируются на электролизе сульфата. При электролизе сульфата соль смешивается с концентрированной серной кислотой и нагревается, чтобы получить сульфат натрия и газообразный хлорид водорода. Хлорид водорода высвобождается из раствора в виде газа вместе с некоторым количеством воды раствора посредством испарения. Затем этот хлорид водорода конденсируется непосредственным образом в виде концентрированной хлористоводородной кислоты в качестве продажного продукта. Раствор сульфата натрия раствор затем подвергается электролизу в электрохимической ячейке, как это описывается следующими уравнениями:
2NaCl+H2SO4+теплота→Na2SO4(водный раствор)+2HCl(газ)
Na2SO4+2H2O+e-→2NaOH+H2SO4+2H2+O2
Первое уравнение выше описывает конверсию хлоридной соли в сульфат элемента I группы. Второе уравнение выше описывает то, что серная кислота воспроизводится во время этапа электролиза. Таким образом, серная кислота функционирует в химической петле двух этапов. В целом, серная кислота является катализатором, который предоставляет возможность преобразования соли и воды в хлористоводородную кислоту и полезные побочные газы.
Как и при электролизе рассола, имеется несколько видов конструкции электрохимической ячейки, из которых более обычными являются мембранная ячейка и диафрагменная ячейка. Оба вида химических ячеек функционируют в соответствии со следующей парой химических уравнений:
Анод: Na2SO4+e-→H2SO4+O2(газ)
Катод: H2O+e-→NaOH+H2(газ)
Таким образом, серная кислота действует в петле, захватывая металлические ионы из соли, таким образом, что электролиз может быть выполнен при меньших затратах энергии по сравнению с электролизом рассола, и затем серная кислота восстанавливается во время этапа электролиза. В дополнение к этому, вместо образования газообразного хлора (Cl2) образуется хлористоводородная кислота (HCl) в качестве конечного продукта. Газообразный водород и газообразный кислород являются ценными конечными продуктами, или они могут быть потреблены на заводе, чтобы получить обратно содержащуюся в них энергию и компенсировать потребление мощности этим процессом. Кроме того, водород и кислород, произведенные мембранными ячейками, являются "чистыми", примерно уровня "для электронной промышленности", и почти полностью свободными от NaCl, серной кислоты или других загрязнений. В качестве такового, водород и кислород могут быть сжаты и перемещены в резервуары в качестве газообразных H2 и O2 класса "для электронной промышленности", применяемых для производства электроэнергии на месте использования, например, в качестве горючей смеси с низкосортным углем или для получения технической выгоды от сжигания. В качестве варианта, водород может быть применен в качестве топлива для бойлера для процессов отделения, которые могут выполняться после обезуглероживания. Технология с применением мембранных ячеек также может быть легко масштабирована от лабораторного уровня до заводского производства посредством добавления небольших дополнительных узлов.
В дополнительных вариантах осуществления кислород, высвобождающийся на этапе электролиза сульфата, может быть рециркулирован к газодиффузионному электроду на стороне катода, чтобы подавить образование водорода (в виде газа) и таким образом исключить образование газообразного водорода. Это устраняет потребление энергии, требующейся для производства водорода и сопутствующей необходимости конвертирования высвобожденного водорода назад в энергию.
A. Применение методик низковольтного электролиза
В некоторых вариантах осуществления данного изобретения электролиз рассола включает методы низковольтного электролиза (LVE), посредством чего улучшается термодинамическая эффективность использования энергии процессом. Определенные варианты осуществления данного изобретения не производят исключительно каустическую соду в качестве конечного продукта, а вместо этого применяют NaOH главным образом в качестве промежуточного абсорбента, чтобы абсорбировать CO2 из дымовых газов перед их выпуском в окружающую среду. Поскольку бизнес, связанный с хлорощелочным производством, обычно включает доставку каустической соды от завода-изготовителя в месту применения, то перемещение больших количество воды в каустической соде является неэкономичным, так что каустик обычно концентрируется до примерно 55 масс.% для транспортировки в виде жидкости посредством энергоемкого удаления воды испарением пара, и в некоторых случаях, он концентрируется до безводного твердотельного состояния, обычно в виде гранул. Эта концентрация достигается, как правило, функционированием электролизных ячеек при напряжениях выше 5 В (так сказать, "при значительном перенапряжении"), что обусловливает достижение вышеуказанных 30-35% NaOH, после чего следует цикл с испарением воды, чтобы достичь 55% (или полностью высушить продукт до безводного, гранулированного состояния и т.д.).
Большинство вариантов осуществления данного изобретения не транспортируют NaOH в качестве продукта, и он может быть произведен в применимых концентрациях (в виде водной абсорбирующей текучей среды) при напряжениях значительно ниже стандартных 5 В и более, применяемых при работе хлорощелочного агрегата. Влияние выполнения LVE на термодинамическую эффективность данного изобретения не может быть переоценено или завышено, поскольку потребляемая мощность точно соответствует простому уравнению постоянного тока:
P=V (напряжение) ·I (ток) · (эффективность по току)
Поскольку ток (I) фиксирован посредством электрохимического процесса (одна пара электронов для каждой молекулы и т.д.), то мощность почти полностью регулируется напряжением (V), требующимся для электролиза (дополнительным значительным фактором является эффективность по току, которая также является функцией приложенного напряжения). Поскольку варианты осуществления данного изобретения выполняют LVE при напряжениях, легко демонстрируемых в ячейках электролиза рассола посредством изменения рабочих условий, таких низких, как 2,15 В, посредством модификаций процесса и геометрических модификаций стандартной электрохимической мембранной ячейки, варианты осуществления данного изобретения потребляют значительно меньшую мощность (кВт·ч) для любого количества образующегося NaOH по сравнению с традиционным хлорощелочным электролизом при высоком напряжении. По этим причинам предпочтительные варианты осуществления данного изобретения включают узлы для электролиза, которые сконструированы для использования всех подходящих технических приемов, чтобы функционировать при низком напряжении, включая, однако, не ограничиваясь ими: функционирование при узком зазоре, повышенное давление, повышенная температура, мембраны большой площади, измененные концентрации анолита и католита и коэффициенты протонирования для ионов. Другие аспекты LVE поясняются подробно в Примере 4.
Энергия, требуемая для конвертирования хлоридной соли элемента I группы в гидроксид I группы, является значительной, и это, в свою очередь, вызывает потребность как в средстве, чтобы избежать какого-либо потребления энергии сверх термодинамически минимальной энергии при электролизе, так и конвертировании побочных продуктов снова в электрическую энергию. Варианты осуществления электролиза сульфата используют тепло из дымовых газов в качестве большой доли энергии реакции. Таким образом, потребление непосредственно самой энергии от мощности станции изменяется от потребления из ценного источника энергии, электричества, к потреблению энергии от источника, рассматриваемого как отходы мощности станции, из теплоты отходных газов. Соответственно варианты осуществления с сульфатом являются более предпочтительными.
B. "Точка безразличия" в отношении применения водорода
Типичный хлорощелочной процесс производит газообразный водород, который сжигается на месте в качестве топлива для бойлера для испарения воды (см. выше), или во многих случаях его образование подавляется применением воздушного электрода; например, узла, который вдувает воздух, содержащий кислород, к катоду, вызывая немедленное протекание восстановительной реакции:
H2(газ)+ 1/2O2(газ) → H2O(жидкость/газ),
которая изменяет электрохимические суммирование энергий и понижает напряжение, необходимое для производства каустика и хлора (в некоторых случаях до такого низкого, как 2,8 В, как указано в различных литературных источниках), за счет отсутствия производства водорода. Преимуществом таких предпочтительных вариантов осуществления данного изобретения является то, что они не нуждаются в водороде в качестве топлива для бойлера для испарения воды.
Некоторые варианты осуществления данного изобретения могут включать процесс с "воздушным электродом", который подавляет образование водорода (и уменьшает до нуля возможность извлечения энергии из такого водорода), однако многие предпочтительные варианты осуществления используют образование водорода либо для возврата энергии, либо в качестве химического сырья для других процессов.
Станции с применением определенных вариантов осуществления данного изобретения поэтому имеют "точку безразличия" в отношении применения водорода, произведенного таким образом; т.е. станция производит водород для возврата его энергии (например, 60% его энергосодержания в случае данного примера), и это количество энергии имеет определенную экономическую ценность, и, вместо использования водорода для возврата энергии, водород может быть обменен в качестве товара или продан за сумму, равную экономической ценности электрической энергии самой по себе или превышающую ее. Таким образом, станции этого типа представляют собой, так сказать, "водородную скважину". Водород производится и потребляется по причине его ценности в электрическом отношении, и любая потребность в водороде для других целей нуждается лишь в обмене этой электрической ценности или ее экономического эквивалента, чтобы поддержать экономику процесса. Этот вариант осуществления предоставляет выгодные последствия для будущих схем "водородной экономики": наличие готового источника водорода, доступного при стоимости, не зависящей от цены, ниже его внутреннего энергосодержания, может оказаться полезной и выгодной особенностью этой технологии.
C. Применение методов оптимизации протонированного рассола
Определенные варианты осуществления данного изобретения намеренно оптимизируют образование водорода вместо его подавления, посредством представленной ниже оптимизации протонированного рассола. Обычная хлорощелочная индустрия применяла, в некоторых случаях, добавление HCl в форме хлористоводородной кислоты к рассолу (NaCl) в анолитной камере. Это "протонирование" рассола оказывает действие, выражающееся в снижении напряжении, требующегося для производства заданного количества каустика, и уменьшает мощность, требуемую для изготовления реагента/абсорбента в определенных вариантах осуществления данного изобретения. В технической литературе, относящейся к хлорощелочному производству, причина этого эффекта снижения напряжения приписывается "нейтрализации NaOH, который возвращается через мембрану", процессу, который изучался по отношению к селективности мембраны и т.д. и является хорошо понятым. Вообще говоря, эта "нейтрализация" представляется как производящая лишь соленую воду [NaOH (возвращающийся) + HCl (анолит) → NaCl + H2O] и не показана как изменяющая стехиометрию продуктов. Однако одним из моментов, который недостаточно хорошо понят или разработан в данной области, является то, что добавление HCl по существу несомненно изменяет стехиометрию уравнения следующим образом:
NaCl+aHCl+H2O→NaOH+(l/2+a/2)H2+(1/2+a/2)Cl2
Это дополнительное количество произведенного водорода и хлора представляет особый интерес для данного изобретения, поскольку некоторые варианты осуществления данного изобретения зависят от извлечения энергии из водорода (которое улучшается, когда производится больше водорода, и более экономично, когда производится больше газообразного хлора, в расчете на моль произведенного абсорбента NaOH). То, что это дополнительное количество водорода для извлечения энергии и хлора для продажи производится в то время, когда общее электрическое напряжение (и, следовательно, мощность и затраты) понижено, приводит определенные варианты осуществления данного изобретения к оптимизации величины "a" для наименьшей энергии для производства реагентов и наибольшей энергии, извлекаемой из продуктов. Оптимум обычно находится между 0,5 и 1,0M HCl в растворе NaCl(водн. р-р). Однако оптимизация является специфической для каждой конструкции ячейки, геометрии, концентрации, температуры и давления режима. Однако для каждой электрохимической ячейки имеется оптимум коэффициента протонирования ("a"), при котором функционирование выполняется при наименьшей энергии. На практике, чрезвычайно высокие величины "a" (>0,15M при 90°C, например) будут, возможно, вызывать немедленное образование пузырей в большинстве коммерчески доступных мембран. Несомненно, несмотря на то что HCl является предпочтительной кислотой для протонирования рассола в данном изобретении, многие другие кислоты могут быть использованы, чтобы протонировать рассол, как это известно специалистам в данной области.
D. Собственное производство HCl, которая применяется для протонирования
Поскольку определенные варианты осуществления данного изобретения используют как введение HCl, так и производство газообразных H2 и Cl2, то протонирование рассола может быть сделано самовоспроизводящим; т.е. газообразные продукты H2 и Cl2 могут быть сожжены (в эффективных топливных элементах или в простых форсунках), чтобы получить газообразный HCl, который может быть затем рециркулирован в анолит для протонирования рассола. Энергия, извлеченная из сжигания H2/Cl2, больше той, которая извлекается из сжигания H2/O2. Это увеличивает термодинамическую эффективность данного изобретения.
Некоторые предпочтительные варианты осуществления данного изобретения применяют путь абсорбция/конверсия/регенерация как "входной каскад процесса концентрирования/абсорбции", который затем используется, чтобы абсорбировать и концентрировать CO2 для применения в геологических, океанических или наземных методах связывания (например, в тех, в которых CO2 инжектируется в углеродные хранилища) посредством указанных ниже или аналогичных средств:
(1) Весь водород сжигается, чтобы получить газообразный HCl.
(2) Весь газообразный HCl реагирует с бикарбонатом натрия, произведенным таким образом
(3) Посредством связанной реакции нейтрализация высвобождается CO2 почти 100%-ной чистоты и восстанавливается соленая вода, которая может быть повторно использована для дальнейших циклов абсорбции.
(4) Посредством этого процесса изобретение используется, чтобы абсорбировать, конвертировать и затем высвобождать CO2, при том конечном эффекте, что газ удаляется из потока дымовых газов и концентрируется для методов связывания, дополнительных к этому процессу.
E. Смешивание карбонатов и бикарбонатов снова с католитическими текучими средами
В отличие от хлорощелочного промышленного применения хлор/водородных ячеек, некоторые варианты осуществления данного изобретения также рециркулируют смеси карбоната и бикарбоната в сторону католита (каустика) электрохимической ячейки. Такие методы многочисленны и разнообразны, однако каждый рабочий режим для процесса в целом имеет оптимум возврата смеси бикарбонат/карбонат в католит, поскольку это может, при некоторых концентрациях и условиях, уменьшить напряжение на ячейке и, следовательно, мощность ячейки.
F. Применение рекуперации отходящей теплоты для нагревания текучих сред
Поскольку определенные варианты осуществления данного изобретения применяются на электростанциях или в случае значительного выпуска CO2 в виде дымовых газов или других горячих газов от сжигания, имеются широкие возможности для использования этого отходящего тепла при оптимизации электрохимической ячейки в отличие от стандартных хлорощелочных процессов. Например, типичная температура поступающих дымовых газов (например, после обработки электростатическим осаждением) может составлять 300°C. Теплообменники могут снижать температуру этих дымовых газов до величины менее 300°C, в то время как нагревание анолитной и католитной текучих сред (которые для LVE должны обычно поддерживаться при >90°C) позволяет некоторым вариантам осуществления данного изобретения функционировать без потерь мощности, связанных с нагревателями анолита и католита.
Отходящая теплота непосредственным образом утилизируется в вариантах осуществления с электролизом сульфата посредством нагревания раствора серной кислоты во время добавления хлоридной соли. Это переводит твердую соль в раствор с серной кислотой и затем переводит бисульфат натрия в сульфат натрия. Теплота, требующаяся для протекания этой химической реакции, является достаточной, чтобы освобождать образованную хлористоводородную кислоту посредством испарения. Потребление этой теплоты из дымовых газов устраняет необходимость в расходовании электрической энергии на последующем этапе электролиза образованного гидроксида. Посредством потребления этой тепловой энергии из источника отходов при электростанции значительное количество электрической энергии не расходуется при электролизе, и, соответственно, энергетические характеристики этих вариантов осуществления оптимизированы.
G. Применение рекуперации отходящей теплоты для энергоснабжения технологического оборудования
Обычно, поскольку дымовые газы, которые имеются на электростанции, выпускаются при температурах между 100°C (типично для очистки скруббером), 300°C (после обработки осаждением) и 900°C (вход для осаждения) или других таких температурах, то значительная отходящая теплота может быть извлечена охлаждением поступающих дымовых газов посредством теплообмена в цикле возврата мощности, примером которого является аммиачно-водный цикл (например, запатентованный процесс "Kalina"), паровой цикл или любой такой цикл, который выполняет такую же термодинамическую возможность. Поскольку некоторые варианты осуществления данного изобретения относятся к мощности постоянного тока, чтобы производить реагент/абсорбент для данного изобретения, то процесс может непосредственным образом получать мощность, полностью или частично, посредством возврата отходящей теплоты, что осуществляется без обычных потерь в трансформаторах, связанных с конвертированием мощности постоянного тока в мощность переменного тока для других видов применения. Кроме того, посредством применения отходящей теплоты для работы машин значительная эффективность может быть достигнута вообще без выполнения этапа генерации электричества. При некоторых условиях количество энергии, получаемой возвратом отходящей теплоты, может полностью соответствовать мощности для вариантов осуществления данного изобретения.
VI. Образование и применение побочных продуктов из процессов обезуглероживание и электролиза
Как указано выше, некоторые варианты осуществления устройств и способов в соответствии с данным изобретением производят ряд полезных побочных продуктов от процессов обезуглероживания и электролиза, включающих газообразный хлор, бикарбонат натрия и газообразный водород. В некоторых вариантах осуществления газообразный водород, произведенный вариантами осуществления данного изобретения, включен в контур повторного использования энергии водорода. В некоторых вариантах осуществления данное изобретение может включать современные технологии мембран из фторсодержащих полимеров, чтобы уменьшить миграцию ионов хлора для процесса обезуглероживания. Поэтому процесс может выполняться без значительных затрат энергии и издержек на отделение ионов хлора; и контуры обезуглероживания и отделения сравнительно свободны от хлорида. По существу вариант осуществления реактор обезуглероживания по данному изобретению может применять обычную соль, воду и выпускаемый диоксид углерода в комбинации с электроэнергией, чтобы получить газообразный хлор, бикарбонат натрия и возврат мощности посредством сжигания водорода следующим образом:
2NaCl+H2O+2CO2+e-→2NaHCO3+Cl2+[½H2 + атм O2→e-]
A. Контур повторного использования энергии водорода
Разработаны четыре технологии, которые могут применять энергию водорода, захваченного вариантами осуществления данного изобретения. Первой является совместное сжигание водорода с углем, чтобы улучшить выбросы от сжигания угля, и вторая технология включает извлечение электроэнергии постоянного тока топливным элементом водород/кислород, третья технология включает сжигание водорода в турбине, соединенной с электрическим генератором, и четвертая технология включает смешивание водорода с природным газом и сжигание этой смеси в турбине, спроектированной для генерации мощности с применением природного газа и соединенной с электрическим генератором. В качестве варианта H2 и Cl2 могут сжигаться в Cl2 и HCl непосредственным образом или посредством топливного элемента или извлечением постоянного тока. Источники тепла от удаления отходящей теплоты или от реакции, которая производит каустическую соду при примерно 135°C в резервуаре, или от самого процесса обезуглероживания, который поглощает различные теплоты раствора, теплоты испарения и теплоту, высвобождающуюся в ходе экзотермической реакции, могут быть утилизированы хорошо известными методами (т.е. ребойлерами и т.д.) на местах расположения электростанций для предварительного нагревания газообразных продуктов сгорания или для других целей.
В одном из вариантов осуществления может быть выгодно коммерческое производство электроэнергии постоянного тока топливными элементами вследствие простоты обращения и безопасного функционирования при давлениях ниже атмосферного. Немедленное потребление произведенного водорода также может непосредственным образом уменьшать стоимость электрической нагрузки для электролиза рассола. Кроме того, поскольку цикл извлечения энергии водорода может быть выполнен не при пике производства H2, Cl2 и NaOH, и H2 может быть затем применен для предоставления электроэнергии во время пиковых нагрузок, то данное изобретение предоставляет возможность получения реагентов при низкой стоимости, наряду с возможностью последующего производства вспомогательной дорогостоящей пиковой электроэнергии и одновременного выполнения процесса обезуглероживания. Экономическая полезность цикла извлечения энергии H2, чтобы увеличить пиковое производство электроэнергии электростанцией посредством пополнения текущего производства энергией от сжигания H2, применяемого либо в виде топлива, либо в топливных элементах, может предусматривать полезность при потреблении на месте.
В качестве альтернативы, предоставляя данный чистый углеродный источник газообразного водорода уровня "для электронной промышленности", муниципальные энергопредприятия общего пользования, промышленные компании и мощности для производства электроэнергии могут получать выгоду от применения произведенного водорода в муниципальных автобусных парках, поездах и других общественных или частных местах применения водородного топлива.
Возможно, оптимальным решением для контура повторного использования энергии является подавление образования водорода в вариантах осуществления с сульфатом. В вариантах осуществления электролиза сульфата высвобождается кислород на аноде. Этот кислород может быть подан насосом к газодиффузионному электроду на катодной стороне электрохимической ячейки, и таким образом предотвращается образование газообразного водорода посредством конвертирования водородных ионов (H+) обратно в воду (H2O) непосредственно на катоде. Это экономит значительное количество электрической энергии, которая могла бы быть использована для производства газообразного водорода. Варианты осуществления с сульфатом особенно подходят для осуществления этого подавления образования водорода, по причине прямого производства кислорода и уже низкого потребления электрической энергии. Конечным результатом является система, которая захватывает диоксид углерода посредством гидроксида и производит лишь хлористоводородную кислоту, в то время как потребляется лишь хлоридная соль.
B. Другие виды применения побочных продуктов от процесса обезуглероживания
В некоторых вариантах осуществления газообразный хлор может быть основным окислительным реагентом, используемым для уничтожения бактерий в оборудовании для обработки воды во всем мире. На хлор и некоторые производные от него на 100+ исходные химикаты, которые произведены из него, часто ссылаются как на включенные в 30%+ ВВП США. Он может быть также использован в производстве наиболее распространенного промышленного химиката, хлористоводородной кислоты. Хлор также интенсивно используется в промышленность пластмасс как наиболее обычный в этой области неуглеродный реагент.
Карбонат натрия является побочным продуктом процесса, описанного в данном изобретении, который обычно используется в производстве мыла, моющих средств и шампуней во всем мире, а также в качестве флюса в производстве стекла. Кроме того, в производственных мощностях, а также в частных домах бикарбонат натрия применяется для смягчения жесткой воды, в соответствии со следующей общей реакцией:
CaCl2 (водн. р-р)+NaHCO3(водн. р-р)→CaCO3(осадок)+NaCl(водн. р-р) +HCl(водн. р-р)
Подобный процесс может быть выполнен с применением карбонатов и бикарбонатов натрия от этого процесса, чтобы выполнить ионный обмен с несколькими солями элементов 1 и 2 групп, чтобы осадить различные карбонаты.
Другим примером побочных продуктов, произведенных из процесса обезуглероживания, является газообразный водород. Газообразный водород, при уровне "для электронной промышленности", является носителем энергии высокого класса. Напротив, произведенное водородное топливо может быть сожжено при более уровнях "загрязнения" угля, чтобы уменьшить выбросы от сгорания, может быть сожжено в качестве топлива для бойлера в ходе процесса отделения или может быть утилизировано в транспортных средствах, работающих на водороде. Во многих вариантах осуществления водород будут сжигаться на месте на электростанции, чтобы существенно уменьшить потребность в энергии, связанную с этапом электрохимической обработки, на котором производится абсорбент. Современная литература указывает, что турбины, оптимизированные для сжигания водорода, еще в течение нескольких лет имеют шанс на успех, и ожидается, что они смогут конвертировать почти 70% термодинамической энергии, содержащейся в газообразном водороде в электрическую мощность. Современные лучшие турбины, работающие на природном газе, которые функционируют при совместном производство энергии, могут обеспечивать 61%-ную конверсию энергии природного газа в электрическую энергию.
В других вариантах осуществления, возможно выполнение транспортировки диоксида углерода в удаленные места связывания следующими способами или их эквивалентами:
(1) На месте электростанции CO2 и другие загрязняющие вещества абсорбируются посредством указанного процесса или любым его вариантом, наряду с образованием водорода, хлора и карбонатов.
(2) На удаленном месте связывания хлористоводородная кислота и карбонаты снова объединяются в ходе реакции нейтрализации, которая образует практически чистый CO2. CO2, произведенный таким образом, может быть затем инжектирован в углеродное хранилище.
Посредством этого достигается тот же самый конечный эффект транспортировки CO2 между местом электростанции и местом связывания, без физической транспортировки CO2 посредством ожижения и транспортировки по трубопроводам, грузовыми автомобилями и т.д.
VII. Удаление ртути/тяжелых металлов
Абсорбция диоксида углерода и нейтрализация более сильнокислых газов из поступающего потока дымовых газов обычно улучшается уменьшением температуры потока дымовых газов и поддержанием более низких температур в абсорбирующих текучих средах. Это интуитивно очевидно и доказано испытаниями в лабораторных и производственных условиях.
Когда выполняется это охлаждение поступающих дымовых газов, оно может сделано таким образом, что теплота, которая перемещается вместе с ними, может быть использована различными средствами, которые приносят выгоду процессу в целом, а именно:
(1) нагреванием католитной и анолитной текучих сред, выгода заключается в функционировании без энергозатратных электрических нагревателей и нагревателей с применением иных средств, и при более высоких температурах реакция электролиза происходит при более низких напряжениях;
(2) испарением воды из смеси карбоната/бикарбоната, являющейся продуктом, выгода заключается в проведении этой операции без применения энергозатратных электрических нагревателей для выполнения отделения и в утилизировании воды для дополнительного применения в процессе;
(3) нагреванием рассолов, используемых в качестве текучей среды, выгода заключается в выполнении этой операции без применения энергозатратных электрических нагревателей;
(4) другими видами применения нагревания в процессе.
Когда охлаждение поступающих дымовых газов выполняется таким образом, что температура дымовых газов падает ниже точки росы смешанных дымовых газов, то вода и различные компоненты выделяются из поступающих дымовых газов в форме водного конденсата, который типично является кислым по своей природе (содержит небольшие количества кислот, образованных из SOx и NOx, присутствующих в дымовых газах, некоторое количество угольной кислоты и т.д.) и содержит ряд различных тяжелых металлов, из которых ртуть является преобладающим компонентов, но также содержатся серен, хром, мышьяк, свинец, германий, ванадий и многие другие тяжелые металлы.
Удаление тяжелых металлов из воды или же удаление воды из тяжелых металлов может быть полезным по экологическим или экономическим причинам. Имеется несколько испытанных способов отделения:
(1) испарение воды, либо естественным образом, либо принудительным нагреванием/конвекцией, которое оставляет тяжелые металлы в виде концентрированных металлических оксидов;
(2) изменение pH водного конденсата от кислых до щелочных условий, что изменяет растворимость металлических компонентов, вызывая частичное или близкое к полному осаждение. Таким образом, может быть использовано естественное осаждение под действием силы тяжести для удаления металлических оксидов посредством процесса седиментации; в качестве альтернативы может быть использована фильтрационная технология, упомянутая в (4) ниже;
(3) обработка текучей среды абсорбирующей смолой, так что тяжелые металлы абсорбируются смолой;
(4) пропускание текучей среды через фильтрующую среду, такую как активированный уголь, либо пассивным образом (пропусканием под действием силы тяжести), либо активным нагнетанием.
Продемонстрировано, что небольшое добавление гидроксида натрия (легко доступного из основного хлорощелочного процесса, описанного в данном документе) может быть использовано, чтобы сместить величину pH от слабокислой до слабощелочной, вызывая осаждение металлических веществ, и что это, при последующей принудительной фильтрации через фильтр с активированным углем, может удалять значительно более 90% захваченных тяжелых металлов. Например, в некоторых лабораторных и производственных демонстрациях было показано, что в случае конденсатов, содержащих вплоть до 35-50 млн-1 ртути, имело место извлечение ртути до ее содержания менее 0,2 млрд-1 (нижний предел для примененной методики анализа).
VIII. Альтернативные пути блокирования газообразного хлора
Предполагается, что крупномасштабное применение определенных процессов связывания диоксида углерода, описанных в данном документе, могло бы вызвать в конечном счете миграцию "чистого" хлорощелочного производства от современных мест его расположения к производству на электростанциях. При таком переходе возникает несколько вопросов, связанных с рынком.
Во-первых, современный хлорощелочной рынок, как предполагает его название, поставляет как хлор, так и щелочь (каустическую соду), и значительная работы была проведена, чтобы обеспечить то, что когда продается одна единица хлора, то одновременно продается одна единица каустической соды; в этом смысле, два рынка - рынок хлора и рынок каустика - связаны между собой долгое время и регулируются совместно для продажи/потребления в стехиометрических соотношениях.
В случае определенных процессов связывания диоксида углерода, описанных в данном документе, производится лишь хлор, в то время как каустическая сода потребляется для целей связывания диоксида углерода. Потребность в каустической соде, следовательно, остается неудовлетворенной посредством данного процесса, и ожидается появление альтернативных средств производства для рынка каустической соды, которые включают, однако не ограничиваются ими, следующие предполагаемые средства:
(1) Кальцинированная сода или карбонат натрия (Na2CO3) является природным минералом, найденным в больших количествах в Соединенных Штатах; он используется во многих видах применения как непосредственный заменитель гидроксида натрия, или каустика;
(2) Гидроксид натрия может быть непосредственным образом произведен из карбоната натрия посредством гидратирования карбоната (добавлением воды) и его нагреванием; т.е. Na2CO3+H2O+теплота→NaOH+CO2. При условии, что CO2 из такого процесса захватывается и связывается, NaOH производится для (сравнительно небольшого) рынка каустика, который не может мигрировать к другим промышленным основаниям;
(3) Другие карбонаты могут быть конвертированы в гидроксиды аналогичными средствами; и
(4) Другие промышленные основания могут заменять гидроксид натрия, в зависимости от конкретного вида применения.
В некоторый момент, рынок хлора становится полностью насыщенным хлором, произведенным определенными процессами связывания диоксида углерода, описанными в данном документе. Объем этого рынка может быть больше или меньше по сравнению с текущим "статическим" рынком хлора. Прекращение зависимости рынка хлора от рынка каустика и потенциальное предоставление больших количеств хлора, произведенного средствами с низкими энергозатратами, могут вызвать эластичность рыночного спроса. Рынки тогда могут быть расширены, чтобы принять большее количество более дешевых, не взаимозависимых продуктов. Однако может быть сделано предположение, что в некоторый момент ионные соединения хлора/газообразный хлор, образованные определенными процессами связывания диоксида углерода, описанными в данном документе, могут производиться в избыточном количестве по сравнению с рынком для хлора.
Предложено несколько средств для направления хлора для надежного применения после того, как рынок насыщен хлором; в некоторых вариантах осуществления эти средства для направления хлора предполагают первоначальную обработку, чтобы преобразовать хлор из газа в жидкость посредством следующей общей реакции:
Cl2(газ)+2 H2O (жидкая фаза)+hv363 нм→2HCl (жидкая фаза)+½ O2 (газ)
Здесь hv363 нм относится к свету с длиной волны примерно 363 нм.
В некоторых вариантах осуществления кислород, произведенный таким образом, может быть возвращен к входу для воздуха самой электростанции, при этом, как было показано в ходе исследований в области электроэнергетики, такие электростанции с подачей воздуха, обогащенного кислородом, имеют (a) повышенные кпд цикла Карно, (b) выходные потоки с более концентрированным CO2, (c) меньший теплообмен для нагревания входящего воздуха, и (d) другие преимущества по сравнению с электростанциями без обогащения кислородом.
Следует заметить, что произведенные в качестве продуктов водород и хлор могут также сожжены непосредственным образом, чтобы получить HCl (газ), который может быть затем нейтрализован в виде газа или может быть смешан с водой, при этом образуется хлористоводородная, или соляная, кислота; показано, что H2 и Cl2 могут быть сожжены в топливном элементе, при непосредственном извлечении электрической энергии постоянного тока; подобным образом, высокая теплота сгорания H2 и Cl2 может быть использована для генерации электроэнергии в более традиционной конструкции форсунка/турбина/генератор.
После того как хлор преобразован в жидкую форму, такую как хлористоводородная кислота (гидратированный HCl), могут быть применены различные средства нейтрализации кислоты, приведенные ниже примеры таких процессов являются иллюстративными, однако не исчерпывающими.
Одной из форм нейтрализации могла бы быть рекомбинация образованной таким образом хлористоводородной кислоты с образованным таким образом карбонат/бикарбонатом натрия, который первоначально адсорбировал CO2 из разбавленного потока дымовых газов (примерно 12% CO2), и регенерация концентрированного потока CO2 (примерно 100% молекулярного CO2) посредством следующей реакции:
HCl+NaHCO3→NaCl+H2O+CO2 (газ)
Эта реакция может быть выполнена простым смешиванием или проведением реакции через соответствующую мембрану, и из кислотно-щелочной батареи, образованной таким образом, может быть извлечена мощность постоянного тока; кроме того, газы при расширении/образовании могут быть захвачены и направлены в генератор (подобно технологии, выполняемой в процессах абсорбции и регенерации амина).
Несмотря на то что эта тотальная регенерация газообразного CO2 может показаться, на первых порах, прямой противоположностью, данный процесс выполняет несколько несколько важных моментов в отношении захвата и связывания CO2:
(1) CO2 захватывается из разбавленного потока (12%) и затем преобразуется в концентрированный поток (~100%);
(2) Дополнительная энергия, в форме мощности постоянного тока или мощности, образованной от генерации расширяющихся газов; и
(3) Реагент, требующийся для электролиза (NaCl), регенерируется и, подвергнувшись соответствующему кондиционированию, подготовлен к тому, чтобы подвергнуться электролизу и абсорбировать CO2 в другом цикле, образуя тем самым химическую петлю.
Применение бикарбоната натрия для нейтрализации хлора является одним из путей выполнения нейтрализации; другие бикарбонаты могут быть использованы аналогичным образом, с тем результатом, что производятся другие соли в качестве продукта, что может быть экономически выгодно в определенных обстоятельствах.
Помимо применения бикарбонатов элементов I группы могут быть применены бикарбонаты элементов II группы (например, CaCO3, известняк), чтобы выполнить нейтрализацию в соответствии со следующей обобщенной реакцией:
G2CO3+2HCl (жидкость/газ)→G2 Cl2 (соль)+CO2 (газ)
Следует заметить, что CO2, высвобождающийся посредством указанной выше реакции, составляет 50% от CO2, образованного в предшествующем примере с применением бикарбоната элемента I группы для нейтрализации. Также следует заметить, что прежние средства возмещения энергии (реакции кислота/основание при прохождении через мембрану, генерация мощности от образования газов и т.д.) все еще применимы.
Нейтрализация хлоридных ионов также может быть выполнена посредством применения карбонатов элементов I группы, как в последующем примере с карбонатом натрия:
Na2CO3 (жидкая фаза)+HCl (жидкая фаза)→NaCl (жидкая фаза)+NaHCO3 (жидкая фаза)
Следует заметить, что этой реакцией, как написано, не регенерируется любой газообразный CO2; при некоторых рабочих режимах CO2 регенерируется, оставляя после себя NaOH (в жидкой фазе); однако если условия регулируются соответствующим образом, то может быть выполнена реакция без генерации. Следует заметить, что в этом случае доступна возможность извлечения энергии системы кислота-основание (но не энергии из регенерации газа).
Среди всех этих реакций металлы I группы могут быть заменены на металлы I группы, и, подобным образом, металлы II группы могут быть заменены на металлы II группы в различных смесях карбоната и бикарбоната.
IX. Спаренный смоченный/насаженый бикарбонатор с жидкостным карбонатором
Первоначальная разработка эффективных узлов для конвертирования газообразного CO2 в бикарбонат была сосредоточена на применении барботажных колонн; эти устройства известны как наиболее эффективные в объемном отношении (объем/конвертированный химикат) обобщенной конструкции. Во время проведения абсорбции потоков искусственных дымовых газов в лабораторных условиях и проведения абсорбции потоков реальных дымовых газов в производственных условиях было продемонстрировано, что абсорбирующая текучая среда проходит от преимущественно гидроксидной формы к преимущественно карбонатной форме и в конечном счете к бикарбонатной форме. Исходя из затрат термодинамической энергии в процессе, следует, что один из вариантов осуществления процесса функционирует при наименьшей общей входной энергии (т.е. при наиболее низких затратах на энергию для электролиза), когда отношение натрия к углероду было минимальным; например, 1:1, как в случае бикарбоната. Некоторые варианты осуществления включают разделение двух основных процессов (т.е. образования карбоната из гидроксида и образования бикарбоната из карбоната), как для исследовательских целей, так и для оптимизации отдельного процесса, посредством применения системы, которая включает как бикарбонатор, так и карбонатор. Показано, что такие узлы приводят к отношению натрия к углероду, близкому к 1:1, или к производству более 95% бикарбоната при некоторых контролируемых условиях. При оптимизации для минимального объема реактора при высокой конверсии в бикарбонат пара барботажных колонн выполняет оба условия.
Однако имеются разные формы оптимизации. Например, наименьшее потребление энергии или наименьшая потребность в энергии на этапе абсорбции/конверсии, являются важным учитываемым условием, и оптимизация этого условия означает разное предпочтительное осуществление процесса; а именно, применение бикарбонатора, который обладает очень низким перепадом давления (сопротивлением) при протекании газа, значительным образом снижает энергию, требующуюся для сжатии (посредством вентилятора или другого устройства с потреблением энергии) дымовых газов, проходящих через устройство. Некоторые варианты осуществления применяют бикарбонатор, который смочен и насажен, однако имеет по существу нулевой уровень жидкости. Такие варианты осуществления могут быть спарены с жидкостным карбонатором, могут быть спарены с подобной смоченным/насаженным карбонатором или могут быть объединены в единственную "униколонну", в которой гидроксид конвертируется в карбонат, частично при его опускании в колонне, и затем "доведенный" до бикарбоната с течением времени выводится из колонны. Каждая из этих разных конструкций колонны имеет склонность к оптимизации разных параметров:
(1) двойная барботажная колонна: наиболее эффективна в отношении объем/конверсия; может достигаться конверсия 95%+ в бикарбонат без последующей обработки с отделением/рециркуляцией;
(2) смоченная/насаженная бикарбонатная колонна с жидкостным карбонатором: более эффективна в отношении энергия/тонны абсорбированного CO2.
(3) смоченные/насаженные двойные колонны: низкое сопротивление, оптимизация с низкой энергией; и
(4) конструкции униколонн: наименьшее число резервуаров.
В зависимости от целевой величины в % удаления CO2 и других проектных параметров, ключевых для конкретной конструкции электростанции (% SOx + NOx в расчете на CO2, пространство, стоимость и т.д.), каждая из этих конструкций или их комбинаций в различном порядке и при разном расположении может составлять предпочтительные варианты осуществления.
X. Электролиз сульфата
Процесс производства абсорбента может быть выполнен посредством электролиза рассола и посредством электролиза сульфата. Варианты осуществления электролиза сульфата содержат ряд химических и электрохимических реакций. Наряду с тем, что производство каустика остается основной причиной выполнения этих процессов, побочные продукты состоят из водорода (H2), кислорода (O2) и хлористоводородной кислоты (HCl). Электролиз сульфата в своей основе более эффективен в отношении электрической энергии, чем электролиз рассола просто потому, что большое количество требуемой энергии может быть получено из отходящей теплоты дымовых газов, а не посредством потребления электрической энергии на этапе электролиза. При электролизе рассола имеется фундаментальный нижний предел для напряжения, требующегося для производства каустика, и этот предел находится вблизи 2,15 В. При электролизе сульфата, когда образование газообразного водорода не подавляется, фундаментальный нижний предел близок к 1,6 В и почти равен эффективной термодинамической энергии, содержащейся в произведенном газообразном водороде. Во-вторых, высвобождение чистого кислорода делает доступ к энергосодержанию этого водорода более непосредственным. При электролизе сульфата, когда образование газообразного водорода подавляется, фундаментальный нижний предел может быть близок к 0,7 В. Это является огромной экономией энергии, требующейся для выполнения этих реакций и обеспечения захвата диоксида углерода.
Этот процесс производит хлористоводородную кислоту непосредственным образом в соответствии со следующим уравнением реакции:
2NaCl+H2SO4+теплота→Na2SO4+2HCl
а не косвенным образом, как при электролизе рассола, и как описано ранее. HCl легче транспортируется, чем газообразный хлор, имеет высокую ценность в качестве исходного химического реагента и не требует энергии для сжатия при доставке на рынок.
Хлористоводородная кислота испаряется вместе с некоторым количеством воды, когда теплота дымовых газов возбуждает реакцию, оставляя сульфат натрия и серную кислоту в смеси перед электролизом. Химический переход, который происходит во время этой стадии электролиза в данном электрохимическом процессе, представлен следующим уравнением:
Na2SO4+2H2O+e-→2NaOH+H2SO4+2H2+O2
Сульфатный ион возвращается назад к первоначальному (трансформация соли) этапу от анода, каустик производится и доставляется к месту обработки дымовых газов, точно также, как при электролизе рассола, и водород и кислород высвобождаются в стехиометрическом соотношении.
Специалист сразу же осознает, что HCl, H2 и O2, являющиеся побочными продуктами, уже обсуждались в данном документе. Варианты осуществления этого изобретения с применением электролиза сульфата будут использовать те же самые последовательные стадии, которые были описаны ранее, и могут использовать такие же способы расчета, которые описаны в данном документе, при оптимизации этого процесса в отношении затрат, потребления энергии или эффективности использования энергии.
Другой вариант осуществления электролиза сульфата по данному изобретению делает возможным высвобождение кислорода на аноде и подает этот кислород к газодиффузионному электроду на катоде, подавляя тем самым образование водорода и сберегая значительное количество энергии для электролиза посредством этого подавления. Результирующим продуктом этого процесса является лишь хлористоводородная кислота в виде продажного побочного продукта, а каустик используется, чтобы абсорбировать диоксид углерода из потока дымовых газов.
ПРИМЕРЫ
Представленные ниже примеры включены, чтобы продемонстрировать предпочтительные варианты осуществления данного изобретения. Эти варианты осуществления предоставляют возможные экономически выгодные решения для уменьшения или даже полного устранения диоксида углерода и других загрязняющих веществ от электростанций посредством предоставления и применения результирующих реагентов в коммерческих целях или в промышленных процессах и/или посредством повторного использования энергии.
Специалистам в данной области следует принимать во внимание, что способы, раскрытые в описанных ниже примерах, представляют собой способы, обнаруженные авторами изобретения и хорошо действующие при практической реализации данного изобретения, и они, соответственно, могут учитываться при создании предпочтительных режимов их практического использования. Тем не менее, в свете представляемого раскрытия изобретения специалисты должны учитывать, что могут быть сделаны многие изменения в описанных здесь конкретных вариантах осуществления при получении таких же или схожих результатов без отклонения от сущности и объема данного изобретения.
Пример 1
Реактор в виде барботажной колонны CO2/NaOH, спроектированный графическими способами
В реакторе в виде барботажной колонны, сконструированном для этого примера, имеются четыре основных потока, а именно:
(1) Жидкость, протекающую в текучую среду барботажной колонны при заданном объемном расходе (Vl = объем текучей среды в единицу времени); в избранном случае объемный расход входящего потока равен объемному расходу выходящего потока. Следовательно, оба равны V1). В этом примере V1=0,001 м3/с.
(2) Vg0 = объемный расход входящего газа, который будет частично или полностью абсорбирован абсорбирующей текучей средой. В этом примере Vg0=0,05 м3/с.
(3) Vg = объемный расход выходящего газа. В этом примере Vg=0,02 м3/с.
Реактор в виде барботажной колонны сконструирован как ограниченный указанными выше условиями. CO2, поступающий с дымовыми газами при содержании шестьдесят процентов, подлежал удалению барботированием через концентрированный раствор гидроксида натрия. Реакция ограничивается массопередачей. Целью данного примера являлось вычисление размера реактора (высоты и диаметра), необходимого для удаления 99,9% диоксида углерода. P=2 атм. (200 кПа), T=298 K. При использовании графических данных, приведенных на Фиг. 8, этот пример описывает конструкцию как высокого реактора (2,36 м) и короткого реактора (0,41 м). Фиг. 8 представляет собой график, показывающий процентную долю CO2, абсорбированного в барботажной колонне, в зависимости от глубины текучей среды и в зависимости от скорости газа на границе раздела при низких скоростях на границе раздела (Schumpe et al., 1979).
Решение с колонной высотой 2,36 м
Конверсия приближается к 100% при приведенной скорости (Ug0) примерно 0,04 м/с. Эта скорость находится в интервале протекания потока с пузырьками (в водоподобных растворах его предел соответствует примерно 0,05 м/с). Зная требуемый объемный расход газа (Vg0), рассчитывали диаметр колонны:
Ac=Vg0/Ug0=0,05/0,04=1,25 м2
Dc=2√(Ac/π)=2√(1,25/π)=1,26 м
Следовательно, для конверсии 99% поступающего CO2 в концентрации 60% требуется колонна высотой 2,36 м, площадью 1,25 м2, имеющая диаметр 1,26 м и общий объем 2,95 м3.
Решение с колонной высотой 0,41 м
Конверсия в колонне высотой 0,41 м требует приведенной скорости газа примерно 0,02 м/с. Аналогично указанному выше:
Ac=Vg0/Ug0=0,05/0,02=2,50 м2
Dc=2√(Ac/π)=2√(2,5/π)=1,78 м
Следовательно, для конверсии 99% поступающего CO2 в концентрации 60% требуется колонна высотой 0,41 м, площадью 2,50 м2, имеющая диаметр 1,78 м и общий объем 1,03 м3.
Подводя итог вышесказанному, посредством этого примера продемонстрировано, что более короткие колонны более эффективны в расчете на объем при абсорбции диоксида углерода из дымовых газов; для этого примера в 3 раза. Поэтому для предпочтительных вариантов осуществления данного изобретения, конструирование нацелено на реакторы с короткими ступенями и/или с несколькими ступенями, состоящими из коротких ступеней.
Пример 2
Барботажная колонна CO2/NaOH, спроектированная с применением коэффициента массопередачи
Целью этого примера было определение коэффициента массопередачи, kla (моль/с/объем), из теоретических построений. Из этого примера было определено, что этот корреляционный способ может потенциально приводить к неубедительным результатам; т.е. этот пример отображает трудность прогнозирования фактических результатов из теоретических соображений, вследствие неопределенности в измерении некоторых критических параметров. Поэтому лишь экспериментальное масштабирование может окончательно определить результат в отношении устройства для крупномасштабного обезуглероживания.
Представленные ниже уравнения для задержки газа (εg) и молярная массопередача (kLa) взяты из корреляций работы Akita и Yoshida (1973) и имеют силу для систем диоксида углерода и воды при относительно больших высотах и диаметрах колонны (т.е. >0,1 м):
Задержка газа
εg=C*[g*Dc2*ρL/σ]1/8*[g*Dc2/vl2]1/12*[µg/√g*Dc]
(1-εg)4
и
Коэффициент массопередачи
kLa(1/сек)=[Cco2*Dco2-h20/Dc2]*[νL/Dco2-h20]0,2*[g*Dc2*ρL/σ]0,62*[g*Dc3/νl/2]*ε11
где
εg = коэффициент задержки газа
Cco2 = концентрация CO2 в дымовых газах
Dc = диаметр колонны
vL=0,0001 м2/с
σ=1 сП=0,1 Па*с
ρL=998 кг/м3
и, соответственно, Dco2-h20P=1,661 м2*Па/с,
поэтому Dco2-HO=1,661/5,067*10(5)=3,278*10(-6) м2/с
Движущей силой является разность между равновесной концентрацией диоксида углерода (Cco2*) и фактической концентрацией диоксида углерода в жидкой фазе (Cco2), которая в этом примере предполагается равной нулю; т.е. присутствующий гидроксид натрия моментально нейтрализует "кислотность" диоксида углерода в воде. Скорость молярного массопереноса в расчете на объем реактора, соответственно, может быть представлена как
Nco2=kLa*[Cco2*-Cco2]=kLa(Cco2*)
Скорость молярного массопереноса, требующаяся для удаления 99,99% диоксида углерода в дымовых газах. Предполагается, что CO2 является идеальным газом при условиях колонны.
Объем/с:
Vg0=0,05 м3/с∴Vco2=0,6*Vg0=0,03 м3/с
Моль/с:
Vco2*P/RT=[0,03M3/с*5 атм]/
[0,082 м3атм/кмоль К*298]*1000 г-моль/1 кмоль=6,14 моль/с
Nco2(моль/с)=0,999(моль удаленного CO2/моль входящего CO2)*6,14 моль/с = 6,13 моль/с
Другие свойства текучей среды для корреляции модели
При задании первоначальной приведенной скорости при предельном значении скорости барботируемого потока (Vg0=0,05 м/с) вычислялись площадь и диаметр колонны:
Ac=Vg0/Ug0=0,05/0,05=1,0 м2
Dc=2√(Ac/π)=2√(1,0/π)=1,13 м
Для реакций задержки газовой фазы в этом примере установлено C=0,2 и предполагается, что приведенная скорость (Ug) является средней величиной скоростей на входе и на выходе; Ug=0,035 м/с= средней величиной для (0,05 м/с, 0,02 м/с), и при применении программы для решения уравнения было найдено, что εg=0,055.
Далее, был вычислен молярный коэффициент массопередачи:
kLa(1/сек)={(0,6*3,278*10-6 м2/с/[0,6 м]2}*[0,0001 м2/с/3,278×10-6 м2/с]*[9,8 м/с2*(0,6 м)2*998 кг/м3/0,0696 кг/с2]*{(9,8 м/с2)*(0,6 м)3/[0,0001 м2/с]2}*(0,055)1,1=0,386/с
kLa=0,386/с
При возвращении к уравнению движущей силы был рассчитан объем реактора (V):
V=Nco2/[(kLa)(Cco2*)]=6,13 моль/с/(0,386/с*(103,6 моль/м3))=0,15 м3
и
Hc=0,15 м3/1 м2=0,15 м
Следовательно, размеры барботажной колонны составляют Dc=1,13 м и Hc=0,15 м, что приводит к значительной разнице по сравнению с фактическими результатами для реальных барботажных колонн.
Некоторые допущения могут объяснить разницу между корреляционными моделями (которые считаются лучшими моделями такого поведения) и фактическими результатами:
(1) Было сделано допущение, что гидроксид натрия обладает свойствами воды (плотность, поверхностное натяжение и т.п.); и
(2) Концентрация CO2 в растворе не может быть в действительности охарактеризована как нулевая; это является более вероятным операндом; например, если эффективная концентрация CO2 не равна нулю, то движущая сила меньше и требуется более высокая колонна.
Следует также заметить, что эта теоретическая корреляция допускается при условии, которое также оказывает негативное влияние: поскольку такие члены, как (vL=0,0001 м2/с), находятся часто в квадрате в знаменателе, то небольшие изменения в их численных значениях оказывают гигантское действие. Этот тип теоретических построений годится для подбора кривых постфактум, однако не является хорошим средством прогнозирования массопередачи для конструкторских целей. Кроме того, имеют место ударные воздействия потока текучей среды на степень абсорбции/конверсии CO2, такие, которые проявляются в конструкциях разного и прогрессирующего масштаба.
Пример 3
Проектирование барботажной колонны CO2/NaOH (глубина) на основании экспериментальных данных
Следует заметить, что достоверность определенных вариантов осуществления данного изобретения в отношении описанной здесь "теории эффективности коротких ступеней" (расстояние соприкосновения газ-жидкость или высота ступени текучей среды 3 м или менее, чтобы достичь абсорбции >90%) подтверждается двумя разными методиками вычислений, которые согласуются с реализованными на практике конструкторскими расчетами в области химического машиностроения. Однако в некоторых случаях (как указано выше) в этих конструкторских расчетах сделаны определенные упрощающие допущения, так что требовалась экспериментальная проверка, которая была выполнена с результатами, представленными на Фиг. 2B и 2C (пояснено более подробно ниже).
В каждом из прогонов при обработке достигалась определенная абсорбция CO2 на протяжении определенного расстояния соприкосновения газ-жидкость (а именно, высоты текучей среды в случаях открытой барботажной колонны без насадки); например, абсорбция 20% на протяжении 30 см текучей среды.
Если газ проходит через вторую колонну той же самой конструкции при тех же самых условиях, такая же абсорбция могла бы происходить снова; т.е. могло бы снова быть абсорбировано 20% от оставшихся 80% первоначального CO2.
Это соотношение в конце концов уменьшается, однако предоставляет высокие абсорбционные характеристики абсорбирующей текучей среды, и склонность хемосорбции к сохранению устойчивой абсорбции даже разбавленного CO2 в дымовых газах, этот эффект игнорируется для этого примера, и результатом является планируемое удаление 90%.
Можно видеть, что повторные прохождения текучей среды через абсорбирующую текучую могут снова уменьшать содержание остающегося CO2 на 20%, и т.д., пока не будет выполнено достаточно проходов, чтобы достигнуть желательного уровня абсорбции (в данном случае 90%).
Это приводит к конструкции с "числом щелочных ступеней", которое определяет глубину текучей среды (в нескольких глубинах ступеней высотой 30 см), которая требуется для достижения 90%. Результаты, полученные в предположении, что каждая стадия абсорбирует одну и ту же процентную долю CO2 в расчете на расстояние, как и предшествующая стадия, приведены на Фиг. 2B и 2C и графически представлены на Фиг. 2D и 2E.
Фиг. 2A показывает устройство для исследования основных особенностей одного из вариантов осуществления обезуглероживающей части данного изобретения. Устройство на Фиг. 2A (или устройство с подобным действием) может функционировать в соответствии с процедурой, описанной ниже.
(1) Узел карбонизации 801 загружается NaOH при испытательной нагрузке (например, 1M NaOH в воде при 25°C) при глубине 30 см, с насадкой или без насадки.
(2) Дымовые газы, искусственные или фактические, в этом случае, соответствующие типичному выпуску дымовых газов от сжигания угля (16% CO2, 84% N2, SOX/NOX<1% или в обычных величинах в млн-1), вводились в узел карбонизации 801, эффективным образом барботировали в колонне без насадки, эффективным образом барботировали или распределялись в колоннах с насадкой, перемещались через текучую среду и выпускались наружу. Газ находится при 25°C, CO2 имеет расход 2 л/мин вместе с другими газами, смешанными пропорционально, и протекает в верхнем направлении через колонну с круглым сечением диаметром 4 дюйма (10,16 см); давление системы может составлять 1 атм (100 кПа) или менее.
(3) Посредством измерения концентрации поступающего CO2 (например, посредством отбора проб для газовой хроматографии или измерения концентрации CO2 в линии) может быть замечено, что CO2 абсорбируется текучей средой, что температуры увеличиваются (экзотермическая реакция), и образцы жидкости для анализа будут показывать присутствие карбоната/бикарбоната/гидроксида в равновесном состоянии, указывая на то, что происходит не только лишь абсорбция CO2, но происходит также его конверсия в карбонатную или бикарбонатную форму. Эксперименты с практическим функционированием показывают, что имеются следующие ключевые "точки перехода" в равновесном состоянии по отношению к pH:
a. При pH<=8,3 предпочтительно происходит образование бикарбоната.
b. При pH>=10 предпочтительно происходит образование карбоната.
(4) Абсорбция/реакция конверсии в карбонат протекает интенсивным и экзотермическим образом до тех пор, пока, с учетом динамики газа, при любом расходе CO2 не абсорбировался/конвертировался, при этом экзотермическая фаза реакции заканчивается, температура сначала выходит на плато и затем понижается, и способность текучей среды к абсорбции, которая падает, когда концентрация ионов OH уменьшается, становится практически нулевой в этот момент. Когда уровни абсорбции начинают падать, величина pH, как правило, примерно равна 8,3 или находится вблизи этого значения; при pH>8,3 абсорбция является сравнительно интенсивной.
(5) Текучая среда перемещается в колонну бикарбонизации 803, и дымовые газы снова вводятся в текучую среду. Абсорбция CO2 прекращалась, и в некоторых случаях она будет проявляться как отрицательная (текучая среда отдает некоторое количество CO2 в перемещающийся через нее поток газа). Температура текучей среды продолжает падать отчасти вследствие некоторого сопутствующего испарения в протекающий газовый поток и также вследствие реакции бикарбонизации, которая имеет место между первоначально образованным карбонатом натрия и остающимся несвязанным CO2, который растворен в текучей среде.
(6) Равновесие продолжает оставаться сдвинутым в сторону образования бикарбоната, и могут быть проведены оптимизации начальной концентрации гидроксида, температур, давлений, расходов, скоростей и завихрения потоков текучей среды и газа и т.д., вплоть до точки образования чистого бикарбоната (99%+).
Фиг. 2B и 2C представляют результаты нескольких серий испытаний, проведенных с загрузкой (NaOH в определенной концентрации размещался в обезуглероживающей системе, как показано на Фиг. 2A). Несколько ключевых моментов продемонстрировано данными на Фиг. 2B и 2C:
(1) Условия могут быть модифицированы в достаточной степени, чтобы образовывать воспроизводимым образом либо чистый карбонат (прогоны 4 и 14), либо чистый бикарбонат (прогоны 28 и 32), и могут быть отрегулированы для достижения разных результатов (или "соотношения ионов" между предельными величинами 1,0-2,0).
(2) Размеры реактора, которые являются результатом этого исследования, для всех случаев со значительной абсорбцией, найдены таковыми, что обычно расстояния соприкосновения газ-жидкость менее 3 м достаточны для достижения 90% абсорбции входящих газов. Следовательно, показано, что короткие ступени с низким сопротивлением могут быть спроектированы таким образом, чтобы достигнуть высоких степеней абсорбции в соответствии с пределами термодинамической эффективности. Иными словами, физический процесс удаления CO2 протекает при уровнях абсорбции, которые могут несомненным образом отвечать термодинамической эффективности системы или выходить за ее пределы. Такие высокие степени абсорбции (входящий газ, выходящий газ) не принимают во внимание энергию и, следовательно, образование CO2. Поэтому поддержание степеней абсорбции CO2 (из текучей среды) и термодинамической эффективности оборудования как двух, безусловно, разных мер важно, чтобы избежать путаницы.
Результаты от Фиг. 2B и 2C (абсорбция CO2 текучей средой) и соотношение ионов в продукте (1,0 = бикарбонат, 2,0 = карбонат) отображены на Фиг. 2D и 2E. Несколько важных выводов может сделано из данных на Фиг. 2B и 2C:
(1) Отмечались такие высокие мгновенные степени адсорбции, как 98% в одиночной ступени абсорбции поступающего CO2.
a. Чистый бикарбонат (NaHCO3) производился в растворе при таких условиях, когда абсорбировалось 25% поступающего CO2 в контакторе газ-жидкость в виде одноступенчатой барботажной колонны с глубиной текучей среды/расстоянием соприкосновения газ-жидкость 0,30 м. Экстраполяция до абсорбции 90% показывает, что расстояния соприкосновения в 3 метра достаточно, чтобы абсорбировать 90% поступающего CO2.
a. Чистый карбонат (Na2CO3) производился в растворе при таких условиях, когда абсорбировалось 70% поступающего CO2 в контакторе газ-жидкость в виде одноступенчатой барботажной колонны с глубиной текучей среды/расстоянием соприкосновения газ-жидкость 0,30 м. Экстраполяция до абсорбции 90% показывает, что расстояния соприкосновения <2 метров достаточно, чтобы абсорбировать 90% поступающего CO2.
c. Различные соотношения карбонатных ионов в продуктах в зависимости от абсорбции показывают, что между этими предельными величинами существует сплошной спектр растворов.
(2) Абсорбирующая текучая среда сохраняет свои абсорбционные характеристики в течение промежутков времени, соответствующих промышленным масштабам (например, 15-240 минут в этих примерах).
(3) Переменные на входе реактора (концентрация, температура, давление, расход газа, время соприкосновения и т.д.) могут быть отрегулированы, чтобы получать чистый бикарбонат, чистый карбонат или их любую промежуточную смесь.
(4) Применение результатов этих лабораторных исследований, чтобы спроектировать реактор с 90% CO2, приводит к решениям с расстоянием соприкосновения газ-жидкость менее 3 м (например, примерной глубиной текучей среды, высотой колонны) и 1 м во многих случаях процесса промышленного масштаба.
Пример 4
Анализ низковольтного электролиза (LVE) для разных химических условий
Фиг. 5 представляет собой график, показывающий рабочие характеристики низковольтного электролиза рассола для разных химических условий. Она отображает некоторые типичные экспериментальные результаты, в которых мембранная хлорощелочная ячейка функционирует при нестандартных условиях, а именно:
(1) pH анолитной текучей среды (протонированного рассола) регулируется посредством контроля pH с применением обратной связи и контролируемого добавления HCl (хлористоводородной кислоты в воде) при pH 1,0, 2,5 и 5,0;
(2) температура анолитной текучей среды поддерживается при заданном значении посредством обратной связи контурами с текучей средой, нагреваемыми электрическими нагревателями; и
(3) напряжение регулируется для каждого условия текучая среда/протонирование/температура при регистрируемом токе через хлорощелочную ячейку 0,01 м2.
На Фиг. 5 представлен ряд экспериментальных данных для этого примера, которые отображают в виде графика фактическое экспериментальное напряжение в зависимости от тока (переводимого в плотности тока, кА/м2, как показано на графике) для электролизной ячейки 0,01 м2, с зазором 13 мм, функционирующей при разных комбинациях температуры и степени протонирования анолитного рассола в качестве текучей среды (регулируемой в этой серии экспериментов контролем pH с применением цепи обратной связи посредством добавления HCl (в виде жидкости) в контур с рассолом.
Следует заметить следующее в отношении этих типичных результатов на Фиг. 5:
(1) При высоких напряжениях (5 В), таких как те, что обычно используются при хлорощелочном применении таких ячеек, обеспечивался максимальный ток (и для данной ячейки, следовательно, максимальная плотность тока).
(2) Более высокая температура рассола при одной и той же величине pH приводила к более высокой плотности тока при данном напряжении.
(3) Более низкая величина pH рассола приводила к увеличенной плотности тока при данном напряжении по сравнению с более высокой величиной pH рассола.
(4) Эти общие тенденции (более высокая температура, более высокая концентрация кислоты) могут быть оптимизированы обычными методами планирования экспериментов для каждой индивидуальной электрохимической ячейки со своей геометрией/компонентным составом, чтобы обеспечить оптимум (кА/м2В) для этой ячейки. Подобные эксперименты для любой хлорощелочной ячейки с увеличенным рабочим давлением приведет к заключению, что увеличенное рабочее давление также улучшает (кА/м2В).
(5) Наклон линий (ΔV/ΔA) является первоначально большим, при сравнительно больших падениях напряжения, происходящих при сравнительно малых падениях тока/плотности тока; однако после достижения точки перегиба (при примерно (2,5V, 10 А/0,01 м2) дальнейшие снижения напряжения приводят к значительным уменьшениям тока и, соответственно, плотности тока.
(6) Эта точка перегиба и соседняя область рабочих условий представляет собой оптимальный компромисс для зависимости напряжения от плотности тока в экономическом аспекте эффективности. Стандартная оптимизация проведения экспериментов может обеспечить достижение оптимального условия с низким напряжением для любого варианта реализации на практике ячейки по данному изобретению.
(7) Применительно единственно к этому примеру, условие для анолита, заключающееся в pH 1,0 и 90°C, предоставляет лучшую Вамперную характеристику, которая, соответственно, является оптимальной рабочей характеристикой, представленной среди этих разных продемонстрированных рабочих характеристик.
(8) Основным недостатком электролиза при низком напряжении является сопутствующее уменьшение плотности тока; величина кА/м2 уменьшается с уменьшением напряжения. Поскольку система должна производить одно и то же число ионов Na+, чтобы абсорбировать одно и то же количестве диоксида углерода, площадь в м2 поверхности мембраны должна быть пропорционально увеличена; например, если плотность тока падает на 50%, то потребуется увеличенная в два раза площадь мембраны, чтобы производить достаточное количество абсорбирующей текучей среды. Это оказывает значительное влияние на стоимость оборудования, поскольку стоимость хлорощелочного оборудования примерно пропорциональна площади мембраны. Низковольтный электролиз предоставляет несколько преимуществ, которые могут, в некоторых вариантах осуществления данного изобретения, обеспечить возможность оптимизации в соответствии с низковольтными характеристиками, которые существенно или полностью компенсируют этот недостаток, связанный с необходимостью большой площади. А именно, могут быть продлены сроки службы мембран и компонентов электролитической ячейки с рассолом, которые функционируют в более мягких/менее энергетически жестких рабочих условиях, которые могут увеличивать долговечность ячейки и/или мембраны. При проектировании специально для условий низкого напряжения может быть уделено внимание некоторой способности к релаксации определенных материалов и критериям эффективности функционирования, которые не рассматриваются как основные в вариантах осуществления с применением низкого напряжения. Некоторые из этих степеней свободы проектирования могут приводить к пониженной стоимости ячеек, что частично или полностью компенсирует увеличенную стоимость мембраны ячейки, изначально обусловленную функционированием при низком напряжении/низкой плотности тока. Посредством этих и многих других способов системы LVE, несмотря на то, что они требуют больших площадей мембраны по сравнению со стандартными хлорощелочными ячейками для производства одного и того же количества NaOH, могут полностью или частично смягчить некоторые из этих дополнительных расходов и эксплуатационных издержек.
(9) Компромисс между преимуществом (более низкое напряжение и, следовательно, более низкая мощность) и недостатком (увеличенная площадь и уменьшенная плотность тока) может быть оптимизирован посредством методики, описанной в Примере 7. Для рабочей характеристики 1,0/90°C, изображенной на Фиг. 5, (которая для этой небольшой группы примеров является лучшей Вамперной характеристики для функционирования LVE), может быть рассчитано Voptlve, и из указанной выше зависимости может быть получен Ioptlve. Следовательно, для данной геометрической конструкции электролизной ячейки, условий температуры, давления, концентрации рассола, степени протонирования, выбора мембраны и т.д. может быть все сделано, чтобы получить лучшую Вамперную кривую или рабочую характеристику, и затем для этой кривой может быть рассчитана оптимальная точка способом по Примеру 7. В этом случае Voptlve составляет 2,88 В и плотность тока Ioptlve составляет 1,04 кА/м2.
(10) В Примере 7 ток при Vopt=2,88 В составляет примерно 5 А в случаях с небольшим протонированием и/или низкой температурой. В рассматриваемом примере ток (и, следовательно, плотность тока) была увеличена более чем в два раза до 10,4 А.
(11) Дополнительное протонирование рассола, температура, давление, концентрация, геометрическое расположение компонентов ячейки, электрические поля и условия могут быть подобным образом оптимизированы, чтобы создать лучший показатель (кА/м2В), однако протонирование само по себе увеличивает количество произведенного стехиометрического водорода, увеличивая тем самым энергоокупаемость системы. Важно заметить, что оптимизация для наименьшей энергии абсорбции/конверсии CO2 может быть достигнута как оптимизацией (кА/м2В) системы, которая уменьшает энергию, требующуюся для производства абсорбирующей текучей среды, так и одновременной оптимизацией получения водорода, доступного для извлечения энергии (и затем оптимизацией эффективности, с которой извлекается энергия этого доступного водорода), и энергия в целом для процесса может быть оптимизирована до ее наименьшего потенциала, для данной практической электрохимической ячейки конкретной конструкции.
(12) В связи с тем, что варианты осуществления данного изобретения могут эффективно абсорбировать CO2 в чрезвычайно разбавленных растворах гидроксида (было продемонстрировано для 0,2M и менее) по сравнению с концентрированными растворами гидроксида, обычно получаемыми в хлорощелочном производстве (типично 33-35% по массе, затем концентрируются дополнительно испарением воды), конструкция хлорощелочных ячеек для работы при низкой концентрации (а также для работы при низком напряжении) предоставляет новые степени свободы для оптимизации конструктивного исполнения при этих нестандартных условиях.
Варианты осуществления данного изобретения не могут нарушать второй закон термодинамики, производя больше энергии водорода, чем энергия, затраченная на производство этого водорода. Это создает предел для минимального напряжения, которое может быть приложено к электрохимической ячейке. В предположении 100%-ной эффективности для возврата энергии водорода и при применении энергосодержания H2 39000 кВт·ч/тонну (нормативная величина EIA) результатом будет являться минимальное напряжение 1,55 В для электролиза рассола. Специалист в данной области может для любой системы с установленной эффективностью водород/возврат электроэнергии и выбранной величины для энергосодержания системы вычислить минимальное достижимое напряжение для этой системы.
На практике факторы термодинамической неэффективности (включающие, однако не ограничивающиеся ими, джоулевы потери, неэффективность тока в ячейке, потери отходящей теплоты и т.д.) и требование о необходимости небольшого перенапряжения при функционировании увеличивают минимальное напряжение, достижимое для данной ячейки. Рассмотренные выше цифры могут несколько зависеть от величины "a", коэффициента протонирования для ионов, поскольку он изменяет количество водород, доступного для возврата энергии.
Тем не менее, плотность тока при низком напряжении определяет величину площади электролиза (хороший скалярный параметр для капитальных затрат), требующуюся для некоторого количества каустика, и при минимальном напряжении требуемая площадь чрезвычайно велика. Соответственно, для работы требуется некоторое напряжение выше минимального напряжения, величина которого зависит от компромисса между капитальными затратами и экологической эффективностью, выбранного в конструкции. Эффективность по току (процентная доля тока, использованного при производстве продукта) уменьшается при низком напряжении, так что оптимизация операции электролиза рассола при низком напряжении не является такой же, что и достижение единственно условия функционирования при низком напряжении. Данные процессы разработаны для функционирования в режиме LVE (ниже 5 В), и при этих напряжениях ниже 5 В потребление мощности существенно улучшается по сравнению с обычными методами.
Пример 5
Термодинамика крупномасштабной конструкции электростанции
Для этого примера разъясняется модель электростанции (включающая определенные варианты осуществления данного изобретения), демонстрирующая работу полномасштабного действующего предприятия, и количественно определяется энергия, требующаяся для извлечения заданного количества CO2, ограничиваемая статистическими пределами, с применением различных средств и способов, включающих следующие:
(1) Термодинамическая эффективность (∂CO2/∂E) может быть приближенной выражена как ΔCO2/ΔE на протяжении достаточно коротких интервалов E (энергии).
(2) Определенные упрощающие допущения могут быть сделаны в отношении конструкции электростанции, такие как те, что представлены на Фиг. 9A, среди них:
a. Основной расход энергии происходит в процессе электролиза; нагнетание, сжатие, управление и т.д. рассматриваются как незначительные по отношению к затратам энергии на изготовление реагентов (электролиз) и при извлечении энергии водорода. Эти величины принимаются равными нулю или <0,1% от мощности, потребляемой в операциях электролиза.
b. Затраты энергии на электролиз могут быть представлены в примерном виде следующим уравнением:
Eout=V·I·EFFcurrent
где V = рабочее напряжение электролизной ячейки
I = ток, требующийся для производства химикатов электрохимической полуреакцией, включающей стехиометрию более чем 1:1, обусловленной протонированием рассола. В данном примере используется соотношение протонирующих ионов 0,05HCl/NaCl, расходуемых при электролизе.
EFFcurrent = эффективность по току, определяющая величину тока, используемую в фактическом производстве химических веществ, при остальном токе, являющемся потерями на джоулево тепло и т.д. В данном примере используется величина, составляющая 97%; каждая электролизная ячейка будет иметь свою собственную уникальную эффективность по току, которая ухудшается и изменяется в течение срока службы ячейки.
c. Энергия, извлекаемая из сжигания водорода (любыми средствами, сжиганием в качестве бойлерного газа, сжигание в топливном элементе и т.д.), определяется как
Ein = 39000 кВт·ч/тонну сжатого H2 ·Число тонн H2 ·EFFdc
где Число тонн H2 = число тонн водорода, произведенного процессом, включая водород, произведенный посредством стехиометрии более чем 1:1, обусловленной протонированием рассола.
EFFdc = эффективность процесса утилизации водорода при конвертировании исходной энергии газообразного водорода в энергию постоянного тока. 60% энергии произведенного водорода извлекается с преобразованием в энергию постоянного тока и применяется для питания большей части процесса электролиза. Имеется несколько средств, посредством которых может быть достигнут этот вид эффективности, включающих, однако не ограничивающихся ими: топливный элемент, турбина для сжигания водорода, смешивание водорода с альтернативным топливом, таким как природный газ, и сжигание в механизме, оптимизированном для этого вида топлива Тепловые коэффициенты полезного действия турбин на водороде (масштаба электростанций) вплоть до 70% могут быть найдены в современной литературе.
d. Энергия, возвращаемая рекуперацией отходящей теплоты, извлекается из теплоты потока поступающих дымовых газов. Поступающие нагретые газы охлаждаются при введении в процесс. В некоторых вариантах осуществления данного изобретения, это охлаждение может быть выполнено поглощением отходящей теплоты и конверсией этой теплоты в электрическую энергию постоянного тока, которая может быть использована для дополнительного/полного/избыточного питания процесса, который составляет данное изобретение. В этом примере рекуперация дополнительной отходящей теплоты не включена.
Структура электростанции для этого примера включает моделирование дымовых газов, выпускаемых от электростанции при нормальных рабочих условиях, как показано на Фиг. 9B. Это включает значительные допущения в отношении состава видов топлива, эффективности самих процессов сжигания, относительной пропорции элементов в процессах сжигания и т.д. Допущения для этого примера представлены на Фиг. 9B и согласуются с выпуском дымовых газов типичной электростанции на слабобитуминозном угле с тепловой мощностью 10000 БТЕ/кВт·ч.
Для данного выпуска дымовых газов имеется потребность в гидроксиде, которая может быть вычислена. Некоторые расчеты приведены здесь. Соотношение ионов ("соотношение ионов" представляет собой соотношение Na/C в реакции абсорбции/конверсии) является таким же, что и соотношение этих элементов в образованном твердотельном продукте. В случае чистого бикарбоната данное соотношение будет составлять 1,0, в случае чистого карбоната соотношение будет составлять 2,0, и для смеси бикарбоната и карбоната соотношение будет находиться между 1,0 и 2,0. Расчет потребности в каустике для этого примера представлен на Фиг. 9C. Для примера, представленного на Фиг. 9C, соотношение ионов составляет 1,0.
Для данной потребности в гидроксиде имеется соответствующая потребность в токе для электролиза, базирующаяся на количестве воды, соли, квадратных метрах поверхности мембраны (скалярный параметр для электрохимических ячеек этого вида) и плотности тока (зависящей от конструкции ячейки, химии процесса и рабочих условий; здесь использована величина 3 кА/м2). Эти расчеты необходимых условий электролиза для этого примера представлены на Фиг. 9D.
Для данной степени электролиза при условиях протонирования имеется заданное количество произведенного газообразного водорода, который сам по себе представляет определенное количество энергии, доступной для извлечения, или же водород используется химическим образом при последующей обработке.
Для данного количества произведенных дымовых газов имеется определенное содержание энергии в отходящей теплоте, которое может быть извлечено из нее при определенной эффективности преобразования в энергию постоянного тока, и это извлеченная электроэнергия может быть использована, чтобы компенсировать энергию постоянного тока, израсходованную процессом при электролизе. Отходящая теплота для этого примера представлена на Фиг. 9E, при выбранной эффективности, в этом случае при 25%, величине, которая превышается различными методами генерации постоянного тока из отходящей теплоты, существующими в настоящее время в данной области.
При этих индивидуальных компонентах ввода и вывода энергии результирующий эффект этих передач энергии может быть обобщен так, как это представлено на Фиг. 9F. На ней энергии представлены в кВт·ч и как процентные доли от базовой мощности электростанции и показан расчет экологической эффективности для этого примера.
В некоторых вариантах осуществления данного изобретения дополнительный топливный элемент H2/Cl2 может быть применен для сжигания газообразных водорода и хлора с целью рециркуляции HCl, использованного для протонирования рассола. В частности, данное количество "сверхстехиометрического" HCl может быть использовано повторно, и теоретически, устранять потребность в добавлении HCl в виде исходного химиката в систему. В реальной практике в систему должно периодически добавляться определенное количество компенсирующего HCl. Сжигание H2 в Cl2 высвобождает больше энергии, чем при сжигании H2/O2. Однако влияние присутствия дополнительных протонов при электролизе должно существенно катализировать производство NaOH при низких напряжениях и высокой величине (кА/м2В) при этих низких напряжениях. Следовательно, для любого данного устройства может быть выполнена оптимизация, чтобы рециркулировать заданное количество H2/Cl2 в HCl и чтобы протонировать поступающий рассол этим количеством HCl. При некоторой оптимальной величине (обычно находящейся между a=0,05 и a=1,0M, или вблизи pH 1 при 90°C) потери в топливном элементе водород/хлор (которые превосходят небольшую выгоду по сравнению с окислением кислородом, предоставляемую хлором) и энергетическая выгодность гидроксида (лучше кА/м2В) будут одновременно оптимальными для системы в целом. Следует заметить, что в этом примере рассчитывается лишь сжигание H2/O2; сжигание H2/Cl2 предоставляет незначительный термодинамический выигрыш от экстрапрочности окисления хлора, однако обратное действие тепловой неэффективности создает слабонегативный, однако рассматриваемый как незначительный, эффект.
A. Расчет экологической эффективности
Расчет экологической эффективности (∂CO2/∂E) и ΔCO2/ΔE для этого примера был выполнен следующим образом:
(1) Было предположено, что имеются три электростанции:
a. Базовая электростанция (приведенная в качестве примера в модели дымовых газов на Фиг. 9B)
b. Электростанция с абсорбцией/конверсией CO2 (которая требует дополнительной мощности для обработки дымовых газов от базовой электростанции и возвращает часть этой мощности от сжигания водорода или расчетной мощности, содержащейся в водороде, если водород является конечным продуктом и не сжигается.
c. Третья, дополнительная, электростанция, которая предоставляет мощность, требующуюся для электростанции с абсорбцией/конверсией CO2. В этом примере характеристики этой электростанции были приняты те же самые, что и для базовой электростанции.
(2) Затем рассчитывались следующие аспекты, относящиеся к CO2 и энергозатратам при обработке 100% для базовой электростанции:
a. CO2 от базовой электростанции (модель дымовых газов)
b. Энергия, произведенная базовой электростанцией
c. Нетто-энергия, требующаяся для процесса абсорбции/конверсии CO2.
d. Нетто-энергия, требующаяся дополнительной электростанцией, предполагается идентичной нетто-энергии, требуемой процессом абсорбции/конверсии CO2.
e. Количество CO2, произведенное дополнительной электростанцией, принимается как пропорциональное энергии, произведенной дополнительной электростанцией, и при той же величине ΔCO2/ΔE, что и для базовой электростанции.
(3) Для указанных выше расчетов были получены следующие результаты:
a. Базовая электростанция - электростанция с тепловой мощностью 10000, производящая 1 ГВт постоянно в расчете на 1 год, производит 8,76 млрд кВт·ч каждый год и выпускает 7446068 тонн CO2 в год, что составляет в среднем 1176 кВт·ч/тонну CO2.
b. Электростанция с абсорбцией/конверсией CO2 - расчет для этого примера (a=0,10, функционирование при 2,1 В, производится чистый бикарбонат, 15% энергии водорода расходуется при сжатии, расходы на нагнетание/сжатие и выгоды от рекуперации отходящей теплоты исключены), 3,648 млрд кВт·ч требуется для абсорбции/конвертирования 100% CO2 базовой электростанции.
c. Дополнительная электростанция - электростанция в этом примере вырабатывает мощность, требующуюся для электростанции с абсорбцией/конверсией CO2, 3,648 млрд кВт·ч, и сама производит (в соответствии с величиной 1176 кВт·ч/тонну CO2, указанной выше) суммарно 3101209 тонн CO2, который предназначен для выпуска в атмосферу.
d. Суммарная генерированная мощность, следовательно, составляет 12,48 ГВт·ч. Общая поставленная мощность составляет, следовательно, 8,76 ГВт·ч. Общее количество образованного CO2 составляет, следовательно, 10,55 мегатонн. Общее количество выпускаемого CO2 составляет, следовательно, 3,101 мегатонн. 29,1% от общей мощности расходуется в процессе абсорбции/конверсии CO2. 71,9% от общего количества CO2 потребляется.
Несколько ключевых моментов иллюстрируются приведенными выше расчетами:
(1) Арифметически, продемонстрировано, что применяются следующие формулы:
% потребленной мощности = 1-% потребленного CO2
% потребленного CO2 = 1-% потребленной мощности
Это образует линию, называемую рабочей характеристикой одного узла, показанную на Фиг. 9A.
(2) Для этого примера (∂CO2/∂E) и ΔCO2/ΔE алгебраически идентичны, а именно:
∂CO2/∂E=(∂CO2/∂E)=0,291/0,719=0,41
Кроме того, могут быть также смоделированы другие экстраполированные случаи, в которых CO2, эмитированный дополнительной электростанцией, сам обрабатывается другим узлом №2 для выполнения процесса абсорбции/конверсии CO2 соответствующей меньшей производительности, и этот узел №2 абсорбции/конверсии соответственно получает питание от дополнительной электростанции №2, и т.д., что приводит к результатам, подобным тем, что представлены в таблице 2 для первых пяти последовательностей итераций.
Несколько моментов, относящихся к таблице 2, важны для данной модели:
(1) Следует заметить, что эффективность процесса, в базовом случае или в любом из случаев последующих итераций, равным образом создает одну и ту же величину (∂CO2/∂E) для системы; эта величина считается постоянной для системы, которая приближенно соответствует ограничениям этой модели и называется, для этих целей, экологической эффективностью процесса.
(2) Ясно, что величина (∂CO2/∂E) постоянна во всех решениях, так что решение может быть получено, когда число итераций предполагается бесконечным, т.е. когда электростанция функционирует таким образом, чтобы потреблять 100% CO2, произведенного электростанцией, посредством простого приема с применением следующего уравнения:
1/(∂CO2/∂E)=% мощности электростенции, требующейся для абсорбции/захвата 100% произведенного CO2
В случае данного примера расчет дает величину 41,6%.
(3) В качестве альтернативы, очевидно, что если нетто-мощность, затраченная на абсорбцию/конверсию, равна нулю (пренебрежимо малое извлечение отходящей теплоты), для данного условия процесса количество абсорбированного и конвертированного CO2 аналогичным образом рано нулю. Следовательно, все рабочие характеристики для электростанций этого типа теоретически пересекаются при (0% мощности, 0% CO2).
(4) Задавая любые две точки в линейной системе, могут быть созданы прямолинейные решения для рабочих линий, которые определяют рабочие характеристики процесса абсорбции/конверсии CO2 следующим образом:
a. для каждого рабочего условия выполняется решение для базового случая, и результирующая точка для решения в случае с одним узлом (% мощности, % CO2) наносится на график зависимости % CO2 (ось y) от % потребленной нетто-мощности (ось x);
b. для этого случая вычисляется (∂CO2/∂E), и для случая с y=100% определяется координата x; и
c. предполагается, что все линии проходят через начало координат. В реальных системах может иметь место некоторое потребление мощности (системы управления, окружение и т.д.) даже при нулевой абсорбции, так что это является идеализированным случаем. На практике эти линии могут быть слегка искривлены и не заканчиваться в начале координат.
(5) Таким образом, может быть создано семейство рабочих характеристик для процессов абсорбции/конверсии CO2 этого типа.
(6) На график такого же типа также могут быть нанесены и сравнены графически конкурентные технологии, например:
a. Конкурентная технология абсорбции MEA (метилэтиламином), потребляющая 30% мощности электростанции, чтобы выполнить абсорбцию 58% CO2, эмитированного перед тем, как была внедрена абсорбция.
b. Кроме того, предположительно 15% мощности электростанции расходуется при ожижении этого CO2 посредством цикла с приложением высокого давления и охлаждением (45% мощности/58% CO2).
c. Это могло бы в таком случае продемонстрировать величину ((∂CO2/∂E), составляющую 1,24; однако имеется дополнительная неучтенная энергия, требующаяся для транспортировки/инжекции/сохранения CO2 на месте связывания.
d. Графически эта конкурентная технология проявляется как менее эффективная, чем пример процесса функционирования электростанции с абсорбцией/конверсией CO2, который является одним из вариантов осуществления данного изобретения; т.е. эта модель показывает, что конкурентная технология потребовала бы 70%+ мощности электростанции, чтобы устранить 100% производимого ею CO2. Следует отметить такие моменты, относящиеся к конкурентной технологии, графически представленные на Фиг. 9A (при ссылках на легенду на графике):
i. В соответствии с оценками 2005 EIA, абсорбция CO2 посредством технологии MEA требует 30% мощности электростанции, чтобы абсорбировать 58% CO2 из произведенных дымовых газов. (Отмечено место на графике на Фиг. 9A (30%, 58%) для одной лишь обработки абсорбцией.)
ii. Посредством таких же оценок, сжатие/ожижение такого количества CO2 потребляет еще 15% мощности электростанции, перемещая рабочий режим такой электростанции к (45%, 58%).
iii. Отсутствует надежная оценка энергии, требующейся для транспортировки жидкого CO2 по трубопроводу или посредством другого транспортирующего устройства, а также вдобавок количества энергии, необходимой для закачивания или инжекции этого CO2 в углеродное хранилище различного рода, и количества энергии, которая может потребоваться для поддержания этого CO2 в указанных хранилищах в течение неограниченного срока. Однако, хотя эти дополнительные количества энергии не могут быть оценены, представляется разумным предположение, что они не равны нулю. Следовательно экологическая эффективность такого устройства, логически рассуждая, хуже, чем компромисс (45%/58%) в затратах мощности, чтобы обеспечить определенную выгоду при уменьшении выбросов CO2. Экстраполяция этой величины до случая удаления 100% показывает, что технология MEA/ожижение/связывание потребляла бы более 70% мощности электростанции. Следует заметить, что типичные конкурентные технологии абсорбции не могут приближаться к 100%-ной абсорбции; т.е. величина абсорбции CO2 58% относилась к электростанции, для которой обрабатывалось 100% отходящих дымовых газов.
B. Расчет пределов экологической эффективности [(∂CO2/∂E)max]
На практике, для данной системы, которая эффективно конвертирует весь произведенный NaOH в NaHCO3 посредством абсорбирования CO2, основным энергетическим показателем является величина кВт·ч/моль NaOH. Хотя мощность в расчете на моль NaOH пропорциональна как напряжению, так и току, ток фиксируется стехиометрией химии процесса. Соответственно, мощность, затраченная на моль CO2, оптимизируется главным образом посредством достижения наименьшего напряжения, при котором эффективно производится гидроксид.
Минимальное напряжение, при котором система для электролиза в соответствии с вариантами осуществления данного изобретения функционирует (как она сконфигурирована в отношении различных концентраций, геометрических размеров, расходов и т.д.), может быть определено посредством наблюдения плотности тока (кА/м2) в зависимости от характеристик напряжения системы и определения наименьшего напряжения, при котором получают значительные ненулевые плотности тока, чтобы изготовить продукт. Изменение физических размеров, узлов генерации электрического поля, геометрии ячеек, состава материалов и условий обработки, чтобы оптимизировать эту характеристический показатель (кА2/м2В), является основным средством оптимизации этих систем, и типичные методик планирования экспериментов применимы для оптимизации производственного процесса для данной физической электростанции.
Помимо практических ограничений, имеется один фундаментальный предел, который применим ко всем системам с заданным соотношением H/Na (коэффициентом протонирования для ионов), а именно:
(1) Устройство не может функционировать таким образом, чтобы производить больше энергии посредством извлечения энергии водорода, чем вводится в систему в ходе электролиза. Для знакомых с термодинамическими принципами будет понятно, что это явилось бы нарушением второго закона термодинамики.
(2) Как результат этого, фундаментальный термодинамический предел может быть ограничен, предоставляя выбор соотношения H/Na, использованного в потребляемом анолите:
a. Для этого примера предполагалось, что H/Na составляет 0,10.
b. Эффективность возврата энергии водорода была установлена при 100%.
c. Было вычислено наименьшее напряжение, при котором может происходить процесс, в котором нетто-энергия, потребляемая системой, равна нулю ("Vmintheo") (т.е. точка, в которой затраты на электролиз равны предполагаемой эффективности возврата энергии водорода 100%).
d. В этом примере это низкое напряжение составляло 1,5526 В. Эта величина сильно зависит от соотношения Na/C, соотношения H/C и эффективности возврата энергии водорода. В этом оптимальном случае Na/C составляет 1,0, и H/C составляет 1,0.
e. При доведении этого расчета до экологической эффективности, решение для единственного узла составляет примерно 7% мощности для абсорбции/конверсии 93% CO2.
f. Обработка в более эффективных рабочих режимах по сравнению с этим теоретическим минимумом возможна посредством:
i. восполнения потребляемой мощности рекуперацией отходящей теплоты; и
ii. энергоснабжения процесса абсорбции/конверсии частично или полностью мощностью, производство которой не вызывает эмиссии CO2 (энергия от гидроэлектростанций, солнечная энергия, энергия ветра, ядерная энергия и т.д.).
Подобным образом, в предположении идеальной эффективности возврата энергии водорода и т.д., как выше, было рассчитано максимальное напряжение, при котором функционирование может быть "экологичным" ("Vmaxeco") (т.е. при котором процесс абсорбции/конверсии CO2 удаляет больше CO2, чем создает):
a. H/Na, Na/C и эффективность возврата энергии водорода были установлены при 1,0, 1.0 и 100% соответственно, как и выше.
b. Рассчитывалось напряжение, при котором удаление CO2 составляло бы 50%.
c. В этом примере, величина Vmaxeco составляет 4,457 В. При этом напряжении и условии процесс протекает на линии ∂CO2=∂E, границе между экологически благоприятным и экологически вредным функционированием.
Следовательно, экологически благоприятное функционирование будет происходить, когда система для электролиза функционирует между Vmintheo (1,5526 В) и Vmaxeco (4,457 В). Функционирование между этими двумя точками может быть воспроизведено многими типичными системами для электролиза. Лабораторные результаты при 2,1 В или ниже могут быть легко воспроизведены посредством регулирования геометрии, концентрации, температуры, давления, расхода и т.д. для электрохимических ячеек, сконструированных таким образом.
C. Влияние электростанции, не создающей парниковый эффект, на экологическую эффективность
Там, где дополнительная электрическая мощность (та, которая питает процесс) производится электростанцией, не эмитирующей газов, создающих парниковый эффект, (GHG) (например, ветряной электростанцией, гидроэлектростанцией, от солнечной энергии, от ядерной энергии и т.д.), дополнительные выбросы CO2 равны нулю, и экологическая эффективность данного изобретения значительно улучшается. Для этого примера, величина 3101209 тонн CO2 в таблице 2 устраняется вместе со всеми другими последующими итерациями и т.д., предоставляя следующий упрощенный результат: весь CO2 абсорбируется/конвертируется (7446069 тонн), и требуемая общая мощность составляет просто 8760000000 в качестве базиса плюс 3648448267 кВт·ч, требуемых для выполнения работы, необходимой, чтобы абсорбировать/конвертировать это базовое количество CO2; требуется лишь 29% от общей мощности, чтобы захватить 100% выбросов CO2 в ходе процесса с электропитанием без образования парниковых газов, по сравнению с 41% от общей мощности, чтобы захватить 100% выбросов CO2 в ходе процесса с электропитанием с образованием парниковых газов. Это означает, что варианты осуществления данного изобретения предоставляют эффективное средство для "заимствования" энергии, когда процесс получает питание при отсутствии выбросов газов, создающих парниковый эффект. Если вместо применения электроэнергии, полученной без образования газов, вызывающих парниковый эффект, для замены электроэнергии, полученной с образованием газов, вызывающих парниковый эффект, на основе 1%:1%, электроэнергия, полученная без образования газов, вызывающих парниковый эффект, используется для питания процессов, которые представляют собой некоторые варианты осуществления данного изобретения, то 1% электроэнергии, полученной без образования газов, вызывающих парниковый эффект, замещает электроэнергию с образованием газов, вызывающих парниковый эффект, с увеличенным коэффициентом, даже сверх электроэнергии, полученной с образованием газов, вызывающих парниковый эффект, в примерах, описанных в данном документе. Можно легко представить случаи, в которых, для данного государства, штата или объекта, определенная доля электроэнергии, полученной без образования газов, вызывающих парниковый эффект, при использовании этим увеличенным образом, могла бы более эффективно обеспечить выполнение любой задачи по снижению выброса CO2; т.е. возможно применение "чистой" мощности с высокой степенью заимствования, чтобы очистить выбросы другой, "грязной" мощности.
В связи с тем, что в некоторых видах применения доступна генерация электроэнергии без образования газов, создающих парниковый эффект, иногда в спорадической форме (например, от солнечной энергии, "парков" ветряных электростанций и т.д.), возможность применения этой мощности, чтобы получить большие количества абсорбента во время непиковых нагрузок, является чрезвычайно выгодным.
Пример 6
Экологическая эффективность различных смоделированных электростанций
Фиг. 10 показывает экологическую эффективность различных смоделированных электростанций, включающих варианты осуществления данного изобретения, и представляет различные условия, которые являются основными факторами в определении экологической эффективности ((∂CO2/∂E)).
Из этих расчетов могут быть в целом сделаны следующие выводы:
(1) При образовании карбоната натрия и применении стандартных хлорощелочных условий процесс мог бы иметь экологическую эффективность >1, и, несмотря на то, что такое функционирование может быть экономически осуществимо, оно производит больше CO2, чем абсорбирует.
(2) Изменение равновесного продукта, чтобы способствовать производству бикарбоната натрия, улучшает экологическую эффективность процесса. В случае изменения условий, таким образом, для производства практически чистого бикарбоната натрия это преимущество является полностью оптимизированным.
(3) Принятая практика низковольтного электролиза надежно смещает процесс в область функционирования, характеризующуюся экологическими эффективностями менее 1,0 (т.е. экологически выгодными процессами абсорбции и конверсии CO2). Оптимизация каждого физического осуществления системы для электролиза достижения для оптимума (кА/м2В) и максимального производства энергии водородом приводит к дополнительному улучшению экологической эффективности.
(4) Связывание процесса абсорбции/конверсии вариантов осуществления данного изобретения с любым числом имеющихся в наличии или созданных для этой цели устройств, которые конвертируют отходящее тепло в электроэнергию постоянного тока, первоначальное вложение энергии в электролиз постоянного тока и нагнетание переменного тока и т.д., могут пополняться или полностью снабжаться от рекуперации отходящей теплоты. Следует заметить, что снабжение в данном изобретении мощностью от генераторов электроэнергии, не выпускающих газы, вызывающие парниковый эффект, делают возможным проведение процесса с непосредственным приближением к 100% абсорбции CO2 (см. обсуждение в Примере 5).
Пример 7
Определение Voptlve (оптимального низкого рабочего напряжения по отношению к емкости или площади ячейки) и Ioptlve (тока при этом рабочем напряжении) для данной рабочей линии Вамперной характеристики для оптимизированной хлорощелочной ячейки для LVE
Здесь показано, что функционирование при пониженном напряжении снижает мощность, требующуюся для производства гидроксида натрия, который применяется в качестве абсорбирующей текучей среды. Таблица 3 показывает расчеты, сделанные из рабочей линии Вамперной характеристики в случае анолита 1,0/90°C на Фиг. 5 (обсуждено выше в Примере 4).
Несколько моментов следует отметить в отношении содержания таблицы 3:
(1) Третья колонка, эффективность по току (безразмерная), представляет долю образованного тока, которая используется в производстве химических продуктов; потери, такие как джоулевы потери и нагревание отходящих текучих сред при электролизе, являются основной причиной неэффективности. Эффективность по току уменьшается с уменьшением напряжения.
(2) Площадь ячейки нормализована для случая 3,975 В (в котором плотность тока, и, следовательно, условие процесса в отношении площади идентичны стандартному электролизу 5 В, проводимому при 3,0 кА/м2). Рассчитывается величина A2/A1 (безразмерная).
Последняя величина, % сбереженной мощности в расчете на безразмерную площадь, представлена на Фиг. 11. Для такой функции точка, при которой имеет место максимальный наклон (изменение используемой мощности в расчете на изменение напряжения), представляет собой оптимум; т.е. при низком напряжении (например, 2,1-2,5 В) наклон (Δмощность/Δм2) сравнительно малый, затем при более высоких напряжениях (например, от 2,5 до примерно 3) наклон (Δмощность/Δм2) возрастает до большей величины и после этого уменьшается до более низкого наклона, по мере того как напряжение продолжает увеличиваться. Это иллюстрирует то, что имеется область большого наклона, связанная с областью малого наклона с каждой стороны; т.е. с каждой стороны этой точки Voptlve изменение используемой мощности в расчете на изменение напряжения менее эффективно.
Вначале была определена функция, хорошо аппроксимирующая фактическое поведение (следует заметить, что формула линии полиномиального тренда получена подбором методом наименьших квадратов). В этом примере: y=-10,164×3+88,256×2-235,06x+198,37 является хорошей аппроксимацией. Затем была вычислена первая производная данной функции посредством обычной обработки полиномов: dy/dx=(3)(-10,164)×2+(2)(88,256)х-235,06 = максимум. Для величин x (вольты) может быть выполнена итерация, которая может быть осуществлена разными методами, чтобы найти максимум этой первой производной, давая в результате 2,894 В в качестве решения.
Следует заметить, что могут быть применены напряжения ниже 2,894 В, что будет предоставлять дополнительную экономию мощности. Некоторые предпочтительные варианты осуществления будут оптимизировать функционирование с низкой мощностью ниже этой "точки естественного оптимума". В таких случаях, применение дополнительной площади в мембране приведет к "субоптимизированной" системе электролиза, и функционирование при низкой мощности для процесса обезуглероживания в целом может извлечь дополнительную выгоду посредством работы ниже этого естественного оптимума для данной подсистемы электролиза. Однако если сделать так, то выгода от соотношения напряжение/мощность после этого уменьшается, наряду с тем, что фактор площади продолжает пропорциональным образом делать функционирование менее эффективным в расчете на площадь.
Ток и плотность тока, которые соответствуют этой величине Voptlve, могут быть определены либо посредством образования аналогичного соотношения методом наименьших квадратов для V и I, либо графически при использовании рабочей характеристики, чтобы определить Ioptlve. В этом примере рассчитанная величина составляет 10,419 А (или для площади ячейки 0,01 м2, как в этом случае), 1,042 кА/м2.
Пример 8
Уменьшение выбросов CO2 с утилизацией карбоната кальция
Представленный ниже вариант осуществления является дополнительным примером того, как общие концепции, описанные выше, могут быть подстроены к выгодным конкретным видам применения, содействовать производству конкретных конечных продуктов, уменьшать количество CO2, произведенного процессом, и/или увеличивать эффективность использования энергии электростанции. На основании идей, изложенных в данном описании, обычному специалисту в данной области будет понятно, что имеются многочисленные другие способы, которыми можно отрегулировать входы, выходы и эффективность использования энергии для данного изобретения.
Варианты осуществления, описанные в этом примере, могут быть применены там, где выгодно уменьшение выбросов CO2 на 50% без необходимости нейтрализации больших количеств хлора в щелочных осадках. Такие варианты могут осуществляться за счет замены функционирования форсунки электростанции процессом, который не является обязательно процессом с последующим сжиганием.
Как пояснено выше, в определенных типичных вариантах осуществления данного изобретения хлористоводородная кислота добавляется к хлориду натрия исходного соляного раствора хлорощелочной электролизной ячейки низкой мощности, предоставляя возможность протекания следующей реакции:
H2O+NaCl+aHCl+энергия→NaOH+(l/2+a/2)H2+(l/2+a/2)Cl2.
В других вариантах осуществления хлористоводородная кислота может не добавляться, предоставляя следующую реакцию:
2 NaCl+2H2O+энергия→2NaOH+H2 +Cl2
В этих вариантах осуществления производятся водород и гидроксид натрия. Как пояснено выше, гидроксид натрия может быть применен, чтобы абсорбировать диоксид углерода отходящего потока для образования карбоната натрия и бикарбоната натрия. Карбонат и бикарбонат натрия могут быть использованы выгодным образом в различных видах применения. Например, суспензионные смеси бикарбоната натрия и карбоната натрия могут быть помещены в виде суспензии в автомобиль-цистерну для применения в различных видах производства детергентов, в производстве стекла в качестве флюса и т.д., а также, как упоминалось выше, для различных видов обработки воды.
В определенных вариантах осуществления, включающих виды применения этой технологии на электростанциях, водород может быть возвращен, выпущен в форсунку электростанции и сожжен. "Повышенная теплота сгорания" (HHV) водорода может быть высвобождена и превращена в пар при сравнительно высоких величинах эффективности. В определенных видах применения может быть достигнута эффективность 88%. Крупномасштабное сжигание водорода может оказывать заметное влияние на рабочие параметры электростанции в целом. Например, в некоторых вариантах осуществления электростанция может быть преобразована из электростанции, работающей на угле (с соотношением водород:углерод 0,0), в "гибридную углеводородную" электростанцию, с соотношением водород:углерод 1,0. Такая электростанция будет производить больше воды в дымовых газах в результате сжигания водорода. В дополнение к этому, температура форсунки будет увеличена вследствие сжигания смеси водород/углерод, которая сгорает при более высокой температуре, чем один углерод.
Гибридная углеводородная электростанция (с соотношением H:C 1,0) производила бы мощность в расчете на тонну CO2 при производительности где-то между электростанцией, работающей на угле (с соотношением H:C 0,0), и электростанцией, работающей на природном газе (с соотношением H:C 3,73). Типичная электростанция, работающая на угле, производит мощность при средней производительности 1051 кВт·ч/тонну CO2, в то время как типичная электростанция, работающая на природном газе, производит мощность при средней производительности 1667 кВт·ч/тонну CO2. В предположении, что увеличение в мощности, произведенной в расчете на тонну выбросов CO2, линейно зависит от соотношения H:C, выработка электроэнергии гибридной углеводородной электростанцией была бы увеличена на 154 кВт·ч/тонну CO2 по отношению к производительности 1205 кВт·ч/тонну CO2. Возможно, что фактическая выработка электроэнергии гибридной углеводородной электростанцией была бы увеличена в большей степени, поскольку увеличение в произведенной мощности на тонну CO2 может быть не совершенно линейной. При сжигании водорода гибридная углеводородная электростанция имела бы выгоду не только от HHV водорода (903 кВТ·ч/CO2), но также имела бы увеличенную эффективность вследствие более высокой температуры форсунки (предполагается 154 кВТ·ч/CO2).
В дополнение к утилизации произведенного водорода, хлор также может быть использован выгодным образом в определенных вариантах осуществления. Более конкретно, хлор может быть перемещен, при первоначальном давлении, через воду, в которой он полностью диссоциирует, образуя хлористоводородную кислоту и хлорноватистую кислоту в соответствии со следующим уравнением:
Cl2+H2O→HOCl+HCl
При добавлении протона (предоставляемого солнечным светом или стимулированным ультрафиолетовым излучением) нестабильная хлорноватистая кислота (HOCl) разлагается, выделяя кислород в соответствии со следующим уравнением:
HOCl+HCl+hV363 нм→2HCl+1/2O2
В некоторых вариантах осуществления кислород может быть возвращен (несжатым, при первоначальном давлении) к входу форсунки электростанции. Присутствие кислорода дополнительно увеличивает интенсивность сжигания в форсунке электростанции и увеличивает рабочую температуру (а также эффективность). В некоторых вариантах осуществления оцененное увеличение эффективности составляет 5-10% в кВт·ч/тонну CO2. Увеличение этой величины привело бы к увеличению на 60-120 кВт·ч/тонну CO2 для обычной электростанции и могло бы улучшить общую эффективность электростанции от базового значения 33% до 34,5%, вплоть до 35,5%.
В некоторых вариантах осуществления удаление хлористоводородной кислоты могло бы быть выполнено посредством объединения кислоты с карбонатом кальция (легкодоступным и находящимся в таких источниках, как известняк) в соответствии со следующим уравнением:
2HCl+CaCO3→CaCl2+CO2 (газ)
Принимая во внимание то, что целью являлось удаление CO2 из потока, объединение хлористоводородной кислоты с карбонатом кальция может показаться парадоксальным, поскольку CO2 при этом производится. Однако тщательное рассмотрение применяемых химических реакций показывает, что только 50% CO2, первоначально абсорбированного гидроксидом натрия (NaOH), освобождается, когда хлористоводородная кислота объединяется с карбонатом кальция. А именно, каждый ион Na абсорбирует одну молекулу CO2 (в бикарбонат) и каждый ион Na производит один ион Cl. В дополнение к этому, при каждом разрушении каждой молекулы CaCO3 абсорбируется два иона Cl (с образованием CaCl2). Поэтому количество высвобожденного CO2 составляет половину от количества абсорбированного CO2. Образованный CO2 будет обладать некоторой величиной первоначального давления, которая может позволить пропустить его через турбину, чтобы извлечь из него некоторую мощность.
В некоторых вариантах осуществления энергия, израсходованная в процессе, описанном выше, относительно невелика, особенно по сравнению с другими процессами удаления CO2. Например, требующаяся общая мощность может быть определена как
Мощность=(-Электролиз+HHV-H2)+[Эффективность соотношения H:C+эффективность O2+эффективность CO2]
Представленные ниже величины могут быть использованы для оценки мощности, потребляемой для удаления CO2:
(-Электролиз+HHV-H2)=-347 кВт·ч/тонну CO2 (согласно исследованию Southwest Research Institute, которое будет вскоре опубликовано; эта величина исключает все эффекты отходящей теплоты и эффекты протонирования).
Эффективность соотношения H:C=+154 кВт·ч/тонну CO2 (в предположении линейной зависимости между углем и природным газом, которая является, возможно, оценкой с запасом)
Эффективность O2=+60 кВт·ч/тонну CO2 (установившееся нижнее значение)
Эффективность CO2=+0 (в предположении, что мощность не регенерируется пропусканием CO2 через турбину)
В некоторых вариантах осуществления общая мощность, требующаяся для удаления CO2, составляла бы, следовательно, 133 кВт·ч/тонну CO2. При применении на электростанции, генерирующей 1260 кВт·ч/тонну CO2, 10,5% мощности, произведенной электростанцией, могло бы быть применено для снижения выбросов CO2 на 50%. Такая система выигрывала бы при сравнении с существующими системами удаления CO2 с применением аминов, которые могут использовать 47% мощности, генерированной электростанцией, чтобы уменьшить выбросы CO2 на 90%.
Пример 9
Экологическая эффективность различных смоделированных электростанций
При рассмотрении влияния рабочей температуры на реакцию электролиза важно помнить, что термодинамическая потребность (брутто) процесса равна
Епотребность=-Еэлектролиз+Еводород
Выявлено, что при стандартных температуре (25°C) и давлении (1 атм (100 кПа)) энергия Гиббса требует, чтобы минимальная энергия для выполнения электролиза составляла -1230,6 кВт·ч/тонну CO2, и что теоретическая максимальная энергия, возвращаемая из водорода, составляет 903,6 кВт·ч/тонну CO2, давая потребность в энергии при 25°C, составляющую (-1230,6-903,6)=-327 кВт·ч/тонну CO2.
При повышенных температурах энергия, требующаяся для выполнения электролиза, снижается, поскольку расчетная величина свободной энергии Гиббса (которая определяет напряжение, при котором происходит электролиз) изменяется; однако, и это важно, энергия, извлекаемая из водорода, остается постоянной. Поэтому при функционировании при повышенных температурах потребность в энергии для процесса в целом уменьшается. Разумеется, при некоторой повышенной температуре энергия, требующаяся для электролиза, будет равна энергии, возвращаемой от водорода, и процесс будет иметь кажущуюся нулевую потребность в энергии.
В случае, когда водород, произведенный этим способом, замещает водород, произведенный риформингом метана, может быть вычислено, что метан, когда потребляется в современной технологии, будет возвращать 887 кВт·ч/тонну CO2. При принятии этого значения в качестве величины возврата энергии (в отличие от теоретической величины 903,6кВт·-ч/тонну CO2) и увеличении температуры до примерно 301°C достигается осуществление реакции электролиза, которая сама потребляет ~887кВт·ч/тонну CO2; т.е. это является решением "нулевой потребности в энергии" первого порядка.
Более пристальное рассмотрение позволит обнаружить, что при этом рабочем режиме тепловая энергия (источник тепла при 30°C+, для этого примера) преобразуется в меньшую электрическую энергию. Это является преобразованием одного источника энергии (тепла) в другой источник энергии или топливо (водород); в качестве такового, процесс связывания диоксида углерода протекает на протяжении своего действия, чтобы преобразовывать иным образом "отходящую теплоту" в топливо или электрическую энергию.
Процесс электролиза, проводимый при повышенных температурах, не является неизвестным процессом; электролиз воды (производящий водород и кислород) смещался в сторону более высоких рабочих температур на протяжении нескольких десятилетий, что позволило обеспечить громадное снижение потребности в энергии при таком его выполнении. В процессах связывания диоксида углерода, описанных в данном документе, могут применяться повышенные температуры (от источников отходящей теплоты на электростанциях), чтобы выполнять то же самое. Подобным образом, парофазный электролиз может быть применен в хлорощелочном электролизе, чтобы уменьшить потребность в энергии.
Функционирование при повышенной температуре требует, чтобы материалы, использованные в хлорощелочных ячейках, могли противостоять высоким температурам (и результирующим высоким давлениям), которые имеют место, когда действуют большие количества тепловой энергии. Многие из материалов, применяемых в стандартных хлорощелочных ячейках, будут нуждаться в модернизации или замене на материалы, подходящие для конструкции и выбранного рабочего режима.
Все способы и устройства, рассмотренные и заявленные в данном документе, могут быть сделаны и выполнены без чрезмерного экспериментирования, принимая во внимание данное описание. Несмотря на то что способы и устройства по данному изобретению описаны в предпочтительных вариантах осуществления, специалистам в данной области техники будет очевидно, что могут быть сделаны изменения применительно к данным способам и устройствам как в отношении этапов, так в отношении последовательности этапов способа, описанного в данном документе, без отклонения от идеи, сущности и объема данного изобретения. Более конкретно, будет очевидно, что определенные композиции, которые химически сходны, могут замещать композиции, описанные в данном документе, притом, что могут быть достигнуты такие же или сходные результаты. Все такие подобные замены и модификации, очевидные специалистам в данной области, считаются находящимися в пределах сущности, объема и идеи данного изобретения, как они определены прилагаемой формулой изобретения.
ССЫЛКИ
Приведенные ниже ссылки, в тех пределах, в которых они предоставляют иллюстративные, процедурные или другие детали в дополнение к тем, что изложены в данном документе, конкретно включены здесь посредством ссылки на них.
"Annual Energy Outlook 2005 (AEO2005)," prepared by the Energy Information Administration, available through National Energy Information Center, EI-30, Washington, DC.
"Carbonate Chemistry for Sequestering Fossil Carbon," by Klaus S. Lackner, in Annual Review of Energy Environment, 2002, by Annual reviews.
"Effects of the Operating Pressure On The Performance of Electrolytic Cell at Elevated Temperatures," by Y. Ogata, M. Yasuda, and F. Hine, Nagoya Institute of Technology, Japan. In Proceedings of the Symposium on Electrochemical Engineering in the Chlor-Alkali and Chlorate Industries, The Electrochemical Society, 1988.
"Electrochemical Hydrogen Technologies - Electrochemical Production and Combustion of Hydrogen," edited by Hartmut Wendt, Institute fur Chemische Technologie, Stuttgart, Elsevier Press 1990.
"Electrochemical Process Engineering - A Guide to the Design of Electrolytic Plant," by F. Goodridge and K. Scott, University of Newcastle upon Tyne, 1995.
"Exergy Study of the Kalina Cycle," by Goran Wall, Chia-Chin Chuang, and Masaru Ishida, presented at 1989 American Society of Mechanical Engineers (ASME), Winter Annual Meeting, San Francisco, California, December 1989, published in "Analysis and Design of Energy Systems: Analysis of Industrial Processes AES Vol. 10-3, pp 73-77 ASME.
"Industrial Electrochemistry," 2nd Edition, edited by Derek Pletcher and Frank Walsh, 1990.
"Modern Chlor-Alkali Technology," edited by M.O. Coultier, Society for the Chemical Industry, London, 1980.
"Modern Chlor-Alkali Technology," Volumes 1-7, The Royal Society of Chemistry Information Services, 1998.
"Some Guidelines for Analysis, Design, and Operational Principles of Bubble Column Reactors," и другая избранная информация, содержащаяся в "Bubble Column Reactors," by Wolf-Dieter Deckwer, Gesellschaft fur Biotechnologische Forschung mbH, Braunsweig, Germany, translated by Robert Field, 1991 ISBN 0-471-91811-3.
"Transport and Structure in Fuel Cell Proton Exchange Membranes," by Michael Anthony Hickner, dissertation submitted to the faculty of Virginia Polytechnic Institute and State University, 2003.
Фигура 8. "Абсорбция CO2 в зависимости от (низкой) скорости газа на границе раздела при разных высотах колонны 0,18M раствором гидроксида натрия в безнасадочной барботажной колонне", из диссертации A. Schumpe, University of Hanover, 1978.
Klara in: EIA Emissions of Greenhouse Gases in the U.S. 2000, EPGA 3rd Annual Power Generation Conference, Hershey PA, 2002.
Mandal, et al., J. Chem. Engineering (Canada), 81:212-219, 2003.
Shah et al., AiCHE J., 28(3):353-379, 1982.
Unit Operations of Chemical Engineering, McGraw-Hill, 3rd edition © 1976, "Gas Absorption" pp. 707-743, after Eckert.
Wie-rong et al., J. Zhejiang University Science, ISSN 1009-3095, 2004.
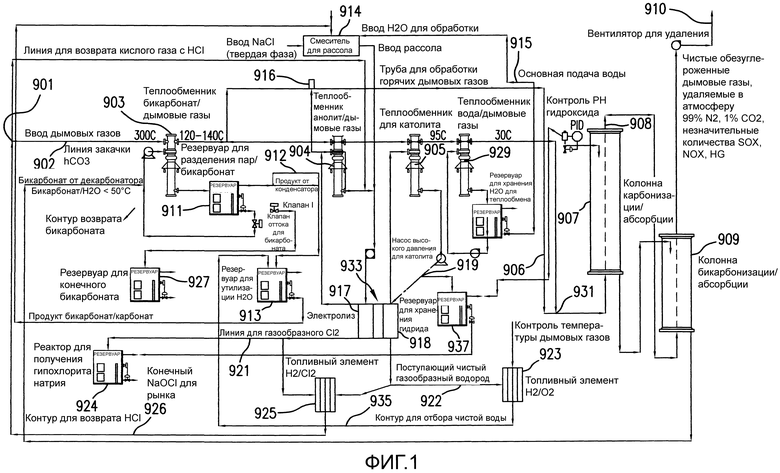
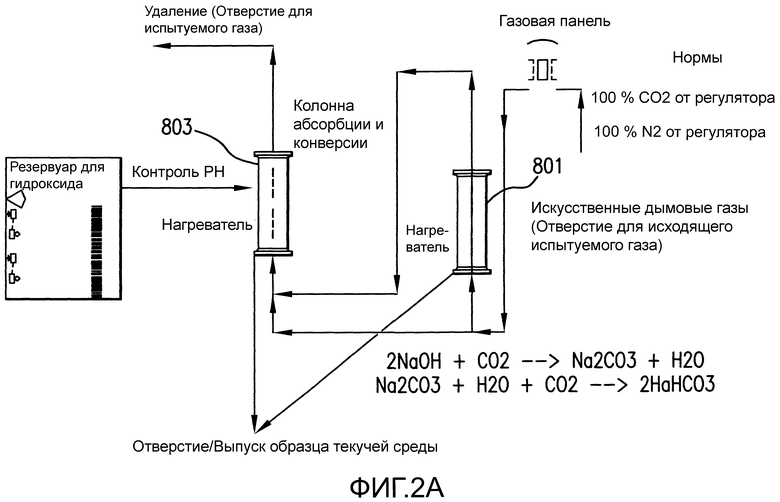
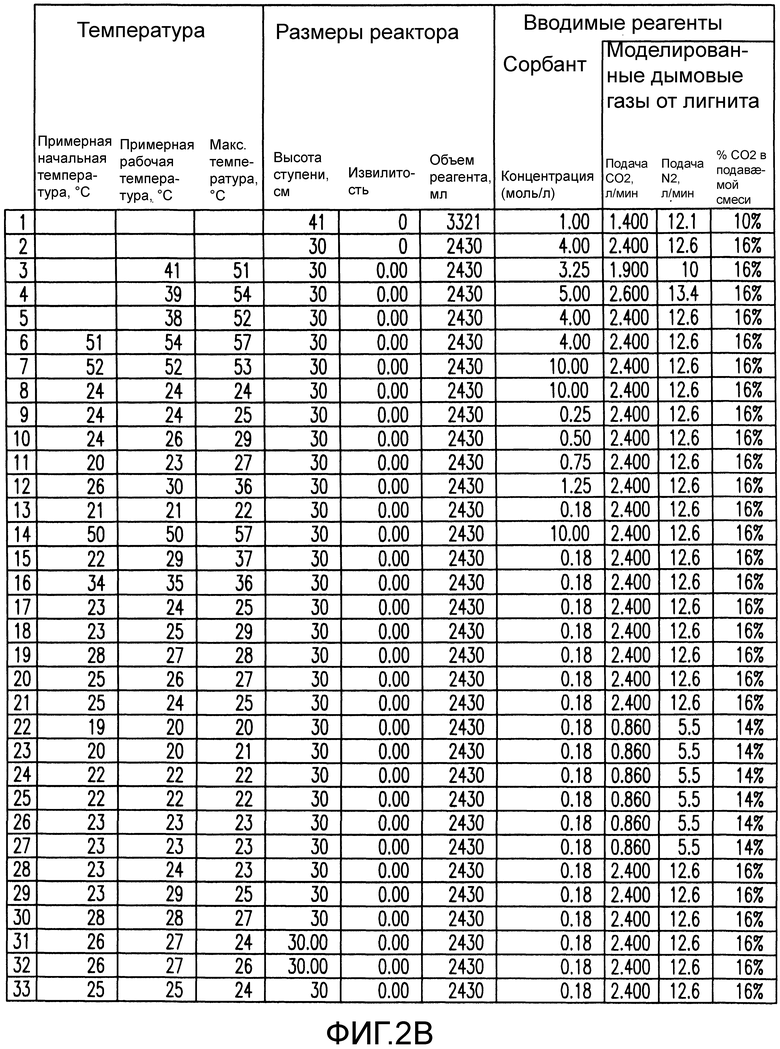
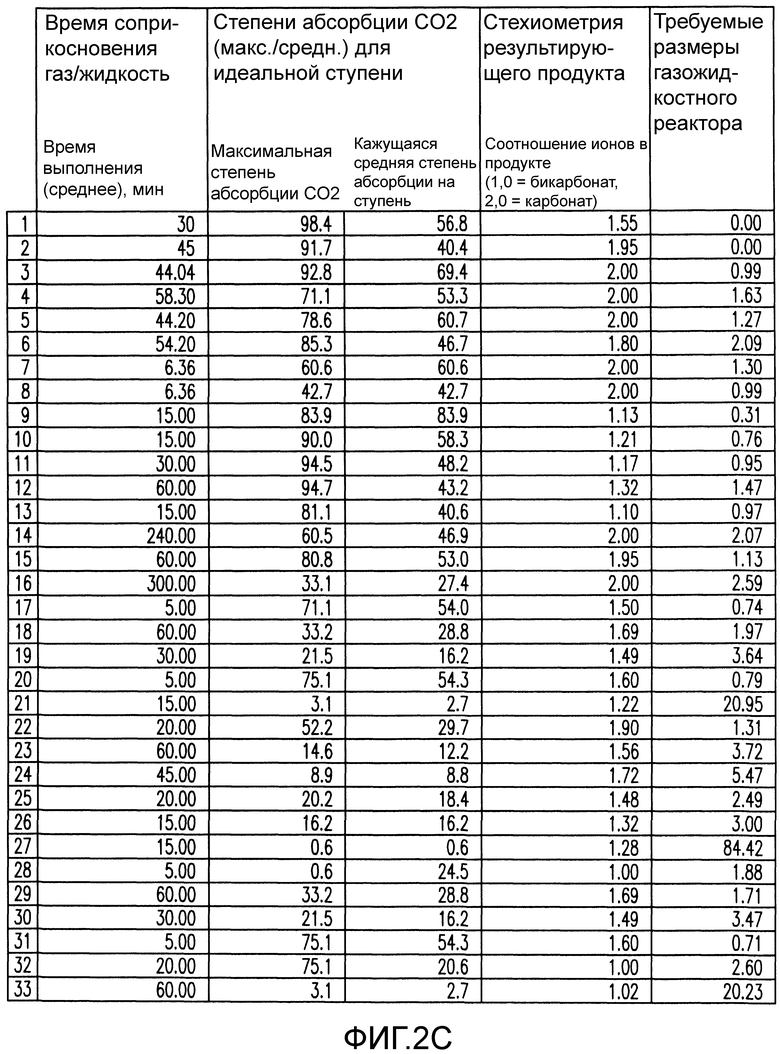
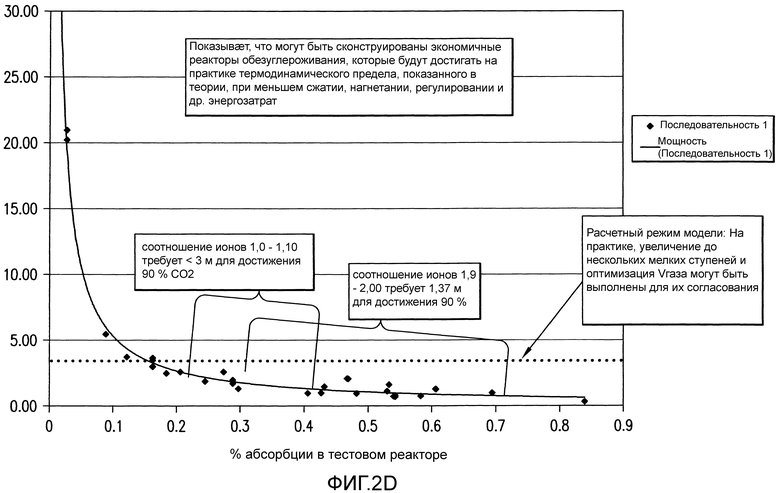
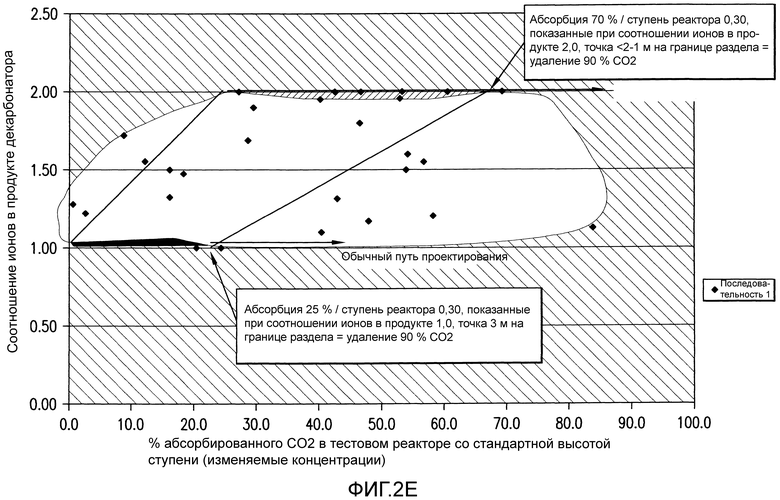
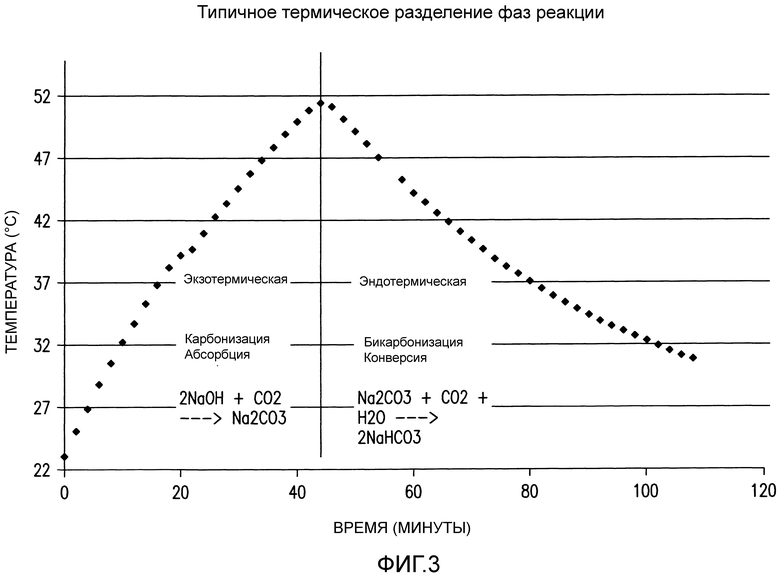
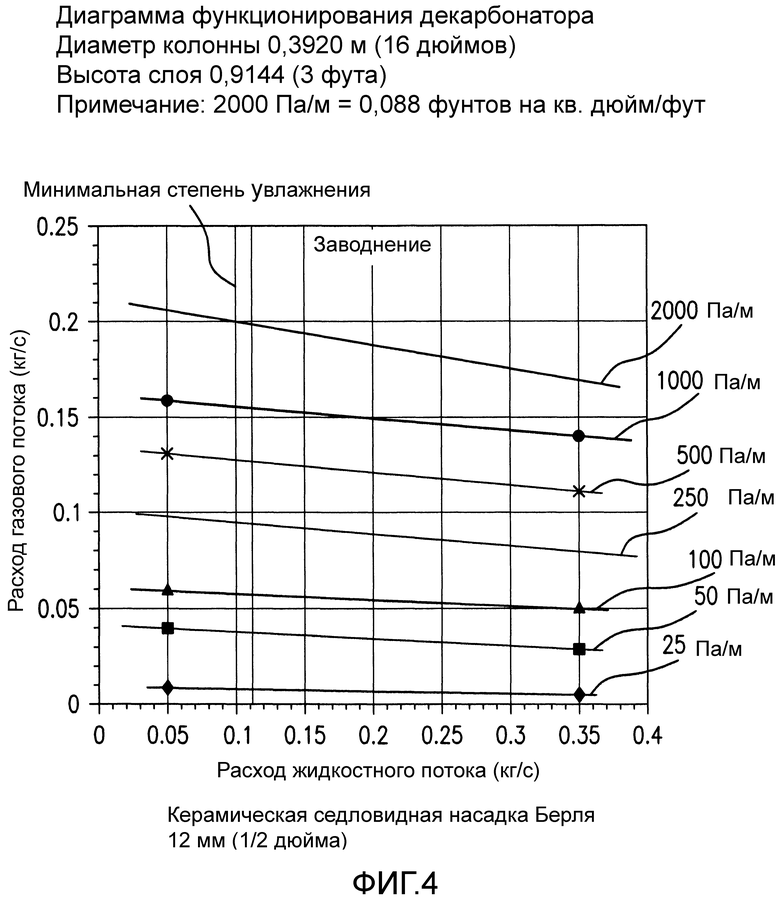
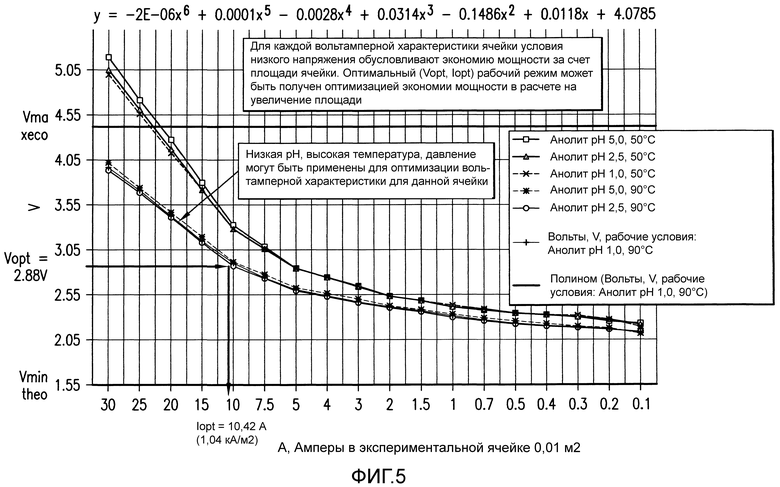
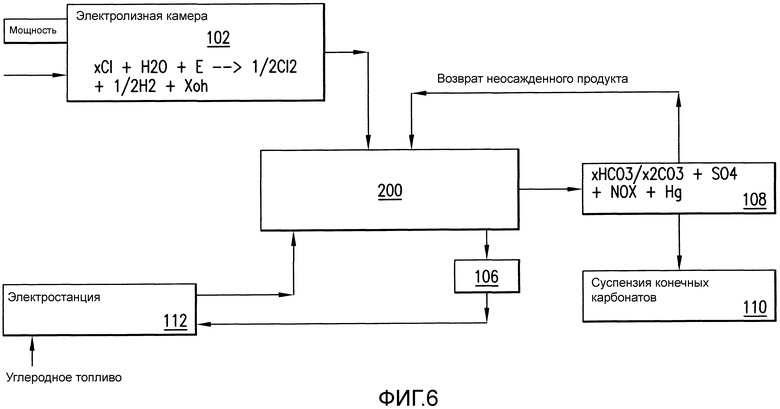
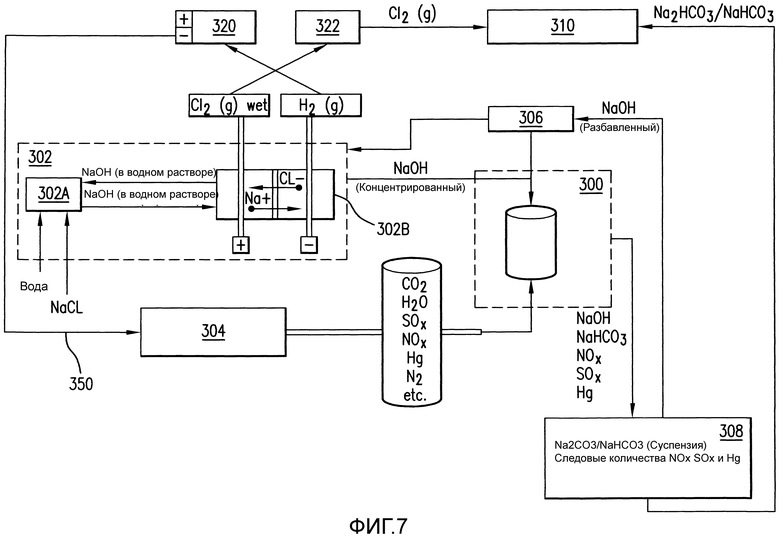
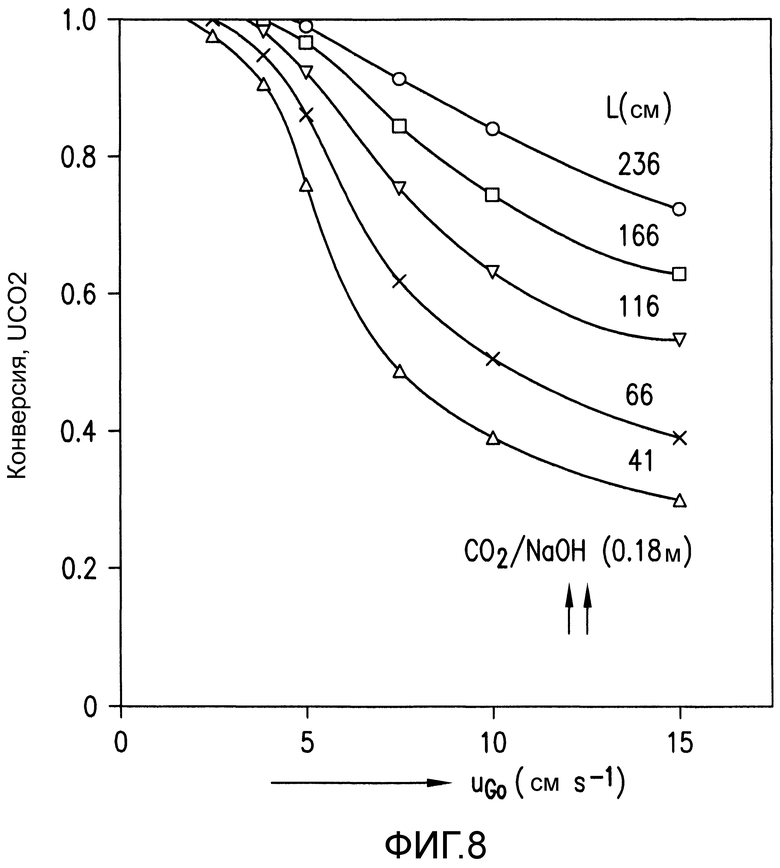
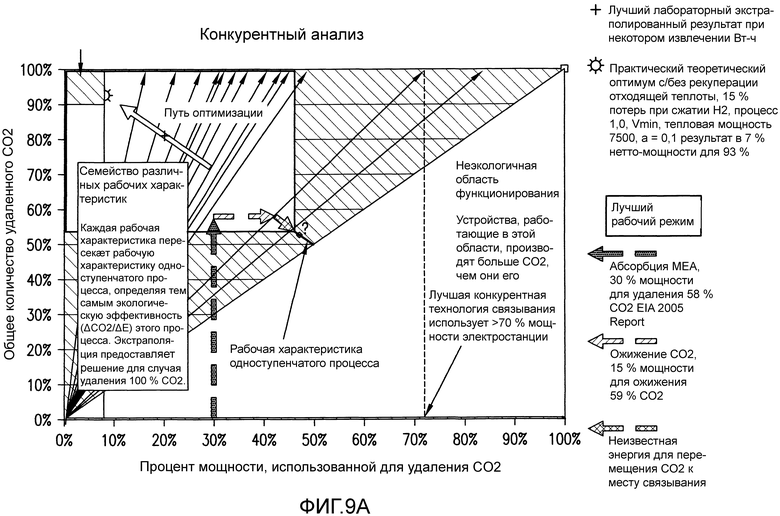

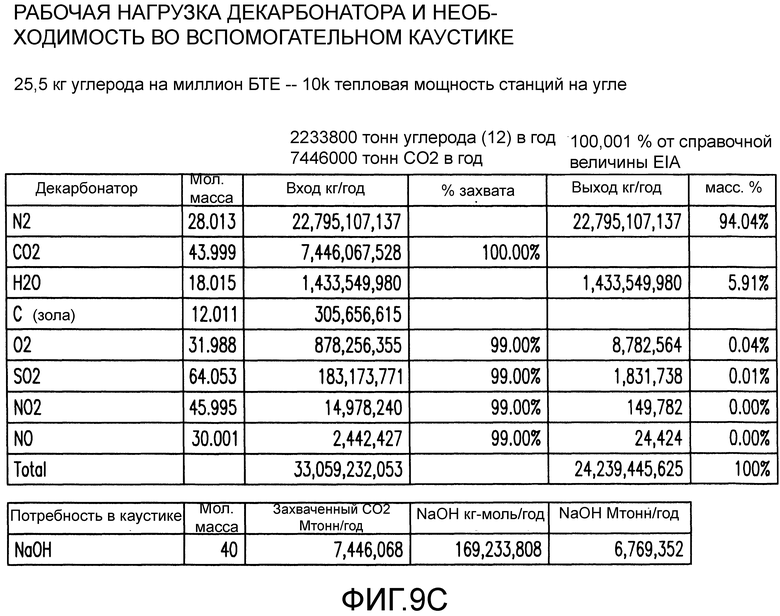
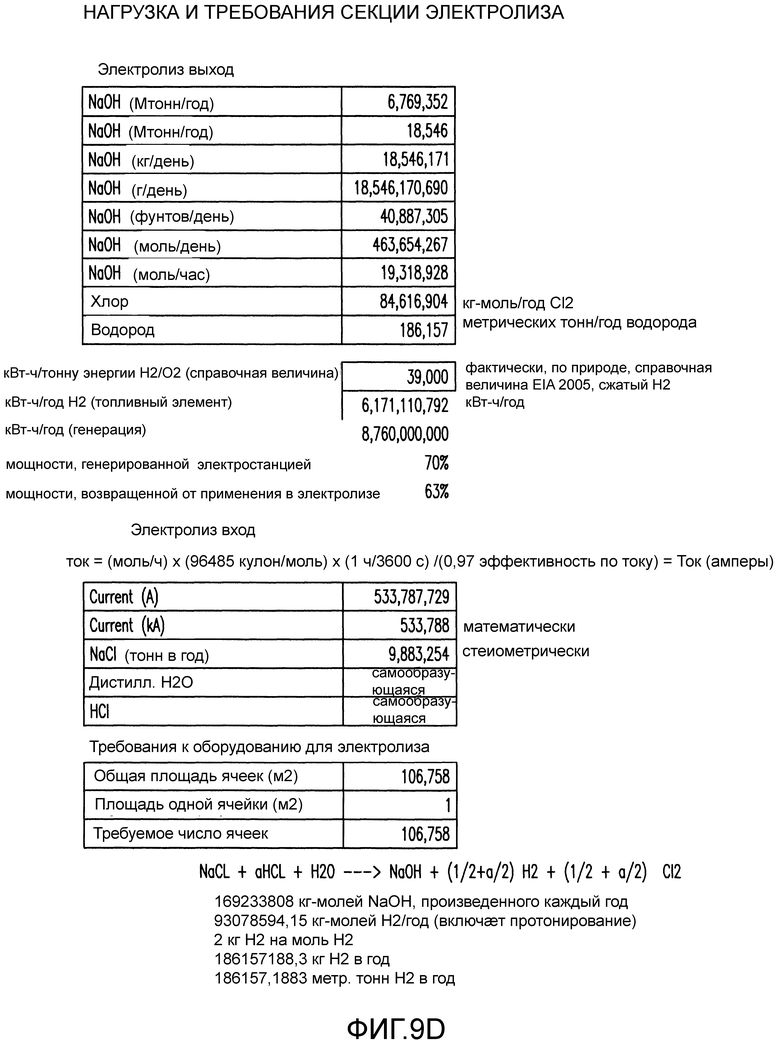


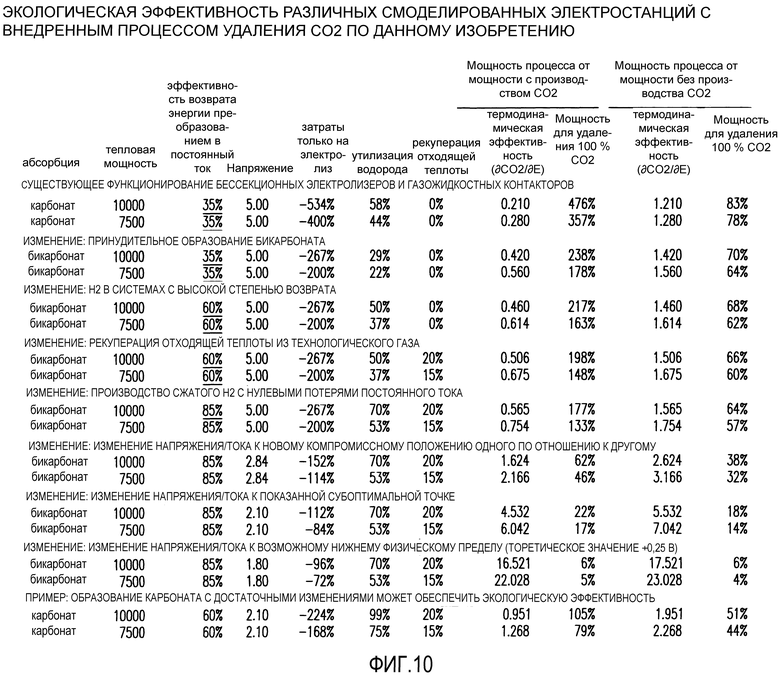
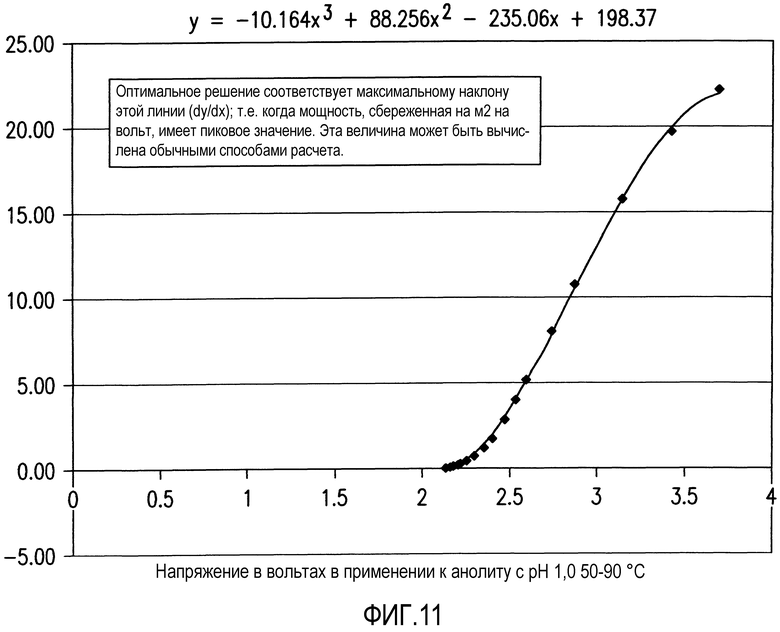
Изобретение относится к удалению диоксида углерода и других загрязняющих веществ из потоков отходов посредством их абсорбции из концентрированных потоков. Способ отделения тяжелых металлов от воды в конденсате дымовых газов от процесса, в котором диоксид углерода удаляется из газового потока на электростанции, содержит получение хлоридной соли и смешивание ее с водой и/или паром, чтобы получить раствор. Затем проводят электролиз раствора, чтобы получить гидроксид и газообразный хлор, смешивают части гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси. Отделяют указанные карбонатные и/или бикарбонатные продукты от смеси, посредством чего диоксид углерода удаляется из газового потока. Затем добавляют части гидроксида к конденсату дымовых газов, чтобы изменить величину его pH с кислой на щелочную, что приводит к осаждению тяжелых металлов, и пропускают конденсат через фильтрующую среду. Технический результат заключается в эффективном отделении тяжелых металлов от воды в конденсате дымовых газов. 4 з.п. ф-лы, 20 ил., 3 пр., 2 табл.
1. Способ отделения тяжелых металлов от воды в конденсате дымовых газов от процесса, в котором диоксид углерода удаляется из газового потока на электростанции, содержащий:
получение хлоридной соли;
смешивание соли с водой и/или паром, чтобы получить раствор;
электролиз раствора, чтобы получить гидроксид и газообразный хлор;
смешивание части гидроксида с потоком дымовых газов, чтобы получить карбонатные продукты, бикарбонатные продукты или смесь карбонатных и бикарбонатных продуктов в образованной смеси;
отделение указанных карбонатных и/или бикарбонатных продуктов от смеси, посредством чего диоксид углерода удаляется из газового потока;
добавление части гидроксида к конденсату дымовых газов, чтобы изменить величину его pH с кислой на щелочную, что приводит к осаждению тяжелых металлов; и
пропускание конденсата через фильтрующую среду.
2. Способ по п.1, в котором хлоридная соль представляет собой хлорид натрия.
3. Способ по п.1, в котором фильтрующая среда содержит активированный уголь.
4. Способ по п.1, в котором конденсат пропускается под действием силы тяжести через фильтрующую среду.
5. Способ по п.1, в котором конденсат активно прокачивается через фильтрующую среду.
| US 20060185985 A1, 24.08.2006; | |||
| WO 2006034339 A1, 30.03.2006; | |||
| US 2006076228 A1, 16.09.2004 | |||
| СПОСОБ КОМБИНИРОВАННОЙ ОЧИСТКИ ПРИРОДНОГО ГАЗА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2004 |
|
RU2270233C1 |
Авторы
Даты
2014-10-27—Публикация
2008-09-19—Подача