Настоящее изобретение касается фармацевтической композиции, пригодной для воздействия на ретикулоэндотелиальную систему, лечения муковисцидоза и хронических болевых синдромов, возникающих при дистрофических заболеваниях опорно-двигательного аппарата или сопутствующих бластоматозным заболеваниям онкологического происхождения, и способ приготовления такой композиции.
В патентах Венгрии N 176202 и Великобритании N 2022998 описана фармацевтическая композиция, применимая для воздействия на ретикулоэндотелиальную систему (РЭС), т.е. на тканевую систему, состоящую из тканей различных типов, находящихся в разных анатомических областях или органах организма человека и животных. Указанная композиция содержит
I) смесь фармацевтически приемлемых водорастворимых соединений бора, фтора, магния, ванадия, марганца, железа, кобальта, никеля, меди, цинка и молибдена, не осаждаемых ни в осадок при контакте друг с другом, ни прочими составными частями композиции, имеющих нейтральную или кислую реакцию (pH) в водной среде;
II) глицин;
III) глицерин;
IV) L-(+)-аскорбиновую кислоту;
V) нейтральную или кислую водорастворимую соль 2, 4, 5, 7-тетрагалофлуоресцеина (согласно действующей номенклатуре 2', 4', 5', 7'-тетрагалофлуоресцеин);
VI) нейтральную или кислую, водорастворимую, фармацевтически приемлемую соль этилендиаминтетрауксусной кислоты;
VII) виннокислый калий-натрий
в соотношениях массовых долей соединение бора:соединение фтора:соединение магния: соединение ванадия:соединение марганца: соединение железа:соединение кобальта:соединение никеля:соединение меди:соединение цинка:соединение молибдена: глицин:глицерин: L-(+) -аскорбиновая кислота:соль 2, 4, 5, 7-тетрагалофлуоресцеина:соль этилендиаминтетрауксусной кислоты:виннокислый калий-натрий, составляющих соответственно (0,01 1):(0,02 1):(0,4 3): (0,02 0,6): (0,1 2):(1 6):(0,1 1):(0,02 2): (0,05 1):1:(0,1 3):(0,01 0,8):(0,1 2):(2 8): (0,01 2):(0,003 0,5):(0,1 3):(0,7 - 10).
Эту композицию готовят, растворяя компоненты в воде, смешивая с фармацевтически приемлемыми в фармации носителями, растворителями и/или наполнителями, с последующим переводом полученной таким образом смеси в лекарственную форму одним из известных методов.
Согласно предпочтительному варианту осуществления изобретения в качестве соединения бора используют борную кислоту; в качестве соединения фтора - фторид натрия или трифторид ванадия; в качестве соединения магния сульфат или хлорид магния или их гидраты; в качестве соединения ванадия ванадат аммония или трифторид ванадия; в качестве соединения марганца сульфат, хлорид или их гидраты; в качестве соединения железа сульфат железа (II) или железа (III) или гидраты железа; в качестве соединения кобальта хлорид или сульфат или их гидраты; в качестве соединения никеля хлорид сульфат или их гидраты; в качестве соединения меди сульфат меди (II) или его гидрат; в качестве соединения цинка сульфат цинка или его гидрат; в качестве соединения молибдена молибдат аммония или натрия.
Согласно следующему предпочтительному варианту осуществления изобретения используют динатриевую соль 2', 4', 5', 7'-тетраиодфлуоресцеина как соль тетрагалофлуоресцеина, динатриевую соль этилендиаминтетрауксусной кислоты в качестве соли этилендиаминтетрауксусной кислоты, а для приготовления водной среды применяют дистиллированную воду.
Целью настоящего изобретения является разработка фармацевтической композиции, приемлемой для лечения муковисцидоза и хронических болевых синдромов, сопутствующих онкологическим заболеваниям или возникающих при дегенеративных заболеваниях опорно-двигательного аппарата, и, кроме того, проявляющей положительные качества прежних композиций, упомянутых выше.
Изобретение основано на установлении того факта, что указанная цель может быть достигнута исключением из выше описанной композиции соли 2', 4', 5', 7'-тетрагалофлуоресцеина и замены ее янтарной кислотой и L-(+)-винной кислотой. Полученная таким образом композиция применима для лечения указанных выше болевых синдромов.
Затем изобретение основано на установлении того факта, что композиция, полученная в результате упомянутой замены составных частей, способна давать эффект традиционных болеутоляющих средств, таких как морфий, используемых при лечении хронических болевых синдромов, сопровождающих онкологические заболевания, а именно позволяет уменьшить дозы и устранить неблагоприятные побочные эффекты обычных болеутоляющих средств, благоприятно действует на переносимость и уменьшает привыкание к лекарственным средствам.
Изобретение основывается на установлении еще одного факта, заключающегося в том, что положительные особенности описанной в вышеупомянутых патентах Венгрии и Великобритании композиции не изменяются при уменьшении нижнего предела массовых соотношений некоторых комплексов.
Таким образом, настоящее изобретение касается фармацевтической композиции, пригодной для воздействия на ретикулоэндотелиальную систему и лечения мукосвицидоза и хронических болей, сопровождающих дистрофические заболевания опорно-двигательного аппарата или онкологические заболевания.
Указанная фармацевтическая композиция включает
I) одно (или более) фармацевтически приемлемое водорастворимое соединение бора, фтора, магния, ванадия, марганца, железа, кобальта, никеля, меди, цинка и молибдена, не осаждаемые ни друг другом, ни прочими составляющими композициями, обладающие нейтральной или кислой реакцией (pH) в водной среде;
II) глицин;
III) глицерин;
IV) L-(+)-аскорбиновую кислоту;
V) янтарную кислоту;
VI) нейтральную или кислую, водорастворимую, фармацевтически приемлемую соль этилендиаминтетрауксусной кислоты;
VII) виннокислый калий-натрий;
VIII) L-(+)-винную кислоту,
где массовые соотношения компонентов соединение бора: соединение фтора: соединение магния:соединение ванадия:соединение марганца:соединение железа: соединение кобальта:соединение никеля: соединение меди:соединение цинка:соединение молибдена:глицин: глицерин:L-(+)-аскорбиновая кислота:янтарная кислота: соль этилендиаминтетрауксусной кислоты:виннокислый калий-натрий:L-(+) -винная кислота составляют (0,01 1):(0,01 1):(0,2 - 3):(0,01 0,6): (0,02 2): (0,15 6):(0,002 1):(0,01 2):(0,01 1):(0,1 3): (0,001 0,8):(0,1 2):(0,2 8): (0,01 2):(0,001 2): (0,01 - 10):(0,01 2).
Патентуемую композицию получают реакцией перечисленных выше компонентов в водной среде, переводя приготовленную смесь в фармацевтическую композицию с одним или более фармацевтически приемлемым разбавителем и/или наполнителем, как обычно.
Заявленную в изобретении фармацевтическую композицию аналогично тому, как это описано в упомянутых ранее патентах Венгрии и Великобритании, готовят на воде, т.е. компоненты можно растворять и смешивать в водной среде.
В дополнение к вышеперечисленным составляющим патентуемая фармацевтическая композиция может включать солюбилизаторы, предпочтительно этанол, буферы для доведения pH до желательной, фармацевтически приемлемой величины, преимущественно соляная или серная кислоты, общепринятые в фармакологии носители, разбавители и наполнители.
При использовании в качестве растворителя дистиллированной воды концентрации ингредиентов I) VIII) могут варьироваться в пределах от 0,001 до 10% по процентному отношению массы к объему.
Предлагаемая в настоящем изобретении фармацевтическая композиция может быть приготовлена из различных комплексных соединений, при смешивании которых в водном растворе образуется более сложный комплекс, остающийся в то же время водорастворимым. Полученный водный раствор может быть сконцентрирован и концентрат абсорбирован наполнителем для приготовления суппозиториев или пессариев.
Согласно предварительному варианту осуществления изобретения фармацевтическая композиция содержит в качестве соединения бора борную кислоту предпочтительно в количестве от 0,01 до 1 мас. к объему; в качестве соединения фтора фторид натрия или трифторид ванадия предпочтительно в количестве от 0,01 до 1 мас. к объему; в качестве соединения магния сульфат, хлорид магния или их гидрат предпочтительно в количестве от 0,2 до 3 мас. к объему; в качестве соединения ванадия ванадат аммония или трихлорид ванадия предпочтительно в количествах от 0,001 до 0,6 мас. к объему; в качестве соединения марганца гидрат сульфата марганца или тетрагидрат хлорида марганца предпочтительно в количестве от 0,02 до 2 мас. к объему; в качестве соединения железа гептагидрат сульфата железа (II) или сульфат железа (III) предпочтительно в количестве от 0,15 до 6 мас. к объему; в качестве соединения кобальта гексагидрат хлорида кобальта или гептагидрат сульфата кобальта предпочтительно в количестве от 0,002 до 1 мас. к объему; в качестве соединения никеля гептагидрат хлорида никеля или сульфат никеля предпочтительно в количестве от 0,01 до 2 мас. к объему; в качестве соединения меди сульфат меди (II) или его пентагидрат предпочтительно в количестве от 0,01 до 1 мас. к объему; в качестве соединения цинка сульфат или гептагидрат цинка предпочтительно в количестве от 0,1 до 3 мас. к объему; в качестве соединения молибдена молибдат аммония ((NH4)6Mo7O24 • 4H2O) или молибдат натрия (Na2MoO4 • 2H2O) предпочтительно в количестве от 0,001 до 0,8 мас. к объему.
Предшествующие и последующие данные, относящиеся к выражению концентраций в единицах мас. к объему, следует понимать как количество вещества, представленное в граммах, растворенное в 100 мл раствора.
Предпочтительные диапазоны концентраций других компонентов фармацевтической композиции согласно настоящему изобретению составляют:
глицин от 0,1 до 2 мас. к объему
глицерин от 0,2 до 8 мас. к объему
L-(+)-аскорбиновая кислота от 0,01 до 2 мас. к объему
янтарная кислота от 0,01 до 2 мас. к объему
динатриевая соль этилендиаминтетрауксусной кислоты от 0,01 до 3 мас. к объему
виннокислый калий-натрий от 0,01 до 10 мас. к объему
L-(+)-винная кислота от 0,01 до 2 мас. к объему
Предпочтительная концентрация этанола (приемлема 96% объемная концентрация), являющегося добавкой, облегчающей растворение, составляет от 0,05 до 10 мас. к объему, в то время как предпочтительное количество фармацевтически приемлемой кислоты (лучше всего соляной или серной) составляет от 0,05 до 1 мас. к объему.
Величина pH патентуемой фармацевтической композиции лежит предпочтительно в диапазоне от 1,9 до 4. Для регулирования величины pH серную или соляную кислоту берут в 1 н концентрации.
Фармацевтическую композицию, отвечающую настоящему изобретению, назначают для приема через полость рта в виде капель, а также ректально или интравагинально в виде суппозиториев или пессариев.
Фармацевтическую композицию для ректального или вагинального назначения готовят, упаривая водный раствор до сиропообразной консистенции, после чего им пропитывают массу для свечей. Ректальные и вагинальные суппозитории формуют из полученной массы методами, общепринятыми в фармацевтической промышленности. Основа для свечей состоит по преимуществу из масла какао, пальмового воска или желатина.
Для иллюстрации изобретения приведены следующие не исчерпывающие область его применения примеры.
Пример 1. Фармацевтическую композицию в количестве 100 л готовят следующим образом.
1. Приготовление комплексообразующих реагентов (лигандов).
a) 300 г "Селектона" B2 (Na2 ЭДТА) растворяют при нагревании в 4 л дистиллированной воды.
b) 200 г виннокислого калия-натрия растворяют в 2 л дистиллированной воды.
c) 50 г янтарной кислоты и 410 г гептагидрата сульфата магния растворяют при нагревании в 2 л дистиллированной воды.
d) 50 г L-(+)-винной кислоты и 94 г моногидрата сульфата марганца растворяют в 1 л дистиллированной воды.
e) 60 г борной кислоты и 600 г глицерина в концентрации по меньшей мере 86,4% (масс. доли) растворяют в присутствии 200 мл дистиллированной воды при слабом нагревании.
f) 230 г глицина растворяют в 800 мл дистиллированной воды при слабом нагревании, затем добавляют сульфат меди и сульфат цинка по прописи п. 4.11.
2. 30 г L-(+)-аскорбиновой кислоты растворяют, встряхивая, в 500 мл подогретой до 50-60oC дистиллированной воды.
3. Если необходимо, регулируют pH до значений в диапазоне 1,9-4, используя L-(+)-аскорбиновую кислоту.
4. Приготовление комплексов.
Комплекс I.
В колбу Эрленмейера объемом 1 л помещают 200 мл воды, 20 г фторида натрия и 20 г ванадата аммония. После растворения содержимое переливают в резервуар с мешалкой объемом 100 л, предварительно заполненный 50 л дистиллированной воды.
Комплекс II.
100 г 5-водного сульфата меди растворяют в 500 мл дистиллированной воды. В другой колбе растворяют 500 г 7-водного сульфата цинка в 1 л дистиллированной воды. Сначала раствор сульфата меди, затем сульфата цинка последовательно вводят в раствор глицина, приготовленного, как описано в п. 1. Образовавшийся сине-фиолетовый раствор вливают, помешивая, в находящийся в резервуаре раствор комплекса I.
Комплекс III.
К 1 л раствора "Селектон" B2, приготовленного по 1. а), добавляют 10 г CoCl2 • 6H2O, 35 г (NH4)6Mo7O24 • 4H2O, 52 г NiSO4 • 7H2O 8 г NH4VO3 в 800 мл дистиллированной воды и растворяют твердые компоненты при нагревании. Полученный раствор добавляют к резервуару, находящемуся в растворе.
Отдельно растворяют 1000 г гептагидрата сульфата железа (II) в 4 л дистиллированной воды, добавив 2 л раствора "Селектона" B2, приготовленного по прописи 1. а); полученный раствор вливают в резервуар, и затем, помешивая, добавляют оставшийся раствор "Селектона" B2. В результате получается голубовато-зеленый мутный раствор.
Комплекс IV.
410 г гептагидрата сульфата магния и 50 г янтарной кислоты растворяют при слабом нагревании в 1 л дистиллированной воды, затем, помешивая, приливают к раствору в резервуар.
Комплекс V.
94 г моногидрата сульфата марганца и 50 г L-(+)-винной кислоты растворяют при нагревании в 500 мл дистиллированной воды, затем полученный раствор приливают к раствору в резервуаре.
Комплекс VI.
60 г борной кислоты и 600 г глицерина растворяют в 200 мл дистиллированной воды при слабом нагревании. Затем полученный раствор доливают к раствору в резервуаре.
5 Получение композиции.
Раствор виннокислого калия-натрия, приготовленный по прописи 1. b), и затем раствор L-(+)-аскорбиновой кислоты, приготовленный в соответствии с прописью 2. помешивая, вливают в раствор, находящийся в резервуаре. Объем раствора доводят до 98 л, добавляя дистиллированную воду. Затем измеряют величину pH раствора, которая должна составлять от 1,9 до 4. Если значение pH превышает 4, его доводят до 3, добавляя дополнительно L-аскорбиновую кислоту. Окончательный объем раствора приводят к 100 л.
Полученный раствор выдерживают в течение 12-24 ч. За это время раствор просветляется, цвет становится желтовато-зеленым. После проверки качества раствор можно расфасовывать.
100 мл полученного таким образом раствора содержат следующие ингредиенты:
метаванадат аммония NH4VO3 0,023 г
фторид натрия NaF 0,20 г
глицин C2H5NO2 0,23 г
сульфат меди (II) CuSO4•5H2O 0,10 г
сульфат цинка ZnSO4•5H2 0,50 г
молибдат аммония (NH4)6Mo7O24•4H2O - 0,035 г
сульфат никеля (II) NiSO4•7H2O 0,052 г
хлорид кобальта (II) CoCI2•6H2O 0,010 г
динатриевая соль этилендиаминтетрауксусной кислоты (Na2ЭДТА•2H2O) C10H14N2O8Na2•2H2O 0,30 г
L-(+)-аскорбиновая кислота C6H8O6 0,30 г
сульфат железа (II) FeSO4•7H2O 1,0 г
сульфат магния (II) MoSO4•7H2O 0,41 г
янтарная кислота C4H6O4 0,050 г
сульфат марганца (II) MnSO4•H2O 0,094 г
L-(+)-винная кислота C4H6O6 0,050 г
борная кислота H3BO3 0,060 г
глицерин (87%) C3H8O3 0,60 г
виннокислый калий-натрий C4H4O6KNa•4H2O - 0,20 г
Пример 2. Композицию готовят по методике примера 1, но количество исходных компонентов подбирают таким образом, чтобы в 100 мл готового раствора содержание ингредиентов составляло
метаванадат аммония 0,068 г
фторид натрия 0,30 г
глицин 1,94 г
сульфат меди (II) 0,012 г
сульфат цинка 2,85 г
молибдат аммония 0,020 г
сульфат никеля (II) 0,070 г
хлорид кобальта (II) 0,0021 г
динатриевая соль этилендиаминтетрауксусной кислоты (Na2ЭДТА•2H2O) 0,20 г
L-(+)-аскорбиновая кислота 0,040 г
сульфат железа (II) 0,153 г
сульфат магния (II) 2,94 г
янтарная кислота 0,030 г
сульфат марганца (II) 0,23 г
L-(+)-винная кислота 1,94 г
борная кислота 0,30 г
глицерин (87%) 7,92 г
виннокислый калий-натрий 0,10 г
Пример 3. Композицию готовят по методике примера 1, но количество исходных компонентов подбирают таким образом, чтобы в 100 мл готового раствора содержание ингредиентов составляло
метаванадат аммония 0,576 г
фторид натрия 0,95 г
глицин 0,50 г
сульфат меди (II) 0,99 г
сульфат цинка 1,00 г
молибдат аммония 0,768 г
сульфат никеля (II) 1,92 г
хлорид кобальта (II) 0,10 г
динатриевая соль этилендиаминтетрауксусной кислоты (Na2ЭДТА•2H2O) 2,97 г
L-(+)-аскорбиновая кислота 1,94 г
сульфат железа (II) 1,50 г
сульфат магния (II) 0,60 г
янтарная кислота 1,98 г
сульфат марганца (II) 1,96 г
L-(+)-винная кислота 0,10 г
борная кислота 0,98 г
глицерин (87%) 1,0 г
виннокислый калий-натрий 9,78 г
Пример 4. Композицию готовят по методике примера 1, но количество исходных компонентов подбирают таким образом, чтобы в 100 мл готового раствора содержание ингредиентов составляло
метаванадат аммония 0,0011 г
фторид натрия 0,012 г
глицин 0,11 г
сульфат меди (II) 0,50 г
сульфат цинка 0,11 г
молибдат аммония 0,0011 г
сульфат никеля (II) 0,012 г
хлорид кобальта (II) 0,97 г
динатриевая соль этилендиаминтетрауксусной кислоты (Na2ЭДТА•2H2O) 0,011 г
L-(+)-аскорбиновая кислота 0,012 г
сульфат железа (II) 5,76 г
сульфат магния (II) 0,206 г
янтарная кислота 0,011 г
сульфат марганца (II) 0,021 г
L-(+)-винная кислота 0,011 г
борная кислота 0,011 г
глицерин (87%) 0,21 г
виннокислый калий-натрий 0,012 г
Далее подробно описаны результаты испытаний и наблюдений фармацевтической активности композиции данного изобретения.
Проверка проводилась в ряде организаций под наблюдением врача.
Группа пациентов, отобранных в качестве испытуемых, включала мужчин и женщин различного возраста. Они получали композицию, отвечающую настоящему изобретению, в виде раствора (1 мл соответствует 18 каплям). Больные получали капли с чаем или легким напитком. Кроме капель пациенты получали от 100 до 300 мг аскорбиновой кислоты в день в виде таблеток или водного раствора в зависимости от дозы препарата в каплях. Больные с повышенным уровнем кислотности кислоту получали факультативно.
А) Испытание болеутоляющего действия при хронических болях, сопровождающих дистрофические заболевания опорно-двигательного аппарата.
Метод обработки результатов: случайная выборка, двойная слепая, с плацебо-контролем.
Место проведения испытания: Ортопедическая клиника медицинского Университета Семмелвайсса, Будапешт.
Композицию примера 1 назначали взрослым пациентам в следующих дозах:
больным с массой тела более 70 кг 3 раза по 20 капель в день в течение 1 недели, затем 2 раза по 20 капель в течение 2 недель и в зависимости от наступления улучшения 2 раза по 10 капель или 1 раз по 10 капель в день в последующие 2 недели,
больные с массой тела менее 70 кг получали 2 раза по 20 капель в день в течение 1 недели, затем 2 раза по 20 капель в течение 2 недель и в зависимости от наступления улучшения 1 раз по 10 капель в день в последующие 1-2 недели.
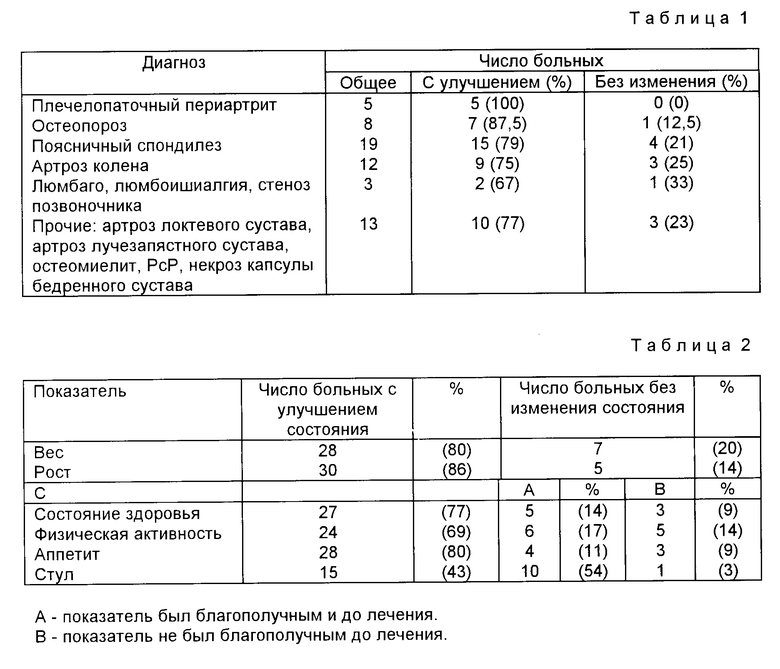
Испытаниями было охвачено 156 больных, из которых эффективно композицию получали 76 пациентов (группа I), а плацебо (группа II) 86 пациентов. Наблюдали улучшение у 57 больных (75%) из группы I и у 26 (32,5%) из группы II. У 19 (25%) и 54 (67%) больных из группы I и II соответственно состояние не изменилось.
Результаты испытаний, сгруппированные по видам заболеваний, приведены в таблице 1.
B) Клинические испытания болеутоляющего действия препарата при болях, сопровождающих онкологические заболевания.
Метод обработки результатов: случайная выборка; с контрольной группой, получавшей морфий.
Испытания проводили в Государственной онкологической клинике, Будапешт.
Испытания были проведены на группе из 35 больных, 17 из них получали каждый раз морфий и композицию примера 2 из расчета 1 капля на кг массы тела (группа I), в то время как 18 пациентов получали только морфий (группа II). В группе I доза морфия была уменьшена вдвое по сравнению с дозой, получаемой пациентами из группы II.
Полного исчезновения болей удалось добиться у 12 больных (71%) из группы I, в то время как тот же эффект был получен у 11 больных (61%) из группы II при введении вдвое больших, чем в группе I доз морфия. Уменьшение, но не полное исчезновение болей наблюдали в группах I и II у 5 (29%) и 39% больных соответственно.
C) Наблюдение за изменением клинического состояния детей, больных муковисцидозом.
Муковисцидоз наследственное заболевание, возникающее при генетических нарушениях, до сих пор считается неизлечимым. Наиболее заметным его проявлением является то, что секрет гланд имеет повышенную по сравнению с нормой вязкость. Так, избыточно вязкая слизь, выделяемая гландами, налипает на поверхности легких и дыхательных путей, покрытых слизистой оболочкой, и не может быть удалена самопроизвольно. Накапливающиеся выделения и развитие на них патогенной флоры приводят к хроническому воспалению, которое может закончиться разрушением легочной ткани. Наиболее серьезным последствием при поражении органов пищеварения является недостаток ферментов в двенадцатиперстной кишке из-за сгущения секрета поджелудочной железы, приводящего к ухудшению переваривания пищи и усвоения питательных веществ. В результате у больных наблюдается обильный, содержащий непереваренные остатки стул, развивается дистрофия.
Получаемое больными лечение обыкновенно сводится к разжижению вязкого секрета и восполнению недостающих ферментов и витаминов. Однако даже при самом внимательном лечении удается купировать далеко не все нарушения. Кроме того, эти пациенты восприимчивее к инфекциям.
Испытания били начаты в группе из 40 детей, страдающих муковисцидозом, 5 из которых, однако, прекратили принимать отвечающую данному изобретению композицию. Таким образом, представлены результаты лечения только 35 детей. Возраст больных варьировал от 3 до 18 лет.
Метод: композицию согласно примеру 3 назначали в течение 6 месяцев при ежедневной дозе 1 капля на 1 кг массы тела.
Испытания проводили в Детской больнице Будапешта.
В результате лечения с использованием композиции, отвечающей настоящему изобретению, улучшилось общее состояние и возросла физическая активность значительной части вылечиваемых детей. У школьников повысилась выносливость к учебным нагрузкам. Улучшился аппетит у большей части детей, и в результате наблюдалась прибавка в весе.
При определении изменений содержания железа и цинка в плазме крови больных было обнаружено, что уровень железа и цинка повысился у 91% и 51% пациентов из групп I и II соответственно, что, вероятно, и играло значительную роль в улучшении состояния больных. Другим благоприятным моментом явилось также увеличение содержания ферритина в плазме крови у 25 (71%) больных.
Результаты наблюдений за клиническим состоянием больных обобщены в таблице 2.
Приведенные выше результаты испытаний неопровержимо доказывают, что композиция, отвечающая настоящему изобретению, обеспечивает весьма благоприятные клинические эффекты при лечении муковисцидоза и хронических болей при заболеваниях опорно-двигательного аппарата дистрофического характера или онкологических заболеваниях.
Доза фармацевтической композиции согласно изобретению зависит от состояния, массы тела больного и вида заболевания. Дневная доза может варьировать от 5 до 500 капель, реально равняясь 20-150 и преимущественно 40-80 каплям в день.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШИПУЧАЯ ТАБЛЕТКА ИЛИ ГРАНУЛА И СПОСОБ ИХ ПРИГОТОВЛЕНИЯ | 1994 |
|
RU2143891C1 |
| Способ получения комплекса иона металла с олиго- или полигалактуроновыми кислотами | 1977 |
|
SU886750A3 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА МИНЕРАЛЬНОГО УДОБРЕНИЯ "МЕГАВИТ-Н" ДЛЯ НЕКОРНЕВОЙ ПОДКОРМКИ РАСТЕНИЙ | 2015 |
|
RU2601975C1 |
| Комплексы иона металла с полигалактуроновыми кислотами,обладающие свойствами переноса ионов металлов в организме | 1978 |
|
SU739077A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОКОНЦЕНТРИРОВАННОГО РАСТВОРА МИНЕРАЛЬНОГО УДОБРЕНИЯ ДЛЯ ПРЕДПОСЕВНОЙ ОБРАБОТКИ СЕМЯН | 2008 |
|
RU2407287C2 |
| ПИЩЕВАЯ ВИТАМИННО-МИНЕРАЛЬНАЯ ДОБАВКА | 2007 |
|
RU2335926C1 |
| Жидкое комплексное средство для аквариумов | 2022 |
|
RU2796453C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА | 1999 |
|
RU2156087C1 |
| Способ получения функционализированной минералами структурированной воды | 2019 |
|
RU2725736C1 |
| ЭНТЕРАЛЬНАЯ СМЕСЬ ДЛЯ КИШЕЧНОГО ЛАВАЖА, КОРРЕКЦИИ МЕТАБОЛИЧЕСКИХ РАССТРОЙСТВ ОРГАНИЗМА, ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДИСБАКТЕРИОЗА КИШЕЧНИКА | 2000 |
|
RU2178696C2 |
Использование: в медицине для воздействия на ретикулоэндотелиальную систему, лечения муковисцидоза и хронических болевых синдромов, сопровождающих заболевания опорно-двигательного аппарата и онкологические заболевания. Сущность изобретения: фармацевтическая композиция содержит (г/100 мл водного раствора) одно или несколько фармацевтически приемлемых, водорастворимых соединений бора 0,01-1, фтора 0,01-1, магния 0,2-3, ванадия 0,001-0,6, марганца 0,02-2, железа 0,15-6, кобальта 0,002-1, никеля 0,01-2, меди 0,01-1, цинка 0,1-3, молибдена 0,001-0,8, не осаждаемых друг другом и прочими компонентами композиции и имеющих нейтральное или кислое значение pH в водной среде, а также содержит глицин 0,1-2, глицерин 0,2-8, L-(+)-аскорбиновую кислоту 0,01-2, нейтральную или кислую, водорастворимую и фармацевтически приемлемую соль этилендиаминтетрауксусной кислоты 0,01-3, виннокислый калий-натрий 0,01-10, янтарную кислоту 0,001-2 и L-(+)-винную кислоту 0,01-2. Указанную фармацевтическую композицию используют в ежедневной дозировке, составляющей от 5 до 500 капель, предпочтительно от 50 до 150 капель. 2 с. и 20 з.п. ф-лы, 2 табл.
Соединения бора 0,01 1
Соединения фтора 0,01 1
Соединения магния 0,2 3
Соединения ванадия 0,001 0,6
Соединения марганца 0,02 2
Соединения железа 0,15 6
Соединения кобальта 0,02 1
Соединения никеля 0,01 2
Соединения меди 0,01 1
Соединения цинка 0,1 3
Соединения молибдена 0,001 0,8
Глицин 0,1 2
Глицерин 0,2 8
L-(+)-аскорбиновая кислота 0,01 2
Янтарная кислота 0,001 2
Указанная соль этилендиаминтетрауксусной кислоты 0,01 3
Виннокислый калий-натрий 0,01 10
L-(+)-винная кислота 0,01 2
2. Композиция по п. 1, отличающаяся тем, что она содержит в качестве соединения бора борную кислоту.
| СПОСОБ ОБЕЗВОЖИВАНИЯ ВОДОНЕФТЯНОЙ ЭМУЛЬСИИ | 1991 |
|
RU2022998C1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1997-10-20—Публикация
1992-07-23—Подача