Изобретение относится к биохимии крови, регуляции системы гемостаза, а именно к новым низкомолекулярным синтетическим ингибиторам тромбообразования.
Катепсин G представляет собой сериновую протеазу, которая выделяется активированными лейкоцитами при воспалительных заболеваниях и обладает антимикробными свойствами. Однако эта протеаза является мощным индуктором агрегации тромбоцитов, что может привести к тромботическим осложнениям при воспалительных заболеваниях. Поэтому поиск новых ингибиторов катепсин-G-индуцированной активации тромбоцитов актуален для решения проблем контроля гемостаза и борьбы с тромботическими осложнениями при воспалении и инфекциях.
Наибольший интерес в этом отношении представляют низкомолекулярные соединения с простым способом получения.
Известны низкомолекулярные ингибиторы тромбообразования, представляющие собой модифицированные простациклины, теофилины и три-тетрапептиды, однако они не ингибируют катепсин-G-индуцированную агрегацию тромбоцитов.
Наиболее близким по действию к заявляемым соединениям является ингибитор катепсина G-эглин. Последний представляет собой низкомолекулярный белок, состоящий из 70-и аминокислот, выделенный из пиявок Hirudo medicinalis. Недостатком этого ингибитора является подавление исключительно протеазной активности, но не индуцированной катепсином G агрегации тромбоцитов. Кроме того, процесс выделения эглина из природного источника пиявок сложен, многостадиен, (включая многократную колоночную и гель-хроматографии) и энергоемок вследствие необходимости многократной лиофилизации белка.
Нами предлагаются новые низкомолекулярные ингибиторы катепсина G общей формулы (I), обладающие способностью подавлять тромбообразование, с простым способом их получения.
Общая формула (I):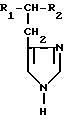
где при R1 CH3(CH2)10-CONH- R2 H-,
а при R1 NH2- R2 -COOCH3.
Конкретно предлагаемые вещества представляют собой дихлоргидрат метилового эфира гистидина (H-His-OMe•2HCl) и N-лауроилгистамин (Lau-HA). Дихлоргидрат метилового эфира гистидина получают этерификацией гистидина метиловым спиртом в кислой среде и выпускается рядом фирм, производящих химические реактивы для пептидного синтеза. N-лауроилгистамин получают ацилированием гистамина хлорангидридом лауриновой кислоты в органическом растворителе с высоким выходом и следующими константами: Т. пл. 121-125oC. ИК-спектр в вазелиновом масле, ν см-1: 1570 (амид I), 1460 (амид II), 1H-ЯМР (CD3OD), d м. д. 0,92 (т, 3Н, w -CH); 1,30 (м, 16Н, 8*CH2); 1,56 (т, 2H, b-CH2); 2,17 (т, 2Н, a-CH2); 2,92 (т, 2Н, a-CH2-HA); 3,50 (т, 2Н, b-CH2-HA); 7,30 (c, 1H, CH-4-Im); 8,80 (c, 1H, CH-2-Im). Найдено, С 69,67; H 10,57; N 14,29. C17H31N3O. Вычислено, С 69,52; H 10,56; N 14,31.
Катепсин G был выделен из нейтрофилов периферической крови человека по методу, описанному ранее. Катепсин G и тромбин (Sigma) были использованы в качестве индукторов агрегации тромбоцитов. Тромбоциты выделяли из венозной крови методом центрифугирования. В качестве антикоагулянта был использован 3,8%-ный водный раствор цитрата натрия в соотношении 1 9 с кровью. Среда для суспендирования тромбоцитов содержала HEPES-буфер 10 мМ, NaCl 150 мМ, KCl 2,7 мМ, NaH3PO4 0,37 мМ, MgCl2 1 мМ, CaCl2 1 мМ, глюкозы 5 мМ, pH 7,4 с аспиразой 0,1 мг/мл. Число тромбоцитов в исследуемых пробах составляло 3•10 в 1 мл. Агрегацию тромбоцитов в суспензии регистрировали на двухканальном агрегометре Labor APACT, Hamburg. Содержание в тромбоцитах цитоплазматического Ca ([Ca]цит) определяли с помощью флуоресцентного кальциевого зонда Fura-2AM, Calbiochem, USA флуориметрическим методом [10] Флуоресценцию регистрировали на спектрофлуориметре Hitachi-3000, Japan. Статическую обработку проводили, используя критерий Стьюдента.
Катепсин G в диапазоне концентраций 0,1 мкМ -10,0 мкМ вызывал развитие прямой дозозависимой агрегации тромбоцитов, которая по форме кривой, величинам амплитуды и максимальной скорости была близка к агрегации клеток, вызванной тромбином (1,0 ед/мл) (см. таблицу). Исходя из этого, при изучении влияния HisOMe•2HCl и LauHA на активированные тромбоциты, катепсин G и тромбин использовались в вышеуказанных концентрациях. В контрольной серии экспериментов была проведена оценка влияния HisOMe•2HCl и LauHA на функциональное состояние неактивированных тромбоцитов. Опыты показали, что HisOMe•2HCl (0,001 мМ 1,0 мМ), равно как и LauHA (0,001 мМ-1,0 мМ) не вызывали развития агрегации тромбоцитов в течение 15-минутной инкубации. Добавление HisOMe•2HCl в суспензию тромбоцитов за 5 мин до их стимуляции катепсином G или тромбином препятствовало агрегации клеток. Наиболее выраженный ингибирующий эффект отмечался при использовании максимальной из исследованных концентраций HisOMe•2HCl, составляющий 1 мМ. HisOMe•2HCl полностью подавлял развитие катепсин- G-индуцированной агрегации тромбоцитов, вызванной тромбином, на фоне HisOMe•2HCl снизилась менее значительно, в среднем на 58% (P<0,01) и 46% (P<0,05) соответственно. Следует отметить, что тромбин-индуцированная агрегация тромбонов в условиях инкубации с HisOMe•2HCl имела двухволновую форму в отличие от одноволновой в контрольной серии экспериментов (в отсутствии HisOMe•2HCl). Уменьшение концентрации HisOMe•2HCl до 0,1 мМ, а также времени инкубации тромбоцитов до 2 мин снижало величину его ингибирующего влияния на катепсин G-, так и тромбининдуцированную агрегацию клеток. LauHA в концентрации 1 мМ также подавлял развитие агрегации тромбоцитов, вызванный катепсином G. Так после 5-минутной инкубации тромбоцитов с LauHA амплитуда катепсин-G-индуцированной агрегации снижалась на 43% (P<0,01), а максимальная скорость на 56% (P<0,01). Величина ингибирующего влияния LauHA на агрегацию тромбоцитов, стимулированных катепсином G, в зависимости от времени инкубации (от 2 до 10 мин) достоверно не изменялась. В то же время нами не было отмечено достоверного снижения показателей агрегации тромбоцитов, индуцированной тромбином, на фоне LauHA. В этих условиях имела место лишь тенденция к снижению амплитуды агрегации в среднем на 16%
Можно считать, что предлагаемые ингибиторы тромбоцитарной активности, индуцированной катепсином G, обладают прямыми антитромбоцитарными свойствами в отличие от антипротеазных свойств эглина. По сравнению с эглином предлагаемые нами ингибиторы являются более простыми для получения. Кроме того, LauHA позволяет селективно ингибировать катепсин- G-индуцированную агрегацию тромбоцитов, не оказывая влияния на тромбинстимулированное тромбообразование. HisOMe•2HCl полностью подавляет катепсин-G-индуцированную агрегацию тромбоцитов, ингибируя в то же время и тромбининдуцированное тромбообразование. Предлагаемые ингибиторы могут найти применение в качестве реагентов для выяснения механизмов нарушения гемостаза, а также в качестве лекарственных фармакологических препаратов, препятствующих тромбообразованию, особенно при инфекционных и воспалительных заболеваниях.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ БИОГЕННЫХ АМИНОВ - МОДУЛЯТОРЫ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2093520C1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИОХЛОРОФИЛЛА А | 1996 |
|
RU2144085C1 |
| СПОСОБ КИНЕТИЧЕСКОГО ОПРЕДЕЛЕНИЯ РОДИЯ | 1994 |
|
RU2102744C1 |
| СПОСОБ ПОДГОТОВКИ ПРОБ К КИНЕТИЧЕСКОМУ ОПРЕДЕЛЕНИЮ РОДИЯ | 1994 |
|
RU2096755C1 |
| ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО ФОТОГЕМ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА | 1996 |
|
RU2128993C1 |
| УСТРОЙСТВО ДЛЯ ИСПЫТАНИЯ АСФАЛЬТОБЕТОНА НА СДВИГОУСТОЙЧИВОСТЬ | 1994 |
|
RU2086950C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТОНЕРА | 1997 |
|
RU2117974C1 |
| ПОЛИМЕРНАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2098353C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВНУТРЕННИХ ДЕФЕКТОВ В ИЗДЕЛИЯХ ИЗ РЕАКТОПЛАСТОВ | 1994 |
|
RU2088910C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОМПОЗИЦИОННОЙ ПОЛИМЕРНОЙ МЕМБРАНЫ ДЛЯ ВЫДЕЛЕНИЯ ДИОКСИДА УГЛЕРОДА ИЗ ГАЗОВЫХ СМЕСЕЙ | 1998 |
|
RU2146169C1 |

Изобретение относится к области медицины, конкретно к фармакологии. Сущность изобретения: имидазолсодержащие соединения общей формулы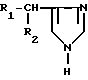
а именно, метиловый эфир гистидина дихлоргидрат и лауроилгистамин ингибируют катепсин-G-индуцированную агрегацию тромбоцитов. Предлагаемые ингибиторы могут найти применение в качестве реагентов для контроля гемостаза, а также фармакологических средств для предотвращения тромбообразования, особенно при инфекционных и воспалительных заболеваниях. 1 табл.
Применение имидазолсодержащих соединений общей формулы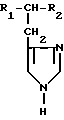
где при R1 CH3-(CH2)1 0-CONH- R2 H-, а при R1 NH2- R2 -COOCH3,
в качестве ингибиторов катепсин G-индуцированной агрегации тромбоцитов.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Гринштейн Дж., Виннц М | |||
| Химия аминокислот и пептидов | |||
| - М.: Мир, 1965, с | |||
| ПРИБОР ДЛЯ СЪЕМКИ ПЛАНА МЕСТНОСТИ | 1922 |
|
SU548A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Синтез молекулярных систем на основе парафинов и их димеров, содержащих донорно-акцепторные заместители, с целью создания на их основе соединений для медицины, науки и техники: Отчет МИТХТ им.М.В.Ломоносова.// Всероссийский научно-технический и информационный центр "Сборник рефератов НИР и ОКР" | |||
| - М., 1994, сер | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| E.Seemuller et al | |||
| Eglin: Elastase-cathepsin inhibitor from Leeches "Method in enzymology", 1981, v | |||
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
| C, p | |||
| Байпас для паровозов | 1923 |
|
SU804A1 |
Авторы
Даты
1997-11-27—Публикация
1994-09-30—Подача