Изобретение относится к области медицинских технологий: неинвазивной атравматичной диагностике гастродуоденальных заболеваний, вызываемых бактериями Helicobacter pylori, далее по тексту хеликобактер.
Распространенность гастритов и гастродуоденитов, ассоциирующихся с этиопатогенной ролью хеликобактеров требует недорогой информативной и простой экспрессной диагностической методики для скрининговых исследований, первичной диагностики, обязательного контроля терапии, так как для лечения хеликобактериоза применяется сложная химиотерапия не гарантирующая полного излечения [1-5]
Для диагностики хеликобактериоза используются бактериологические, серологические и биохимические методы [2 и 3] Биохимический тест обычно совмещается с эндоскопическим исследованием и опирается на анализ уреазной активности биоптатов [2 и 3] Он не только инвазивен, травматичен, но и может способствовать распространению инфекции. Серологические (иммуноферментные) методы определения антител к хеликобактеру связаны с отбором крови и по сути также травматичны. Помимо широко распространенных биохимических тестов: уреазного теста [3] CLO-теста [6] Campi-test [3] быстрого уреазного теста [6] его варианта уреазного "Де-нол®теста", фирма Яманучи Юроп Б.В. [7] связанных с эндоскопическим исследованием и биопсией, существуют неинвазивные методы биохимического анализа in vivo, также основанные на реакции гидролиза мочевины под действием высокоактивной уреазы хеликобактеров. Они позволяют обнаружить внеклеточную уреазу, продуцируемую хеликобактером, по продуктам гидролиза мочевины: двуокиси углерода и аммиаку, причем углекислый газ и аммиак определяются в воздухе ротовой полости (выдыхаемом воздухе) различными высокоточными физико-химическими методами с использованием приемов газового анализа [2, 3 и 5] Селективность и чувствительность всех этих методик базируется на использовании высокой активности микробной уреазы. При этом в качестве субстрата in vivo используют мочевину, меченную изотопом 14C, 13C или 15N. Меченая по атому углерода или азота мочевина принимается перорально в небольшом количестве и не может нанести существенный ущерб здоровью человека, даже в случае приема радиоактивного изотопа 14C. Преимуществом метода является прямая зависимость результата от активности уреазы в желудке или двенадцатиперстной кишке, так как определяемое содержание 13C, 14C или 15N не зависит от характера азотистого обмена пациента. Однако недостатком метода является использование изотопов, в том числе радиоактивного 14C, и сложная и дорогостоящая экспериментальная техника: высокоточные масс-спектрометры и масс-спектрографы или датчики по контролю радиоактивности. Наиболее совершенным из этих методов является метод диагностики хеликобактериоза по содержанию 13C в выдыхаемом воздухе [2, 10-12] Согласно этой методике, пациент принимает 75 мг мочевины состава 13C1H
В случае применения радиоактивной мочевины (меченная 14C от 3 до 10 мкК) используются поглотители углекислого газа и активность обычно определяется жидкостным сцинтиллятором. При этом контролируется кинетика нарастания в дозы на моль CO2 (общего) на единицу массы в единицу времени. Метод ограничен в применении у детей и беременных женщин [2]
Определение изотопа 15N в воздухе ротовой полости затруднено из-за высокой сорбции аммиака желудочным соком (крайне низкая концентрация NH3 при приеме меченой мочевины), поэтому 15N после приема меченной по азоту мочевины в количестве 3 мг/кг массы тела определяют в моче, собирая ее в течение 2 ч порциями. Метод доступен по приборной базе, атравматичен и неинвазивен, но длителен и трудоемок [2 и 21]
Наиболее близким к заявленному способу диагностики хеликобактериоза по сути физико-химических измерений и биохимических процессов является способ диагностики, построенный на измерении содержания аммиака вне зависимости от его изотопного состава (интегрально) в воздухе ротовой полости (выдыхаемом воздухе) [13-20] Аммиак, выделяющийся в желудке при гидролизе уреазой хеликобактера мочевины, транссудируемой в полость желудка, не связывается полностью соляной кислотой, и его равновесная концентрация может быть легко измерена любым надежным высокочувствительным методом с использованием аналитических методик, обычно применяемых в газовом анализе. Способ предполагает, что аммиак, выделившийся из кислой среды желудка, легко выходит наружу по пищеводу в ротовую полость, и его концентрация в выдыхаемом воздухе обусловлена только активностью микробной уреазы, при этом концентрация мочевины в крови и других биологических жидкостях остается стабильной. Другие патологические состояния, кроме хеликобактериоза, сопровождающиеся гипераммониемией, повышают выделение аммиака с потом но не приводят к повышению его концентрации в воздухе ротовой полости. Измерение уровня аммиака в ротовой полости может проводиться с помощью линейно-колористических индикаторных трубок (линейных газоанализаторов [22] ГОСТ 12.1.005-76; С 2.262 ТУ ЧЗХР) или с помощью спектро-фотометрической методики (ГОСТ 17.2.4.03-81 ОХРАНА ПРИРОДЫ. АТМОСФЕРА Индофенольный метод определения аммиака), а также с помощью ион-селективных электродов [23] Данный способ не предполагает внесения мочевины в организм извне, тем более, что иные пути появления аммиака в контролируемых концентрациях несущественны. В отличие от контроля по содержанию аммиака в воздухе ротовой полости, контроль по CO2 без привлечения радионуклидной нагрузки в составе описанных выше методик невозможен, так как без введения меченых атомов невозможно отличить CO2, образующийся в желудке при гидролизе мочевины, от CO2, выдыхаемого через легкие.
Способ измерения содержания аммиака в воздухе ротовой полости с помощью одноразовых индикаторных трубок [13-20] наиболее прост и дешев, не требует дезинфекции и специальной квалификации химика-аналитика, позволяет производить исследование экспрессивно (в течение 10-15 мин) не требует специальной подготовки пациента, неинвазивен. Результаты сопоставимы с другими методами диагностики хеликобактериоза, но приведенная в качестве диагностической концентрация аммиака 0,8-1,0 мг/м3 [13-20] ориентирована на контроль сильного инфицирования у взрослых пациентов с выраженными признаками гастродуоденальной патологии. Снижение диагностического порога концентрации аммиака по 0,6 мг/м3 и ниже приводит к большому числу ложноположительных результатов. При использовании метода в педиатрической практике он оказался недостаточно информативен у детей раннего возраста (в силу особенностей азотистого обмена) и давал существенные расхождения результатов с другими методами диагностики хеликобактериоза.
С целью устранения зависимости от особенностей азотистого обмена пациентов и повышения чувствительности диагностической методики без потери селективности предлагается способ диагностики хеликобактериоза, в основе которого кинетическая методика оценки степени инвазии Helicobacter pylori in vivo по приросту содержания аммиака в воздухе ротовой полости во времени после приема пациентом единичной порции мочевины нормального изотопного состава: 12C1H
Содержание аммиака в воздухе ротовой полости можно оценивать также фотоколориметрически или по времени, через которое произойдет изменение окраски сорбента или сорбционного раствора, содержащего буфер и индикатор. В последнем случае через слой жидкого или пленочного сорбента на носителе продувается или аспирируется воздух из ротовой полости. Можно оценивать содержание аммиака и с помощью ионселективных электродов, абсорбируя аммиак из воздуха ротовой полости в растворы кислой природы (например, каплю 10% раствора H2SO4).
Аммиак, определяемый в воздухе ротовой полости, является продуктом реакции расщепления мочевины в желудке с помощью уреазы, выделяемой хеликобактером: 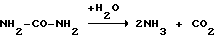 . Данная реакция в естественных условиях находится в динамическом состоянии и зависит от количества транссудируемой через слизистую оболочку желудка мочевины, поэтому фоновая концентрация аммиака натощак не всегда достоверно отражает истинную уреазную активность микроба, зависит от особенностей азотистого обмена и, как указывалось выше, нередко дает ложноотрицательные или сомнительные результаты.
. Данная реакция в естественных условиях находится в динамическом состоянии и зависит от количества транссудируемой через слизистую оболочку желудка мочевины, поэтому фоновая концентрация аммиака натощак не всегда достоверно отражает истинную уреазную активность микроба, зависит от особенностей азотистого обмена и, как указывалось выше, нередко дает ложноотрицательные или сомнительные результаты.
Прием мочевины нормального изотопного состава, предлагаемый в данной методике, при наличии уреазы пилорического хеликобактера, вызывает усиленное образование аммиака и приводит к нарастанию его содержания в воздухе ротовой полости. Положительным тест считается при:
1) Нарастании содержания аммиака в воздухе ротовой полости через 10-15 мин после приема 500 мг мочевины более, чем на 0,5 мг/м3 по сравнению с исходным.
2) Содержании аммиака в воздухе ротовой полости через 10-15 мин после приема 500 мг мочевины 0,9 мг/м3 и выше, независимо от фонового содержания.
3) Содержании аммиака в воздухе ротовой полости, измеренном со второй по десятую минуты после приема 500 мг мочевины, 0,9 мг/м3 и выше, независимо от фонового содержания.
4) Величине удельной скорости нарастания концентрации аммиака в воздухе ротовой полости в первые 5 мин после приема 500 мг мочевины, равной или выше (2,2 ± 0,2) • 10-8 с-1, вычисленной как частное от деления измеряемой концентрации аммиака в моль/м3, умноженной на объем газовой пробы в м3, на массу навески мочевины в моль и время измерения в секундах:
5) Выделении 1,2•10-2 мг= 0,7•10-6 г•моль и выше аммиака в первые 6 мин после приема 500 мг мочевины при общем количестве аммиака, выделяющегося в ротовую полость после приема данного количества мочевины, равном около 0,15 мг. В этом случае при использовании методики на линейно-колористических газоанализаторах удобнее оперировать скоростью нарастания концентрации аммиака или приростом концентрации за время не более 10 мин с момента введения мочевины в желудок (перорально, через зонд или канал эндоскопа). Проба положительна при скорости нарастания концентрации аммиака свыше 0,12 мг/м3 в мин в первые 10 мин после приема мочевины или в том случае, если, изморенная за 6 мин аспирации, концентрация отличается от исходной на 0,6 мг/м3 и более.
6) Оценке формы кинетической кривой превращения единичной порции субстрата (мочевины), внесенной извне в желудок, как кинетической зависимости, соответствующей быстрому гидролизу с выходом концентрации аммиака в ротовой полости на исходный уровень за 50 мин и меньше для порции мочевины 500 мг (фиг.1) и менее.
7) Достижении максимальной концентрации аммиака в воздухе ротовой полости по оценке кинетической кривой превращения единичной порции мочевины (500 мг) за определенное время и/или величине этой концентрации
а) сильное инфицирование при концентрации 1,5-4,0 мг/м3 через 5-10 мин.
б) слабое инфицирование при концентрации 0,6-1,5 мг/м3 через 10-20 мин.
в) отсутствие инфицирования при концентрации 0,1-0,6 мг/м3 через 20-40 мин.
Предложенный диагностический способ отражает истинную уреазную активность хеликобактера, что позволяет судить о степени инвазии и не зависит от особенностей азотистого обмена. Данный метод позволяет увеличить достоверность результатов анализа, является простым, неинвазивным, может быть широко использован в медицинской практике как с целью диагностики хеликобактериоза, так, и с целью контроля за эффективностью терапии. Предлагаемое изобретение, по сравнению с вышеописанными методами с нагрузкой мочевиной, не требует дорогой техники и веществ измененного изотопного состава.
Пример 1: Девочка в возрасте 9 лет, с эндоскопически подтвержденным антральным поверхностным гастритом, была обследована по методике "Аэротест" следующим образом:
Перед исследованием ребенок не принимал пищу в течение 12 ч. У девочки был измерен фоновый уровень аммиака посредством индикаторной трубки, внутренний диаметр которой 2 мм, внешний 4 мм, общая длина 100 мм, расстояние до наполнителя 45 мм, высота столбика наполнителя 35 мм, наполнитель закреплен ватными тампонами из хлопковой ваты (2 мм нижний тампон и 1 мм верхний). В качестве наполнителя использован индикаторный порошок на основе силикогеля 10-20 мк, предварительно обработанный таким образом, что он содержит 20 мг индикатора бромфенолового синего в 21 г H2SO4 в 100 мл индикаторного порошка. Индикаторная трубка располагалась у пациентки таким образом, чтобы воздух отбирался из глубоких отделов ротовой полости и не попадала слюна. Через индикаторную трубку аспирировали 2 дм3 воздуха из ротовой полости со скоростью 0,2 дм3/мин, электромеханическим аспиратором. Окрашенный столбик практически отсутствовал, индикационный эффект выражался в окрашивании нескольких зерен лобового слоя, что соответствовало содержанию аммиака в воздухе ротовой полости в концентрации намного меньшей, чем 0,1 мг/м3 по градуировке индикаторной трубки. Аналогичное содержание подтверждалось измерениями по методике ГОСТ 17.2.4.03-81 и методике [26]
Вышеописанная часть примера 1 полностью соответствует методике [3 и 13] по которой диагностический результат является отрицательным.
Затем девочка приняла внутрь 500 мг мочевины нормального изотопного состава в 10 мл воды. Через 15 мин после приема мочевины измерение содержания аммиака в воздухе ротовой полости было повторено аналогичным вышеописанному методом. Содержание аммиака соответствовало 0,9 мг/м3 Проведенные уреазный тест с биоптатом, бактериоскопия и серологическое исследование (тест "Элайза") свидетельствовали о наличии пилорического хеликобактера.
Пример 2: Мальчик в возрасте 12 лет с эндоскопически подтвержденным эрозивным дуоденитом обследован аналогичным образом. Фоновая концентрация аммиака в воздухе ротовой полости составила 0,9 мг/м3, после приема 500 мг мочевины 1,7 мг/м3 прирост 0,8 мг/м3. Результат исследования резко положительный. Наличие хеликобактера подтверждено также уреазным тестом и бактериоскопией.
Пример 3: Мужчина 37 лет с эндоскопически подтвержденной язвенной болезнью двенадцатиперстной кишки обследован по описанной методике трижды: натощак, через 15 мин после приема мочевины и через 30 мин после приема 500 мг мочевины. Содержание аммиака в воздухе ротовой полости натощак составило 0,5 мг/м3, через 15 мин после приема 500 мг мочевины 1,6 мг/м3, через 30 мин 0,6 мг/м3. То есть максимальный прирост аммиака после приема мочевины отмечен через 15 мин, а через 30 мин его уровень практически вернулся к исходным цифрам. Наличие хеликобактера подтверждено также серологически и уреазным тестом.
Пример 4: Девочка в возрасте 5 лет с эндоскопически подтвержденным распространенным гастродуоденитом обследована по описанной методике. Фоновая концентрация аммиака в воздухе ротовой полости составила 0,1 мг/м3, после приема 500 мг мочевины 0,3 мг/м3, что расценено как отрицательный результат. Уреазный тест и серологическое исследование также дали отрицательные результаты.
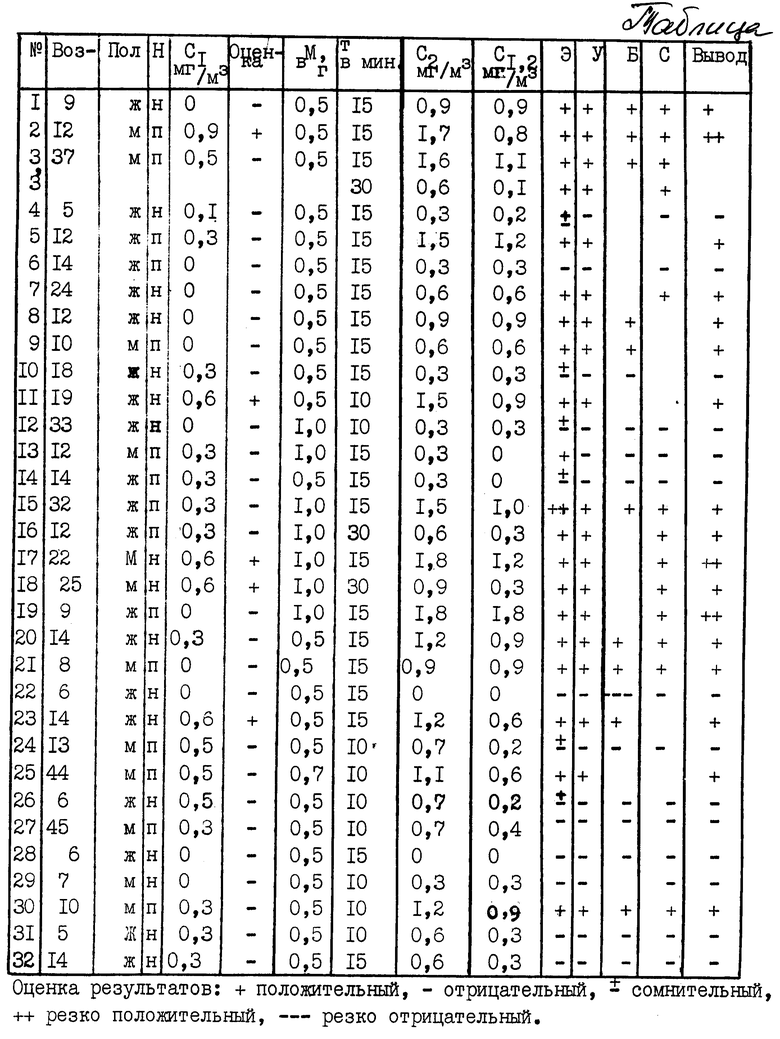
Ниже в таблице представлены результаты диагностических измерений содержания аммиака в ротовой полости натощак и после приема мочевины, где N - номер исследования, H- кислотообразующая функция (н нормальная, п - повышена, с понижена), м количество принятой мочевины, τ время повторного исследования после приема мочевины, C1 исходная концентрация аммиака в воздухе ротовой полости, C2 концентрация аммиака в воздухе ротовой полости после приема мочевины; C1,2 прирост концентрации аммиака (разница концентраций фоновой и после нагрузки); Э - признаки наличия хеликобактериоза по эндоскопическим данным, где У результат уреазного теста с биоптатом, Б результат бактериоскопии, С результат серологического исследования.
Всего обследовано 32 больных в возрасте от 5 до 45 лет. Все больные разделены на 3 группы в зависимости от результатов исследования уровня аммиака в воздухе ротовой полости до и после нагрузки мочевиной.
В I группе отмечен отрицательный результат исследования до (0,5 мг/м3 и ниже) и после нагрузки мочевиной (ниже 0,9 мг/м3, нарастание ниже 0,5 мг/м3). Часть обследованных больных в этой группе не имела клинических и эндоскопических признаков гастродуоденальной патологии, у остальных выявлены эндоскопические признаки воспаления (поверхностный гастрит). Отсутствие хеликобактера у больных этой группы подтверждено также другими известными методами: уреазный тест, бактериоскопия, серология.
То есть отрицательный результат исследования уровня аммиака в воздухе ротовой полости после нагрузки мочевиной позволяет говорить об отсутствии хеликобактера пилори.
В II группе отмечался отрицательный результат исследования до нагрузки (0,5 мг/м3 и ниже) и положительный (0,9 мг/м3 и выше, нарастание 0,6 мг/м3 и более) после нагрузки мочевиной. У всех больных этой группы были выявлены отчетливые эндоскопические признаки хронической гастродуоденальной патологии (хронический гастродуоденит, язвенная болезнь 12-перстной кишки). Наличие хеликобактера у них подтверждено также другими методами уреазный тест, бактериоскопия, серологически.
Следовательно, исследование уровня аммиака в воздухе ротовой полости без нагрузки (фоновое) может давать ложноотрицательные результаты, и только нагрузка мочевиной позволяет обнаружить присутствие хеликобактера.
У больных III группы отмечены положительные результаты исследования и до (0,6 мг/м3 и выше), и после (0,9 мг/м3 и выше) как правило, с отчетливым нарастанием концентрации аммиака после нагрузки (0,6 мг/м3 и выше). У всех больных этой группы выявлены эндоскопические признаки хронической гастродуоденальной патологии (хронический гастродуоденит, язвенная болезнь), наличие хеликобактера подтверждено и другими методами: уреазный тест, бактериоскопия. Следовательно, нагрузка мочевиной в этой группе больных сделала результаты исследования более наглядными в оценке степени уреазной активности.
Примеры, приведенные ниже, характеризуют дополнительные диагностические возможности метода по экспрессности, количественным, качественным и дифференцирующим возможностям по сравнению с другими, в том числе и дыхательными тестами [2, 5, 9, 12] и подтверждают оценочные критерии, приведенные выше [стр.6, 6а, пп. 3-7]
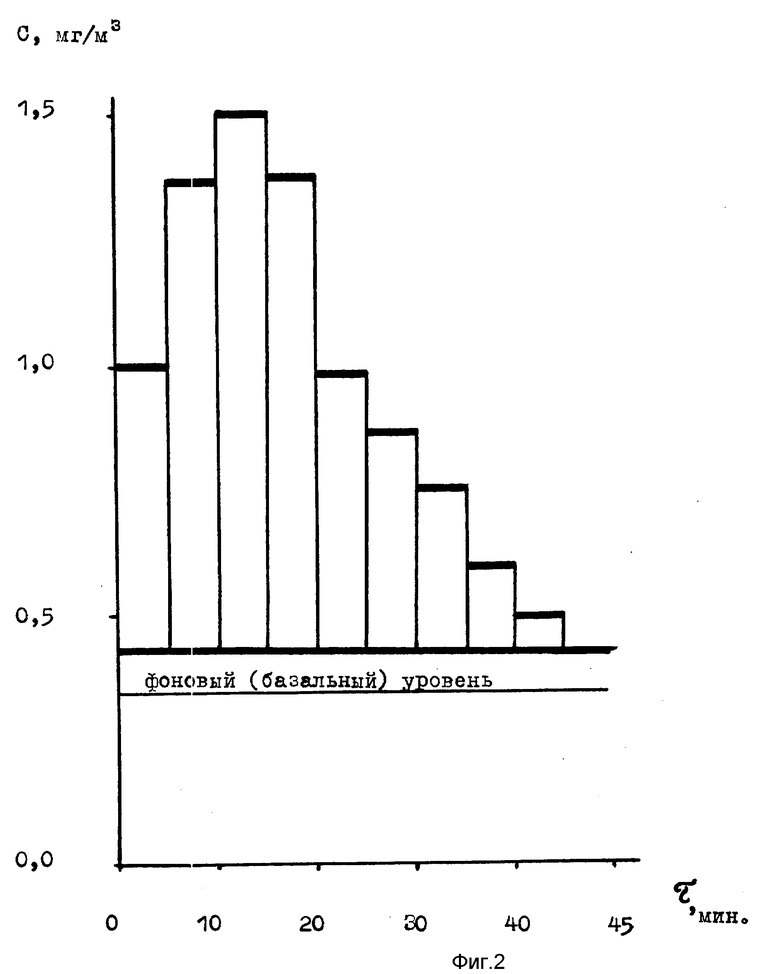
Пример 33: Пациент, обследовавшийся ранее (пример 25), обследовался повторно через две недели. Терапия между обследованиями не проводилась. Фоновый уровень аммиака в воздухе ротовой полости был измерен по линейно-колористической методике, как в примере 1. Затем пациент принял перорально раствор 500 мг мочевины в 10 мл воды и 10 мл воды ополоснул рот. Процедура проводилась натощак. После этого измерялось содержание аммиака в воздухе ротовой полости, отбирая по 2 дм3 воздуха каждые 5 мин (непрерывный отбор в течение часа). В результате была получена зависимость изменения концентрации во времени (фиг.2), соответствующая кинетической кривой 2 на фиг.1.
Пример 34: Проводили аналогично примеру 33 за исключением того, что мочевину давали пациенту в виде манной каши. Полученная кривая соответствовала кривой 3 (фиг.1).
Пример 35: Проводили аналогично примеру 33 за исключением того, что 500 мг мочевины давали пациенту в виде раствора в молоке. Полученная зависимость соответствовала кривой 3 (фиг.1).
Пример 36: Обследование проводили аналогично примеру 33 за исключением того, что пациенту после выхода кинетической кривой на исходный уровень вновь дали 500 мг мочевины перорально в 10 мл воды. Затем была повторно зафиксирована зависимость роста концентрации аммиака во времени, аналогичная предшествующей, то есть соответствующая кривой 2 (фиг.1).
Пример 37: Мужчина 44 лет, ранее не лечившийся, страдающий хроническим эрозивным гастритом, диагноз которого подтвержден эндоскопически, а наличие хеликобактера подтверждено уреазным тестом и серологически, обследован аналогично примеру 33. В результате была получена зависимость (фиг.3), отражающая быструю кинетику разложения мочевины (кривая 1, фиг.1). В ходе этого исследования концентрация аммиака в воздухе ротовой полости измерялась двумя тестами параллельно, со смещением во времени в 2 мин. При этом величина удельной скорости составила 1,3 • 10-7 с-1 [стр.6, п.4] а средняя скорость нарастания концентрации аммиака превышала 0,3 мг/м3 в мин на начальном этапе измерения.
Пример 38: Аналогичен примеру 37, но состоял в том, что пациенту (мужчине 44 лет) было введено перорально 3 г мочевины в 10 мл воды, рот прополоснут водой и измерена зависимость повышения концентраций аммиака в воздухе ротовом полости. Зависимость представлена на фиг.1, кривая 1'.
Пример 39: женщина 21 года обследована аналогично примеру 37 с той лишь разницей, что при получении зависимости концентрации аммиака в ротовой полости от времени, измерение проводилось параллельно тремя индикаторными трубками, отбирая 2 дм3 за 6 мин со смещением пробоотбора в две минуты. Полученная зависимость, представленная на фиг. 4, соответствует кинетической кривой 1 на фиг.1 и имеет максимум С=3,2 мг/м3 через 7-8 мин от начала пробоотбора после приема 500 мг мочевины. Средняя скорость нарастания концентрации аммиака составила 0,3±0,1 мг/м3 в мин. Величина удельной скорости была равна (1,2± 0,3)•10-7 с-1, то есть концентрация уреазы в желудке обследуемой превышала в пять раз значимую величину (2,2±0,2)•10-8 с-1, что указывает на существенное инфицирование, если при оценке руководствоваться линейной зависимостью удельной скорости от содержания фермента, выделяемого микроорганизмами, и не учитывать влияния pH на ферментативную активность, предполагая нулевой порядок реакции в ее начале, исходя из избытка субстрата и воды. Инфицированность пациентки подтверждается характером эндоскопической картины (антральный гастрит), положительным уреазным тестом и серологическими данными.
Пример 40: Аналогичен примеру 39 с той лишь разницей, что исследование было проведено после курса лечения омепразолом и амоксициллином в течение 2 недель. Зависимость, полученная в ходе исследования, аналогична кривой 3 на фиг. 1 и свидетельствует о подавлении хеликобактера, что подтверждено и другими методами: отрицательный уреазный тест и бактериоскопия.
Пример 41: женщина 43 лет, страдавшая хроническим гастритом, прошедшая курс тройной антихеликобактериозной терапии, не предъявляющая жалоб в настоящее время, обследована аналогично примеру 39. Была получена кривая, аналогичная кривой 3 на фиг.1. Скорость прироста содержания аммиака в воздухе ротовой полости после приема 500 мг мочевины составила 0,07 мг/м3 в мин; величина удельной скорости около 0,5•10-8 с-1, что в 4 раза ниже значимой (2,2±0,2)•10-8 с-1 на графической зависимости максимум DC по Δτ содержания аммиака в воздухе ротовой полости наблюдался через 25-30 мин, причем численная величина концентрации при исходной 0,3±0,1 мг/м3 не превышает 0,7±0,2 мг/м3, то есть прирост не превышает 0,4±0,2 мг/м3, что указывает на отсутствие инфицирования хеликобактером. Это подтверждено также отрицательным уреазным тестом и результатами бактериоскопии.
Из примеров 1 32, характеризующих наиболее простой тип оценки экспериментальных данных, и примеров 33 40, характеризующих различные подходы к оценке результатов кинетических измерений in vivo превращения единичной порции субстрата (мочевины) для оценки присутствия в желудке микробной уреазы хеликобактеров, следует, что упрощенные подходы к оценке аналитического сигнала (в данном случае содержания аммиака в воздухе ротовой полости), полученного в ходе сложной дифференциальной кинетики, осложненной процессом массопередачи (транспортировки в ротовую полость) позволяют получить отклик (аналитический результат), количественно характеризующий ферментативную активность хеликобактеров на качественно ином уровне, чем в случае оценки биоптатов, когда оценивается микрочастица ткани желудка, что далеко от интегральной оценки состояния, или в случае аналогичных методик in vivo, где CO2, меченый изотопным маркером, проходит достаточно сложный путь в кровотоке, о чем свидетельствуют опубликованные кинетические зависимости, существенно отличающиеся от полученных по настоящему методу в сторону более длительного течения процесса. Методика с привлечением маркера N15 нецелесообразна из-за длительности и связана со сбором мочи. В то же время использование дорогих приборов и изотопов ничем не оправдано, так как эти сложные методы не превосходят по чувствительности традиционные методы газового анализа, каким и является настоящий способ диагностики хеликобактериоза, где более высокая чувствительность достигается за счет накопления анализируемого вещества в ничтожном объеме твердого сорбента, причем анализ совмещается с пробоотбором, что очень важно при практической работе, когда исследователь уже в ходе пробоотбора может судить о результате и, следовательно, может судить о "испорченном" результате в силу "случайных" причин, связанных с работой аппаратуры и погрешностями любой аналитической процедуры.
Мысль о том, что аммиак не может из желудка, где среда достаточно кислая, попасть в ротовую полость, не только не соответствует действительности, но и ничем не подкреплена теоретически. Единственным препятствием для его обнаружения и измерения как над раствором соляной кислоты в желудке, так и в более нейтральной среде ротовой полости, служит очень низкая его концентрация, требующая совершенного аналитического подхода, который позволяет достичь высокой чувствительности без потери химической селективности. Сорбция аммиака в концентрациях, равновесных с раствором соляной кислоты (желудочным соком), практически неосуществима нейтральным растворами (слизистыми оболочками пищевода и рта); аммиак, находящийся в газовой фазе, над солянокислым раствором, будучи достаточно летучим газом, легко проникает за счет диффузии через сфинктеры в глотку, где перемешивается с воздухом из легких, и поступает в рот, частично разбавляясь. Благодаря этому возможно измерить без проникновения в желудок практически равновесную с желудочным содержимым концентрацию аммиака, постоянно поддерживаемую динамическим равновесием NH
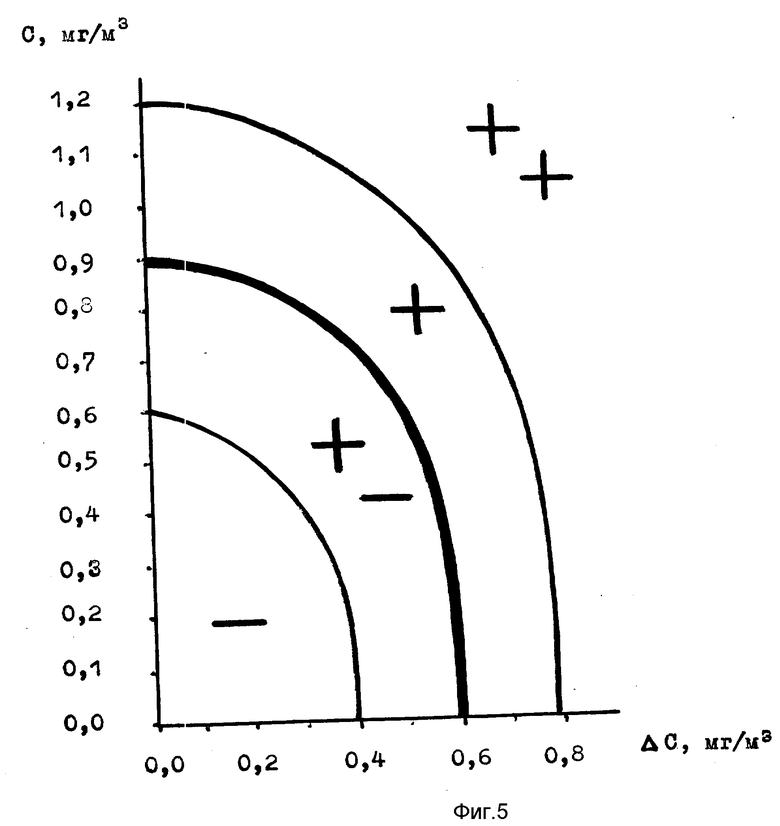
В упрощенном варианте связь аналитических параметров с диагностическим результатом лучше представить в виде номограммы (фиг.5), где одновременно оценивается динамический процесс образования аммиака из мочевины, транссудируемой через стенку желудка из крови, по фоновой концентрации аммиака в ротовой полости и процесс образования аммиака из мочевины, внесенной в желудок извне, по приросту концентрации аммиака в воздухе ротовой полости, измеренной со второй по десятую минуты после приема порции мочевины (500 мг). Оба процесса проходят под действием одной и той же уреазы хеликобактера и совместно описываются достаточно сложными кинетическими зависимостями (дифференциальная кинетика). Поэтому аналитический отклик позволяет лишь в определенных пределах характеризовать эти процессы. Существенным фактором является величина порции мочевины, вводимой извне, и наличие других осложняющих факторов. Поэтому исследование проводится натощак.
Литература
1. Зварту Э.Э. Рысс Е.С. Фармакотерапия гастродуоденальных язв. СПб. Наука, 1992, 174 с.
2. Аруин Л. И. Григорьев П.Я. Исаков В.А. Яковенко Э.П. Хронический гастрит. Амстердам: 1993, 362 с.
3. Сафонова Н.В. Жебрун А.Б. Гастрит, язвенная болезнь и хеликобактериоз. СПб. НИИЭиМ им.Пастера /рекомендации для врачей/ 1993, 40 с.
4. Стародуб Е.М. Гаврилюк М.Е. Чайка Н.А. Геликобактериоз и язвенная болезнь. Л. 1991, 32 с.
5. John H. Woalsh, Walter L. Peterson. The Treatment of Helicobacter Pylori Infection in The Managment of Peptic Ulcer Disease. Review Article, The New England Journal of Medicine, v.333, N 15, p.984-991.
6. Marshall B.J. coll. Rapid urease test in management of Campylobacter-associated gastritis.-Amer. J.Gastroenterol. 1987, v.82, p.200-210.
7. "Де-нол®-тест.. Уникальный уреазный тест для быстрой диагностики Helicobacter pylori" Рекламный проспект Yamanouchi, 1995, с.4. (Vaira D. et al. Am. J. Gastroenterol. 1989, 84:836-37)
8. Bell G. and coll. C-urea Breath test, a non-invasive test for Campylobacter pylori in the stomach. Lancet. 1987, v.1, p.1367-1368.
9. Marshall B.J. Surveyor l. Carbon 14 urea Breath test for diagnosis of Campylobacter pylori associated gastritis. J. Nucl. Med. 1988, v.29, p.11-16.
10. Marshall B.J. et al. A20-minute breath test for Helicobacter pylori.
Am. J. Gastroenterol 1991, v.86, p.438-445.
11. Graham DY. et all. Campylobacter pylori detected noninvasively by the 13C-urea Breath test. Lancet, 1987, v.1, p.1174-1177.
12. Logan RPH. Dill S. Bauer F.E. et all. The European 13C-urea breath test for the detection of Helicobacter pylori. Eur J. Gastroenterol Hepatol.
1991, v.3, p.915.
13. N.V.Safonova et al. The Respiratory Test for detecting Helicobacteriosis. Workshop Helicobacter pylori and the new concepts in gastro-duodenal diseases. Okt.30-31, 1992; Charles University, Prague - Czechoslovakia, Abstruct book, P3.
14. Способ лабораторной диагностики хеликобактериоза. Жебрун А.Б. с соавт. заявка на патент России, N 93-029859/14 (028016)
15. Safonova N.V. et al.-"AEROTEST" for Helicobacter pylori diagnosis: - "Campylobacter meets Helicobacter: The Joint meeting; Meeting of the European Helicobacter Pylori Study Group. Brussels, Sept 21-25, 1993. Acta Gastroenterologica Belgica, 1993, v.56, p.1-224, p.84.
16. Милейко В. Е. и др. Новый тест для диагностики хеликобактериоза. - Актуальные проблемы инфекционной патологии, ч. 1: Кишечные и респираторные инфекции. СПб. НИИЭиМ им.Пастера, 1993, с.45.
17. Сафонова Н.В. и др. Аэротест неинвазивный экспресс-метод для диагностики хеликобактериоза. Тезисы докладов Первого национального конгресса по профилактической медицине. СПб. 1994, т.III, с.44-45 прототип.
18. Милейко В.Е. Михайленко В.С. Использование методов газового анализа для ранней диагностики хеликобактериоза, фенилкетонурии, сахарного диабета по контролю метаболитов в выдыхаемом воздухе. Тезисы докладов I национального конгресса по профилактической медицине. СПб. 1994, т.II, с.16.
19. Paikov V.L. Helicobacter pylori infection among early-age children of Saint-Peterburg. The Am. J. of Gastroenterology, v.89, N.8, 1994, p.1353.
20. Zhebrun A.B. et al. Evaluation of laboratory tests for diagnosis of children's Helicobacter Pylori infection. The Am. Journ. Gastroenterology, v.89, N 8, 1994, p.1394.
21. Guolong et al. Detection of Helicobacter pylori infection in humans using N-urea method. Rev. Esp. Digest. 1990, v.78, Suppl.1, p.22-23.
22. Болковец С.В. Индикаторный состав для линейно-колористического определения аммиака. Авторское свидетельство СССР N 1458815 AI; C 01 N 31/22.
23. Джагацпанян И.Э. Автоматизированынй измерительный модуль для диагностики хеликобактериоза. СПб. 1995, автореф.канд. дисс. на соискание уч.степени канд.технических наук.
24. Шарапов В. М. и др. Способ получения индикаторной массы. Авторское свидетельство СССР N 1180065 A; B 01 Y 20/10, C 01 N 31/22
25. Таньков К. Н. и др. Способ получения индикаторной массы. Авторское свидетельство СССР N 1111813 A; C 01 N 31/22
26. Акулова Н. А. Способ определения аммиака. Авторское свидетельство СССР N 1140034; C 01 N 31/22.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ХЕЛИКОБАКТЕРИОЗА ПО ОЦЕНКЕ УРЕАЗНОЙ АКТИВНОСТИ БИОЛОГИЧЕСКОГО МАТЕРИАЛА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1997 |
|
RU2184781C2 |
| СПОСОБ ИССЛЕДОВАНИЯ УРЕАЗНОЙ АКТИВНОСТИ | 1998 |
|
RU2176792C2 |
| СПОСОБ ДИАГНОСТИКИ ХЕЛИКОБАКТЕРИОЗА | 1993 |
|
RU2091796C1 |
| СПОСОБ ДИАГНОСТИКИ ИНФЕКЦИИ HELICOBACTER PYLORI У БОЛЬНЫХ С ХИРУРГИЧЕСКОЙ ПАТОЛОГИЕЙ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ | 2009 |
|
RU2440583C2 |
| СПОСОБ ДИАГНОСТИКИ ИНФЕКЦИИ ЖЕЛУДКА, ВЫЗВАННОЙ HELICOBACTER PYLORI | 2013 |
|
RU2521340C1 |
| СПОСОБ НЕИНВАЗИВНОЙ ДИАГНОСТИКИ ИНФЕКЦИИ HELICOBACTER PYLORI ИН ВИВО И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2003 |
|
RU2263468C2 |
| СПОСОБ ВЫЯВЛЕНИЯ УРЕАЗОПРОДУЦИРУЮЩИХ МИКРООРГАНИЗМОВ "БЫСТРЫЙ УРЕАЗНЫЙ ТЕСТ ГЕЛИКОБАКТЕР ТЕСТ" И УСТРОЙСТВО ДЛЯ ЕГО ПРИМЕНЕНИЯ | 2013 |
|
RU2540473C2 |
| СПОСОБ ДИАГНОСТИКИ ПИЛОРИЧЕСКОГО ХЕЛИКОБАКТЕРИОЗА | 2001 |
|
RU2189592C1 |
| СПОСОБ ДИАГНОСТИКИ ПИЛОРИЧЕСКОГО ХЕЛИКОБАКТЕРИОЗА | 2000 |
|
RU2194276C2 |
| Способ моделирования хеликобактериоза | 2018 |
|
RU2690943C1 |


Использование: диагностика заболеваний, вызываемых бактериями Helicobacter pylori. Сущность изобретения: в способе диагностики хеликобактериоза in vivo, включающем определение содержания аммиака в воздухе ротовой полости, оценку степени инфицированности пациента проводят по приросту содержания аммиака после приема перорально мочевины нормального изотопного состава. 4 з.п.ф-лы, 5 ил., 1 табл.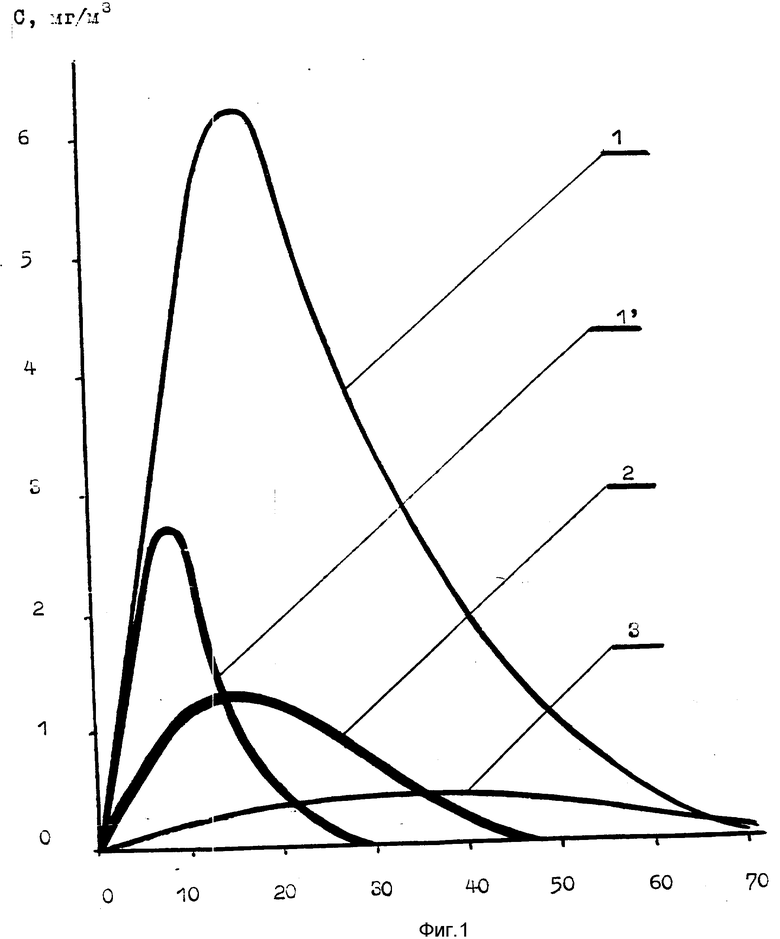
| Сафонова Н.В | |||
| и др | |||
| Аэротест - неинвазивный экспресс-метод для диагностики хеликобактериоза | |||
| Тезисы докладов Первого национального конгресса по профилактической медицине | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
Авторы
Даты
1997-12-27—Публикация
1996-02-20—Подача